1.本发明属于磷酸铁制备技术领域,具体涉及一种片状电池级磷酸铁的制备方法。
背景技术:
2.随着新能源汽车快速发展,动力锂离子电池需求不断提高,其中,磷酸铁锂(lifepo4)被认为是锂离子电池最理想的正极材料。目前,制备磷酸铁锂多采用磷酸铁作为前驱物原料,磷酸铁产品的质量与纯度直接影响磷酸铁锂的品质。
3.在本领域,用于制备磷酸铁锂的磷酸铁被称为电池级磷酸铁。由于电池级磷酸铁对杂质要求极高,对基础原料要求苛刻,通常使用高纯度的磷酸或者磷酸盐和铁盐反应,然而高纯度原材料的成本非常高。因此,亟需一种能够大幅度降低磷酸铁成本的制备方法,从而降低锂离子电池的生产成本。
4.随着磷酸铁制备业的发展,廉价铁源和磷源成为技术人员关注的焦点。
5.目前,制备电池级磷酸铁使用的铁源一般采用硫酸盐形式,以硫酸亚铁为铁源的主流工艺可根据使用的中和剂和其他阳离子的不同分为铵盐法和钠盐法。铵盐法与钠盐法制备磷酸铁后母液中均含有大量的na
和nh
4
,使后续母液处理困难;并且使用硫酸铁或硫酸亚铁作为铁源制备磷酸铁的反应体系中含有大量so
42-,使制备的磷酸铁二水合物中夹带部分硫酸根,影响产品纯度。因此,有必要在形成磷酸铁前,对反应体系中的so
42-进行净化,最大化避免so
42-对磷酸铁产品的影响。现有技术中鲜有对磷酸铁反应体系中的so
42-进行清除的报道。
6.湿法磷酸是制备磷酸铁最常使用的磷源。湿法磷酸是由硫酸或盐酸等强酸分解磷矿,经过液固分离后所得的含有多种杂质的磷酸。湿法磷酸成本低廉,来源广泛,但是未净化的湿法磷酸中含有ca、mg、al、fe、f等杂质,若要用于生产电池级磷酸铁需要进一步净化。
7.专利文献cn 202110746350.2公开了一种电池级磷酸铁的制备方法,其中磷酸铁的铁源为硫酸亚铁,磷源为湿法磷酸,技术人员首先选择将湿法磷酸与碱性化合物混合熟化,将湿法磷酸净化后得到磷清液;将硫酸亚铁氧化为硫酸铁;硫酸铁与磷清液反应得到磷酸铁浆液,液固分离得到磷酸铁。首先,所述技术方案中选择碱性化合物为氨水、氢氧化钠、氢氧化钾等,使磷酸铁制备后的母液中含有大量na
、nh
4
,为后续母液处理增加难度。其次,硫酸铁与磷清液的反应体系中含有大量so
42-,这样会使得生成的磷酸铁产品中硫含量升高,影响磷酸铁产品品质。
技术实现要素:
8.为了避免以硫酸亚铁盐为铁源时,反应体系中的so
42-对磷酸铁产品的影响,本发明提供的制备方法首先在反应体系中加入硫酸根沉淀剂,沉淀剂与体系中的so
42-反应生成沉淀,使在形成磷酸铁产品之前先将体系中的so
42-进行净化,得到的磷酸铁产品中硫杂质含量更低。进一步的,本发明使用的硫酸根沉淀剂还能将湿法磷酸中的部分杂质沉淀分离,如f离子等,在无需对湿法磷酸进行除杂处理的基础上也能制备得到杂质含量低的磷酸铁
产品。
9.本发明包括如下技术方案:
10.第一方面,本发明提供一种片状电池级磷酸铁的制备方法,所述方法包括:
11.(1)向湿法磷酸中加入碱性钙盐至体系ph为2.5-4.0,得到磷酸钙盐溶液;
12.(2)将磷酸钙盐溶液与硫酸亚铁溶液按照ca/s摩尔比为0.8-2.5混合,在温度为20-80℃条件下反应,过滤,得到硫酸钙沉淀和脱硫液;
13.(3)向脱硫液中加入氧化剂充分氧化,同时加入ph调节剂控制溶液ph值为1.2-1.6,升温至90-95℃,固液分离,得到粗磷酸铁,洗涤,烘干,煅烧,得到磷酸铁产品。
14.优选的,步骤(3)分离粗磷酸铁后的滤液回流至步骤(1)制备磷酸钙盐的体系中。本发明提供的制备工艺为了使体系中的硫酸根彻底脱除,实际上磷酸钙盐溶液是大过量的,因此,步骤(3)分离粗磷酸后的母液是稀磷酸体系,将稀磷酸回流至步骤(1)中不仅可以实现磷的回收利用,还具有稀释湿法磷酸的作用,减少工业用水稀释湿法磷酸。
15.步骤(1)所述的碱性钙盐选自碳酸钙或碳酸钙含量≥5%的矿物质、石灰(cao)、石灰乳(ca(oh)2)、磷酸钙、磷酸氢钙中的一种或两种以上的组合,其中,碳酸钙含量≥5%的矿物质包括但不限于石灰石、大理石、方解石。
16.在本发明的优选实施方式中,所述碱性钙盐选自碳酸钙。
17.本发明所述的湿法磷酸是指是指使用硫酸分解磷矿得到的有一定杂质含量的h3po4溶液。
18.步骤(2)所述的磷酸亚铁溶液来自硫酸与铁反应得到的硫酸亚铁溶液,或者,将含有fe
2
和fe
3
的混合溶液经过还原制备得到。
19.按照本发明提供的方法将磷酸钙盐溶液与硫酸亚铁溶液按照ca/s摩尔比为1-2.0,具体如1.0、1.1、1.2、1.3、1.4、1.5、1.6、1.7、1.8、1.9、2.0,混合,此时钙离子是过量的,钙离子与硫酸根离子形成硫酸钙沉淀,过滤硫酸根彻底脱除,同时还能脱除部分杂质离子,如f离子等。
20.进一步,优选将磷酸钙盐溶液与硫酸亚铁溶液按照ca/s摩尔比为1-1.5混合。更优选的,ca/s摩尔比为1.3-1.5。
21.本发明步骤(3)所述的氧化剂选自双氧水、臭氧、空气、过氧化钠、过硫酸铵中的一种或两种以上的组合。
22.在本发明的优选实施方式中,所述氧化剂为双氧水。
23.步骤(3)向体系中加入氧化剂将磷酸亚铁氧化成磷酸铁,反应方程式为:2fe
2
2h2po
4- h2o2 2h2o
→
2fepo4·
2h2o
↓
2h
,氧化过程产生的会使反应体系的ph降低,同时磷酸铁沉淀消耗体系中的水,进一步降低反应体系ph。当体系的ph<1.2时,磷酸铁则无法沉淀,因此,此时需要向体系中加碱性ph调节剂控制体系ph在1.2-1.6之间,保证磷酸铁可正常析出。
24.本发明使用的ph调节剂选自水、氨水、氢氧化钠中的一种或两种以上的组合。由于氨水中含有n,氢氧化钠中含有na,均会向体系中引入其他杂质元素,本发明最优选的ph调节剂选自水。
25.在本发明的最优选实施方式中,所述片状电池级磷酸铁的制备方法包括如下步骤:
26.(1)在预中和罐中,以湿法磷酸为原料加水稀释,调整湿法磷酸p浓度为2.3-4.9,加入碱性钙盐使体系ph为2.5-4.0,30℃-80℃条件下反应1-4h得到磷酸钙盐溶液;
27.(2)将磷酸钙盐溶液通入脱硫罐中,加入硫酸亚铁溶液,磷酸钙盐溶液与硫酸亚铁按照ca/s摩尔比为1-1.5混合,20-80℃条件下反应,过滤,得到硫酸钙沉淀和脱硫液;
28.(3)将脱硫液通入氧化罐中,加入氧化剂充分氧化,同时加入ph调节剂控制溶液ph值为1.2-1.6,升温至90-95℃,固液分离,得到粗磷酸铁,滤液回流至预中和罐中;
29.(4)使用纯水对粗磷酸铁进行洗涤,直至洗水电导率低于500us/cm;
30.(5)烘干,煅烧,得到磷酸铁产品。
31.常规制备电池级磷酸铁使用的铁源一般采用硫酸盐的形式,而硫酸亚铁为铁源的主流工艺可根据使用的中和剂和其他阳离子的不同可分为铵盐法和钠盐法;硫酸铵盐和硫酸钠盐溶解度较大不会进入磷酸铁的沉淀中,但铵盐法与钠盐法制备磷酸铁后母液中均含有大量的钠离子与铵根离子,处理困难;硫酸根体系制备的磷酸铁二水物中依然会夹带部分的硫酸根;在煅烧过程中硫酸根会溢出,影响磷酸铁锂电池的能量密度。
32.本发明提供的片状磷酸铁制备方法具有如下技术优势:
33.(1)本发明技术人员开创性的在磷酸亚铁体系中使用过量钙离子与硫酸根生成硫酸钙沉淀,将体系中的硫酸根离子彻底脱除,实现深度脱硫,为生成磷酸铁创造一个低硫酸根环境,再通过氧化磷酸亚铁制备得到磷酸铁。解决了常规方法由于硫酸钙残留造成磷酸铁产品中钙硫升高的问题。
34.(2)本发明技术人员预料不到的发现,先使用过量磷酸钙盐脱除体系硫酸根后制备得到的磷酸铁产品晶体形状为片状,与现有技术中高纯铁粉与磷酸制备得到的磷酸铁产品晶体形状非常相似,说明按照本发明提供的方法可以制备得到质量很高的磷酸铁产品。
35.(3)本发明在氧化得到粗磷酸亚铁后,将滤液回流至磷酸钙盐制备体系中,形成残余磷酸与钙盐的循环利用。
36.(4)本发明在制备电池级磷酸铁过程中先将湿法磷酸与碱性钙盐预中和反应得到磷酸钙盐溶液,再将得到的磷酸钙盐与硫酸亚铁混合制备磷酸铁,这种操作方式与将湿法磷酸、碱性钙盐、硫酸亚铁溶液同时混合反应相比,技术人员预料不到的发现,先进行预中和反应再与硫酸亚铁反应制备得到的硫酸钙纯度更高,品质更好。因为将碱性钙盐与硫酸亚铁、湿法磷酸同时混合,无法避免的会造成反应体系局部碱性过高,部分铁会生成氢氧化铁沉淀,与硫酸钙一起沉淀出来,不仅会导致体系铁损较大,而且影响硫酸钙品质。
附图说明
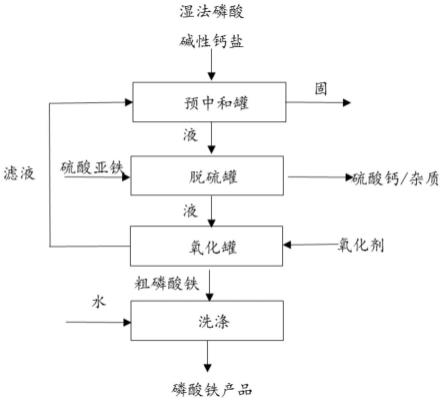
37.图1片状电池级磷酸铁制备工艺流程图
38.图2实施例1制备的磷酸铁产品电镜图(2万倍)
39.图3对照2市售磷酸铁产品电镜图(2万倍)
具体实施方式
40.下面将对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅是本发明的部分实施例,而不是全部。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例都属于本发明保护的范围。
41.本发明实施例使用的湿法磷酸和硫酸亚铁成分如下表所示:
42.表1湿法磷酸成分表
[0043][0044]
表2硫酸亚铁成分表
[0045][0046]
电池级磷酸铁的制备
[0047]
实施例1
[0048]
s1:在预中和罐中,以湿法磷酸为原料加水稀释,调整湿法磷酸总p浓度为3.0,加入碳酸钙使体系ph为4.0,40℃条件下反应2h得到磷酸钙盐溶液;
[0049]
s2:将磷酸钙盐溶液通入脱硫罐中,加入硫酸亚铁溶液,磷酸钙盐溶液与硫酸亚铁按照ca/s摩尔比为1.5混合,35℃条件下反应,过滤,得到硫酸钙沉淀和脱硫液;
[0050]
s3:将脱硫液通入氧化罐中,加入双氧水充分氧化,同时加入水调节体系ph值为1.2,升温至95℃,固液分离,得到粗磷酸铁,滤液回流至预中和罐中;
[0051]
s4:使用纯水对粗磷酸铁进行洗涤,直至洗水电导率低于500us/cm;
[0052]
s5:烘干,煅烧,得到磷酸铁产品。图2是本实施例制备得到的磷酸铁产品电镜图,从图中可以看到磷酸铁呈片状,与以纯度99%的铁粉和工业磷酸一铵为原料,使用氨水调节ph值制备得到的磷酸铁(对照2)产品电镜图(图3)相似。
[0053]
实施例2
[0054]
制备方法与原料同实施例1,区别仅在于步骤s1中加入碳酸钙使体系ph为3.0,40℃条件下反应2h得到磷酸钙盐溶液,其他步骤同实施例1,最终制备得到磷酸铁产品。
[0055]
实施例3
[0056]
制备方法与原料同实施例1,区别仅在于步骤s1中加入碳酸钙使体系ph为2.5,40℃条件下反应2h得到磷酸钙盐溶液,其他步骤同实施例1,最终制备得到磷酸铁产品。
[0057]
实施例4
[0058]
制备方法与原料同实施例1,区别仅在于步骤s2中磷酸钙盐溶液与硫酸亚铁按照ca/s摩尔比为1.0混合,其他步骤同实施例1,最终制备得到磷酸铁产品。
[0059]
实施例5
[0060]
制备方法与原料同实施例1,区别仅在于步骤s2中磷酸钙盐溶液与硫酸亚铁按照ca/s摩尔比为1.3混合,其他步骤同实施例1,最终制备得到磷酸铁产品。
[0061]
实施例6
[0062]
制备方法与原料同实施例1,区别仅在于步骤s2中磷酸钙盐溶液与硫酸亚铁按照ca/s摩尔比为2.0混合,其他步骤同实施例1,最终制备得到磷酸铁产品。
[0063]
对比例1
[0064]
参照实施例1的加料量,省略其步骤s1的预中和环节,将湿法磷酸溶液、硫酸亚铁溶液和碳酸钙一起加入脱硫罐中混合,保证ca/s摩尔比为1.5,35℃条件下反应,过滤,得到硫酸钙沉淀和脱硫液;分离出硫酸钙,将脱硫液通入氧化罐中,加入双氧水充分氧化,同时加入水调节体系ph值为1.2,升温至95℃,固液分离,得到粗磷酸铁,滤液丢弃;使用纯水对粗磷酸铁进行洗涤,直至洗水电导率低于500us/cm;烘干,煅烧,得到磷酸铁产品。
[0065]
效果例1磷酸铁产品参数检测
[0066]
检测本发明实施例1-6制备的磷酸铁成分,结果如下表所示。其中,对照1磷酸铁为云南某新能源公司所提供样品,是二次还原铁粉和磷酸为原料,使用nh3调节ph值制备得到;对照2磷酸铁为四川某饲料钙盐公司的新能源研发基地所提供样品,是二次还原铁粉和磷酸为原料,使用naoh调节ph值制备得到。
[0067]
表3磷酸铁产品成分表
[0068][0069]
根据上表数据可以看出实施例1-3中随着碳酸钙调节磷酸ph值的降低,磷酸铁产品品质下降,实施例1中磷酸铁品质最高。在碳酸酸钙调节ph值过程中发现,当ph值高于3.5后磷酸损失量变大,p浓度下降。实施例4-6随着ca/s的增加,实现深度脱s,产品中s含量大幅降低。但当ca/s为2时(实施例6),过量的钙会导致产品中ca含量升高。因此ca/s最佳比例为1.3-1.5。从上表数据还可以看出,对照1和对照2的市售磷酸铁产品中s含量明显偏高。
[0070]
效果例2硫酸钙产品品质检测
[0071]
通过比较实施例1-6和对比例1得到的硫酸钙品质,本发明技术人员发现,先将湿法磷酸与碳酸钙在预中和罐中进行初反应制备得到磷酸钙盐溶液,再与硫酸亚铁溶液混合后制备得到的硫酸钙沉淀纯度更高,品质更好。表4为实施例1-6和对比例1制备工艺得到的硫酸钙产品纯度检测数据。
[0072]
表4硫酸钙产品纯度(%)
[0073]
实施例1实施例2实施例3实施例4实施例5实施例6对比例197.1296.4193.5197.3397.0896.8388.41
[0074]
通过上表数据表可以看到,对比例1的硫酸钙产品纯度最差,因为当把湿法磷酸溶液、硫酸亚铁溶液和碳酸钙一起加入脱硫罐后,无法避免的会发生溶液局部过碱使部分亚
铁离子发生沉淀,这部分沉淀会随着硫酸钙沉淀一起被分离出来,不仅会造成硫酸钙产品纯度不高以外,还会造成反应体系的铁损失。
[0075]
最后应说明的是:以上各实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述各实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。
