舒肝宁注射液及其特征化合物在制备oats抑制剂中的应用
技术领域
1.本发明属于中药技术领域,具体涉及舒肝宁注射液及其特征化合物在制备oats抑制剂中的应用。
背景技术:
2.肾脏是机体重要的排泄器官之一,临床常用药物大多需要经肾排泄,其中一部分药物的主要排泄器官即为肾脏。肾近曲小管介导的分泌和重吸收是肾脏排泄过程的重要组成部分,肾近曲小管上皮细胞中的药物浓度与分布于其基底膜侧和顶膜侧的转运体密切相关。分布于肾近曲小管上皮细胞基底膜侧的转运体以摄取型转运体为主,介导阴离子底物从血液向近曲小管转运,分为有机阳离子转运体和有机阴离子转运体(oats);分布于顶膜侧的转运体以外排型转运体为主。其中,有机阴离子转运体oat1和oat3对药物及其代谢物的肾排泄起着关键作用,受其影响的药物包括抗生素类、质子泵抑制剂、以及部分抗肿瘤药等临床常用药物,抑制oat1和oat3能够减少这些药物的排泄,提高其血药浓度,从而降低用药剂量,减少药物过量带来的不良反应。另有研究发现,抑制oat1和oat3还可作为减少汞致肾毒性的方法之一。
技术实现要素:
3.针对以上技术问题,本发明提供了一种舒肝宁注射液及其特征化合物在制备oats抑制剂中的应用。本发明通过实验研究发现,舒肝宁注射液及其特征化合物黄芩苷、千层纸素a能够抑制oat1和oat3转运体,栀子苷和绿原酸能够抑制oat3转运体,故可用于制备通过抑制上述转运体的oats抑制剂。
4.为达到上述发明目的,本发明实施例采用了如下技术方案:
5.第一方面,本发明提供舒肝宁注射液在制备oats抑制剂中的应用,所述oats抑制剂为抑制oat1和oat3转运体的抑制剂。
6.本发明通过研究发现,舒肝宁注射液对主要表达于肾脏的oat1和oat3转运体具有显著的抑制作用。舒肝宁注射液的上述抑制作用使其能够用于制备抑制oat1和oat3的oats抑制剂。
7.第二方面,本发明还提供舒肝宁注射液的特征化合物在制备oats抑制剂中的应用,所述特征化合物为黄芩苷、千层纸素a、栀子苷或绿原酸中的至少一种,所述oats抑制剂为抑制oat1和/或oat3转运体的抑制剂。经实验发现,黄芩苷是oat1,oat3的底物,低浓度的黄芩苷对oat3介导的底物摄取有明显的抑制作用,高浓度的黄芩苷对oat1、oat3转运体介导的底物摄取均表现出较强抑制作用,可用于制成抑制oat1和/或oat3的oats抑制剂;低浓度和高浓度的千层纸素a对oat1、oat3转运体介导的底物摄取均表现出较强抑制作用,可用于制成抑制oat1和/或oat3的抑制剂;高浓度的栀子苷选择性地抑制oat3介导的底物摄取,可用于制成抑制oat3的抑制剂;低浓度的绿原酸对于oat3介导的底物摄取有一定的抑制作用,浓度增加时该抑制作用相应增加,并对oat1介导的底物摄取表现出一定的抑制作用,可
用于制成抑制oat1和/或oat3的oats抑制剂。
8.第三方面,本发明还提供一种增强经肾排泄药物的疗效的药物,所述药物的活性成分包括黄芩苷、千层纸素a、栀子苷和绿原酸中的至少一种。
9.结合第三方面,所述经肾排泄药物包括抗生素类药物、质子泵抑制剂、他汀类药物、缬沙坦、利福平以及经肾排泄的抗肿瘤药。
10.结合第三方面,当所述药物的活性成分包括黄芩苷和千层纸素a中的至少一种时,所述药物为抑制oat1和/或oat3转运体的药物;当所述药物的活性成分包括栀子苷和绿原酸中的至少一种时,所述药物为抑制oat3转运体的药物。
11.优选地,所述药物的剂型为静脉注射剂。以上单体口服生物利用度低,不易达到抑制oat1、oat3所需浓度,故优选采用静脉注射的给药方式。
12.可选地,所述药物还包括药学上可接受的辅料。辅料的具体类别和用量根据制剂需求进行常规选择即可,本发明对此不做限定。
13.第四方面,本发明还提供一种减少汞致肾毒性的药物,所述药物的活性成分包括黄芩苷、千层纸素a、栀子苷和绿原酸中的至少一种。
14.结合第四方面,当所述药物的活性成分包括黄芩苷和千层纸素a中的至少一种时,所述药物为抑制oat1和/或oat3转运体的药物;当所述药物的活性成分包括栀子苷和绿原酸中的至少一种时,所述药物为抑制oat3转运体的药物。
15.优选地,所述药物的剂型为静脉注射剂。
16.可选地,所述药物还包括药学上可接受的辅料。辅料的具体类别和用量根据制剂需求进行常规选择即可,本发明对此不做限定。
17.本发明的有益效果在于:本发明通过实验研究发现,舒肝宁注射液及其特征化合物黄芩苷、千层纸素a能够抑制oat1和oat3转运体,栀子苷和绿原酸能够抑制oat3转运体,故舒肝宁注射液及上述特征化合物可用于制备oats抑制剂,进而能够用于制备通过抑制相应转运体来增强经肾排泄药物的疗效的药物以及减少汞致肾毒性的药物。在临床使用经肾排泄药物时,可将其与舒肝宁注射液或含有黄芩苷、千层纸素a、栀子苷和绿原酸中的至少一种的药物配合使用,以降低经肾排泄药物的给药剂量,减少后者引起的其他方面的不良反应。当临床预防、治疗汞致肾毒性时,可结合具体的治疗方案和舒肝宁注射液及其上述特征化合物的药理作用进行单独用药或联合用药,以减少汞对肾脏的损伤。
附图说明
18.图1为本发明实施例1中舒肝宁注射液三个临床相关浓度对转运体的抑制作用;
19.图2为本发明实施例1中舒肝宁注射液浓度依赖性抑制作用及半数抑制浓度;
20.图3为本发明实施例1中黄芩苷、千层纸素a、栀子苷、绿原酸在7个slc转运体细胞与ev细胞内含量的比值;
21.图4为本发明实施例1中黄芩苷、千层纸素a、栀子苷、绿原酸在转运体中的抑制作用;
22.图5为本发明实施例1中黄芩苷、千层纸素a、栀子苷、绿原酸在转运体中的浓度依赖性抑制曲线及ic
50
;
23.图6为本发明实施例2中舒肝宁注射液对呋塞米血药浓度和清除率的影响;
具体实施方式
24.为了使本发明的目的、技术方案及优点更加清楚明白,以下结合附图及实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
25.舒肝宁注射液,清热解毒,利湿退黄,益气扶正,保肝护肝。用于湿热黄疸,症见面目俱黄,胸肋胀满,恶心呕吐,小便黄赤,乏力,纳差,便溏;急、慢性病毒性肝炎见前述症状者。目前并未见舒肝宁注射液作为oats抑制剂的报道。
26.本发明通过实验研究发现,舒肝宁注射液及其部分特征性化合物对oat1和oat3转运体有不同程度的抑制作用,可作为oats抑制剂,一方面可利用该机制来减少经肾排泄药物的排泄,提高其血药浓度,进而减少给药量,另一方面可以通过该机制来减少汞所致的肾毒性。
27.以下通过具体实施例对本发明的方案进行说明。
28.以下实施例中所采用的其他原料、试剂等,如无特殊说明,均从商业途径获得。
29.实施例1
30.本实施例提供了舒肝宁注射液及其特征化合物对oat1、oat3的抑制作用。
31.1.材料与方法
32.1.1细胞
33.过表达oat1、oat3、p-gp、bcrp转运蛋白的细胞,以及相应的空载细胞(ev)。
34.1.2主要试剂
35.舒肝宁注射液(贵州瑞和制药有限公司,生产批号20200325)。
36.黄芩苷(阿拉丁,99%),千层纸素a(上海源叶,99%),绿原酸(索莱宝,98%),栀子苷(索莱宝,98%),6-羧基荧光素、罗丹明、赫斯特试剂(rho123,上海源叶),丙磺舒(sigma,98%),酮康唑(sigma,99%),新生霉素(阿拉丁,95%)。其他普通化学品(如氯化钠等)购自天津江天化工技术股份有限公司。
37.1.3主要仪器
38.ultimate 3000超高性能液体系统(thermo fisher scientific,san jose,ca,usa);q-exactive
tm
混合四极杆-orbitrap质谱仪(thermo fisher scientific,san jose,ca,usa)细胞间超净工作台:thermo fisher(中国)公司;co2恒温培养箱:thermo fisher(中国)公司;细胞计数仪:上海睿钰生物科技有限公司;微量移液器:eppendorf(上海)国际贸易有限公司;分析天平:德国sartorius集团;ph计:德国sartorius集团;酶标仪:瑞士tecan公司。
39.1.4实验方法
40.1.4.1细胞培养
41.将细胞复苏,以含10%胎牛血清,1%pen/strep的dmem常规培养,第三代至第十代细胞用于实验。
42.1.4.2底物实验
43.选取舒肝宁注射液的4个特征化合物(黄芩苷,栀子苷,千层纸素a,绿原酸)进行单体底物验证。
44.将过表达oat1、oat3、p-gp、bcrp转运蛋白的细胞及相应的ev细胞以相同数量接种
于12孔板内。以上4个特征化合物单体以100μm的终浓度( /-阳性抑制剂)加入细胞中进行摄取实验初步鉴定。摄取实验结束后以反复“冻-融”方式获得细胞裂解液,用于液质定量。p-gp和bcrp细胞底物采用transwell细胞小室进行外排作用验证,收集小室两侧液体进行检测。
45.1.4.3抑制实验
46.按照舒肝宁注射液说明书推荐使用剂量和方法,确定三个临床相关剂量0.2%,1%,4%(v/v)进行注射液整体抑制作用评估。与底物实验相同,分别对4个特征化合物进行摄取抑制实验,选择100μm单体抑制作用》50%的化合物,在相应转运体中进行剂量响应曲线的绘制。
47.1.4.4液质检测
48.1.4.4.1液相条件
49.采用ultimate 3000超高性能液体系统检测。
50.色谱柱:waters acquity uplc beh c18(250mm
×
4.6mm,1.7μm)
51.流动相:流动相a为0.1%v/v甲酸水溶液,流动相b为乙腈。
52.梯度洗脱程序为:0
→
6分钟,98%a
→
0%a,2%b
→
100%b;6
→
8分钟,0%a
→
0%a,100%b
→
100%b;8
→
8.5分钟,0%a
→
98%a,100%b
→
2%b;8.5
→
10分钟,98%a
→
98%a,2%b
→
2%b。
53.柱温:35℃;
54.流速:0.3ml/min;
55.进样量:2μl;
56.样品室温度:15℃;
57.1.4.4.2质谱条件
58.通过q-exactive
tm
混合四极杆-orbitrap质谱仪采集样品的质谱数据。
59.电喷雾电离源(esi源)的主要参数如下:喷雾电压,(-)-esi为3.0kv,( )-esi为3.5kv;鞘气压力,35psi;辅助气体压力,10arb(n2,纯度99.9%);吹扫气体压力,0arb;毛细管温度,400℃;辅助气加热温度,450℃。
60.full-ms的扫描范围为m/z100-1500,分辨率设置为70,000。
61.应用数据相关扫描(dd-ms2)来获取高质量的二级质谱数据。通过高能碰撞诱导解离(hcd)自动选择前5个最强的前体进行ms/ms碎裂。dd-ms2的参数:分辨率,17,500;隔离窗口,4m/z。归一化碰撞能量(nce)设置为30、40和50v。所有数据均由thermo scientific xcalibur 4.0软件(thermo fisher scientific)记录和处理。
62.2.实验结果与讨论
63.2.1舒肝宁注射液
64.不同浓度的舒肝宁注射液对转运蛋白oat1、oat3、p-gp、bcrp有不同程度的抑制作用,如图1所示。
65.舒肝宁注射液对主要表达于肾脏的oat1和oat3的抑制作用最强,在最低浓度(0.2%)条件下对oats的抑制率》70%;
66.舒肝宁注射液对于abc家族的两个外排转运体p-gp和bcrp抑制作用较弱。
67.以上数据表明oat1和oat3容易受到舒肝宁注射液的影响,且影响作用远大于p-gp
和bcrp。该结果提示舒肝宁注射液可用于制成通过抑制转运体oat1和oat3而减少汞致肾毒性的药物。
68.为进一步探究舒肝宁注射液的抑制作用,绘制注射液剂量依赖性响应曲线,并评估半数抑制浓度(ic
50
)。如图2所示,舒肝宁注射液在oat1和oat3中的ic
50
均小于1
‰
注射液浓度,对外排转运体p-gp和bcrp的抑制作用弱于摄取类转运体,提示临床使用时的最大血药浓度可能会抑制肾脏oat1和oat3的主动分泌。
69.2.2特征化合物
70.在slc转运体对黄芩苷的摄取实验中,oat1,oat3细胞内的化合物含量与ev细胞内的比值分别为4.10,3.87倍。可见,在当前实验条件下,黄芩苷是这两个转运体的底物。而千层纸素a、栀子苷、绿原酸在oat1,oat3和空载细胞中的含量比值均低于2,可见,在当前实验条件下,千层纸素a、栀子苷、绿原酸不是这两个转运体的底物。如图3所示。
71.将以上四种单体以10μm和100μm的浓度分别进行抑制作用考察,如图4所示:当化合物以低浓度(10μm)处理细胞时,黄芩苷对oat3介导的底物摄取表现出明显的抑制作用(62.5%);栀子苷对oat1、oat3的抑制作用均不明显;千层纸素a对oat1和oat3表现出同等强度的抑制作用(》50%);绿原酸可将oat3介导的6-cf转运的能力降低一半。当单体以高浓度(100μm)处理细胞时,黄芩苷和千层纸素a对oat1、oat3转运体介导的底物摄取均表现出较强抑制作用;栀子苷选择性地抑制oat3介导的6-cf转运,然而对结构功能相近的oat1没有明显抑制作用;绿原酸在oat3介导的跨膜转运中的抑制率》50%。
72.综合上述分析,本部分得到以下结论:1)注射液中的黄芩苷和千层纸素a最容易引发oat1、oat3转运体抑制;2)栀子苷和绿原酸表现出很强的oat3选择性抑制,这可能取决于化合物结构与膜蛋白上的活性位点。
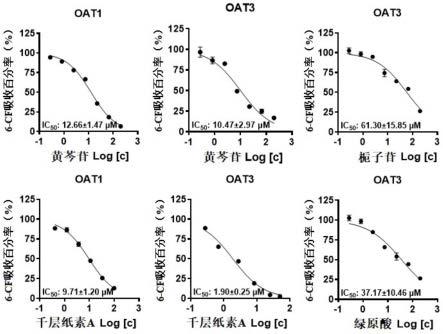
73.将图4中100μm单体抑制作用》50%的化合物,在相应转运体中进行剂量响应曲线的绘制,并评估ic
50
。如图5所示,黄芩苷在oat1和oat3中的ic
50
约为10μm;栀子苷在oat3中的ic
50
约为60μm;千层纸素a是当前作用最强的oat3的抑制剂,其ic
50
《2μm;绿原酸在oat3中的ic
50
约为40μm。
74.实施例2
75.本实施例提供了舒肝宁注射液作为oats抑制剂增强呋塞米疗效的应用。呋塞米是一种强效利尿药,经由oats转运进入肾脏进行主动分泌。
76.1、实验材料
77.舒肝宁注射液(贵州瑞和制药有限公司,生产批号20200325)。
78.sd雄性大鼠,200~220g,实验前12h禁食(不禁水)。
79.将上述雄性大鼠随机分为两组,分别为对照组和实验组,每组8只。
80.2、给药方案
81.对照组大鼠按10mg/kg的剂量尾静脉注射生理盐水,10min后按10mg/kg(以活性成分计)的剂量尾静脉注射呋塞米注射液;
82.实验组大鼠按10mg/kg的剂量尾静脉注射舒肝宁注射液,10min后按10mg/kg(以活性成分计)的剂量尾静脉注射呋塞米注射液。
83.3、实验结果
84.如图6所示,与对照组相比,实验组大鼠的呋塞米血药浓度增加,清除率降低。
85.实施例3
86.本实施例提供一种通过抑制oat1和oat3转运体以增强经肾排泄药物的疗效的静脉注射剂,活性成分为黄芩苷。
87.实施例4
88.本实施例提供一种通过抑制oat1和oat3转运体以增强经肾排泄药物的疗效的静脉注射剂,活性成分为千层纸素a。
89.实施例5
90.本实施例提供一种通过抑制oat1和oat3转运体以增强经肾排泄药物的疗效的静脉注射剂,活性成分为黄芩苷和千层纸素a。
91.实施例6
92.本实施例提供一种通过抑制oat3转运体以增强经肾排泄药物的疗效的静脉注射剂,活性成分为栀子苷。
93.实施例7
94.本实施例提供一种通过抑制oat3转运体以增强经肾排泄药物的疗效的静脉注射剂,活性成分为绿原酸。
95.实施例8
96.本实施例提供一种通过抑制oat3转运体以增强经肾排泄药物的疗效的静脉注射剂,活性成分为栀子苷和绿原酸。
97.实施例9
98.本实施例提供一种通过抑制oat1和oat3转运体以减少汞致肾毒性的静脉注射剂,活性成分为黄芩苷。
99.实施例10
100.本实施例提供一种通过抑制oat1和oat3转运体以减少汞致肾毒性的静脉注射剂,活性成分为千层纸素a。
101.实施例11
102.本实施例提供一种通过抑制oat1和oat3转运体以减少汞致肾毒性的静脉注射剂,活性成分为黄芩苷和千层纸素a。
103.实施例12
104.本实施例提供一种通过抑制oat3转运体以减少汞致肾毒性的静脉注射剂,活性成分为栀子苷。
105.实施例13
106.本实施例提供一种通过抑制oat3转运体以减少汞致肾毒性的静脉注射剂,活性成分为绿原酸。
107.实施例14
108.本实施例提供一种通过抑制oat3转运体以减少汞致肾毒性的静脉注射剂,活性成分为栀子苷和绿原酸。
109.以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换或改进等,均应包含在本发明的保护范围之内。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。