1.本发明涉及一种质子泵抑制药物及其制备方法,特别涉及奥美拉唑钠冻干粉针剂及制备方法。
背景技术:
2.奥美拉唑钠为胃壁细胞质子泵抑制剂,能特异性地抑制壁细胞顶端膜构成的分泌性微管和胞浆内的管状泡上的h
、k
-atp酶,从而有效地抑制胃酸的分泌。由于h
、k
-atp酶是壁细胞泌酸的最后一个过程,故本品抑酸能力强大。它不仅能非竞争性抑制促胃液素、组胺、胆碱及食物、刺激迷走神经等引起的胃酸分泌,而且能抑制不受胆碱或h2受体阻断剂影响的部分基础胃酸分泌,对h2受体拮抗剂不能抑制的由二丁基环腺苷酸(dcamp)刺激引起的胃酸分泌也有强而持久的抑制作用。本品对胃蛋白酶分泌也有抑制作用,对胃黏膜血流量改变不明显,也不影响体温、胃腔温度、动脉血压、静脉血红蛋白、动脉氧分压、二氧化碳分压及动脉血ph。
3.注射用奥美拉唑钠临床应用较广泛,药效迅速,可减少胃肠道粘膜的刺激性,且冻干粉针剂易于贮藏、方便运输且更能保证无菌无热原。原研为阿斯利康公司的,处方组成为奥美拉唑钠、依地酸二钠、氢氧化钠、注射用水。
4.奥美拉唑钠是苯并咪唑类化合物奥美拉唑的钠盐,化学名称为5-甲氧基-2-{[(4-甲氧基-3,5-二甲基-2-吡啶基)-甲基]-亚磺酰基}-1h-苯并咪唑钠。奥美拉唑钠溶液稳定性不好,放置时间过长容易氧化降解变色,有关物质增长快。
[0005]
现有技术中有大量研究工作致力于奥美拉唑钠冻干粉针剂的处方优化或冻干工艺的优化。
[0006]
专利cn200610042004.1公开了一种由奥美拉唑钠、甘露醇、依地酸二钠、ph调节剂组成的冻干粉针剂。
[0007]
专利cn200810062160.3公开了一种由奥美拉唑钠、β-环糊精、亚硫酸钠、依地酸二钠、硼砂-碳酸钠组成的冻干粉针剂。
[0008]
专利cn200810211501.9公开了一种由奥美拉唑钠、葡聚糖、稳定剂、亚硫酸钠、聚甲基丙烯酸甲酯、冻干骨架组成的复杂处方。相比原研处方增加了很多辅料,不仅提高了制剂成本,而且在临床应用上大大增加了潜在的不良反应风险。
技术实现要素:
[0009]
本发明提供了一种奥美拉唑钠冻干粉针剂及其制备方法,主要通过控制ph调节范围,同时降低配液过程及灌装过程中注射用水的温度来维持药液的稳定性,获得的冻干成品质量更稳定,处方工艺简单,制备的冻干粉针剂质量及稳定性好。
[0010]
本发明提供了一种奥美拉唑钠冻干粉针剂,它是由奥美拉唑钠、依地酸二钠和氢氧化钠组成,其中,在单位剂量中,奥美拉唑钠和依地酸二钠分别为40mg和1.5mg。
[0011]
在本发明的实施方案中,所述奥美拉唑钠冻干粉针剂是由如下制备方法制得的,
所述制备方法包括配液,所述的配液为:
[0012]
先将依地酸二钠溶于80%注射用水,用氢氧化钠水溶液调节ph,再加入奥美拉唑钠搅拌溶解,补加剩余注射用水至全量。
[0013]
在本发明的实施方案中,所述奥美拉唑钠冻干粉针剂是由如下制备方法制得的,所述制备方法在配液后还包括过滤和灌装。
[0014]
在一些实施方案中,本发明优选的氢氧化钠溶液调节ph范围为11.3~11.8。
[0015]
在一些实施方案中,本发明优选的配液温度以及灌装过程中贮藏为不超过15℃。
[0016]
在一些实施方案中,所述制备方法包括将处方量依地酸二钠溶于温度不高于15℃注射用水中,用1m氢氧化钠溶液调节ph值为11.3~11.8,再加入处方量奥美拉唑钠溶解,补足注射用水至全量,药液存储及灌装过程中温度不得高于15℃;再经串联的0.45μm和0.22μm聚醚砜滤器过滤,灌装,冻干,出箱即得奥美拉唑钠冻干粉针。
[0017]
在一些实施方案中,本发明还提出了奥美拉唑钠冻干粉针剂的冻干过程,优选地,90min降温至-40℃预冻120min;升华干燥:90min升温至-5℃,保持600min;解析干燥:20min升温至5℃,保持45min,20min升温至15℃,保持45min,20min升温至25℃,保持150min。
[0018]
另一方面,本发明提供了一种奥美拉唑钠冻干粉针剂的制备方法,所述的制备方法包括步骤如下:
[0019]
(1)配液
[0020]
先将依地酸二钠溶于80%注射用水,用氢氧化钠水溶液调节ph,再加入奥美拉唑钠搅拌溶解,补加剩余注射用水至全量;
[0021]
(2)过滤和灌装
[0022]
将步骤(1)得到的溶液进行过滤,然后灌装;
[0023]
(3)冻干
[0024]
将灌装后的产品进行冻干。
[0025]
在上述实施方案中,本发明氢氧化钠溶液调节ph范围为11.3~11.8。
[0026]
在上述实施方案中,所述过滤为经串联的0.45μm和0.22μm聚醚砜滤器过滤。
[0027]
在上述实施方案中,本发明所述配液、灌装过程以及存储中的温度为不超过15℃。
[0028]
在一些实施方案中,所述制备方法包括将处方量依地酸二钠溶于温度不高于15℃注射用水中,用1m氢氧化钠溶液调节ph值为11.3~11.8,再加入处方量奥美拉唑钠溶解,补足注射用水至全量,药液存储及灌装过程中温度不得高于15℃;再经串联的0.45μm和0.22μm聚醚砜滤器过滤,灌装,冻干,出箱即得奥美拉唑钠冻干粉针。
[0029]
在上述实施方案中,所述冻干的程序为:90min降温至-40℃预冻120min;升华干燥:90min升温至-5℃,保持600min;解析干燥:20min升温至5℃,保持45min,20min升温至15℃,保持45min,20min升温至25℃,保持150min。
[0030]
有益效果:本发明制备的奥美拉唑钠冻干粉针剂,在制备过程中冻干原液稳定性好,存放时间长;成品性状色泽稳定,复溶性、质量稳定性好。。
具体实施方式
[0031]
下面通过实施例来进一步描述本发明。对于本领域技术人员而言,根据本发明的教导,采用现有技术对下列实施例进行等同替换式改进仍属于本发明的保护范围。
[0032]
实施例1-3
[0033]
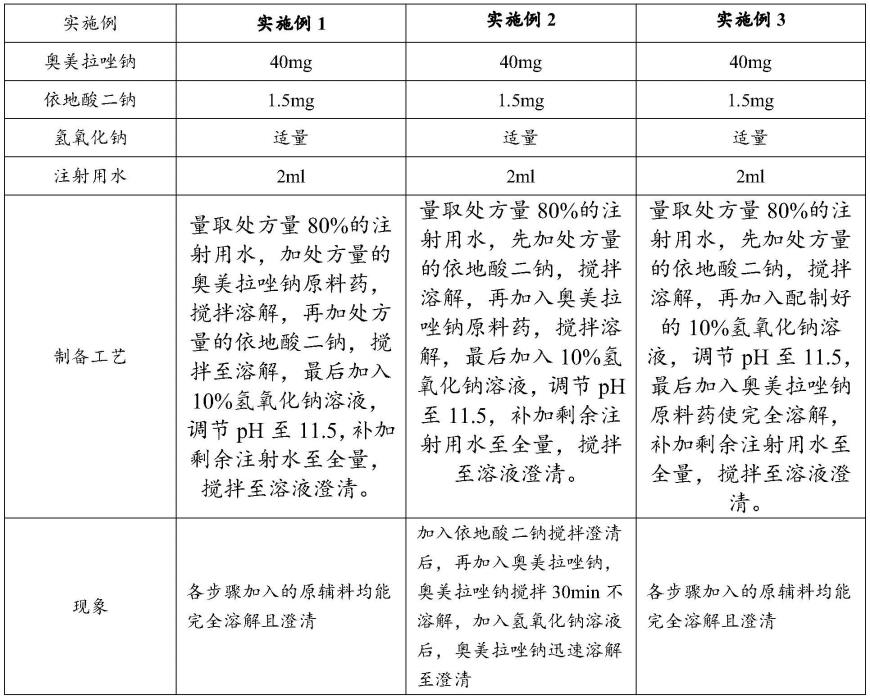
按上述原辅料比例制备奥美拉唑钠冻干原液,具体制备过程如下:
[0034][0035]
实施例2配液顺序得到的药液不澄清,奥美拉唑钠无法完全溶解,不符合中间产品质量标准。考虑到奥美拉唑钠的溶液稳定性与液体ph值相关较大,碱性条件溶液稳定性好,因此不选用实施例1的配液顺序,优选实施例3进行配液,即处方量80%的水溶解依地酸二钠后,用10%氢氧化钠溶液调节ph,再加入奥美拉唑钠搅拌溶解后,补加剩余水至全量。
[0036]
实施例4-8
[0037]
按上述原辅料比例制备奥美拉唑钠冻干原液,具体制备过程如下:
[0038]
实施例实施例4实施例5实施例6实施例7实施例8奥美拉唑钠40mg40mg40mg40mg40mg依地酸二钠1.5mg1.5mg1.5mg1.5mg1.5mg氢氧化钠适量适量适量适量适量注射用水2ml2ml2ml2ml2mlph调节值11.011.311.511.812.0
[0039]
冻干原液制备过程:量取处方量80%的注射用水,先加处方量的依地酸二钠,搅拌溶解至澄清,加入配制好的10%氢氧化钠溶液,调节ph,再加入奥美拉唑钠原料药使完全溶解,补加剩余注射用水至全量,搅拌至溶液澄清,。将药液分别灌装至西林瓶中,充氮密封,分别至15℃、20℃和30℃条件下,8h后取出,经串联的0.45μm和0.22μm聚醚砜滤器过滤,灌装量为2.0ml。
[0040]
冻干工艺:将药液灌装放入冻干箱中,进行冷冻干燥:90min降温至-40℃预冻
120min;升华干燥:90min升温至-5℃,保持600min;解析干燥:20min升温至5℃,保持45min,20min升温至15℃,保持45min,20min升温至25℃,保持150min。
[0041]
表1实施例4-8药液在不同温度下放置8h后的药液颜色和冻干成品外观
[0042][0043][0044]
表2实施例4-8冻干成品在高温40℃和60℃条件下外观及有关物质变化情况
[0045][0046]
从表1和表2中可以看出,配液ph和药液温度对奥美拉唑钠冻干粉针剂质量影响显著。药液温度越低,成品质量外观性状越好,优选配液温度不超过15℃,灌装贮藏温度不宜超过8小时。配液ph范围对药液稳定性和成品复溶后ph影响较大,优选配液ph范围为11.3~11.8。
[0047]
实施例9-11
[0048]
按上述原辅料比例制备奥美拉唑钠冻干原液,具体制备过程如下:
[0049]
实施例实施例9实施例10实施例11奥美拉唑钠40mg40mg40mg依地酸二钠1.5mg1.5mg1.5mg氢氧化钠适量适量适量注射用水2ml2ml2mlph调节值11.511.511.5
[0050]
冻干原液制备过程:量取处方量80%的注射用水降温至15℃以下,先加处方量的依地酸二钠,搅拌溶解至澄清,加入配制好的10%氢氧化钠溶液,调节ph,再加入奥美拉唑钠原料药使完全溶解,补加剩余注射用水至全量,搅拌至溶液澄清,。将药液分别灌装至西林瓶中,8h后取出,经串联的0.45μm和0.22μm聚醚砜滤器过滤,灌装量为2.0ml。冻干前药液温度保持不超过15℃。
[0051][0052]
表3实施例9-11冻干成品质量对比
[0053][0054]
从表3可以看出,解析干燥阶段快速升温对制剂成品的外观、水分、碱度、复溶和有关物质均无显著影响,且均符合2020年中国药典“注射用奥美拉唑钠”质量标准要求。故优
选进行冷冻干燥程序为:90min降温至-40℃预冻120min;升华干燥:90min升温至-5℃,保持600min;解析干燥:20min升温至5℃,保持45min,20min升温至15℃,保持45min,20min升温至25℃,保持150min。
[0055]
按照实施例9确定的配液工艺和冻干工艺制备1批奥美拉唑钠冻干粉针,按市售包装后,并与原研洛赛克同时放置于加速条件40℃
±
2℃、相对湿度75%rh
±
%rh条件下,分别于0、3、6月取样一次,对性状、碱度、有关物质及含量进行测定,结果见表4。
[0056]
表4实施例9的奥美拉唑钠冻干粉针加速试验结果
[0057][0058]
从表4中可以看出,本发明的奥美拉唑钠冻干粉针剂在加速条件下质量稳定性不劣于原研洛赛克,且均符合2020版中国药典二部“注射用奥美拉唑钠”的质量标准要求。本发明的奥美拉唑钠冻干粉针剂处方工艺简单合理,处方组成与原研一致,可满足大生产的需求,经过加速稳定性考察表明,本发明的奥美拉唑钠冻干粉针剂稳定性好。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。