1.本发明涉及磁共振放射治疗技术领域,特别是涉及一种磁共振放射治疗机质控仿真模体构建方法及系统。
背景技术:
2.近年来,为解决传统治疗机器x射线影像引导软组织分辨率不足够,无法清晰捕捉到肿瘤和周围危及器官的变化的难题,磁共振系统和放射治疗系统集成在同一平台,自此mr放射治疗机进入到放射治疗领域。目前,放射治疗的计划设计大多为调强放射治疗,计划子野繁多且形状各异;mr影像中心和放射治疗中心通常可能存在偏差;m r图像受磁场或其他因素影像可能发生畸变,次级电子在静态磁场中受洛伦兹力改变,实际运动路径发生了扭转,导致电子流效应,从而影响了mr放射治疗机中的剂量分布。针对这些mr放射治疗机面临的问题,业内专家和物理师设计了各个mr放射治疗机质控的步骤和对应的模体,来进行mr图像和剂量的质量控制,包括水箱,日检模体,调强验证模体,图像验证模体等等。
3.然而,由于受磁共振对其工作环境和安全性的严格要求,常规放射治疗机质控模体无法直接应用于mr放射治疗机。现有用于mr放射治疗机质量控制检测模体大多依赖于进口或者厂商配置,价格昂贵、功能相对单一且不易使用。mr加速研究表明mr图像的几何畸变和剂量影响等都与模体的大小位置息息相关,例如,在离中心20cm的体积内,mr图像的几何畸变基本控制在1mm以内,超过此范围的图像畸变迅速增加,在离中心20~25cm的范围内,部分区域的图像畸变》 2mm。另外对于每个患者肿瘤位置和大小都不相同,如果采用现有技术的模体,只能显示当下模体的图像和受照剂量,无法和临床关心的靶区和器官相关联。
技术实现要素:
4.本发明的目的是提供一种磁共振放射治疗机质控仿真模体构建方法,通过根据临床需求定制化设计个体质控仿真模体,解决现有质控模体的应用缺陷,可以满足临床案例的个体化治疗需求,既可单独用于mr放射治疗机图像和剂量的质量控制,又可实现从图像引导到剂量验证的端对端测试验证,为磁共振放射治疗机的放疗应用提供可靠的质量保证。
5.为了实现上述目的,有必要针对上述技术问题,提供了一种磁共振放射治疗机质控仿真模体构建方法及系统。
6.第一方面,本发明实施例提供了一种磁共振放射治疗机质控仿真模体构建方法,所述方法包括以下步骤:
7.获取待构建模体的结构文件;所述结构文件包括患者外轮廓、靶区和感兴趣器官的structure文件;
8.将所述结构文件导入3d打印重建系统,生成第一仿真模体;
9.确定所述第一仿真模体的待测目标位置和所需测量设备;所述待测目标位置包括靶区位置和感兴趣器官位置;
10.获取所需测量设备对应的设备插件,并将所述设备插件插至所述待测目标位置,得到第二仿真模体,以及将所述第二仿真模体进行3d 打印,得到镂空模体;
11.获取待构建模体的医学图像的成像参数信息,根据所述成像参数信息,拟合确定靶区和感兴趣器官对应填充材料的浓度配比;
12.将靶区和感兴趣器官的填充材料按照对应的浓度配比加入黏合剂内,加热熔合并填充至所述镂空模体的对应位置,冷却得到质控仿真模体。
13.进一步地,所述3d打印重建系统包括3d slicer系统。
14.进一步地,所述医学图像包括ct图像和mr图像;所述成像参数信息包括靶区和感兴趣器官的t1弛豫时间、t2弛豫时间与ct数值;所述填充材料包括调节t1弛豫时间材料、调节t2弛豫时间材料和调节ct数值材料。
15.进一步地,所述调节t1弛豫时间材料为三氯化钆、二乙烯三胺五乙酸螯合镍和镓中的一种;所述调节t2弛豫时间材料为琼脂糖;所述调节ct数值材料为硫酸钡、碳酸钙和玻璃微球的一种;所述黏合剂为卡拉胶和明胶中的一种。
16.进一步地,所述获取待构建模体的医学图像的成像参数信息,根据所述成像参数信息,拟合确定靶区和感兴趣器官对应填充材料的浓度配比的步骤包括:
17.根据预设浓度梯度,分别将调节t1弛豫时间材料、调节t2弛豫时间材料和调节ct数值材料单独加入黏合剂,获取对应不同浓度值下的t1弛豫时间、t2弛豫时间和ct数值;
18.根据不同浓度值下的t1弛豫时间、t2弛豫时间和ct数值,拟合得到对应的t1弛豫时间模型、t2弛豫时间模型和ct数值模型;
19.分别根据靶区和感兴趣器官的成像参数信息,结合t1弛豫时间模型、t2弛豫时间模型和ct数值模型,分别确定靶区和感兴趣器官对应填充材料的浓度配比。
20.进一步地,所述加热熔合并填充至所述镂空模体的对应位置的步骤包括:
21.根据预设温度进行加热,并在均匀搅拌后填充至所述镂空模体的对应位置。
22.进一步地,所述冷却得到质控仿真模体的步骤还包括:
23.采用热塑性材料对所述质控仿真模体的外口进行封装。
24.第二方面,本发明实施例提供了一种磁共振放射治疗机质控仿真模体构建系统,所述系统包括:
25.结构获取模块,用于获取待构建模体的结构文件;所述结构文件包括患者外轮廓、靶区和感兴趣器官的structure文件;
26.模体预建模块,用于将所述结构文件导入3d打印重建系统,生成第一仿真模体,并确定所述第一仿真模体的待测目标位置和所需测量设备;所述待测目标位置包括靶区位置和感兴趣器官位置;
27.插件配置模块,用于获取所需测量设备对应的设备插件,并将所述设备插件插至所述待测目标位置,得到第二仿真模体,以及将所述第二仿真模体进行3d打印,得到镂空模体;
28.浓度选取模块,用于获取待构建模体的医学图像的成像参数信息,根据所述成像参数信息,拟合确定靶区和感兴趣器官对应填充材料的浓度配比;
29.模体生成模块,用于将靶区和感兴趣器官的填充材料按照对应的浓度配比加入黏合剂内,加热熔合并填充至所述镂空模体的对应位置,冷却得到质控仿真模体。
30.第三方面,本发明实施例还提供了一种计算机设备,包括存储器、处理器及存储在存储器上并可在处理器上运行的计算机程序,所述处理器执行所述计算机程序时实现上述方法的步骤。
31.第四方面,本发明实施例还提供一种计算机可读存储介质,其上存储有计算机程序,所述计算机程序被处理器执行时实现上述方法的步骤。
32.上述本技术提供了一种磁共振放射治疗机质控仿真模体构建方法及系统,通过所述方法,实现了通过将获取待的构建模体的结构文件导入3d打印重建系统生成第一仿真模体后,确定待测目标位置和所需测量设备,并获取所需测量设备的设备插件插至待测目标位置得到第二仿真模体,并将第二仿真模体进行3d打印得到镂空模体,再获取待构建模体医学图像的成像参数信息,拟合确定靶区和感兴趣器官对应填充材料的浓度配比,并将靶区和感兴趣器官的填充材料按照对应的浓度配比加入黏合剂加热熔合并填充至镂空模体,冷却得到质控仿真模体的技术方案。与现有技术相比,该磁共振放射治疗机质控仿真模体构建方法,能够根据临床需求定制化设计个体质控仿真模体,有效满足临床案例的个体化治疗需求,既可单独用于mr放射治疗机图像和剂量的质量控制,又可实现从图像引导到剂量验证的端对端测试验证,为磁共振放射治疗机的放疗应用提供可靠的质量保证。
附图说明
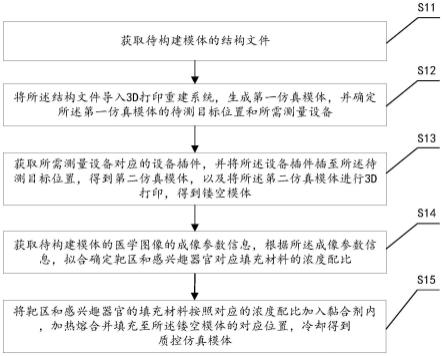
33.图1是本发明实施例中磁共振放射治疗机质控仿真模体构建方法的流程示意图;
34.图2是本发明实施例中二维医学图像及对应三维重建图像的示意图;
35.图3是本发明实施例中磁共振放射治疗机质控仿真模体构建系统的结构示意图;
36.图4是本发明实施例中计算机设备的内部结构图。
具体实施方式
37.为了使本技术的目的、技术方案和有益效果更加清楚明白,下面结合附图及实施例,对本发明作进一步详细说明,显然,以下所描述的实施例是本发明实施例的一部分,仅用于说明本发明,但不用来限制本发明的范围。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
38.本发明考虑到由于受磁共振对工作环境和安全性的严格要求,导致常规放射治疗机的质控模体无法用于mr放射治疗机,而现有用于 mr放射治疗机质量控制检测模体大多依赖于进口或者厂商配置,功能单一、价格昂贵且不能满足临床个体差异化需求,进而无法为磁共振放射应用提供很好的质量保证的应用缺陷,提供了一种基于3d打印的磁共振放射治疗机质控仿真模体构建方法用于定制化构建质控仿真模体,以确保治疗的高精度效果;下述实施例将对本发明的一种磁共振放射治疗机质控仿真模体构建方法进行详细说明。
39.在一个实施例中,如图1所示,提供了一种磁共振放射治疗机质控仿真模体构建方法,包括以下步骤:
40.s11、获取待构建模体的结构文件;所述结构文件可理解为具体病例的治疗相关结构数据,包括患者外轮廓、靶区和感兴趣器官的 structure文件;其中,患者外轮廓可理解为皮肤;感兴趣器官可理解为放疗科医生认为受靶区照射影响较大的组织,也称危及器官;上述结构文件可理解为医生在如图2左边所示的放射治疗计划系统的ct图像或mr图像上勾
画处相应的区域保存得到结构(structure)dicom文件。
41.s12、将所述结构文件导入3d打印重建系统,生成第一仿真模体,并确定所述第一仿真模体的待测目标位置和所需测量设备;所述待测目标位置包括靶区位置和感兴趣器官位置;其中,所述3d打印重建系统原则上可以使用解读dicom格式文件的3d系统,本实施例优选地,采用3d slicer系统;所需测量设备根据患者采用核磁共振放射机治疗所需的剂量测量设备,包括电离室、半导体探测仪、胶片和热释光剂量仪等;
42.将获取的患者外轮廓、靶区和感兴趣器官的structure文件加载至 3d打印重建系统后,就可以由该3d打印重建系统完成所需打印结构文件的3d重建,得到没有添加剂量测量插件的第一仿真模体。对应的第一仿真模体上的待测目标位置理解为需要测量的病例部位,可根据实际病例的情况确定,且所需测量设备也是根据实际治疗需求选取。
43.s13、获取所需测量设备对应的设备插件,并将所述设备插件插至所述待测目标位置,得到第二仿真模体,以及将所述第二仿真模体进行3d打印,得到镂空模体;其中,所需测量设备与设备插件必须配套使用,因测量设备的大小和形状可能都有差异,具体设备插件可以是矩形或圆柱形,测量设备从外插入至内,即需要根据测量设备的形状大小定制设备插件的插孔,可在3d打印重建系统中预先对常用的测量设备设置固定的设备插件,若需要使用一个新的测量设备,则只要知道它的尺寸,也可以通过勾画添加到系统内。将测量设备插入对应的设备插件后,再将设备插件插入重建的第一仿真模体的3d待测目标位置替换对应的组织,就是将插件经过的肿瘤(靶区)或正常感兴趣器官组织的位置直接替换为对应的设备插件,得到如图二右侧图像所示的包含所需测量设备(电离室测量孔与胶片横断面插孔)的第二仿真模体;至此得到的第二仿真模体包括仿真模体外部及内部基本轮廓,经过3d打印就能获取靶区和感兴趣器官位置都是镂空的镂空模体,后续可根据需求通过下述步骤在各个镂空部位填入所需的填充材料,构建得到完整的个体定制化质控仿真模体。
44.s14、获取待构建模体的医学图像的成像参数信息,根据所述成像参数信息,拟合确定靶区和感兴趣器官对应填充材料的浓度配比;其中,所述医学图像包括ct图像和mr图像;所述成像参数信息包括靶区和感兴趣器官的t1弛豫时间、t2弛豫时间与ct数值;所述填充材料可理解为实际影响t1弛豫时间、t2弛豫时间和ct数值的材料,包括调节t1弛豫时间材料、调节t2弛豫时间材料和调节ct数值材料,具体的,各种材料的选取可根据实际需求结合现有技术确定,优选地,调节t1弛豫时间材料可为三氯化钆、二乙烯三胺五乙酸螯合镍和镓等;调节t2弛豫时间材料为琼脂糖等;调节ct数值材料为硫酸钡、碳酸钙和玻璃微球等;所述黏合剂理论上可以使用与组织的生物、化学和物理相似性高的水凝胶,本实例优选采用卡拉胶或明胶。需要说明的是,上述各种材料的选取并不局限于以罗列的内容,若采用其他影响 t1弛豫时间、t2弛豫时间和ct数值的材料不会影响本发明方法的实现,即也在本发明的保护范围内;
45.在实际的镂空模体填充过程中,需要先根据实际应用需求确定所要使用调节t1弛豫时间的化学成分a,调节t2弛豫时间的化学成分 b,调节ct数值的化学成分c,并通过治疗计划系统中读取到ct、mr扫描图像中具体器官和靶区分别对应的t1、t2和ct值,例如,在1.5t mr扫描前列腺得到平均数值为:t1=1245、t2=92、hu=34;肝脏对应的平均数值分别为:t1=609、t2=47、hu=50;即不同的部位对应的t1、t2和ct值均不相同,所需的各个填充材料的浓度配比各不相同,需要在确定调节t1弛豫时间材料,调节t2弛豫时间材料,调节ct
数值材料后,进一步确定靶区及各个感兴趣器官的各种填充材料的浓度配比,用于实际填充所用;
46.具体的,所述获取待构建模体的医学图像的成像参数信息,根据所述成像参数信息,拟合确定靶区和感兴趣器官对应填充材料的浓度配比的步骤包括:
47.根据预设浓度梯度,分别将调节t1弛豫时间材料、调节t2弛豫时间材料和调节ct数值材料单独加入黏合剂,获取对应不同浓度值下的t1弛豫时间、t2弛豫时间和ct数值;需要说明的是,影响t1弛豫时间的a材料浓度值、影响t2弛豫时间的b材料浓度值和影响ct数值的c材料浓度值均与t1弛豫时间的倒数、t2弛豫时间的倒数和ct 数值线性相关;
48.根据不同浓度值下的t1弛豫时间、t2弛豫时间和ct数值,拟合得到对应的t1弛豫时间模型、t2弛豫时间模型和ct数值模型;其中, t1弛豫时间模型、t2弛豫时间模型和ct数值模型形式相同,可以理解为是分别以t1弛豫时间的倒数、t2弛豫时间的倒数和ct数值作为因变量,以影响t1弛豫时间的a材料浓度值、影响t2弛豫时间的b 材料浓度值和影响ct数值的c材料浓度值作为自变量,进行拟合得到的模型;在具体拟合过程中,需要先将不同浓度值下的t1弛豫时间、 t2弛豫时间先转换为对应倒数值,再与对应的ct数值一起联合使用,结合对应a材料浓度值、b材料浓度值和c材料浓度值拟合得到所需的t1弛豫时间模型、t2弛豫时间模型和ct数值模型;对应的,t1 弛豫时间模型、t2弛豫时间模型和ct数值模型可表示为:
49.y=ax1 bx2 cx3 e
ꢀꢀꢀꢀ
(1)
50.其中,y表示器官/靶区的t1弛豫时间的倒数、t2弛豫时间的倒数和ct数值;x1、x2和x3分别表示影响t1弛豫时间、t2弛豫时间和ct 数值的a、b、c材料的浓度比例(即为与t1弛豫时间的倒数、t2弛豫时间的倒数和ct数值线性相关的浓度值);a、b和c分别表示通过线性拟合可直接确定的对于a、b、c材料的拟合参数,e为常数项;
51.分别根据靶区和感兴趣器官的成像参数信息,结合t1弛豫时间模型、t2弛豫时间模型和ct数值模型,分别确定靶区和感兴趣器官对应填充材料的浓度配比;其中,靶区或感兴趣器官的浓度配比求解过程可理解为,将根据靶区或感兴趣器官对应的实测t1、t2和ct代入 (1)式就可以得到一个三元一次方程组,求解可得到对应的x1、x2和 x3,即得到了对应的浓度配比。
52.s15、将靶区和感兴趣器官的填充材料按照对应的浓度配比加入黏合剂内,加热熔合并填充至所述镂空模体的对应位置,冷却得到质控仿真模体;其中,所述加热熔合并填充至所述镂空模体的对应位置的步骤包括:
53.根据预设温度进行加热,并在均匀搅拌后填充至所述镂空模体的对应位置;对应的预设温度优选的为60度以上,即将靶区和感兴趣器官对应的影响t1弛豫时间、t2弛豫时间和ct数值的a、b、c材料按照上述得到浓度配比添加至黏合剂加热搅拌至均匀熔合后填充至镂空模体的对应区域内,待溶液冷却转为固态,即可得到图2右边所示的 3d质控仿真模体;此外,为了防止模体内填充料的晃动和脱离,本实施例优选地,采用热塑性材料对所述质控仿真模体的外口进行封装,其中热塑性材料包括pla,此处不作具体限制。
54.通过上述步骤即可实现了采用3d打印方法得到同时包含靶区和感器趣器官和测量插件的,满足临床案例各异化的需求,便于分析图像和剂量结果,确保治疗的高精度的质控仿真模体,该质控仿真模体可以代替患者本身,最终测量到从mr扫描定位到计划执行整
个过程造成的总体剂量误差,如可按照下述方法步骤使用该模体监测目标位置剂量:
55.1)对质控仿真模体进行ct扫描;2)扫描后将质控仿真模体医学图像和患者医学图像进行刚性配准,确保两者间位置保持一致,设定摆位标记点;3)将图像文件传输至治疗计划系统;4)将已完成的患者计划移植到此模体ct图像上,重新进行剂量计算,取得插件剂量仪的点剂量d计算或二维剂量分布;5)按照摆位标记点将模体放置到 mr治疗机上,在mr扫描后,放置测量设备执行治疗计划;6)读取电离室/热释光等一维设备的点剂量d测量,直接比对点剂量偏差δ= (d测量-d计算)/d计算,或扫描胶片剂量分布,使用二维剂量通过率gamma来评估剂量差异。
56.同时,还可以使用质控仿真模体实现mr图像和ct图像的定量比对,发现是否存在因为机器软硬件原因导致的图像畸变或伪影,具体检测过程如下:
57.1)在mr或ct影像图像质控结果良好的情况下,扫描质控仿真模体的ct、t1和t2图像,将这些图像设置为各自类型图像的基准;
58.2)在日常扫描质控仿真模体时,使用如下所示的平均绝对误差mae、峰值信噪比psnr和γ公式进行定量分析:
[0059][0060][0061][0062]
其中,y是这次扫描图像像素的实际数值,yi是基准图像像素的数值, n是模体内所有像素的数量;r2(y,yi)表示两像素位置距离平方,δd表示距离容差,可以用的1或2mm标准;δ2(y,yi)表示两像素间数值差异的平方,δd表示数值差异容差,可以用的1%或2%标准。psnr和γ数值越低则与原基准图像差异越大,出现伪影或畸变概率也越高。
[0063]
综上,使用本发明方法得到的质控仿真模体,能够有效监测患者目标位置剂量的合理使用和医学图像的可靠性,确保治疗的高精度和患者的治疗安全。
[0064]
本技术实施例通过将获取的病例对应的结构文件导入3d打印重建系统进行3d重建后,在待测目标位置插入实际治疗过程所需的测量设备后采用3d打印技术得到镂空模体,再根据实际病例医学图像的 t1弛豫时间、t2弛豫时间与ct数值,确定靶区和感兴趣器官对应填充材料的浓度配比,并将靶区和感兴趣器官的填充材料按照对应的浓度配比加入黏合剂加热熔合并填充至镂空模体,冷却封口得到质控仿真模体的方法,能够根据临床需求简单高效的得到个体定制化质控模体,有效满足临床案例的个体化治疗需求的同时,既可单独用于mr 放射治疗机图像和剂量的质量控制,又可实现从图像引导到剂量验证的端对端测试验证,为磁共振放射治疗机的放疗应用提供可靠的质量保,具有较高的应用价值。
[0065]
需要说明的是,虽然上述流程图中的各个步骤按照箭头的指示依次显示,但是这些步骤并不是必然按照箭头指示的顺序依次执行。除非本文中有明确的说明,这些步骤的执行并没有严格的顺序限制,这些步骤可以以其它的顺序执行。
[0066]
在一个实施例中,如图3所示,提供了一种磁共振放射治疗机质控仿真模体构建系统,所述系统包括:
[0067]
结构获取模块1,用于获取待构建模体的结构文件;所述结构文件包括患者外轮廓、靶区和感兴趣器官的structure文件;
[0068]
模体预建模块2,用于将所述结构文件导入3d打印重建系统,生成第一仿真模体,并确定所述第一仿真模体的待测目标位置和所需测量设备;所述待测目标位置包括靶区位置和感兴趣器官位置;
[0069]
插件配置模块3,用于获取所需测量设备对应的设备插件,并将所述设备插件插至所述待测目标位置,得到第二仿真模体,以及将所述第二仿真模体进行3d打印,得到镂空模体;
[0070]
浓度选取模块4,用于获取待构建模体的医学图像的成像参数信息,根据所述成像参数信息,拟合确定靶区和感兴趣器官对应填充材料的浓度配比;
[0071]
模体生成模块5,用于将靶区和感兴趣器官的填充材料按照对应的浓度配比加入黏合剂内,加热熔合并填充至所述镂空模体的对应位置,冷却得到质控仿真模体。
[0072]
关于一种磁共振放射治疗机质控仿真模体构建系统的具体限定可以参见上文中对于一种磁共振放射治疗机质控仿真模体构建方法的限定,在此不再赘述。上述一种磁共振放射治疗机质控仿真模体构建系统中的各个模块可全部或部分通过软件、硬件及其组合来实现。上述各模块可以硬件形式内嵌于或独立于计算机设备中的处理器中,也可以以软件形式存储于计算机设备中的存储器中,以便于处理器调用执行以上各个模块对应的操作。
[0073]
图4示出一个实施例中计算机设备的内部结构图,该计算机设备具体可以是终端或服务器。如图4所示,该计算机设备包括通过系统总线连接的处理器、存储器、网络接口、显示器和输入装置。其中,该计算机设备的处理器用于提供计算和控制能力。该计算机设备的存储器包括非易失性存储介质、内存储器。该非易失性存储介质存储有操作系统和计算机程序。该内存储器为非易失性存储介质中的操作系统和计算机程序的运行提供环境。该计算机设备的网络接口用于与外部的终端通过网络连接通信。该计算机程序被处理器执行时以实现一种磁共振放射治疗机质控仿真模体构建方法。该计算机设备的显示屏可以是液晶显示屏或者电子墨水显示屏,该计算机设备的输入装置可以是显示屏上覆盖的触摸层,也可以是计算机设备外壳上设置的按键、轨迹球或触控板,还可以是外接的键盘、触控板或鼠标等。
[0074]
本领域普通技术人员可以理解,图4中示出的结构,仅仅是与本技术方案相关的部分结构的框图,并不构成对本技术方案所应用于其上的计算机设备的限定,具体的计算设备可以包括比图中所示更多或更少的部件,或者组合某些部件,或者具有同的部件布置。
[0075]
在一个实施例中,提供了一种计算机设备,包括存储器、处理器及存储在存储器上并可在处理器上运行的计算机程序,处理器执行计算机程序时实现上述方法的步骤。
[0076]
在一个实施例中,提供了一种计算机可读存储介质,其上存储有计算机程序,计算机程序被处理器执行时实现上述方法的步骤。
[0077]
综上,本发明实施例提供的磁共振放射治疗机质控仿真模体构建方法及系统,其磁共振放射治疗机质控仿真模体构建方法实现了通过将获取待的构建模体的结构文件导入3d打印重建系统生成第一仿真模体后,确定待测目标位置和所需测量设备,并获取所需测量设备的设备插件插至待测目标位置得到第二仿真模体,并将第二仿真模体进行 3d打
印得到镂空模体,再获取待构建模体医学图像的成像参数信息,拟合确定靶区和感兴趣器官对应填充材料的浓度配比,并将靶区和感兴趣器官的填充材料按照对应的浓度配比加入黏合剂加热熔合并填充至镂空模体,冷却得到质控仿真模体的技术方案,该磁共振放射治疗机质控仿真模体构建方法,能够根据临床需求定制化设计个体质控仿真模体,有效满足临床案例的个体化治疗需求,既可单独用于mr放射治疗机图像和剂量的质量控制,又可实现从图像引导到剂量验证的端对端测试验证,为磁共振放射治疗机的放疗应用提供可靠的质量保证。
[0078]
本说明书中的各个实施例均采用递进的方式描述,各个实施例直接相同或相似的部分互相参见即可,每个实施例重点说明的都是与其他实施例的不同之处。尤其,对于系统实施例而言,由于其基本相似于方法实施例,所以描述的比较简单,相关之处参见方法实施例的部分说明即可。需要说明的是,上述实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实施例中的各个技术特征所有可能的组合都进行描述,然而,只要这些技术特征的组合不存在矛盾,都应当认为是本说明书记载的范围。
[0079]
以上所述实施例仅表达了本技术的几种优选实施方式,其描述较为具体和详细,但并不能因此而理解为对发明专利范围的限制。应当指出的是,对于本技术领域的普通技术人员来说,在不脱离本发明技术原理的前提下,还可以做出若干改进和替换,这些改进和替换也应视为本技术的保护范围。因此,本技术专利的保护范围应以所述权利要求的保护范围为准。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。