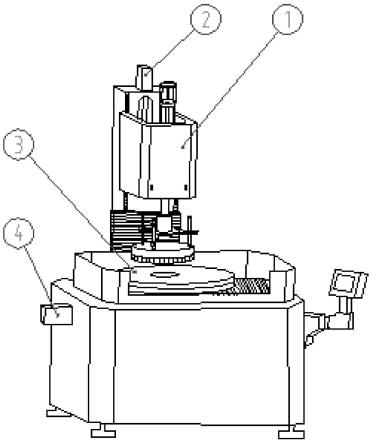
1.本发明涉及一种金属纳米团簇及其制备方法和应用,具体为一种可用于催化氢官能团化反应的金属纳米团簇及其制备方法。
背景技术:
2.以铁、钴等地球上储量丰富的廉价金属为核心的生物酶在自然界中广泛存在,其在生命体内的多种生物合成反应中起到了至关重要的催化作用。其活性中心常常包含活性金属团簇,如一氧化碳脱氢酶(codh)中的铁硫簇,承担着电子传递的重要作用。然而,至今为止人们对这些金属团簇的探索极为有限,这也是现代有机化学领域中一项具有挑战性的难题。
3.不饱和键的氢官能团化反应包括氢化、硼氢化、硅氢化、不饱和三键的半氢化等,广泛应用于有机合成中。该类反应大多需要贵金属和配体的参与,以保证转化效率及其化学选择性。近年来,科学家们设计并合成得到一系列铁、钴、镍、锰等金属的络合物,并将其应用于多种有机化学转化中。然而,这些络合物中的配体大多需要多步合成,耗时耗力,价格昂贵,限制了其在生产中的应用。此外,很多配体和络合物稳定性差,难以在空气中稳定存在,进一步限制了其应用价值。
4.因此,发展无配体参与的金属团簇催化剂具有重要的科研和实用价值。
技术实现要素:
5.为解决上述问题,本发明提供了一种金属纳米团簇,用作催化剂,催化不饱和键的氢官能团化反应,如氢化反应、硼氢化反应、硅氢化反应、不饱和三键的半氢化反应等。
6.本发明的第一方面,提供一种金属纳米团簇的制备方法,所述制备方法包括以下步骤:
7.金属盐和还原剂在碱作用下发生反应获得所述金属纳米团簇。
8.在另一优选例中,所述金属盐选自下组:锰盐、铁盐、钴盐、镍盐、铜盐,其中,
9.所述锰盐为mnf2、mncl2、mncl2·
4h2o、mnbr2、mnbr2·
4h2o、mni2、mni2·
4h2o、mnso4、mnso4·
h2o、mnso4·
4h2o、mn(co)5br、mn(oac)2、mn(oac)2·
4h2o、mn(oac)3·
2h2o、mn(acac)2、mn(acac)3、环戊二烯三羰基锰、甲基环戊二烯三羰基锰中的一种或两种以上;
10.所述铁盐为fef2、fecl2、febr2、fei2、fef3、fecl3、fecl3·
6h2o、febr3、febr3·
2thf、feso4、feso4·
h2o、feso4·
6h2o、fe(oac)2、fe(oh)(oac)2、fe2(co)9、fe3(co)
12
、fe(acac)2、fe(acac)3、fe(otf)3、fe(bf4)2·
6h2o、fe(nh3)2(so4)2、fe(nh3)2(so4)2·
6h2o、fe2(so4)3·
h2o、k3fe(cn)6、fe(clo4)3、fe(clo4)3·
h2o中的一种或两种以上;
11.所述钴盐为cof2、cof3、cocl2、cocl2·
h2o、cobr2、cobr2·
h2o、coi2、co(oac)2、co(acac)2、co(acac)3、co(nh3)6cl3、co(pph3)3cl、co(dppe)cl2、co2co3、co2(co)8中的一种或两种以上;
12.所述镍盐为nicl2、nicl2·
6h2o、nibr2、nibr2·
h2o、nii2、ni(acac)2、ni(oac)2、ni
(oac)2·
4h2o、ni(otf)2、ni(clo4)2·
6h2o、ni(bf4)2·
6h2o、ni(no3)2·
6h2o、niso4·
6h2o、ni(cod)2、ni(dme)cl2、ni(dme)br2、ni(dppe)cl2、ni(dppp)cl2、ni(pcy3)2cl2、ni(pph3)2cl2、ni(pph3)2br2、ni(nh3)6br2中的一种或两种以上;
13.所述铜盐为cucl、cubr、cui、cuf2、cucl2、cucl2·
2h2o、cubr2、cucn、cuoac、cu(oac)2、cu(oac)2·
h2o、cu(otf)2、cu(cn)4(pf6)、cu2(otf)2ph、cuso4、cu(nh4)2(so4)2·
6h2o、cuso4·
6h2o、cu(bf4)2、cu(bf4)2·
6h2o中的一种或两种以上。
14.在另一优选例中,所述还原剂为硼烷或者硅烷,其中,
15.所述硼烷为频哪醇硼烷、9-硼双环[3.3.1]壬烷、儿茶酚硼烷、硼烷-氨络合物中的一种或两种以上;
[0016]
所述硅烷为苯硅烷、二苯基硅烷、三苯基硅烷、苯基二甲基硅烷、二甲基(乙基)硅烷、二丙基(乙基)硅烷、二丁基(乙基)硅烷、二乙基硅烷、三乙基硅烷、二甲基苄基硅烷、二甲基苯乙基硅烷、三甲氧基硅烷、三乙氧基硅烷、三异丙氧基硅烷、苯基二乙氧基硅烷、二异丙基乙氧基硅烷、1,1,3,3-四甲基二硅氧烷中的一种或两种以上。
[0017]
在另一优选例中,所述碱为叔丁醇钾、叔丁醇钠、叔丁醇锂、异丙醇钾、异丙醇钠、异丙醇锂、乙醇钾、乙醇钠、乙醇锂、甲醇钾、甲醇钠、甲醇锂、碳酸锂、碳酸钠、碳酸钾、碳酸铯、氟化铯、氟化钾、氟化钠、氟化锂、醋酸铯、醋酸钾、醋酸钠、醋酸锂、双三甲基硅基胺基钾、双三甲基硅基胺基钠、双三甲基硅基胺基锂、三乙基硼氢化钾、三乙基硼氢化钠、三乙基硼氢化锂、三乙胺、二异丙基乙基胺、正丁基锂、甲基锂、苯基锂、格氏试剂中的一种或两种以上。
[0018]
在另一优选例中,所述反应在有机溶剂中进行或者无溶剂进行,所述有机溶剂为苯、甲苯、二甲苯、二氯甲烷、氯仿、四氯化碳、1,2-二氯乙烷、乙醚、四氢呋喃、甲基叔丁基醚、乙二醇二甲醚、乙二醇二乙醚、二乙二醇二甲醚、1,4-二氧六环、甲醇、乙醇、异丙醇、叔丁醇、正戊烷、正己烷、环己烷、n,n-二甲基甲酰胺、n,n-二甲基乙酰胺或二甲基亚砜中的一种或两种以上的混合溶剂。
[0019]
在另一优选例中,所述金属纳米团簇的粒径为0.1~200nm,所述反应底物与所述金属盐的摩尔比可为1:0.00001~0.1,也可以为其他比值。
[0020]
在另一优选例中,所述的碱与还原剂的摩尔比为0.001~3:1。
[0021]
本发明的第二方面,提供一种金属纳米团簇,由第一方面所述的制备方法制备获得。
[0022]
本发明的第三方面,提供第二方面所述的金属纳米团簇的用途,用作催化剂。
[0023]
在另一优选例中,所述催化剂用于催化不饱和键的氢官能团化反应。
[0024]
在另一优选例中,所述氢官能团化反应选自氢化反应、硼氢化反应、硅氢化反应、不饱和三键的半氢化反应。
[0025]
本发明的第四方面,提供一种催化剂,所述催化剂包含第三方面所述的金属纳米团簇。
[0026]
在另一优选例中,所述催化剂用于催化不饱和键的氢官能团化反应。
[0027]
在另一优选例中,所述氢官能团化反应选自氢化反应、硼氢化反应、硅氢化反应、不饱和三键的半氢化反应。
[0028]
本发明的第五方面,提供一种氢官能团化反应方法,所述氢官能团化反应方法包
括以下步骤:
[0029]
提供一混合物,所述混合包括反应底物、金属盐、碱和还原剂;
[0030]
其中,金属盐和还原剂在碱作用下发生反应获得金属纳米团簇,所述金属纳米团簇作为催化剂催化反应底物的氢官能团化反应;
[0031]
其中,所述反应底物选自:烯烃、炔烃、腈、亚胺、醛、酮、酸、酯和酰胺。
[0032]
在另一优选例中,所述金属盐选自下组:锰盐、铁盐、钴盐、镍盐、铜盐,其中,
[0033]
所述锰盐为mnf2、mncl2、mncl2·
4h2o、mnbr2、mnbr2·
4h2o、mni2、mni2·
4h2o、mnso4、mnso4·
h2o、mnso4·
4h2o、mn(co)5br、mn(oac)2、mn(oac)2·
4h2o、mn(oac)3·
2h2o、mn(acac)2、mn(acac)3、环戊二烯三羰基锰、甲基环戊二烯三羰基锰中的一种或两种以上;
[0034]
所述铁盐为fef2、fecl2、febr2、fei2、fef3、fecl3、fecl3·
6h2o、febr3、febr3·
2thf、feso4、feso4·
h2o、feso4·
6h2o、fe(oac)2、fe(oh)(oac)2、fe2(co)9、fe3(co)
12
、fe(acac)2、fe(acac)3、fe(otf)3、fe(bf4)2·
6h2o、fe(nh3)2(so4)2、fe(nh3)2(so4)2·
6h2o、fe2(so4)3·
h2o、k3fe(cn)6、fe(clo4)3、fe(clo4)3·
h2o中的一种或两种以上;
[0035]
所述钴盐为cof2、cof3、cocl2、cocl2·
h2o、cobr2、cobr2·
h2o、coi2、co(oac)2、co(acac)2、co(acac)3、co(nh3)6cl3、co(pph3)3cl、co(dppe)cl2、co2co3、co2(co)8中的一种或两种以上;
[0036]
所述镍盐为nicl2、nicl2·
6h2o、nibr2、nibr2·
h2o、nii2、ni(acac)2、ni(oac)2、ni(oac)2·
4h2o、ni(otf)2、ni(clo4)2·
6h2o、ni(bf4)2·
6h2o、ni(no3)2·
6h2o、niso4·
6h2o、ni(cod)2、ni(dme)cl2、ni(dme)br2、ni(dppe)cl2、ni(dppp)cl2、ni(pcy3)2cl2、ni(pph3)2cl2、ni(pph3)2br2、ni(nh3)6br2中的一种或两种以上;
[0037]
所述铜盐为cucl、cubr、cui、cuf2、cucl2、cucl2·
2h2o、cubr2、cucn、cuoac、cu(oac)2、cu(oac)2·
h2o、cu(otf)2、cu(cn)4(pf6)、cu2(otf)2ph、cuso4、cu(nh4)2(so4)2·
6h2o、cuso4·
6h2o、cu(bf4)2、cu(bf4)2·
6h2o中的一种或两种以上。
[0038]
在另一优选例中,所述还原剂为硼烷或者硅烷,其中,
[0039]
所述硼烷为频哪醇硼烷、9-硼双环[3.3.1]壬烷、儿茶酚硼烷、硼烷-氨络合物中的一种或两种以上;
[0040]
所述硅烷为苯硅烷、二苯基硅烷、三苯基硅烷、苯基二甲基硅烷、二甲基(乙基)硅烷、二丙基(乙基)硅烷、二丁基(乙基)硅烷、二乙基硅烷、三乙基硅烷、二甲基苄基硅烷、二甲基苯乙基硅烷、三甲氧基硅烷、三乙氧基硅烷、三异丙氧基硅烷、苯基二乙氧基硅烷、二异丙基乙氧基硅烷、1,1,3,3-四甲基二硅氧烷中的一种或两种以上。
[0041]
在另一优选例中,所述碱为叔丁醇钾、叔丁醇钠、叔丁醇锂、异丙醇钾、异丙醇钠、异丙醇锂、乙醇钾、乙醇钠、乙醇锂、甲醇钾、甲醇钠、甲醇锂、碳酸锂、碳酸钠、碳酸钾、碳酸铯、氟化铯、氟化钾、氟化钠、氟化锂、醋酸铯、醋酸钾、醋酸钠、醋酸锂、双三甲基硅基胺基钾、双三甲基硅基胺基钠、双三甲基硅基胺基锂、三乙基硼氢化钾、三乙基硼氢化钠、三乙基硼氢化锂、三乙胺、二异丙基乙基胺、正丁基锂、甲基锂、苯基锂、格氏试剂中的一种或两种以上。
[0042]
在另一优选例中,所述混合物中不包含有机溶剂,或者包含有机溶剂。
[0043]
在另一优选例中,所述反应在有机溶剂中进行或者无溶剂进行,所述有机溶剂为苯、甲苯、二甲苯、二氯甲烷、氯仿、四氯化碳、1,2-二氯乙烷、乙醚、四氢呋喃、甲基叔丁基
醚、乙二醇二甲醚、乙二醇二乙醚、二乙二醇二甲醚、1,4-二氧六环、甲醇、乙醇、异丙醇、叔丁醇、正戊烷、正己烷、环己烷、n,n-二甲基甲酰胺、n,n-二甲基乙酰胺或二甲基亚砜中的一种或两种以上的混合溶剂。
[0044]
在另一优选例中,所述的碱与还原剂的摩尔比为0.001~3:1。
[0045]
在另一优选例中,所述的碱、还原剂与反应底物的摩尔比为0.01~1:1~10:1。所述的碱、还原剂与反应底物的摩尔比为0.01~1:1~10:1。
[0046]
在另一优选例中,所述氢官能团化反应的路线为:
[0047][0048]
在碱作用下,金属盐和还原剂反应生成金属纳米团簇催化剂,催化式1化合物发生氢官能团化反应得到式2和式3化合物,
[0049]
各式中,r选自:h、c1-c6烷基、c1-c6烷氧基、卤素、c1-c6烷基硅基(三甲基硅基)、(c1-c6烷基)3硅氧基(叔丁基二甲基硅氧基)。
[0050]
在另一优选例中,所述氢官能团化反应的路线为:
[0051][0052]
在碱作用下,金属盐和还原剂反应生成金属纳米团簇催化剂,催化式4化合物发生氢官能团化反应得到式5化合物,进一步酸化得到式6化合物,
[0053]
各式中,r选自:c1-c10烷基、c3-c8环烷基、c6-c10芳基;任选地被选自下组的基团取代:c1-c6烷基、c1-c6卤代烷基、卤素、c1-c6烷氧基、c6-c10芳基、c6-c10芳基-o-。
[0054]
在另一优选例中,所述还原剂为频哪醇硼烷。
[0055]
在另一优选例中,所述氢官能化反应为硼氢化反应。
[0056]
本发明提供一混合物,所述混合物包括金属盐、碱、还原剂(硅烷或硼烷)、反应底物;所述的金属盐在混合物体系中现场生成所述金属纳米团簇,所述金属纳米团簇现场催化反应底物反应;其中,所述反应底物选自取代或未取代的烯烃、炔烃、腈、亚胺、醛、酮、酸、酯和酰胺,为无溶剂或溶解于有机溶剂中。
[0057]
本发明中所提供的金属纳米团簇在反应体系中原位生成,可以高效地催化不饱和键的氢官能团化反应。本发明的金属纳米团簇用于催化不饱和键的氢官能团化反应有许多优点:(1)使用元素储量丰富、廉价、商业化的廉价金属盐作为催化剂前体,避免了铱、铑、钯等贵金属的使用;(2)不需要各种空气敏感、稳定性较差、需多步化学反应制备得到的配体参与反应,具有经济性;(3)催化剂用量少、活性高,反应速度快。
[0058]
应理解,在本发明范围内中,本发明的上述各技术特征和在下文(如实施例)中具体描述的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。说明书中所揭示的各个特征,可以被任何提供相同、均等或相似目的的替代性特征取代。限于篇幅,在此不再一一累述。
附图说明
[0059]
图1为本发明实施例1溶剂为四氢呋喃获得的金属纳米团簇的透射电镜图。
[0060]
图2为本发明实施例1溶剂为四氢呋喃获得的金属纳米团簇与硼烷、苯乙烯形成的中间体的saesi-tof质谱图。
[0061]
具体实施方法
[0062]
体现本发明特征与优点的典型实施方式将在以下的说明中详细叙述。应理解的是本发明能够在不同的实施方式上具有各种的变化,其皆不脱离本发明的范围,且其中的说明及图示在本质上是当作说明之用,而非用以限制本发明。
[0063]
本发明提供了一种金属纳米团簇的制备方法,包括,提供一混合液,所述混合液包括金属盐、碱和还原剂;使所述混合液体系发生氧化还原反应,以将所述金属盐所包含的金属离子还原为金属原子,所述金属原子形成所述金属纳米团簇,所述金属纳米团簇作为催化剂催化有机反应;其中,所述反应底物选自取代或未取代的烯烃、炔烃、腈、亚胺、醛、酮、酸、酯和酰胺,为无溶剂或溶解于有机溶剂中。
[0064]
具体地,所述反应底物与所述金属盐的摩尔比优选为1:0.00001~0.02。
[0065]
具体地,所述金属盐选自下组:锰盐、铁盐、钴盐、镍盐、铜盐,其中,
[0066]
所述锰盐为mnf2、mncl2、mncl2·
4h2o、mnbr2、mnbr2·
4h2o、mni2、mni2·
4h2o、mnso4、mnso4·
h2o、mnso4·
4h2o、mn(co)5br、mn(oac)2、mn(oac)2·
4h2o、mn(oac)3·
2h2o、mn(acac)2、mn(acac)3、环戊二烯三羰基锰、甲基环戊二烯三羰基锰中的一种或两种以上;
[0067]
所述铁盐为fef2、fecl2、febr2、fei2、fef3、fecl3、fecl3·
6h2o、febr3、febr3·
2thf、feso4、feso4·
h2o、feso4·
6h2o、fe(oac)2、fe(oh)(oac)2、fe2(co)9、fe3(co)
12
、fe(acac)2、fe(acac)3、fe(otf)3、fe(bf4)2·
6h2o、fe(nh3)2(so4)2、fe(nh3)2(so4)2·
6h2o、fe2(so4)3·
h2o、k3fe(cn)6、fe(clo4)3、fe(clo4)3·
h2o中的一种或两种以上;
[0068]
所述钴盐为cof2、cof3、cocl2、cocl2·
h2o、cobr2、cobr2·
h2o、coi2、co(oac)2、co(acac)2、co(acac)3、co(nh3)6cl3、co(pph3)3cl、co(dppe)cl2、co2co3、co2(co)8中的一种或两种以上;
[0069]
所述镍盐为nicl2、nicl2·
6h2o、nibr2、nibr2·
h2o、nii2、ni(acac)2、ni(oac)2、ni(oac)2·
4h2o、ni(otf)2、ni(clo4)2·
6h2o、ni(bf4)2·
6h2o、ni(no3)2·
6h2o、niso4·
6h2o、ni(cod)2、ni(dme)cl2、ni(dme)br2、ni(dppe)cl2、ni(dppp)cl2、ni(pcy3)2cl2、ni(pph3)2cl2、ni(pph3)2br2、ni(nh3)6br2中的一种或两种以上;
[0070]
所述铜盐为cucl、cubr、cui、cuf2、cucl2、cucl2·
2h2o、cubr2、cucn、cuoac、cu(oac)2、cu(oac)2·
h2o、cu(otf)2、cu(cn)4(pf6)、cu2(otf)2ph、cuso4、cu(nh4)2(so4)2·
6h2o、cuso4·
6h2o、cu(bf4)2、cu(bf4)2·
6h2o中的一种或两种以上。优选地,所述金属盐为cocl2、cobr2、coi2中的一种;可以将所述金属盐加入有机溶液中,配置成固定浓度的溶液加入反应体系。
[0071]
具体地,所述的碱为叔丁醇钾、叔丁醇钠、叔丁醇锂、乙醇钾、乙醇钠、乙醇锂、甲醇钾、甲醇钠、甲醇锂、碳酸锂、碳酸钠、碳酸钾、碳酸铯、氟化铯、氟化钾、氟化钠、氟化锂、醋酸铯、醋酸钾、醋酸钠、醋酸锂、双三甲基硅基胺基钾、双三甲基硅基胺基钠、双三甲基硅基胺基锂、三乙基硼氢化钾、三乙基硼氢化钠、三乙基硼氢化锂、三乙胺、二异丙基乙基胺、正丁基锂、甲基锂、苯基锂、格氏试剂中的一种或两种以上。优选地,反应中所选的碱为叔丁醇
钾、叔丁醇钠中的至少一种。
[0072]
具体地,所述的混合液为无溶剂或加入有机溶剂,所选的有机溶剂为苯、甲苯、二甲苯、二氯甲烷、氯仿、四氯化碳、1,2-二氯乙烷、乙醚、四氢呋喃、甲基叔丁基醚、乙二醇二甲醚、乙二醇二乙醚、二乙二醇二甲醚、1,4-二氧六环、甲醇、乙醇、异丙醇、叔丁醇、正戊烷、正己烷、环己烷、n,n-二甲基甲酰胺、n,n-二甲基乙酰胺或二甲基亚砜中的至少一种;优选地,反应中所选的有机溶剂为乙醚、四氢呋喃中的一种;优选地,反应底物在溶液中的浓度为0.2~5.0mol/l。
[0073]
具体地,所述的还原剂为硼烷或者硅烷。所述硼烷为频哪醇硼烷、9-硼双环[3.3.1]壬烷、儿茶酚硼烷、硼烷-氨络合物中的至少一种;所述硅烷为苯硅烷、二苯基硅烷、三苯基硅烷、苯基二甲基硅烷、二甲基(乙基)硅烷、二丙基(乙基)硅烷、二丁基(乙基)硅烷、二乙基硅烷、三乙基硅烷、二甲基苄基硅烷、二甲基苯乙基硅烷、三甲氧基硅烷、三乙氧基硅烷、三异丙氧基硅烷、苯基二乙氧基硅烷、二异丙基乙氧基硅烷、1,1,3,3-四甲基二硅氧烷中的一种或两种以上。。优选地,反应中所选的还原剂为频哪醇硼烷或苯硅烷中的一种。
[0074]
具体地,所述的碱、还原剂与反应底物的摩尔比为0.01~1:1~10:1。优选地,所述的碱、还原剂与反应底物的摩尔比为0.05~0.1:1~5:1;
[0075]
本发明的金属纳米团簇的制备方法所制备的金属团簇的粒径为0.1~200 nm,每个金属团簇含有几个到几百个金属原子。
[0076]
本发明中所提供的金属纳米团簇在反应体系中原位生成,可以高效地催化不饱和键的氢官能团化反应;所述的催化反应在惰性气体氛围下发生,于-78℃~100℃下反应0.1~72小时得到目标产物;优选为0~25℃。
[0077]
本发明的金属纳米团簇用于催化不饱和键的氢官能团化反应有许多优点:(1)使用元素储量丰富、廉价、商业化的廉价金属盐作为催化剂前体,避免了铱、铑、钯等贵金属的使用;(2)不需要各种空气敏感、稳定性较差、需多步化学反应制备得到的配体参与反应,具有经济性;(3)催化剂用量少、活性高,反应速度快。
[0078]
下面通过实施例对本发明进行具体的描述,有必要在此指出的是:以下实施例只用于对本发明进行进一步说明,不能理解为对本发明保护范围的限制,本领域的技术人员根据本发明的上述内容作出的一些非本质的改进和调整均属于本发明的保护范围。
[0079]
实施例1
[0080]
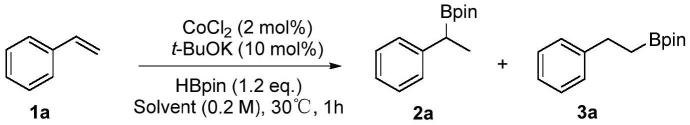
本实施例以苯乙烯为反应底物,叔丁醇钾为碱,频哪醇硼烷为还原剂,与金属盐cocl2现场制备金属纳米团簇催化剂,在不同溶剂下,催化底物苯乙烯的硼氢化反应。反应式如下:
[0081][0082]
反应如下:在手套箱中,cocl2(1.04mg,0.008mmol),叔丁醇钾(4.5mg,0.04mmol)和苯乙烯(41.6mg,0.4mmol)分别加入一10ml样品瓶中,加入表1中溶剂(2ml),加入频哪醇硼烷(61.4mg,0.48mmol)。室温下搅拌一小时后,在空气中淬灭,柱层析纯化,得到硼氢化产物。
[0083]
图1为溶剂为四氢呋喃获得的金属纳米团簇的透射电镜图,表明钴盐在还原剂和碱的作用下生成了纳米团簇。
[0084]
图2为溶剂为四氢呋喃获得的金属纳米团簇与硼烷、苯乙烯形成的中间体的saesi-tof质谱图,根据分子量判断为co3与苯乙烯、hbpin的结合,证明了催化体系中存在钴纳米团簇。
[0085]
表1:溶剂对硼氢化反应的影响
[0086][0087]
产率和选择性由气相色谱测定:1h nmr(400mhz,cdcl3)δ7.32
–
7.21(m,4h),7.19
–
7.12(m,1h),2.47(q,j=7.4hz,1h),1.37(d,j=7.5hz,3h),1.23(d,j=5.4hz,12h)ppm.
13
c nmr(101mhz,cdcl3)δ145.0,128.4,127.9,125.2,83.3,24.7,24.7,17.1ppm.
[0088]
实施例2
[0089]
本实施例以苯乙烯为反应底物,使用不同的碱,四氢呋喃为溶剂,频哪醇硼烷为还原剂,与金属盐coi2现场制备金属纳米团簇催化剂,催化底物苯乙烯的马氏硼氢化反应。反应式如下:
[0090][0091]
反应如下:在手套箱中,coi2(2.5mg,0.008mmol),碱(0.04mmol)和苯乙烯(41.6mg,0.4mmol)分别加入一10ml样品瓶中,加入thf(2ml),加入频哪醇硼烷(61.4mg,0.48mmol)。室温下搅拌一小时后,在空气中淬灭,柱层析纯化,得到硼氢化产物。
[0092]
表2:碱对硼氢化反应的影响
[0093][0094]
实施例3
[0095]
本实施例以苯乙烯为反应底物,叔丁醇钾为碱,四氢呋喃为溶剂,频哪醇硼烷为还原剂,与不同的金属钴盐现场制备金属纳米团簇催化剂,催化底物苯乙烯的硼氢化反应。反应式如下:
[0096][0097]
反应如下:在手套箱中,金属钴盐(0.008mmol),碱(4.5mg,0.04mmol)和苯乙烯(41.6mg,0.4mmol)分别加入一10ml样品瓶中,加入thf(2ml),加入频哪醇硼烷(61.4mg,0.48mmol)。室温下搅拌一小时后,在空气中淬灭,柱层析纯化,得到硼氢化产物。
[0098]
表3:金属钴盐前体对硼氢化反应的影响
[0099][0100]
实施例4
[0101]
本实施例以4-甲基苯乙烯为反应底物,叔丁醇钾为碱,四氢呋喃为溶剂,频哪醇硼烷为还原剂,与coi2现场制备金属纳米团簇催化剂,催化烯烃的硼氢化反应。反应式如下:
[0102][0103]
反应如下:在手套箱中,coi2(1.56mg,0.005mmol),叔丁醇钾(11.2mg,0.1mmol)和4-甲基苯乙烯(118.2mg,1.0mmol)分别加入一10ml样品瓶中,加入thf(5ml),加入频哪醇硼烷(153.6mg,1.2mmol)。室温下搅拌一小时后,在空气中淬灭,柱层析纯化,得到硼氢化产物。2b为主产物,无色油状物,93%产率,b/l=42/1。1h nmr(400mhz,chloroform-d)δ7.20
–
7.03(m,4h),2.43(q,j=7.5hz,1h),2.34(s,3h),1.35(d,j=7.5hz,3h),1.24(d,j=5.1hz,12h)ppm.
13
c nmr(101mhz,chloroform-d)δ142.0,134.4,129.1,127.7,83.3,24.7,24.7,21.1,17.4ppm.备注:实施例4-12中的b/l指支链硼氢化产物与线性硼氢化产物的比例,由核磁1h-nmr粗谱确定。
[0104]
实施例5
[0105]
本实施例以3-甲基苯乙烯为反应底物,叔丁醇钾为碱,四氢呋喃为溶剂,频哪醇硼烷为还原剂,与coi2现场制备金属纳米团簇催化剂,催化烯烃的硼氢化反应。反应式如下:
[0106][0107]
反应如下:在手套箱中,coi2(1.56mg,0.005mmol),叔丁醇钾(11.2mg,0.1mmol)和3-甲基苯乙烯(118.2mg,1.0mmol)分别加入一10ml样品瓶中,加入thf(5ml),加入频哪醇硼烷(153.6mg,1.2mmol)。室温下搅拌一小时后,在空气中淬灭,柱层析纯化,得到硼氢化产物。2c为主产物,无色油状物,91%产率,b/l=43/1。1h nmr(400mhz,chloroform-d)δ7.25
–
7.17(m,1h),7.13
–
7.06(m,2h),7.04
–
6.97(m,1h),2.47(q,j=7.5hz,1h),2.38(s,3h),1.40(d,j=7.4hz,3h),1.27(d,j=5.5hz,12h)ppm.
13
c nmr(101mhz,chloroform-d)δ145.0,137.8,128.7,128.3,126.0,124.9,83.3,24.7,24.7,21.6,17.3ppm.
[0108]
实施例6
[0109]
本实施例以4-叔丁基苯乙烯为反应底物,叔丁醇钾为碱,四氢呋喃为溶剂,频哪醇硼烷为还原剂,与coi2现场制备金属纳米团簇催化剂,催化烯烃的硼氢化反应。反应式如下:
[0110][0111]
反应如下:在手套箱中,coi2(1.56mg,0.005mmol),叔丁醇钾(11.2mg,0.1mmol)和4-叔丁基苯乙烯(160.3mg,1.0mmol)分别加入一10ml样品瓶中,加入thf(5ml),加入频哪醇硼烷(153.6mg,1.2mmol)。室温下搅拌一小时后,在空气中淬灭,柱层析纯化,得到硼氢化产物。2d为主产物,无色油状物,88%产率,b/l=18/1。1h nmr(400mhz,chloroform-d)δ7.36
–
7.29(m,2h),7.23
–
7.16(m,2h),2.46(q,j=7.5hz,1h),1.41
–
1.31(m,12h),1.26(d,j=5.0hz,12h)ppm.
13
c nmr(101mhz,chloroform-d)δ147.6,141.7,127.4,125.2,83.2,34.3,31.5,24.7,24.7,17.3ppm.
[0112]
实施例7
[0113]
本实施例以4-氟苯乙烯为反应底物,叔丁醇钾为碱,四氢呋喃为溶剂,频哪醇硼烷为还原剂,与coi2现场制备金属纳米团簇催化剂,催化烯烃的硼氢化反应。反应式如下:
[0114][0115]
反应如下:在手套箱中,coi2(1.56mg,0.005mmol),叔丁醇钾(11.2mg,0.1mmol)和4-氟苯乙烯(122.1mg,1.0mmol)分别加入一10ml样品瓶中,加入thf(5ml),加入频哪醇硼烷(153.6mg,1.2mmol)。室温下搅拌一小时后,在空气中淬灭,柱层析纯化,得到硼氢化产物。2e为主产物,无色油状物,96%产率,b/l=31/1。1h nmr(400mhz,chloroform-d)δ7.22
–
7.14(m,2h),7.00
–
6.91(m,2h),2.43(q,j=7.5hz,1h),1.33(d,j=7.6hz,3h),1.22(d,j=4.8hz,12h)ppm.
13
c nmr(101mhz,chloroform-d)δ162.0,159.6,140.5,140.5,129.0,128.9,115.0,114.8,83.3,24.6,24.5,17.2ppm.
19
f nmr(376mhz,chloroform-d)δ-118.96ppm.
[0116]
实施例8
[0117]
本实施例以3-氟苯乙烯为反应底物,叔丁醇钾为碱,四氢呋喃为溶剂,频哪醇硼烷为还原剂,与coi2现场制备金属纳米团簇催化剂,催化烯烃的硼氢化反应。反应式如下:
[0118][0119]
反应如下:在手套箱中,coi2(1.56mg,0.005mmol),叔丁醇钾(11.2mg,0.1mmol)和3-氟苯乙烯(122.1mg,1.0mmol)分别加入一10ml样品瓶中,加入thf(5ml),加入频哪醇硼烷(153.6mg,1.2mmol)。室温下搅拌一小时后,在空气中淬灭,柱层析纯化,得到硼氢化产物。2f为主产物,无色油状物,84%产率,b/l=46/1。1h nmr(400mhz,chloroform-d)δ7.28
–
7.16(m,1h),7.06
–
6.91(m,2h),6.88
–
6.79(m,1h),2.47(q,j=7.1hz,1h),1.35(d,j=7.5hz,3h),1.23(d,j=4.5hz,12h)ppm.
13
c nmr(101mhz,chloroform-d)δ164.2,161.7,147.7,147.6,129.5,129.5,123.4,123.4,114.6,114.4,112.0,111.8,83.4,24.8,24.6,24.5,16.7ppm.
19
f nmr(376mhz,chloroform-d)δ-113.97ppm.
[0120]
实施例9
[0121]
本实施例以4-三甲基硅基苯乙烯为反应底物,叔丁醇钾为碱,四氢呋喃为溶剂,频哪醇硼烷为还原剂,与coi2现场制备金属纳米团簇催化剂,催化烯烃的硼氢化反应。反应式如下:
[0122][0123]
反应如下:在手套箱中,coi2(1.56mg,0.005mmol),叔丁醇钾(11.2mg,0.1mmol)和4-三甲基硅基苯乙烯(176.3mg,1.0mmol)分别加入一10ml样品瓶中,加入thf(5ml),加入频哪醇硼烷(153.6mg,1.2mmol)。室温下搅拌一小时后,在空气中淬灭,柱层析纯化,得到硼氢化产物。2g为主产物,无色油状物,70%产率,b/l=9/1。1h nmr(400mhz,chloroform-d)δ7.50
–
7.44(m,2h),7.29
–
7.23(m,2h),2.47(q,j=7.5hz,1h),1.38(d,j=7.5hz,3h),1.26(d,j=4.6hz,12h),0.29(s,9h)ppm.
13
c nmr(101mhz,chloroform-d)δ145.6,136.2,133.4,127.3,83.3,24.7,24.6,17.1,-1.0ppm.
[0124]
实施例10
[0125]
本实施例以4-甲氧基苯乙烯为反应底物,叔丁醇钾为碱,四氢呋喃为溶剂,频哪醇硼烷为还原剂,与coi2现场制备金属纳米团簇催化剂,催化烯烃的硼氢化反应。反应式如下:
[0126][0127]
反应如下:在手套箱中,coi2(1.56mg,0.005mmol),叔丁醇钾(11.2mg,0.1mmol)和4-甲氧基苯乙烯(134.2mg,1.0mmol)分别加入一10ml样品瓶中,加入thf(5ml),加入频哪醇硼烷(153.6mg,1.2mmol)。室温下搅拌一小时后,在空气中淬灭,柱层析纯化,得到硼氢化产
物。2h为主产物,无色油状物,94%产率,b/l=26/1。1h nmr(400mhz,chloroform-d)δ7.22
–
7.14(m,1h),6.86
–
6.77(m,2h),6.73
–
6.65(m,1h),3.79(s,3h),2.43(q,j=7.5hz,1h),1.33(d,j=7.5hz,3h),1.22(d,j=5.1hz,12h)ppm.
13
c nmr(101mhz,chloroform-d)δ159.6,146.6,129.2,120.3,113.5,110.5,83.3,55.0,24.6,24.6,17.0ppm.
[0128]
实施例11
[0129]
本实施例以4-二甲基叔丁硅氧基苯乙烯为反应底物,叔丁醇钾为碱,四氢呋喃为溶剂,频哪醇硼烷为还原剂,与coi2现场制备金属纳米团簇催化剂,催化烯烃的硼氢化反应。反应式如下:
[0130][0131]
反应如下:在手套箱中,coi2(1.56mg,0.005mmol),叔丁醇钾(11.2mg,0.1mmol)和4-二甲基叔丁硅氧基苯乙烯(234.4mg,1.0mmol)分别加入一10ml样品瓶中,加入thf(5ml),加入频哪醇硼烷(153.6mg,1.2mmol)。室温下搅拌一小时后,在空气中淬灭,柱层析纯化,得到硼氢化产物。2i为主产物,无色油状物,89%产率,b/l=16/1。1hnmr(400mhz,chloroform-d)δ7.11
–
7.03(m,2h),6.79
–
6.69(m,2h),2.37(q,j=7.5hz,1h),1.30(d,j=7.6hz,3h),1.20(d,j=5.8hz,12h),0.98(s,9h),0.19(s,6h)ppm.
13
cnmr(101mhz,chloroform-d)δ153.0,137.4,128.5,119.8,83.1,25.7,24.6,24.5,18.2,17.1,-4.4ppm.
[0132]
实施例12
[0133]
本实施例以萘-2-乙烯为反应底物,叔丁醇钾为碱,四氢呋喃为溶剂,频哪醇硼烷为还原剂,与coi2现场制备金属纳米团簇催化剂,催化烯烃的硼氢化反应。反应式如下:
[0134][0135]
反应如下:在手套箱中,coi2(6.26mg,0.02mmol),叔丁醇钾(11.2mg,0.1mmol)和萘-2-乙烯(154.2mg,1.0mmol)分别加入一10ml样品瓶中,加入thf(5ml),加入频哪醇硼烷(153.6mg,1.2mmol)。室温下搅拌一小时后,在空气中淬灭,柱层析纯化,得到硼氢化产物。2j为主产物,白色固体,97%产率,b/l=12/1。1h nmr(400mhz,chloroform-d)δ7.85
–
7.75(m,3h),7.71
–
7.66(m,1h),7.51
–
7.37(m,3h),2.66(q,j=7.5hz,1h),1.48(d,j=7.4hz,3h),1.24(d,j=6.2hz,12h)ppm.
13
c nmr(101mhz,chloroform-d)δ142.7,134.0,131.8,127.8,127.60,127.55,127.3,125.7,125.4,124.9,83.5,24.7,24.7,16.9ppm.
[0136]
实施例13
[0137]
本实施例以苯甲腈为反应底物,叔丁醇钾为碱,频哪醇硼烷为还原剂,在不同溶剂中,与coi2现场制备金属纳米团簇催化剂,催化底物苯甲腈的硼氢化反应。反应式如下:
[0138][0139]
反应如下:在手套箱中,coi2(1.56mg,0.005mmol),叔丁醇钾(5.6mg,0.05mmol)和
苯甲腈(51.6mg,0.5mmol)分别加入一10ml样品瓶中,加入不同的溶剂(2ml),加入频哪醇硼烷(140.8mg,1.1mmol)。室温下搅拌4小时后,在空气中淬灭。加入盐酸酸化为对应的盐酸盐。
[0140][0141]
反应底物的转化率由气相色谱测定;1h nmr(400mhz,dmso-d6)δ8.38(s,3h),7.63
–
7.17(m,5h),4.02(s,2h)ppm.
13
c nmr(101mhz,dmso-d6)δ134.6,129.4,128.9,128.8,42.5ppm.
[0142]
实施例14
[0143]
本实施例以4-甲基苯甲腈为反应底物,叔丁醇钾为碱,乙醚为溶剂,频哪醇硼烷为还原剂,与coi2现场制备金属纳米团簇催化剂,催化腈的硼氢化反应。反应式如下:
[0144][0145]
反应如下:在手套箱中,coi2(6.26mg,0.02mmol),叔丁醇钾(11.2mg,0.1mmol)和4-甲基苯甲腈(117.2mg,1.0mmol)分别加入一10ml样品瓶中,加入乙醚(2ml),加入频哪醇硼烷(281.6mg,2.2mmol)。室温下搅拌4小时后,在空气中淬灭。加入盐酸乙醚溶液酸化为对应的盐酸盐。6b,白色固体,》99%产率。1h nmr(400mhz,dmso-d6)δ8.25(s,3h),7.38
–
7.29(m,2h),7.25
–
7.15(m,2h),3.95(s,2h),2.29(s,3h)ppm.
13
cnmr(101mhz,dmso-d6)δ138.1,131.5,129.4,129.4,42.3,21.2ppm.
[0146]
实施例15
[0147]
本实施例以3-甲基苯甲腈为反应底物,叔丁醇钾为碱,乙醚为溶剂,频哪醇硼烷为还原剂,与coi2现场制备金属纳米团簇催化剂,催化腈的硼氢化反应。反应式如下:
[0148][0149]
反应如下:在手套箱中,coi2(6.26mg,0.02mmol),叔丁醇钾(11.2mg,0.1mmol)和3-甲基苯甲腈(117.2mg,1.0mmol)分别加入一10ml样品瓶中,加入乙醚(2ml),加入频哪醇硼烷(281.6mg,2.2mmol)。室温下搅拌4小时后,在空气中淬灭。加入盐酸乙醚溶液酸化为对应的盐酸盐。6c,白色固体,89%产率。1h nmr(400mhz,dmso-d6)δ8.48(s,3h),7.35
–
7.24(m,3h),7.23
–
7.15(m,1h),3.96(s,2h),2.31(s,3h)ppm.
13
c nmr(101mhz,dmso-d6)δ138.1,134.5,130.0,129.3,128.9,126.4,42.5,21.4ppm.
[0150]
实施例16
[0151]
本实施例以2-甲基苯甲腈为反应底物,叔丁醇钾为碱,乙醚为溶剂,频哪醇硼烷为还原剂,与coi2现场制备金属纳米团簇催化剂,催化腈的硼氢化反应。反应式如下:
[0152][0153]
反应如下:在手套箱中,coi2(6.26mg,0.02mmol),叔丁醇钾(11.2mg,0.1mmol)和2-甲基苯甲腈(117.2mg,1.0mmol)分别加入一10ml样品瓶中,加入乙醚(2ml),加入频哪醇硼烷(281.6mg,2.2mmol)。室温下搅拌4小时后,在空气中淬灭。加入盐酸乙醚溶液酸化为对应的盐酸盐。6d,白色固体,88%产率。1h nmr(400mhz,dmso-d6)δ8.29(s,3h),7.42
–
7.33(m,1h),7.30
–
7.18(m,3h),3.99(s,2h),2.33(s,3h)ppm.
13
c nmr(101mhz,dmso-d6)δ137.1,132.8,130.7,129.7,128.8,126.4,39.8,19.3ppm.
[0154]
实施例17
[0155]
本实施例以4-叔丁基苯甲腈为反应底物,叔丁醇钾为碱,乙醚为溶剂,频哪醇硼烷为还原剂,与coi2现场制备金属纳米团簇催化剂,催化腈的硼氢化反应。反应式如下:
[0156][0157]
反应如下:在手套箱中,coi2(6.26mg,0.02mmol),叔丁醇钾(11.2mg,0.1mmol)和4-叔丁基苯甲腈(159.2mg,1.0mmol)分别加入一10ml样品瓶中,加入乙醚(2ml),加入频哪醇硼烷(281.6mg,2.2mmol)。室温下搅拌4小时后,在空气中淬灭。加入盐酸乙醚溶液酸化为对应的盐酸盐。6e,白色固体,92%产率。1h nmr(400mhz,dmso-d6)δ8.30(s,3h),7.50
–
7.33(m,4h),3.98(s,2h),1.28(s,9h)ppm.
13
c nmr(101mhz,dmso-d6)δ151.3,131.6,129.2,125.7,42.2,34.8,31.5ppm.
[0158]
实施例18
[0159]
本实施例以4-苯基苯甲腈为反应底物,叔丁醇钾为碱,乙醚为溶剂,频哪醇硼烷为还原剂,与coi2现场制备金属纳米团簇催化剂,催化腈的硼氢化反应。反应式如下:
[0160][0161]
反应如下:在手套箱中,coi2(6.26mg,0.02mmol),叔丁醇钾(11.2mg,0.1mmol)和4-苯基苯甲腈(179.2mg,1.0mmol)分别加入一10ml样品瓶中,加入乙醚(2ml),加入频哪醇硼烷(281.6mg,2.2mmol)。室温下搅拌4小时后,在空气中淬灭。加入盐酸乙醚溶液酸化为对应的盐酸盐。6f,白色固体,》99%产率。1h nmr(400mhz,dmso-d6)δ8.41(s,3h),7.74
–
7.63(m,4h),7.59
–
7.53(m,2h),7.50
–
7.42(m,2h),7.41
–
7.33(m,1h),4.04(s,2h)ppm.
13
c nmr(101mhz,dmso-d6)δ140.6,140.0,133.8,130.1,129.4,128.1,127.2,127.1,42.2ppm.
[0162]
实施例19
[0163]
本实施例以萘-2-甲腈为反应底物,叔丁醇钾为碱,乙醚为溶剂,频哪醇硼烷为还原剂,与coi2现场制备金属纳米团簇催化剂,催化腈的硼氢化反应。反应式如下:
[0164][0165]
反应如下:在手套箱中,coi2(6.26mg,0.02mmol),叔丁醇钾(11.2mg,0.1mmol)和萘-2-甲腈(153.2mg,1.0mmol)分别加入一10ml样品瓶中,加入乙醚(2ml),加入频哪醇硼烷(281.6mg,2.2mmol)。室温下搅拌4小时后,在空气中淬灭。加入盐酸乙醚溶液酸化为对应的盐酸盐。
[0166]
6g,白色固体,97%产率。1h nmr(400mhz,dmso-d6)δ8.38(s,3h),8.03
–
7.82(m,4h),7.67
–
7.45(m,3h),4.18(s,2h)ppm.
13
c nmr(101mhz,dmso-d6)δ133.0,132.2,128.6,128.4,128.2,128.1,127.1(2c),127.0,126.9,42.7ppm.
[0167]
实施例20
[0168]
本实施例以4-甲氧基苯甲腈为反应底物,叔丁醇钾为碱,乙醚为溶剂,频哪醇硼烷为还原剂,与coi2现场制备金属纳米团簇催化剂,催化腈的硼氢化反应。反应式如下:
[0169][0170]
反应如下:在手套箱中,coi2(6.26mg,0.02mmol),叔丁醇钾(11.2mg,0.1mmol)和4-甲氧基苯甲腈(133.2mg,1.0mmol)分别加入一10ml样品瓶中,加入乙醚(2ml),加入频哪醇硼烷(281.6mg,2.2mmol)。室温下搅拌4小时后,在空气中淬灭。加入盐酸乙醚溶液酸化为对应的盐酸盐。6h,白色固体,98%产率。1h nmr(400mhz,dmso-d6)δ8.41(s,3h),7.46
–
7.32(m,2h),7.00
–
6.87(m,2h),3.90(s,2h),3.74(s,3h)ppm.
13
c nmr(101mhz,dmso-d6)δ159.7,131.0,126.4,114.3,55.6,42.0ppm.
[0171]
实施例21
[0172]
本实施例以4-氟苯甲腈为反应底物,叔丁醇钾为碱,乙醚为溶剂,频哪醇硼烷为还原剂,与coi2现场制备金属纳米团簇催化剂,催化腈的硼氢化反应。反应式如下:
[0173][0174]
反应如下:在手套箱中,coi2(6.26mg,0.02mmol),叔丁醇钾(11.2mg,0.1mmol)和4-氟苯甲腈(121.1mg,1.0mmol)分别加入一10ml样品瓶中,加入乙醚(2ml),加入频哪醇硼烷(281.6mg,2.2mmol)。室温下搅拌4小时后,在空气中淬灭。加入盐酸乙醚溶液酸化为对应的盐酸盐。6i,白色固体,96%产率。1h nmr(400mhz,dmso-d6)δ8.27(s,3h),7.61
–
7.45(m,2h),7.33
–
7.19(m,2h),4.02(s,2h)ppm.
13
c{
19
f}nmr(101mhz,dmso-d6)δ162.6,131.9,131.0,115.8,41.9ppm.
19
f nmr(376mhz,dmso-d6)δ-112.96ppm.
[0175]
实施例22
[0176]
本实施例以3-氟苯甲腈为反应底物,叔丁醇钾为碱,乙醚为溶剂,频哪醇硼烷为还原剂,与coi2现场制备金属纳米团簇催化剂,催化腈的硼氢化反应。反应式如下:
[0177][0178]
反应如下:在手套箱中,coi2(6.26mg,0.02mmol),叔丁醇钾(11.2mg,0.1mmol)和3-氟苯甲腈(121.1mg,1.0mmol)分别加入一10ml样品瓶中,加入乙醚(2ml),加入频哪醇硼烷(281.6mg,2.2mmol)。室温下搅拌4小时后,在空气中淬灭。加入盐酸乙醚溶液酸化为对应的盐酸盐。6j,白色固体,99%产率。1h nmr(400mhz,d2o)δ7.56
–
7.34(m,1h),7.34
–
6.99(m,3h),4.16(s,2h)ppm.
13
c nmr(151mhz,d2o)δ162.4,160.8,133.82,133.77,130.1,130.0,123.67,123.65,115.1,115.0,114.7,114.6,41.6ppm.
19
f nmr(376mhz,d2o)δ-110.33(q,j=8.4hz)ppm
[0179]
实施例23
[0180]
本实施例以2-氟苯甲腈为反应底物,叔丁醇钾为碱,乙醚为溶剂,频哪醇硼烷为还原剂,与coi2现场制备金属纳米团簇催化剂,催化腈的硼氢化反应。反应式如下:
[0181][0182]
反应如下:在手套箱中,coi2(6.26mg,0.02mmol),叔丁醇钾(11.2mg,0.1mmol)和2-氟苯甲腈(121.1mg,1.0mmol)分别加入一10ml样品瓶中,加入乙醚(2ml),加入频哪醇硼烷(281.6mg,2.2mmol)。室温下搅拌4小时后,在空气中淬灭。加入盐酸乙醚溶液酸化为对应的盐酸盐。6k,白色固体,99%产率。1h nmr(400mhz,d2o)δ7.54
–
7.37(m,2h),7.32
–
7.14(m,2h),4.23(s,2h)ppm.
13
c nmr(151mhz,d2o)δ160.7,159.1,130.8,130.7,130.3,130.2,124.0,123.9,118.6,118.5,114.8,114.7,36.21,36.19ppm.
19
f nmr(376mhz,d2o)δ-115.74(q,j=7.5,7.1hz)ppm.
[0183]
实施例24
[0184]
本实施例以4-氯苯甲腈为反应底物,叔丁醇钾为碱,乙醚为溶剂,频哪醇硼烷为还原剂,与coi2现场制备金属纳米团簇催化剂,催化腈的硼氢化反应。反应式如下:
[0185][0186]
反应如下:在手套箱中,coi2(6.26mg,0.02mmol),叔丁醇钾(11.2mg,0.1mmol)和4-氯苯甲腈(137.6mg,1.0mmol)分别加入一10ml样品瓶中,加入乙醚(2ml),加入频哪醇硼烷(281.6mg,2.2mmol)。室温下搅拌4小时后,在空气中淬灭。加入盐酸乙醚溶液酸化为对应的盐酸盐。6l,白色固体,99%产率。1h nmr(400mhz,dmso-d6)δ8.28(s,3h),7.60
–
7.41(m,4h),4.03(s,2h)ppm.
13
c nmr(101mhz,dmso-d6)δ133.6,133.5,131.5,128.9,41.8ppm.
[0187]
实施例25
[0188]
本实施例以4-三氟甲基苯甲腈为反应底物,叔丁醇钾为碱,乙醚为溶剂,频哪醇硼烷为还原剂,与coi2现场制备金属纳米团簇催化剂,催化腈的硼氢化反应。反应式如下:
[0189][0190]
反应如下:在手套箱中,coi2(6.26mg,0.02mmol),叔丁醇钾(11.2mg,0.1mmol)和4-三氟甲基苯甲腈(171.1mg,1.0mmol)分别加入一10ml样品瓶中,加入乙醚(2ml),加入频哪醇硼烷(281.6mg,2.2mmol)。室温下搅拌4小时后,在空气中淬灭。加入盐酸乙醚溶液酸化为对应的盐酸盐。6m,白色固体,95%产率。1h nmr(400mhz,dmso-d6)δ8.62(s,3h),7.86
–
7.60(m,4h),4.11(s,2h)ppm.
13
c{
19
f}nmr(101mhz,dmso-d6)δ139.4,130.4,129.4,125.8,124.7,42.1ppm.
19
f nmr(376mhz,dmso-d6)δ-60.32ppm.
[0191]
实施例26
[0192]
本实施例以1-辛腈为反应底物,叔丁醇钾为碱,乙醚为溶剂,频哪醇硼烷为还原剂,与coi2现场制备金属纳米团簇催化剂,催化腈的硼氢化反应。反应式如下:
[0193][0194]
反应如下:在手套箱中,coi2(6.26mg,0.02mmol),叔丁醇钾(11.2mg,0.1mmol)和1-辛腈(125.2mg,1.0mmol)分别加入一10ml样品瓶中,加入乙醚(2ml),加入频哪醇硼烷(281.6mg,2.2mmol)。室温下搅拌4小时后,在空气中淬灭。加入盐酸乙醚溶液酸化为对应的盐酸盐。6n,白色固体,74%产率。1h nmr(400mhz,dmso-d6)δ8.02(s,3h),2.71(t,j=7.7hz,2h),1.53(p,j=7.3hz,2h),1.36
–
1.11(m,10h),0.84(t,j=6.5hz,3h)ppm.
13
c nmr(101mhz,dmso-d6)δ39.1,31.6,29.0,28.9,27.3,26.3,22.5,14.4ppm.
[0195]
实施例27
[0196]
本实施例以叔丁腈为反应底物,叔丁醇钾为碱,乙醚为溶剂,频哪醇硼烷为还原剂,与coi2现场制备金属纳米团簇催化剂,催化腈的硼氢化反应。反应式如下:
[0197][0198]
反应如下:在手套箱中,coi2(6.26mg,0.02mmol),叔丁醇钾(11.2mg,0.1mmol)和叔丁腈(69.1mg,1.0mmol)分别加入一10ml样品瓶中,加入乙醚(2ml),加入频哪醇硼烷(281.6mg,2.2mmol)。室温下搅拌4小时后,在空气中淬灭。加入盐酸乙醚溶液酸化为对应的盐酸盐。6o,白色固体,》99%产率。1h nmr(400mhz,dmso-d6)δ8.05(s,3h),2.61(d,j=7.0hz,2h),1.88(hept,j=13.5,6.8hz,1h),0.92(d,j=6.7hz,6h)ppm.
13
cnmr(101mhz,dmso-d6)δ46.0,26.7,20.3ppm.
[0199]
实施例28
[0200]
本实施例以环己腈为反应底物,叔丁醇钾为碱,乙醚为溶剂,频哪醇硼烷为还原剂,与coi2现场制备金属纳米团簇催化剂,催化腈的硼氢化反应。反应式如下:
[0201][0202]
反应如下:在手套箱中,coi2(6.26mg,0.02mmol),叔丁醇钾(11.2mg,0.1mmol)和
环己腈(109.2mg,1.0mmol)分别加入一10ml样品瓶中,加入乙醚(2ml),加入频哪醇硼烷(281.6mg,2.2mmol)。室温下搅拌4小时后,在空气中淬灭。加入盐酸乙醚溶液酸化为对应的盐酸盐。6p,白色固体,90%产率。1h nmr(400mhz,dmso-d6)δ7.99(s,3h),2.59(d,j=6.9hz,2h),1.78
–
1.44(m,6h),1.25
–
1.01(m,3h),0.96
–
0.80(m,2h)ppm.
13
c nmr(101mhz,dmso-d6)δ44.8,35.8,30.3,26.1,25.5ppm.
[0203]
实施例29
[0204]
本实施例以苯丁腈为反应底物,叔丁醇钾为碱,乙醚为溶剂,频哪醇硼烷为还原剂,与coi2现场制备金属纳米团簇催化剂,催化腈的硼氢化反应。反应式如下:
[0205][0206]
反应如下:在手套箱中,coi2(6.26mg,0.02mmol),叔丁醇钾(11.2mg,0.1mmol)和苯丁腈(140.6mg,1.0mmol)分别加入一10ml样品瓶中,加入乙醚(2ml),加入频哪醇硼烷(281.6mg,2.2mmol)。室温下搅拌4小时后,在空气中淬灭。加入盐酸乙醚溶液酸化为对应的盐酸盐。6q,白色固体,75%产率。1h nmr(400mhz,dmso-d6)δ8.13(s,3h),7.39
–
7.09(m,5h),2.76(t,j=7.0hz,2h),2.59(t,j=7.1hz,2h),1.70
–
1.48(m,4h)ppm.
13
c nmr(101mhz,dmso-d6)δ142.2,128.8,128.7,126.2,38.9,35.0,28.2,27.0ppm.
[0207]
实施例30
[0208]
本实施例以4-氰基吡啶为反应底物,叔丁醇钾为碱,乙醚为溶剂,频哪醇硼烷为还原剂,与coi2现场制备金属纳米团簇催化剂,催化腈的硼氢化反应。反应式如下:
[0209][0210]
反应如下:在手套箱中,coi2(6.26mg,0.02mmol),叔丁醇钾(11.2mg,0.1mmol)和4-氰基吡啶(104.1mg,1.0mmol)分别加入一10ml样品瓶中,加入乙醚(2ml),加入频哪醇硼烷(281.6mg,2.2mmol)。室温下搅拌4小时后,在空气中淬灭。加入盐酸乙醚溶液酸化为对应的盐酸盐。6r,白色固体,74%产率。1h nmr(400mhz,d2o)δ8.86(d,j=6.0hz,2h),8.12(d,j=6.0hz,2h),4.57(s,2h)ppm.
13
c nmr(101mhz,d2o)δ153.2,141.7,126.2,41.6ppm.
[0211]
在本发明提及的所有文献都在本技术中引用作为参考,就如同每一篇文献被单独引用作为参考那样。此外应理解,在阅读了本发明的上述讲授内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本技术所附权利要求书所限定的范围。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。