1.本发明属于生物医药技术领域,具体涉及一种含有奥美拉唑镁的药物组合物及其制剂。
背景技术:
2.奥美拉唑镁为抗酸类非处方药。分子式是c
17h19
mgn3o3s;本品为h
,k
-atp酶质子泵抑制剂,通过小肠吸收后,经血液循环在胃壁浓集,从而抑制胃酸。临床上奥美拉唑镁肠溶片用于治疗十二指肠溃疡、胃溃疡和返流性食管炎:与抗生素联合用药,治疗感染幽门螺杆菌的十二指肠溃疡;治疗非甾体类抗炎药相关的消化性溃疡和胃十二指肠糜烂;预防非甾体类抗炎药引起的消化性溃疡、胃十二指肠糜烂或消化不良症状;亦用于慢性复发性消化性溃疡和反流性食管炎的长期治疗;用于胃-食管反流病的烧心感和反流的对症治疗;溃疡样症状的对症治疗及酸相关性消化不良;用于卓-艾氏综合征的治疗。
3.2004年6月,美国率先批准了奥美拉唑碳酸氢钠的常释制剂,即复方奥美拉唑口服干混悬剂(奥美拉唑/碳酸氢钠),在该制剂中碳酸氢钠取代肠溶包衣发挥防止奥美拉唑于吸收前遇酸降解的作用,适用于活动性十二指肠溃疡、胃食管反流病的短期治疗以及已愈合糜烂性食管炎的维持治疗。同年12月,40mg/1.68g规格的复方奥美拉唑
ロ
服干混悬剂在美国批准临床,并增加适应症用于良性胃溃疡的短期治疗和降低危重患者上消化道出血的风险。
4.中国专利cn102727516b公开了一种复方奥美拉唑胶囊及其制备方法,奥美拉唑原料通过180目,碳酸氢钠粒度为80~150目,每单位制剂硬脂酸镁用量6~10mg,交联羧甲基纤维素钠用量6~18mg。
5.中国专利cn103006691a公开了一种奥美拉唑碳酸氢钠复方胶囊剂,该胶囊剂由奥美拉唑胃溶小丸和碳酸氢钠、崩解剂、润滑剂混合均匀,填充胶囊而成,在盐酸溶液中,碳酸氢钠迅速释放,奥美拉唑在碳酸氢钠释放完全后再迅速释放。
6.中国专利cn 101816641b公开了一种制备含有奥美拉唑的速释胶囊的方法,每单位制剂由20mg奥美拉唑、1100mg碳酸氢钠和适量的药用辅料组成(增溶剂为十二烷基硫酸钠、粘合剂为5%聚维酮、崩解剂为交联羟甲基纤维素钠,润滑剂为硬脂酸镁),采用制粒生产工艺灌装胶囊。该制剂使用的辅料及生产工艺较多。
7.上述专利均未考虑奥美拉唑/碳酸氢钠复方制剂的稳定性,因此,开发一种工艺简单、制剂稳定性较好的奥美拉唑/碳酸氢钠的制剂,具有重要意义。
技术实现要素:
8.基于上述原因,申请人通过多次创造性的试验,申请人研究得到一种新的含有奥美拉唑镁的药物组合物,该药物组合物中,不使用填充剂,而只使用崩解剂羧甲淀粉钠;本发明的药物组合物中的崩解剂,不是简单的替换,而是通过相容性试验等创造性的试验筛选获得的,采用本发明的制剂处方,特别是采用崩解剂羧甲淀粉钠,奥美拉唑镁/碳酸氢钠
复方制剂中有关物质变化小,稳定性好,溶出度符合质量标准的要求。
9.本发明通过下述技术方案实现。
10.一种含有奥美拉唑镁的药物组合物,该药物组合物含有奥美拉唑镁、碳酸氢钠、崩解剂和润滑剂。
11.上述所述的一种含有奥美拉唑镁的药物组合物,其中奥美拉唑镁10-11重量份,碳酸氢钠1000-1600重量份,崩解剂10-25重量份,润滑剂2-10重量份。
12.上述所述一种含有奥美拉唑镁的药物组合物,其中奥美拉唑镁10-11重量份,碳酸氢钠1000-1600重量份,崩解剂10-25重量份,润滑剂2-10重量份。
13.上述所述的一种含有奥美拉唑镁的药物组合物,其中崩解剂包括羧甲淀粉钠。
14.上述所述的一种含有奥美拉唑镁的药物组合物,其中润滑剂包括硬脂酸镁、滑石粉、微粉硅胶。
15.上述所述一种含有奥美拉唑镁的药物组合物,该药物组合物制备成胶囊。
16.上述所述一种含有奥美拉唑镁的药物组合物,其中所述胶囊剂的制备方法为:
17.(1)将奥美拉唑镁、碳酸氢钠、崩解剂和润滑剂过80目筛;
18.(2)将奥美拉唑镁、碳酸氢钠和崩解剂进行预混处理;
19.(3)将润滑剂加入步骤(2)中,进行总混处理;
20.(4)将步骤(3)制得的混合物制成胶囊。
21.本发明具有下述所述的有益的技术效果:
22.1、本发明药物组合物中未使用常用的辅料填充剂,仅仅使用崩解剂和润滑剂,就符合质量标准对于溶出度的要求,减少辅料的用量,有利于降低成本,具有更高的安全性。
23.2、本发明的崩解剂经过筛选性试验研究获得的,而不是想当然的简单替换,通过对于制剂稳定性研究,特别是相容性的研究表明,采用羧甲淀粉钠作为奥美拉唑镁/碳酸氢钠制剂中的崩解剂,
24.3、本发明工艺简单,不需要将原料制备成纳米化原料,就可以很好的符合溶出度的要求。
具体实施方式
25.为了使本发明实现的技术手段、创作特征、达成目的与功效易于明白了解,下面结合具体实施例进一步阐明本发明,但下述实施例仅为本发明的优选实施例,并非全部。基于实施方式中的实施例,本领域技术人员在没有做出创造性劳动的前提下所获得其它实施例,都属于本发明的保护范围。
26.下述实施例中的实验方法,如无特殊说明,均为常规方法,下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
27.一、辅料筛选试验
28.【检查】有关物质照高效液相色谱(中国药典2020年版四部通则0512)测定,避光操作,临用新制。
29.供试品溶液取本品内容物适量(约相当于奥美拉唑20mg),置100ml量瓶中,加乙腈27ml,振摇,用磷酸盐缓冲液(ph7.6)稀释至刻度,摇匀,滤过。
30.对照品溶液精密量取供试品溶液适量,用磷酸盐缓冲液(ph7.6)-乙腈(73:27)稀
释制成每1ml中约含0.2μg的溶液。
31.系统适用性溶液取奥美拉唑对照品和杂质d对照品各适量,用磷酸盐缓冲液(ph7.6)-乙腈(73:27)溶解并稀释制成每1ml中均约含0.02mg的混合溶液。
32.色谱条件用十八烷基硅烷键合硅胶为填充剂;乙腈-磷酸盐缓冲液(ph7.6)(1.4g/l的十二水合磷酸氢二钠溶液,用磷酸调至ph值7.6)(25:75)为流动相;检测波长为302nm;流速为每分钟1.0ml;色谱柱温为30℃;进样体积20μl。
33.系统适用性要求系统适用性溶液色谱图中,奥美拉唑峰与杂质d峰之间的分离度应大于2.0,理论塔板数按奥美拉唑计算不小于2000。
34.测定法精密量取供试品溶液与对照溶液各20μl分别注入液相色谱仪,记录色谱图至主成分保留时间的5倍。
35.限度供试品溶液色谱图中如有杂质峰,杂质d的峰面积不得大于对照品峰面积的5倍(0.5%),杂质e峰面积不得大于对照品峰面积的2倍(0.2%),其他单个杂质峰面积不得大于对照品峰面积的2倍(0.2%),各杂质的峰面积和不得大于对照品峰面积的20倍(2.0%)。
36.【含量测定】奥美拉唑镁照高效液相色谱法(中国药典2020年版四部通则0512)测定。
37.供试品溶液取本品10粒,将内容物分别倾入100ml(10mg规格)或200ml(20mg规格)量瓶中,囊壳用甲醇5ml(10mg规格)或10ml(20mg规格)洗净,洗液并入量瓶中,加甲醇5ml(10mg规格)或10ml(20mg规格),振摇1分钟,再加入甲醇-0.05mol/l氢氧化钠溶液(20:80)80ml(10mg规格)或130ml(20mg规格),超声5分钟,用甲醇-0.05mol/l氢氧化钠溶液(20:80)稀释至刻度,摇匀,滤过。
38.对照品溶液取奥美拉唑镁对照品(约相当于奥美拉唑20mg),精密称定,置200ml量瓶中,加甲醇20ml,振摇1分钟,加入甲醇-0.05mol/l氢氧化钠溶液(20:80)130ml,超声5分钟使溶解,用甲醇-0.05mol/l氢氧化钠溶液(20:80)稀释至刻度,摇匀。
39.色谱条件用辛烷基硅烷键合硅胶为填充剂;以磷酸盐缓冲液(ph7.6)-乙腈(65:35)为流动相;检测波长为302nm;色谱柱柱温度为30℃;流速为每分钟1.0ml;进样体积20μl。
40.系统适用性要求理论塔板数按奥美拉唑峰计算不小于2000。
41.测定法精密量取供试品溶液与对照品溶液,分别注入液相色谱仪,记录色谱图,按外标法以峰面积计算每粒含量,并求出10粒的平均含量。
42.碳酸氢钠取本品20粒,精密称定,计算平均装量,取内容物,混合均匀,研细,精密称取适量(约相当于碳酸氢钠1g),加水50ml振摇使碳酸氢钠溶解,照电位滴定法测定,用盐酸滴定液(0.5mol/l)滴定。每1ml盐酸滴定液(0.5mol/l)相当于42.00mg的nahco3。
43.原料与各辅料按照1:1的配比进行混合,同时将原料和各辅料按照一定的配比进行混合,考察总混物料的相容性情况,原辅料单一配比和总混粉放置条件为40℃/75%rh(敞口)和40℃/75%rh(闭口)条件,同时总混粉增加高温60℃和光照条件放样,放样时间高湿为30天,高温为30天,光照为10天,并在实验过程中分阶段进行取样,首先检测敞口样品,如果敞口30天样品检测结果符合预期,闭口条件及其他时间点样品不进行检测;如果敞口30天样品检测结果没有达到预期目的,在进行其他样品检测。
44.处方信息
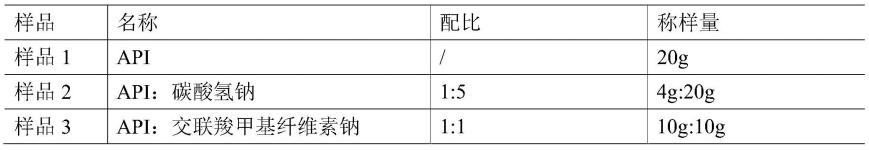
45.按照不同配比进行原辅料的称量及混合,详细组成见下表。
46.表1原辅料相容性各样品组成
[0047][0048][0049]
数据统计:样品放样前后性状及增失重率统计:采用称量瓶放样,记录放样前后样品重量,计算样品增失重率,为检测含量提供数据支持,同时通过性状考察,判断原辅料相容性情况。
[0050]
表2原辅料相容性结果(制剂)
[0051][0052][0053]
表3原辅料相容性结果(制剂)
[0054][0055]
表4原辅料相容性结果(分析)
[0056]
[0057][0058]
总结:通过对原辅料相容性的结果分析,崩解剂交联羧甲基纤维素钠和原料不相容,其他辅料与原料相容性结果均较好。参比制剂在高湿条件和高温条件下杂质增长较快,自制样品在高温条件下较为稳定。下一步实验需更换崩解剂种类,单独进行原料与不同崩解剂进行相容性考察工作。
[0059]
下一步试验思路:1、更换崩解剂种类,暂定崩解剂为交联聚维酮、羧甲淀粉钠和低取代羟丙纤维素,同时与原料进行混合进行相容性考察工作。崩解剂种类考察试验实验思路:前期原辅料相容性考察时崩解剂交联羧甲基纤维素钠和原料不相容,其他辅料与原料相容性结果均较好。所以更换崩解剂,筛选出合适的崩解剂。
[0060]
处方信息:按照不同配比进行原辅料的称量及混合,详细组成见下表。
[0061]
表5原辅料相容性各样品组成
[0062]
[0063][0064]
数据统计:样品放样前后性状及增失重率统计,采用称量瓶放样,记录放样前后样品重量,计算样品增失重率,为检测含量提供数据支持,同时通过性状考察,判断原辅料相容性情况。
[0065]
表6崩解剂种类考察性状增失重结果统计
[0066]
[0067]
[0068]
[0069]
[0070][0071]
小结:从实验结果可得,性状上在高温60℃条件下,含有api样品在放置后有类白色粉末变为类黄色粉末,空白辅料组颜色无变化;在高湿敞口条件下,均有结块现象;
[0072]
在高湿敞口条件下,交联聚维酮(斯泰克)、交联聚维酮(亚什兰)、羧甲淀粉钠与api 1:1混合样品增重严重,超过5%,每个样品放置15天与放置30天增重差异不大,这可能与崩解剂吸湿上限有关。在高湿闭口条件下个样品增重不明显。在高温、光照条件下各样品均有不同程度的失重。
[0073]
原辅料相容性试验结论:照《化学药物制剂研究基本技术指导原则》进行原辅料相容性试验,根据辅料经验用量分析原料与各辅料的处方比例,取原料与各辅料适量,以一定的比例混合均匀,在高温(60℃),加速(75%,40℃)条件下放置30天,分别于0天、30天取样,光照(5000lx)条件下放置10天,分别于0天、10天取样,考察性状、含量、有关物质、吸湿增重的变化。具体试验结果见下表。
[0074]
表7奥美拉唑镁与辅料相容性的试验结果
[0075][0076]
[0077]
从上述结果可以得出,奥美拉唑镁原料药在高温条件下稳定性稍差,高温60℃条件下总杂较室温0天条件下增加。奥美拉唑镁和各辅料相容性均相对较好,在高温、加速条件下总杂与室温条件下相当。奥美拉唑镁肠溶片在高温、加速条件下杂质增长均较快,且增长量较大,自制样品在加速条件下较为稳定。
[0078]
二、崩解剂羧甲淀粉钠用量考察实验报告
[0079]
崩解剂羧甲淀粉钠用量考察:
[0080]
实验思路:前期崩解剂种类考察实验结果显示羧甲淀粉钠与奥美拉唑镁碳酸氢钠胶囊中原辅料相容性较好,所以初步确定崩解剂采用羧甲基淀粉钠。此实验考察崩解剂羧甲淀粉钠用量(0%、1%、2%、3%、4%、5%)对奥美拉唑镁碳酸氢钠胶囊20mg规格产品溶出曲线影响情况。同时通过考察含量均匀度情况确定在工艺过程中药粉是否混合均匀。
[0081]
处方信息:按照不同崩解剂加入量制备处方,其余辅料用料不变,通过改变整体胶囊内容物重量保证崩解剂的加入量不同,测定胶囊的溶出曲线。
[0082]
表8不同崩解剂处方组成
[0083][0084]
数据统计装量考察结果在胶囊灌装过程中,胶囊的装量差异均在合格范围内。
[0085]
表9不同处方灌装量
[0086][0087]
溶出条件考察数据统计
[0088]
根据前期实验结果,首先溶出介质采用ph7.4,篮法50rpm。溶出数据如下表。
[0089]
表10不同处方溶出曲线比较
[0090]
[0091][0092]
小结:通过对不同崩解剂羧甲淀粉钠处方的溶出曲线考察,随着崩解剂的加入量增加,5min的溶出量逐渐增大,崩解剂加入量为1%-3%时,对前期的溶出量无明显影响。在15min时f10溶出量是最高的超过了85%,目标处方f3接近85%。f5、f6两个处方前期溶出量较高,但后期溶出平台低,可能是装量低影响。
[0093]
根据以目标处方f3为准计算其他处方f2值均大于50,,崩解剂用量在目标处方的基础上变化
±
1%及
±
2%的范围与目标处方比较均相似。
[0094]
1.3.3f5、f6溶出曲线情况比较
[0095]
溶出条件为介质采用ph7.4,篮法50rpm,结果如下:
[0096]
表11f5、f6溶出曲线比较
[0097][0098]
其他溶出条件考察情况
[0099]
表12f2 100rpm条件比较
[0100][0101]
小结:通过f2对溶出转数考察,结果显示。100rpm溶出速度较50转快,前期溶出量较高,后期溶出平台液较高。50转时在30min时溶出量大于85%,而在100转时在10min时就接近85%。
[0102]
表13含量均匀度
[0103]
[0104][0105]
小结:f1-f6其a 2.2s值均小于15,符合含量均匀度要求,说明按照等量递增添加碳酸氢钠以及过筛工艺可以将药粉完全混匀。
[0106]
数据分析总结:随着崩解剂羧甲淀粉钠用量增大,前期溶出量会逐渐增大,崩解剂用量在目标处方的基础上变化
±
1%及
±
2%的范围与目标处方比较均相似。
[0107]
含量均匀度结果显示利用等量递增添加碳酸氢钠并于其他原辅料过筛5遍可以完全混匀。
[0108]
制备实施例
[0109]
实施例1
[0110]
奥美拉唑镁10g,碳酸氢钠1000g,崩解剂羧甲淀粉钠10g,润滑剂硬脂酸镁2g。
[0111]
(1)将奥美拉唑镁、碳酸氢钠、崩解剂和润滑剂过80目筛;
[0112]
(2)将奥美拉唑镁、碳酸氢钠和崩解剂进行预混处理;
[0113]
(3)将润滑剂加入步骤(2)中,进行总混处理;
[0114]
(4)将步骤(3)制得的混合物制成胶囊。
[0115]
实施例2
[0116]
奥美拉唑镁11g,碳酸氢钠1600g,崩解剂羧甲淀粉钠25g,润滑剂硬脂酸镁10g。
[0117]
(1)将奥美拉唑镁、碳酸氢钠、崩解剂和润滑剂过80目筛;
[0118]
(2)将奥美拉唑镁、碳酸氢钠和崩解剂进行预混处理;
[0119]
(3)将润滑剂加入步骤(2)中,进行总混处理;
[0120]
(4)将步骤(3)制得的混合物制成胶囊。
[0121]
实施例3
[0122]
奥美拉唑镁10.3g,碳酸氢钠1100g,崩解剂羧甲淀粉钠10.3g,润滑剂硬脂酸镁6g。
[0123]
(1)将奥美拉唑镁、碳酸氢钠、崩解剂和润滑剂过80目筛;
[0124]
(2)将奥美拉唑镁、碳酸氢钠和崩解剂进行预混处理;
[0125]
(3)将润滑剂加入步骤(2)中,进行总混处理;
[0126]
(4)将步骤(3)制得的混合物制成胶囊。
[0127]
显然,上述实施例仅仅是为清楚地说明本发明所做的举例,而并非是对本发明实施方式的限定。其目的在于让熟悉此项技术的人士能够了解本发明的内容并据以实施,并不能以此限制本发明的保护范围。凡在本发明的精神和原则之内所做的任何修改、等同替换和改进等,均应包含在本发明权利要求的保护范围之内。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。