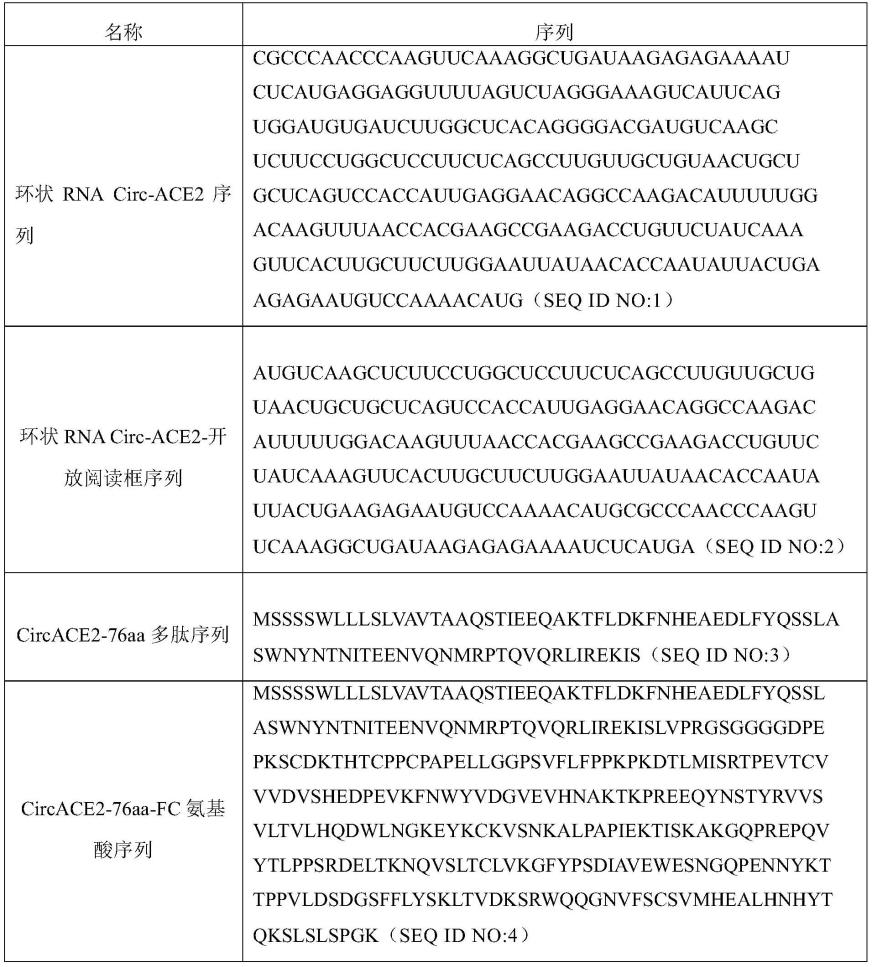
ccuguucuaucaaaguucacuugcuucuuggaauuauaacaccaauauuacugaa gagaauguccaaaacaug。
10.根据本发明实施例的环状rna序列翻译的多肽可显著抑制新型冠状病毒对细胞的侵 染能力。
11.根据本发明的实施例,上述环状rna分子还可以进一步包括如下附加技术特征至少之 一:
12.根据本发明的实施例,所述环状rna分子是由编码血管紧张素转化酶2的mrna序 列的第二外显子单独环化形成。
13.根据本发明的实施例,所述环化发生在胎盘组织中。
14.根据本发明的实施例,所述环状rna分子是由1)或2)所示核苷酸序列的起始核苷 酸和末端核苷酸相连形成,所述起始核苷酸设置为所述环状rna分子的第一位核苷酸。
15.根据本发明的实施例,所述环状rna编码区包括所述环状rna分子的第104位核苷 酸到第45位核苷酸。
16.根据本发明的实施例,所述环状rna编码区的核酸序列包括下列序列的至少之一:1) seq id no:2所示的rna序列;2)与1)具有至少70%同一性的rna序列,优选地,具 有至少80%同一性的rna序列,优选地,具有至少85%同一性的rna序列,优选地, 具有至少90%同一性的rna序列,优选地,具有至少95%同一性的rna序列,更优选 地,具有至少99%同一性的rna序列。
17.根据本发明实施例,所述seq id no:2的具体序列为:
18.augucaagcucuuccuggcuccuucucagccuuguugcuguaacugcugcuc aguccaccauugaggaacaggccaagacauuuuuggacaaguuuaaccacgaagc cgaagaccuguucuaucaaaguucacuugcuucuuggaauuauaacaccaauauu acugaagagaauguccaaaacaugcgcccaacccaaguucaaaggcugauaagag agaaaaucucauga。
19.根据本发明实施例的环状rna编码区核酸序列翻译的多肽可显著抑制新型冠状病毒 侵染细胞的能力。
20.在本发明的第二方面,本发明提出了一种多肽。根据本发明的实施例,所述多肽的氨 基酸序列包括下列序列的至少之一:1)seq id no:3所示的氨基酸序列;2)与1)具有至 少70%同一性的氨基酸序列,优选地,具有至少80%同一性的氨基酸序列,优选地,具有 至少85%同一性的氨基酸序列,优选地,具有至少90%同一性的氨基酸序列,优选地,具 有至少95%同一性的氨基酸序列,更优选地,具有至少99%同一性的氨基酸序列。根据本 发明实施例,所述多肽可显著抑制新型冠状病毒对细胞的侵染能力。
21.根据本发明实施例,所述seq id no:3的具体序列为:
22.msssswlllslvavtaaqstieeqaktfldkfnheaedlfyqsslaswnyntnitee nvqnmrptqvqrlirekis。
23.根据本发明的实施例,上述多肽还可以进一步包括如下附加技术特征至少之一:
24.根据本发明的实施例,所述多肽含有信号肽序列。
25.根据本发明的实施例,所述信号肽的氨基酸序列为msssswlllslvavtaa。
26.根据本发明的实施例,所述多肽存在于胎盘组织中。
27.在本发明的第三方面,本发明提出了一种融合蛋白。根据本发明的实施例,所述融合 蛋白包括第一、二方面所述的多肽和fc,所述多肽的c端与fc的n端相连。根据本发明 实
施例,所述融合蛋白可显著抑制新型冠状病毒对细胞的侵染能力。
28.根据本发明的实施例,所述融合蛋白还可以进一步包括如下附加技术特征至少之一:
29.根据本发明的实施例,所述融合蛋白包括下列序列的至少之一:1)seq id no:4所 示的氨基酸序列;2)与1)具有至少70%同一性的氨基酸序列,优选地,具有至少80% 同一性的氨基酸序列,优选地,具有至少85%同一性的氨基酸序列,优选地,具有至少90% 同一性的氨基酸序列,优选地,具有至少95%同一性的氨基酸序列,更优选地,具有至少 99%同一性的氨基酸序列。
30.根据本发明实施例,所述seq id no:4的具体序列为:
31.msssswlllslvavtaaqstieeqaktfldkfnheaedlfyqsslaswnyntnitee nvqnmrptqvqrlirekislvprgsggggdpepkscdkthtcppcpapellggpsvflfpp kpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvv svltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqv sltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvf scsvmhealhnhytqkslslspgk。
32.在本发明的第四方面,本发明提出了一种分离的核酸。根据本发明的实施例,所述分 离的核酸编码第三方面所述的融合蛋白。根据本发明实施例的分离的核酸序列翻译的融合 蛋白可显著抑制新型冠状病毒侵染细胞的能力。
33.根据本发明的实施例,所述分离的核酸还可以进一步包括如下附加技术特征至少之一:
34.根据本发明的实施例,所述核酸包括下列序列的至少之一:1)seq id no:5所示的 核苷酸序列;2)与1)具有至少70%同一性的核苷酸序列,优选地,具有至少80%同一 性的核苷酸序列序列,优选地,具有至少85%同一性的核苷酸序列,优选地,具有至少90% 同一性的核苷酸序列,优选地,具有至少95%同一性的核苷酸序列,更优选地,具有至少 99%同一性的核苷酸序列。
35.根据本发明实施例,所述seq id no:5的具体序列为:
36.atgtcaagctcttcctggctccttctcagccttgttgctgtaactgctgctcagtc caccattgaggaacaggccaagacatttttggacaagtttaaccacgaagccgaaga cctgttctatcaaagttcacttgcttcttggaattataacaccaatattactgaagaga atgtccaaaacatgcgcccaacccaagttcaaaggctgataagagagaaaatctcac tggtgcccagaggctccggcggcggcggcgatcctgagcccaaatcttgtgacaaaa ctcacacatgcccaccgtgcccagcacctgaactcctggggggaccgtcagtcttcc tcttccccccaaaacccaaggacaccctcatgatctcccggacccctgaggtcacatg cgtggtggtggacgtgagccacgaagaccctgaggtcaagttcaactggtacgtgga cggcgtggaggtgcataatgccaagacaaagccgcgggaggagcagtacaacagca cgtaccgtgtggtcagcgtcctcaccgtcctgcaccaggactggctgaatggcaagg agtacaagtgcaaggtctccaacaaagccctcccagcccccatcgagaaaaccatct ccaaagccaaagggcagccccgagaaccacaggtgtacaccctgcccccatcccggg atgagctgaccaagaaccaggtcagcctgacctgcctggtcaaaggcttctatccca gcgacatcgccgtggagtgggagagcaatgggcagccggagaacaactacaagacc acgcctcccgtgctggactccgacggctccttcttcctctacagcaagctcaccgtgg acaagagcaggtggcagcaggggaacgtcttctcatgctccgtgatgcatgaggctc tgcacaaccactacacgcagaagagcctctccctgtctccgggtaaatga。
37.在本发明的第五方面,本发明提出了一种表达载体。根据本发明的实施例,所述表
以便抑制新型冠状病毒侵染细胞。
48.根据本发明的实施例,所述多肽或融合蛋白在混合体系中的终浓度为10μg/ml或160 μg/ml。根据本发明实施例,所述多肽在混合体系中的终浓度为10μg/ml时可以将新冠假 病毒侵染细胞的能力抑制91.61%,终浓度为160μg/ml时可以将新冠假病毒侵染细胞的能 力抑制95.50%;所述融合蛋白(重组多肽)在混合体系中的终浓度为10μg/ml时可以将 新冠假病毒侵染细胞的能力抑制52.11%,终浓度为160μg/ml时可以将新冠假病毒侵染细 胞的能力抑制92.18%,根据本发明实施例中多肽或融合蛋白在混合体系中的终浓度给药, 适于保持药物的药效。
49.本发明的附加方面和优点将在下面的描述中部分给出,部分将从下面的描述中变得明 显,或通过本发明的实践了解到。
附图说明
50.本发明的上述和/或附加的方面和优点从结合下面附图对实施例的描述中将变得明显和 容易理解,其中:
51.图1是根据本发明实施例的ace2 mrna分子在人体各组织中的表达量情况的分布图;
52.图2是根据本发明实施例的环状rna circ-ace2在人体各组织中的表达量情况分布图;
53.图3是根据本发明实施例的环状rna circ-ace2形成的模式图,其中,ace2 rna于 第二外显子(exon2)位置发生剪切环化形成环状rna circ-ace2;
54.图4是根据本发明实施例的rna circ-ace2的pcr产物测序验证环状rna circ-ace2 环化序列的结果图,其中,pcr结果图由左至右的方向为pcr产物序列3’端到5’的方向;
55.图5是根据本发明实施例的环状rna circ-ace2的跨越接口的编码阅读框的分析图, 其中,环状rna分子的编码序列为环状rna分子序列的第104位核苷酸至45位核苷酸 跨越环化接口的核苷酸序列,具体序列为图中划线序列;
56.图6是根据本发明实施例的circace2-76aa多肽和ace2编码的蛋白质的氨基酸序列 的比对分析图,其中,与ace2蛋白氨基酸序列比对,circace2-76aa含有ace2的n端 62个氨基酸以及携带特异性14个氨基酸(rptqvqrlirekis)的c末端;
57.图7是根据本发明实施例的环状rna circ-ace2分子翻译的多肽的质谱鉴定结果图;
58.图8是根据本发明实施例的circace2-76aa的氨基酸序列在线程序分析图;
59.图9是根据本发明实施例的circace2-76aa在荧光显微镜下的细胞定位图;
60.图10是根据本发明实施例的化学合成多肽circace2-76aa检测新型冠状假病毒侵染细 胞实验中假病毒携带的egfp基因表达量差异倍数的结果图;以及
61.图11是根据本发明实施例的重组蛋白circace2-76aa-fc检测新型冠状假病毒侵染细 胞实验中假病毒携带的egfp基因表达量差异倍数的的结果图。
具体实施方式
62.下面详细描述本发明的实施例,所述实施例的示例在附图中示出。下面通过参考附图 描述的实施例是示例性的,旨在用于解释本发明,而不能理解为对本发明的限制。
63.术语解释
64.在文中,术语“新型冠状病毒”、“新冠病毒”、“covid-19”、均指引发新型冠状 病毒肺炎的病原体。
65.同一性,本发明,为了比较两个或更多个核苷酸序列,可以通过将[第一序列中与相应 位置的核苷酸相同的核苷酸的数目相除]来计算第一序列和第二序列之间的“序列同一性
”ꢀ
的百分比。第二个序列中的核苷酸]减去[第一个序列中核苷酸的总数],然后乘以[100%], 其中第二个核苷酸序列中每个核苷酸的缺失,插入,取代或添加-相对于第一核苷酸序列
‑ꢀ
被认为是单个核苷酸(位置)上的差异。
[0066]
或者,可以使用标准设置,使用用于序列比对的已知计算机算法,例如ncbi blast v2.0, 计算两个或多个核苷酸序列之间的序列同一性程度。
[0067]
用于确定序列同一性程度的一些其他技术,计算机算法和设置例如在wo 04/037999, ep 0 967 284,ep 1 085 089,wo 00/55318,wo 00/78972,wo 98/49185和gb 2357768-a。
[0068]
同一性,本发明,为了比较两个或多个氨基酸序列,第一氨基酸序列和第二氨基酸序 列之间的“序列同一性”百分比可以通过将[第一氨基酸序列中的氨基酸残基数目除以与[第 二个氨基酸序列中相应位置的氨基酸残基]相同,为[第一个氨基酸序列中核苷酸的总数], 然后乘以[100%],其中每个缺失,插入,取代或添加与第一氨基酸序列相比,第二氨基酸 序列中氨基酸残基的“残基”被认为是单个氨基酸残基(位置)上的差异,即,如本文所 定义的“氨基酸差异”。
[0069]
备选地,可以再次使用标准设置,使用已知的计算机算法来计算两个氨基酸序列之间 的序列同一性程度,例如上述用于确定核苷酸序列的序列同一性程度的算法。
[0070]
通常,为了根据上文概述的计算方法确定两个氨基酸序列之间的“序列同一性”的百 分比,将具有最大氨基酸残基数量的氨基酸序列作为“第一”氨基酸氨基酸序列,另一个 氨基酸序列将作为“第二”氨基酸序列。
[0071]
同样,在确定两个氨基酸序列之间的序列同一性程度时,技术人员可以考虑所谓的“保 守”氨基酸取代,其通常可以描述为其中氨基酸残基被替换为的氨基酸取代。具有相似化 学结构的另一个氨基酸残基,其对多肽的功能,活性或其他生物学特性几乎没有影响或基 本没有影响。这样的保守氨基酸取代在本领域中是众所周知的,例如,从wo 04/037999, gb-a-2357768,wo 98/49185,wo 00/46383和wo 01/09300;和wo 01/09300。可以基 于来自wo 04/037999以及wo 98/49185的相关教导以及从其中引用的其他参考文献中选 择和/或(优选)这种取代的类型和/或组合。
[0072]
本实施例发明人对环状rna circatlas综合数据库进行深度分析挖掘,发明人发现了 ace2基因在胎盘组织中特异性形成了一个环状rna分子,所述环状rna分子是由ace2 rna的第二外显子单独环化形成,发明人将其命名为circ-ace2;对环状rna circ-ace2 序列分析及实验验证结果提示circace2可以翻译含有分泌信号肽的多肽,所述多肽为一 个全新的多肽分子,发明人将其命名为circace2-76aa,该多肽长度为76个氨基酸。本发 明通
过化学合成多肽circace2-76aa以及真核细胞表达融合人类免疫球蛋白g的fc片段 获得重组多肽circace2-76aa-fc,利用新冠假病毒体外侵染人hace2-293t细胞的策略验 证circace2-76aa的抗病毒功能,结果显示化学合成circace2-76aa多肽以及重组多肽 circace2-76aa-fc能明显抑制新冠假病毒的细胞侵染能力,本发明涉及到的circace2-76aa 多肽以及重组多肽circace2-76aa-fc可以成为抑制covid-19病毒感染的候选分子。
[0073]
下面将对实施例作具体介绍。下述实施例中所使用的实验方法如无特殊说明,均为常 规方法。下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
[0074]
实施例1环状rna circ-ace2在分离的胎盘组织中的识别与鉴定
[0075]
本实施例中的人胎盘组织来自于临床妇产科孕妇自然分娩后的废弃胎盘。
[0076]
1、分离的胎盘组织中环状rna circ-ace2的识别
[0077]
ace2 mrna在人多个组织中广泛表达,该基因在人体各组织表达分布如图1所 示。发明人通过对环状rna circatlas综合数据库进行深度分析挖掘,发现在分离的胎 盘组织中ace2基因特异性的发生了环化剪切,形成了环状rna circ-ace2,如图2 所示。
[0078]
2、分离的胎盘组织中环状rna circ-ace2测序鉴定
[0079]
设计特异性检测环状rna circ-ace2的pcr检测引物,引物上游序列为: 5'gaagccgaagacctgttcta3',下游序列为:5'tcttatcagcctttgaacttgg 3',扩增片段大小为114bp。用trizol法提取分离的胎盘组织标本总rna,采用逆转录 试剂盒(vazyme公司),用随机引物将rna逆转录成cdna,pcr扩增反应体系及 条件如下:pcr为50μl总体系,具体是2
×
pcr mix(vazyme公司)25μl,上、下 游引物(10mm)各2μl,cdna模板1μl,用灭菌水补足至50μl体系。反应条件为: cdna预变性为95℃,时间为3min,第一步扩增:变性,温度为95℃,时间为30s, 退火,温度60℃,时间为30s,延伸,温度为72℃,时间为30s,35次循环,pcr反 应循环后72℃继续延伸3min,然后16℃保存。pcr产物经过1.5%浓度的琼脂糖凝胶 分离,割胶纯化后做sanger dna序列测定。由图3可以看出,环状rna circ-ace2 为ace2 mrna的第二个单独外显子经过环化剪切形成的环形的rna分子。由图4所 示,发明人通过pcr产物sanger dna测序的方法鉴定环状rna circ-ace2的准确环 化接口,circ-ace2 rna的序列长度为289nt,具体核酸序列如seq id no:1所示。
[0080]
3、对rna circ-ace2进行编码潜能分析
[0081]
根据rna circ-ace2的核酸序列运用orf finder在线程序进行编码潜能分析, 发现环状rna circ-ace2含有一个跨越环状rna接口的阅读框,如图5所示,环状 rna circ-ace2翻译多肽的编码区由231个碱基组成,碱基序列如seq id no:2所示; rna circ-ace2翻译多肽长度为76个氨基酸,本发明中将其命名为circace2-76aa, 氨基酸序列如seq id no:3所示。将circace2-76aa和rna ace2编码的蛋白氨基酸 序列进行比对分析,结果显示,circace2-76aa含有ace2的n端62个氨基酸以及携 带特异性14个氨基酸(rptqvqrlirekis)的c末端,如图6所示。
[0082]
实施例2环状rna circ-ace2翻译的多肽circace2-76aa鉴定
[0083]
1、环状rna circ-ace2表达质粒设计构建
[0084]
根据环状rna circ-ace2序列信息,通过全基因化学合成的方法获得目标序列, 然后将序列通过限制性内切酶ecori和bamhi构建到环状rna表达载体pcd5-cir(吉 赛生物)。
[0085]
2、构建红色荧光蛋白融合表达质粒circace2-76aa-mcherry
[0086]
根据环状rna表达载体circrna mini vector(addgeneid:#60648)环状rna表 达设计方法,设计circace2-76aa和红色荧光蛋白mcherry融合环状rna表达载体 circace2-76aa-mcherry,将mcherry基因片段本身的起始密码子atg和终止密码子去 掉,插入到circace2-76aa的终止密码子前端,序列两端添加circrna mini vector载 体的环化介导序列,最终设计的表达框架如seq id no:7所示;circace2-76aa-mcherry 环状rna融合表达框架设计后,通过全基因化学合成的方法获得表达框架,然后用 ecori和bamhi限制性内切酶位点将表达框架构建到pcdna3.1( )表达载体中。
[0087]
3、circace2-76aa-mcherry转染hace2-293t细胞
[0088]
将环状rna circ-ace2表达质粒转染293t细胞后,将环状rna circ-ace2表达产物 进行sds-page蛋白电泳、考马斯亮蓝染色,割胶进行质谱鉴定。如图7所示,质谱鉴定 到由环状rna circ-ace2翻译的跨越环化接口的肽段;质谱打到的肽段序列为 qnmrptavqr,序列显示未环状rna circ-ace2翻译的末端特异性氨基酸序列;对 circace2-76aa多肽进行氨基酸序列分析发现,分析采用signalp-4.1在线程序,如图8所 示,circace2-76aa不含有跨膜氨基酸序列,含有典型的分泌信号肽序列,circace2-76aa 的分泌信号肽序列为n端的17个氨基酸组成,序列为msssswlllslvavtaa;通过荧 光显微镜利用融合的mcherry红色荧光蛋白进行circace2-76aa多肽定位观察,发现 circace2-76aa多肽具有向细胞外分泌的特征,结果如图9所示。
[0089]
实施例3化学合成多肽circace2-76aa方法
[0090]
本实施例委托上海波肽生物公司进行多肽的化学合成,多肽采用固相合成法。肽链合 成:采用fmoc/pybop方法。fmoc保护基团的脱除用30%六氢吡啶的dmf溶液;肽链从 树脂上的切落用切肽试剂(三氟乙酸/结晶苯酚/水/乙二硫醇/甲乙硫醚/=81.5/5/5/5/2.5/1)。 多肽纯化及检测:使用c18反相柱子,条件为:a相为95%的水(甲醇配比),b相为95% 的甲醇(甲醇配比),然后各加0.1%的tfa,常规条件:在上样品之前先用a相平衡柱 子15分钟,然后上样,从a相到b相为25分钟梯度。检测波长:220nm,流速:1ml/min, 先用a溶液平衡柱子,上样后,从a到b溶液梯度洗脱25min,收集目标肽;合成的多肽 采用质谱仪做质谱鉴定。
[0091]
实施例4 circace2-76aa-fc多肽重组表达质粒构建及真核细胞表达纯化
[0092]
1、构建多肽重组表达质粒
[0093]
根据circace2-76aa的编码核酸序列及人的免疫球蛋白igg序列,设计重组表达框架, 其核酸序列如seq id no:5所示;使用分段pcr扩增及重叠pcr拼接扩增的策略获得 circace2-76aa-fc表达框架,然后将框架用ecori和bamhi内切酶位点链接到pcdna3.1 ( )载体中。
[0094]
2、表达质粒真核细胞转染
[0095]
细胞培养到2.5-3.0million/ml的密度,在温度为37℃,转速为120rpm,8%co2条件 下采用2l的培养瓶培养500ml的细胞;按照每500ml细胞转染0.5mg的质粒,pei为质 粒的量的2.7倍来转染。首先准备10ml新鲜培养基(以500ml为例子),先加入50μg 质粒,混匀,慢慢加入相应的量的pei,孵育5~10min(可观察到培养基从原先的透明状态 变为稍微浑浊),孵育结束后加入到细胞中,将细胞在33℃、co2为8%、转速为120rpm 条件下表达,表达
6天可以收集细胞上清,表达结束。
[0096]
3、circace2-76aa-fc重组多肽的纯化
[0097]
在收集管上每管加5ml的中和液(1m tris-hcl ph8.0),akta prue柱子(akta prue 柱子:含protein a(cytiva公司,货号:17040301))用binding buffer(20mm磷酸盐)平 衡,细胞上清液为500ml,加入到纯化柱子体积设置为1500ml,上柱子后用binding buffer (20mm磷酸盐)洗杂蛋白80ml,elution buffer(0.1m柠檬酸,ph3.0)洗脱100ml,收 集管每管5ml,取峰位置的收集管跑胶,确定有蛋白的收集管,浓缩蛋白,最后将蛋白置 换到pbs里。
[0098]
实施例5 circace2-76aa多肽、重组circace2-76aa-fc测试covid-19新型冠状假 病毒侵染细胞实验
[0099]
使用商业化新型冠状病毒s蛋白重组假病毒和稳定过表达人ace2全长基因293t细胞 株hace2-293t(广州派真生物公司)可以模拟病毒入侵细胞的过程,将化学合成的 circace2-76aa多肽(seq id no:6)及在293t中做真核表达获得的重组多肽 circace2-76aa-fc(seq id no:4)分别和新冠假病毒混合孵育,然后侵染hace2-293t 细胞,具体操作如下:在96孔板中铺hace2-293t细胞,密度1
×
104个细胞/孔;12小时 细胞贴壁,做假病毒covid-19侵染实验;每孔细胞加入5μl假病毒(约1万个病毒颗粒), 以及不同浓度的多肽,假病毒和多肽按照比例先在体外100μl dmem完全培养基中混匀, 常温放置30min,假病毒侵染细胞前加终浓度8μg/ml聚凝胺。
[0100]
通过新冠假病毒中携带的egfp基因序列,采用提取侵染后细胞的基因组dna,进行 qpcr荧光定量检测,定量检测化学合成circace2-76aa多肽及重组circace2-76aa-fc在 抑制新冠假病毒covid-19侵染细胞中的作用,具体操作如下:假病毒感染hace2-293t 细胞15h后;抽走细胞培养基,每孔直接加入100μl细胞基因组dna提取裂解液,将细 胞在96孔板中混匀裂解后,转移到1.5ml离心管中,然后提取基因组dna,无菌水溶解 提取的dna,取1μl基因组dna做qpcr荧光定量检测,检测假病毒携带的egfp基因 整合到细胞基因组的情况,gapdh基因做内参,评估新冠假病毒侵染hace2-293t细胞的 能力。
[0101]
qpcr检测:qpcr检测按照荧光定量反应试剂盒qpcr试剂盒(vazyme公司)的说 明书配置反应体系,qpcr反应体系为20μl,10μl的2x sybr green pcr master mix, 上、下游引物(10μm)各加0.4μl,模板dna加1μl,最后用无菌去离子水补足至20μl; 荧光定量pcr反应条件:cdna预变性为95℃,时间为5min;第一步扩增:变性,温 度为95℃,时间为10s,退火,温度为60℃,时间为35s(此步骤收集荧光信号);40次 循环,然后进行熔解曲线分析:温度60℃~95℃收集荧光信号。qpcr检测引物的序列为:egfp-上游引物:5'ttcaaggaggacggcaacat 3',egfp-下游引物:5' tggcggatcttgaagttcac 3',引物扩增大小为119bp。
[0102]
由图10可以看出,化学合成的多肽circace2-76aa在10μg/ml浓度下可以将新冠假病 毒侵染细胞的能力抑制91.61%,160μg/ml浓度下可以将新冠假病毒侵染细胞的能力抑制 95.50%。图11显示,重组circace2-76aa-fc在10μg/ml浓度下可以将新冠假病毒侵染细 胞的能力抑制52.11%,160μg/ml浓度下可以将新冠假病毒侵染细胞的能力抑制92.18%, 具体结果如图11所示。
[0103]
表1:
[0104]
[0105]
[0106][0107]
注:划线序列为环状rna介导序列
[0108]
在本说明书的描述中,参考术语“一个实施例”、“一些实施例”、“示例”、“具体示例”、 或“一些示例”等的描述意指结合该实施例或示例描述的具体特征、结构、材料或者特点包 含于本发明的至少一个实施例或示例中。在本说明书中,对上述术语的示意性表述不必须 针对的是相同的实施例或示例。而且,描述的具体特征、结构、材料或者特点可以在任一 个或多个实施例或示例中以合适的方式结合。此外,在不相互矛盾的情况下,本领域的技 术人员可以将本说明书中描述的不同实施例或示例以及不同实施例或示例的特征进行结合 和组合。
[0109]
尽管上面已经示出和描述了本发明的实施例,可以理解的是,上述实施例是示例性的, 不能理解为对本发明的限制,本领域的普通技术人员在本发明的范围内可以对上述实施例 进行变化、修改、替换和变型。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。