1.本发明属于幽门螺杆菌治疗技术领域,具体涉及一种黑磷纳米颗粒片及其制备方法和应用。
背景技术:
2.幽门螺杆菌(helicobacter pylori,h.pylori)是一种高度流行的革兰氏阴性细菌,感染全世界约50%的人口的胃粘膜。研究证实由于h.pylori定植在胃黏膜的深处,抗h.pylori的药物不易到达此位置,另一方面由于胃本身的排空作用使得药物在胃中的停留时间过短。而且随着各种抗生素的使用,h.pylori的耐药性问题使得按照标准方案进行的治疗变得更加困难。例如,标准的一线三联疗法,包括质子泵抑制剂和两种抗生素,通常是克拉霉素和阿莫西林或甲硝唑,其疗效下降到近70%,低于最初80%的目标。综合以上因素,如何克服耐药性问题,并使得药物在胃部长时间停留以达到有效的治疗浓度从而增加进入胃粘膜深处的几率是现如今治疗h.pylori的研究方向。因此,纳米药物由于其自身的高载药量,生物相容性以及响应性释放的特性使得其在治疗h.pylori感染中占据一席之地。
3.口服给药依然是目前治疗h.pylori感染的主要方式,不过胃粘膜表面的粘膜屏障和大量的粘液虽然可以通过清除病原体和外来颗粒保护暴露的上皮表面,但同时也构成了纳米药物吸收过程中的较大障碍;另一方面,粘液形成的酸性环境也严重影响着口服抗菌药物发挥作用。因此,由于口服药物穿透黏膜和跨越上皮吸收屏障的能力较差,以及对酸环境的不耐受,导致口服药物并不能达到预期的效果。本项目拟设计一种具有优异的粘液穿透能力,细胞膜穿透能力并具有酸响应作用的新型纳米复合物,以促进口服药物的吸收,增强对h.pylori感染的抵抗作用。
技术实现要素:
4.解决的技术问题:本发明针对上述技术问题,提供一种黑磷纳米颗粒片及其制备方法和应用。本发明涉及的由异乌药内酯(isl)和鼠李糖脂(rhl)自组装的黑磷(bp)纳米颗粒片制备是全新的制备工艺,流程简便、操作简单、产量比较高;而且该工艺制备的纳米颗粒片不仅对h.pylori有特异性的抑制作用,具有优异的粘液和细胞膜穿透能力,还具有酸响应以及光热转化能力。
5.技术方案:黑磷纳米颗粒片的制备方法,首先将黑磷(bp)浸没在n,n
’‑
二甲基甲酰胺 (dmf)溶液中,经超声后离心制成黑磷纳米片;随后将异乌药内酯(isl)母液与黑磷纳米片混合并超声溶解,再加入鼠李糖脂(rhl)溶于上述混合物中,经超声充分混匀后,采用纳米沉淀法滴加ph 7.4的进行组装;组装完毕后用透析袋在磷酸缓冲液中透析,至磷酸缓冲液澄清透明;最后用真空冷冻干燥器将所得样品干燥得黑磷纳米颗粒片。
6.上述黑磷纳米片的具体制备步骤为:取块状bp 500mg,浸没于dmf(n,n
’‑
二甲基甲酰胺)中,300w冰浴探头超声2h后,经6000rpm离心4min,取上清,随后将上清12000rpm 离心
4min后取沉淀,重悬于dmf中配制成1mg/ml的bp纳米片重悬液备用。
7.上述组装的具体方法为:配制好1mg/ml的isl的dmf母液,再取100μg bp纳米片与 50μg isl混合并用100μl的dmf溶解,该混合物溶液超声5min后,再取1mg rhl溶于上述混合物中,超声5min后,在混合物中滴加ph 7.4溶液900μl,组装完成后,接着再在 ph 7.4磷酸缓冲液中透析4h以除去有机溶剂和未包封的isl。
8.上述方法制得的黑磷纳米颗粒片。
9.上述黑磷纳米颗粒片在制备治疗幽门螺杆菌药物中的应用。
10.治疗幽门螺杆菌药物,有效成分为上述的黑磷纳米颗粒片。
11.有益效果:本发明成功制备一种含异乌药内酯和鼠李糖抗h.pylori的黑磷纳米片,该纳米复合物制备简单,颗粒分散性好,稳定性高,具有较好的抗幽门螺旋杆菌和酸响应的作用。
附图说明
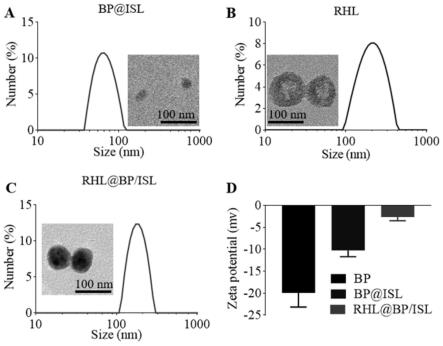
12.图1为rhl@bp/isl纳米片的合成和表征示意图,其中bp@isl(a)、rhl(b)和 rhl@bp/isl(c)水动力粒径分布及透射电镜图像;bp@isl、rhl和rhl@bp/isl纳米复合物的zeta电位(d);
13.图2为rhl@bp/isl纳米片的光热转化能力和不同酸性条件下对isl药物释放率示意图,其中(a)rhl@bp/isl纳米片在808nm近红外激光照射10min下的红外热成像图;(b) isl体外释放研究:rhl@bp/isl纳米片在808nm激光照射下不同ph(ph 7.4和ph 3.0) 的累积释放曲线。数据以均数
±
标准差表示(n=3);
14.图3为rhl@bp/isl纳米片的体外抗菌能力;
15.图4为纳米复合物在体内的分布和代谢情况示意图;
16.图5为纳米复合物在体内光热转化实验示意图,其中rhl@bp/isl纳米复合物在动物模型体内经808nm激光照射10min下的红外热像图(a)、bp@isl光热曲线(b)、rhl@bp/isl 光热曲线(c);
17.图6为rhl@bp/isl纳米片的体内抗菌作用示意图;
18.图7rhl@bp/isl纳米片的体内抗菌作用;
19.图8h&e和tunel染色检测rhl@bp/isl纳米片在体内对胃粘膜的修复作用;
20.图9免疫荧光染色检测rhl@bp/isl纳米片在体内对炎症因子的恢复作用;
21.图10rhl@bp/isl纳米片细胞毒性检测。
具体实施方式
22.实施例1
23.材料与方法
24.1.黑磷(bp)纳米片处理方法:取块状bp 500mg,浸没于dmf(n,n
’‑
二甲基甲酰胺) 中,300w冰浴探头超声2h后,经6000rpm离心4min,取上清,随后将上清12000rpm离心4min后取沉淀,重悬于dmf中配制成1mg/ml的bp纳米片重悬液备用。
25.2.rhl@bp/isl的组装方法:采用纳米沉淀法,具体为配制好1mg/ml的isl的dmf 母液,再取100μg bp纳米片与50μg的isl混合并用100μl的dmf溶解,该混合物溶液超声5min充
分混合后,再取1mg rhl溶于上述混合物中,超声5min后,在混合物中缓慢滴加ph 7.4磷酸缓冲液900μl,组装完成后,测定其粒径及电位,接着再在ph 7.4磷酸缓冲液中透析4h以除去有机溶剂和未包封的isl,再测定其粒径及电位。
26.3.载药量测试方法:取组装好经透析后的rhl@bp/isl混合溶液100μl,加入100μl色谱乙腈,超声10min使该纳米混合物充分溶解释放出疏水核心里的isl,再经hplc上样检测其isl含量,hplc方法:流动相:甲醇:乙腈:水=30:30:40,等度洗脱,柱温:40℃,流速:1ml/min,检测波长:235nm,洗脱时间:15min。
27.4.粒径及zeta电位:将bp纳米片重悬液,rhl及rhl@bp/isl纳米复合物分别加入样品池,置于zetasizer nano zs激光粒度仪中,使用动态光散射(dls)法测量其粒径,使用电泳光散射(els)法测量其zeta电势。
28.5.透射电子显微镜考察:取适量bp,rhl及rhl@bp/isl纳米复合物分散于去离子水中,吸取10μl样品溶液,滴至碳涂层铜网上,在红外灯下烤干。置于透射电子显微镜下观察样品形态,加速电压80kv。
29.6.rhl@bp/isl纳米复合物光热转化能力的考察:为考察黑磷纳米复合物光热转化能力,以pbs设为对照组,制备0.5ml的rhl@bp/isl溶液置于ep管中,用808nm近红外激光发射器对ep管进行照射(1.0w/cm2,照射10分钟),对每一样品照射时,使光源与ep管距离相同,并使光斑覆盖分散液全部区域。用数字万用表记录下照射过程中分散液温度变化,探针置于分散液中心部位且不与ep管接触。照射过程中,用热成像仪记录ep管热辐射图像。
30.7.isl从rhl@bp/isl纳米复合物中释放效率的考察:为更好的模拟isl从rhl@bp/isl 纳米复合物中释放的实际环境,实验考察了ph 7.4(生理环境),ph 3.0(胃部酸性环境)条件下,808nm激光照射后isl从rhl@bp/isl纳米复合物中的释放效率。精密称取 rhl@bp/isl纳米复合物,分散于10ml不同ph的去离子水中,置于37℃水浴中缓慢震摇。每一样品制备多分,分别于0、2、4、6、8、10及12小时,将样品从水浴中取出,12000 g离心30分钟,上清液用hplc分析isl释放量。对于光照组,808nm激光(1.0w/cm2,照射10分钟)或650nm激光(0.5w/cm2,照射10分钟)于0小时进行一次。
31.液相色谱条件:
32.色谱柱:c18,4.6
×
50mm,3.5μm。
33.流动相:a为添加0.01%磷酸的去离子水,b为添加0.01%磷酸的乙腈。流动相从5%含量b逐渐变为95%含量b,梯度时间为1.3分钟。
34.流速:1.8ml/min
35.柱温:45℃
36.检测后,按标准曲线计算ly的释放量,并以释放量对时间作图,得到isl从rhl@bp/isl 纳米复合物中释放的累计释放曲线。
37.8.菌株:标准菌株26695、g27、南京医科大学毕洪凯实验室赠送、hyq002和hyq003 (甲硝唑、克拉霉素、左氧氟沙星耐药)右江民族医学院耐药微生物感染防治研究中心从临床分离。
38.9.培养基和主要试剂:哥伦比亚培养基、脑心浸液培养基、选择性抗生素(万古霉素、多粘菌素b、甲氧苄氨嘧啶)、血清、奥美拉唑、阿莫西林、克拉霉素、革兰氏染色液、细菌基因组dna提取试剂盒、幽门螺杆菌16s rrna特异性引物。
39.10.检测药物在不同的ph条件中对h.pylori的抑菌浓度(100μl体系)
40.(1)药物制备:配备rhl@bp/isl、rhl@bp、rhl@isl、rhl、isl 0.1mg/ml。
41.(2)mic板制备:取ph3.0、ph4.5、ph6.0、ph7.0培养基90μl加入96孔板中。
42.(3)菌液制备:取固体平板上对数期生长的h.pylori(hyq002、26695、g27、hyq003) 用bhi培养基制作成菌悬液,调整浓度od600为0.3(1
×
108cfu/ml),稀释10倍,为 1
×
107cfu/ml,备用。
43.(4)接种菌液:取10μl加至96孔板中(使菌液终浓度为1
×
106cfu/ml)。
44.(5)加入药物:加入预先配备的药物,使药物终浓度为0.125μg/ml,pbs作为阴性对照。将96孔板放置三气震荡培养箱中。
45.(6)取菌涂板:药物作用一定时间后(如1h、2h、4h),从孔中取100μl培养的菌液稀释(10、100倍等),涂布于无抗菌化合物的哥伦比亚琼脂平板,置三气培养箱培养3-4天。
46.(7)结果判断:计算琼脂平板上生长的细菌个数,每个药物重复3次试验。
47.11.构建动物模型体内检测rhl@bp/isl纳米复合物对h.pylori的抑制效果
48.rhl@bp/isl纳米复合物、isl中药单体、奥美拉唑、阿莫西林及克拉霉素均溶解稀释为10mg/ml。实验动物:c57bl/6。
49.动物分组:实验组将造模成功的感染组(hyq003)平均分成5组,分别为奥美拉唑 阿莫西林 克拉霉素组、奥美拉唑 rhl@bp/isl纳米复合物组(28mg/kg)、奥美拉唑 rhl@bp/isl纳米复合物组(7mg/kg)、rhl@bp/isl纳米复合物组(28mg/kg)、rhl@bp/isl纳米复合物组(7mg/kg)、rhl@bp/isl纳米复合物(7mg/kg) nir 10min 组和pbs组,每组10只;未感染h.pylori的10只小鼠为阴性对照组。
50.(2)动物给药:实验组灌胃给药,有奥美拉唑的组先给予奥美拉唑,30min后再给其它药物,给完药物后禁食禁水4小时;小鼠体重按照平均20g/只计算,给药量为奥美拉唑 138.2mg/kg、阿莫西林28.5mg/kg、克拉霉素14.3mg/kg、rhl@bp/isl纳米复合物7mg/kg每天给药1次,连续3次;阴性对照组给pbs溶液,容量、次数同上;rhl@bp/isl纳米复合物(7mg/kg) nir 10min组用红外线照射小鼠10min。每天给药1次,连续给药3天。
51.(3)药效检测:停药后第2天感染组的小鼠称重并计算平均体重,眼球采血,行断颈处死,取胃组织,破碎,h.pylori的分离培养和鉴定及计算定植量。部分胃组织进行石蜡切片并做h&e染色检查、tunel染色检查,炎症因子做免疫荧光检查。
52.12.药物细胞毒性检测
53.对rhl@bp/isl纳米复合物进行安全性初步评估,用cck-8方法检测化合物细胞毒性,具体如下:
54.(1)制备ges-1和bgc823细胞悬液,调浓度为1
×
105。
55.(2)接种到96孔板中:每孔100μl,同样的样本做3个重复。
56.(3)37℃培养箱中培养24小时。
57.(4)加入rhl@bp/isl纳米复合物,使得工作浓度分别为:20μg/ml、15μg/ml、10μg/ml、 5μg/ml、0μg/ml,设加药不加细胞组。
58.(5)37℃培养箱中培养24小时。
59.(6)加入10μl cck8,轻敲混匀后培养4小时。
60.(7)在450nm测定吸光度,根据以下公式计算存活率:
61.细胞存活率=[(as-ab)]/[(ac-ab)]
×
100%
[0062]
其中,as为有药物、cck-8、细胞培养基孔,ac为没有药物,只有cck-8和细胞培养基孔,ab为没有药物和细胞、只有cck-8和培养基孔。根据计算的存活率建立生存曲线。
[0063]
结果
[0064]
1.rhl@bp/isl纳米片的合成和表征
[0065]
采用纳米沉淀法法制备了rhl@bp isl纳米片。isl与bp纳米片母液的质量比为1:2,经超声混合后,将rhl以1:4的比例溶解在上述混合溶液中,将ph 7.4的磷酸缓冲液在超声条件下缓慢滴加进混合溶液中制备得到rhl@bp isl纳米片。制备完成后,通过透析法去除游离的isl。采用动态光散射法(dls)测定了制备的bp@isl、rhl和rhl@bp/isl纳米片的水动力粒径。结果如图1:a-c所示,bp@isl粒径为83.9nm,多分散系数为0.135。 rhl粒径为132.1nm,多分散系数为0.216,rhl@bp isl粒径与rhl相似,为120.4,多分散系数为0.152。透射电子显微镜(tem)的结果与dls得到的粒径一致(图1-d)。zeta 电势结果显示,bp电势为-19.97
±
3.19mv,bp@isl电势为-10.23
±
1.46mv,rhl@bp isl电势为-2.63
±
0.86mv。在制备过程中,bp纳米片的氧化增强,表面负电荷增加。rhl涂层可以降低bp纳米片的表面负电荷。
[0066]
2.评价rhl@bp/isl纳米片的光热转化能力和不同酸性条件下对isl药物释放率
[0067]
在808nm激光近红外照射下,光能转化为热能并提高环境温度是bp纳米片光热治疗的基本要求。为了研究bp纳米片的光热转化能力以及功能化对bp纳米片光热转化能力的影响,将rhl@bp/isl纳米复合物分散于去离子水中,在808nm,1.0w/cm2,10min的近红外光照射下检测该纳米复合物的温度变化。从图2-a中可以看出,在10min内,纳米复合物的温度升高了20℃,这证实了bp的光热转换能力,可以有效提高环境温度,且样品之间的温度没有显著差异,说明功能化并没有影响bp的光热能力。通过在不同的酸性条件下,体外释放实验研究了rhl@bp/isl纳米复合物中isl在不同条件下的释放情况。在ph 3.0条件下,近红外照射10min后12h isl的累积释放率为87.40%
±
0.09,明显高于其他组(p《0.001) (图2-b)。这些结果表明,近红外光热作用能显著促进isl的释放,而rhl的包封使得该纳米复合物具有酸响应作用。
[0068]
3.rhl@bp isl纳米片的体外抗菌功能
[0069]
该研究检测了rhl@bp/isl纳米片及其组分在不同的ph(3.0、4.5、6.0、7.0)条件下对h.pylori的敏感菌株26695、g27和耐药菌株hyq002、hyq003抑制情况。结果如图3所示。在ph 3.0条件下,rhl@bp/isl纳米片(0.125mg/ml)组在给药2小时后,抑菌率达到99.999%,且经过nir 10min后抑菌效果更好,其抑菌效果明显优于ph 4.5、6.0、7.0(p《 0.001)。这一结果说明,rhl在bp纳米颗粒上的包封可为药物提供酸响应作用,并且bp的光热转换能力可以显著提高药物的抑菌效果。
[0070]
rhl@bp isl纳米片的体内代谢情况
[0071]
cy5标记的纳米药物通过灌胃治疗动物:利用体内成像技术观察该纳米复合物在体内的分布和代谢时间。如图4所示,我们在给药后4小时检测到,该纳米复合物在胃内荧光水平较强,而在其他地方荧光水平较弱。体内光热转化实验结果表明,口服4小时后rhl@bp isl 纳米片具有明显的光热转化能力,但未加rhl的纳米片组和isl组的光热转化能力大幅度减弱(图5)。
[0072]
rhl@bp isl纳米片的体内抗菌作用
[0073]
详见抗菌示意图(图6)。
[0074]
体内治疗效果:rhl@bp isl nir组对h.pylori的定植抑制作用、对胃粘膜炎症组织修复作用及炎症因子恢复明显优于三联治疗组(奥美拉唑 阿莫西林 甲硝唑)(p《0.001),且在rhl@bp isl nir、rhl@bp isl、rhl@bp isl 抑酸剂(奥美拉唑)中,rhl@bp isl nir效果最明显(p《0.05)(图7),同时克服h.pylori对甲硝唑和克拉霉素的耐药性,可以作为一线药物治疗h.pylori感染导致急性或慢性胃炎,如图7-9所示。
[0075]
rhl@bp/isl纳米片细胞毒性检测
[0076]
rhl@bp/isl纳米片在20μg/ml对ges-1(a)和bgc823(b)无明显的细胞毒性作用,存活率均在90%以上,可以作为一线药物治疗h.pylori,如图10所示。
[0077]
以上所述仅是本发明的优选实施方式,本发明的保护范围并不仅局限于上述实施例,凡属于本发明思路下的方案均属于本发明的保护范围。应当指出,对于本技术领域的人员来说,在不脱离本发明原理前提下的若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。