含有噻托溴铵和奥达特罗的可吸入溶液制剂
优先事项声明
1.本技术要求美国临时专利申请日的权益,申请号63/011,867,于2020年4月17日提交;申请号63/011,224,于2020年4月16日提交;以及2020年4月16日提交的申请号63/011,220,上述三篇专利的内容通过引用整体并入本文。
背景技术:
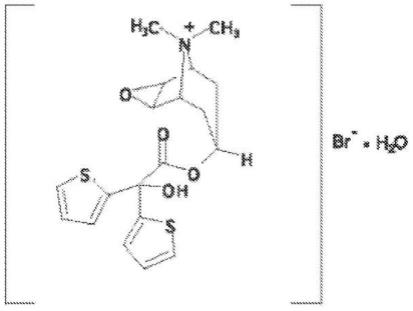
2.噻托溴铵一水合物在化学上描述为(1α,2β,4β,5α,7β)-7-[(羟基二-2-噻吩基乙酰基)氧基]-9,9-二甲基-3-氧杂-9-氮杂三环[3.3.1.02,4]壬烷溴化物一水合物,具有以下化学结构:
[0003]
盐酸奥达特罗,化学上描述为2h-l,4-苯并恶嗪-3h(4h)-1,6-羟基-8-[(lr)-l-羟基-2-[[2-(4-甲氧基苯基))-1,1-二甲基乙基]-氨基]乙基]-,单盐酸盐,公开于us7220742、us7491719、us7056916、us7727984中,并具有以下化学结构:
[0004]
噻托溴铵是一种长效毒蕈碱拮抗剂,通常称为抗胆碱能药。它对毒蕈碱受体亚型m1至m5具有相似的亲和力。在气道中,它通过抑制平滑肌上的m3受体表现出药理作用,导致支气管扩张。人类和动物来源的受体和离体器官制剂显示出拮抗作用的竞争性和可逆性。
[0005]
奥达特罗是一种长效β-2-肾上腺素能激动剂(laba),可激活气道平滑肌上的β-2肾上腺素能受体,引起支气管扩张。beta-2受体是支气管平滑肌中的肾上腺素能受体。这两种化合物具有有价值的药理特性。噻托溴铵和奥达特罗可在治疗哮喘或慢性阻塞性肺病(包括慢性支气管炎和肺气肿)中提供治疗益处。
[0006]
本发明涉及溶解在水中的噻托溴铵和奥达特罗或其药学上可接受的盐与优选使用雾化吸入装置施用的非活性成分的不含推进剂的可吸入制剂,以及产生的不含推进剂的
可吸入气雾剂由此。本发明公开的药物制剂特别适用于雾化吸入,与干粉吸入相比,其具有更好的肺沉积(通常高达55-60%)。
[0007]
本发明的药物制剂特别适用于通过雾化吸入给药活性物质,尤其适用于治疗哮喘和慢性阻塞性肺病。
技术实现要素:
[0008]
本发明涉及可通过雾化吸入给药的噻托溴铵和奥达特罗及其药学上可接受的盐或溶剂化物的药物制剂。本发明的药物制剂符合高质量标准。
[0009]
本发明的一个方面是提供含有噻托溴铵和奥达特罗或其药学上可接受的盐的水性药物制剂,其满足使用上文提及的吸入器实现制剂的最佳雾化所需的高标准。制剂中活性物质的药学稳定性应为若干年,优选一年,更优选三年。
[0010]
另一方面是提供不含推进剂的制剂,其为包含噻托溴铵和奥达特罗或其药学上可接受的盐的溶液,其可以使用吸入器在压力下雾化,吸入器优选为雾化吸入器装置,以提供气雾剂,其中气溶胶的粒径可重现地落在指定范围内。
[0011]
本发明的另一方面是提供药物制剂,其是包含噻托溴铵和奥达特罗或其药学上可接受的盐和其他无活性赋形剂的溶液,其可以使用基于超声波或基于气压的雾化器/吸入器通过雾化吸入给药。药物制剂表现出适合于允许几个月或几年,优选1-6个月,更优选一年,最优选三年的储存时间的稳定性。
[0012]
更具体地,另一方面是提供一种稳定的药物制剂,该制剂是含有噻托溴铵和奥达特罗或其药学上可接受的盐和其他赋形剂的水溶液,其可以使用超声、喷射或网状雾化器通过雾化吸入给药.本发明的制剂具有显着的长期稳定性。在一个实施方案中,制剂在约15℃至约25℃的温度下具有至少约6-24个月的储存时间。
具体实施方式
[0013]
使用合适的吸入器施用不含推进剂气体的液体制剂是有利的,以实现活性物质在肺中的更好分布。此外,增加通过吸入递送的药物的肺沉积是非常重要的。
[0014]
目前,传统的pmdi或dpi(干粉吸入)装置只能将大约20-30%的药物输送到肺部,导致大量药物沉积在口腔和喉部,可以进入胃和通过口腔消化系统引起不必要的副作用和/或二次吸收。
[0015]
因此,本领域需要通过吸入来改善药物递送以显着增加肺沉积。
[0016]
本发明的药物制剂是一种溶液,该溶液被雾化器转化为气溶胶,用于肺部。药液由雾化器通过高压喷射。
[0017]
可用于施用本发明的药物制剂的雾化装置是这样的那些装置,其中可以在一次抽吸中雾化少于约8毫升的药物溶液,优选少于约2毫升,最优选少于约1毫升。毫升,以便气雾剂的可吸入部分对应于治疗有效量。由一次抽吸形成的气雾剂的平均粒度小于约15微米,优选小于约10微米。溶液制剂不得含有任何可能与吸入器相互作用并影响溶液或产生的气雾剂的药物质量的成分。此外,药物制剂中的活性物质在储存时非常稳定,可以直接给药。
[0018]
因此,本发明的一个方面是提供一种包含噻托溴铵和奥达特罗或其药学上可接受的盐的水性药物制剂,其满足所需的高标准以便能够使用吸入器实现溶液的最佳雾化前文
提到。优选地,药物制剂中的活性物质是稳定的,并且具有几年的储存时间,优选一年,更优选三年。
[0019]
本发明的另一方面是提供不含推进剂的制剂,其为包含噻托溴铵和奥达特罗或其药学上可接受的盐的溶液,其使用吸入器,优选雾化吸入器在压力下雾化,其中所述药物组合物通过产生的气溶胶可重现地落在指定的粒径范围内。
[0020]
另一方面是提供一种水性药物制剂,该制剂是含有噻托溴铵和奥达特罗或其药学上可接受的盐以及其他可以通过吸入给药的无活性赋形剂的溶液。
[0021]
根据本发明,噻托溴铵和奥达特罗的任何药学上可接受的盐或溶剂合物可用于制剂。当术语噻托溴铵或和奥达特罗在本发明的范围内使用时,它分别被视为是指噻托溴铵或其盐或溶剂化物和奥达特罗或其盐或溶剂化物。
[0022]
在一个实施方案中,噻托溴铵的盐是噻托溴铵一水合物并且奥达特罗的盐是奥达特罗盐酸盐。
[0023]
在一个实施方案中,活性物质是噻托溴铵一水合物和奥达特罗盐酸盐的组合。
[0024]
在根据本发明的制剂中,噻托溴铵和奥达特罗溶解在溶剂中。在一种实施方式中,溶剂是水。
[0025]
最终药物制剂中噻托溴铵和奥达特罗的浓度取决于所需的治疗效果。在一个实施方案中,制剂中奥达特罗的浓度介于约18.2μg/100ml和约182mg/100ml之间,例如约25mg/100ml。在一实施例中,噻托溴铵的浓度介于约20.7μg/100ml与约207mg/100ml之间,例如约28mg/100ml。
[0026]
在根据本发明的制剂中,如果需要,可以通过向制剂中加入酸或碱作为ph调节剂来调节ph。在一种实施方式中,加入盐酸和/或氢氧化钠作为ph调节剂。
[0027]
其他类似的ph调节剂可用于本发明。合适的ph调节剂的实例是柠檬酸和/或其盐。
[0028]
选择ph以维持活性成分的稳定性。在一个实施例中,ph范围为约1.0至约5.0,例如约2.0至约3.5。
[0029]
在根据本发明的制剂中,如果需要,制剂中可以包括稳定剂或络合剂。合适的稳定剂或络合剂包括但不限于依地酸(edta)或其一种已知盐、依地酸二钠或依地酸二钠二水合物。在一个实施例中,该制剂含有依地酸和/或其盐。
[0030]
其他类似的稳定剂或络合剂可用于本发明。其他稳定剂或络合剂包括但不限于柠檬酸、依地酸二钠和依地酸二钠二水合物。
[0031]
如本文所用,短语“络合剂”是指能够进入络合键的分子。在一种实施方式中,这些化合物具有络合阳离子的作用。在一个实施方案中,稳定剂或络合剂的浓度为约1mg/100ml至约500mg/100ml,例如约10mg/100ml至约200mg/100ml。在一个实施方案中,络合剂是浓度为约1mg/100ml至约500mg/100ml的乙二胺四乙酸二钠二水合物。
[0032]
在根据本发明的制剂中,如果需要,可以通过添加等渗调节剂例如氯化钠来调节制剂的等渗状态。在一个实施例中,该制剂含有氯化钠。
[0033]
在一个实施方案中,氯化钠的量为约0.8%(w/v)至约1.0%(w/v),例如,约0.9%(w/v)。
[0034]
在一个实施方案中,奥达特罗或其盐是奥达特罗盐酸盐,其中奥达特罗盐酸盐的剂量为约3μg至约80μg,优选约3μg至约50μg,更优选约5μg至约50μg。约30μg,且噻托溴铵或
其盐为噻托溴铵一水合物,其中噻托溴铵一水合物的剂量为约3μg至约80μg,优选约3μg至约50μg,更优选约5μg至约30μg。
[0035]
在制剂的一个实施方案中,噻托溴铵和奥达特罗存在于溶液中。
[0036]
当使用吸入器施用制剂时,如果制剂的所有成分都存在于溶液中是有利的。
[0037]
如本文所用的短语“添加剂”是指任何药理学上可接受的和治疗上有用的物质,其不是活性物质,但可以与活性物质一起配制在药理学合适的溶剂中,以提高药物的质量。优选地,这些物质在所需治疗的背景下没有明显的药理作用,或者至少没有不期望的药理作用。
[0038]
合适的添加剂包括但不限于其他稳定剂、络合剂、抗氧化剂、表面活性剂和/或防腐剂,其延长成品药物制剂的保质期、维生素和/或本领域已知的其他添加剂。
[0039]
药物制剂在雾化器中被转化为去往肺部的气雾剂。药液由雾化器通过高压喷射。实施例
[0040]
材料和试剂:噻托溴铵一水合物,来自中国南昌安诺文制药有限公司;盐酸奥达特罗,来自中国上海卡鲁兰科技有限公司;氯化钠,来自默克;柠檬酸,来自默克;氢氧化钠,来自中国上海泰坦试剂有限公司;盐酸,来自中国上海泰坦试剂有限公司;50%苯扎氯铵(简称bac)水溶液可商购,可从光谱制药有限公司购买;乙二胺四乙酸二钠是市售的,可以从默克公司购买。实施例1
[0041]
样品i、样品ii和样品iii吸入溶液的制备如下:将表1中提供的量的活性和非活性成分溶解在90ml纯水中,然后将所得溶液调节至用盐酸或氢氧化钠达到目标ph值。然后加入纯水至最终体积为100ml。表1-100ml可吸入制剂样品i、样品ii和样品iii的成分含量成分样品i样品ii样品iii盐酸奥达特罗18.2μg1.82mg182mg噻托溴铵一水合物20.7μg2.07mg207mg氯化钠0.8g0.9g1.0g盐酸或氢氧化钠至ph1.0至ph3.0至ph5.0纯水加至100ml加至100ml加至100ml实施例2
[0042]
样品iv吸入溶液的制备如下:将活性成分和非活性成分按照表2中提供的量溶解在90ml纯净水中,然后用盐酸或氢氧化钠将所得溶液调节至目标ph值.然后加入纯水至最终体积为100ml。表2 100ml可吸入制剂样品iv成分含量成分样品iv盐酸奥达特罗0.547mg
噻托溴铵一水合物0.620mg氯化钠0.9g盐酸至ph2.9纯水加至100ml实施例3
[0043]
使用雾化吸入器喷雾样品iv。malvern spraytec(stp5311)用于测量所得液滴的粒径。粒度分布在表3中提供。表3雾化吸入器样品iv的粒径分布实施例4表4样品iv的渗透压样品编号渗透压样品iv290mosm实施例5
[0044]
ph对稳定性的影响。
[0045]
稳定性高度依赖于ph。根据表5制备六个样品。将表5中提供的量的奥达特罗盐酸盐(称为oh)和噻托溴铵一水合物(称为tb)溶解在40ml纯水中。然后分别用hcl将样品1-5的ph值调节至ph 2.0、2.5、3.0、3.5、4.0。样品6的ph值未调整(ph值为6.3)。然后对所得混合物进行超声处理直至组分完全溶解。然后加入纯水至最终体积为50毫升。
[0046]
六个样品的配方如表5所示。每个样品在60℃下储存28天。表6-8中提供了每个样品稳定性的实验数据。表5不同ph值下tb和oh筛选的配方设计
成分样品1样品2样品3样品4样品5样品6tb14mg14mg14mg14mg14mg14mgoh12.5mg12.5mg12.5mg12.5mg12.5mg12.5mghcl调整至ph2.0调整至ph2.5调整至ph3.0调整至ph3.5调整至ph4.0未调整ph纯水50ml50ml50ml50ml50ml50ml
[0047]
杂质a,cas号:4746-63-8
[0048]
杂质f,cas号:704-38-1
[0049]
杂质olo-14:表6:不同ph值下的稳定性(条件:0天)nd:未检测到表7:不同ph值的稳定性(条件:60℃,7天,75%rh)
表8:不同ph值的稳定性(条件:60℃,14天,75%rh)表8:不同ph值的稳定性(条件:60℃,14天,75%rh)表9:不同ph值下的稳定性(条件:60℃,28天,75%rh)
[0050]
从表6-9可以看出,含oh和tb的溶液在ph 2.0至3.5下稳定,oh和tb溶液在ph 2.0至3.0下最稳定。实施例6
[0051]
空气动力学粒度分布:将表10中提供的量的50%苯扎氯铵水溶液(称为50%bac)和依地酸二钠二水合物溶解在900ml纯水中。用hcl将ph值调节至ph 3.4。将根据表10中提供的量的oh和tb加入到溶液中并且对所得混合物进行超声处理直至完全溶解。然后加入纯净水至最终体积为1000毫升。表10:样品7的成分含量表10:样品7的成分含量
[0052]
空气动力学粒度分布使用安德森规模撞击器(aci)测定。吸入装置购自勃林格殷格翰制药有限公司,名为stiolto respimat。stiolto respimat吸入器靠近aci入口,直到看不到气溶胶。aci的流速设置为28.3l/分钟,并在环境温度和90%的相对湿度(rh)下操作。
[0053]
将样品7的溶液排放到aci中。根据部分的粒度,将剂量的部分沉积在aci的不同阶
段。每个级分都从台上洗掉并使用hplc进行分析。
[0054]
结果在下表11中提供。表11:通过respimat吸入给药的oh和tb吸入制剂样品7的空气动力学粒度分布
[0055]
fpf值越大,雾化效率越高。
[0056]
以上结果证实本发明的制剂具有良好的雾化效果。实施例7
[0057]
稳定性实验:将表12中提供的量的50%苯扎氯铵水溶液(称为50%bac)和依地酸二钠二水合物溶解在4500ml纯水中。用hcl将ph值调节至ph 2.85。将表12中提供的量的tb和oh加入到溶液中并且对所得混合物进行超声处理直至完全溶解。然后加入纯水至最终体积为5000ml。表12:样品8的成分含量表12:样品8的成分含量
[0058]
样品8在40℃/75%rh下保持0、1、3、6个月。结果在下表13中提供。表13:样品8的稳定性结果(条件:40℃
±
2℃/75%
±
5%rh) 0个月1个月3个月6个月外观澄清溶液澄清溶液澄清溶液澄清溶液
tb中的杂质and0.30.41.13tb中的杂质fndndnd0.06oh-4ndndnd0.03olo-14ndnd0.120.25总杂质小于报告限0.30.521.38tb含量%100.96100.36100.8298.36oh含量%100.74100.52102.9100.76edta含量%99.6898.87100.48103.06bac含量%100.67102.89100.95102.46
[0059]
如表13所示,在ph 2.85下,tb和oh溶液显示出良好的稳定性。tb和oh溶液在40℃
±
2℃/75%
±
5%rh下可稳定约6个月。
[0060]
虽然上面已经描述了本发明的各种实施例,但是应当理解,它们仅通过示例而非限制的方式呈现。例如,本发明不限于图示或描述的物理布置或尺寸。本发明也不限于任何特定的设计或构造材料。因此,本发明的广度和范围不应限于上述示例性实施例中的任一个,而应仅根据所附权利要求及其等效物来定义。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。