1.本公开涉及治疗或预防有需要的受试者的炎症性肺病的方法。
背景技术:
2.与多种病况相关的呼吸疾病在普通人群中极为常见。在许多情况下,它们伴有炎症,这会加重肺部病况。诸如哮喘、过敏性鼻炎、慢性阻塞性肺病(copd)和急性呼吸窘迫综合征(ards)等疾病是工业化国家的常见疾病,并且它们的医疗保健费用极高。这些疾病最近在患病率、发病率和死亡率方面都以惊人的速度增加。尽管如此,它们的根本原因仍然知之甚少。
3.因此,患有炎症性肺病和/或其相关病况或症状的患者仍然存在未满足的治疗需求,需要新的治疗选择。
技术实现要素:
4.本发明人出人意料地确定,通过施用间充质谱系前体细胞或干细胞(mlpsc),可在具有高循环c反应蛋白(crp)基线水平的受试者中实现炎症性肺病的治疗。这些发现提出了一种对炎症性肺病患者进行分层以进行mlpsc治疗的策略。
5.因此,在第一实例中,本公开涉及治疗或预防有需要的人类受试者的炎症性肺病的方法,所述方法包括向受试者施用包含间充质谱系前体或干细胞(mlpsc)的组合物,其中受试者具有高循环c反应蛋白(crp)。在一个实例中,受试者具有至少2mg/ml的初始循环crp水平。在另一实例中,受试者具有至少3mg/ml的初始循环crp水平。在另一实例中,受试者具有至少3mg/ml或至少4mg/ml的初始循环crp水平。在另一实例中,受试者具有至少4mg/ml的初始循环crp水平。
6.在一个实例中,其中炎症性肺病选自由以下组成的组:急性呼吸窘迫综合征(ards)、慢性阻塞性肺病(copd)、特发性肺纤维化(ipf)、肺动脉高压(pah)、哮喘、囊性纤维化、肺炎、间质性肺病或其中的一者或多者。
7.在另一实例中,炎症性肺病是由病毒感染引起的。病毒感染可由例如鼻病毒、流感病毒、呼吸道合胞病毒(rsv)或冠状病毒引起。
8.在一个实例中,炎症性肺病是由冠状病毒感染引起的。冠状病毒可能是严重急性呼吸综合征冠状病毒(sars-cov)、中东呼吸综合征冠状病毒(mers-cov)、covid-19、229e、nl63、oc43或khu1。在一个实例中,冠状病毒是sars-cov、mers-cov或covid-19。
9.在一个实例中,根据本公开治疗的受试者感染了病毒,并且具有至少4mg/ml的循环crp水平。在另一实例中,根据本公开治疗的受试者感染了病毒,并且具有2至6mg/ml的循环crp水平。例如,受试者可能感染了鼻病毒、流感病毒、呼吸道合胞病毒(rsv)或冠状病毒,并且具有至少4mg/ml的循环crp水平。在另一实例中,受试者可能感染了冠状病毒,并且具有至少4mg/ml的循环crp水平。例如,受试者可能感染了严重急性呼吸综合征冠状病毒(sars-cov)、中东呼吸综合征冠状病毒(mers-cov)、covid-19、229e、nl63、oc43或khu1,并
且具有至少4mg/ml的循环crp水平。在另一实例中,受试者可能感染了sars-cov、mers-cov或covid-19,并且具有至少4mg/ml的循环crp水平。
10.在另一实例中,本公开的方法包括以下步骤:i)选择循环crp水平大于或等于4mg/l的患有炎症性肺病的受试者,和ii)向受试者施用包含间充质谱系前体或干细胞(mlpsc)的组合物。
11.在一个实例中,mlpsc已被冷冻保存和解冻。在一个实例中,mlpsc是从中间冷冻保存的mlpsc群体中培养扩增的。在另一实例中,mlpsc被培养扩增至少约5代。在一个实例中,mlpsc每百万个mlpsc表达至少13pg tnfr1。在一个实例中,mlpsc每百万个mlpsc表达约13pg至约44pg tnfr1。在一个实例中,培养扩增的mlpsc被培养扩增至少20次群体倍增。在另一实例中,培养扩增的mlpsc被培养扩增至少30次群体倍增。在一个实例中,mlpsc是间充质干细胞(msc)。在另一实例中,mlpsc是同种异体的。例如,mlpsc可为同种异体msc。
12.在一个实例中,所述组合物是静脉内施用的。
13.在一个实例中,本公开的方法包括施用1
×
107至2
×
108个细胞。例如,可在第0、30、60和90天施用多个剂量的1
×
107至2
×
108个细胞。在一个实例中,本公开的方法包括每剂量施用约1
×
108个细胞。在一个实例中,在基线时施用一个剂量,随后在90天内每月一次地施用3个后续剂量。
14.在一个实例中,受试者在治疗后fev1有所改善。在一个实例中,受试者在接受第一剂量的细胞后的120天内具有相对于基线至少0.02或至少0.05的fev1变化。在一个实例中,在接受第一剂量的细胞后的120天内,受试者的fev1相对于基线的变化至少为0.05。在一个实例中,受试者在治疗后fvc有所改善。在一个实例中,受试者在接受第一剂量的细胞后的120天内具有相对于基线至少0.05或至少0.1的fvc变化。在一个实例中,受试者在治疗后fev1/fvc有所改善。在另一实例中,受试者在接受第一剂量的细胞后的120天内具有相对于基线至少0.01或至少0.015的fev1/fvc变化。在另一实例中,受试者在接受第一剂量的细胞后的150天内具有相对于基线至少0.01或至少0.015的fev1/fvc变化。在一个实例中,受试者在治疗后显示出6分钟步行测试的改善。在一个实例中,受试者在接受第一剂量的细胞后的60天内显示出至少40米或至少50米的6分钟步行测试的改善。在一个实例中,受试者在接受第一剂量的细胞后的120天内显示出至少40米或至少50米的6分钟步行测试的改善。在一个实例中,受试者在接受第一剂量的细胞后的120天内显示出fev1、fvc和6分钟步行测试的改善。
15.在一个实例中,受试者在接受第一剂量的细胞后的120天内表现出fev1和fvc的改善。在一个实例中,受试者在接受第一剂量的细胞后的120天内显示出fev1、fvc和6分钟步行测试的改善。在一个实例中,受试者在接受第一剂量的细胞后的120天内显示出fvc的改善。在另一实例中,所述组合物还包含plasma-lyte a、二甲亚砜(dmso)、人血清白蛋白(hsa)。在一个实例中,所述组合物还包含plasma-lyte a(70%)、dmso(10%)、hsa(25%)溶液,所述hsa溶液包含5%hsa和15%缓冲液。
16.在一个实例中,所述组合物包含大于6.68
×
106个活细胞/ml。
附图说明
17.图1:fev1相对于bl(l)(crp≥4mg/ml)的变化。
18.图2:fev1/fvc相对于bl(crp≥4mg/ml)的变化。
19.图3:fvc相对于bl高(crp≥4mg/ml)的变化。
20.图4:总6mw距离(米)相对于bl(crp≥4mg/ml)的变化。
具体实施方式
21.在整个本说明书中,除非另有明确说明或上下文另有要求,否则对单个步骤、物质组合物、步骤组或物质组合物组的引用应理解为包括那些步骤、物质组合物、步骤组或物质组合物组中的一个和复数个(即一个或多个)。
22.本领域技术人员将理解,本文描述的公开内容容易受到除具体描述的那些之外的变化和修改。应当理解,本公开包括所有这样的变化和修改。本公开还包括在本说明书中单独或共同提及或指示的所有步骤、特征、组合物和化合物,以及所述步骤或特征的任何和所有组合或任何两者或更多者。
23.本公开的范围不受本文描述的具体实施方案的限制,所述具体实施方案仅用于举例说明的目的。如本文所述,功能等效的产品、组合物和方法显然在本公开的范围内。
24.除非另有明确说明,否则本文公开的任何实例均应视为经适当变更后适用于任何其它实例。
25.除非另有明确定义,否则本文使用的所有技术和科学术语均应视为具有与本领域(例如细胞培养、分子遗传学、干细胞分化、免疫学、免疫组织化学、蛋白质化学和生物化学)普通技术人员通常所理解相同的含义。
26.除非另有说明,否则本公开中使用的外科技术是本领域技术人员熟知的标准程序。
27.获得和富集间充质谱系干细胞或前体细胞群体的方法是本领域已知的。例如,间充质谱系干细胞或前体细胞的富集群体可通过使用流式细胞术和基于使用在间充质谱系干细胞或前体细胞上表达的细胞表面标记物的细胞分选程序来获得。
28.本文引用或参考的所有文件,以及本文引用的文件中引用或参考的所有文件,连同本文或以引用方式并入本文的任何文件中提及的任何产品的任何制造商说明书、描述、产品规格和产品表,均特此以引用方式全部并入本文。
29.所选定义
30.术语“和/或”,例如“x和/或y”应被理解为意指“x和y”或“x或y”,并应被视为对两种含义或任何一种含义提供明确支持。
31.如本文所用,除非有相反说明,否则术语“约”是指指定值的 /-10%,更优选 /-5%。
32.在整个本说明书中,词语“包含(comprise)”或例如“包含(comprises)”或“包含(comprising)”的变化形式将被理解为暗示包括所陈述的要素、整数或步骤,或要素、整数或步骤组,但不排除任何其它要素、整数或步骤,或要素、整数或步骤组。
33.除非上下文另有说明,否则如本文所用,单数形式“一(a/an)”和“所述”包括单数和复数个参考物。
[0034]“分离的”或“纯化的”意指已与其自然环境的至少一些组分分离的细胞。此术语包括细胞与其自然环境的总体物理分离(例如从供体中去除)。术语“分离的”包括通过例如解
离改变细胞与其所直接的相邻细胞的关系。术语“分离的”不指组织切片中的细胞。当用于指细胞群时,术语“分离的”包括由本公开的分离的细胞的增殖产生的细胞群。
[0035]
术语“传代(passage)”、“传代(passaging)”或“传代培养”在本公开的上下文中用于指已知的细胞培养技术,所述技术用于使细胞在培养条件下在长时间段内保持存活和生长,以便细胞数量可不断增加。一个细胞系的传代培养程度通常用“传代数”来表示,传代数一般用于指代细胞被传代培养的次数。在一个实例中,一次传代包括去除非贴壁细胞并留下贴壁的间充质谱系前体或干细胞。接着可将此类间充质谱系前体或干细胞从底物或烧瓶中解离(例如通过使用蛋白酶,如胰蛋白酶或胶原酶),可添加培养基,可进行任选的洗涤(例如通过离心),且接着间充质谱系前体或干细胞可重新铺板或重新接种至一个或多个总表面积更大的培养容器中。间充质谱系前体或干细胞接着可继续在培养中扩增。在另一实例中,去除非贴壁细胞的方法包括非酶处理步骤(例如用edta)。在一个实例中,间充质谱系前体或干细胞在汇合(例如约75%至约95%汇合)处或附近传代。在一个实例中,以约10%、约15%或约20%细胞/ml培养基的浓度接种间充质谱系前体或干细胞。
[0036]
如在本公开的上下文中使用的术语“培养基(medium)”或“培养基(media)”包括培养中细胞周围环境的组分。设想培养基有助于和/或提供适合于允许细胞生长的条件。培养基可以是固体、液体、气体或各相和材料的混合物。培养基可包括液体生长培养基以及不维持细胞生长的液体培养基。示例性气体培养基包括在培养皿或其它固体或半固体支持物上生长的细胞所暴露于的气相。
[0037]
如本文所用,术语“治疗(treating)”、“治疗(treat)”或“治疗(treatment)”包括施用间充质谱系干细胞或前体细胞和/或其后代和/或源自其的可溶性因子的群体,从而减少或消除炎症性肺病的至少一种症状。在一个实例中,治疗包括施用培养扩增的间充质谱系干细胞或前体细胞群体。在一个实例中,治疗反应是相对于基线确定的。
[0038]
在一个实例中,治疗是基于受试者肺量测定测量确定的。在一个实例中,肺量测定测量是根据美国呼吸护理协会(aarc)肺量测定临床实践指南(american association for respiratory care:aarc clinical practice guideline:spirometry,1996年更新,respir care.,41:629-638)确定的。
[0039]
在一个实例中,治疗改善了受试者的fev1。在一个实例中,观察到fev1的改善是相对于基线变化至少0.02或至少0.05。在另一实例中,观察到fev1的改善是相对于基线变化0.02至0.06。在另一实例中,观察到fev1的改善是相对于基线变化0.02至0.05。在一个实例中,在接受第一剂量的细胞后的120天、150天或180天内观察到上述fev1的改善。在一个实例中,在三个月内接受四个剂量的细胞后观察到上述fev1的改善。在一个实例中,在接受4亿个细胞的总剂量后观察到上述fev1的改善。
[0040]
在一个实例中,治疗改善了受试者的fvc。在一个实例中,观察到fvc的改善是相对于基线变化至少0.05或至少0.1。在另一实例中,观察到fvc的改善是相对于基线变化0.05至0.15。在另一实例中,观察到fvc的改善是相对于基线变化0.05至0.1。在一个实例中,在接受第一剂量的细胞后的120天或150天内观察到上述fvc的改善。在一个实例中,在三个月内接受四个剂量的细胞后观察到上述fvc的改善。在一个实例中,在接受4亿个细胞的总剂量后观察到上述fvc的改善。
[0041]
在另一实例中,治疗改善了受试者的fev1/fvc。在一个实例中,观察到fev1/fvc的
改善是相对于基线变化至少0.007或至少0.013。在另一实例中,观察到fev1/fvc的改善是相对于基线变化0.007至0.014。在另一实例中,观察到fev1/fvc的改善是相对于基线变化0.007至0.014。在一个实例中,在接受第一剂量的细胞后的120天、150天或180天内观察到上述fev1/fvc的改善。在一个实例中,在三个月内接受四个剂量的细胞后观察到上述fev1/fvc的改善。在一个实例中,在接受4亿个细胞的总剂量后观察到上述fev1/fvc的改善。
[0042]
在另一实例中,治疗改善了受试者的6分钟步行测试。在一个实例中,6分钟步行测试的改善是至少40米或至少50米。在一个实例中,6分钟步行测试的改善是40至60米。在一个实例中,6分钟步行测试的改善40至50米。在一个实例中,在接受第一剂量的细胞后的60天或90天内观察到上述6分钟步行测试的改善。在一个实例中,在两个月内接受两个剂量的细胞后观察到上述6分钟步行测试的改善。在一个实例中,在接受第一剂量的细胞后的120天或150天内观察到上述6分钟步行测试的改善。在一个实例中,在三个月内接受四个剂量的细胞后观察到上述6分钟步行测试的改善。在一个实例中,在接受4亿个细胞的总剂量后观察到上述6分钟步行测试的改善。
[0043]
在一个实例中,6分钟步行测试结果是根据ats statement:guidelines for the six-minute walk test(2002)am j respir crit care med.,166:111-7确定的。
[0044]
如本文所用,术语“预防(prevent)”或“预防(preventing)”包括施用间充质谱系干细胞或前体细胞和/或其后代和/或源自其的可溶性因子的群体,从而停止或抑制本文公开的炎症性肺病的至少一种症状的发展。
[0045]
在本公开的上下文中使用的术语“炎症性肺病”是指由呼吸道和/或肺中正在进行的炎症过程引起的疾病。例如,copd是呼吸道和肺组织都受到影响的炎症性肺病。这可以表现为慢性阻塞性支气管炎和肺气肿的组合,其中前者是支气管慢性炎症的结果,且后者是由于肺泡破裂造成的。炎症性肺病的其它实例包括急性呼吸窘迫综合征(ards)、特发性肺纤维化(ipf)、肺动脉高压(pah)、哮喘、囊性纤维化、肺炎和间质性肺病。在一个实例中,炎症性肺病由病毒感染引起。例如,炎症性肺病可由鼻病毒、流感病毒、呼吸道合胞病毒(rsv)或冠状病毒引起。在一个实例中,炎症性肺病可由冠状病毒引起。例如,冠状病毒可为冠状病毒(sars-cov)、中东呼吸综合征冠状病毒(mers-cov)或covid-19。在一个实例中,炎症性肺病的特征在于上述适应症的组合。例如,炎症性肺病可包括copd和ards。
[0046]“c反应蛋白”或“crp”是一种炎症介质,其水平在急性炎症复发的情况下会升高,并且一旦炎症消退就会迅速恢复正常。在一个实例中,根据本公开治疗的受试者具有高循环crp水平。术语“高循环crp水平”在本公开的上下文中用于指具有炎症性肺病症状和>1mg/ml的循环crp水平的受试者。在一个实例中,具有高循环crp水平的受试者可被诊断为患有炎症性肺病并且具有>1mg/ml的循环crp水平。
[0047]
在一个实例中,根据本公开治疗的受试者具有≥1.5mg/ml的初始循环crp水平。在另一实例中,根据本公开治疗的受试者具有≥2mg/ml的初始循环crp水平。在一个实例中,根据本公开治疗的受试者具有≥3mg/ml的初始循环crp水平。在一个实例中,根据本公开治疗的受试者具有≥3.5mg/ml的初始循环crp水平。在另一实例中,受试者具有≥4mg/ml的初始循环crp水平。在另一实例中,受试者具有≥5mg/ml、≥6mg/ml、≥7mg/ml、≥8mg/ml、≥9mg/ml、≥10mg/ml的初始循环crp水平。在一个实例中,受试者具有2mg/ml至10mg/ml的初始循环crp水平。在另一实例中,受试者具有3mg/ml至10mg/ml的初始循环crp水平。在另一
实例中,受试者具有2mg/ml至15mg/ml的初始循环crp水平。在另一实例中,受试者具有2mg/ml至20mg/ml的初始循环crp水平。
[0048]
在一个实例中,本公开的方法抑制受试者的疾病进展或疾病并发症。“抑制”受试者的疾病进展或疾病并发症意指预防或减少受试者的疾病进展和/或疾病并发症。
[0049]
如本文所用,术语“受试者”是指人类受试者。例如,受试者可以是成年人。在另一实例中,受试者可以是儿童。在另一实例中,受试者可以是青少年。诸如“受试者”、“患者”或“个体”的术语是在本公开的上下文中可互换使用的术语。
[0050]
根据本公开治疗的受试者可具有指示炎症性肺病的症状和≥4mg/ml的初始循环crp水平。指示炎症性肺病的示例性症状包括疲劳、呼吸困难、呼吸短促、不能运动或运动能力下降、带或不带血或粘液的咳嗽、吸气或呼气时疼痛、喘息、胸闷、无法解释的体重减轻和肌肉骨骼疼痛。在一个实例中,炎症性肺病是基于肺功能测试来诊断的。例如,炎症性肺病可根据用力肺活量(fvc)、一秒用力呼气量(fev1)和用力呼气流量(fef)中的一者或多者来诊断。在一个实例中,根据fev1/fvc比诊断炎症性肺病。
[0051]
在另一实例中,受试者是18-75岁。在另一实例中,受试者患有copd。在另一实例中,受试者患有ards。在另一实例中,受试者患有ipf。在另一实例中,受试者患有pah。在另一实例中,受试者患有哮喘。在另一实例中,受试者患有囊性纤维化。在另一实例中,受试者患有肺炎。在另一实例中,受试者患有间质性肺病。在另一实例中,受试者患有其组合,例如copd和ards。
[0052]
在另一实例中,受试者患有继发于病毒感染的ards。在一个实例中,受试者ards继发于鼻病毒、流感病毒、呼吸道合胞病毒(rsv)或冠状病毒感染。在一个实例中,受试者ards继发于冠状病毒感染。例如,受试者ards可继发于sars-cov、mers-cov或covid-19感染。
[0053]
在另一实例中,本公开的方法预防或治疗患有轻度copd的受试者。在另一实例中,本公开的方法预防或治疗患有中度copd的受试者。在另一实例中,本公开的方法预防或治疗患有重度copd的受试者。在另一实例中,本公开的方法预防或治疗患有极重度copd的受试者。在另一实例中,本公开的方法预防或治疗患有中度或重度copd的受试者。在另一实例中,本公开的方法预防或治疗患有中度、重度或极重度copd的受试者。在一个实例中,copd的严重程度是根据阻塞性肺病全球倡议(gold)的copd标准确定的(参见例如rabe等,(2007)respir crit care med.,176:532-555)。在此实例中,患有copd的受试者的fev1/fvc比可小于0.70。在一个实例中,在fev1/fvc比<0.70的受试者中,以下者用于诊断copd的严重程度:
[0054]-gold 1-轻度:fev1≥80%预测值;
[0055]-gold 2-中度:50%≤fev1<80%预测值;
[0056]-gold 3-重度:30%≤fev1<50%预测值;
[0057]-gold 4-极重度:fev1<30%预测值。
[0058]
如本文所用,术语“遗传上未修饰的”是指未通过用核酸转染修饰的细胞。为避免疑义,在本公开的上下文中,用编码ang1的核酸转染的间充质谱系前体或干细胞将被认为是遗传修饰的。
[0059]
术语“总剂量”在本公开的上下文中用于指根据本公开治疗的受试者接受的细胞总数。在一个实例中,总剂量由一次细胞施用组成。在另一实例中,总剂量由两次细胞施用
组成。在另一实例中,总剂量由三次细胞施用组成。在另一实例中,总剂量由四次或更多次细胞施用组成。例如,总剂量可由两到四次细胞施用组成。
[0060]
间充质谱系前体细胞
[0061]
如本文所用,术语“间充质谱系前体或干细胞(mlpsc)”是指具有自我更新能力同时保持多能性和分化成多种细胞类型的能力的未分化多能细胞,所述细胞类型为间充质来源,例如成骨细胞、软骨细胞、脂肪细胞、基质细胞、成纤维细胞和肌腱,或非中胚层来源,例如肝细胞、神经细胞和上皮细胞。为免生疑问,“间充质谱系前体细胞”是指可分化成间充质细胞的细胞,例如骨、软骨、肌肉和脂肪细胞以及纤维结缔组织。
[0062]
术语“间充质谱系前体或干细胞”包括亲本细胞和其未分化的后代。所述术语还包括间充质前体细胞、多能基质细胞、间充质干细胞(msc)、血管周围间充质前体细胞和其未分化的后代。
[0063]
间充质谱系前体或干细胞可为自体的、同种异体的、异种的、同基因的或等基因的。自体细胞是从它们将被重新植入的同一个体中分离出来的。同种异体细胞是从同一物种的供体中分离出来的。异种细胞是从另一个物种的供体中分离出来的。同基因或等基因细胞是从基因相同的生物体,例如双胞胎、克隆或高度近交的研究动物模型中分离出来的。
[0064]
在一个实例中,间充质谱系前体或干细胞是同种异体的。在一个实例中,同种异体间充质谱系前体或干细胞被培养扩增并冷冻保存。
[0065]
间充质谱系前体或干细胞主要存在于骨髓中,但也显示存在于多种宿主组织中,包括例如脐带血和脐带、成人外周血、脂肪组织、骨小梁和牙髓。它们也存在于皮肤、脾脏、胰腺、脑、肾、肝、心脏、视网膜、脑、毛囊、肠、肺、淋巴结、胸腺、韧带、肌腱、骨骼肌、真皮和骨膜中;并且能够分化成种系,例如中胚层和/或内胚层和/或外胚层。因此,间充质谱系前体或干细胞能够分化成大量细胞类型,包括但不限于脂肪、骨、软骨、弹性、肌肉和纤维结缔组织。这些细胞进入的特定谱系定型和分化途径取决于机械影响和/或内源性生物活性因子的各种影响,例如生长因子、细胞因子和/或宿主组织建立的局部微环境条件。
[0066]
术语“富集(enriched)”、“富集(enrichment)”或其变化形式在本文中用于描述与未处理的细胞群(例如在其原生环境中的细胞)相比时,一种特定细胞类型的比例或多种特定细胞类型的比例增加的细胞群。在一个实例中,富集间充质谱系前体或干细胞的群体包含至少约0.1%或0.5%或1%或2%或5%或10%或15%或20%或25%或30%或50%或75%的间充质谱系前体或干细胞。在这方面,将采用术语“富集间充质谱系前体或干细胞的细胞群”来明确支持术语“包含x%间充质谱系前体或干细胞的细胞群”,其中x%是如本文所述的百分比。在一些实例中,间充质谱系前体或干细胞可形成克隆形成集落,例如cfu-f(成纤维细胞)或其子集(例如50%或60%或70%或70%或90%或95%)可具有此活性。
[0067]
在本公开的一个实例中,间充质谱系前体或干细胞是间充质干细胞(msc)。msc可为均质组合物或可为富集msc的混合细胞群。可通过培养贴壁的骨髓或骨膜细胞获得均质的msc组合物,且可通过用独特的单克隆抗体鉴定的特定细胞表面标记物来鉴定msc。例如,在美国专利第5,486,359号中描述了一种用于获得富集msc的细胞群的方法。msc的替代来源包括但不限于血液、皮肤、脐带血、肌肉、脂肪、骨骼和软骨膜。在一个实例中,msc是同种异体的。在一个实例中,msc被冷冻保存。在一个实例中,msc被培养扩增并冷冻保存。
[0068]
在另一实例中,间充质谱系前体或干细胞是cd29 、cd54 、cd73 、cd90 、cd102 、
cd105 、cd106 、cd166 、mhc1 msc。
[0069]
分离或富集的间充质谱系前体或干细胞可通过培养在体外进行扩增。分离或富集的间充质谱系前体或干细胞可冷冻保存、解冻且随后通过培养在体外扩增。
[0070]
在一个实例中,分离或富集的间充质谱系前体或干细胞以50,000个活细胞/cm2接种在培养基(无血清或补充血清),例如补充有5%胎牛血清(fbs)和谷氨酰胺的α最低必需培养基(αmem)中,并使其在37℃、20%o2下粘附在培养容器上过夜。随后根据需要更换和/或改变培养基,并将细胞在37℃、5%o2下再培养68至72小时。
[0071]
如本领域技术人员将理解的,培养的间充质谱系前体或干细胞在表型上不同于体内细胞。例如,在一个实施方案中,它们表达一种或多种以下标记物:cd44、ng2、dc146和cd140b。培养的间充质谱系前体或干细胞在生物学上也不同于体内细胞,与体内的大部分非循环(静止)细胞相比具有更高的增殖率。
[0072]
在一个实例中,细胞群从包含可选择形式的stro-1 细胞的细胞制备物中富集。在这点上,术语“可选择形式”将被理解为意指细胞表达允许选择stro-1 细胞的标记物(例如细胞表面标记物)。标记物可以是但不一定是stro-1。例如,如本文所述和/或例示的,表达stro-2和/或stro-3(tnap)和/或stro-4和/或vcam-1和/或cd 146和/或3g5的细胞(例如间充质前体细胞)也表达stro-1(并且可以是stro-1明亮的)。因此,细胞为stro-1 的指示并不意味着细胞仅通过stro-1表达来选择。在一个实例中,至少基于stro-3表达来选择细胞,例如,它们是stro-3 (tnap )。
[0073]
提及细胞或其群体的选择不一定需要从特定组织来源中进行选择。如本文所述,stro-1 细胞可选自或分离自或富集自多种来源。也就是说,在一些实例中,这些术语为从包含stro-1 细胞(例如间充质前体细胞)的任何组织或血管化组织或包含周细胞(例如stro-1 周细胞)的组织或本文所述的任何一种或多种组织中进行选择提供支持。
[0074]
在一个实例中,本公开中使用的细胞表达一种或多种单独地或共同地选自由以下组成的组的标记物:tnap 、vcam-1 、thy-1 、stro-2 、stro-4 (hsp-90β)、cd45 、cd146 、3g5 或其任何组合。
[0075]“单独地”意指本公开分别包括所述标记物或标记物组,并且尽管单独的标记物或标记物组可能未在本文中单独列出,但所附权利要求书可彼此分开且可分割地定义此类标记物或标记物组。
[0076]“共同地”意指本公开包括所述标记物或标记物组的任何数量或组合,并且尽管本文可能未具体列出此类标记物或标记物组的数量或组合,但所附权利要求可与标记物或标记物组的任何其它组合分开且可分割地定义此类组合或子组合。
[0077]
如本文所用,术语“tnap”旨在包括组织非特异性碱性磷酸酶的所有同种型。例如,所述术语包括肝同种型(lap)、骨同种型(bap)和肾同种型(kap)。在一个实例中,tnap是bap。在一个实例中,如本文所用的tnap是指可结合stro-3抗体的分子,所述抗体由根据布达佩斯条约的规定于2005年12月19日以保藏登记号pta-7282保藏于atcc的杂交瘤细胞系产生。
[0078]
此外,在一个实例中,stro-1 细胞能够产生克隆形成cfu-f。
[0079]
在一个实例中,显著比例的stro-1 细胞能够分化成至少两种不同的种系。stro-1 细胞可定型的谱系的非限制性实例包括骨前体细胞;对胆管上皮细胞和肝细胞具有多能
性的肝细胞祖细胞;可产生进展为少突胶质细胞和星形胶质细胞的胶质细胞前体的神经受限细胞;进展为神经元的神经元前体;心肌和心肌细胞的前体,葡萄糖反应性胰岛素分泌胰腺β细胞系。其它谱系包括但不限于成牙本质细胞、产生牙本质的细胞和软骨细胞,以及以下的前体细胞:视网膜色素上皮细胞、成纤维细胞、皮肤细胞(例如角质形成细胞)、树突细胞、毛囊细胞、肾导管上皮细胞、平滑肌和骨骼肌细胞、睾丸祖细胞、血管内皮细胞、肌腱、韧带、软骨、脂肪细胞、成纤维细胞、骨髓基质、心肌、平滑肌、骨骼肌、周细胞、血管细胞、上皮细胞、胶质细胞、神经元、星形胶质细胞和少突胶质细胞。
[0080]
在一个实例中,间充质谱系前体或干细胞从单个供体或多个供体获得,其中供体样品或间充质谱系前体或干细胞随后被汇集,且接着培养扩增。
[0081]
本公开所包括的间充质谱系前体或干细胞也可在施用于受试者之前冷冻保存。在一个实例中,间充质谱系前体或干细胞在施用于受试者之前进行培养扩增和冷冻保存。
[0082]
在一个实例中,本公开包括间充质谱系前体或干细胞以及其后代、源自其的可溶性因子和/或从中分离的细胞外囊泡。在另一实例中,本公开包括间充质谱系前体或干细胞以及从中分离的细胞外囊泡。例如,有可能在适合将细胞外囊泡分泌至细胞培养基中的条件下培养扩增本公开的间充质前体谱系或干细胞一段时间。随后可从培养基中获得分泌的细胞外囊泡用于疗法。
[0083]
如本文所用,术语“细胞外囊泡”是指脂质颗粒,所述脂质颗粒从细胞中自然释放并且尺寸在约30nm到大至10微米范围内,尽管典型地它们的尺寸小于200nm。它们可含有来自释放细胞(例如间充质干细胞;stro-1
细胞)的蛋白质、核酸、脂质、代谢物或细胞器。
[0084]
如本文所用,术语“外泌体”是指一种细胞外囊泡,其尺寸通常在约30nm至约150nm范围内,并起源于哺乳动物细胞的内体区室,它们所述该区室运输到细胞膜并释放。它们可含有核酸(例如rna;微rna)、蛋白质、脂质和代谢物,并通过从一个细胞分泌并被其它细胞吸收以递送其货物而在细胞间通信中发挥作用。
[0085]
细胞的培养扩增
[0086]
在一个实例中,间充质谱系前体或干细胞被培养扩增。“培养扩增的”间充质谱系前体或干细胞培养基与新鲜分离的细胞的区别在于它们已在细胞培养基中培养并传代(即传代培养)。在一个实例中,培养扩增的间充质谱系前体或干细胞被培养扩增约4-10代。在一个实例中,间充质谱系前体或干细胞被培养扩增至少5、至少6、至少7、至少8、至少9、至少10代。例如,间充质谱系前体或干细胞可培养扩增至少5代。在一个实例中,间充质谱系前体或干细胞可培养扩增至少5-10代。在一个实例中,间充质谱系前体或干细胞可培养扩增至少5-8代。在一个实例中,间充质谱系前体或干细胞可培养扩增至少5-7代。在一个实例中,间充质谱系前体或干细胞可培养扩增超过10代。在另一实例中,间充质谱系前体或干细胞可培养扩增超过7代。在这些实例中,干细胞可在冷冻保存之前进行培养扩增,以提供中间冷冻保存的mlpsc群体。在一个实例中,本公开的组合物由中间冷冻保存的mlpsc群体制备。例如,中间冷冻保存的mlpsc群体可在施用之前进一步培养扩增,如下文进一步论述的。因此,在一个实例中,间充质谱系前体或干细胞被培养扩增并冷冻保存。在这些实例的一个实施方案中,间充质谱系前体或干细胞可从单个供体或多个供体获得,其中供体样品或间充质谱系前体或干细胞随后被汇集,且接着进行培养扩增。在一个实例中,培养扩增方法包括:
[0087]-i.通过传代扩增来扩增活细胞的数量以提供至少约10亿个活细胞的制备物,其中传代扩增包括建立分离的间充质谱系前体或干细胞的原代培养物,且接着从先前培养物中连续建立分离的间充质谱系前体或干细胞的第一非原代(p1)培养物;
[0088]-ii.通过传代扩增将分离的间充质谱系前体或干细胞的p1培养物扩增至间充质谱系前体或干细胞的第二非原代(p2)培养物;和
[0089]-iii.制备和冷冻保存从间充质谱系前体或干细胞的p2培养物中获得的过程中的中间间充质谱系前体或干细胞制备物;以及
[0090]-iv.将冷冻保存的过程中的中间间充质谱系前体或干细胞制备物解冻并通过传代扩增来扩增过程中的中间间充质谱系前体或干细胞制备物。
[0091]
在一个实例中,扩增的间充质谱系前体或干细胞制备物具有抗原谱和活性谱,其包括:
[0092]-i.少于约0.75%cd45 细胞;
[0093]-ii.至少约95%cd105 细胞;
[0094]-iii.至少约95%cd166 细胞。
[0095]
在一个实例中,相对于对照,扩增的间充质谱系前体或干细胞制备物能够抑制cd3/cd28活化的pbmc的il2ra表达至少约30%。
[0096]
在一个实例中,培养扩增的间充质谱系前体或干细胞被培养扩增约4-10代,其中间充质谱系前体或干细胞在至少2或3代后被冷冻保存,随后进行进一步培养扩增。在一个实例中,间充质谱系前体或干细胞被培养扩增至少1、至少2、至少3、至少4、至少5代,冷冻保存,且接着进一步培养扩增至少1、至少2、至少3、至少4、至少5代,随后进行施用或进一步冷冻保存。
[0097]
在一个实例中,本公开的组合物中的大多数间充质谱系前体或干细胞具有大约相同的代数(即,它们在彼此的约1或约2或约3或约4次细胞倍增内)。在一个实例中,本公开组合物中细胞倍增的平均数量为约20至约25倍。在一个实例中,本公开组合物中的细胞倍增的平均数量为由原代培养物产生的约9至约13(例如约11或约11.2)倍,加上每代约1、约2、约3或约4倍(例如每代约2.5倍)。当分别通过约1、约2、约3、约4、约5、约6、约7、约8、约9和约10次传代产生时,本公开组合物中的示例性平均细胞倍增为约13.5、约16、约18.5、约21、约23.5、约26、约28.5、约31、约33.5和约36中的任一者。
[0098]
可使用本领域已知的任何设备和细胞处理方法进行间充质谱系前体或干细胞分离和离体扩增的过程。本公开的各种培养扩增实施方案采用需要对细胞进行操作的步骤,例如接种、补料、解离贴壁培养物或洗涤的步骤。任何操作细胞的步骤都有可能损伤细胞。尽管间充质谱系前体或干细胞在制备过程中通常可承受一定量的损伤,但细胞优选通过充分执行给定步骤的处理程序和/或设备进行操作,同时最小化对细胞的损伤。
[0099]
在一个实例中,间充质谱系前体或干细胞在包括以下各者的装置中洗涤:细胞源袋、洗涤溶液袋、再循环洗涤袋、具有入口和出口端口的旋转膜过滤器、滤液袋、混合区、用于经洗涤细胞的最终产品袋和合适的管,例如,如us 6,251,295中所述,所述专利以引用方式并入本文。
[0100]
在一个实例中,根据本公开的间充质谱系前体或干细胞组合物在cd105阳性和cd166阳性以及cd45阴性方面是95%均质的。在一个实例中,这种均质性通过离体扩增,即
通过多次群体倍增而持续存在。在一个实例中,组合物包含至少一个治疗剂量的间充质谱系前体或干细胞,并且间充质谱系前体或干细胞包含小于约1.25%的cd45 细胞、至少约95%的cd105 细胞和至少约95%的cd166 细胞。在一个实例中,这种均质性在低温储存和解冻后持续存在,其中细胞通常也具有约70%或更高的活力。
[0101]
在一个实例中,本公开的组合物包含间充质谱系前体或干细胞,其表达大量的tnfr1,例如每百万个间充质谱系前体或干细胞大于13pg tnfr1。在一个实例中,这种表型在整个离体扩增和低温储存过程中是稳定的。在一个实例中,每百万个间充质谱系前体或干细胞在约13至约179pg(例如约13pg至约44pg)范围内的tnfr1水平的表达与期望的治疗潜力相关,所述期望的治疗潜力也通过离体扩增和冷冻保存而持续存在。
[0102]
在一个实例中,培养扩增的间充质谱系前体或干细胞以至少110pg/ml的量表达肿瘤坏死因子受体1(tnfr1)。例如,间充质谱系前体或干细胞可以至少150pg/ml、或至少200pg/ml、或至少250pg/ml、或至少300pg/ml、或至少320pg/ml、或至少330pg/ml、或至少340pg/ml、或至少350pg/ml的量表达tnfr1。
[0103]
在一个实例中,间充质谱系前体或干细胞以至少13pg/106个细胞的量表达tnfr1。例如,间充质谱系前体或干细胞以至少15pg/106个细胞、或至少20pg/106个细胞、或至少25pg/106个细胞、或至少30pg/106个细胞、或至少35pg/106个细胞、或至少40pg/106个细胞、或至少45pg/106个细胞、或至少50pg/106个细胞的量表达tnfr1。
[0104]
在另一实例中,本文公开的间充质谱系前体或干细胞抑制t细胞上的il-2rα表达。在一个实例中,间充质谱系前体或干细胞可抑制il-2rα表达至少约30%,或者至少约35%,或者至少约40%,或者至少约45%,或者至少约50%,或者至少约55%,或者至少约60%。
[0105]
在一个实例中,本公开的组合物包含至少一个治疗剂量的间充质谱系前体或干细胞,其例如可包含至少约1亿个细胞或约1.25亿个细胞。
[0106]
细胞的修饰
[0107]
本公开的间充质谱系前体或干细胞可以在施用时,细胞的裂解被抑制的方式改变。抗原的改变可诱导免疫无反应性或耐受性,从而防止诱导免疫反应的效应阶段(例如细胞毒性t细胞生成、抗体产生等),所述阶段最终导致在正常免疫反应中排斥外来细胞。可被改变以实现此目标的抗原包括例如mhc i类抗原、mhc ii类抗原、lfa-3和icam-1。
[0108]
间充质谱系前体或干细胞也可被遗传修饰以表达对横纹骨骼肌细胞的分化和/或维持重要的蛋白质。示例性蛋白质包括生长因子(tgf-β、胰岛素样生长因子1(igf-1)、fgf)、生肌因子(例如myod、生肌素、生肌因子5(myf5)、生肌调节因子(mrf))、转录因子(例如gata-4)、细胞因子(例如心肌营养素(cardiotropin)-1)、神经调节素家族成员(例如神经调节素1、2和3)和同源盒基因(例如csx、tinman和nkx家族)。
[0109]
本公开的组合物
[0110]
在本公开的一个实例中,间充质谱系前体或干细胞和/或其后代和/或源自其的可溶性因子以组合物的形式施用。在一个实例中,此类组合物包含药学上可接受的载体和/或赋形剂。因此,在一个实例中,本公开的组合物可包含培养扩增的间充质谱系前体或干细胞。
[0111]
术语“载体”和“赋形剂”是指在本领域中惯常用于促进活性化合物的储存、施用和/或生物活性的物质组合物(参见例如remington
′
s pharmaceutical sciences,第16版,
mac publishing company(1980)。载体还可减少活性化合物的任何不良副作用。合适的载体例如是稳定的,例如不能与载体中的其它成分反应。在一个实例中,载体在用于治疗的剂量和浓度下不会在受体中产生显著的局部或全身副作用。
[0112]
适用于本公开的载体包括常规使用的那些,例如水、盐水、右旋糖水溶液、乳糖、林格氏溶液(ringer
′
s solution)、缓冲溶液、透明质酸和二醇是示例性液体载体,特别是(当等渗时)用于溶液。合适的药物载体和赋形剂包括淀粉、纤维素、葡萄糖、乳糖、蔗糖、明胶、麦芽、大米、面粉、白垩、硅胶、硬脂酸镁、硬脂酸钠、单硬脂酸甘油酯、氯化钠、甘油、丙二醇、水、乙醇等。
[0113]
在另一实例中,载体是培养基组合物,例如细胞在其中生长或悬浮。例如,此类培养基组合物不会在其所施用的受试者中引起任何不利影响。
[0114]
示例性载体和赋形剂不会不利地影响细胞的活力和/或细胞减轻、预防或延迟代谢综合征和/或肥胖症的能力。
[0115]
在一个实例中,载体或赋形剂提供缓冲活性以将细胞和/或可溶性因子维持在合适的ph下,从而发挥生物活性,例如,载体或赋形剂是磷酸盐缓冲盐水(pbs)。pbs代表有吸引力的载体或赋形剂,因为它与细胞和因子的相互作用最小并且允许细胞和因子的快速释放,在这种情况下,本公开的组合物可生产为液体,用于直接应用至血流或应用至组织或组织周围或附近的区域中,例如通过注射。
[0116]
间充质谱系前体或干细胞和/或其后代和/或源自其的可溶性因子也可掺入或包埋在与受体相容且降解成对受体无害的产物的支架内。这些支架为要移植到受体受试者中的细胞提供支持和保护。天然和/或合成的可生物降解的支架是此类支架的实例。
[0117]
在本公开的实践中可成功地使用多种不同的支架。示例性支架包括但不限于生物可降解支架。天然可生物降解支架包括胶原蛋白、纤连蛋白和层粘连蛋白支架。适用于细胞移植支架的合成材料应该能够支持广泛的细胞生长和细胞功能。此类支架也可以是可再吸收的。合适的支架包括聚乙醇酸支架(例如由vacanti等j.ped.surg.23:3-91988;cima等biotechnol.bioeng.38:1451991;vacanti等plast.reconstr.surg.88:753-9 1991所述);或合成聚合物,例如聚酸酐、聚原酸酯和聚乳酸。
[0118]
在另一实例中,间充质谱系前体或干细胞和/或其后代和/或源自其的可溶性因子可在凝胶支架(例如来自upjohn company的gelfoam)中施用。
[0119]
本文所述的组合物可单独施用或作为与其它细胞的混合物施用。不同类型的细胞可在即将或快要施用前与本公开的组合物混合,或者它们可在施用前一起共培养一段时间。
[0120]
在一个实例中,组合物包含有效量或治疗或预防有效量的间充质谱系前体或干细胞和/或其后代和/或源自其的可溶性因子。例如,组合物包含约1
×
105个干细胞至约1
×
109个干细胞或约1.25
×
103个干细胞至约1.25
×
107个干细胞/kg(80kg受试者)。要施用的细胞的确切数量取决于多种因素,包括受试者的年龄、体重和性别,以及所治疗疾病的范围和严重程度。
[0121]
在一个实例中,施用50
×
106至200
×
107个细胞。在其它实例中,施用60
×
106至200
×
106个细胞或75
×
106至150
×
106个细胞。在一个实例中,施用75
×
106个细胞。在另一实例中,施用150
×
106个细胞。
[0122]
在一个实例中,组合物包含大于5.00
×
106个活细胞/ml。在另一实例中,组合物包含大于5.50
×
106个活细胞/ml。在另一实例中,组合物包含大于6.00
×
106个活细胞/ml。在另一实例中,组合物包含大于6.50
×
106个活细胞/ml。在另一实例中,组合物包含大于6.68
×
106个活细胞/ml。
[0123]
在一个实例中,本公开的方法包括施用6亿个细胞的总剂量。例如,根据本公开治疗的受试者可接受多个剂量的上述组合物,只要细胞的总剂量不超过6亿个细胞。例如,受试者可接受3个剂量的2亿个细胞。在一个实例中,细胞的总剂量是5亿个细胞。在一个实例中,细胞的总剂量是4亿个细胞。例如,受试者可接受4个剂量的1亿个细胞。在一个实例中,受试者在基线时接受1个剂量的1亿个细胞,随后在三个月内每月一次地施用三个剂量的1亿个细胞。
[0124]
在一个实例中,间充质谱系前体或干细胞占组合物的细胞群体的至少约5%、至少约10%、至少约15%、至少约20%、至少约25%、至少约30%、至少约35%、至少约40%、至少约45%、至少约50%、至少约55%、至少约60%、至少约65%、至少约70%、至少约75%、至少约80%、至少约85%、至少约90%、至少约95%、至少约99%。
[0125]
本公开的组合物可被冷冻保存。可使用本领域已知的慢速冷却方法或
‘
快速’冷冻方案进行间充质谱系前体或干细胞的冷冻保存。优选地,与未冷冻细胞相比,冷冻保存的方法维持冷冻保存细胞的类似表型、细胞表面标记物和生长速率。
[0126]
冷冻保存的组合物可包含冷冻保存溶液。冷冻保存溶液的ph典型地为6.5至8,优选7.4。
[0127]
冷冻保存溶液可包含无菌、非热原等渗溶液,例如plasmalyte a
tm
。100ml plasmalyte a
tm
含有526mg氯化钠,usp(nacl);502mg葡萄糖酸钠(c6h
11
nao7);368mg三水合乙酸钠,usp(c2h3nao2·
3h2o);37mg氯化钾,usp(kcl);和30mg氯化镁,usp(mgcl2·
6h2o)。它不合抗菌剂。用氢氧化钠调节ph。ph为7.4(6.5至8.0)。
[0128]
冷冻保存溶液可包含profreeze
tm
。冷冻保存溶液可另外或替代地包含培养基,例如αmem。
[0129]
为了促进冷冻,通常将冷冻保护剂,例如二甲亚砜(dmso)添加至冷冻保存溶液中。理想情况下,冷冻保护剂应该对细胞和患者无毒、无抗原性、化学惰性、解冻后提供高存活率并允许移植而无需清洗。然而,最常用的冷冻保护剂dmso显示出一些细胞毒性。羟乙基淀粉(hes)可用作替代物或与dmso结合使用,以降低冷冻保存溶液的细胞毒性。
[0130]
冷冻保存溶液可包含dmso、羟乙基淀粉、人血清组分和其它蛋白质填充剂中的一者或多者。在一个实例中,冷冻保存的溶液包含约5%人血清白蛋白(hsa)和约10%dmso。冷冻保存溶液还可包含甲基纤维素、聚乙烯吡咯烷酮(pvp)和海藻糖中的一者或多者。
[0131]
在一个实施方案中,将细胞悬浮在42.5%profreeze
tm
/50%αmem/7.5%dmso中并在控速冷冻机中冷却。
[0132]
可将冷冻保存的组合物解冻并直接施用于受试者或添加至例如包含ha的另一溶液中。或者,可将冷冻保存的组合物解冻并将间充质谱系前体或干细胞在施用前重新悬浮在替代载体中。
[0133]
在一个实例中,本公开的细胞组合物可包含plasma-lyte a、二甲亚砜(dmso)和人血清白蛋白(hsa)。例如,本公开的组合物可包含plasma-lyte a(70%)、dmso(10%)、hsa
(25%)溶液,所述hsa溶液包含5%hsa和15%缓冲液。
[0134]
在一个实例中,本文所述的组合物可作为单一剂量施用。
[0135]
在一些实例中,本文所述的组合物可以多个剂量施用。例如,至少2、至少3、至少4个剂量。在其它实例中,本文所述的组合物可以至少5、至少6、至少7、至少8、至少9、至少10个剂量施用。
[0136]
在一个实例中,间充质谱系前体或干细胞可在施用于受试者之前进行培养扩增。本领域已知各种细胞培养方法。在一个实例中,间充质谱系前体或干细胞被培养扩增约4-10代。在一个实例中,间充质谱系前体或干细胞被培养扩增至少4、至少5、至少6、至少7、至少8、至少9、至少10代。在一个实例中,间充质谱系前体或干细胞被培养扩增至少5代。在这些实例中,干细胞可在冷冻保存之前进行培养扩增。
[0137]
在一个实例中,间充质谱系前体或干细胞在施用之前在无血清培养基中进行培养扩增。
[0138]
在一些实例中,细胞包含在不允许细胞进入受试者循环但允许细胞分泌的因子进入循环的腔室中。以这种方式,可通过允许细胞将因子分泌至受试者的循环中来将可溶性因子施用于受试者。这样的腔室同样可植入受试者体内的部位以增加可溶性因子的局部水平。
[0139]
在一个实例中,间充质谱系前体或干细胞可全身施用。在一个实例中,可将间充质谱系前体或干细胞施用于受试者呼吸道。在一个实例中,可将间充质谱系前体或干细胞施用于受试者的肺。在另一实例中,本公开的组合物是静脉内施用的。在另一实例中,组合物是静脉内施用的并施用于受试者呼吸道。
[0140]
在一个实例中,间充质谱系前体或干细胞每周施用一次。例如,间充质谱系前体或干细胞可每两周每周施用一次。在一个实例中,间充质谱系前体或干细胞可每月施用一次。在一个实例中,在两周内每周一次地施用两剂间充质谱系前体或干细胞。在另一实例中,每两周每周一次地施用两剂间充质谱系前体或干细胞。在另一实例中,在两周内施用四剂间充质谱系前体或干细胞,随后每月一次地施用后续剂量。在一个实例中,可每两周每周一次地施用两剂间充质谱系前体或干细胞,随后每月一次地施用后续剂量。在一个实例中,每月施用四个剂量。
[0141]
在一个实例中,根据本公开将包含细胞的组合物施用于具有高循环crp水平的受试者。在一个实例中,本公开的方法包括以下步骤:i)选择具有大于或等于2mg/l的循环crp水平的患有炎症性肺病的受试者,和ii)向受试者施用包含间充质谱系前体或干细胞(mlpsc)的组合物。在一个实例中,受试者循环crp水平大于或等于3mg/l。在另一实例中,受试者循环crp水平大于或等于4mg/l。在一个实例中,将间充质干细胞施用于受试者。在另一实例中,受试者患有根据本公开的copd和ards中的一者或两者。在一个实例中,选择涉及从待治疗的受试者获得一个或多个样品并测量样品中的循环crp水平。
[0142]
本领域技术人员将理解,可对上述实施方案进行多种改变和/或修改,而不背离本公开的广泛一般范围。因此,本实施方案在所有方面都被视为说明性而不是限制性的。
[0143]
以下具体实施例应被解释为仅仅是说明性的,而不以任何方式限制本公开的其余部分。无需进一步详细说明,相信本领域技术人员可根据本文的描述充分利用本发明。
[0144]
本技术要求2020年3月5日提交的澳大利亚临时专利申请2020900685的优先权,所
述申请的全部内容以引用方式并入本文。
[0145]
实施例
[0146]
离体培养扩增的成人同种异体骨髓源性间充质干细胞(msc),用于治疗炎症性肺病
[0147]
组合物
[0148]
组合物由从健康成人供体的骨髓中分离出来的培养扩增的间充质基质细胞(cemsc)构成。最终组合物包含在plasma-lyte a、二甲亚砜(dmso)和人血清白蛋白(hsa)中配制的cemsc。
[0149]
目标
[0150]
确定:
[0151]-安全性
[0152]-fev1相对于基线的变化。
[0153]-fev1/fvc相对于基线的变化。
[0154]-fvc相对于基线的变化。
[0155]-总6mw距离相对于基线的变化。
[0156]
测量
[0157]
在施用支气管扩张剂后进行肺量测定测量,包括fev1和fvc。基线测量被认为是在支气管扩张剂后,在就诊2(研究第0天)时的第一次研究药物输注之前进行的测量。根据美国呼吸护理协会(aarc)肺量测定临床实践指南(www.rcjournal.com/cpgs/spirupdatecpg.html)进行肺量测定测试。
[0158]
在所有研究就诊中都进行了6分钟步行测试(mwt)。6mwt的程序遵循美国胸科学会指南。记录了步行前后的心率和sao2。还记录了沿着30米(100英尺)走廊步行6分钟的距离,以及步行前后使用borg量表的受试者呼吸困难程度和疲劳程度。
[0159]
受试者
[0160]
基于基线时(即治疗前)的循环crp水平将慢性阻塞性肺病(copd)患者分为以下三组:
[0161]-基线时循环crp水平≥4mg/ml和循环crp水平<4mg/ml的患者;
[0162]-基线时循环crp水平≥3mg/ml和循环crp水平<3mg/ml的患者;
[0163]-基线时循环crp水平≥2mg/ml和循环crp水平<2mg/ml的患者。
[0164]
所有copd患者的炎症性肺病都接受了每月静脉内注射的msc剂量的治疗。受试者在基线(第0天)时接受了1亿个msc,且接着再接受每个月(第30天、第60天和第90天)施用一次的三个剂量的1亿个细胞。在第120天(施用最后一个剂量后30天)分析fev1、fvc和6分钟步行测试。
[0165]
分析
[0166]
与用安慰剂治疗的患者相比,循环crp≥4mg/l的患者组在用细胞治疗后显示出肺功能显著改善(图1至图4;表1和表4)。例如,在第一次给药后的120天内,接受msc的crp≥4mg/l的患者组的fev1相对于基线的变化为0.0625,相比之下,安慰剂组为-0.1(图1)。在第一次给药后的150天内,接受msc的crp≥4mg/l的患者组的fev1/fvc相对于基线的变化为0.02,相比之下,安慰剂组为0.002(图2)。在第一次给药后的120天内,接受msc的crp≥4mg/
l的患者组的fvc相对于基线的变化为0.11,相比之下,安慰剂组为-0.25(图3)。在第一次给药后的120天内,接受msc的crp≥4mg/l的患者组表现出52.2米的六分钟步行测试的改善,相比之下,安慰剂组为约-3.1米(图4)。
[0167]
与用安慰剂治疗的患者相比,循环crp≥3mg/l的患者组在用细胞治疗后也显示出肺功能显著改善(表2)。例如,在第一次给药后的120天内,接受msc的crp≥3mg/l患者组的fev1相对于基线的变化为0.05,相比之下,安慰剂组为-0.1。在第一次给药后的120天内,接受msc的crp≥3mg/l的患者组的fvc相对于基线的变化为0.11,相比之下,安慰剂组为-0.22。在第一次给药后的120天内,接受msc的crp≥4mg/l的患者组表现出42.6米的6分钟步行测试的改善,相比之下,安慰剂组为约6.0米。
[0168]
与用安慰剂治疗的患者相比,循环crp≥2mg/l的患者组在用细胞治疗后也显示出肺功能显著改善(表3)。例如,在第一次给药后的120天内,接受msc的crp≥2mg/l的患者组的fvc相对于基线的变化为0.042,相比之下,安慰剂组为-0.20。
[0169]
这些结果显示出令人惊讶的效果,因为msc治疗在循环crp水平逐渐升高的患者中显示出越来越大的益处。因此,循环crp为2mg/ml的患者的反应不如循环crp为3mg/ml的患者,后者的反应不如循环crp为4mg/ml的患者。这是出乎意料的,因为小分子疗法或其它生物制剂(例如单克隆抗体)在通过循环crp测量的炎症水平最低的患者中具有最大功效,并且它们的效果随着crp水平的增加而逐渐减弱。
[0170]
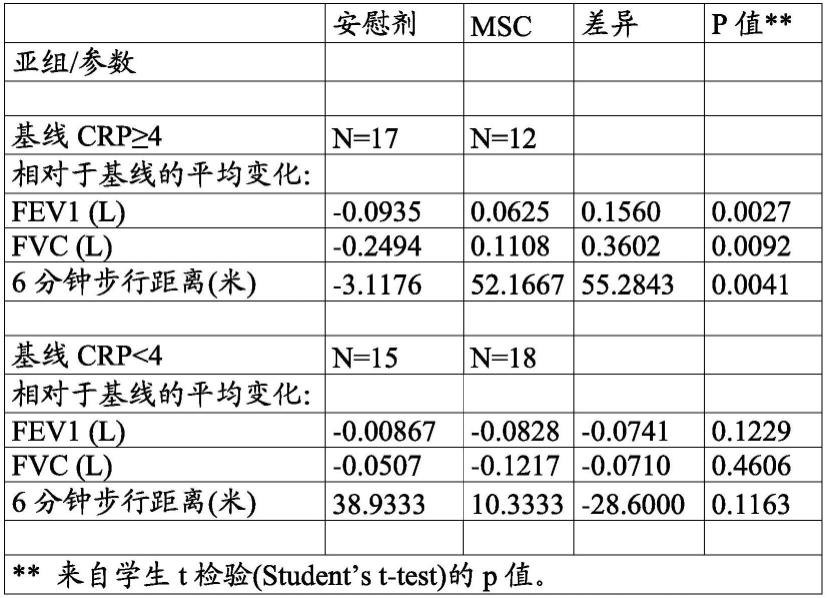
表1:crp亚组的第120天功效分析:基线crp≥4mg/ml的受试者与基线crp<4mg/ml的受试者相比。
[0171][0172]
表2:crp亚组的第120天功效分析:基线crp≥3mg/ml的受试者与基线crp<3mg/ml的受试者相比。
[0173][0174][0175]
表3:crp亚组的第120天功效分析:基线crp≥2mg/ml的受试者与基线crp<3mg/ml的受试者相比。
[0176][0177]
表4:fev1(l)和6分钟步行距离(米)的统计分析,相对于基线crp≥4mg/ml的基线受试者的变化。
[0178][0179][0180]
*使用重复测量的混合效应模型(mmrm)的所有就诊的总体治疗效果。
[0181]
**使用重复测量的混合效应模型(mmrm),根据就诊最小二乘均值的治疗简单差异。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。