1.本发明涉及医药技术领域,具体涉及一种秋水仙碱水凝胶微针及其制备方法。
背景技术:
2.痛风是发达国家和发展中国家常见的炎症性关节炎,由尿酸钠(msu)晶体积累引发。一种急性痛风关节炎(aga),表现为极度疼痛、肿胀、发烧和受影响关节活动困难,严重影响日常生活。因此,aga始终是整个医学领域的基础研究焦点。目前,有几种有效的治疗方法可以缓解aga的疼痛和炎症反应,即通过抑制肿瘤坏死因子(tnf)-α、白细胞介素(il)-6、il-1β等多种炎症因子,抑制炎症细胞功能,包括非甾体抗炎药(nsaid)、皮质激素和秋水仙碱等多种炎症因子来降低炎症反应。然而,经常口服col可导致不良反应,如胃肠道副反应。2007年秋水仙碱贴剂被注册为药品,这可能为透皮给药领域开辟新的机遇。虽然透皮方法可以绕过上述限制,但是秋水仙碱的高水溶性和较差的皮肤渗透性使透皮给药具有挑战性。
3.微针(mn)是一种具有广阔应用前景的新型无痛透皮给药技术,具有较高的安全性。与其他mn相比,水凝胶微针具有更高的载药能力和可调的药物释放,从而避免了秋水仙碱爆发释放引起的毒性反应。一般来说,水凝胶微针在干燥状态下具有一定的硬度,并在进入皮肤后吸收间质液体膨胀成3d网络,从而释放药物。这些因素往往与聚合物交联比直接相关,但交联点在聚合物网络中的不均匀分布,使得传统的水凝胶微针具有较弱的脆性,导致在肘关节等较厚的角质层皮肤中使用困难。水凝胶微针的力学性能和膨胀性能的不兼容,使得药物难以在微针合理应用时间内释放。
4.因此,开发一种具有高溶胀性和高机械韧性的秋水仙碱水凝胶微针具有重要的前景。
技术实现要素:
5.为了克服现有技术的缺点与不足,本发明的首要目的在于提供一种秋水仙碱水凝胶微针的制备方法,该方法制备得到的秋水仙碱水凝胶微针具有高溶胀性和高机械韧性。
6.本发明是通过以下技术方案实现的:
7.一种秋水仙碱水凝胶微针的制备方法,包括如下步骤:
8.(1)将丙烯酰胺、n,n
’‑
双(丙烯酰基)半胱胺和irgacure 2959溶于超纯水中,得到透明凝胶溶液;
9.(2)将得到的透明凝胶溶液倒入pdms模具中,低速离心,然后超声,消除气泡;
10.(3)将盛有透明凝胶溶液的pdms模具置于紫外光下照射,然后在烘箱中风干,得到水凝胶微针;
11.(4)在水凝胶微针中加入秋水仙碱溶液,溶胀后风干,脱模,得到秋水仙碱水凝胶微针。
12.优选地,步骤(1)中,所述透明凝胶溶液中丙烯酰胺、n,n
’‑
双(丙烯酰基)半胱胺和
irgacure 2959与透明凝胶溶液的质量比分别为10~35wt%、0.01~0.1wt%和0.01~0.2wt%。
13.优选地,步骤(2)中,所述低速离心的速度为3000~4000rpm/min,时间为5~20min。
14.优选地,步骤(3)中,所述紫外光下照射的条件为315~400nm,100~500w,照射时间为10~60min。
15.本发明还提供一种秋水仙碱水凝胶微针,由上述制备方法制备得到。
16.与现有技术相比,本发明具有如下有益效果:
17.(1)本发明水凝胶微针通过高度亲水的单体(丙烯酰胺)与具有紫外光响应性二硫键的交联剂(n,n
’‑
双(丙烯酰基)半胱胺)制备,克服了普通水凝胶微针交联点不均匀的缺点,制备得到的水凝胶微针的针型完整,矩阵排列整齐,网络交联点分布均匀,具有优异的机械韧性(>10n/针)和超强溶胀能力(>2500%);
18.(2)本发明制备得到的秋水仙碱水凝胶微针在48h内的累积释放率大于80%,释放曲线符合一级方程,且具有生物相容性,可以有效治疗大鼠急性痛风的炎症,为新型秋水仙碱治疗剂型的开发和治疗提供新的思路和策略。
附图说明
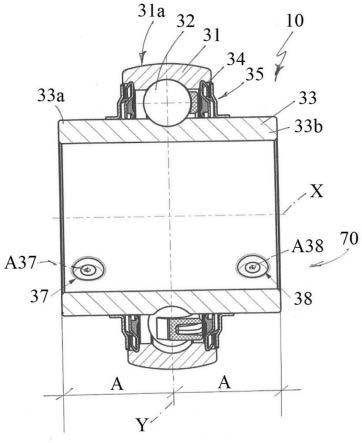
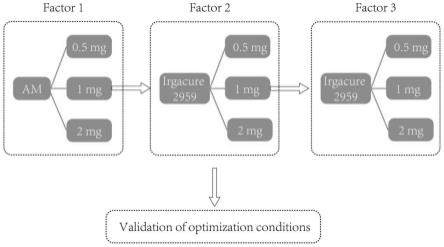
19.图1为连续单因素优化示意图;
20.图2为本发明水凝胶微针中不同含量的am(0.5、1和2g)、irgacure 2959(1、5和10mg)和baca(1、2和4mg)在5ml水形成的凝胶溶液对微针的破裂力和水凝胶的溶胀行为的影响的研究。其中,(a,b)为单体丙烯酰胺(am)对力-位移曲线、溶胀比(n=3)的影响;(c,d)为光引发剂(irgacure 2959)对mn的力-位移曲线、溶胀比的影响(n=3);(e,f)为交联剂(baca)对mn的力-位移曲线、溶胀比的影响(n=3);
21.图3为本发明mn的表观表征,(a)微针的照片;(b)微针的光学显微图像,4
×
;(c)微针的光学显微镜(下,4
×
)和钙黄绿素微针的荧光倒置显微镜(上,5
×
)的比较;(d,e)微针的扫描电镜图像;(f)显示多孔结构的冻干微针的sem图像;
22.图4为本发明微针的能谱分析(eds)图像;
23.图5为本发明秋水仙碱微针的显微镜图片;
24.图6为本发明的微针的体外表征,(a)不同交联剂和引发剂制备的微针的力-位移曲线,(i)以baca为交联剂,以irgacure 2959为光引发剂制备的微针;(ii)以mba为交联剂,irgacure 2959为光引发剂制备的blank-mn;(iii)以baca为交联剂,k2o8s2为热引发剂制备的blank-mn;(b)本发明微针的溶胀率-时间曲线(n=3);(c)秋水仙碱微针的药物累积透皮释放与一级动力学拟合曲线(n=6);(d)钙黄绿素微针体外皮肤释放的皮肤渗透行为在共聚焦显微镜下成像;
25.图7为为本发明微针的插入研究,(a)膜层插入率;(b)大鼠皮肤插入孔的亚甲蓝染色图;(c)钙黄绿素微针皮肤插入物的共聚焦显微镜图像;
26.图8为本发明微针的体内外生物相容性研究图,(a)空白微针、秋水仙碱微针和秋水仙碱溶液对人类永生化表皮细胞(hacat)存活率的影响;(b)各组微针应用于大鼠腹部皮肤后的he染色切片图混合tunel染色切片图;
27.图9为大鼠踝关节肿胀及炎性细胞因子水平,(a)左踝关节注射尿酸单钠(msu)晶体混悬液与右踝关节注射生理盐水后的水肿图像比较;(b)大鼠踝关节注射尿酸单钠(msu)晶体混悬液和生理盐水后足部体积随时间的变化(n=6);(c)col-mn治疗后急性痛风大鼠的足趾肿胀度;(d-f)治疗后大鼠血清炎性因子il-1β(d)、il-6(e)、肿瘤坏死因子-α(f)水平;
28.图10为经col-mn治疗后血浆外渗(a)和髓过氧化物酶活性(b)的反应(n=6)。
具体实施方式
29.下面通过具体实施方式来进一步说明本发明,以下实施例为本发明较佳的实施方式,但本发明的实施方式并不受下述实施例的限制。
30.性能测试方法:
31.1.1、质构仪表征
32.采用tms-pilot质构仪的压缩模式进行mn的标准力学测试。从mn取出一根针,放置在质构仪的不锈钢底板上,针尖朝上。直径为6mm的圆柱形探头以30mm/min的速度落下,与针阵接触时,施加0.03n的触发力,并持续保存力,直到达到0.3mm的位移。
33.1.2、溶胀度表征
34.根据m
t-m0/m0方程计算微针的溶胀能力,其中m0和m
t
代表各配方水凝胶在磷酸盐缓冲液(pbs 7.4)中浸泡0-24h前后的质量。
35.1.3、critic权重分析
36.利用spssau软件(https://spssau.com/)对数据进行归一化处理,剔除单位维,计算指标间的变异性、冲突性、信息量、权重系数和综合得分。
37.实施例1:
38.一种秋水仙碱水凝胶微针的制备方法,包括如下步骤:
39.(1)将1g丙烯酰胺(am)、2mg n,n
’‑
双(丙烯酰基)半胱胺(baca)和5mg irgacure2959溶于5ml超纯水中,得到透明凝胶溶液;
40.(2)将得到的透明凝胶溶液倒入pdms模具中,低速离心(3500rpm,5min),然后超声,消除气泡;
41.(3)将盛有透明凝胶溶液的pdms模具置于紫外光(365nm,300w)下照射20min,然后在烘箱中风干,得到水凝胶微针(blank-mn);
42.(4)在水凝胶微针中加入秋水仙碱溶液,溶胀12h后风干,脱模,得到秋水仙碱水凝胶微针(col-mn)。
43.对比例1:
44.本对比例与实施例1的区别为步骤(1)中用n,n-亚甲基双丙烯酰胺(mba)代替n,n
’‑
双(丙烯酰基)半胱胺(baca)作为交联剂。
45.对比例2:
46.本对比例与实施例1的区别为步骤(1)中用30mg过硫酸钾(k2o2s2)代替irgacure-2959作为引发剂,步骤(3)用在烘箱中加热6h代替紫外光照20min。
47.将实施例1和对比例1-2制备得到的微针,采用tms-pilot质构仪的压缩模式进行mn的标准力学测试,结果如图6a所示,实施例1的微针破裂力为11.53n/needle,对比例1的
微针破裂力为8.11n/needle,对比例2的微针破裂力为3.61n/needle。相比于对比例1和2,实施例1需要更大的力,才能达到相同的压缩量,说明实施例1的机械强度高于对比例1和2。以前的研究已经确定每根针需要大于0.058n才能使微针插入皮肤,实施例1的微针在所需的力下的位移小于0.1mm,表明本发明制备得到的微针机械强度足够大,足以穿透皮肤。
48.另外,本发明通过研究发现,丙烯酰胺单体(am)、交联剂(baca)及光引发剂的含量对水凝胶微针的理化性能有比较大的影响。为此,本发明通过连续单因素实验优化微针的工艺参数,研究了不同含量am(0.5、1和2g)、irgacure 2959(1、5和10mg)和baca(1、2和4mg)在5ml纯水中形成的预凝胶溶液分别对blank-mn的破裂力和水凝胶的溶胀的影响。因素水平表见下表1,根据图1中顺序实施对比:
49.表1
[0050][0051]
结合图2与表2-3,当微针溶液中am的含量为0.5g时,由于溶胀超过了固有弹性强度,造成了力学断裂,水凝胶网的结构完整性丧失(图2b)。然后,除该条件外,通过标准间相关(critical)加权法对破裂力和溶胀度这两个指标的权重系数进行加权,得到综合以上两个性质的综合得分。破裂力的变异性、冲突、信息含量和重量系数与溶胀度的几乎相等(表2),说明两项指标的重复性低,冲突性高。
[0052]
各组指标及综合得分见表3。综合分数的结果显示“am1mg”处方的微针与“am2mg”处方的微针同等重要。因此选择了溶胀度较高的微针“am 1mg”用于后续筛选。其次,irgacure2959浓度对凝胶溶胀度的影响不显著(图2d),而破裂力的权重较高(表2)。根据综合评分,筛选出破裂力更高的“irgacure-2959 5mg”微针(表3)。同理,最终以综合评分较高的“baca2mg”微针为最优配方(表3)。
[0053]
表2
[0054][0055]
表3
[0056][0057]
实施例2表观表征
[0058]
2.1、水凝胶微针的表观表征。
[0059]
用光学显微和扫描电子显微镜(sem)观察了微针的三维结构和冻干后微针的表面形貌。用倒置荧光显微镜观察钙黄绿素微针尖端的荧光分布。用能谱分析仪(eds)扫描微针针尖的c、h、o、s元素。
[0060]
水凝胶微针为实施例1步骤(1~3)得到的产品(blank-mn)。冻干后微针的制备与实施例1步骤(1~3)中不同的是步骤(3)中用冷冻干燥代替风干。钙黄绿素微针的制备与实施例1步骤(1~4)中不同的是步骤(1)中用钙黄绿素代替秋水仙碱。
[0061]
结合图3-4,制备了均匀排列的400个mn的阵列(图3a)。光学显微镜显示了高约500μm、底宽约300μm的样品的尺寸(图3b)。钙黄绿素在微针针尖中分布均匀,表明亲水性小分子化合物可以通过溶胀和消溶胀的方法均匀分布在微针中(图3c)。扫描电子显微镜显示mn呈规则的圆锥形,尖端锋利,表面具有类似于人皮肤的多层结构(图3e,d)。这可能是因为均聚丙烯酰胺很难质子化,不会形成局部势能。电势的均匀可能是力学性能均匀的原因,也可能是决定其宏观力学行为的根本原因。表面具有均匀的孔隙(图3f),这种多孔结构有利于药物的溶解和扩散。能谱(eds)结果表明,水凝胶微针中二硫键分布均匀(图4)。
[0062]
2.2、秋水仙碱水凝胶微针的表观表征
[0063]
用光学显微镜观察秋水仙碱微针的表观形态。
[0064]
秋水仙碱水凝胶微针为实施例1步骤(1~4)得到的产品(col-mn)。
[0065]
如图5,实施例1制得的秋水仙碱水凝胶微针表观结构良好,具有尖锐的针尖,阵列排列均匀,针尖结构均一,与水凝胶微针相比没有结构损坏。
[0066]
实施例3水凝胶微针的体外表征
[0067]
3.1、微针的溶胀度表征
[0068]
用天平称量实施例1称量微针的初始重量m0,随后将其浸入50ml ph 7.4的磷酸盐缓冲液(pbs)中室温溶胀24h。定时取出,用滤纸除去多余的表面水,并称重,记为m
t
,使用m
t-m0/m0方程计算。由于pbs非常类似皮肤间质液,所以选择其作为溶胀介质,并在其他类似的研究中用于模拟皮肤间质液。
[0069]
水凝胶微针为实施例1步骤(1~3)得到的产品(blank-mn)。
[0070]
结合图6b,本发明制备得到的水凝胶微针(blank-mn)的溶胀率在8h达到平衡,最高溶胀度为2708%。
[0071]
3.2、体外透皮扩散实验
[0072]
从-20℃冰箱取离体大鼠腹部皮肤,解冻,在生理盐水中平衡30min,然后根据扩散池直径进行适当裁剪。保鲜膜底部为真皮层,顶部为表皮层,皮肤覆盖在保鲜膜上。表皮用滤纸干燥。应用微针30s。将搅拌器加入到接收单元中。转速为600rpm,温度为(32
±
0.2℃)。扩散池中加入搅拌器和10ml pbs(ph 7.4),恒温32℃。磁性搅拌器以600转/分的速度连续搅拌。感受器腔内充满液体,直到接触到皮肤,然后启动计时器。
[0073]
分别在1、2、4、6、8、10、12、24、36、48h自动采样1ml,同时自动填充1ml液体。采用hplc(waters corporation,usa),采用unitaryl c18(4.6mm
×
250mm,5μm)色谱柱,定量分析样品的col浓度。流动相为甲醇-水(60:40)。柱温30℃,检测波长254nm,进样量10μl,流速1.0ml/min。计算秋水仙碱的浓度。
[0074]
秋水仙碱水凝胶微针为实施例1步骤(1~4)得到的产品(col-mn)。
[0075]
如图6c,秋水仙碱水凝胶微针(col-mn)在48h内累积释放率可达80%以上,用一级动力学方程弥合释放曲线,表明与秋水仙碱水凝胶微针(col-mn)具有缓释作用。
[0076]
3.3、载药微针的体外透皮扩散行为研究
[0077]
本方法用钙黄绿素代替秋水仙碱作为模拟药物,借钙黄绿素在皮肤中的荧光分布来表征药物的扩散行为,其余同实施例1。
[0078]
采用钙黄绿素微针、巴马微型猪皮和自动透皮扩散仪,从-20℃冰箱取离体大鼠腹部皮肤,解冻,在生理盐水中平衡30min,然后根据扩散池直径进行适当裁剪。保鲜膜底部为
真皮层,顶部为表皮层,皮肤覆盖在保鲜膜上。表皮用滤纸干燥。应用微针30s。将搅拌器加入到接收单元中。转速为600rpm,温度为(32
±
0.2℃)。扩散池中加入搅拌器和10ml pbs(ph 7.4),恒温32℃。磁性搅拌器以600rpm的速度连续搅拌。感受器腔内充满液体,直到接触到皮肤,然后启动计时器。在2、6、12、24、48h分别取皮,清洗、冷冻切片,在激光扫描共聚焦显微镜下观察。
[0079]
如图6d,药物渗透的过程包括药物从微针到皮肤的渗透过程和药物从表皮向真皮扩散的过程。根据荧光分布,前一过程在12h内占主导地位,后一过程在12~24h内占主导地位,24~48h内钙黄绿素仍在皮肤内持续释放。
[0080]
3.4、膜插入研究
[0081]
秋水仙碱水凝胶微针为实施例1步骤(1~4)得到的产品(col-mn)。
[0082]
八层膜一层一层排列,深度约为1mm。将其放置在一片牙蜡上作为机械支撑,使用“拇指压力”应用于实施例1秋水仙碱水凝胶微针每个阵列原型。通过使用光学显微镜对每层上产生的孔进行计数,评估微针的穿透力。根据公式(3)计算:每层膜的孔数百分比。
[0083]
如图7a,展示了秋水仙碱水凝胶微针(col-mn)的穿透结果,秋水仙碱水凝胶微针(col-mn)的插入率接近100%,表明本发明制备得到的秋水仙碱水凝胶微针(col-mn)有足够的能力穿透皮肤。
[0084]
3.5、离体大鼠腹部皮肤插入研究
[0085]
秋水仙碱水凝胶微针为实施例1步骤(1~4)得到的产品(col-mn)。
[0086]
取大鼠腹部皮肤,去除皮下粘连,用生理盐水清洗,滤纸干燥,用保鲜膜包裹,20℃冰箱保存。手动将微针插入大鼠皮肤10min后取出。然后,用1%亚甲蓝溶液(100μl)均匀分布于孔部10min。用滤纸吸收多余溶液,用生理盐水浸泡洗净皮肤,用滤纸干燥表面,成像。
[0087]
如图7b,表明本发明制备得到的秋水仙碱水凝胶微针(col-mn)能够以接近100%的效率穿透皮肤。
[0088]
3.6、猪皮插入研究
[0089]
采用钙黄绿素代替秋水仙碱作为模拟药物。
[0090]
将钙黄绿素微针应用于猪皮上48h后,立即用低温超薄切片机将猪皮切成5μm厚的薄片,在激光共聚焦扫描显微镜下观察。如图7c,表明微针有效穿透猪皮并形成微通道。
[0091]
实施例4微针的体内外生物相容性研究
[0092]
4.1、细胞毒性研究
[0093]
blank-mn为实施例1步骤(1~3)得到的产品。col-mn为实施例1步骤(1~4)得到的产品。
[0094]
用cck-8试剂盒检测5mgcol、blank-mn和col-mn(含5mg col)对人角质形成细胞(hacat)活性的细胞毒性。研究前,3个样品在10ml dmem完全培养基中浸泡24h,将hacat细胞按1
×
106个/孔的密度接种于96孔板上,培养过夜。然后,细胞在不同样品浸泡液中孵育24h。处理后的细胞在37℃下与10%cck-8孵育1h,使用酶标仪在450nm处测量吸光度。测量三次。结果以细胞活力百分比表示,与未处理的对照细胞比较。
[0095]
如图8a,与col组相比,blank-mn和col-mn显示出更高的细胞安全性。
[0096]
4.2、组织病理学实验和皮肤组织细胞凋亡实验
[0097]
blank-mn为实施例1步骤(1~3)得到的产品。col-mn为实施例1步骤(1~4)得到的产品。
[0098]
大鼠腹部皮肤剃毛、脱毛,应用blank-mn 24或48h,col-mn 24或48h,用医用胶带固定。分别于24、48h取腹部皮肤组织,10%中性福尔马林固定18h,石蜡包埋。制作4μm厚切片,分别用苏木精-伊红(h&e)和原位末端标记法(tunel)染色观察组织病理学改变和细胞凋亡情况。显微镜下可见炎性细胞,激光扫描共聚焦显微镜下可见凋亡细胞。
[0099]
如图8b,在显微镜下观察空白微针和秋水仙碱微针处理24h和48h大鼠腹部皮肤he切片的病理变化,并与空白对照组(未处理的皮肤)比较,研究微针使用的安全性。与空白对照组的皮肤相比,blank-mn处理的皮肤切片显示几乎相似的细胞完整性。col-mn处理的皮肤切片无炎症,但由于秋水仙碱与微管的结合作用,在一定程度上抑制了细胞增殖,对皮肤的刺激较小。同时各组tunel染色证实微针在载药前后均未引起细胞凋亡。
[0100]
实施例5药效试验
[0101]
以往的研究表明,il-1β的产生和释放是痛风炎症的第一个和最重要的事件。tnf-α可增强中性粒细胞的活性。促炎细胞因子il-6是启动先天免疫反应的关键。滑液接触尿酸钠晶体导致细胞坏死、巨噬细胞释放、中性粒细胞死亡和炎症。我们对尿酸钠晶体(msu)诱导的各组大鼠足踝肿胀皮肤施用实施例1的col-mn或给其灌胃col片溶液(i.g.col),以足肿胀体积、炎症因子水平、血浆外渗、mpo活性等炎症反应评价治疗效果,col-mn直接下调巨噬细胞ros的产生,抑制中性粒细胞趋化,从而抑制晶状体诱导的炎症反应。
[0102]
5.1、动物
[0103]
6-8周龄雄性sd大鼠(体重180g-200g)由安徽中医药大学动物实验中心提供。所有动物实验均经安徽中医药大学伦理委员会批准。动物伦理号:ahucm-rats-2019001。大鼠在动物设施标准化条件下饲养,在实验前12h内,禁食不禁水。
[0104]
5.2、尿酸钠晶体诱导大鼠急性痛风模型的建立
[0105]
尿酸钠(msu)晶体悬浮于无菌生理盐水中。手术前使用70%的酒精对脚踝部位进行消毒。将大鼠分为生理盐水组和msu组,每组6只。注射msu前在踝关节上方5mm处用不可磨灭的标记物画一条水平线,以统一足趾体积的测量标准。然后,将0.2ml msu悬液(25mg/ml)通过21号针头插入大鼠胫骨前肌肌腱内侧,针头尖斜置至45
°
处注入大鼠踝关节。对照组注射0.2ml生理盐水。然后,用足趾体积测量仪测量大鼠足趾体积。
[0106]
结合图9(a,b),通过在踝关节腔内注射尿酸钠(msu)诱导急性痛风性关节炎的速率模型,评估了秋水仙碱微针体内的药效学,以观察其抗炎作用,并与生理盐水比较。24h后,与生理盐水处理大鼠相比,msu处理大鼠踝关节明显肿胀,爬行受限(图9a)。msu组大鼠踝关节出现广泛肿胀,在注射msu后3h出现肿胀,24h肿胀达到高峰,直至注射msu后96h(图9b)。
[0107]
5.3秋水仙碱微针对大鼠急性痛风进展的抑制作用
[0108]
采用spss(26版)软件对数据进行分析。数据以“平均值
±
标准差”表示。两组之间的数值变量采用无配对t检验。采用单因素方差分析(anova)结合bonferroni事后验进行多重比较。*p《0.05、**p《0.01、***p《0.001为差异具有统计学意义。
[0109]
5.3.1、大鼠的分组、造模与给药
[0110]
将大鼠随机分为4组:1)空白组(blank),2)模型组(model),3)秋水仙碱水凝胶微
针组(col-mn),4)秋水仙碱片溶液灌胃组(i.g.col),每组10只。除空白组外,其余大鼠均建立急性痛风模型。2h后,col-mn组大鼠足踝处灌胃含1mg col的col-mn,并用医用胶布固定。i.g.col组大鼠给予col片水溶液(1mg/ml)0.5mg/kg。
[0111]
5.3.2、足体积测量
[0112]
用足趾体积测量仪测量大鼠足趾初始体积。24h后,测量各组大鼠足趾体积。
[0113]
治疗结束时,模型对照组大鼠足肿胀体积增加80%。相比之下,经col-mn或i.g.col处理后,足部肿胀体积的关系变化增加至50%左右,逐渐减少至模型组厚度的37%以下(图9c)。
[0114]
5.3.3、il-1β、tnf-α和il-6等炎症因子水平测定
[0115]
取大鼠腹主动脉血,静置2h后离心,取上层血清,保存于-80℃。根据制造商的说明书,使用来自酶联免疫吸附试验(elisa)试剂盒分析和测定四组的il-1β、tnf-α和il-6等炎症因子水平。用酶标仪测量吸光度值(od)。
[0116]
与模型组比较,col-mn和i.g.col处理后大鼠血清中il-1β、il-6和tnf-α炎症因子水平降低(图9d~f)。
[0117]
5.3.4、大鼠踝关节血浆外渗检测
[0118]
注射的踝关节滑膜腔用30μl(10μl,3次)pbs冲洗,获得滑膜灌洗样品。以牛血清白蛋白(bsa)为标准,采用bradford(1976)比色法测定总蛋白含量。
[0119]
msu注射后24h,炎症引起血浆外渗,可被col-mn和i.g.col在一定程度上抑制(图10a)。
[0120]
5.3.5、大鼠踝关节中性粒细胞检测
[0121]
通过测量mpo活性评价滑膜灌洗液中中性粒细胞的存在。将踝关节称重,剪碎,匀浆。采用髓过氧化物酶(mpo)测定试剂盒检测各组mpo活性。
[0122]
msu注射后24h,踝关节处产生中性粒细胞,可被col-mn和i.g.col在一定程度上抑制(图10b)。
[0123]
综上,本发明制备的mn和col-mn的针型完整,矩阵排列整齐,网络交联点分布均匀,具有优异的机械性能和溶胀性能。col-mn的载药量可以达到有效治疗剂量,透皮扩散具有缓释作用。col-mn可以通过透皮给药进而发挥良好的抗炎作用,有效治疗尿酸钠晶体诱导的大鼠的急性痛风。为新型秋水仙碱治疗剂型的开发和治疗提供新的思路和策略。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。