1.本说明书一个或多个实施例涉及有机磷化合物合成技术领域,尤其涉及一种芳基膦氧化合物及其制备方法。
背景技术:
2.芳基膦氧类化合物作为一类重要的有机磷化合物,在作为药物中间体、功能材料、有机合成配体以及农药等方面均显示出优秀的性质并且被广泛应用。因此,芳基膦酸酯的合成在近年来受到了有机合成科研人员的广泛关注。
3.另一方面,芳基硫盐是一种具有不挥发,易制备,无毒和良好的热稳定性等优点,近几十年中在有机合成领域引起了广泛关注,而且已经逐渐代替了常规的硫化物来参与偶联反应。与常规的用于有机合成的硫化物相比,由于芳基硫盐的缺电子特性,因此它们的碳-硫键比芳基硫化物更容易断裂,而且反应过程中作为衍生基团离去的硫化物比衍生自芳基硫化物的硫醇盐阴离子具有更低的化学毒性。
4.目前,尽管有许多合成芳基膦氧类化合物的报道,但未见以钯催化下芳基硫盐与膦氧化合物进行交叉偶联反应制备芳基膦氧化合物的方法。综上所述,本技术现提出一种芳基膦氧化合物及其制备方法来解决上述出现的问题。
技术实现要素:
5.有鉴于此,本说明书一个或多个实施例的目的在于提出一种芳基膦氧化合物及其制备方法,以解决背景技术中提出的问题。
6.基于上述目的,本说明书一个或多个实施例提供了一种芳基膦氧化合物,具有式i所示结构:
[0007][0008]
其中,r为氢、氟、羟基、苯基、烷基、烷氧基、三氟甲基、酰基或酯基;z1,z2为烷基、烷氧基或芳基。
[0009]
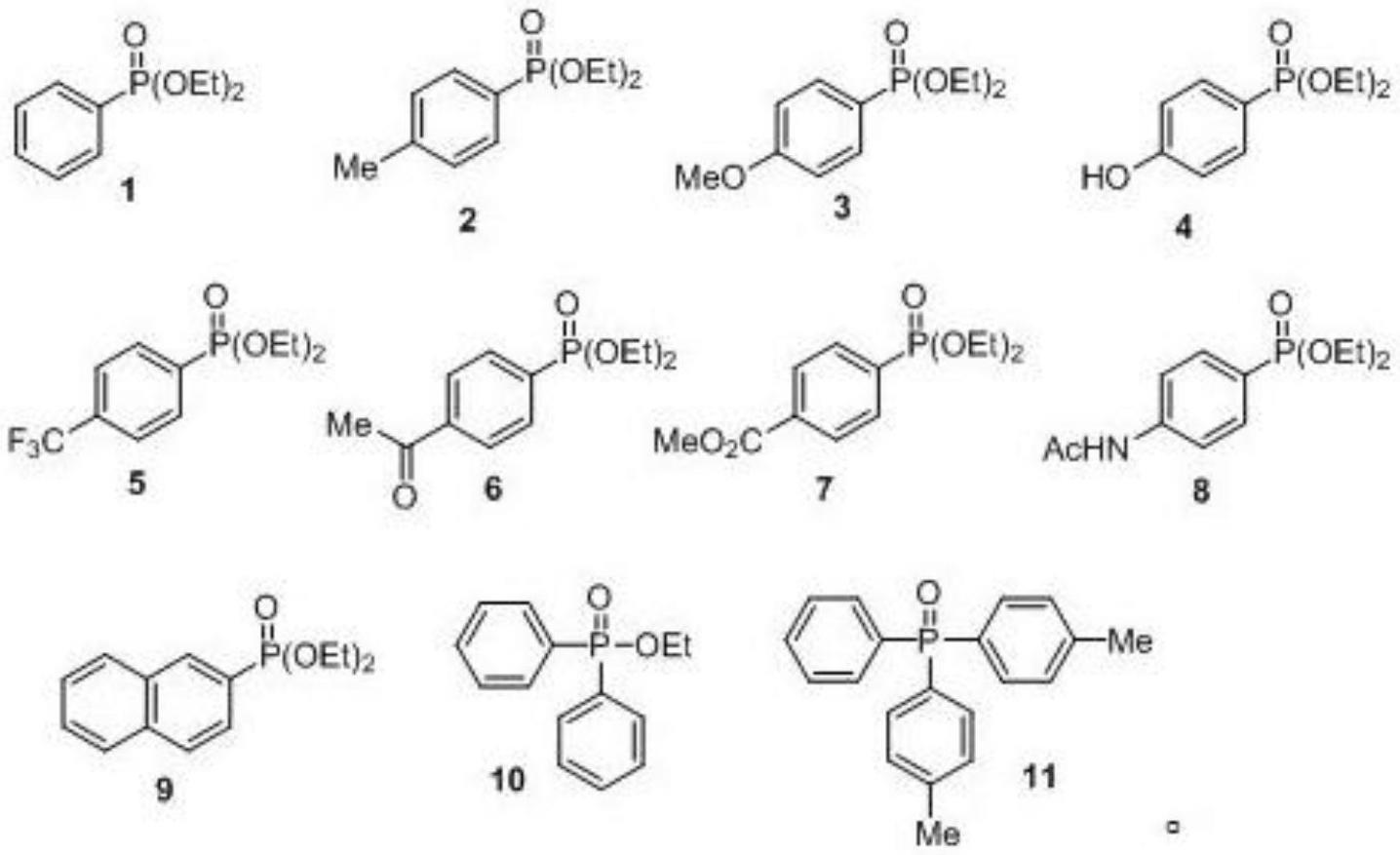
优选的,所述芳基膦氧化合物包括:
[0010][0011]
一种芳基膦氧化合物的制备方法,包括以下步骤:
[0012]
将芳基硫盐、膦氧化合物、钯催化剂、膦配体、碱添加剂和溶剂混合,在氮气气氛中和加热条件下交叉偶联反应形成ar-p键,从而得到芳基膦氧化合物;
[0013]
其中,所述芳基硫盐具有式ii所示结构:
[0014][0015]
其中,r为氢、氟、羟基、苯基、烷基、烷氧基、三氟甲基、酰基或酯基等;r1,r2为苯基或烷基;
[0016]
所述芳基硅试剂具有式iii所示结构:
[0017][0018]
其中,z1,z2为烷基、烷氧基或芳基。
[0019]
更为优选的,所述芳基硫盐、膦氧化合物、钯催化剂、膦配体、碱添加剂的摩尔比为(1.0~3.0):1.0:(0.01~0.2):(0.01~0.2):(1.0~2.0)。
[0020]
更为优选的,所述催化反应在油浴的条件下进行,所述油浴的温度为60℃~130℃,所述催化反应的时间为10h~24h。
[0021]
更为优选的,所述钯催化剂为pdcl2、pd(oac)2、pd2(dba)3、pd(dppf)cl2、pd(pph3)2cl2或pd(acac)2。
[0022]
更为优选的,所述膦配体为jnhnphos、xphos、sphos或ruphos,这些配体具有式iv所示结构:
[0023][0024]
更为优选的,所述碱添加剂为三乙胺、碳酸钠、磷酸钠、碳酸钾、碳酸铯、磷酸钾、磷酸氢二钠、磷酸氢二钾、碳酸氢钠、氢氧化钠和氢氧化钾的一种或几种混合。
[0025]
更为优选的,所述溶剂为dmf(n,n-二甲基甲酰胺)、dma(二甲基乙酰胺)、dmso(二甲基亚砜)、thf(四氢呋喃)、异丙醇、二氯乙烷、1,4-二氧六环、乙醇、异丙醇和叔戊醇的一种或几种混合;所述溶剂的体积与所述膦氧化合物的物质的量之比为1l:(0.1~0.3)mol。
[0026]
更为优选的,将芳基硫盐和膦氧化合物作为反应底物,与溶剂混合后加入钯催化剂、膦配体和碱添加剂,在氮气中以油浴加热条件进行反应,经tlc检测反应完成后进行萃取和浓缩,通过柱层析分离,得到芳基膦氧化合物。
[0027]
从上面所述可以看出,本发明的有益效果:本发明提供了一种钯催化下芳基硫盐与膦氧化合物进行交叉偶联反应制备芳基膦氧化合物的方法。该方法反应条件温和、底物普适性好,所采用的芳基硫盐具有不挥发、易制备、毒性小和良好的热稳定性等优点,对于活性药物分子和功能材料的研发具有重要价值。
附图说明
[0028]
为了更清楚地说明本说明书一个或多个实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本说明书一个或多个实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
[0029]
图1-图3为本发明中实施例一制备的产物的核磁氢谱、碳镨和磷谱图;
[0030]
图4-图6为本发明中实施例二制备的产物的核磁氢谱、碳镨和磷谱图;
[0031]
图7-图9为本发明中实施例三制备的产物的核磁氢谱、碳镨和磷谱图;
[0032]
图10-图12为本发明中实施例四制备的产物的核磁氢谱、碳镨和磷谱图;
[0033]
图13-图15为本发明中实施例五制备的产物的核磁氢谱、碳镨和磷谱图;
[0034]
图16-图18为本发明中实施例六制备的产物的核磁氢谱、碳镨和磷谱图;
[0035]
图19-图21为本发明中实施例七制备的产物的核磁氢谱、碳镨和磷谱图;
[0036]
图22-图24为本发明中实施例八制备的产物的核磁氢谱、碳镨和磷谱图;
[0037]
图25-图27为本发明中实施例九制备的产物的核磁氢谱、碳镨和磷谱图;
[0038]
图28-图30为本发明中实施例十制备的产物的核磁氢谱、碳镨和磷谱图;
[0039]
图31-图33为本发明中实施例十一制备的产物的核磁氢谱、碳镨和磷谱图;
[0040]
图34为本发明实施例中化学反应的示意图。
具体实施方式
[0041]
为使本公开的目的、技术方案和优点更加清楚明白,以下结合具体实施例,对本公开进一步详细说明。
[0042]
请参阅图1-图5,一种芳基膦氧化合物,具有式i所示结构:
[0043][0044]
其中,r为氢、氟、羟基、苯基、烷基、烷氧基、三氟甲基、酰基或酯基;z1,z2为烷基、烷氧基或芳基。
[0045]
作为上述方案的改进方案,所述芳基膦氧化合物包括:
[0046][0047]
一种芳基膦氧化合物的制备方法,包括以下步骤:
[0048]
将芳基硫盐、膦氧化合物、钯催化剂、膦配体、碱添加剂和溶剂混合,在氮气气氛中和加热条件下交叉偶联反应形成ar-p键,从而得到芳基膦氧化合物;
[0049]
其中,所述芳基硫盐具有式ii所示结构:
[0050][0051]
其中,r为氢、氟、羟基、苯基、烷基、烷氧基、三氟甲基、酰基或酯基等;r1,r2为苯基或烷基;
[0052]
所述芳基硅试剂具有式iii所示结构:
[0053][0054]
其中,z1,z2为烷基、烷氧基或芳基。
[0055]
作为上述方案的改进方案,所述芳基硫盐、膦氧化合物、钯催化剂、膦配体、碱添加剂的摩尔比为(1.0~3.0):1.0:(0.01~0.2):(0.01~0.2):(1.0~2.0)。
[0056]
作为上述方案的改进方案,所述催化反应在油浴的条件下进行,所述油浴的温度为60℃~130℃,所述催化反应的时间为10h~24h。
[0057]
作为上述方案的改进方案,所述钯催化剂为pdcl2、pd(oac)2、pd2(dba)3、pd(dppf)cl2、pd(pph3)2cl2或pd(acac)2。
[0058]
作为上述方案的改进方案,所述膦配体为jnhnphos、xphos、sphos或ruphos,这些配体具有式iv所示结构:
[0059][0060]
作为上述方案的改进方案,所述碱添加剂为三乙胺、碳酸钠、磷酸钠、碳酸钾、碳酸铯、磷酸钾、磷酸氢二钠、磷酸氢二钾、碳酸氢钠、氢氧化钠和氢氧化钾的一种或几种混合。
[0061]
作为上述方案的改进方案,所述溶剂为dmf(n,n-二甲基甲酰胺)、dma(二甲基乙酰胺)、dmso(二甲基亚砜)、thf(四氢呋喃)、异丙醇、二氯乙烷、1,4-二氧六环、乙醇、异丙醇和叔戊醇的一种或几种混合;所述溶剂的体积与所述膦氧化合物的物质的量之比为1l:(0.1~0.3)mol。
[0062]
作为上述方案的改进方案,将芳基硫盐和膦氧化合物作为反应底物,与溶剂混合后加入钯催化剂、膦配体和碱添加剂,在氮气中以油浴加热条件进行反应,经tlc检测反应完成后进行萃取和浓缩,通过柱层析分离,得到芳基膦氧化合物。
[0063]
实施例1
[0064]
一种芳基膦氧类化合物,具有式i-(1)所示结构:
[0065][0066]
制备方法:在反应管中加入0.36mmol二甲基(苯基)硫三氟甲磺酸盐、0.3mmol磷酸钾、0.015mmol醋酸钯、0.015mmol x-phos和2ml异丙醇,向其中加入0.3mmol亚磷酸二乙酯,接着进行气体置换,充入氮气,将所得混合液置于80℃下搅拌反应16h。反应结束后通过柱层析分离纯化,柱层析洗脱液中石油醚和乙酸乙酯的体积比为10:1,得到纯化后的目标产物,产率为72%。
[0067]
对所得产物的结构进行表征,核磁共振氢谱、核磁共振碳镨和核磁共振磷谱图分别如图1、图2和图3所示,结构表征数据如下所示:
[0068]1h nmr(400mhz,cdcl3)δ7.79
–
7.73(m,2h),7.55
–
7.47(m,1h),7.45
–
7.38(m,2h),4.16
–
3.97(m,4h),1.27(t,j=7.1hz,6h).
13
c nmr(101mhz,cdcl3)δ132.3(d,j=3.0hz),131.6(d,j=9.9hz),128.4(d,j=15.0hz),128.2(d,j=186.8hz),62.0(d,j=5.4hz),
16.2(d,j=6.5hz).
31
pnmr(162mhz,cdcl3)δ18.82.
[0069]
实施例2
[0070]
一种芳基膦氧类化合物,具有式i-(2)所示结构:
[0071][0072]
制备方法:在反应管中加入0.36mmol二甲基(对甲苯基)硫三氟甲磺酸盐、0.3mmol磷酸钾、0.015mmol醋酸钯、0.015mmol x-phos和2ml异丙醇,向其中加入0.3mmol亚磷酸二乙酯,接着进行气体置换,充入氮气,将所得混合液置于80℃下搅拌反应16h。反应结束后通过柱层析分离纯化,柱层析洗脱液中石油醚和乙酸乙酯的体积比为10:1,得到纯化后的目标产物,产率为65%。
[0073]
对所得产物的结构进行表征,核磁共振氢谱、核磁共振碳镨和核磁共振磷谱图分别如图4、图5和图6所示,结构表征数据如下所示:
[0074]1h nmr(400mhz,cdcl3)δ7.66(dd,j=13.1,8.0hz,2h),7.24(dt,j=7.8,4.0hz,2h),4.23
–
3.91(m,4h),2.36(s,3h),1.27(t,j=7.1hz,6h).
13
c nmr(101mhz,cdcl3)δ142.8(d,j=3.1hz),131.7(d,j=10.3hz),129.1(d,j=15.4hz),124.8(d,j=190.0hz),61.8(d,j=5.3hz),21.5(d,j=1.2hz),16.2(d,j=6.6hz).
31
p nmr(162mhz,cdcl3)δ19.57.
[0075]
实施例3
[0076]
一种芳基膦氧类化合物,具有式i-(3)所示结构:
[0077][0078]
制备方法:在反应管中加入0.36mmol二甲基(4-甲氧基苯基)硫三氟甲磺酸盐、0.3mmol磷酸钾、0.015mmol醋酸钯、0.015mmol x-phos和2ml异丙醇,向其中加入0.3mmol亚磷酸二乙酯,接着进行气体置换,充入氮气,将所得混合液置于80℃下搅拌反应16h。反应结束后通过柱层析分离纯化,柱层析洗脱液中石油醚和乙酸乙酯的体积比为10:1,得到纯化后的目标产物,产率为70%。
[0079]
对所得产物的结构进行表征,核磁共振氢谱、核磁共振碳镨和核磁共振磷谱图分别如图7、图8和图9所示,结构表征数据如下所示:
[0080]1h nmr(400mhz,cdcl3)δ7.80
–
7.65(m,2h),6.98
–
6.85(m,2h),4.17
–
3.91(m,4h),3.81(s,3h),1.27(t,j=7.1hz,6h).
13
c nmr(101mhz,cdcl3)δ162.8(d,j=3.4hz),133.7(d,j=11.4hz),119.3(d,j=194.9hz),113.9(d,j=16.0hz),61.8(d,j=5.3hz),55.2,16.2(d,j=6.6hz).
31
p nmr(162mhz,cdcl3)δ19.77.
[0081]
实施例4
[0082]
一种芳基膦氧类化合物,具有式i-(4)所示结构:
[0083][0084]
制备方法:在反应管中加入0.36mmol二甲基(4-羟基苯基)硫三氟甲磺酸盐、0.3mmol磷酸钾、0.015mmol醋酸钯、0.015mmol x-phos和2ml异丙醇,向其中加入0.3mmol亚磷酸二乙酯,接着进行气体置换,充入氮气,将所得混合液置于80℃下搅拌反应16h。反应结束后通过柱层析分离纯化,柱层析洗脱液中石油醚和乙酸乙酯的体积比为5:1,得到纯化后的目标产物,产率为67%。
[0085]
对所得产物的结构进行表征,核磁共振氢谱、核磁共振碳镨和核磁共振磷谱图分别如图10、图11和图12所示,结构表征数据如下所示:
[0086]1h nmr(400mhz,cdcl3)δ9.95(s,1h),7.65-7.60(m,2h),7.08
–
6.92(m,2h),4.23
–
3.91(m,4h),1.30(t,j=7.1hz,6h).
13
c nmr(101mhz,cdcl3)δ161.8(d,j=3.3hz),133.7(d,j=11.7hz),116.1(d,j=196.2hz),116.0(d,j=16.4hz),62.3(d,j=5.4hz),16.2(d,j=6.6hz).
31
pnmr(162mhz,cdcl3)δ21.10.
[0087]
实施例5
[0088]
一种芳基膦氧类化合物,具有式i-(5)所示结构:
[0089][0090]
制备方法:在反应管中加入0.36mmol二甲基(4-三氟甲基苯基)硫三氟甲磺酸盐、0.3mmol磷酸钾、0.015mmol醋酸钯、0.015mmol x-phos和2ml异丙醇,向其中加入0.3mmol亚磷酸二乙酯,接着进行气体置换,充入氮气,将所得混合液置于80℃下搅拌反应16h。反应结束后通过柱层析分离纯化,柱层析洗脱液中石油醚和乙酸乙酯的体积比为10:1,得到纯化后的目标产物,产率为70%。
[0091]
对所得产物的结构进行表征,核磁共振氢谱、核磁共振碳镨和核磁共振磷谱图分别如图13、图14和图15所示,结构表征数据如下所示:
[0092]1h nmr(400mhz,cdcl3)δ7.91(dd,j=13.0,8.0hz,2h),7.68(dd,j=8.1,3.5hz,2h),4.23
–
3.96(m,4h),1.29(t,j=7.1hz,6h).
13
c nmr(101mhz,cdcl3)δ133.9(dd,j=32.7,3.3hz),132.7(d,j=185.7hz),132.1(d,j=10.2hz),125.2(dq,j=15.1,3.7hz),123.4(d,j=272.7hz),62.4(d,j=5.5hz),16.2(d,j=6.4hz).
31
p nmr(162mhz,cdcl3)δ16.29.
[0093]
实施例6
[0094]
一种芳基膦氧类化合物,具有式i-(6)所示结构:
[0095]
[0096]
制备方法:在反应管中加入0.36mmol二甲基(4-乙酰苯基)硫三氟甲磺酸盐、0.3mmol磷酸钾、0.015mmol醋酸钯、0.015mmol x-phos和2ml异丙醇,向其中加入0.3mmol亚磷酸二乙酯,接着进行气体置换,充入氮气,将所得混合液置于80℃下搅拌反应16h。反应结束后通过柱层析分离纯化,柱层析洗脱液中石油醚和乙酸乙酯的体积比为10:1,得到纯化后的目标产物,产率为46%。
[0097]
对所得产物的结构进行表征,核磁共振氢谱、核磁共振碳镨和核磁共振磷谱图分别如图16、图17和图18所示,结构表征数据如下所示:
[0098]1h nmr(400mhz,cdcl3)δ8.08
–
7.94(m,2h),7.90-7.85(m,2h),4.22
–
3.97(m,4h),2.60(s,3h),1.29(t,j=7.1hz,6h).
13
c nmr(101mhz,cdcl3)δ197.4,139.7(d,j=3.2hz),133.2(d,j=186.5hz),132.0(d,j=10.0hz),128.0(d,j=15.1hz),62.3(d,j=5.5hz),26.7,16.2(d,j=6.4hz).
31
p nmr(162mhz,cdcl3)δ16.87.
[0099]
实施例7
[0100]
一种芳基膦氧类化合物,具有式i-(7)所示结构:
[0101][0102]
制备方法:在反应管中加入0.36mmol二甲基(4-(甲氧基羰基)苯基)硫三氟甲磺酸盐、0.3mmol磷酸钾、0.015mmol醋酸钯、0.015mmol x-phos和2ml异丙醇,向其中加入0.3mmol亚磷酸二乙酯,接着进行气体置换,充入氮气,将所得混合液置于80℃下搅拌反应16h。反应结束后通过柱层析分离纯化,柱层析洗脱液中石油醚和乙酸乙酯的体积比为10:1,得到纯化后的目标产物,产率为57%。
[0103]
对所得产物的结构进行表征,核磁共振氢谱、核磁共振碳镨和核磁共振磷谱图分别如图19、图20和图21所示,结构表征数据如下所示:
[0104]1h nmr(400mhz,cdcl3)δ8.10-8.07(m,2h),7.92
–
7.77(m,2h),4.21
–
3.98(m,4h),3.91(s,3h),1.29(t,j=7.1hz,6h).
13
c nmr(101mhz,cdcl3)δ166.1,133.4(d,j=3.3hz),133.1(d,j=185.3hz),131.7(d,j=10.1hz),129.3(d,j=15.0hz),62.3(d,j=5.5hz),52.4,16.2(d,j=6.4hz).
31
p nmr(162mhz,cdcl3)δ17.02.
[0105]
实施例8
[0106]
一种芳基膦氧类化合物,具有式i-(8)所示结构:
[0107][0108]
制备方法:在反应管中加入0.36mmol二甲基(4-乙酰氨基苯基)硫三氟甲磺酸盐、0.3mmol磷酸钾、0.015mmol醋酸钯、0.015mmol x-phos和2ml异丙醇,向其中加入0.3mmol亚磷酸二乙酯,接着进行气体置换,充入氮气,将所得混合液置于80℃下搅拌反应16h。反应结束后通过柱层析分离纯化,柱层析洗脱液中石油醚和乙酸乙酯的体积比为10:1,得到纯化后的目标产物,产率为50%。
[0109]
对所得产物的结构进行表征,核磁共振氢谱、核磁共振碳镨和核磁共振磷谱图分
别如图22、图23和图24所示,结构表征数据如下所示:
[0110]1h nmr(400mhz,cdcl3)δ9.26(s,1h),7.71(dd,j=9.6,5.2hz,3h),7.65(d,j=8.6hz,1h),4.12
–
3.97(m,4h),2.17(s,3h),1.28(t,j=7.1hz,6h).
13
c nmr(101mhz,cdcl3)δ169.5,142.7(d,j=3.4hz),132.6(d,j=10.8hz),121.8(d,j=193.3hz),119.2(d,j=15.3hz),62.2(d,j=5.5hz),24.4,16.2(d,j=6.6hz).
31
p nmr(162mhz,cdcl3)δ18.91.
[0111]
实施例9
[0112]
一种芳基膦氧类化合物,具有式i-(9)所示结构:
[0113][0114]
制备方法:在反应管中加入0.36mmol二甲基(奈-2-基)硫三氟甲磺酸盐、0.3mmol磷酸钾、0.015mmol醋酸钯、0.015mmol x-phos和2ml异丙醇,向其中加入0.3mmol亚磷酸二乙酯,接着进行气体置换,充入氮气,将所得混合液置于80℃下搅拌反应16h。反应结束后通过柱层析分离纯化,柱层析洗脱液中石油醚和乙酸乙酯的体积比为10:1,得到纯化后的目标产物,产率为70%。
[0115]
对所得产物的结构进行表征,核磁共振氢谱、核磁共振碳镨和核磁共振磷谱图分别如图25、图26和图27所示,结构表征数据如下所示:
[0116]1h nmr(400mhz,cdcl3)δ8.42(d,j=15.5hz,1h),7.90(dd,j=11.2,6.6hz,2h),7.85(d,j=7.9hz,1h),7.78
–
7.71(m,1h),7.61
–
7.50(m,2h),4.35
–
3.88(m,4h),1.32(t,j=7.1hz,6h).
13
c nmr(101mhz,cdcl3)δ134.9(d,j=2.7hz),134.0(d,j=10.2hz),132.2(d,j=16.7hz),128.8,128.3(d,j=14.3hz),128.2,127.7,126.8(d,j=1.0hz),126.3(d,j=9.8hz),125.2(d,j=187.9hz),62.1(d,j=5.3hz),16.3(d,j=6.5hz).
31
p nmr(162mhz,cdcl3)δ19.17.
[0117]
实施例10
[0118]
一种芳基膦氧类化合物,具有式i-(10)所示结构:
[0119][0120]
制备方法:在反应管中加入0.36mmol二苯基(丙基)硫三氟甲磺酸盐、0.3mmol磷酸钾、0.015mmol醋酸钯、0.015mmol x-phos和2ml异丙醇,向其中加入0.3mmol苯基膦酸乙酯,接着进行气体置换,充入氮气,将所得混合液置于80℃下搅拌反应16h。反应结束后通过柱层析分离纯化,柱层析洗脱液中石油醚和乙酸乙酯的体积比为10:1,得到纯化后的目标产物,产率为82%。
[0121]
对所得产物的结构进行表征,核磁共振氢谱、核磁共振碳镨和核磁共振磷谱图分别如图28、图29和图30所示,结构表征数据如下所示:
[0122]1h nmr(400mhz,cdcl3)δ7.87
–
7.78(m,4h),7.54
–
7.47(m,2h),7.44(tdd,j=8.2,3.4,1.3hz,4h),4.10(p,j=7.1hz,2h),1.36(t,j=7.0hz,3h).
13
c nmr(101mhz,cdcl3)δ
132.0(d,j=2.7hz),131.5(d,j=136.2hz),131.5(d,j=10.1hz),128.4(d,j=13.1hz),61.0(d,j=5.9hz),16.4(d,j=6.7hz).
31
pnmr(162mhz,cdcl3)δ31.39.
[0123]
实施例11
[0124]
一种芳基膦氧类化合物,具有式i-(11)所示结构:
[0125][0126]
制备方法:在反应管中加入0.36mmol二苯基(丙基)硫三氟甲磺酸盐、0.3mmol磷酸钾、0.015mmol醋酸钯、0.015mmol x-phos和2ml异丙醇,向其中加入0.3mmol双(对甲基苯基)氧化膦,接着进行气体置换,充入氮气,将所得混合液置于110℃下搅拌反应16h。反应结束后通过柱层析分离纯化,柱层析洗脱液中石油醚和乙酸乙酯的体积比为10:1,得到纯化后的目标产物,产率为64%。
[0127]
对所得产物的结构进行表征,核磁共振氢谱、核磁共振碳镨和核磁共振磷谱图分别如图31、图32和图33所示,结构表征数据如下所示:
[0128]1h nmr(400mhz,cdcl3)δ7.69
–
7.61(m,2h),7.58
–
7.48(m,5h),7.43(ddd,j=8.4,6.6,2.9hz,2h),7.28
–
7.21(m,4h),2.38(s,6h).
13
c nmr(101mhz,cdcl3)δ142.3(d,j
c-p
=2.9hz),132,5,132.0(d,j
c-p
=10.3hz),132.0(d,j
c-p
=9.9hz),131.7(d,j
c-p
=2.8hz),129.4(d,j
c-p
=106.4hz),129.2(d,j
c-p
=12.5hz),128.3(d,j
c-p
=12.1hz),21.6.
31
p nmr(162mhz,cdcl3)δ29.4.
[0129]
本说明书一个或多个实施例旨在涵盖落入所附权利要求的宽泛范围之内的所有这样的替换、修改和变型。因此,凡在本说明书一个或多个实施例的精神和原则之内,所做的任何省略、修改、等同替换、改进等,均应包含在本公开的保护范围之内。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。