α-羟基化脂肪酸代谢产物、其医学用途以及作为生物标志物的用途
1.发明的技术领域
2.本发明涉及具有一个或多个不饱和度、具有奇数烃链的脂肪酸,其中所述脂肪酸的化学结构对应于单不饱和或多不饱和α-羟基化脂肪酸的代谢产物的化学结构。本发明还涉及包含所述奇数链脂肪酸的组合物、其医学用途以及其作为用单不饱和或多不饱和α-羟基化脂肪酸(所述脂肪酸是所述α-羟基化脂肪酸的代谢产物)治疗患者的功效指示剂的用途。
3.发明背景
4.已知膜脂质组成的变化影响细胞信号传导,这可能导致疾病的发展或逆转疾病以及预防疾病。类似地,聚焦于调节膜脂质水平的治疗性干预可以预防和逆转(治愈)病理过程。
5.一般而言,化学结构呈现奇数碳原子的脂肪酸还未被考虑为具有治疗相关性,因为在人类中并且一般在哺乳动物中,存在的绝大多数脂肪酸是偶数链的,通常为14至24个碳原子,奇数链的脂肪酸的存在非常罕见且仅限于痕量。
6.目前,科学文献中可用的数据表明,脂肪酸的微小结构差异对生物活性具有重要影响,并且因此对治疗活性也具有重要影响。众所周知,许多药物具有已知的不良作用或对于多种细胞或组织是有毒的。前药是这样的化合物,所述化合物在摄入时发生代谢反应并且产生对患者或受试者的健康有影响的药剂或药物(即其代谢产物)。
7.因此,在一方面,前药形式的治疗活性化合物的施用允许随时间调节所述化合物的分布和吸收,因为其代谢允许仅在其中发生将所述前药转化为其活性代谢产物的代谢反应的那些细胞或组织中产生药物(即代谢产物)。在这方面,这些前药具有其他优点,诸如允许活性代谢产物的延迟或受控施用,避免其可能对身体具有有害影响的累积。在另一方面,与将会在相应前药的自发代谢期间发生的那些相比,所述治疗活性代谢产物的鉴定和合成允许更强烈地起作用,使得可以在受控的时间范围内施用更高的治疗活性剂量。因此,本发明的一个目的是提供衍生自其他化合物或前药的治疗活性化合物(代谢产物),以便单独地、借助于它们的前药或与它们各自的前药组合地施用这样的代谢产物,使得可以根据患者的状况和待治疗的病理状况来调节治疗作用和可能的不良副作用。
8.发明简述
9.一种化合物,其选自由以下各项组成的组:式(ii)的化合物,或者其药学或营养学上可接受的盐或酯:
10.cooh-(ch2)
a-(ch=ch-ch2)
b-(ch2)
c-ch311.(ii)
12.和式(iii)的化合物,或者其药学或营养学上可接受的盐或酯:
13.cooh-(ch2)
a-(ch=ch-ch2)
m-(ch2)
3-(ch=ch-ch2)
(b-1-m)-(ch2)
c-ch314.(iii)
15.其中a是1至14的整数;b是1至7的整数;c是0、3或6并且m=0;并且其中a 3b c 3是
偶数整数。
16.更特别地,本发明涉及一种化合物,其选自由以下各项组成的组:
17.式(ii)的化合物,或者其药学或营养学上可接受的盐或酯:
18.cooh-(ch2)
a-(ch=ch-ch2)
b-(ch2)
c-ch319.(ii)
20.其中:a=6、b=1并且c=6;或a=6、b=2并且c=3;或a=6、b=3并且c=0;或a=3、b=3并且c=3;或a=2、b=4并且c=3;或a=2、b=5并且c=0;
21.和式(iii)的化合物,或者其药学或营养学上可接受的盐或酯:
22.cooh-(ch2)
a-(ch=ch-ch2)
m-(ch2)
3-(ch=ch-ch2)
(b-1-m)-(ch2)
c-ch323.(iii)
24.其中a=1、b=6、c=0并且m=0。
25.本发明还涉及一种化合物,其选自由如本文所述的式(ii)的化合物和式(iii)的化合物组成的组,其用作药物,并且特别地,其用于诱导神经再生以及用于预防和/或治疗(包括维持治疗)选自由以下各项组成的组的疾病或病理:神经系统疾病或神经退行性疾病;癌症;赘生物;炎性疾病;心血管疾病;皮肤和皮下组织病理;代谢病理;神经性疼痛;瘫痪;睡眠障碍;消化病理;肌肉骨骼和结缔组织疾病;泌尿生殖系统病理;和代谢疾病。
26.本发明还涉及一种药物组合物或营养组合物,其至少包含选自由式(ii)的化合物和式(iii)的化合物组成的组的第一化合物,以及任选的式(i)的化合物,如本文所述。
27.最后,本发明涉及一种测定在受试者中用式(i)的化合物或用其药学上可接受的盐或酯治疗性或预防性地治疗疾病或病理的功效的体外方法,其中所述方法包括在体外在所述受试者的生物样品中测定如本文所述的式(ii)的化合物或式(iii)的化合物、或者其羧酸根阴离子、或者由其在体内或体外形成的衍生物的量,其中所述量与治疗所述疾病或病理的功效有关。
28.发明描述
29.本发明涉及一种化合物,其选自由以下各项组成的组:式(ii)的化合物,或者其药学或营养学上可接受的盐或酯:
30.cooh-(ch2)
a-(ch=ch-ch2)
b-(ch2)
c-ch331.(ii)
32.和式(iii)的化合物,或者其药学或营养学上可接受的盐或酯:
33.cooh-(ch2)
a-(ch=ch-ch2)
m-(ch2)
3-(ch=ch-ch2)
(b-1-m)-(ch2)
c-ch334.(iii)
35.其中a是1至14的整数;b是1至7的整数;c是0至14的整数;m是0至(b-1)的整数;并且其中a 3b c 3是偶数整数。
36.本发明的a、b、c和m的所有值都是大于或等于零的整数。一旦在式中定义了b的值,则m的值就被定义为0至(b-1)的整数,其中b的所述值是已经在1至7中定义的值。出于本发明的目的,在并未指明特定的式或组成时,a、b、c和m的值适用于本文所述的所有式和组成。
37.在本发明的一个实施方案中,a是1至7的整数;b是2至7的整数;c是0、3或6,m是0并且a 3b c 3是偶数整数。在本发明的另一个实施方案中,a是1至14的整数;b是1;c是0、3或6,m是0;并且其中a 3b c 3是偶数整数。
38.最优选地,对于本发明的所有实施方案,m=0并且因此本发明涉及一种化合物,其选自由以下各项组成的组:式(ii)的化合物,或者其药学或营养学上可接受的盐或酯:
39.cooh-(ch2)
a-(ch=ch-ch2)
b-(ch2)
c-ch340.(ii)
41.和式(iii)的化合物,或者其药学或营养学上可接受的盐或酯:
42.cooh-(ch2)
a 3-(ch=ch-ch2)
(b-1)-(ch2)
c-ch343.(iii);
44.其中a是1至14的整数;b是1至7的整数;c是0、3或6;并且其中a 3b c 3是偶数整数。
45.本发明的一个优选实施方案涉及一种式(ii)或式(iii)的化合物的药学或营养学上可接受的盐或酯。更优选地,所述盐是钠盐,并且所述酯是甲酯或乙酯。
46.本发明的式(ii)或式(iii)的化合物对应于式(i)的化合物或者其药学或营养学上可接受的盐或酯的代谢产物的那些式:
47.cooh-choh-(ch2)
a-(ch=ch-ch2)
b-(ch2)
c-ch348.(i)
49.其中a是1至14的整数;b是1至7的整数;c是0至14的整数;m是0至(b
–
1)的整数;并且其中a 3b c 3是偶数整数。
50.因此,式(i)的化合物是具有偶数个碳原子(a 3b c 3是偶数整数)的单不饱和或多不饱和α-羟基化脂肪酸。
51.在一方面,偶数链的式(i)的2-羟基单不饱和脂肪酸是奇数链的式(ii)的其他单不饱和脂肪酸的前药,因为所述前药经历脱羧过程。
52.在另一方面,偶数链的式(i)的2-羟基多不饱和脂肪酸是奇数链的其他单不饱和或多不饱和脂肪酸的前药,在其中发生脱羧但不发生式(i)的化合物的双键中的一个的氢化的情况下,衍生自式(i)的前药的化合物将是式(ii)的化合物,而在其中发生双键中的一个的氢化和式(i)的化合物的脱羧的情况下,衍生自式(i)的前药的化合物将是式(iii)的化合物,其中取决于m的值,氢化的双键可以在不同的位置。
53.以例示的方式,图1a和图8f示出了通过2-羟基二十二碳六烯酸(dha-h)(即式(i)的化合物)的α-氧化在细胞水平上产生(6z,9z,12z,15z,18z)-二十一碳(heneicose)-6,9,12,15,18-五烯酸(hpa)(即其式(iii)的代谢产物)的代谢方案。根据该途径,dha-h前药是一种2-羟基化多不饱和脂肪酸,其通过一系列代谢步骤转化为hpa:(1)通过与辅酶a缀合而激活dha-h;(2)由2-羟基酰基-coa裂解酶介导的裂解,从而产生具有奇数个碳原子的醛;(3)醛脱氢酶作用于醛,从而氢化双键中的一个,以将其转化为酸(hpa)。
54.因此,根据本发明,如果hpa是其中a=1、b=6、c=0的式(i)的前药的代谢产物(所述式(i)的前药是22个碳原子和6个共轭双键的ω-3多不饱和α-羟基化脂肪酸(dha-h)),则hpa是式(iii)的化合物,其中m=0。然而,对于hpa是其中a=4、b=5并且c=0的式(i)的前药的代谢产物的情况(所述式(i)的前药是22个碳原子和5个双键的ω-3多不饱和α-羟基化脂肪酸(2-羟基-二十二碳五烯酸)),hpa可以是式(ii)的化合物。本发明的一个实施方案涉及式(iii)的化合物,其中a=1、b=6、c=0和m=0。
55.此外,图8示出了式(i)的其他脂肪酸的代谢方案。具体地,图8a示出了2-羟基-亚
油酸(la-h)(其中a=6、b=2和c=3的式(i)的化合物)在经历脱羧后产生(8z,11z)-十七碳-8,11-二烯酸(hda,c17:2ω-6)(其是其中a=6、b=2并且c=3的式(ii)的化合物)的代谢方案。图8b示出了2-羟基-α-亚麻酸(ala-h)(其是其中a=6、b=3并且c=0的式(i)的化合物)在经历脱羧后产生(8z,11z,14z)-十七碳-8,11,14-三烯酸(hta ω-3,c17:3ω-3)(其是其中a=6,b=3并且c=0的式(ii)的化合物)的代谢方案。在另一方面,图8c示出了2-羟基-γ-亚麻酸(gla-h)(其是其中a=3、b=3并且c=3的式(i)的化合物)在经历脱羧后产生(5z,8z,11z)-十七碳-5,8,11-三烯酸(hta ω-6,c17:3ω-6)(其是其中a=3、b=3并且c=3的式(ii)的化合物)的代谢方案。图8d示出了2-羟基-花生四烯酸(ara-h)(其是其中a=2、b=4并且c=3的式(i)的化合物)在经历脱羧后产生(4z,7z,10z,13z)-十九碳-4,7,10,13-四烯酸(nta,c:19:4ω-6)(其是其中a=2、b=4并且c=3的式(ii)的化合物)的代谢方案。最后,图8e示出了2-羟基-二十碳五烯酸(epa-h)(其是其中a=2、b=5并且c=0的式(i)的化合物)在经历脱羧后产生(4z,7z,10z,13z,16z)-十九碳-4,7,10,13,16-五烯酸(npa,c19:5ω-3)(其是其中a=2、b=5并且c=0的式(ii)的化合物)的代谢方案。
56.在另一方面,根据图11的代谢方案,式(i)的化合物也可以是具有偶数个碳原子的单不饱和α-羟基化脂肪酸。根据该途径,前药2-羟基油酸(2ohoa)的钠盐是一种2-羟基化单不饱和脂肪酸,其通过一系列代谢步骤转化为8z-十七碳烯酸(8z-十七碳烯酸或c17:1n-9):(1)在依赖于atp(三磷酸腺苷)和镁(mg
2
)的过程中,通过酰基-coa连接酶的激活;(2)2ohoa-coa将经受2-羟基植烷酰基(fitanoyl)-coa裂解酶(2-羟基酰基-coa裂解酶1,hacl1)的活性影响,从而形成中间体单不饱和醛;(3)醛脱氢酶将负责在依赖于nad
(烟酰胺腺嘌呤二核苷酸)的过程中将所述中间体醛转化为8z-十七碳烯酸。因此,根据本发明,8z-十七碳烯酸是其中a=6、b=1并且c=6的式(ii)的化合物,其是17个碳原子的ω-9单不饱和α-羟基化脂肪酸,其由2-羟基油酸或者其药学上可接受的盐或酯(其是式(i)的前药)的代谢产生。
57.尽管式(i)的化合物的医学用途是已知的,但是本发明描述了它们的代谢产物(即式(ii)或式(iii)的化合物)的式,在所述式(i)的化合物的代谢之后其在体内提供特异性和差异化治疗作用,因此所述式(i)的化合物充当其前药。因此,本发明提供了一种根据疾病的性质和待治疗患者的预后来调整治疗性治疗的方式。
58.具体地,本发明公开了治疗有效的α-羟基化单不饱和或多不饱和脂肪酸的代谢产物的具体式。因此,本发明进一步描述了所述式(ii)或式(iii)的代谢产物单独作为药物的用途,从而允许控制施用的量;或其与其式(i)的前药组合作为药物的用途;或其通过施用所述式(i)的前药作为药物的用途,从而允许在治疗期间随时间调节所施用的强度和剂量。此外,借助于其式(i)的前药的施用来施用式(ii)或式(iii)的化合物因此使得可以调节药物的分布和吸收,因为其代谢使得可以仅在其中发生转化所述前药的代谢反应的那些细胞或组织中产生相应的药物,其中在所述细胞中获得活性化合物。在任何情况下,本说明书都涉及式(ii)的化合物和式(iii)的化合物二者,无论是通过化学合成获得(参见实施例1),还是在式(i)的化合物的代谢期间获得。
59.在这方面,出于本发明的目的,术语“代谢产物”用于指定这样的式(ii)或式(iii)的化合物,无论它们的来源是式(i)的化合物在受试者体内的代谢,还是这样的式(ii)或式(iii)的化合物是合成获得的产物。因此,出于本发明的目的,术语式(i)的化合物与术语“式(i)的前药”可互换地使用,并且同样,术语“式(ii)的化合物”和“式(iii)的化合物”分别与术语“式(ii)的代谢产物”和“式(iii)的代谢产物”可互换地使用,因为无论是通过化学合成获得还是由式(i)的化合物的天然代谢产生,所述式(ii)和式(iii)的化合物都具有式(i)的化合物的代谢产物的化学结构或化学式,所述式(i)的化合物因此充当其前药。
60.为了举例说明本发明,本发明的实施例表明由式(i)的前药发挥的治疗作用如何与式(ii)或式(iii)的代谢产物对身体的治疗作用是直接相关的,并且还显示出由式(ii)和式(iii)的化合物本身发挥的治疗作用。因此,如实施例7.3中所示,式(ii)的代谢产物c17:1n-9的细胞累积越大,施用2-羟基油酸(ohoa)(式(i)的化合物)的钠盐在小鼠中产生的异种肿瘤尺寸减小就越大。因此,2ohoa的钠盐的治疗作用与其向代谢产物c17:1n-9的转化部分有关。在另一方面,本发明的实施例6.2证实,由2ohoa的掺入形成代谢产物c17:1n-9(8z-十七碳烯酸)在肿瘤细胞和非肿瘤细胞之间是不同的。与2ohoa相比,胶质瘤细胞显示出在它们的c17:1n-9水平方面的显著增加(图13b和d),而在非肿瘤细胞中,检测到的2ohoa水平显著高于其代谢产物c17:1n-9的水平。此外,实施例和附图显示出由式(i)的化合物(例如dha-h)介导的抗增殖作用至少部分地由其hpa代谢产物(式(iii)的化合物)介导,因为抑制由dha-h形成这种化合物导致更低的dha-h的抗增殖作用(图4b)。这些结果表明,式(i)的化合物的治疗价值部分地与其式(ii)或式(iii)的代谢产物的生物活性有关,所述式(i)的化合物充当式(ii)的化合物的真正前药。
61.在另一方面,在与施用式(i)的化合物(诸如dha-h)的相同实验条件下施用式(ii)或式(iii)的化合物(诸如hpa)导致hpa水平比源自dha-h的那些水平高一个数量级,这将意味着hpa的治疗活性可能高于dha-h的治疗活性。这种效果是由于式(i)的前药(dha-h)与其式(iii)的代谢产物(hpa)之间的结构差异所致。事实上,在本发明中,证实了与非羟基化类似物相比,dha的α-羟基化形式(dha-h)的摄取被阻止(图5c)。如果与非羟基化脂肪酸相比,dha-h摄取被阻止,那么在施用dha-h和hpa之后观察到的hpa的不同细胞内水平必定是由于这些化合物由细胞从细胞外介质的不同摄取所致。此外,如实施例6.3所示,代谢产物c17:1n-9的ic
50
值低于其前药2ohoa的ic
50
值,从而确认了其更大的抗增殖效力。此外,如图3b所示,肿瘤中的hpa水平与异种模型中的肿瘤尺寸呈负相关。因此,式(i)的化合物(前药)的治疗作用通过增加的代谢产物的存在而增强。
62.在另一方面,如图5所示,在相同的条件下,使用hpa的钠盐(通过化学合成获得的代谢产物,如实施例1中所述)的处理对培养物诱导的死亡率程度比使用dha-h的钠盐(前药)或dha的钠盐(天然类似物)的处理诱导的死亡率程度显著得多。因此,代谢产物的施用允许提供比通过施用前药获得的治疗作用更突出的治疗作用。
63.然而,如实施例6.3所示,c17:1n-9通过代替其前药直接施用而在肿瘤细胞和非肿瘤细胞二者中具有抗增殖作用,由此所述式(ii)的代谢产物c17:1n-9的通过其式(i)的前药2ohoa的施用提供了产生治疗作用的选择性方式,从而在不产生不希望的不良作用并且在维持疗法中同样有用的情况下允许所述疗法的更长时间施用。具体地,奇数链脂肪酸通过β-氧化被代谢,产生丙酰-coa。与偶数链脂肪酸不同,偶数链脂肪酸的代谢以产生乙酰-coa结束,乙酰-coa又经由克雷布斯循环(krebs cycle)被代谢。丙酰-coa可以转化为丙酸,如果其累积,则会引起作为不良作用的代谢性酸中毒。在生物素和维生素b12依赖性过程中,丙酰-coa可以代谢地转化为琥珀酰-coa(其经由克雷布斯循环被代谢)。这个过程不是
脂肪酸的通常代谢途径,因为在哺乳动物体内,绝大多数的脂肪酸是偶数链的。因此,这种代谢途径选择性地影响奇数链多不饱和脂肪酸(诸如式(ii)和式(iii)的代谢产物),并且在这样的奇数链代谢产物的细胞内浓度过高或存在导致生物素或维生素b12缺乏的特定病理情况的情形下可以是饱和的,从而导致上述丙酸酸中毒的不良作用。
64.因此,直接向细胞施用的代谢产物具有在某些情况下是不希望的毒素。这种毒性可以在施用式(i)的前药或化合物时被调节,可以调节式(ii)或(iii)的代谢产物的作用和毒性。在这方面,与非羟基化脂肪酸相比,前药的较慢摄取在避免过高的细胞内代谢产物浓度方面可以是有用的,并且因此在避免可能的丙酸累积方面可以是有用的。因此,取决于代谢条件、施用方案和待治疗的病理,并且特别是在需要更强烈的治疗作用的那些情况下,或者在持续时间缩短的治疗中,可能期望使用式(ii)或式(iii)的代谢产物,或者其药学上可接受的盐或酯;而在其他情况下,诸如在长期治疗或维持治疗中,可能期望通过使用式(i)的前药或者其药学上可接受的盐或酯(诸如dha-h的钠盐)来使用时间受控的施用。因此,通过使用偶数链的式(i)的化合物作为前药来施用式(ii)或式(iii)的代谢产物允许时间调控地施用它们的式(ii)或式(iii)的代谢产物(其具有奇数链)。
65.由于所有这些原因,本发明显示出借助于它们的式(i)的前药的施用来施用式(ii)或式(iii)的化合物如何允许它们的奇数链代谢产物的时间调控的施用。
66.因此,本发明使得可以根据疾病的性质和待治疗患者的预后来调整疗法,以使用代谢产物或式(i)的化合物(即前药)作为药物。在一方面,在其中需要短期急性治疗活性的情况下,代谢产物的使用将是更合适的或优先的,以获得快速且显著的效果。在另一方面,当需要长期治疗时,例如在慢性疾病中,或者如果需要维持治疗,则根据疾病的时间和情况/严重程度,可以推荐或优先使用前药或以不同比率组合前药和代谢产物的组合物。
67.因此,一般而言,式(ii)和(iii)化合物及其药学或营养学上可接受的盐的使用对生物体是有益的,如本技术的实施例所示。当需要长期或高剂量施用时,当以受控方式施用所述式(ii)和(iii)的化合物时,作为它们的代谢的结果,通过施用相应的式(i)的前药,这些式(ii)和(iii)的化合物的作用使得可以避免源自它们的代谢和累积的不良作用。以这种方式,具有式(i)的前药提供了一种在发生不良副作用的风险较低的情况下施用式(ii)或式(iii)的代谢产物并随时间以持续方式提供治疗有效量的所述代谢产物的方法,因为具有式(i)的前药一旦施用就会被代谢。因此,根据代谢条件、施用方案和待治疗的病理,可能期望直接使用式(ii)或式(iii)的化合物或者其药学上可接受的盐或酯(代谢产物),或可能期望通过使用式(i)的前药或者其药学上可接受的盐或酯(前药)或它们的组合(前药 代谢产物)来使用时间受控的施用。
68.因此,本发明的一个方面涉及一种化合物,其选自由以下各项组成的组:式(ii)的化合物,或者其药学上可接受的盐或酯:
69.cooh-(ch2)
a-(ch=ch-ch2)
b-(ch2)
c-ch370.(ii)
71.和式(iii)的化合物,或者其药学上可接受的盐或酯:
72.cooh-(ch2)
a-(ch=ch-ch2)
m-(ch2)
3-(ch=ch-ch2)
(b-1-m)-(ch2)
c-ch373.(iii);
74.其中a是1至14的整数;b是1至7的整数;c是0至14的整数;m是0至(b
–
1)的整数;并
且其中a 3b c 3是偶数整数,其用作药物,并且特别地用于诱导神经再生以及用于预防和/或治疗(包括维持治疗)选自由以下各项组成的组的疾病或病理:神经系统疾病或神经退行性疾病;癌症;赘生物;炎性疾病;心血管疾病;皮肤和皮下组织病理;代谢病理;神经性疼痛;瘫痪;睡眠障碍;消化病理;肌肉骨骼和结缔组织疾病;泌尿生殖系统病理;和代谢疾病。
75.出于本发明的目的,术语“维持治疗”或“维持疗法”被定义为作为对首要或主要治疗或疗法的补充而施用的治疗性治疗,其目的是预防或延迟在用主要治疗或疗法治疗后已得到完全或部分缓解的疾病的复发,或在主要疗法的治疗结束后减缓疾病的发展。
76.优选地,本发明涉及式(ii)的化合物或式(iii)的化合物,或者其药学上可接受的盐或酯,其用于疾病或病理的治疗或维持疗法,并且更优选地用于癌症的治疗或维持疗法。
77.因此,本发明的一个实施方案涉及化合物在制备药物中的用途,所述化合物选自由如本文所述的式(ii)的化合物或者其药学上可接受的盐或酯以及式(iii)的化合物或者其药学上可接受的盐或酯组成的组,所述药物用于诱导神经再生或用于预防和/或治疗(包括维持治疗)选自由以下各项组成的组的疾病或病理:神经系统疾病或神经退行性疾病;癌症;赘生物;炎性疾病;心血管疾病;皮肤和皮下组织病理;代谢病理;神经性疼痛;瘫痪;睡眠障碍;消化病理;肌肉骨骼和结缔组织疾病;泌尿生殖系统病理;和代谢疾病。
78.本发明的另一个实施方案涉及在患者中预防和/或治疗疾病或病理的方法或者诱导神经再生的方法,其中所述方法包括向所述患者施用有效量的选自由以下各项组成的组的化合物:式(ii)的化合物,或者其药学上可接受的盐或酯:
79.cooh-(ch2)
a-(ch=ch-ch2)
b-(ch2)
c-ch380.(ii)
81.和式(iii)的化合物,或者其药学上可接受的盐或酯:
82.cooh-(ch2)
a-(ch=ch-ch2)
m-(ch2)
3-(ch=ch-ch2)
(b-1-m)-(ch2)
c-ch383.(iii);
84.其中a是1至14的整数;b是1至7的整数;c是0至14的整数;m是0至(b
–
1)的整数;并且其中a 3b c 3是偶数整数。
85.出于本发明的目的,有效量或治疗有效量应理解为提供治疗作用而不对患者引起不可接受的毒性作用的量。药物的有效量或剂量取决于化合物和所治疗的病况或疾病,以及例如所治疗的患者的年龄、体重和临床状况,施用形式,患者的临床病史,疾病的严重度,以及所施用的化合物的效力。
86.此外,本发明的一个实施方案涉及一种化合物,其选自由以下各项组成的组:式(ii)的化合物:
87.cooh-(ch2)
a-(ch=ch-ch2)
b-(ch2)
c-ch388.(ii)
89.和式(iii)的化合物:
90.cooh-(ch2)
a-(ch=ch-ch2)
m-(ch2)
3-(ch=ch-ch2)
(b-1-m)-(ch2)
c-ch391.(iii);
92.其用于预防和/或治疗疾病或病理或者用于诱导神经再生,其中所述预防和/或治疗或者神经再生的诱导的特征在于施用式(i)的化合物或前药,或者其药学上可接受的盐或酯:
93.cooh-choh-(ch2)
a-(ch=ch-ch2)
b-(ch2)
c-ch394.(i)
95.并且其中所述式(i)的化合物被代谢而产生治疗有效量的:
96.式(ii)的化合物:
97.cooh-(ch2)
a-(ch=ch-ch2)
b-(ch2)
c-ch398.(ii)
99.或式(iii)的化合物:
100.cooh-(ch2)
a-(ch=ch-ch2)
m-(ch2)
3-(ch=ch-ch2)
(b-1-m)-(ch2)
c-ch3101.(iii);
102.并且其中a是1至14的整数;b是1至7的整数;c是0至14的整数;m是0至(b
–
1)的整数;并且其中a 3b c 3是偶数整数。
103.优选地,所述疾病选自由以下各项组成的组:神经系统疾病或神经退行性疾病;癌症;赘生物;炎性疾病;心血管疾病;皮肤和皮下组织病理;代谢病理;神经性疼痛;瘫痪;睡眠障碍;消化病理;肌肉骨骼和结缔组织疾病;泌尿生殖系统病理;和代谢疾病。
104.因此,本发明的另一个方面涉及一种施用有效量的如本文所述的式(ii)的化合物或式(iii)的化合物用于预防和/或治疗疾病或病理或用于诱导神经再生和/或预防神经变性的方法,其中所述式(ii)的化合物或所述式(iii)的化合物以如本文所述的式(i)的前药或者其药学上可接受的盐或酯的方式施用。
105.本发明还涉及一种预防和/或治疗疾病或病理的方法;其中所述方法包括施用有效量的如本文所述的式(ii)的化合物的前药或者其药学上可接受的盐或酯;或式(iii)的化合物的前药或者其药学上可接受的盐或酯;其中所述式(ii)或式(iii)的化合物的前药具有式(i),或者其药学上可接受的盐或酯,如本文所述。
106.此外,本发明涉及一种预防和/或治疗疾病或病理或者诱导神经再生和/或预防神经变性的方法,其中所述方法包括向有需要的患者施用有效量的式(i)的化合物,或者其药学上可接受的盐或酯:
107.cooh-choh-(ch2)
a-(ch=ch-ch2)
b-(ch2)
c-ch3108.(i)
109.其中式(i)的化合物在所述患者的体内被代谢而产生治疗有效量的以下代谢产物:
[0110]-具有式(ii)的代谢产物:
[0111]
cooh-(ch2)
a-(ch=ch-ch2)
b-(ch2)
c-ch3[0112]
(ii)
[0113]
或
[0114]-具有式(iii)的代谢产物:
[0115]
cooh-(ch2)
a-(ch=ch-ch2)
m-(ch2)
3-(ch=ch-ch2)
(b-1-m)-(ch2)
c-ch3[0116]
(iii);
[0117]
其中a是1至14的整数;b是1至7的整数;c是0至14的整数;m是0至(b
–
1)的整数;并且a 3b c 3是偶数整数,其中所述代谢产物负责在患者中预防和/或治疗所述疾病或病理以及诱导神经再生和/或预防神经变性。优选地,在施用有效量的式(i)的化合物后,在所述
患者的体内存在具有式(ii)或具有式(iii)的代谢产物。
[0118]
在一个优选的实施方案中,在施用后,所述式(i)的化合物的超过1%、10%、超过40%、超过50%和至多99%被代谢为式(ii)或式(iii)的代谢产物。
[0119]
另一个实施方案涉及一种预防和/或治疗疾病或病理的方法,所述疾病或病理选自由以下各项组成的组:神经系统疾病或神经退行性疾病;癌症;赘生物;炎性疾病;心血管疾病;皮肤和皮下组织病理;代谢病理;神经性疼痛;瘫痪;睡眠障碍;消化病理;肌肉骨骼和结缔组织疾病;泌尿生殖系统病理;和代谢疾病,以及用于诱导神经再生和/或预防神经变性的方法;其中所述方法包括向患者施用有效量的具有式(i)的结构的前药,或者其药学上可接受的盐或酯:
[0120]
cooh-choh-(ch2)
a-(ch=ch-ch2)
b-(ch2)
c-ch3[0121](i)[0122]
其中所述前药在体内转化以将活性化合物释放到所述患者的细胞中;其中所述活性化合物具有以下的结构:
[0123]-式(ii):
[0124]
cooh-(ch2)
a-(ch=ch-ch2)
b-(ch2)
c-ch3[0125]
(ii)
[0126]
或
[0127]-式(iii):
[0128]
cooh-(ch2)
a-(ch=ch-ch2)
m-(ch2)
3-(ch=ch-ch2)
(b-1-m)-(ch2)
c-ch3[0129]
(iii)
[0130]
其中a是1至14的整数;b是1至7的整数;c是0至14的整数;m是0至(b
–
1)的整数;并且a 3b c 3是偶数整数。
[0131]
优选地,所述转化是化学过程或生理过程。出于本发明的目的,术语“化学过程”是指前药在体内通过化学反应转化以释放活性化合物,其中前药是化学反应的试剂或底物,而活性化合物是反应产物。此外,出于本发明的目的,术语“生理过程”是指由于在有机体中自然发生的事件或过程(例如由于酶的活性)所致的转化。
[0132]
此外,虽然式(i)的化合物经由其式(ii)或式(iii)的代谢产物而在治疗上起作用,但是所述式(i)的化合物也显示出独立于所述代谢途径的生物活性,如本发明的实施例6.4所示。
[0133]
因此,本发明的另一个实施方案涉及选自由如本文所述的式(ii)的化合物和式(iii)的化合物组成的组的化合物,或者涉及其药学上可接受的盐或酯,其用作药物,并且特别地根据本发明用于诱导神经再生和/或预防神经变性和/或用于预防和/或治疗疾病或病理,其特征在于所述化合物在式(i)的化合物或它的药学上可接受的盐或酯之前、在其之后或与其联合施用:
[0134]
cooh-choh-(ch2)
a-(ch=ch-ch2)
b-(ch2)
c-ch3[0135](i)[0136]
其中a是1至14的整数;b是1至7的整数;c是0至14的整数并且a 3b c 3是偶数整数;并且其中a、b和c的所述值与式(ii)的化合物或式(iii)的化合物的a、b和c的值相同或不同。
[0137]
此外,本发明涉及一种诱导神经再生和/或预防神经变性的方法,或者涉及一种预防和/或治疗疾病或病理的方法,所述方法包括向患者施用有效量的式(ii)的化合物或式(iii)的化合物,或者其药学上可接受的盐或酯,其中所述方法的特征在于其还包括施用如本文所述的式(i)的化合物,或者其药学上可接受的盐或酯;并且其中所述式(i)的化合物在所述式(ii)或式(iii)的化合物之前、在其之后或与其联合施用。
[0138]
出于本发明的目的,术语“前药”是指在施用至受试者后通过代谢过程转化为第二治疗活性化合物的化合物。
[0139]
在另一方面,出于本发明的目的,术语“受试者”是指人或动物。
[0140]
出于本发明的目的,术语“药学上可接受的”是指由联邦政府或州政府的监管机构授权或批准的或在欧洲、美国或其他公认的药典中列出的在动物或人类中使用的化合物或物质。在整个本说明书中,所述术语主要适用于根据本公开定义的式(i)、(ii)和(iii)的化合物的盐和酯。
[0141]
因此,术语“药学上可接受的盐”是指化合物的盐,所述盐也具有衍生其的母体化合物的所需药理学活性。优选地,药学上可接受的盐是钠盐。
[0142]
出于本发明的目的,术语“酯”是指其中属于羧酸部分的羟基已被烷氧基替代的任何化合物。在本发明的一个优选实施方案中,酯是甲酯或乙酯。更优选地,酯是乙酯。
[0143]
出于本发明的目的,术语“营养学上可接受的”是指可用于营养产品的所有物质。因此,出于本发明的目的,术语“营养品”或“营养组合物”是指膳食补充剂,其可单独服用或与其他食物组合服用,并且对摄取其的受试者的健康产生有益效果,尤其是在预防疾病方面。在整个本说明书中,所述术语主要适用于根据本公开定义的式(i)、(ii)和(iii)的化合物的盐和酯。
[0144]
出于本发明的目的,术语“立体异构体”是指具有相同化学式和相同原子序列但在空间上具有不同三维取向的那些化合物,并且包括由手性碳的存在产生的立体异构体r和s(其还使用命名法( )和(-)),以及由构成双键的碳的取代基的排列产生的立体异构体e和z(其也使用顺式/反式命名法)。因此,由于式(i)的前药包含手性碳(相对于羧基的α碳),所以本发明还包括关于所述手性碳的构型的两种立体异构体r和s,以及两者的任何混合物。在另一方面,由于式(i)的前药及其式(ii)或(iii)的代谢产物均包含c=c双键,所以本发明还包括对于它们的每一个双键的所有e和z立体异构体。在一个优选的实施方案中,式(i)的前药、式(ii)的化合物和式(iii)的化合物的所有双键都具有全顺式构型。因此,如果式(i)的前药具有由其双键确定的顺式/反式(或e/z)立体化学构型,则式(ii)或式(iii)的代谢产物对于其含有的双键也将具有这样的构型。
[0145]
出于本发明的目的,术语“包含”表示它包括一组特定的特征(例如,一组特征a、b和c),并且被解释为意指它包括那些特征(a、b和c),但是不排除存在其他特征(例如,特征d或e),前提是它们不会使权利要求不可实行。此外,出于本发明的目的,术语“含有”、“包括”、“具有”或“涵盖”及其复数形式应被视为术语“包含”的同义词。在另一方面,如果使用术语“由
……
组成”,则装置/方法/产品中不存在除所述术语后的那些特征之外的其他特征。在这方面,出于本发明的目的,术语“包含”可以由术语“由
……
组成”或“基本上由
……
组成”中的任一个代替。因此,“包含”可以是指一组特征a、b和c,其还可以包括其他特征,诸如e和d,前提是这样的特征不会使权利要求不可实行,但是这样的术语“包含”也包括其中
一组特征“由”或“基本上由”a、b和c“组成”的情形。
[0146]
此外,本发明使得可以支持在维持治疗(维持疗法)中施用式(i)的化合物,特别是2ohoa,或者其药学上可接受的盐或酯,更优选地2ohoa的钠盐,其中所述式(i)的化合物或者其药学上可接受的盐或酯在一段时间内以不同的时间间隔施用,其式(ii)或式(iii)的代谢产物的累积浓度是治疗有效性的量度。因此,测定使用式(i)的化合物或者其药学上可接受的盐或酯进行治疗的功效的所述体外方法包括测定式(ii)或式(iii)的化合物、或其羧酸根阴离子、或由其形成的衍生物的量。
[0147]
在这方面,出于本发明的目的,术语“生物标志物”是指第一化合物或物质,或者所述第一化合物或物质的衍生物,其可以用于测定使用第二化合物或物质进行治疗的反应和/或功效。因此,出于本发明的目的,式(ii)或式(iii)的代谢产物可以用作用于测定使用式(i)的化合物进行治疗的反应和/或功效的生物标志物。
[0148]
因此,本发明的另一个方面涉及一种用于测定在受试者中使用式(i)的化合物或者使用其药学上可接受的盐或酯的疾病或病理的治疗性或预防性治疗或者神经再生诱导治疗的功效的体外方法:
[0149]
cooh-choh-(ch2)
a-(ch=ch-ch2)
b-(ch2)
c-ch3[0150](i)[0151]
其中所述方法包括在体外在所述受试者的生物样品中测定以下化合物的量:
[0152]-式(ii)的化合物:
[0153]
cooh-(ch2)
a-(ch=ch-ch2)
b-(ch2)
c-ch3[0154]
(ii)
[0155]
或
[0156]-式(iii)的化合物:
[0157]
cooh-(ch2)
a-(ch=ch-ch2)
m-(ch2)
3-(ch=ch-ch2)
(b-1-m)-(ch2)
c-ch3[0158]
(iii)
[0159]
或者其羧酸根阴离子,或者由其在体内或体外形成的衍生物,其中所述量与治疗的功效有关;并且其中a是1至14的整数;b是1至7的整数;c是0至14的整数;m是0至(b
–
1)的整数;并且其中a 3b c 3是偶数整数。
[0160]
因此,所述方法包括测定式(ii)或式(iii)的化合物、它们相应的羧酸根阴离子或由其形成的衍生物的量。
[0161]
所述式(ii)或(iii)的化合物的衍生物可以通过使包含在体外样品中的所述式(ii)或(iii)的化合物与用于获得其衍生物的物质反应而在体外形成。在这种情况下,本发明的方法包括测定在体外形成的所述式(ii)或式(iii)的衍生物的量。例如,用于检测脂肪酸的一些技术需要它们事先进行化学修饰,并且因此,通过气相色谱法的检测通常需要脂肪酸样品(在这种情况下是式(ii)或式(iii)的化合物)转化为其相应的甲酯用以进行检测和定量。
[0162]
在另一方面,所述式(ii)或式(iii)的化合物的衍生物可以是代谢衍生物或在体内形成的衍生物(体内发生的反应的结果)、作为所述式(ii)或式(iii)的化合物与另一种脂质、蛋白质、酶、核苷酸、碳水化合物等的反应的结果形成的衍生物。因此,所述衍生物可以是所述式(ii)或式(iii)的化合物的酯,诸如例如甘油磷脂(诸如磷脂酰胆碱、磷脂酰乙
醇胺、磷脂酰丝氨酸、磷脂酰肌醇、磷脂酰甘油、磷脂酸或其任何溶血形式,诸如溶血磷脂酰胆碱、溶血磷脂酰乙醇胺等)、缩醛磷脂(烷基或烯基)、胆固醇酯、甘油脂诸如三酰甘油(甘油三酯)或二酰甘油、心磷脂、鞘脂、具有辅酶a的硫酯(酰基-coa)或酰基肉碱等。在这种情况下,本发明的方法包括在体外测定生物样品中的所述代谢衍生物(或体内形成的衍生物)的量。
[0163]
因此,所述式(ii)或式(iii)的化合物或它们相应的羧酸根阴离子或由其在体内或体外形成的衍生物的量与在受试者中使用式(i)的化合物治疗和/或预防疾病或病理或者进行神经再生诱导治疗的功效有关,其中与对照组相比,所述式(ii)或式(iii)的化合物或其羧酸根阴离子或其衍生物的水平与使用所述式(i)的化合物或其药学上可接受的盐或酯来治疗性或预防性地治疗疾病或病理的功效有关。
[0164]
本发明的另一个方面涉及以下化合物的用途:
[0165]-式(ii)的化合物:
[0166]
cooh-(ch2)
a-(ch=ch-ch2)
b-(ch2)
c-ch3[0167]
(ii)
[0168]
或
[0169]-式(iii)的化合物:
[0170]
cooh-(ch2)
a-(ch=ch-ch2)
m-(ch2)
3-(ch=ch-ch2)
(b-1-m)-(ch2)
c-ch3[0171]
(iii)
[0172]
或者其相应的羧酸根阴离子,或者由其在体内或体外形成的衍生物,所述用途用于在体外测定使用式(i)的化合物或其药学上可接受的盐或酯来治疗性或预防性地治疗疾病或病理或者进行神经再生诱导治疗的功效:
[0173]
cooh-choh-(ch2)
a-(ch=ch-ch2)
b-(ch2)
c-ch3[0174](i)[0175]
其中a是1至14的整数;b是1至7的整数;c是0至14的整数;m是0至(b
–
1)的整数;并且其中a 3b c 3是偶数整数。
[0176]
更优选地,疾病或病理选自由以下各项组成的组:神经系统疾病或神经退行性疾病;癌症;赘生物;炎性疾病;心血管疾病;皮肤和皮下组织病理;代谢病理;神经性疼痛;瘫痪;睡眠障碍;消化病理;肌肉骨骼和结缔组织疾病;泌尿生殖系统病理;和代谢疾病。仍更优选地,疾病或病理选自神经系统疾病或神经退行性疾病;癌症;炎性疾病;和代谢疾病。
[0177]
在一个更优选的实施方案中,所述方法测定使用式(i)的化合物的药学上可接受的盐并且甚至更优选地使用式(i)的化合物的钠盐进行治疗的功效。
[0178]
在本发明的一个实施方案中,生物样品是血液样品(包括血浆或血清)、尿液样品、唾液样品、组织活检、脑脊液或汗液样品。
[0179]
本发明还涉及一种药物组合物,其至少包含选自由以下各项组成的组的第一化合物:
[0180]-式(ii)的化合物,或者其药学上可接受的盐或酯:
[0181]
cooh-(ch2)
a-(ch=ch-ch2)
b-(ch2)
c-ch3[0182]
(ii)
[0183]
和
[0184]-式(iii)的化合物,或者其药学上可接受的盐或酯:
[0185]
cooh-(ch2)
a-(ch=ch-ch2)
m-(ch2)
3-(ch=ch-ch2)
(b-1-m)-(ch2)
c-ch3[0186]
(iii)
[0187]
其中所述组合物任选地包含式(i)的第二化合物,或者其药学上可接受的盐或酯:
[0188]
cooh-choh-(ch2)
a-(ch=ch-ch2)
b-(ch2)
c-ch3[0189](i)[0190]
并且其中a是1至14的整数;b是1至7的整数;c是0至14的整数;m是0至(b
–
1)的整数;并且a 3b c 3是偶数整数;
[0191]
以及至少一种药学上可接受的赋形剂。
[0192]
本发明还涉及一种药物组合物,其至少包含选自由以下各项组成的组的第一化合物:
[0193]-式(ii)的化合物的药学上可接受的盐或酯:
[0194]
cooh-(ch2)
a-(ch=ch-ch2)
b-(ch2)
c-ch3[0195]
(ii)
[0196]
和
[0197]-式(iii)的化合物的药学上可接受的盐或酯:
[0198]
cooh-(ch2)
a-(ch=ch-ch2)
m-(ch2)
3-(ch=ch-ch2)
(b-1-m)-(ch2)
c-ch3[0199]
(iii)
[0200]
其中所述组合物任选地包含式(i)的化合物的药学上可接受的盐或酯:
[0201]
cooh-choh-(ch2)
a-(ch=ch-ch2)
b-(ch2)
c-ch3[0202](i)[0203]
并且其中a是1至14的整数;b是1至7的整数;c是0至14的整数;m是0至(b
–
1)的整数;并且a 3b c 3是偶数整数;
[0204]
以及至少一种药学上可接受的赋形剂。
[0205]
本发明的另一个实施方案涉及一种药物组合物,其至少包含选自由式(ii)的化合物和式(iii)的化合物组成的组的第一化合物,其中所述组合物任选地包含如上所述的式(i)的化合物的药学上可接受的盐或酯;以及至少一种药学上可接受的赋形剂;其用作药物;并且特别地,用于诱导神经再生和/或预防神经变性,以及用于预防和/或治疗选自由以下各项组成的组的疾病或病理:神经系统疾病或神经退行性疾病;癌症;赘生物;炎性疾病;心血管疾病;皮肤和皮下组织病理;代谢病理;神经性疼痛;瘫痪;睡眠障碍;消化病理;肌肉骨骼和结缔组织疾病;泌尿生殖系统病理;和代谢疾病。
[0206]
在本发明的一个优选实施方案中,所述至少第一化合物是式(ii)的化合物或式(iii)的化合物的药学上可接受的盐或酯,和/或所述第二化合物是式(i)的化合物的药学上可接受的盐或酯。
[0207]
本发明的一个实施方案涉及药物组合物在制备药物中的用途,所述药物组合物至少包含选自由以下各项组成的组的第一化合物:式(ii)的化合物和式(iii)的化合物,或者其药学上可接受的盐或酯,其中所述组合物任选地包含如上所述的式(i)的化合物,或者其药学上可接受的盐或酯;以及至少一种药学上可接受的赋形剂;所述药物用于诱导神经再生和/或预防神经变性,和/或用于预防和/或治疗疾病或病理。
[0208]
本发明的另一个实施方案涉及一种预防和/或治疗疾病或病理或者用于诱导神经再生和/或预防神经变性的方法;其中所述方法包括向有需要的患者施用有效量的药物组合物,所述药物组合物至少包含选自由以下各项组成的组的第一化合物:式(ii)的化合物和式(iii)的化合物,或者其药学上可接受的盐或酯,其中所述组合物任选地包含如上所述的式(i)的化合物,或者其药学上可接受的盐或酯;以及至少一种药学上可接受的赋形剂。
[0209]
优选地,所述疾病或病理选自由以下各项组成的组:神经系统疾病或神经退行性疾病;癌症;赘生物;炎性疾病;心血管疾病;皮肤和皮下组织病理;代谢病理;神经性疼痛;瘫痪;睡眠障碍;消化病理;肌肉骨骼和结缔组织疾病;泌尿生殖系统病理;和代谢疾病。
[0210]
本领域技术人员可以选择本领域已知的一种或多种药学上可接受的媒介物或赋形剂,使得药物组合物适合施用至人类受试者和动物二者。
[0211]
在本发明的一个优选实施方案中,所述赋形剂是白蛋白,例如:卵白蛋白,乳白蛋白,人、牛、鼠或兔来源的天然或重组白蛋白,更优选地,人血清白蛋白或牛血清白蛋白。
[0212]
本发明中公开的药物组合物也可以在其他疗法之前或之后共同施用。优选地,这样的额外疗法是放射疗法、用于治疗肿瘤的电场(肿瘤治疗电场)、免疫疗法或化学疗法。更优选地,本发明中公开的药物组合物还可以在包括施用替莫唑胺(temozolomide)的疗法之前或之后共同施用。
[0213]
这样的施用可以是成人或儿科患者的治疗的一部分。在一个优选的实施方案中,所述药物组合物在放疗治疗、化疗治疗、用于治疗肿瘤的电场治疗(肿瘤治疗电场)或免疫治疗性治疗之前或之后共同施用。
[0214]
在本发明的一个实施方案中,本文公开的药物组合物包含至少一种额外的治疗组分或活性化合物。所述额外的治疗组分或活性化合物提供加合或协同的生物活性。出于本公开的目的,术语“活性化合物”或“治疗组分”应当用来意指当施用至人类或动物时发挥治疗作用的化学或生物实体。这样的活性化合物或额外的治疗组分可以是细胞疗法、小分子疗法、免疫疗法、放射疗法等。
[0215]
在额外的治疗组分或活性化合物中,有用于治疗神经退行性疾病的化合物、抗癌剂、代谢调节化合物、心血管药物以及肥胖和超重调节剂。
[0216]
在治疗组分或额外的活性化合物中还有用于治疗神经退行性疾病的化合物、化学治疗剂、代谢调节化合物、心血管药物以及肥胖和超重调节剂。优选地,所述活性化合物或所述疗法是化学治疗剂、细胞治疗剂或免疫治疗剂。
[0217]
在一个优选的实施方案中,所述药物组合物还包含选自由以下各项组成的组的化学治疗剂:铂基抗肿瘤剂;抗有丝分裂化学治疗剂;聚二磷酸腺苷核糖聚合酶(parp)抑制剂;i型拓扑异构酶抑制剂;ii型拓扑异构酶抑制剂;埃博霉素(epothilone);环骨架干扰物(cyclo-skeletal perturber);烷基化剂;组蛋白脱乙酰酶抑制剂;激酶抑制剂;抗叶酸剂;肽类抗生素;类视黄醇;长春花生物碱和胸苷酸合成酶抑制剂。更优选地,化学治疗剂选自由以下各项组成的组:贝伐单抗(bevacizumab)、卡莫司汀(carmustine)、环磷酰胺(cyclophosphamide)、美法仑(melphalan)、异环磷酰胺(ifosfamide)、白消安(busulfan)、替莫唑胺、氮芥(mechlorethamine)、苯丁酸氮芥(chlorambucil)、美法仑、达卡巴嗪(dacarbazine)、柔红霉素(daunorubicin)、阿霉素(doxorubicin)、表柔比星(epirubicin)、伊达比星(idarubicin)、米托蒽醌(mitoxantrone)、戊柔比星(valubicin)、
紫杉醇(paclitaxel)、多西他赛(docetaxel)、白蛋白结合型紫杉醇(abraxane)、泰索帝(taxotere)、埃博霉素、伏立诺他(vorinostat)、罗米地辛(romidepsin)、伊立替康(irinotecan)、托泊替康(topotecan)、喜树碱(camptothecin)、依沙替康(exatecan)、勒托替康(lurtotecan)、依托泊苷(etoposide)、替尼泊苷(teniposide)、他氟泊苷(tafluposide)、硼替佐米(bortezomib)、厄洛替尼(erlotinib)、吉非替尼(gefitinib)、伊马替尼(imatinib)、维莫非尼(vemurafenib)、维莫德吉(vismodegib)、阿扎胞苷(azacytidine)、硫唑嘌呤(azathioprine)、卡培他滨(capecitabine)、阿糖胞苷(cytarabine)、克拉屈滨(cladribine)、氟达拉滨(fludarabine)、去氧氟尿苷(doxifluridine)、氟尿嘧啶(fluorouracil)、吉西他滨(gemocytebine)、羟基脲(hydroxyurea)、巯基嘌呤(mercaptopurine)、甲氨蝶呤(methotrexate)、培美曲塞(pemetrexed)、氮杂硫芘(azathiopyrene)、硫鸟嘌呤(thioguanine)、视黄酸(retinoic acid)、博来霉素(bleomycine)、放线菌素(actinomicine)、卡铂、顺铂、奥沙利铂(oxaliplatin)、维甲酸(tretinoine)、阿利维a酸(alitretinoin)、贝沙罗汀(bexarotene)、拓扑替康(topotecan)、长春碱(vinblastin)、长春新碱(vincristin)、长春地辛(vindesin)和长春瑞滨(vinorelbin)。更优选地,额外的化学治疗剂是替莫唑胺。
[0218]
在这方面,脂质在整合细胞膜时可以控制细胞信号传导的事实认为它们还可以调节细胞的生理状态,并且因此调节一般健康状态。因此,本文公开的化合物可用于诱导神经再生以及预防和/或治疗不同的疾病和病理,特别是选自由以下各项组成的组的疾病和病理:神经系统疾病或神经退行性疾病;癌症;赘生物;炎性疾病;心血管疾病;皮肤和皮下组织病理;代谢病理;神经性疼痛;瘫痪;睡眠障碍;消化病理;肌肉骨骼和结缔组织疾病;泌尿生殖系统病理;和代谢疾病。
[0219]
出于本发明的目的,神经系统的疾病是影响神经系统(中枢和外周二者)的所有疾病。在这个组中有神经退行性疾病,出于本发明的目的,其是这样的异质性病症组,其特征在于中枢神经系统或外周神经系统的结构和功能的进行性变性。
[0220]
优选地,神经退行性疾病选自由脊髓损伤和神经源性疼痛组成的组。出于本发明的目的,术语“诱导神经再生”是指神经功能的再生。在另一方面,出于本发明的目的,术语“预防神经变性”表示治疗导致已经在进行中的神经退行性过程的停止,或治疗防止神经变性的发作或进展。
[0221]
这些神经退行性过程中的一些涉及患者认知能力或运动损伤方面的显著降低。神经退行性过程、神经病症和神经精神病症具有神经元变性或其组分诸如脂质(例如髓磷脂)或膜蛋白(例如肾上腺素能受体、5-羟色胺能受体等)改变的共同基础。
[0222]
特别地,神经退行性疾病选自由以下各项组成的组:(i)中枢神经系统的炎性疾病,诸如细菌性脑膜炎、非细菌性脑膜炎、急性出血性坏死性脑病、其他脑炎、脊髓炎和脑脊髓炎、非特指型(nos)脑室炎、颅内和鞘内脓肿和肉芽肿、硬膜外和硬膜下脓肿、静脉炎、颅内和鞘内血栓性静脉炎和中枢神经系统的炎性疾病的后遗症;(ii)主要影响中枢神经系统的全身性萎缩,诸如吉兰-巴雷综合征(guillan-barre)、糖尿病性神经病变、华勒氏变性(wallerian degeneration)、路易体痴呆(lewy body dementia)、额颞叶痴呆、亨廷顿舞蹈病(huntington's chorea)、亨廷顿痴呆(huntington's dementia)、遗传性共济失调;脊髓性肌萎缩和相关综合征,诸如韦-霍二氏病(werdnig-hoffman);主要影响中枢神经系统的
全身性萎缩、脊髓灰质炎后综合征;运动神经元疾病,诸如肌萎缩性侧索硬化和进行性延髓麻痹;(iii)锥体外系和运动障碍,诸如帕金森病(parkinson's disease)、继发性帕金森症(secondary parkinsonism)、抗精神病药恶性综合征、药物诱发的继发性帕金森症脑炎后帕金森症(drug-induced secondary parkinsonism post-encephalitic parkinsonism)、血管性帕金森症(vascular parkinsonism)、基底核退行性疾病、哈-斯二氏病(hallervorden-spatz)、进行性核上性眼肌麻痹、进行性核上性麻痹、纹状体黑质变性、原发性震颤肌张力障碍、药物性震颤、肌阵挛、药物性舞蹈病、药物性抽搐、器质性抽搐、药物性运动障碍、静坐不能、不宁腿综合征、僵人综合征和良性颤抖发作;(iv)其他神经系统退行性疾病,诸如阿尔茨海默病(alzheimer's disease)、早发性或迟发性阿尔茨海默病、额颞叶痴呆诸如皮克病(pick's disease)、酒精引起的神经系统变性、阿尔珀斯病(alpers disease)、利氏病(leigh's disease)、路易体痴呆、轻度认知障碍、皮质基底节变性、原发性退行性痴呆(包括阿尔茨海默氏痴呆(alzheimer's dementia),老年和早老形式,卒中);(v)中枢神经系统脱髓鞘疾病,诸如髓质、脑干的多发性硬化(播散性、全身性或非特指型(nos));急性播散性脱髓鞘、弥漫性中枢神经系统硬化;(vi)发作性和阵发性病症,诸如反复发作的癫痫和癫痫发作、特发性癫痫和癫痫发作、癫痫大发作、非特异性失张力性或阵挛性癫痫、lennox-gastaut综合征、癫痫痉挛、非特指型癫痫、偏头痛、头痛、短暂性脑缺血事故及相关综合征、睡眠障碍和眩晕;(vii)神经、神经根和神经丛病症,诸如三叉神经病症、面神经病症、颅神经病症、神经根和神经丛病症、上肢或下肢单神经病变和华勒氏变性;(viii)外周神经系统的多神经病变和其他病症,包括遗传性和特发性神经病变,诸如roussy-levy综合征、雷夫苏姆病(refsum's disease);炎性多神经病变;多神经病变后遗症,诸如吉兰-巴雷后遗症(guillan-barre sequelae)、血清神经病变;其他多神经病变,诸如药物、酒精、毒剂、放射性神经病变;炎性和中毒性多神经病变的后遗症;(ix)肌肉和神经肌肉接头疾病,诸如重症肌无力和其他肌神经病症、肌肉和神经肌肉接头病症;(x)脑瘫和其他麻痹综合征,包括偏瘫、截瘫、四肢瘫痪;(xi)其他神经系统病症,诸如复杂区域性疼痛综合征、神经性疼痛、无调性神经系统病症、外周自主神经病变、脑积水、脑囊肿、赖利-戴综合征(riley-day syndrome)、多系统自主神经系统变性、海马硬化、近中硬化、糖尿病性神经病变或wolfram综合征、肾上腺脑白质营养不良、脑白质营养不良和脊髓损伤;(xii)由诸如血管性痴呆、不明痴呆、抑郁等生理状况引起的精神和行为障碍;与精神活性物质滥用有关的行为障碍;精神分裂症、分裂型障碍、妄想性障碍和其他与情绪无关的精神障碍;情绪(情感)障碍,诸如躁狂发作、双相型情感障碍、重度抑郁症、循环情感性障碍、情绪恶劣性障碍;焦虑症、分离性、应激相关和其他非精神病性躯体形式精神障碍;与生理障碍和生理因素相关的行为综合征,诸如进食障碍、睡眠障碍;人格障碍、冲动障碍、病态赌博;智力残疾;言语障碍、写作、学习障碍、精神活性物质使用障碍和成瘾行为。
[0223]
出于本发明的目的,“神经性疼痛”被定义为由体感神经系统的损伤或疾病引起的疼痛,如由国际疼痛研究协会(iasp)所定义的。体感神经系统包括感觉神经元和对身体表面或体内的变化作出反应的神经通路。出于本发明的目的,术语瘫痪是指由中枢或外周神经系统的损伤或疾病引起的身体某些部位的部分或全部活动性丧失。在另一方面,术语睡眠障碍是指包括由中枢或外周神经系统问题或病理引起的睡眠启动和维持方面的问题的那些障碍。这样的睡眠障碍的非限制性实例包括失眠、嗜睡诸如发作性睡病、睡眠呼吸暂
停、不宁腿综合征、昼夜节律障碍和深眠状态等。
[0224]
某些神经退行性疾病可以导致其中发展失明、听力问题、定向障碍、情绪障碍等的过程。典型的神经退行性病症的一个实例是阿尔茨海默病,其中观察到斑块的形成,主要由来自改变的蛋白质加工的β-淀粉样肽形成,随后在细胞外部累积。此外,高度磷酸化的tau蛋白的神经丝缠结出现在细胞内部。这一过程与胆固醇代谢的改变以及随之而来的某些膜脂质(诸如二十二碳六烯酸)水平的改变有关。在另一方面,多种神经退行性病变,诸如帕金森病、阿尔茨海默病、老年性痴呆(或路易体痴呆),与α-突触核蛋白的纤维状聚集体的病理性累积有关,其引起细胞甘油三酯的代谢的重要改变。事实上,这些和其他神经退行性疾病的发展与血清或细胞脂质(诸如胆固醇、甘油三酯、鞘磷脂、磷脂酰乙醇胺等)水平的改变有关。这再次表明,脂质在神经元、胶质细胞、神经、大脑、小脑和脊髓的正常发挥功能中起到至关重要的作用,考虑到中枢神经系统中的大量脂质,这是合乎逻辑的。
[0225]
阿尔茨海默病(ad)是一种神经退行性疾病,迄今为止其尚无有效疗法或治疗,并且其病理生理学在很大程度上仍是未知的。在过去十年中已经设计和开发了多种药物和疗法,以阻止或减缓这种疾病的神经退行性过程特性。然而,目前还不知晓成功完成iii期人体临床试验的治疗。由于抗淀粉样蛋白/tau疗法的临床试验几乎完全失败,大多数疗法都受到淀粉样蛋白级联假设的启发(该假设目前存在争议)。
[0226]
在另一方面,各种类型的硬化症和其他神经退行性过程都与“脱髓鞘”有关,其最终结果是神经轴突的覆盖物中的脂质损失,这意味着随之而来的是电信号的传播过程的改变。髓磷脂是包围许多神经元的轴突的脂质层,并且由胶质细胞(分别处于外周和中枢水平的雪旺细胞和少突胶质细胞)的质膜的一系列螺旋折叠形成。由于所有这些原因,已经表明脂质在神经退行性疾病的发展中起到重要作用。此外,已表明天然多不饱和脂肪酸对神经退行性过程的发展具有适度的预防作用。事实上,中枢神经系统中最丰富的脂质是二十二碳六烯酸(dha),其丰度在许多神经退行性过程(诸如阿尔茨海默病)中发生改变。
[0227]
此外,代谢疾病优选选自由以下各项组成的组:肥胖、超重、高胆固醇血症、高甘油三酯血症、糖尿病和胰岛素抵抗。代谢疾病形成一组以某些分子的累积或缺乏为特征的病理。一个典型的实例是高于正常水平的葡萄糖、胆固醇和/或甘油三酯的累积。在全身水平(例如升高的血浆水平)和在细胞水平(例如在细胞膜中)二者的葡萄糖、胆固醇和/或甘油三酯的水平升高与导致在多种水平的功能障碍的细胞信号传导的改变相关,并且通常是由某些酶的活性或这样的蛋白质的控制方面的错误造成的。其中最重要的代谢障碍是高胆固醇血症(高胆固醇水平)和高甘油三酯血症(高甘油三酯水平)。这些疾病的发生率、发病率和死亡率都很高,因此它们的治疗是首要关注的问题。其他重要的代谢障碍是特征在于葡萄糖水平的控制存在问题的糖尿病和胰岛素抵抗。这些代谢病理与其他病理过程诸如癌症、高血压、肥胖、动脉硬化等的出现有关。已经确定了与上述代谢病理相关的另一种病理过程,并且它本身可以构成一种作为代谢综合征的新代谢病理。
[0228]
出于本发明的目的,赘生物被定义为当细胞增殖超过它们应有的或在适当的时间并未被破坏时出现的异常组织块。赘生物是良性的(非癌性的)或恶性的(癌性的)。术语“赘生物”相当于“肿瘤”。存在多种类型的癌症,包括例如口腔癌和咽癌、其他消化器官的癌症、其他呼吸器官的癌症、骨和关节软骨癌、黑素瘤和其他恶性皮肤赘生物、间皮癌和软组织癌、生殖器官的癌症、尿道癌、眼癌、脑癌和其他神经系统区域的癌症、甲状腺癌和其他内分
[0240]
(ii)
[0241]
和
[0242]-式(iii)的化合物,或者其营养学上可接受的盐或酯:
[0243]
cooh-(ch2)
a-(ch=ch-ch2)
m-(ch2)
3-(ch=ch-ch2)
(b-1-m)-(ch2)
c-ch3[0244]
(iii)
[0245]
其中所述组合物任选地包含式(i)的第二化合物,或者其营养学上可接受的盐或酯:
[0246]
cooh-choh-(ch2)
a-(ch=ch-ch2)
b-(ch2)
c-ch3[0247](i)[0248]
并且其中a是1至14的整数;b是1至7的整数;c是0至14的整数;m是0至(b
–
1)的整数;并且a 3b c 3是偶数整数;
[0249]
以及至少一种营养学上可接受的赋形剂。
[0250]
本发明还涉及一种营养组合物,其至少包含选自由以下各项组成的组的第一化合物:
[0251]-式(ii)的化合物的营养学上可接受的盐或酯:
[0252]
cooh-(ch2)
a-(ch=ch-ch2)
b-(ch2)
c-ch3[0253]
(ii)
[0254]
和
[0255]-式(iii)的化合物的营养学上可接受的盐或酯:
[0256]
cooh-(ch2)
a-(ch=ch-ch2)
m-(ch2)
3-(ch=ch-ch2)
(b-1-m)-(ch2)
c-ch3[0257]
(iii)
[0258]
其中所述组合物任选地包含式(i)的化合物的营养学上可接受的盐或酯:
[0259]
cooh-choh-(ch2)
a-(ch=ch-ch2)
b-(ch2)
c-ch3[0260](i)[0261]
并且其中a是1至14的整数;b是1至7的整数;c是0至14的整数;m是0至(b
–
1)的整数;并且a 3b c 3是偶数整数;
[0262]
以及至少一种营养学上可接受的赋形剂。
[0263]
本发明还涉及一种营养组合物,其至少包含选自由以下各项组成的组的第一化合物:式(ii)的化合物和式(iii)的化合物,或者其营养学上可接受的盐或酯,其中所述组合物任选地包含如上所述的式(i)的化合物,或者其营养学上可接受的盐或酯,其用于预防疾病或病理。
[0264]
另外,本发明还涉及一种预防疾病或病理的方法,所述方法包括向受试者施用有效量的营养组合物,所述营养组合物至少包含选自由以下各项组成的组的第一化合物:式(ii)的化合物和式(iii)的化合物,或者其营养学上可接受的盐或酯,所述组合物任选地包含如上所述的式(i)的化合物,或者其营养学上可接受的盐或酯。
[0265]
优选地,所述疾病或病理选自由以下各项组成的组:神经系统疾病或神经退行性疾病;癌症;赘生物;炎性疾病;心血管疾病;皮肤和皮下组织病理;代谢病理;神经性疼痛;瘫痪;睡眠障碍;消化病理;肌肉骨骼和结缔组织疾病;泌尿生殖系统病理;和代谢疾病。
[0266]
优选地m=0,并且本发明所公开的每一个实施方案(包括涉及式(ii)或式(iii)的
化合物、包含它们的药物组合物和营养组合物、它们的第一和第二医学用途、诱导神经再生和/或预防神经变性的方法或者预防和/或治疗疾病或病理的方法以及测定治疗功效的用途和体外方法的那些实施方案)涉及选自由以下各项组成的组的化合物:式(ii)的化合物,或者其药学或营养学上可接受的盐或酯:
[0267]
cooh-(ch2)
a-(ch=ch-ch2)
b-(ch2)
c-ch3[0268]
(ii)
[0269]
和式(iii)的化合物,或者其药学或营养学上可接受的盐或酯:
[0270]
cooh-(ch2)
a 3
‑‑
(ch=ch-ch2)
(b-1)-(ch2)
c-ch3[0271]
(iii)
[0272]
其中a是1至14的整数;b是1至7的整数;c是0、3或6;并且其中a 3b c 3是偶数整数。
[0273]
还优选地m=0,并且本发明所公开的每一个实施方案(包括涉及式(ii)或式(iii)的化合物、包含它们的药物组合物和营养组合物、它们的第一和第二医学用途、诱导神经再生和/或预防神经变性的方法或者预防和/或治疗疾病或病理的方法以及测定治疗功效的用途和体外方法的那些实施方案)涉及:式(ii)的化合物的药学或营养学上可接受的盐或酯:
[0274]
cooh-(ch2)
a-(ch=ch-ch2)
b-(ch2)
c-ch3[0275]
(ii)
[0276]
或者式(iii)的化合物的药学上可接受的盐或酯:
[0277]
cooh-(ch2)
a 3-(ch=ch-ch2)
(b-1)-(ch2)
c-ch3[0278]
(iii)
[0279]
其中a是1至14的整数;b是1至7的整数;c是0、3或6;并且其中a 3b c 3是偶数整数。
[0280]
仍更优选地m=0,并且本发明所公开的每一个实施方案(包括涉及式(ii)或式(iii)的化合物、包含它们的药物组合物和营养组合物、它们的第一和第二医学用途、诱导神经再生和/或预防神经变性的方法或者预防和/或治疗疾病或病理的方法以及测定治疗功效的用途和体外方法的那些实施方案)涉及选自由以下各项组成的组的化合物:
[0281]-式(ii)的化合物,或者其药学或营养学上可接受的盐或酯:
[0282]
cooh-(ch2)
a-(ch=ch-ch2)
b-(ch2)
c-ch3[0283]
(ii)
[0284]
其中:a=6、b=1并且c=6;或a=6、b=2并且c=3;或a=6、b=3并且c=0;或a=3、b=3并且c=3;或a=2、b=4并且c=3;或a=2、b=5并且c=0;
[0285]
和
[0286]-式(iii)的化合物,或者其药学或营养学上可接受的盐或酯:
[0287]
cooh-(ch2)
a 3-(ch=ch-ch2)
(b-1)-(ch2)
c-ch3[0288]
(iii)
[0289]
其中a=1、b=6并且c=0。
[0290]
还更优选地m=0,并且本发明所公开的每一个实施方案(包括涉及式(ii)或式(iii)的化合物、包含它们的药物组合物和营养组合物、它们的第一和第二医学用途、诱导
神经再生和/或预防神经变性的方法或者预防和/或治疗疾病或病理的方法以及测定治疗功效的用途和体外方法的那些实施方案)涉及选自由以下各项组成的组的化合物:
[0291]-式(ii)的化合物的药学或营养学上可接受的盐或酯:
[0292]
cooh-(ch2)
a-(ch=ch-ch2)
b-(ch2)
c-ch3[0293]
(ii)
[0294]
其中:a=6、b=1并且c=6;或a=6、b=2并且c=3;或a=6、b=3并且c=0;或a=3、b=3并且c=3;或a=2、b=4并且c=3;或a=2、b=5并且c=0;
[0295]
和
[0296]-式(iii)的化合物的药学或营养学上可接受的盐或酯:
[0297]
cooh-(ch2)
a 3-(ch=ch-ch2)
(b-1)-(ch2)
c-ch3[0298]
(iii)
[0299]
其中a=1、b=6并且c=0。
[0300]
仍更优选地,所述盐是钠盐,并且所述酯是乙酯。
[0301]
在本发明的一个实施方案中,本文所述的药物组合物和营养组合物包含浓度在0.01%至99.99%w/w的式(i)的化合物以及式(ii)的化合物或式(iii)的化合物,优选地组合物包含10%至80%w/w,或者甚至更优选地浓度在20%至80%w/w。在本发明的另一个实施方案中,本文所述的组合物包含式(i)的前药以及式(ii)的化合物或式(iii)的化合物,其中所述组合的比率在0.01:100至100:0.01、优选1:5至5:1并且最优选1:2至2:1的范围内。
[0302]
在另一个方面,本发明的药物组合物或营养组合物可以存在于小瓶、安瓿、散剂、胶囊、片剂、囊剂、溶液、糖浆、软膏、霜剂、乳剂、凝胶、贴剂、控释制剂、栓剂、胚珠剂(egg)等中。这些制剂可用于尤其通过口服、舌下、胃肠道、直肠、肠胃外(静脉内、动脉内、肌内和皮下)、呼吸道、局部(眼、耳、透皮)施用。施用途径可以由本领域技术人员以简单的方式确定。
[0303]
本发明的组合物可以为耐胃性(gastro-resistant)组合物的形式,以防止它们的组分因胃环境的低ph而降解。在某些实施方案中,本发明的组合物还包含一种或多种额外的组分或赋形剂,诸如稀释剂、抗氧化剂、甜味剂、胶凝剂、调味剂、填充剂或其他媒介物,诸如胶体无水二氧化硅和单硬脂酸甘油酯。所述组合物可以为胶囊、封袋(envelope)、纸或其他包装的形式。用于制备药物组合物的常规技术可以用于制备所述组合物。例如,上文公开的化合物可以与载体混合、或被载体稀释、或封闭在可以为安瓿、胶囊、封袋、纸或其他包装形式的载体内。当载体是稀释剂时,它可以是充当用于活性化合物的媒介物、赋形剂或介质的固体、半固体或液体材料。合适的稀释剂的一些实例是水、盐水溶液、醇、聚乙二醇、多羟基乙氧基化蓖麻油、花生油、橄榄油、乳糖、白土(terra alba)、蔗糖、环糊精、直链淀粉、硬脂酸镁、滑石、明胶、琼脂、果胶、阿拉伯胶、硬脂酸、纤维素烷基醚、硅酸、脂肪酸、脂肪酸胺、脂肪酸甘油单酯和甘油二酯、季戊四醇的脂肪酯、聚乙烯、羟甲基纤维素和聚乙烯吡咯烷酮。类似地,载体或稀释剂可以包括本领域已知的任何缓释材料,诸如单硬脂酸甘油酯或二硬脂酸甘油酯,单独地或与蜡混合。所述组合物还可以包括润湿剂、抗氧化剂、乳化剂和悬浮剂、防腐剂、甜味剂和调味剂。可以将本发明的组合物配制成在利用本领域熟知的方法施用至患者之后提供本文公开的化合物的快速、持续或延迟释放。
[0304]
所公开的组合物可以是固体组合物或液体溶液。在本发明的一个非限制性实施方
案中,所述组合物是固体组合物,其可以包含20-80%的式(i)的化合物和/或式(ii)或式(iii)的化合物、20-80%的稀释剂、0.1-20%的抗氧化剂、0.01-10%的甜味剂、0.1-20%的胶凝剂和0.01-10%的调味剂。在本发明的另一个非限制性实施方案中,所述组合物是用于口服施用的溶液,其包含20至80%的式(i)的化合物和/或式(ii)或式(iii)的化合物、20至80%的稀释剂、0.1至20%的抗氧化剂、0.01至10%的甜味剂、0.1至20%的胶凝剂和0.01至10%的调味剂。
[0305]
药物组合物可以进行灭菌,并且如果需要,可以与助剂、乳化剂、影响渗透压的盐、缓冲剂和/或着色物质等(它们不会与上面公开的化合物不利地反应)混合。
附图说明
[0306]
图1.a示出了2-羟基二十二碳六烯酸(dha-h)通过α-氧化产生(6z,9z,12z,15z,18z)-二十一碳-6,9,12,15,18-五烯酸(hpa)的细胞代谢的方案。dha-h在依赖于atp(三磷酸腺苷)和镁(mg
2
)的过程中需要由酰基-coa合成酶激活。dha-h-coa将经受2-羟基植烷酰基-coa裂解酶(2-羟基酰基-coa裂解酶1,hacl1)的活性影响,导致形成应含有5或6个双键的中间体多不饱和醛。hacl1的活性依赖于焦磷酸硫胺素(tpp)和mg
2
,并且可以被竞争性拮抗剂(例如羟基硫胺素)抑制。醛脱氢酶将负责在依赖于nad
(烟酰胺腺嘌呤二核苷酸)的过程中将中间体醛转化为hpa。b.dha-h在hek293t细胞中通过α-氧化而代谢地转化为hpa。纵坐标轴表示dha-h(b1和b3)和hpa(b2和b4)的细胞内水平(nmol/mg蛋白质),而横坐标轴表示利用dha-h钠盐持续24小时的处理浓度(μm)(b1和b2)或利用30μm恒定浓度的dha-h钠盐的温育时间(h)(b3和b4)(包括未处理的对照(c))。黑色柱表示在没有额外刺激的细胞中的结果,白色柱表示在同时用1mm羟基硫胺素处理后的结果,并且条纹柱表示在用10mm羟基硫胺素处理后的结果。dha-h和hpa均作为浓度和温育时间的函数而增加,其中从24小时开始,在30μm的dha-h钠盐暴露下,hpa水平显著高于dha-h水平。这种hpa的增加在10mm羟基硫胺素(其抑制hcla1酶)的存在下受到抑制,证实在这种代谢转化中涉及α-氧化。这些柱表示平均值
±
标准误差,并且统计分析利用单因素anova和tukey多重评价检验来进行:*p《0.05,当将hpa水平与dha-h水平在相同条件下进行比较时;#p《0.05,当比较在存在和不存在10mm羟基硫胺素的值时。c.在用dha-h钠盐处理后,hek293t中的dha(二十二碳六烯酸的非羟基天然形式)的内源性水平没有改变。纵坐标轴表示dha的细胞内水平(nmol/mg蛋白质),而横坐标轴表示利用dha-h钠盐持续24小时的处理浓度(μm)(c1)或利用30μm恒定浓度的dha-h钠盐的温育时间(c2)(包括未处理的对照(c))。作为浓度或温育时间的函数,利用dha-h钠盐的处理对dha水平没有任何显著影响。这些柱表示平均值
±
标准误差,并且统计分析采用单向anova和tukey多重评价检验进行。根据这些结果,可以得出的结论是,在这种情况下,dha-h或其钠盐的施用不会改变dha(二十二碳六烯酸)的内源性水平,也不会改变所研究的其他细胞脂肪酸的内源性水平,但是利用dha-h的处理仅导致hpa水平的增加,这意味着通过用dha-h处理并且特别是用其钠盐处理所获得的治疗作用是由hpa介导的,而不是通过调节内源性来源的其他脂肪酸的水平介导的。
[0307]
图2.a.用dha-h钠盐治疗的小鼠表现出剂量依赖性的hpa大脑累积,其中在大脑中检测不到dha-h。纵坐标轴表示相对于利用dha-h的钠盐(a1)和dha的钠盐(a1和a2)的治疗剂量(mg/kg)的hpa(a1)或dha(a2)的大脑水平(nmol/mg蛋白质)。a1:
●
动物wt;
○
5xfad。
a2:黑色柱指的是wt动物,而白色柱指的是5xfad。在慢性施用dha-h钠盐(4个月;5个剂量/周m-f;3至7月龄;在7个月时处死)后,在wt和5xfad小鼠的大脑中测定hpa和dha的水平。hpa在两种小鼠品系的大脑中类似地累积,这取决于所施用的dha-h钠盐的剂量(a1:
●
r2=0.9292,p=0.0002;
○
r2=0.9704,p《0.0001)。dha水平在实验条件之间没有显著差异(a2)。数据显示为平均值
±
标准误差,并且统计分析通过单向anova和tukey多重评价检验进行:*p《0.05,与对照(用媒介物治疗的小鼠)相比。因此,当在健康小鼠和阿尔茨海默病的转基因模型中施用前药dha-h,特别是其钠盐时,在大脑水平上发生hpa的显著累积,而没有检测到前药(dha-h)的存在,也没有dha的内源性水平的变化。b.用dha-h钠盐治疗的5xfad小鼠表现出与大脑hpa水平直接相关的认知改善。纵坐标轴表示已提交(committed)的总错误(b1)、参考记忆错误(rme)(b2)或工作记忆错误(wme)(b3)的数量,而横坐标轴表示hpa的大脑水平(nmol/mg蛋白质)。认知评估是通过在图2a中所示的相同动物的治疗的最后一个月期间测试8-臂径向迷宫来完成的。绘制了来自整个研究动物群体的个体实验点,并且将来自5xfad动物的数据调整为逆多项式回归f(x)=y0 (a/x)。与各个参数的回归对应的r2和p的值如下所示:总错误、rme和wme相对于hpa的大脑浓度:c1:r2=0.9146和p=0.0311;c2:r2=0.9252和p=0.0243;c3:r2=0.7785和p=0.0346。获得的数据表明,hpa大脑水平的最小增加与空间认知的改善有关。图中的每个点表示每种病理/治疗条件的平均值
±
标准误差:
●
wt 媒介物,
▼
wt dha-h 20mg/kg;
◆
wt dha-h 200mg/kg;
○
5xfad 媒介物;
△
5xfad dha-h 5mg/kg;
▽
5xfad dha-h 20mg/kg;
□
5xfad dha-h 50mg/kg;
◇
5xfad dha-h 200mg/kg。这些结果表明,大脑hpa水平的适度增加与空间认知的改善显著相关,而空间认知是阿尔茨海默病中受影响最大的认知能力之一。
[0308]
图3.a.用dha-h的钠盐治疗的小鼠在u118细胞异种肿瘤中表现出hpa的肿瘤累积(无法检测到dha-h)。纵坐标轴表示肿瘤中的dha(黑色柱)和hpa(白色柱)的水平(pmol/mg组织),而横坐标轴表示治疗条件(媒介物和dha-h 200mg/kg)。将处于3月龄的nude(免疫抑制)小鼠皮下注射7.5.106个u118细胞(iv级人多形胶质母细胞瘤)。在开始口服治疗(媒介物或dha-h钠盐200mg/kg)之前,在皮下水平允许肿瘤生长10天,其维持42天直至处死。异种肿瘤的脂质分析揭示了不存在dha-h(检测不到的水平)。这些柱表示每种治疗条件的平均值
±
标准误差。b.肿瘤hpa水平与异种模型中的肿瘤尺寸呈负相关。对于两种治疗条件:
○
媒介物和
●
dha-h的钠盐200mg/kg,纵坐标轴表示肿瘤的尺寸(cm3),而横坐标轴表示肿瘤中的hpa水平(pmol/mg组织)。在用dha-h钠盐治疗的动物的肿瘤中hpa的存在与肿瘤体积(a2)具有统计学显著的线性关系,其中:r2=0.4296并且p=0.0029。结果表明,异种肿瘤中的hpa水平与肿瘤尺寸具有统计学显著的负线性关系。在靶器官中不存在dha-h母体分子的情况下,这些证据表明靶器官中hpa的存在具有体内治疗作用。
[0309]
图4.a.dha-h是一种前药,其在u118细胞中通过α-氧化代谢地转化为hpa。纵坐标轴表示dha(黑色柱)、dha-h(白色柱)和hpa(条纹柱)的细胞内水平(nmol/mg蛋白质),而横坐标轴表示在存在或不存在用羟基硫胺素1mm和10mm的同时处理的情况下的处理条件:对照(c)和dha-h的钠盐150μm(48小时)。在用dha-h的钠盐处理的细胞中,dha-h和hpa二者都增加。这种hpa的增加在1mm和10mm羟基硫胺素的存在下受到抑制,证实在这种代谢转化中涉及α-氧化。这些柱表示平均值
±
标准误差,并且统计分析利用单向anova和tukey多重评价检验进行:*p《0.05,当仅比较hpa水平时。b.dha-h向hpa的代谢转化对于存在抗肿瘤作用
是必需的。纵坐标轴表示细胞活力(在没有羟基硫胺素的情况下,对照-c-的%),而横坐标轴表示在存在和不存在使用1mm羟基硫胺素的同时处理的情况下的处理条件:对照(c-黑色柱)和dha-h的钠盐150μm、48小时(白色柱)。用dha-h处理u118细胞显著降低了培养物的活力,而用羟基硫胺素(单独)的处理对细胞活力没有影响。然而,与没有羟基硫胺素的效果相比,当用dha-h的钠盐与羟基硫胺素同时进行处理时,这种化合物的抗增殖作用显著降低。这些柱表示平均值
±
标准误差,并且统计分析利用单向anova和tukey多重评价检验进行:*p《0.05,当与对照(c)相比时;#p《0.05,当与在存在和不存在羟基硫胺素的情况下的dha-h的作用相比时。
[0310]
图5.a.在用dha-h钠盐、dha钠盐和hpa处理后培养物中的u118细胞的活力。纵坐标轴表示细胞活力(未处理的对照的%),而横坐标轴表示不同的处理条件:对照(黑色柱)、dha-h钠盐(150μm,48小时-白色柱)、dha(150μm,48小时-条纹柱)和hpa(150μm,48小时-网格柱)。相比于由dha-h(前药)或dha(天然类似物)诱导的培养物死亡率,在相同条件下用hpa处理诱导更显著程度的培养物死亡率。这种作用可能是由于hpa典型的抗增殖作用和毒性作用的混合,这在相同实验条件下不可归因于dha-h或dha。这些柱表示平均值
±
标准误差,并且统计分析利用单向anova和tukey多重评价检验进行:*p《0.05,当与对照相比时。b.在用dha-h的钠盐和hpa处理的培养物中的u118细胞中的hpa的细胞内水平。纵坐标轴表示hpa的水平(nmol/mg蛋白质),而横坐标轴表示处理条件:dha-h的钠盐(150μm,48小时
–
黑色柱)和hpa(5-150μm,48小时
–
白色柱)。施用150μm的dha-h钠盐导致相当于通过在5μm下的hpa处理本身所产生的hpa水平的hpa水平。用150μm hpa处理导致hpa的细胞内水平显著高于通过相同浓度的前药施用所产生的hpa的细胞内水平。这些柱表示平均值
±
标准误差。
[0311]
c.在存在(c1)或不存在(c2)培养基的情况下hek293t细胞中的dha-h和dha的水平。纵坐标轴表示培养基中的dha-h(
●
)和dha(
○
)的水平(在时间0处的初始水平的%),而横坐标轴表示温育时间(h)。培养基中脂质的浓度为30μm,并且将培养板温育长达72h。在存在细胞培养物(c1)的情况下,由于通过细胞的dha摄取,培养基中的dha水平在48h和72h显著下降,而dha-h水平在长达72h内保持不变。在不存在细胞培养物(c2)的情况下,dha和dha-h二者的水平随时间保持恒定。这些柱表示平均值
±
标准误差,并且统计分析利用单向anova和tukey多重评价检验进行:*p《0.05,当与对照相比时。
[0312]
图6.a、b和c:在小鼠转基因模型(5xfad)中,用hpa酸或其前药dha-h的慢性治疗防止阿尔茨海默病的典型的认知衰退。认知评估通过8-臂径向迷宫测试进行。动物在3至7月龄接受治疗,并且在治疗的最后一个月期间进行测试。在这个测试期间,考虑了测试期间产生的总错误(a)、参考记忆错误(rme)(b)和工作记忆错误(wme)(c)。每个柱表示径向迷宫测试的最后一周期间的错误的平均值
±
sem。黑色柱表示wt小鼠所产生的错误。空白柱表示用媒介物(5%乙醇)治疗的5xfad转基因小鼠所产生的错误。条纹柱表示用dha-h(20mg/kg/天)治疗的5xfad小鼠所产生的错误。方格柱表示用hpa(20mg/kg/天)治疗的5xfad小鼠所产生的错误。结果显示出以类似方式用dha-h和hpa治疗的5xfad小鼠的认知改善。这些柱表示每种治疗条件的平均值
±
标准误差,并且统计分析通过单向anova和tukey多重评价检验进行:*p《0.05,当与健康对照(wt)相比时,并且#p《0.05,当与5xfad对照条件(用媒介物治疗)相比时。
[0313]
图7.a:在异种模型中,在存在用hpa钠盐或其前药dha-h的治疗的情况下,肿瘤生
长在体内受到抑制。纵坐标轴表示肿瘤的尺寸(cm3),而横坐标轴表示经过的治疗天数。为了在3月龄的nude(免疫抑制)小鼠中诱导异种肿瘤,在动物背侧胁(8-12周龄,30-35g)的两侧上皮下地接种7.5.106个人类iv级(u-118 mg)胶质母细胞瘤细胞。在10天后,肿瘤变得可见,具有的体积大约为0.1cm3。将动物随机分为具有相似平均肿瘤体积的组,并且接受42天的每日口服治疗:
○
媒介物(未治疗的对照)、dha-h
▲
(200mg/kg/天)和
■
hpa(200mg/kg/天)。肿瘤体积(v)计算为ν=a2×
l/2,其中a是肿瘤的宽度并且l是其长度。将对于每种治疗条件获得的数据调整为指数生长曲线。b:与未治疗的对照相比,hpa和前药dha-h显著减小异种肿瘤的体积。纵坐标轴表示在治疗开始后42天诱导的肿瘤体积,而横坐标轴表示治疗条件。呈现了参与研究的动物的个体化数据:
○
载体(未治疗的对照)、dha-h
▲
(200mg/kg/天)和
■
hpa(200mg/kg/天)。这些柱表示每种治疗条件的平均值
±
标准误差,并且统计分析通过单向anova和tukey多重评价检验进行:*p《0.05,当与对照条件相比时。
[0314]
图8. 2-羟基化多不饱和脂肪酸(前药,pufa-h)经由α-氧化产生其相应的非羟基化代谢产物的细胞代谢的示意性方案,所述非羟基化代谢产物比初始分子少一个碳原子。在依赖于atp(三磷酸腺苷)和镁(mg
2
)的过程中,羟基化脂肪酸需要通过酰基-coa合成酶的激活。这种pufa-h-coa将经受2-羟基酰基-coa裂解酶(hacl,同工型1或2,取决于细胞类型)的活性影响,这将导致中间体多不饱和醛的形成。hacl的活性依赖于焦磷酸硫胺素(tpp)和mg
2
,并且可以被竞争性拮抗剂(诸如羟基硫胺素)抑制。在依赖于nad
(烟酰胺腺嘌呤二核苷酸)的过程中,醛脱氢酶将负责中间体醛向最终脂肪酸的转化。a.2-羟基-亚油酸(la-h)产生(8z,11z)-十七碳-8,11-二烯酸(hda)的细胞转化的方案。b.2-羟基-α-亚麻酸(ala-h)到(8z,11z,14z)-十七碳-8,11,14-三烯酸(htaω-3)的细胞转化的方案。c.2-羟基-γ-亚麻酸(gla-h)产生(5z,8z,11z)-十七碳-5,8,11-三烯酸(hta ω-6)的细胞转化的方案。d.2-羟基-花生四烯酸(ara-h)产生(4z,7z,10z,13z)-十九碳-4,7,10,13-四烯酸(nta)的细胞转化的方案。e.2-羟基-二十碳五烯酸(epa-h)产生(4z,7z,10z,13z,16z)-十九碳-4,7,10,13,16-五烯酸(npa)的细胞转化的方案。f.2-羟基二十二碳六烯酸(dha-h)产生(6z,9z,12z,15z,18z)-二十一碳-6,9,12,15,18-五烯酸(hpa)的细胞转化的方案。
[0315]
图9.通过利用相应的前药处理hek293t细胞,通过带有火焰离子化检测器(gc-fid)的气相色谱法获得的不同色谱图的放大区域:a.(1)对照(媒介物)和(2)la-h(100μm,24h)。白色箭头表示la-h母体分子的色谱峰,黑色箭头表示对应于hda代谢产物的色谱峰。hda的形成在10mm羟基硫胺素的存在下受到抑制。b.(1)对照(媒介物)和(2)ala-h(100μm,24h)。白色箭头表示ala-h母体分子的色谱峰,黑色箭头表示对应于代谢产物hta ω-3的色谱峰。ω-3hta的形成在10mm羟基硫胺素的存在下受到抑制。c.(1)对照(媒介物)和(2)gla-h(100μm,24h)。白色箭头表示母体分子gla-h的色谱峰,黑色箭头表示对应于代谢产物hta ω-6的色谱峰。ω-6hta的形成在10mm羟基硫胺素的存在下受到抑制。d.(1)对照(媒介物)和(2)ara-h(100μm,24h)。白色箭头表示ara-h母体分子的色谱峰,黑色箭头表示对应于nta代谢产物的色谱峰。nta的形成在10mm羟基硫胺素的存在下受到抑制。e.(1)对照(媒介物)和(2)epa-h(100μm,24h)。白色箭头表示epa-h母体分子的色谱峰,黑色箭头表示对应于npa代谢产物的色谱峰。npa的形成在10mm羟基硫胺素的存在下受到抑制。f.(1)对照(媒介物)和(2)dha-h(100μm,24h)。白色箭头表示hpa母体分子的色谱峰,黑色箭头表示对应于hpa代谢产物的色谱峰。hpa的形成在10mm羟基硫胺素的存在下受到抑制。
[0316]
图10.用hpa和其他奇数链多不饱和脂肪酸处理防止兴奋性毒性诱导的神经元死亡。通过由视黄酸和bdnf(脑源性神经营养因子)从人sh-sy5y神经母细胞瘤的分化获得神经元培养物。通过向培养基中加入nmda(10mm)和钙/甘氨酸(530μm/10mm)来诱导经由兴奋性毒性的神经元死亡,持续1小时。为了测试不同研究化合物(hda或c17:2ω-6、htaω-3或c17:3ω-3、htaω-6或c17:3ω-6、nta或c19:4ω-6和hpa或c21:5ω-3)的神经保护作用,预处理进行24小时:媒介物(黑色柱)、1μm(白色柱)、3μm(点状柱)和10μm(条纹柱)。在这些实验条件下测试的处理证实,这些化合物可以从3μm浓度开始防止兴奋性毒性诱导的死亡。这些柱表示每种处理条件的平均值
±
标准误差,并且统计分析通过单向anova和tukey多重评价检验进行:*p《0.05,当与对照条件(媒介物预处理)相比时。
[0317]
图11.通过α-氧化产生8z-十七碳烯酸(c17:1n9)的2-ohoa(lam561)细胞代谢的示意性方案。2-ohoa在依赖于atp(三磷酸腺苷)和镁(mg2 )的过程中需要通过酰基-coa连接酶的激活。2ohoa-coa将会受到2-羟基植烷酰基-coa裂解酶(2-羟基酰基-coa裂解酶1,hacl1)的活性影响,导致形成中间体单不饱和醛。hacl1的活性依赖于焦磷酸硫胺素(tpp)和mg
2
,并且可以被竞争性拮抗剂(例如羟基硫胺素)抑制。在依赖于nad
(烟酰胺腺嘌呤二核苷酸)的过程中,醛脱氢酶将负责中间体醛到8z-十七碳烯酸的转化。
[0318]
图12.u-118 mg胶质瘤细胞中的脂肪酸的组成的分析。(a)代表性色谱图示出了通过气相色谱法测定的在存在400μm 2ohoa钠盐或不存在处理(对照)的情况下温育24小时的u-118 mg细胞中的脂肪酸的组成。保留时间(min):c17:1n-9(10.12),oa(13.01),2ohoa(16.87),以及作为内部对照的c17:0十七烷酸(10.81)。(b)在色谱图中鉴定的不同脂肪酸的定量(oa、2ohoa和c17:1n-9)。黑色柱对应于对照中的每种脂肪酸的浓度,并且白色柱对应于在用2ohoa钠盐处理后的脂肪酸的浓度。这些柱示出了三个独立实验的平均值
±
sem(以nmol表示,并且按每mg蛋白质标准化)。统计学显著性利用学生t检验确定(***p《0.001,相对于对照)。
[0319]
图13.在用2ohoa钠盐处理后的不同胶质瘤和非肿瘤细胞系中的脂肪酸组成的分析。代表性色谱图示出了通过气相色谱分析测定的,在不存在(对照)或存在2ohoa钠盐(400μm,24小时)的情况下处理之后,在胶质瘤细胞:(a)和(b)u-251 mg;(c)和(d)sf-295;和非肿瘤细胞:(e)和(f)mrc-5(人类成纤维细胞);(g)和(h)小鼠星形细胞中,在色谱图中鉴定的脂肪酸的组成(左)和不同脂肪酸的定量(c17:0、oa、2ohoa和c17:1n-9)(右)。黑色柱对应于对照中每种脂肪酸的浓度,并且白色柱对应于在用2ohoa钠盐处理后的脂肪酸浓度。包括c17:0十七烷酸作为内部对照。这些柱示出了三个独立实验的平均值
±
sem(以nmol表示,并且按每mg蛋白质标准化)。统计学显著性利用学生t检验确定(**p《0.01,***p《0.001,相对于对照)。
[0320]
图14. 2ohoa钠盐、oa和c17:1n-9钠盐对胶质瘤细胞的细胞活力和增殖的影响。用增加剂量的2ohoa(0-1000μm)钠盐(a1、b1和c1);oa(0-300μm)(a2、b2和c2);以及c17:1n-9(0-300μm)钠盐(a3、b3和c3)处理72小时的不同胶质瘤细胞系(a1-a3)u-118 mg;(b1-b3)u-251 mg;和(c1-c3)sf-295的活力曲线。活力通过结晶紫染色测定。每个值表示具有至少三个生物学重复的三个独立实验的平均值
±
sem(以相对于用媒介物处理的细胞(100%)的百分比表示)。
[0321]
图15. 2ohoa钠盐、c17:1n-9钠盐和oa对非肿瘤细胞的细胞活力和增殖的影响。用
增加剂量的2ohoa钠盐(0-1000μm)(a1和b1);oa(0-300μm)(a2和b2);以及c17:1n-9钠盐(0-300μm)(a3和b3)处理72小时的(a1-a3)mrc-5(人类成纤维细胞);以及(b1-b3)小鼠星形细胞的非肿瘤细胞活力曲线;活力通过结晶紫染色测定。每个值表示具有至少三个生物学重复的三个独立实验的平均值
±
sem(以相对于用载体处理的细胞(100%)的百分比表示)。
[0322]
图16.不同脂肪酸对不同细胞系中的增殖和死亡的标志物的影响的分析。免疫印迹呈现了在处理72h后,脂肪酸(200μm oa、200μm c17:1n-9钠盐和400μm 2ohoa钠盐)对涉及胶质瘤细胞:(a)u-118 mg;(b)u-251 mg;和(c)sf-295;以及非肿瘤细胞:(d)mrc-5(人类成纤维细胞);和(e)小鼠星形细胞中的2ohoa调节的细胞死亡和信号传导通路的多种蛋白质的影响。
[0323]
图17.在抑制α-氧化后在u-118 mg胶质瘤细胞中的脂肪酸组成的分析以及羟基硫胺素对u-118 mg胶质瘤细胞的细胞存活率的影响。(a)通过气相色谱法测定的,在用400μm 2ohoa处理24小时的、用增加剂量(1-10mm)的羟基硫胺素(α-氧化抑制剂)预温育90分钟的u-118 mg细胞中的2ohoa和c17:1n-9脂肪酸的定量。结果显示为三个独立实验的平均值
±
sem(以nmol表示,并且按每mg蛋白质标准化)。统计学显著性利用学生t检验确定(*p《0.05,***p《0.001,将2ohoa的量与在不存在羟基硫胺素的情况下在400μm的2ohoa后检测到的量进行比较;$$p《0.01,$$$p《0.001,将c17:1n-9的量与在不存在羟基硫胺素的情况下在400μm的2ohoa后形成的量进行比较)。(b)利用羟基硫胺素预温育(90分钟)并且在不存在(对照)或存在2ohoa钠盐(400μm,72小时)的情况下处理的u-118 mg细胞的活力(通过用台盼蓝的活体排除染色测定)。结果表示为三个独立实验的平均细胞计数
±
sem。统计学显著性利用学生t检验确定(***p《0.001,相对于不存在2ohoa和羟基硫胺素,对照-0;并且$$p《0.01,$$$p《0.001,相对于在没有利用羟基硫胺素预温育下用2ohoa的处理)。
[0324]
图18.代谢产物c17:1n-9对2ohoa的作用的影响。不同人类胶质瘤细胞系:(a)u-251 mg和(b)sf-295;和非肿瘤细胞:(c)人类mrc-5成纤维细胞和(d)小鼠星形细胞的活力;全部细胞系都在不存在或存在2ohoa钠盐(400μm,72小时)的情况下处理并且利用或没有利用羟基硫胺素预温育(90分钟)。通过用台盼蓝的活体排除染色来测定细胞活力。结果表示为三个独立实验的平均细胞计数
±
sem。统计学显著性利用学生t检验确定(**p《0.01和***p《0.001,相对于不存在2ohoa和羟基硫胺素;并且$p《0.05,相对于单独用2ohoa处理)。
[0325]
图19.通过经由羟基硫胺素抑制其形成,代谢产物c17:1n-9对2ohoa在不同细胞系中的增殖和死亡的标志物中的作用的分析。免疫印迹呈现了在处理7h后,与羟基硫胺素(2mm)组合或并未与其组合的2ohoa(400μm)对涉及胶质瘤细胞:(a)u-118 mg;(b)u-251 mg;和(c)sf-295;和非肿瘤细胞:(d)mrc-5(人类成纤维细胞);以及(e)小鼠星形细胞中的2ohoa调节的细胞死亡和信号传导通路的各种蛋白质的影响。
[0326]
图20.在用2ohoa钠盐处理24小时后的大鼠血浆中的脂肪酸组成的分析。(a)代表性色谱图示出了通过气相色谱法测定的在用2ohoa(2mg/kg,24小时)急性处理后的不同时间(0、1、2、3、4、6、8和24小时)处获得的大鼠血浆样品中的脂肪酸组成。c17:0十七烷酸在色谱图中作为内部对照进行定量。(b)在色谱图中鉴定的2ohoa和c17:1n-9脂肪酸的定量。结果显示为4只动物的平均值
±
sem,并且以nmol表示,并且按每ml血浆标准化。统计学显著性利用wilcoxon检验确定(*p《0.05和**p《0.01,相对于在0小时处的基线水平;$p《0.05和$$p《0.01,相对于2ohoa脂肪酸水平)。
十七碳-8,11-二烯酸)获自lipopharma therapeutics(西班牙)。十七烷酸(c17:0)购自sigma-aldrich并且二十一碳五烯酸(hpa游离酸;c21:5n-3)和(4z,7z,10z,13z,16z)-十九碳-4,7,10,13,16-五烯酸(npa游离酸;c19:5ω-3)购自cayman chemicals(michigan,美国)。d( )-葡萄糖(测试的细胞培养物)、丙酮酸钠、l-gln(测试的细胞培养物)、乙酰氯和n,o-双(三甲基甲硅烷基)乙酰胺、氯化钠、磷酸钠、edta(乙二胺四乙酸)和tris-碱购自sigma-aldrich。相比之下,氯仿、乙醇、甲醇、盐酸和己烷从scharlab(西班牙)获得。肝素(5000单位/ml)购自hospira invicta s.a.(西班牙),氯胺酮(anesketin 100mg/ml)购自eurovet animal health bv(荷兰),甲苯噻嗪(xilagesic 20mg/ml)购自laboratorios calier s.a.(西班牙),并且羟基硫胺素盐酸盐购自santa cruz biotechnology(德国)。
[0335]
对于hpa的制备,根据反应方案1,从(5z,8z,11z,14z,17z)-二十碳(eicose)-5,8,11,14,17-五烯酸(epa(c20:5,ω-3))进行化学合成。现有技术公开了hpa的化学合成(larsen等人,1997,lipids 32(7),707-714.doi:10.1007/s11745-997-0090-4)。反应在不存在光的情况下并且在氮气气氛中进行。
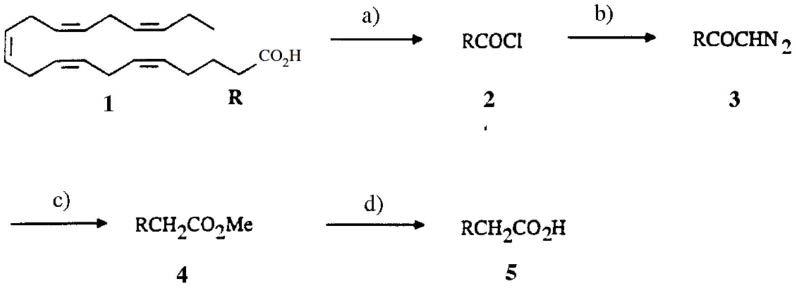
[0336][0337]
方案1
[0338]
试剂和条件:a)(cocl)2/phh 1.5h rt.,b)ch2n2/乙醚20min.0℃,c)agobz(cat.),et3n/thf/h2o
[0339]
本发明的hpa的钠盐的合成已由用编号5指定的化合物(当r是ch
3-ch
2-(ch=ch-ch2)
5-ch2ch
2-时)进行,所述化合物对应于hpa(c
21
)。所述盐在酸碱反应下获得,利用mtbe/hcl进行液-液萃取,并且利用naome调节ph从而以良好收率获得hpa的钠盐。通过调整起始底物,可以对hda、htaω-3、htaω-6、nta和npa的合成执行类似的程序。
[0340]
1.2.ohoa、oa和c17:1n-9
[0341]
脂质化合物2ohoa的钠盐、oa的钠盐和c17:1n-9的钠盐购自medalchemy,sl(西班牙)。
[0342]
wo1997049667公开了c17:1n-9的化学合成。在n2气氛下,在25℃,将8z-十七碳烯(66mg,0.26mmol,1当量)和2-甲基-2-丁烷(1.6ml,15.1mmol,58当量)在tbuoh(6.5ml)中的溶液通过滴加naclo2(80%,208mg,2.3mmol,9当量)和nah2po4.h2o(250mg,1.8mmol,7当量)在去离子水中的溶液(2.5ml)进行处理。将反应混合物再搅拌15分钟,然后在真空中浓缩。将剩余物用水(30ml)处理,并且将水层用etoac(3
×
30ml)萃取。将有机层用(na2so4)干燥,过滤,并且在真空中浓缩。色谱法(sio2,2
×
13cm,10-20%etoac-己烷梯度洗脱)得到27ml(66mg,95%),为透明油状物。本发明的c17:1n-9的钠盐的合成已由化合物c17:1n-9进行。所述盐在酸碱反应下获得,利用mtbe/hcl进行液-液萃取,并且用naome调节ph,从而以良好
收率获得c17:1n-9的钠盐。
[0343]
实施例2:具有dha-h和hpa的组合物
[0344]
不限制本发明范围的组合物的一些实施例在下文中一般性地描述。
[0345]
组分组成%w/w组成%w/w组成%w/wdha-h3.601.3hpa03.61.3dmso80.080.080.0水16.416.416.4总计100100100
[0346]
表1.示例性局部使用制剂
[0347][0348][0349]
表2.示例性口服制剂
[0350]
组分组成%w/whpa63.3甘油三酯25.5单硬脂酸甘油酯6.66香料(aroma)2.22超氧化物歧化酶1.11胶体二氧化硅1.11总计100
[0351]
表3.示例性口服制剂软胶囊
[0352]
实施例3:利用dha-h和hpa的细胞测定
[0353]
为了描述dha-h到hpa(c21:5ω-3)的代谢转化,以及la-h到hda(c17:2ω-6)、ala-h到htaω-3(c17:3ω-3)、gla-h到htaω-6(c17:3ω-6)、ara-h到nta(c19:4ω-6)、epa-h到npa(c19:5ω-3)的转化,采用hek293t(人胚肾细胞293t)细胞培养物,其是一种胚胎的非肿瘤细胞系,被广泛用于生理条件下的人代谢研究。
[0354]
将hek293t细胞在补充有10%fbs(胎牛血清;gibco,thermo-fisher)、2mm l-gln、25mm d( )-葡萄糖、1mm丙酮酸钠和青霉素/链霉素的达尔伯克改良伊格尔培养基(dmem;达尔伯克改良伊格尔培养基(dubelcco's modified eagle's medium),biowest,法国)中进行培养。将小鼠神经母细胞瘤n2a细胞维持在补充有5%fbs和青霉素/链霉素的dmem和
opti-mem(gibco,thermo-fisher)的1:1(v:v)混合物中。两种细胞系均在37℃在5%co2的气氛中进行温育。
[0355]
将hek293t细胞与dha-h和dha在10、30和100μm下温育24小时,并且在30μm下温育6、48和72小时。这些细胞还与la-h、ala-h、gla-h、ara-h和epa-h在100μm下温育24小时。hek293t细胞还在相同条件下在dha-h的存在下与羟基硫胺素在1和10mm的最终羟基硫胺素浓度下一起温育。使用冷磷酸盐缓冲盐水溶液(pbs),将hek293t细胞通过移液管与板分离。细胞通过离心(1000xg,4℃下10min)回收并且用冷pbs洗涤两次,然后在-80℃下冷冻。为了分析细胞培养基中的dha-h和dha水平,将90mm直径板在存在或不存在附着的hek293t细胞(5.105个细胞/板)的情况下用11ml的含有30μm dha-h或dha的完全细胞培养基填充。将这些板如上所述进行温育并且在0、6、24、48和72小时处收集板的1ml等分试样。将细胞培养基的等分试样立即在4℃下以1000xg离心10分钟以移除任何细胞悬浮液,并且将无细胞等分试样在-20℃下储存。
[0356]
u-118 mg、mia-paca 2和a549细胞系经由sigma-aldrich co(st louis,mo)从欧洲细胞培养物保藏中心(ecacc)获得,并且在37℃在5%co2气氛中维持在补充有10%fbs(gibco,thermo-fisher)的rpmi(roswell park memorial institute)培养基(u-118 mg和a549)或dmem(mia-paca 2)中。最终在存在或不存在羟基硫胺素(oxytymine)(1或10mm)的情况下,将u-118 mg、mia-paca 2和a549细胞在为获得表4的结果而进行的测定的描述中所描述的条件下进行处理。使用台盼蓝活体排除染色(scharlab)或通过细胞增殖试剂盒ii(roche)在b
ü
rker室中分析细胞存活率。简言之,在处理前24小时,将细胞以3
×
103个细胞/孔的密度接种在96孔板中,然后在存在或不存在目标化合物的情况下以图中所示的浓度和时间进行培养。在不同的时间后,根据制造商的说明,通过添加xtt来确定噬斑活细胞。将细胞在37℃在5%co2中温育,直到形成恒定颜色,并且使用参考波长为650nm的酶标仪(fluostar omega,bmg labtech,德国)在495nm处记录吸光度。
[0357]
将sh-sy5y人神经母细胞瘤细胞维持在补充有10%fbs(sigma)、青霉素/链霉素(paa)、非必需氨基酸(sigma)和2mm l-gln(sigma)的dmem-f12(invitrogen)中。按照标准程序进行这些细胞到神经元表型的分化。简言之,将细胞接种在用聚-l-赖氨酸预处理的板上,并且在24小时后,将培养基更换为补充有10μm视黄酸(sigma)的新鲜培养基。然后将细胞在黑暗中温育5天,并且将培养基更换为无血清培养基并且补充50ng/ml的人脑源性神经营养因子(hbdnf;alomone labs;tel aviv,以色列)。最后,将细胞温育6天以完成分化。将神经元用1.3和10μm的化合物hda、htaω-3、htaω-6、nta、npa和hpa处理24小时,然后在含有甘氨酸(530μm,sigma)和钙(10mm,sigma)的培养基中用nmda(n-甲基-d-天冬氨酸,10mm,sigma)诱导兴奋性毒性。
[0358]
与细胞培养物中的前药水平相比,用dha-h处理导致高hpa细胞水平(图1b)。在图1b中,在用dha-h的处理下在hek293t细胞中显示了dha-h和hpa的细胞内水平。两种化合物的累积作为处理浓度或温育时间的函数是明显的,但是从24小时温育和30μm处理开始,hpa水平显著高于前药的水平。hpa水平的增加在存在羟基硫胺素(一种2-羟基酰基-coa裂解酶的竞争性拮抗剂)的伴随治疗的情况下受到抑制(在1mm下部分抑制并且在10mm下几乎全部抑制)(参见图1a)。在这方面,还发现了dha(非羟基化天然形式)的内源性水平不会因利用dha-h的这种处理而改变(图1c)。
[0359]
类似地,图8示出了这种相同的代谢途径对用作前药的其他2-羟基化多不饱和脂肪酸诸如la-h、ala-h、gla-h、ara-h和epa-h是有效的,从而分别得到hda、htaω-3、hta ω-6、nta、npa(图9所示的色谱图)。所有这些代谢产物都显示出治疗活性,如下面的图10和表4所示:
[0360][0361]
表4.人胶质母细胞瘤(u118 mg)、胰腺癌(mia-paca 2)和人肺腺癌(a549)细胞系中的ic50值
[0362]
图8和9中描述的不同代谢产物的抗肿瘤活性是通过在肿瘤细胞培养物中用这些分子(hda或c17:2ω-6,hta ω-3或c17:3ω-3,hta ω-6或c17:3ω-6,nta或c19:4ω-6,npa或c19:5ω-3和hpa或c21:5ω-3)直接处理测定的,测定这些化合物中的每一种对肿瘤细胞培养物的ic50值(抑制浓度50:诱导50%的肿瘤细胞群死亡的研究化合物的浓度)。使用的细胞培养物对应于不同类型的癌症:u118-mg(人类iv级胶质母细胞瘤)、mia-paca 2(胰腺癌)和a549(小细胞肺腺癌)。不同的化合物显示出对不同肿瘤细胞系的可变ic50值,从而证实了它们中的一些对诱导某些类型的肿瘤细胞的选择性死亡的选择性。
[0363]
实施例4:使用dha-h和hpa的体内试验
[0364]
阿尔茨海默病的5xfad模型是一种双转基因ps1/app小鼠,其带有与家族性ad(tg6799系)相关的五种人类突变:app中的瑞典(k670n/m671l)、佛罗里达151(i716v)和伦敦(v717i);以及人类ps1中的临床突变m146l和l286v。两种转基因都在thy-1启动子的控制下表达,并且小鼠从4月龄时表现出认知减退(oackley等人,2006,neurosci 26(40),10129-10140.doi:10.1523/jneurosci.1202-06.2006)。5xfad转基因动物和野生型(wt)从jackson laboratories(usa)获得,并且通过将杂合转基因小鼠与b6/sjl wt(f1)繁殖体杂交而维持在b6/sjl遗传背景中。将动物以12h-12h明-暗循环在22℃(
±
2℃)的受控温度和70%的湿度下圈养,其中自由获得标准实验室饮食(panlab a03,barcelona,西班牙)。
[0365]
转基因雄性wt和5xfad小鼠以5、20、50和200mg/kg的每日剂量口服接受溶解在5%乙醇中的dha-h(或dha),或单独的媒介物。在另一方面,在独立的测定中,这些动物还已用hpa(20mg/kg)和dha-h(20g/kg)治疗,以比较两种化合物在这个模型中的效果。这些治疗在小鼠达到3月龄时开始(每周给药5天)并且持续直到7月龄。在治疗的最后一个月期间,将所有动物都保持在低热量饮食上,以进行选定的行为空间学习和记忆测试(径向臂迷宫)。总计46只动物用于图2所示的研究:用媒介物治疗的wt(n=3),用dha-h(20mg/kg,n=3;和200mg/kg,n=3)治疗的wt,用dha(20mg/kg,n=3)治疗的wt;用dha-h(5mg/kg,n=6;20mg/
kg,n=5;50mg/kg,n=6;和200mg/kg,n=7)治疗的5xfad(n=5),以及用dha治疗的5xfad(20mg/kg,n=5)。总计20只动物用于图6的研究:用媒介物治疗的wt(n=5),用媒介物治疗的5xfad(n=5),用dha-h(20mg/kg,n=5)和hpa(20mg/kg,n=5)治疗的5xfad。在行为测试后,将小鼠在正常饮食(和治疗)下再维持一周,之后将它们用氯胺酮/甲苯噻嗪(100/10mg/kg)的腹腔内注射进行麻醉,并且心内地输注50ml的肝素化盐水。立即取出动物大脑并且在冷表面上沿中线解剖。一旦小脑被移除,就将每个无小脑的一半在液氮中冷冻并且在-80℃下储存。在相对湿度为40-60%的无菌气流下并且在12-小时的暗/亮循环下,将nude(swiss)crl:nu(ico)-foxn1 nu
小鼠(8-12周龄,30-35g,charles river laboratories,paris,法国)保持在恒温柜(28℃,ehret,labor-u-pharmatechnik)中。它们的饮食由随意的具有饲料的标准饮食(labdiet 22%大鼠-小鼠繁殖,sodispan)组成。为了引起异种肿瘤,在动物背侧胁的两侧上皮下地接种7.5
×
106个u-118 mg细胞,并且在一周后,肿瘤变得可见,其体积大约为100mm3。将动物随机分为具有相似平均肿瘤体积的组,并且接受42天的每日口服治疗:媒介物、dha-h(200mg/kg)和hpa(200mg/kg)。图3的研究包括用媒介物治疗的动物(未治疗的对照;n=6)和用dha-h(200mg/kg;n=9)治疗的动物。图7示出了用媒介物治疗的动物(未治疗的对照;n=6)、用dha-h(200mg/kg;n=8)治疗的动物和用hpa(200mg/kg;n=8)治疗的动物。肿瘤体积(v)计算为ν=a2×
l/2,其中a是肿瘤的宽度并且l是其长度。在完成治疗后,将小鼠通过颈椎脱臼处死,并且将异种肿瘤解剖并且在液氮中和在-80℃下冷冻。使用的所有方案均由巴利阿里群岛大学生物伦理委员会(bioethics committee of the university of the balearic islands)批准,并且符合国家和国际动物福利准则。在健康小鼠和阿尔茨海默病的转基因模型(5xfad)的使用中,发现存在hpa在大脑水平上的显著累积,而无法检测到母体分子(dha-h),dha(非羟基化天然形式)的内源性水平也没有发生变化(图2a)。
[0366]
径向臂迷宫测试
[0367]
如上所述进行空间行为测试,其中进行了一些改进(fiol-deroque等人,2013,biogerontology 14(6),763-775.doi:10.1007/s10522-013-9461-4)。所有动物都被隔离并且经受热量限制到正常体重的80-85%,并且在这些条件下保持一周,然后开始测试并且直到测试结束。在饮食限制之后并且在试验开始前3天,动物每天在八臂径向迷宫测试(le766/8,panlab sl,西班牙)中训练两次,持续3天。将每只小鼠放置在迷宫的中心,并且允许寻找奖励,即位于每个臂末端处的45mg食物颗粒(dustless precision pellets,bio-serv,usa)。当动物设法找到八个准备好的臂或未能在10分钟内完成所有臂时,每次任务(session)结束。用数字视频跟踪系统(带有sedacomv1.3软件的le 8300,panlab,sl,西班牙)记录每只动物的活动,并且在训练之后,开始实验范式。在所有实验任务(每天1次任务)中,与训练方案相比,只准备了四个臂,并且当动物设法找到所有四个准备好的臂或在10分钟后未能找到时每次任务结束。考虑以下各项对性能进行评价:(1)执行测试的时间;(2)工作记忆错误(wme,重新进入之前访问过的准备好的臂)的数量;(3)参考记忆错误(rme,进入未准备好的臂)的数量;以及(4)错误的总数(wme rme)。测试每周重复5天,持续3周。在测试后,在屠宰前再随意饲喂动物一周。
[0368]
从这个意义上说,可以观察到在阿尔茨海默病模型小鼠中在大脑水平上的hpa水平与空间和联想记忆的评价测试(径向迷宫测试)中的行为参数具有统计学显著的反比关
系(图2b)。这些结果表明,大脑hpa水平的适度增加与空间认知的改善显著相关。同样,直接施用hpa与施用dha-h对所分析的相同行为参数的参数具有相似的影响(图6)。
[0369]
实施例5:涉及实施例3和4的脂质提取和脂肪酸转甲基化
[0370]
将以上实施例中使用的hek293t或u-118 mg细胞通过上下移液用冷低渗缓冲液(1mm edta,20mm tris-hcl[ph 7.4])裂解。在脂质提取之前,对细胞裂解物进行超声脉冲(4个循环,10s/循环,10w)。对于大脑分析,使用桨式匀浆器(polytron pt3100),在蛋白酶抑制剂(roche)的存在下,将每只动物的组织在冷pbs中以1:10(p:v)进行匀浆。将匀浆物进行超声处理,制成等分试样并且储存在-80℃。每个样品中只有一个等分试样(含有约8mg蛋白质/等分试样)经受脂质提取。通过改进的lowry方法(bio-rad dc蛋白质测定)来测定脂质提取前的蛋白质含量。
[0371]
将十七烷酸(c17:0)添加到经受脂质提取的样品中作为内标,并且用氯仿:甲醇提取脂质(eggers和schwudke,2016)。简言之,将0.75体积的水相(其已含有生物样品)与2体积的氯仿和1体积的甲醇混合。将该混合物涡旋1分钟并且以1000xg离心10分钟。将下层有机相收集并且用1ml的pbs:甲醇(1:1,v:v)洗涤,并且将所得的有机相在氩气流下干燥。在氩气气氛下,通过将脂质混合物在3ml的甲醇:乙酰氯(10:1,v:v)中在100℃温育90分钟,使含有提取的脂质的膜发生转甲基化(christie,1993)。将所得的脂肪酸甲酯(fame)用己烷萃取,向转甲基化反应中加入3ml的h2o和1ml的己烷,并且将混合物充分地涡旋。在室温下离心(1000
×
g,持续10分钟)后,收集含有fame的上层相,并且将剩余的体积用1ml的己烷洗涤两次。将己烷相合并,在氩气流下蒸发,并且重新悬浮于60μl的己烷(用于细胞样品、细胞培养基和血浆的分析)中或重新悬浮于200μl的己烷(用于大脑样品的分析)中。为了检查脂肪酸化合物是否被羟基化,将分离的fame用三甲基甲硅烷基进行第二次衍生化(alderson等人,2004,jbiol chem 279(47),48562-48568.doi:10.1074/jbc.m406649200)。简言之,将fame在氩气流下干燥,并且将脂质膜溶解在n,o-双(三甲基甲硅烷基)乙酰胺(0.1-5.0mg脂质,对于200-400μl三甲基甲硅烷基化试剂)中,然后将其在加盖的小瓶中在70℃加热30min。将溶剂蒸发并且将脂质膜重新悬浮在己烷中用于分析。当研究中的脂肪酸被羟基化时,fame的保留时间作为这种第二次衍生化的结果而发生变化。然而,如果研究中的脂肪酸没有被羟基化,则不管第二次衍生化如何,所得的fame都显示出相同的保留时间。
[0372]
在存在或不存在羟基硫胺素(α-氧化的竞争性抑制剂)的情况下,评价了在这些细胞中用前药dha-h的处理所产生的hpa水平(图4a)。结果表明,将dha-h添加到u-118 mg细胞培养物中导致hpa水平显著增加。这种增加在存在用1或10mm羟基硫胺素的同时处理的情况下受到抑制,从而证实dha-h到hpa的转化是由α-氧化介导的。用dha-h对培养物中的u-118 mg细胞进行处理对dha(非羟基化天然形式)的内源性水平没有影响。在培养物中的相同细胞上,在存在或不存在1mm羟基硫胺素的情况下用dha-h进行活力测定(图4b),证明了1mm羟基硫胺素对细胞活力没有影响。
[0373]
在另一方面,添加dha-h(150μm,48h)对u118-mg细胞呈现显著的抗增殖作用。然而,在1mm羟基硫胺素的存在下,这种作用部分地逆转(以统计学显著的方式)。此时,应该记住,这个浓度的羟基硫胺素足以完全抑制由dha-h引起的hpa水平的增加。然后这些结果表明,由dha-h介导的对u-118 mg细胞的抗增殖作用至少部分地是由hpa介导的,因为抑制由dha-h形成这种化合物会转化为较低的dha-h的抗增殖作用(图4b)。与施用dha-h前药和dha
的天然形式相比,还研究了hpa对u-118 mg细胞的培养物的抗增殖作用。相对于dha-h和dha,hpa对u-118 mg的抗增殖作用要高得多(参见图5a)。当与dha-h相比时,这种作用可以通过由dha-h和hpa诱导的hpa细胞内水平的差异来解释(参见图5b)。事实上,图5c示出了与非羟基化类似物相比,dha的羟基化形式的摄取被阻止。
[0374]
实施例6:利用2ohoa和c17:1n-9的体外测定
[0375]
下面描述的实验中使用的2ohoa钠盐的浓度以及处理的持续时间根据测定的类型而变化,为200μm或400μm和24或72小时。在一些实验系列中,c17:1n-9钠盐溶液以200μm的浓度使用,持续24或72小时。
[0376]
为了制备这些溶液,我们从100mm的储备等分试样开始。为了制备这个起始等分试样,在培养罩内将相应毫克的脂质化合物(粉末)溶解在无水乙醇和高压蒸汽处理的蒸馏水(体积1:1,通常制备1ml的等分试样,使得添加500μl乙醇和500μl水),将溶液在10分钟内引入在37℃的培养箱中,使得脂质化合物溶解,随后进行搅拌。
[0377]
6.1.2ohoa u-118 mg胶质瘤细胞和非肿瘤细胞的掺入和代谢
[0378]
为了确认2ohoa掺入到胶质瘤细胞膜并且确定在用2ohoa处理后脂肪酸谱是否发生变化,通过气相色谱法对在不存在(对照)或存在400μm 2ohoa钠盐的情况下温育24h的u-118 mg人胶质瘤细胞的总脂质进行分析。胶质瘤细胞中的脂肪酸水平的分析表明,相对于对照,在用2ohoa钠盐处理后的oa水平没有变化(图12)。此外,仅在经处理的细胞中,由于在色谱图中鉴定了一个峰,在处理24小时后观察到2ohoa的细胞掺入,这与其标准物对应。在另一方面,值得注意的是在经处理的细胞的色谱图中出现了一个几乎完全是新的峰。在经处理的细胞中检测到这个新峰的水平升高,其累积量几乎是2ohoa(10.81
±
0.34nmol/mg蛋白质)的两倍(19.71
±
0.39nmol/mg蛋白质)。在用于确定其身份的多个研究后,确认了这个新峰对应于顺式-8-十七碳烯脂肪酸(c17:1n-9)。c17:1n-9的形成是2ohoa的α-氧化的结果(图11)。
[0379]
6.2.在用2ohoa钠盐处理后在不同的胶质瘤和肿瘤细胞中的脂肪酸组成的分析
[0380]
通过气相色谱法,在不存在或存在2ohoa钠盐的钠盐(400μm,24小时)的情况下温育后,与非肿瘤细胞、人成纤维细胞(mrc-5)和小鼠星形细胞的原代培养物相比,分析了其他胶质瘤细胞系(u-251 mg和sf-295)中的脂质膜的脂肪酸组成。在所分析的任何细胞系中,在用2ohoa钠盐处理后,均未观察到oa的量的显著变化(图13)。然而,在用2ohoa处理24小时后,在其他胶质瘤细胞系和非肿瘤细胞中都观察到2ohoa的掺入以及代谢产物c17:1n-9的形成(图13)。代谢产物c17:1n-9的形成(由于2ohoa的掺入)在肿瘤细胞和非肿瘤细胞之间不同。胶质瘤细胞(u-251 mg和sf-295)显示出它们的c17:1n-9水平的显著增加;累积比2ohoa高97.42%和108.03%(分别为19.16
±
0.53相对于9.21
±
0.41nmol/mg和18.38
±
1.97相对于9.31
±
1.44nmol/mg)(图13b和13d,表5)。相比之下,在非肿瘤细胞中,检测到的2ohoa水平显著高于其代谢产物c17:1n-9的水平。与其代谢产物c17:1n-9相比,2ohoa在人mrc-5成纤维细胞中多累积46%(26.31
±
4.32相对于14.00
±
1.92nmol/mg)并且在小鼠星形细胞中多累积38.27%(12.28
±
0.90相对于7.58
±
0.70nmol/mg)(图13f和13h,表5)。
[0381][0382][0383]
表5:在用2ohoa处理后在不同的胶质瘤和非肿瘤细胞系中的脂肪酸2ohoa和c17:1n-9的水平。通过气相色谱法测定的,在用2ohoa(400μm,24小时)处理后,在不同的胶质瘤细胞系u-118 mg、u-251 mg和sf-295(上)以及非肿瘤mrc-5和星形细胞(下)中的2ohoa和c17:1n-9脂肪酸的定量值。结果对应于三个独立实验的平均值
±
sem(以nmol表示,并且按每mg蛋白质标准化)。
[0384]
6.3.2ohoa、c17:1n-9对胶质瘤细胞的细胞活力和增殖的影响
[0385]
为了评价c17:1n-9的抗增殖作用,测定了其ic
50
(对应于使体外细胞活力降低50%所需的化合物的量),以及其对涉及2ohoa的作用机制的蛋白质的调节的影响。为此,将胶质瘤细胞系(u-118 mg、u-251 mg和sf-295)和非肿瘤细胞系(mrc-5和星形细胞)用增加浓度的c17:1n-9、oa和2ohoa钠盐处理72小时。在处理完成后,通过结晶紫染色技术测定ic
50
。细胞活力测定的结果表明,在处理72小时后,三种化合物2ohoa、oa和c17:1n-9以浓度依赖性方式对所有测试的胶质瘤细胞均具有抗增殖作用。此外,在所研究的非肿瘤细胞mrc-5和星形细胞中,没有观察到2ohoa对其细胞活力的影响,但是oa和c17:1n-9脂肪酸确实对相同的非肿瘤细胞产生了抗增殖作用(图14和15)。在u-118 mg、u-251 mg和sf-295胶质瘤细胞中,2ohoa钠盐的ic
50
值分别为432.75
±
10.77、429.96
±
9.67和399.14
±
11.47μm(表6)。对于非肿瘤细胞mrc-5和星形细胞,2ohoa的ic
50
为1000μm。对于化合物c17:1n-9,在胶质瘤细胞u-118 mg、u-251 mg和sf-295中的ic
50
值分别为222.04
±
9.09、220.35
±
7.93和248.85
±
6.02μm。
[0386]
因此,c17:1n-9对胶质瘤和非肿瘤细胞都诱导了高度相似的抗增殖作用。同时,用2ohoa处理仅影响不同的胶质瘤细胞系的活力,而不影响非肿瘤细胞的活力。在u-118 mg、u-251 mg和sf-295胶质瘤细胞中,2ohoa的ic
50
值分别是代谢产物c17:1n-9的ic
50
值的1.90、1.95和1.60倍(表6)。此外,2ohoa的ic
50
值分别是其非羟基类似物oa的ic
50
值的1.92、1.80和1.56倍。c17:1n-9显示出更高的抗增殖效力的事实可能是由于它在细胞中的累积能力高于2ohoa。
[0387][0388]
表6.不同细胞系在用2ohoa、oa和c17:1n-9处理后的ic
50
值。胶质瘤细胞系(u-118 mg、u-251 mg和sf-295)和非肿瘤细胞(mrc-5和星形细胞)的ic
50
的总结,根据图16和17中获得的结果计算。获得的ic
50
值对应于三个独立实验的平均值,并且利用统计程序graphpad prism 6.0(s形模型)使用剂量-反应方程计算。
[0389]
6.4.不同脂肪酸对不同细胞系中的增殖和死亡标志物的影响的分析
[0390]
分析了代谢产物c17:1n-9对因2ohoa的影响而改变的不同信号传导通路的影响。为此,将不同的胶质瘤细胞系(u-118 mg、u-251 mg和sf-295)和非肿瘤细胞系(mrc-5和小鼠星形细胞)用接近每种化合物的ic
50
的剂量(200μm c17:1n.9,200μm oa或400μm 2ohoa)处理72小时,并且通过蛋白质印迹来分析它们对不同信号传导蛋白的影响。
[0391]
结果表明,用2ohoa处理提高了bip、chop和cjun磷酸化的水平,并且降低了akt的磷酸化和细胞周期蛋白d3水平。相反,用c17:1n-9处理不会在这些蛋白质中的任何一种中产生变化(图16)。这表明由代谢产物c17:1n-9诱导的死亡是经由不同于2ohoa的途径触发的。
[0392]
6.5.在抑制α-氧化后的u-118 mg胶质瘤细胞中的脂肪酸组成的分析以及羟基硫胺素对u-118 mg胶质瘤细胞的细胞存活率的影响的测定
[0393]
为了确认c17:1n-9酸由2ohoa通过α-氧化形成,使用了氯化羟基硫胺素,除了其他功能外,其抑制酶2-羟基植烷酰基-coa裂解酶(hacl1,α-氧化中的关键酶)。为此,首先将u-118 mg胶质瘤细胞与1或10mm羟基硫胺素一起预温育90分钟,然后用400μm的2ohoa钠盐处理24小时,并且通过气相色谱法分析脂肪酸。在通过气相色谱法检测的某些脂肪酸的分析中,相对于仅用2ohoa钠盐而没有用羟基硫胺素处理的细胞,在用羟基硫胺素预温育并且用2ohoa钠盐处理的u-118 mg胶质瘤细胞中观察到c17:1n-9的显著减少(图17a)。相对于在不存在羟基硫胺素的情况下在2ohoa处理的细胞中达到的代谢产物的量,这种减少在用1mm羟基硫胺素预温育后为51.35%(17.17
±
1.07到8.35
±
0.36nmol/mg蛋白质);并且在用10mm羟基硫胺素预温育后为58.45%(7.13
±
0.39nmol/蛋白质)。相比之下,与仅用2ohoa钠盐处理的那些细胞相比,在用2ohoa钠盐和高达3mm羟基硫胺素处理的细胞之间在2ohoa的量方面没有检测到显著差异(图17a)。然而,在用2ohoa钠盐和4mm羟基硫胺素处理的细胞中观察到2ohoa的量显著增加了12.33%(12.41
±
0.75到15.74
±
0.24nmol/蛋白质);并且在10mm羟基硫胺素的情况下为52.94%(18.98
±
0.42nmol/蛋白质)。因此,由于抑制α-氧化,羟基硫胺素抑制了c17:1n-9的形成,并且从4mm开始增加了2ohoa的量,从而确认了2ohoa到c17:1n-9的代谢途径。
[0394]
接下来,为了确定通过2ohoa的α-氧化的2ohoa代谢的抑制是否对细胞活力具有影响,通过使用台盼蓝的活体排除染色来研究在不存在或存在2ohoa(400mm,72小时)的情况下温育后以及以上述剂量用羟基硫胺素预温育的u-118 mg胶质瘤细胞的细胞存活率。羟基
硫胺素诱导了u-118 mg胶质瘤细胞的存活率的显著降低。详细地,在1mm下诱导了12.16
±
0.5%的死亡,在2mm下诱导了21.17
±
1.76%的死亡,直到在10mm羟基硫胺素下达到了27.13
±
0.41%的最大细胞存活率抑制(图7b)。这些结果确认了已知的羟基硫胺素的体外抗肿瘤作用。
[0395]
在另一方面,细胞用2ohoa钠盐温育诱导了24.71
±
1.88%的细胞死亡;并且在与1mm羟基硫胺素组合后,细胞活力恢复5%(20.94
±
1.97%的死亡);并且在2mm羟基硫胺素的情况下为17.26%(11.71
±
1.14%的死亡)(图17b)。
[0396]
鉴于图17a和b,观察到c17:1n-9的水平在羟基硫胺素的最低和最高浓度之间没有太大变化。这可以基于以下进行解释:在低浓度(1.2mm)下,羟基硫胺素本身的细胞毒性较小,但是其在减少c17:1n-9的产生方面的作用非常明显。在这些浓度下,我们看到了降低c17:1n-9水平的效果,但是在更高浓度的羟基硫胺素下,我们开始看到由羟基硫胺素本身产生的更大细胞毒性,这是看起来随着高浓度的2ohoa钠盐而被增强的效果。在高浓度下检测到更多累积的2ohoa,这表明2ohoa钠盐的施用本身也会产生细胞毒性,并且在这样的浓度下它会增加羟基硫胺素的细胞毒性作用。
[0397]
6.6.代谢产物c17:1n-9对2ohoa的作用的影响
[0398]
为了研究代谢产物c17:1n-9是否可以参与2ohoa的作用,研究了与羟基硫胺素的预温育对细胞存活率和2ohoa调节的蛋白质的影响。为此,通过对利用使用台盼蓝的活体排除染色的细胞进行计数,分析了用2ohoa(400μm,72小时)处理并且与2mm羟基硫胺素预温育(90分钟)或未与其预温育的不同胶质瘤和非肿瘤细胞系的细胞存活率。此外,还研究了2ohoa调节的蛋白质(蛋白质印迹)。在胶质瘤细胞中,在与2mm羟基硫胺素温育72小时后观察到细胞存活率的显著降低。羟基硫胺素在u-251 mg和sf-295细胞中分别诱导18.51
±
0.58%和17.35
±
0.63%的细胞死亡(图18a和18b)。这些结果支持羟基硫胺素对胶质瘤细胞的体外抗肿瘤作用。用2ohoa处理细胞分别在u-251 mg和sf-295中诱导23.22
±
1.32%和23.97
±
1.25%的细胞死亡。在与2mm羟基硫胺素组合后,在细胞活力方面存在显著恢复,在u-251 mg细胞中为12%(14.07
±
1.62%的死亡)并且在sf-295细胞中为17.25%(10.85
±
0.58%的死亡)。相比之下,在非肿瘤细胞中,所测试的处理均未对细胞存活率产生影响(图18c和18d)。
[0399]
对于涉及胶质瘤细胞中的不同信号传导通路和细胞死亡的蛋白质的研究,羟基硫胺素对胶质瘤细胞中bip、chop、c-jun磷酸化、akt磷酸化和d3细胞周期蛋白的水平的影响程度与2ohoa相同,尽管较温和(图19),但是当组合时,由2ohoa诱导的调节受到抑制。这一事实证实了,2ohoa在c17:1n-9方面的代谢是增强其抗肿瘤作用所必需的。相反,在任何处理之后都未观察到非肿瘤细胞系中这样的信号传导蛋白的变化(图19)。虽然2ohoa在其在c17:1n-9方面的代谢受到抑制时具有抗增殖活性,但是代谢产物c17:1n-9的形成对2ohoa的作用机制有很大影响,从而增强其抗增殖作用,并且证实了2ohoa也是产生活性代谢产物17:1n-9的前药。
[0400]
实施例7:利用2ohoa和c17:1n-9的体内试验
[0401]
7.1在用2ohoa处理24小时后大鼠血浆中的脂肪酸组成的分析
[0402]
研究了2ohoa及其代谢产物c17:1n-9在动物血浆中的药代动力学特性(profile)。在这种情况下,大鼠用作实验的动物模型。大鼠比小鼠具有更大的体积,并且是用于研究临
床前研究中定义的持续施用最大耐受剂量的2ohoa(2g/kg)的效果的最合适模型。
[0403]
对于本研究,向12-14周龄的大鼠口服施用2g的2ohoa/kg钠盐,持续15天。随后,在从第1天(急性治疗)和第15天(慢性治疗)的不同时间(0、1、2、3、4、6、8和24小时)处提取血浆样品。最后,通过气相色谱法分析血浆样品中的脂肪酸谱。在分析色谱图后,在急性治疗(第一天施用)后收集的血浆样品中检测到的2ohoa和c17:1n-9脂肪酸是明显的(图20a)。
[0404]
两种化合物2ohoa和c17:1n-9在急性治疗后的大鼠血浆中显示出非常相似的药代动力学特性(图20b)。观察到2ohoa和c17:1n-9水平的显著增加,在施用2ohoa的2小时处达到最大血浆浓度(26.23
±
5.79nmol2ohoa/ml血浆和60.47
±
6.53nmol c17:1n-9/ml血浆)。随后血浆2ohoa和c17:1n-9水平下降,在24小时处达到谷值(分别为2.80
±
0.69和14.03
±
2.20nmol/ml血浆)。然而,尤其是在c17:1n-9的情况下,没有达到初始水平(分别为1.22
±
0.33和8.45
±
2.52nmol/ml血浆)。慢性治疗后的c17:1n-9代谢产物的水平高于2ohoa的水平(图21b)。在施用2ohoa前(0小时;1.22
±
0.33nmol 2ohoa/ml血浆,相对于8.45
±
2.52nmol c17:1n-9/血浆)、在8小时后(7.12
±
1.56nmol 2ohoa/ml血浆,相对于23.31
±
5.18nmol c17:1n-9/血浆)和在24小时处(2.80
±
0.69nmol 2ohoa/ml血浆,相对于14.03
±
2.21nmol c17:1n-9/血浆),两种化合物之间的差异是显著的。
[0405]
7.2.免疫抑制小鼠的异种肿瘤的脂肪酸的组成分析
[0406]
为了研究作为2ohoa通过α-氧化代谢的产物的c17:1n-9的形成在动物模型中的作用,在免疫抑制小鼠的异种肿瘤的模型中检测和分析了代谢产物c17:1n-9的水平(与2ohoa的水平相比)。为此,将u-118 mg成胶质细胞瘤细胞注射到免疫抑制小鼠中,并且在一周后,开始口服且每天地用媒介物或2ohoa钠盐(200mg/kg)治疗小鼠,持续42天。在治疗完成后,将小鼠安乐死并且移除肿瘤,对于2ohoa和c17:1n-9脂肪酸通过气相色谱法处理脂质。在用这种化合物治疗的小鼠的异种肿瘤中未检测到脂肪酸2ohoa,因为没有观察到对应于2ohoa的保留时间中的峰(图22a)。相比之下,在用2ohoa治疗的小鼠的肿瘤中检测到2ohoa的代谢产物c17:1n-9脂肪酸(0.25
±
0.04nmol c17:1n-9/g组织)(图22b)。
[0407]
7.3.在肿瘤的体积与代谢产物c17:1n-9的量之间的相关性
[0408]
研究了在肿瘤中存在的c17:1n-9代谢产物的水平相对于肿瘤的体积之间的可能相关性,作为在2ohoa的掺入和代谢与化合物在肿瘤中的功效之间的关系的指示。在获得的图表中,观察到在肿瘤中存在的c17:1n-9的量与肿瘤的体积之间存在负相关性(图23)。对于用2ohoa治疗的小鼠的肿瘤,在c17:1n-9的量和肿瘤体积之间获得了-0.8248的决定系数r和0.0001的p-值。换言之,肿瘤的体积越小,在其中检测到的c17:1n-9代谢产物就越多。这些结果表明代谢产物c17:1n-9具有显著的抗肿瘤活性,并且2ohoa是这种化合物的有效前药。
[0409]
7.4.在用2ohoa治疗后的患有晚期胶质瘤的人类患者中的脂肪酸组成分析
[0410]
在来自8名患者的血浆样品中对2ohoa和c17:1n-9脂肪酸进行检测和定量,这些患者在2ohoa(min-001-1203)的临床i/iia期中对利用12g/天的2ohoa钠盐持续至少一个3-周周期的治疗有反应或无反应。血浆样品在不同时间(在用2ohoa治疗后0、2、4、6、8小时以及8、15、21和28天后)处获得,并且随后使用气相色谱技术进行脂肪酸分析。
[0411]
在色谱图中,在来自所分析的患者的所有血浆样品中检测到2ohoa及其c17:1n-9代谢产物(图24a)。在所有患者(表现出临床反应的那些患者(有反应者)和不表现出临床反
应的那些患者(无反应者)二者)中观察到非常相似的药代动力学特性(图24b)。两种化合物均在2ohoa施用4小时时达到峰值水平。分析所有患者(有反应者和无反应者)的结果,在第一次摄入药物后4小时获得53.08
±
6.52nmol的2ohoa/ml血浆的值和122.80
±
10.61nmol的c17:1n-9/ml血浆的值(图24c)。随后,2ohoa和c17:1n-9的水平逐渐下降,直到治疗后8小时(分别为25.39
±
3.99和92.89
±
9.39nmol/ml血浆)。在治疗8天(192小时)时,观察到两种血浆化合物的量显著增加,192小时(25.39
±
3.99nmol/ml 2ohoa血浆和141.10
±
16.35nmol/ml c17:1n-9血浆)。化合物2ohoa和c17:1n-9在患者血浆中随时间累积,如在用2ohoa治疗15天(360小时)后观察到的(分别为184.70
±
25.60和366.9
±
72.47nmol/ml 2ohoa和c17:1n.9血浆)(图24c)。
[0412]
应注意的是,与细胞和动物中发生的情况类似,所有患者的血浆中的代谢产物c17:1n-9的水平均高于2ohoa的水平(图14b),在施用2ohoa 8小时后显著更高(图24c)。在已用2ohoa治疗8天和15天的患者中,观察到c17:1n-9水平分别是2ohoa的3.66倍和2.20倍(分别为92.89
±
9.39和311.10
±
37.38nmol c17:1n-9/ml血浆,与25.39
±
3.99和141.10
±
16.35nmol 2ohoa/ml血浆相比)。最后,在用2ohoa治疗21天时,c17:1n-9水平为2ohoa的1.90倍(分别为366.9
±
72.47nmol c17:1n-9/ml血浆,与184.70
±
25.60nmol 2ohoa/ml血浆相比)。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。