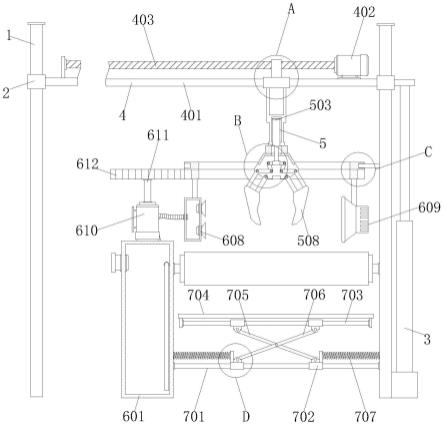
1.本发明属于生物医药技术领域,具体涉及紫云英苷在制备抗流感病毒药物中的应用。
背景技术:
2.流感(influenza)是由流感病毒(influenza virus)引起的急性呼吸道传染病,具有感染宿主广泛、传播迅速、致病率高等特点。其中甲型流感病毒容易引发流感大流行,对人类和动物的生命健康造成了严重的威胁。疫苗是预防流感的主要策略,但流感病毒的高度变异,疫苗研发的滞后性以及对不同流感毒株不能产生交叉保护作用等缺陷限制了疫苗的有效使用,抗流感病毒药物则成为流感病毒防控的又一重要手段。
3.目前,临床上可用的抗流感病毒药物包括m2离子通道抑制剂(如,金刚烷胺(amantadine)、金刚乙胺(rimantadine)和金刚烷衍生物(adamantane derivative)、神经氨酸酶抑制剂(如,奥司他韦(oseltamivir)、帕拉米韦(palamivir))和扎那米韦(zanamivir))以及rna依赖性rna聚合酶(rna-dependent rna polymerase,rdrp)抑制剂(如,法匹拉韦(favipiravir)和巴洛沙韦(baloxavir))。m2离子通道抑制剂因多年使用已造成临床流行毒株对其耐药,神经氨酸酶抑制剂的耐药毒株也在日益增加。因此,迫切需要开发更多的新型高效抗流感病毒药物来应对流感疫情。
[0004]“老药新用”策略为开发新的药物节约了大量时间和资源成本。从已有小分子化合物中,筛选可能的抗病毒药物成分并完成体外抗病毒药物效果的验证,对于治疗病毒感染性疾病方面具有明显的优势和广阔的发展前景,由于其毒性较低,副作用较小,有着较为广泛的临床适用性。
[0005]
紫云英苷,英文名为astragalin,又称黄芪苷、山奈酚-3-o-葡萄糖苷或者山奈酚-3-o-β-d-葡萄糖苷,是一种存在于黄芪等多种传统中草药中的天然黄酮类化合物。研究表明,紫云英苷具有抗炎、抗氧化、抗病毒、镇痛、抗菌和抗过敏等作用,并能增强机体抵抗力、刺激干扰素的产生、抗心律失常、扩张血管和保护心肌等作用。因此受到广泛关注。但有关紫云英苷抗流感病毒的研究尚未见报道。
技术实现要素:
[0006]
有鉴于此,本发明的目的在于提供紫云英苷在制备抗流感病毒药物中的应用,紫云英苷能在体外显著抑制甲型流感病毒a/puerto rico/8/1934(h1n1)的复制增殖,具有良好的体外抗流感病毒活性。
[0007]
本发明提供了紫云英苷在制备抗流感病毒药物中的应用。
[0008]
优选的,所述抗流感病毒包括抑制流感病毒的复制增殖。
[0009]
优选的,所述流感病毒包括甲型流感病毒。
[0010]
优选的,所述甲型流感病毒包括甲型流感病毒h1n1。
[0011]
优选的,所述紫云英苷为所述药物中的唯一活性成分。
[0012]
本发明还提供了紫云英苷在制备预防和/或治疗流感的药物中的应用。
[0013]
优选的,所述流感包括甲型流感。
[0014]
优选的,所述甲型流感包括甲型流感病毒h1n1引起的甲型流感。
[0015]
优选的,所述紫云英苷为所述药物中的唯一活性成分。
[0016]
本发明提供了紫云英苷在制备抗流感病毒药物中的应用。本发明采用甲型流感病毒h1n1作为模式病毒,使用空斑抑制实验在mdck细胞上评价了紫云英苷的体外抗流感病毒药效学,探讨了紫云英苷在制备抗流感病毒药物中的可能性,发现紫云英苷能在体外显著抑制甲型流感病毒a/puerto rico/8/1934(h1n1)的复制增殖,具有良好的体外抗流感病毒活性,为进一步开发广谱抗流感病毒的药物奠定了基础,具有重要的开发价值和推广意义。
附图说明
[0017]
图1为紫云英苷的化学分子结构示意图;
[0018]
图2为紫云英苷的细胞毒性检测结果;曲线图为不同浓度紫云英苷作用下的mdck细胞活性情况拟合曲线,横坐标为紫云英苷的药物浓度,纵坐标为细胞存活率,结果显示,紫云英苷在mdck细胞中产生的药物50%细胞毒性浓度(halfcytotoxic concentration,cc
50
)为1176μg/ml,具有良好的安全性。
[0019]
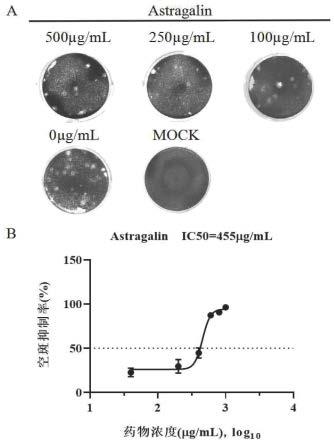
图3为不同浓度紫云英苷对流感病毒病毒a/puerto rico/8/1934(h1n1)的抗病毒效果;其中,a为不同浓度紫云英苷对a/puerto rico/8/1934(h1n1)病毒复制的空斑抑制结果示意图;b为不同浓度紫云英苷在mdck细胞中对a/puerto rico/8/1934(h1n1)病毒复制的抑制效果拟合曲线图。横坐标为紫云英苷的药物浓度,纵坐标为空斑抑制率,其中方框深色点拟合的曲线表示对0.0004moi剂量的流感病毒a/puerto rico/8/1934(h1n1)空斑点数的抑制效率;结果显示,紫云英苷在mdck细胞中可有效抑制a/puerto rico/8/1934(h1n1)的病毒复制,使用moi=0.0004剂量的流感病毒a/puerto rico/8/1934(h1n1)病毒复制效率受到50%抑制的药物有效浓度ic
50
为455μg/ml。
具体实施方式
[0020]
本发明提供了紫云英苷在制备抗流感病毒药物中的应用。
[0021]
在本发明中,所述抗流感病毒优选的包括抑制流感病毒的复制增殖。紫云英苷在mdck细胞中抑制流感病毒a/puerto rico/8/1934(h1n1)的ic
50
为455μg/ml。
[0022]
在本发明中,所述流感病毒优选的包括甲型流感病毒;所述甲型流感病毒优选的包括甲型流感病毒h1n1。
[0023]
在本发明中,所述紫云英苷优选的为所述药物中的唯一活性成分。
[0024]
本发明还提供了紫云英苷在制备预防和/或治疗流感的药物中的应用。
[0025]
在本发明中,所述流感优选的包括甲型流感;所述甲型流感优选的包括甲型流感病毒h1n1引起的甲型流感。
[0026]
在本发明中,所述紫云英苷优选的为所述药物中的唯一活性成分。
[0027]
在本发明中,所述紫云英苷的化学分子结构示如图1所示。
[0028]
下面结合具体的实施例对本发明做进一步的详细说明,所述是对本发明的解释而不是限定。以下实施例中未注明具体条件的实验方法,通常按照常规条件如《分子克隆实验
指南》(第三版,科学出版社,2005)等本领域常用工具书中所述的条件,或按试剂生产厂家所建议的条件进行。
[0029]
实施例1:cck-8法检测紫云英苷的细胞毒性检测
[0030]
本发明中涉及的流感病毒的敏感细胞系为mdck细胞,为测试紫云英苷的安全用药浓度,本实施例使用cck-8法检测了紫云英苷在敏感细胞系mdck中的毒性。
[0031]
首先制备紫云英苷储存液,用1ml dmso溶液溶解25mg紫云英苷颗粒,配制成终浓度为25mg/ml的溶液,待完全溶解后,0.22μm过滤,置于4℃冰箱保存。之后,将mdck细胞按照3
×
104细胞/孔接种100μl于96孔培养板,37℃,5%co2孵箱培养24h;使用含1%终浓度的青链霉素、2μg/ml终浓度的tpck-胰蛋白酶、2%牛血清白蛋白组分v的dmem培养基作为维持液稀释药物,以2000μg/ml作为紫云英苷的最高起始浓度,依次进行二倍比稀释成梯度浓度的药物工作液。pbs洗细胞2遍后,吸取不同浓度药物各100μl/孔加入96孔细胞板,每个浓度设6个重复孔,于37℃,5%co2孵箱继续培养48~72h。培养结束后,每孔加入10μl cck-8溶液,将细胞板置于37℃、5%co2培养箱中孵育1~4h,使用酶标仪记录450nm处的吸光度,各浓度吸光值都需与阴性对照(0μm)和正常细胞对照做比较。根据公式计算:细胞存活率(%)=(实验孔吸光值-空白孔吸光值)/(细胞对照孔吸光值-空白孔吸光值)
×
100%。通过graphpad prism 8.0软件计算平均值和标准差拟合曲线作图,将药物浓度转换为对数值后计算紫云英苷的细胞毒性cc
50
。结果如图2拟合曲线所示,紫云英苷在mdck胞中的cc
50
为1176μg/ml,该结果提示,紫云英苷在细胞中的毒性小,安全性良好。
[0032]
实施例2:空斑抑制法测定紫云英苷的体外抗流感病毒活性效果
[0033]
2.1空斑法测定流感病毒a/puerto rico/8/1934(h1n1)的滴度
[0034]
先配制微晶纤维素(avicel)储存液,称取2.4gavicel粉末溶于100ml蒸馏水中,用磁力搅拌器搅拌1h后,121℃高压灭菌30min,室温储存备用;使用2
×
dmem高糖培养基配制1.2%浓度的avicel,并加入终浓度2μg/ml的tpck-胰蛋白酶作为覆盖层。将mdck细胞按照2.5
×
105细胞/孔接种1.5ml于12孔培养板中,使用含10%胎牛血清的dmem培养于37℃,5%co2孵箱培养24h;次日,使用含1%终浓度的青链霉素、2μg/ml终浓度的tpck-胰蛋白酶、2%牛血清白蛋白组分v的dmem培养基作为维持液稀释病毒;弃掉12孔细胞板中的细胞生长液,吸取pbs溶液洗板2遍;每孔加入稀释好的不同感染指数(multiplicity of infection,moi)剂量病毒400μl,每个稀释度3个重复孔,35℃,5%co2培养箱孵育1h;之后,吸弃病毒液,加1.2%浓度的avicel覆盖层1.5ml,于35℃,5%co2孵箱中继续培养48h。最后,弃去覆盖层,吸取4℃预冷的4%多聚甲醛固定细胞,40min后弃掉固定液,用pbs洗2遍,使用1%结晶紫溶液400μl/孔在室温进行染色,10min后甩去结晶紫,用慢速自来水冲洗,自然晾干后进行空斑计数,细胞瓶内圆形不着色的透明区即为一个空斑单位,选择空斑数量合适、易于区分的稀释度进行计数。空斑形成单位(pfu/ml)=每孔平均空斑数/每孔病毒接种量(ml)
×
病毒稀释度。
[0035]
2.2病毒感染与药物作用
[0036]
将mdck细胞按照2.5
×
105细胞/孔接种1.5ml于12孔培养板中,使用含10%胎牛血清的dmem培养于37℃,5%co2孵箱培养24h;次日,使用病毒感染复数为0.0004moi感染剂量的流感病毒a/puertorico/8/1934(h1n1),400μl/孔感染mdck细胞,35℃,5%co2培养箱吸附1h;期间,使用等体积的2
×
dmem高糖培养基与浓度为2.4%的avicel贮存液配制成浓度
为1.2%的avicel,并加入终浓度2μg/ml的tpck-胰蛋白酶作为覆盖液,使用含1.2%浓度的avicel覆盖液配制不同浓度的紫云英苷,以1000μg/ml作为起始浓度,设置终浓度分别为1000、600、200和0μg/ml的系列浓度的药物,同时设置相应不加药物的细胞对照孔和仅加病毒的病毒对照孔;在流感病毒吸附后,加入含有不同药物浓度的avicel覆盖层1.5ml/孔,35℃,5%co2培养箱48h,之后,吸弃除avicel-药物覆盖层,每孔加入4%多聚甲醛1ml进行固定;弃液固定液后,加入1%浓度的结晶紫400μl/孔进行染色,10min后甩去结晶紫,用慢速自来水冲洗,自然晾干后进行空斑计数,结果如图3中的a所示。
[0037]
根据公式进行计算,空斑抑制率(%)=(病毒对照孔空斑数-实验孔空斑数)/病毒对照孔空斑数
×
100%,将不同浓度下获得的空斑抑制率结果使用graphpad prism 8.0软件计算平均值和标准差拟合曲线作图,得到紫云英苷抗流感病毒作用的拟合曲线,结果如图3中的b所示,紫云英苷在mdck细胞中抑制流感病毒a/puerto rico/8/1934(h1n1)的ic
50
为455μg/ml。
[0038]
尽管上述实施例对本发明做出了详尽的描述,但它仅仅是本发明一部分实施例而不是全部实施例,人们还可以根据本实施例在不经创造性前提下获得其他实施例,这些实施例都属于本发明保护范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。