一种pd-l1调控剂及其应用
技术领域
1.本发明涉及能够抑制pd-l1的调控剂及其在肿瘤治疗中的应用,特 别涉及叶酸循环的抑制剂,其通过抑制pd-l1的水平达到肿瘤免疫治疗 的目的。
背景技术:
2.近年来癌症治疗研究领域的热点之一,当属免疫治疗,即通过调动患 者自身抵抗力(免疫细胞)来抵御、杀死肿瘤细胞。其中,pd-l1/pd-1 通路的研究及其在免疫治疗中的应用受到了广泛的关注。
3.程序性死亡受体-1(programmed death-1,pd-1)是一种重要的免疫抑 制分子,主要参与t细胞的活化调控,可以调节免疫应答的强弱程度和 持续时间。当pd-1的开关打开,就会启动一系列反应,抑制t细胞活性, 而打开pd-1开关的关键因素之一,就是pd-1的配体pd-l1 (programmed death ligand 1)。pd-l1/pd-1抗体属于免疫检查点阻断 药物。其作用机理通俗来讲,就是肿瘤细胞借助pd-l1与t细胞的pd-1 结合,逃避t细胞的识别,使得肿瘤细胞可以在体内增殖和扩散。而 pd-l1/pd-1抗体则可以阻断pd-1/pd-ls信号通路,恢复t细胞对肿瘤 细胞识别和杀伤(anticancer agents med chem.2015;15(3):307-13. hematol oncol stem cell ther.2014mar;7(1):1-17.trends mol med. 2015jan;21(1):24-33.immunity.2013jμl 25;39(1):61-73.j clin oncol. 2015jun 10;33(17):1974-82.)。pd-1/pd-l1抗体自2014年首个药物获批 以来已经革新了多种癌症的治疗。美国fda从2014年末至今,依次批准 了pembrolizumab(keytruda)和nivolumab(opdivo)(均为抗pd-1 抗体)用于治疗晚期黑色素瘤、非小细胞肺癌、肾细胞癌、霍奇金淋巴瘤 及头颈部鳞状细胞癌。
4.然而,pd-l1/pd-1通路阻断后,被抑制的效应t细胞功能恢复,有 可能引起机体对自身抗原发生免疫反应而导致自身组织损伤,导致严重不 良反应。此外,部分患者有先天的耐药性,或者发生继发性耐药(oncology (williston park).2014nov;28suppl 3:15-28.)。
5.2019年5月15日,来自瑞士的一个科学家团队在nature reviewsclinical oncology上发表了题为《免疫检查点抑制剂的副作用:流行病学、 管理和监测》的综述文章(nat rev clin oncol.2019sep;16(9):563-580.doi: 10.1038/s41571-019-0218-0),总结了到目前为止出现的不同类型的免疫相 关不良事件(immune-related adverse events,iraes)。其中的统计数据显示, 约10%接受pd-1抗体治疗的患者会发生≥3级iraes。5%
–
20%接受治疗 的患者有包括疲劳、头痛、关节痛、皮疹、瘙痒、肺炎、腹泻和/或结肠 炎、肝炎和内分泌疾病在内的毒性反应。与pd-1抗体治疗相关的大多数 iraes发生在开始治疗后的头6个月。keytruda似乎与opdivo有相似的 毒性。此外,ctla-4抗体与pd-1抗体的联合增加了iraes的发生率和 严重程度。一项比较yervoy opdivo联合治疗与yervoy单药治疗疗效的 ii期试验数据显示,联合治疗组≥3级毒性的发生率要高得多(54%vs 24%)。与yervoy单药治疗相比,联合治疗过程中,iraes也发生地更早。
6.因此,有必要寻求其它不依赖抗体的、能够阻断或减弱pd-l1/pd-1 通路的调控剂用于肿瘤的治疗。
技术实现要素:
7.发明人意外发现,抑制参与叶酸循环的亚甲基四氢叶酸脱氢酶 (methylenetetrahydrofolate dehydrogenase)例如亚甲基四氢叶酸脱氢 酶1(mthfd1)、亚甲基四氢叶酸脱氢酶1样蛋白(mthfd1l)、亚甲 基四氢叶酸脱氢酶2(mthfd2)或亚甲基四氢叶酸脱氢酶2样蛋白 (mthfd2l),特别是mthfd2,能够抑制肿瘤细胞中pd-l1的表达, 使其能够被t细胞识别和杀伤,达到肿瘤治疗的目的。基于该发现,发 明人完成了本发明。
8.在本公开的第一个方面,提供一种抑制细胞中pd-l1的方法,其包 括使所述细胞暴露于叶酸循环的抑制剂。
9.在本公开的第二个方面,提供一种抑制肿瘤细胞生长的方法,其包括 使所述肿瘤细胞暴露于叶酸循环的抑制剂。
10.在本公开的第三个方面,提供一种治疗肿瘤的方法,其包括向有此需 要的对象施用叶酸循环的抑制剂。
11.在本公开的一些实施方案中,所述抑制剂抑制5,10-methf到 10-formyl-thf的转化,特别地所述抑制剂抑制将5,10-methf转化为10-formyl-thf的酶,更特别地所述酶是亚甲基四氢叶酸脱氢酶2 (mthfd2)或亚甲基四氢叶酸脱氢酶2样蛋白(mthfd2l),优选地 所述抑制剂特异性抑制mthfd2和mthfd2l之一,更优选地所述抑制 剂特异性抑制mthfd2。
12.在本公开的另一些实施方案中,所述抑制剂抑制10-formyl-thf到 formate的转化,特别地所述抑制剂抑制将10-formyl-thf转化为 formate的酶,更特别地所述酶是亚甲基四氢叶酸脱氢酶1样蛋白 (mthfd1l)。
13.在本公开的另一些实施方案中,所述抑制剂抑制formate到 10-formyl-thf的转化,特别地所述抑制剂抑制将formate转化为 10-formyl-thf的酶,更特别地所述酶是亚甲基四氢叶酸脱氢酶1 (mthfd1)。
14.在本公开的另一些实施方案中,所述抑制剂抑制10-formyl-thf到 5,10-methf的转化,特别地所述抑制剂抑制将10-formyl-thf转化为 5,10-methf的酶,更特别地所述酶是亚甲基四氢叶酸脱氢酶1 (mthfd1)。
15.在本公开的一些实施方案中,所述抑制剂可以是小分子化合物、多核 苷酸、蛋白质(如抗体)或病毒。
16.优选地,所述抑制剂为多核苷酸,其包含靶向抑制亚甲基四氢叶酸脱 氢酶1(mthfd1)、亚甲基四氢叶酸脱氢酶2(mthfd2)、亚甲基四氢 叶酸脱氢酶1样蛋白(mthfd1l)或亚甲基四氢叶酸脱氢酶2样蛋白 (mthfd2l)基因表达的序列,例如所述多核苷酸是rna干扰抑制剂, 特别地,所述多核苷酸长度为10-100、15-30或18-25,例如12、13、14、 15、16、17、18、19、20、21、22、23、24、25、26、27、28、29或30。
17.更优选地,所述多核苷酸包含ggaugcuucacuuugucaa(seqid no:26)、gaaugaagacucuacugua(seq id no:27)、 aguucuaaguuuauugcaa(seq id no:28)、 uggcaaugcuaaugaagaa(seq id no:33)、 cucgcggcaguucgguaaga(seq id no:30)、 guguggccguuuguugccug(seq id no:36)、 gcugcagguaagaacacaag(seq id no:38)中任一
项所示的序列, 或其互补序列。
18.所述多核苷酸的形式可以是小干扰rna(sirna)、短发夹rna (shrna)或小向导rna(sgrna)。
19.优选地,所述多核苷酸为短发夹rna,所述短发夹rna序列包含 ggaugcuucacuuugucaa(seq id no:26)或其互补序列,特 别地所述短发夹rna的序列为ccggggaugcuucacuuugucaacucgaguugacaaagugaagcaucc(seq id no:39)。
20.优选地,所述多核苷酸为小干扰rna,所述小干扰rna序列包含 ggaugcuucacuuugucaa(seq id no:26)、 uggcaaugcuaaugaagaa(seq id no:33),或其互补序列;特 别地所述小干扰rna如seq id no:26或seq id no:33所示。
21.优选地,所述多核苷酸为小向导rna,所述小向导rna序列包含 cucgcggcaguucgguaaga(seq id no:30)、 guguggccguuuguugccug(seq id no:36)、 gcugcagguaagaacacaag(seq id no:38),或其互补序列; 特别地所述小向导rna如seq id no:30、seq id no:36或seq idno:38所示。
22.在本公开的第四个方面,提供一种多核苷酸,所述多核苷酸包含靶向 抑制亚甲基四氢叶酸脱氢酶1(mthfd1)、亚甲基四氢叶酸脱氢酶2 (mthfd2)、亚甲基四氢叶酸脱氢酶1样蛋白(mthfd1l)或亚甲基 四氢叶酸脱氢酶2样蛋白(mthfd2l)基因表达的序列,例如所述多核 苷酸是rna干扰抑制剂,特别地,所述多核苷酸长度为10-100、15-30 或18-25,例如12、13、14、15、16、17、18、19、20、21、22、23、24、 25、26、27、28、29或30。
23.在本公开的一些实施方案中,所述多核苷酸包含ggaugcuucacuuugucaa(seq id no:26)、 gaaugaagacucuacugua(seq id no:27)、 aguucuaaguuuauugcaa(seq id no:28)、 uggcaaugcuaaugaagaa(seq id no:33)、 cucgcggcaguucgguaaga(seq id no:30)、 guguggccguuuguugccug(seq id no:36)、 gcugcagguaagaacacaag(seq id no:38)中任一项所示的序列, 或其互补序列。
24.所述多核苷酸的形式可以是小干扰rna(sirna)、短发夹rna (shrna)或小向导rna(sgrna)。
25.优选地,所述多核苷酸为短发夹rna,所述短发夹rna序列包含 ggaugcuucacuuugucaa(seq id no:26)或其互补序列,特 别地所述短发夹rna的序列为ccggggaugcuucacuuugucaacucgaguugacaaagugaagcaucc(seq id no:39)。
26.优选地,所述多核苷酸为小干扰rna,所述小干扰rna序列包含 ggaugcuucacuuugucaa(seq id no:26)、 uggcaaugcuaaugaagaa(seq id no:33),或其互补序列;特 别地所述小干扰rna如seq id no:26或seq id no:33所示。
27.优选地,所述多核苷酸为小向导rna,所述小向导rna序列包含 cucgcggcaguucgguaaga(seq id no:30)、 guguggccguuuguugccug(seq id no:36)、 gcugcagguaagaacacaag(seq id no:38),或其互补序列; 特别地所述小向导rna如seq id no:30、seq id no:36或seq idno:38所示。
28.在本公开的第五个方面,还提供一种载体,其包含本公开第四方面所 述的多核苷酸。
29.在本公开的第六个方面,还提供一种溶瘤病毒,其包含或表达本公开 第四方面所述的多核苷酸。
30.在本公开的第七个方面,还提供一种药物组合物,其包含本公开第四 方面所述的多核苷酸、第五个方面所述的载体、或第六个方面所述的溶瘤 病毒,以及药学上可接受的辅料。
31.在本公开的第八个方面,还提供与以上第四个方面对应的用途,例如 所述多核苷酸在制备用于治疗肿瘤的药物中的用途。
32.在本公开的第九个方面,还提供与以上第四个方面对应的用途限定的 抑制剂,例如用于治疗肿瘤的抑制剂,特别地所述抑制剂包含本公开第四 方面所述的多核苷酸。
33.在本公开的一些实施方案中,所述肿瘤选自白血病、淋巴瘤、骨髓瘤、 脑肿瘤、头颈部鳞状细胞癌、非小细胞肺癌、鼻咽癌、食道癌、胃癌、胰 腺癌、胆囊癌、肝癌、结直肠癌、乳腺癌、卵巢癌、宫颈癌、子宫内膜癌、 子宫肉瘤、前列腺癌、膀胱癌、肾细胞癌和黑色素瘤。
34.在本公开的另一些实施方案中,还包括向所述对象施用额外的抗肿瘤 治疗。所述额外的抗肿瘤治疗可以是化学治疗、放射治疗、靶向治疗和免 疫治疗。
35.在本公开的第十个方面,提供一种筛选肿瘤治疗剂的方法,包括
36.1)提供候选物质;和
37.2)检测所述候选物质是否抑制叶酸循环,特别地,检测所述候选物 质是否抑制5,10-methf到10-formyl-thf的转化、10-formyl-thf到 formate的转化、formate到10-formyl-thf的转化、和/或10-formyl-thf 到5,10-methf的转化;更特别地,检测所述候选物质是否抑制选自以下 的酶:亚甲基四氢叶酸脱氢酶1(mthfd1)、亚甲基四氢叶酸脱氢酶2 (mthfd2)、亚甲基四氢叶酸脱氢酶1样蛋白(mthfd1l)和亚甲基 四氢叶酸脱氢酶2样蛋白(mthfd2l);
38.其中所述转化被抑制表明所述候选物质可用作肿瘤治疗剂。
39.在本公开的第十一个方面,提供一种鉴定肿瘤治疗剂的方法,包括
40.1)提供候选物质;和
41.2)检测所述候选物质是否抑制叶酸循环,特别地,检测所述候选物 质是否抑制5,10-methf到10-formyl-thf的转化、10-formyl-thf到 formate的转化、formate到10-formyl-thf的转化、和/或10-formyl-thf 到5,10-methf的转化;更特别地,检测所述候选物质是否抑制亚甲基四 氢叶酸脱氢酶1(mthfd1)、亚甲基四氢叶酸脱氢酶2(mthfd2)、亚 甲基四氢叶酸脱氢酶1样蛋白(mthfd1l)和亚甲基四氢叶酸脱氢酶2 样蛋白(mthfd2l);
42.其中所述转化被抑制表明所述候选物质可用作肿瘤治疗剂。
附图说明
43.图1示叶酸循环中的酶的细胞定位和所催化反应。
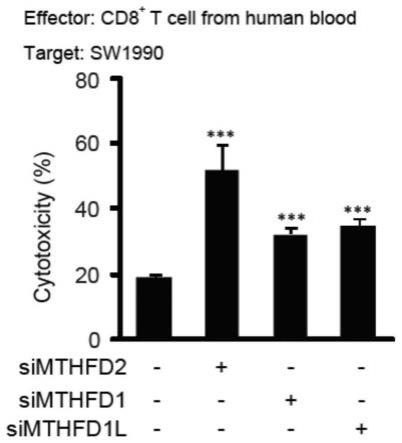
44.图2示细胞毒性检测结果。sw1990细胞转染对照或sirnas并与活 化的人cd8 效应t细胞孵育16小时,然后通过乳酸脱氢酶(ldh)释 放测定法测定其细胞毒性。
45.图3示细胞毒性检测结果。a:sw1990细胞转染对照或sgrna并与 活化的人cd8 效应t细胞孵育16小时,然后通过乳酸脱氢酶(ldh) 释放测定法测定其细胞毒性;b:用shrna转染pan02细胞,与来自ot-1 小鼠的活化脾细胞一起温育16小时,通过ldh释放测定法测量细胞毒 性。
46.图4a示kaplan-meier分析胰管腺癌、肾透明细胞癌、肺腺癌、乳 腺癌、肝肝癌中
mthfd2低、高表达患者的总生存期(kaplan-meier分 析,对数秩检验见图);图4b示sirnas转染不同癌细胞,并与活化的人 cd8 效应t细胞孵育16小时,通过ldh释放测定法测量细胞毒性。
47.图5示mthfd2-d168e突变体对pd-l1 mrna水平(a)和pd-l1 蛋白水平(b)的影响。
48.图6示下调或敲除mthfd2抑制pd-l1的mrna和蛋白表达。a: sirnas转染48小时的sw1990细胞通过实时pcr分析pd-l1 mrna 水平;b:用抗体进行免疫印迹分析;c:通过慢病毒将sgrnas转染 sw1990细胞构建稳定细胞系,使用抗体进行免疫印迹分析。
49.图7示mthfd2过表达对pd-l1 mrna和蛋白水平的影响。a:用 表达载体转染sw1990细胞,通过实时pcr分析pd-l1 mrna水平; b:使用抗体进行免疫印迹分析检测pd-l1蛋白水平。
50.图8示simthfd2抑制ifn-γ诱导的pd-l1增加。用sirna转染不 同癌细胞24小时,然后再用20ng/ml ifn-γ处理24小时,使用所示的 抗体进行免疫印迹分析。
51.图9示shmthfd2对t细胞免疫缺陷型无胸腺裸鼠中肿瘤的治疗效 果。a:肿瘤大小照片;b:统计学结果。数据表示均值
±
s.e.m,n=8只小 鼠每组。
52.图10示shmthfd2对c57小鼠中肿瘤的治疗效果。a:肿瘤大小照 片;b:统计学结果。数据表示均值
±
s.e.m,n=8只小鼠每组。
53.图11示携带shrna的溶瘤腺病毒感染sw1990细胞(a)和人t细 胞(b)免疫印迹分析结果。
54.图12示细胞毒性检测结果。携带shrna的溶瘤腺病毒感染细胞后, 用乳酸脱氢酶(ldh)释放法测定感染t细胞和感染sw1990细胞的细胞毒 性。
55.图13示携带shrna的溶瘤腺病毒与免疫细胞的联合治疗。将5
×
10
6 sw1990细胞皮下注射进通过静脉注射人外周血单核细胞重建人免疫系 统的重度免疫缺陷小鼠体内,每3天注射携带所示shrna的溶瘤腺病毒 或生理盐水,每4天测量肿瘤体积。
56.以上图中,*代表p《0.05,**代表p《0.01,***代表p《0.001(t检 验)。
具体实施方式
57.除非特别指出,本文所用术语具有所属领域技术人员通常理解的含义。 以下提供了本文中使用的一些术语的定义,如果对这些术语有其他解释, 则以本文给出的定义为准。
58.本文所指“抑制pd-l1”,是指抑制pd-l1功能,使pd-l1功能减弱 或丧失,这可以是抑制pd-l1表达或者抑制pd-l1活性。
59.本文所指“叶酸循环”,是指细胞内由thf介导的一碳单位传递过程, 各步骤由特异性酶催化。
60.本文所指“叶酸循环抑制剂”,是指能够抑制叶酸循环途径的物质,所 述抑制剂可以是抑制参与叶酸循环的各种酶的表达,也可以是抑制参与叶 酸循环的各种酶的活性。
61.本文所指“特异性地抑制”,是指抑制能力有差异。“特异性地抑制 mthfd2”是指抑制mthfd2的能力强于mthfd2l的能力;例如使 mthfd2活性降低90%,而使mthfd2l活性降低不超过50%;再例 如仅抑制mthfd2而不抑制mthfd2l。“不抑制”是指活性降低不超过 例如10%、20%、30%、40%、50%。
62.本文所指“抑制肿瘤细胞生长”,是指使经处理的肿瘤细胞生长低于未 处理的肿瘤细胞,包括减缓肿瘤细胞生长速度,使肿瘤细胞减少,或使肿 瘤细胞死亡。
63.本文所指“rna干扰(rnainterference,rnai)”,是指小分子rna 可以特异性地降解或抑制同源mrna表达,从而抑制或关闭特定基因表 达的现象,在进化过程中高度保守。
64.本文所指“shrna(short hairpin rna)”,是指短发卡rna,包含 一条正义链片段和互补的反义链片段,并在正义链和反义链之间含有一个 环状序列,可形成发卡样的双链rna。在细胞质中被dicer酶加工成 sirna,识别靶序列发挥rna干扰作用。
65.本文所指“sirna(small interference rna)”,是指小干扰rna, 通常为18~25nt的双链rna分子,可在细胞质中发挥rna干扰作用, 即干扰含有互补核苷酸序列的特定mrna,导致其翻译受阻。
66.本文所指“sgrna(small guide rna)”,是指小向导rna,也是一 种小型非编码rna,具有基因编辑功能。
67.本文所指“靶序列”,是指mrna上被小分子rna识别的特定序列。
68.本文所指“识别序列”,是指小分子rna例如shrna或sgrna中能 够识别或结合特定mrna的序列或其互补序列。
69.本文所指“治疗”是指有益于目标对象健康状况的任何措施,例如可以 是预防疾病发生,降低疾病发生风险,减缓或阻碍疾病进程,抑制或停止 疾病相关细胞或实体(如肿瘤细胞或肿瘤实体)的生长,杀死疾病相关细 胞(如肿瘤细胞),使疾病相关实体(如肿瘤实体)缩小,减小或消除疾 病相关症状,防止或减缓疾病相关并发症的发生或发展,抑制或减缓疾病 转移,提高患病对象生存率。
70.本文所指“肿瘤治疗”或“抗肿瘤治疗”是指有助于预防或延迟肿瘤发 生、降低肿瘤发生风险,减缓或阻碍肿瘤进程,抑制或停止肿瘤细胞或肿 瘤实体的生长,杀死肿瘤细胞,使肿瘤实体停止生长或缩小,减小或消除 肿瘤相关症状(如肿瘤疼痛),防止或减缓肿瘤相关并发症的发生或发展, 抑制或减缓肿瘤转移,提高患病对象生存率的任何措施。抗肿瘤治疗例如 可以是手术切除、化学治疗、放射治疗、靶向治疗和免疫治疗中的一种或 更多种。在医疗实践中,为了减缓或消除患病对象的不健康状态,医学专 业人员经常选择一种或更多种适用的肿瘤治疗措施。
71.本文所指“包括”、“包含”、“含有”是指,除了列出的特征要素以外, 还可以有其他附加的特征要素。特别地,也可以仅由所列出的特征要素组 成。
72.本文所指“选自”是指从多个候选项中选择。当适用时,在未特别指出 的情况下,所述“选自”可以是从多个候选项中选择一种或更多种候选项。实施例
73.下面将结合实施例对本发明的实施方案进行详细描述。本领域技术人 员将会理解,下列实施例仅用于说明本发明,而不应视为限制本发明的范 围。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。 所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产 品。i.实验材料
74.mthfd2抗体(d8w9u,no.41377,1:1000)、pd-l1抗体( no.13684,1:1000),o-glcnac抗体(ctd110.6,no.9875,1:1000)均 购自cell signaling technology。
ogt(ab96718,1:1000)和pd-l1 (ab205921,1:1000)购自abcam。m2磁珠(m8823)和 β-actin过氧化物酶抗体(a3854)购自sigma。从invitrogen公司获得抗 flag-tag抗体(pa1-984b,1:1000)。myc抗体(10828-1-ap,1:10000) 购自proteintech。从sangon获得p-stat-1(d155017,1:1000)和stat-1 (d190766,1:1000)抗体。pten抗体(af1426,1:10000)来自beyotime。 从ebioscience公司获得cd45 efluor 450(b220,48-0452-82)和cd8a 单克隆抗体(4sm15,14-0808-82)。人cd3(300314)、人cd28(302914)、 il-2(589102)、小鼠cd3(100207)、小鼠cd28(102111)抗体均来自 biolegend。easysep human cd8 pos sel kit(17853)、lymphoprep(07851) 和easyseptm(18000)购自stemcell technologies。人ifn-γ (11725-hnas)和小鼠ifn-γ(50709-mnah)均来自sino biological。
75.利用synbio技术合成sirnas,其中
76.人mthfd2 sirna:ggaugcuucacuuugucaa(seq id no: 26);
77.人mthfd1 sirna:gaaugaagacucuacugua(seq id no: 27);
78.人mthfd1l sirna:aguucuaaguuuauugcaa(seq id no: 28)。
79.ly294002(hy-10108)购自mce。雷帕霉素(abs810030)购自absin。 udp(a600979)、utp(a620570)、尿苷(a610570)、腺嘌呤(a600013)、鸟 嘌呤(a610246)、腺苷(a600016)、鸟嘌呤(a610250)、胞嘧啶(a600138)、s
ꢀ‑
腺苷-l-蛋氨酸(sam,a506555)、烟酰胺(nam,a510659)购自sangon。
80.其中一些试剂的研究资源标识符(rrids)如下:pcdh-flag-c-myc rrid:addgene102626,人crispr代谢基因敲除文库rrid: addgene110066。ii.实验方法1.细胞系的培养
81.用含10%胎牛血清(fbs)的rpmi1640培养sw1990细胞 (crl-2172
tm
)。含10%胎牛血清(fbs)的改良eagle培养基(dmem)培 养hpde(crl-4036
tm
)、hepg2(hb-8065
tm
)、a549(ccl-185
tm
)、 mcf-7(htb-22
tm
)、hct-116(ccl-247
tm
)、786-o(crl-1932
tm
) 和pan02(crl-2553
tm
)细胞株。在37℃的细胞培养箱,5%co2的加 湿气下培养。所有的细胞系均来自atcc。2.mthfd2敲除的稳定转染细胞系构建
82.将mthfd2 sgrna克隆入lenticrispr-v1载体(addgene plasmid #49535),测序正确后,利用慢病毒包装体系制备病毒,感染sw1990细 胞,构建mthfd2敲除的稳定转染细胞系。具体方法参见文献:improved lentiviral vectors and genome-wide libraries for crispr screening. sanjana ne*,shalem o*,zhang f.nature methods(2014),genome-scale crispr-cas9 knockout screening in human cells.shalem o*,sanjana ne*,hartenian e,shi x,scott da,mikkelsen t,heckl d,ebert bl, root de,doench jg,zhang f(2014).science,343,83-7.
83.构建克隆所用的合成序列如下(下划线示识别序列):
84.sgmthfd2_1f:caccgctcgcggcagttcggtaaga(seq id no:1);
85.sgmthfd2_1r:aaactcttaccgaactgccgcgagc(seq id no:2);
86.sgmthfd2_2f:caccggtgtggccgtttgttgcctg(seq id no:3);
87.sgmthfd2_2r:aaaccaggcaacaaacggccacacc(seq id no:4);
88.sgmthfd2_3f:caccggctgcaggtaagaacacaag(seq id no:5);
89.sgmthfd2_3r:aaaccttgtgttcttacctgcagcc(seq idno:6)。
90.通过syno assembly(synbio technologies)将mthfd2 cdna(seqid no:7)克隆入plenti-gfp-flag vector(obio technology)中生成 plenti-mthfd2-flag。
91.使用syno assembly(synbio technologies)将人和小鼠pd-l1的cdna 克隆入plenti-gfp-flag载体中生成plenti-pd-l1-flag,用于过表达 pd-l1。
92.人pd-l1和小鼠pd-l1扩增引物如下:
93.人pd-l1_f:atgaggatatttgctgtctttatattcatgacctactg(seq id no:8);
94.人pd-l1_r:cgtctcctccaaatgtgtatcactttgc(seq id no:9);
95.鼠pd-l1_f:atgaggatatttgctggcattatattcacagc (seq id no:10);
96.鼠pd-l1_r:cgtctcctcgaattgtgtatcatttcgg(seq idno:11)。
97.小鼠shmthfd2片段由genewiz生物科技有限公司合成。将 shmthfd2片段插入pgipz载体生成pgipz小鼠mthfd2 shrna (pgipz-mthfd2-shrna)。
98.合成的人shmthfd2序列用于克隆构建和表达:ccggggatgcttcactttgtcaactcgagttgacaaagtgaag catccttttt(seq id no:12)
99.合成的鼠shmthfd2序列用于克隆构建和表达:ccgggcagttgaagaaacatacaatctcgagattgtatgtttct tcaactgcttttt(seq id no:13)。3.小鼠胚胎成纤维细胞(mef)的培养
100.为了在小鼠胚胎成纤维细胞体系中验证mthfd2的功能,在小鼠妊 娠12.5-14.5d期间收获胎儿。除小鼠的头部和肝脏外的内脏组织用2ml 胰蛋白酶洗净、切碎、消化,再进行高强度的吹混,直到它变成单个细胞 的悬浮液。细胞在含10%胎牛血清的dmem中培养,每3-4天传代一次。4.外周血单核细胞(pbmcs)和cd8 t细胞的分离
101.健康人白细胞血(buffy coats)购自天津血液中心。pbmcs通过淋 巴细胞分离剂(stemcell)结合密度梯度离心法进行分离。简单的说 就是将白细胞血添加到预先加入了等体积淋巴细胞分离剂的锥形管中,放 入离心机以400g转速离心30分钟,4℃停止运行。中间层需小心地移到 一个新的锥形管,加入三倍体积的pbs稀释后,再以300g的转速离心10 分钟。之后,用25-30毫升pbs离心洗涤两次,转速为200g,每次15 分钟。收获的沉淀被视为pbmcs,以1*108细胞/毫升的密度进行悬浮。
102.使用easysep human cd8 pos sel kit(stemcell)按照说明书从 pbmcs中分离cd8 t细胞。将0.1-2.5ml的上述重悬细胞转移到5ml 的聚苯乙烯圆底管中。pbmcs先加入100μl精选鸡尾酒(selection cocktail, 人cd8正选抗体混合物),混合室温(rt)孵育3min,再加入50μl快速球 粒(rapidspheres
tm
),同样条件孵育。孵育后用磁铁将细胞分离。分离 的cd8 t细胞在rpmi 1640培养基中重悬,与2μg/ml cd3、cd28和 10ng/ml il-2(biolegend)孵育48-96h,活化后的cd8 t细胞用于后续的 t细胞杀伤实验。5.cd8 t细胞介导的肿瘤细胞杀伤实验
103.贴壁肿瘤细胞sw1990、hepg2、a549、mcf-7、hct-116、786o(4*104细胞/孔)均铺于24孔板。将活化的cd8 t细胞(2*105细胞/孔)以效应靶 比5的比例加入每个孔中,并与贴壁
肿瘤细胞共培养16小时。孵育结束 后,离心400g,5min,各组收集上清液,按厂家说明进行ldh释放测定 (beyotime)。利用biotek酶标仪在490nm处检测吸光度。6.溶瘤腺病毒构建
104.由genewiz直接合成shmthfd2的表达盒,该表达盒含有u6启动 子序列,能够转录shmthfd2的序列以及连续5个t的rna聚合酶
ⅲꢀ
的转录终止子,使用noti
‑‑
xhoi酶切位点插入腺病毒穿梭载体pshuttle
ꢀ‑
sp-e1a(
△
24bp)-e1b(参见cn201810097442.0)。然后利用穿梭载体 和大肠杆菌bj5183株中腺病毒骨架质粒的同源重组产生腺病毒质粒。病 毒在hek-293细胞中被包装和扩增。采用离子交换色谱和分子筛色谱进 行纯化。使用快速滴度腺病毒滴度免疫测定试剂盒(cell biolabs,sandiego,ca,usa)测定病毒滴度。
105.表达盒包含如下序列:
106.shmthfd2-1:ggatgcttcactttgtcaactcgagttgacaaagtgaagcatcc ttttt(seq id no:14);
107.shmthfd2-2:gtggcaatgctaatgaagaactcgagttcttcattagcattgccacttttt(seq id no:15)。7.细胞转染和处理
108.按照说明书使用lipofectamine 3000(thermofisher)和rnai max (thermofisher)分别将不同的质粒和sirnas转入sw1990、hpde、hepg2、 a549、mcf-7、hct-116、786o和pan02细胞。携带scrambleshrna 或shmthfd2的溶瘤腺病毒以2.5moi的量感染sw1990细胞48小时。
109.用20ng/ml的ifn-γ刺激细胞4、8、12、24小时。将udp、utp、 尿苷、腺嘌呤、鸟嘌呤、腺苷、鸟嘌呤、胞嘧啶、sam、nam(sangon) 按规定浓度加入细胞24小时。8.动物实验
110.肿瘤异种移植的c57bl/6j小鼠和balb/c裸鼠均购自北京维通利华 实验动物技术有限公司。m-nsg(nod-prkdcscidil2rgem1/smoc)小鼠 来自上海模式生物中心。ot-i小鼠由第三军医大学提供。所有动物被放 置在无特定病原体(spf)环境中,光照12小时/黑暗12小时,自由获得食 物和水。将溶于150μl pbs的2*106的pan02细胞注射到6周龄雄性裸 鼠(每组8只)皮下,左侧和右侧双侧成瘤。采用公式“体积=(宽^2)
×
长/2
”ꢀ
计算肿瘤体积。6周龄雄性c57bl/6j小鼠,每只异种移植均注射5*106的pan02细胞。m-nsg小鼠侧翼皮下注射5
×
106个sw1990细胞成瘤。 平均肿瘤体积达到100mm3后,每只小鼠注射2
×
107人pbmc。4天后, 每3天向肿瘤内注射含1.5
×
107个病毒颗粒的溶瘤腺病毒或盐水。在第28 天收集肿瘤异种移植物。所有动物实验均经天津医科大学伦理委员会批准。9.小鼠脾细胞分离及细胞杀伤实验
111.将ot-i小鼠处死,置于干净的解剖板上。剖腹手术切除脾脏,并在 10毫升pbs中通过70-μm滤网以分离组织。含脾细胞的溶液以400g转 速离心5分钟。细胞沉淀洗涤完成后,在含2μg/ml cd3,cd28 and 10 ng/ml il-2(biolegend)的培养基中重悬培养48-96小时。将pan02细胞置 于24孔板中,用5μg/ml ova肽刺激12小时。将活化的pbmcs(2*10^5 cells/well)以效应靶比为5的比例加入到pan02细胞中,共培养16小时。 使用上述ldh释放试剂盒(beyotime)检测细胞杀伤的细胞毒性。10.流式细胞仪免疫荧光分析
112.转染mthfd2sirna和pd-l1质粒的sw1990细胞进行免疫荧光染 色:从培养皿中刮取细胞,用pbs洗涤。每一个样品与pd-l1抗体(abcam, clone28-8)在冰上置于避光条件下孵育30分钟。采用流式细胞术检测 sw1990中pd-l1的免疫荧光。
113.取c57bl/6j小鼠异种移植物,在0.2%胶原酶iv溶液中切成1mm3 碎块,37℃,轻摇4小时。将从组织中分离出来的细胞用40-μm网筛过 滤,用pbs稀释至10^6细胞/ml。样品在避光条件下与cd45 efluor 450 (ebioscience)孵育30分钟。流式细胞仪(bd)采集细胞,用flowjo软件(treestar)分析数据。11.免疫沉淀和免疫印迹
114.用预冷的ripa裂解液(beyotime)和蛋白酶抑制剂或磷酸酶抑制剂套 装提取培养细胞或肿瘤组织中的蛋白,然后用相应抗体进行免疫沉淀和免 疫印迹。蛋白质由sds聚丙烯酰胺凝胶电泳分离,然后转移到pvdf膜 (bio-rad)上,用如下抗体孵育:mthfd2(cst,1:1,1000),pd-l1(cst, 1:1,000),o-glcnac(cst,1:1,000),ogt(abcam,1:1,000), m2磁珠(sigma)和β-actin-过氧化物酶抗体(sigma,1:5000), myc(proteintech 1:1,000),p-stat-1(sangon 1:1,000)及stat-1(songon 1:1,000)。使用化学发光成像系统(tanon)显影、拍照。12.rna提取
115.以trizol试剂(invitrogen)裂解sw1990细胞,用minibestuniversal rna提取试剂盒(takara)提取其总rna。13.实时定量聚合酶链反应
116.使用trizol rna分离试剂(invitrogen)从细胞或肿瘤组织中提取总 rna,并使用ii第一链cdna合成supermix(transgen)将 rna逆转录为cdna。用sybr master mix(yeasen)进行实时荧光定量 pcr。用2
‑△△
t法计算基因表达的倍数变化,以β-actin为内参。
117.pcr引物序列为:
118.mthfd2_f:tggctgcgacttctctaatg(seq id no:16);
119.mthfd2_r:ccttccagaaatgacaacagc(seq id no:17);
120.mthfd1_f:gcgccagcagaaatcctga(seq id no:18);
121.mthfd1_r:aggtacttgctccttcaactga(seq id no:19);
122.mthfd1l_f:ctgccttcaagccggttctt(seq id no:20);
123.mthfd1l_r:tttcctgcatcaagttgtcgt(seq id no:21);
124.pd-l1_f:tggcatttgctgaacgcattt(seq id no:22);
125.pd-l1_r:tgcagccaggtctaattgtttt(seq id no:23);
126.β-actin_f:cgtaccactggcatcgtgat(seq id no:24);
127.β-actin_r:aggtagtcagtcaggtcccg(seq id no:25)。14.统计分析
128.数据表示为平均值
±
s.e.m.统计学显着性设定为p《0.05。使用t检验 (2个独立样本)分析两组之间的显着性差异。kaplan-meier方法是用 对数秩检验来分析生存数据。除非另有说明,否则在graphpad prism 7 中进行统计分析。所有实验至少重复三次。图例中显示了n个数字。
实施例1:导致肿瘤对t细胞杀伤耐受的代谢基因
129.发明人在研究中意外发现,叶酸循环通路中的酶(图1)在肿瘤细胞 中高表达,且在t细胞治疗后明显下调,特别是亚甲基四氢叶酸脱氢酶 同工酶mthfd2、mthfd1和mthfd1l。
130.通过设计合成sirnas分别敲低(knock-down)mthfd2、mthfd1 和mthfd1l。其中针对人mthfd2的sirna序列为 ggaugcuucacuuugucaa(seq id no:26),针对人mthfd1的 sirna序列为gaaugaagacucuacugua(seq id no:27),针对 人mthfd1l的sirna序列为aguucuaaguuuauugcaa(seq id no:28)。结果显示,这些sirnas本身没有明显的细胞毒性,但显著增 加了t细胞诱导的细胞死亡,其中,敲除mthfd2表现出最显著的效果 (图2)。
131.有研究标明,mthfd2是一种在胚胎期细胞或肿瘤细胞中特异性表 达的叶酸循环酶(yang,m.and k.h.vousden,serine and one-carbon metabolism in cancer.nat rev cancer,2016.16(10):p.650-62)。我们在多 种肿瘤细胞系中检测到显著的mthfd2 mrna表达,例如sw1990细胞、 hct116细胞、panc-1细胞、mcf-f细胞、7860细胞和hepg2细胞。 采用常规sgrna技术构建敲除mthfd2的sw1990细胞,构建时使用 的序列为caccgctcgcggcagttcggtaaga(seq id no:29), 针对的靶序列为ctcgcggcagttcggtaaga(seq id no:30)。用shrna转染pan02细胞,针对的靶序列为 gctcatgaagaacaccattat(seq id no:32)。进行效应t细胞和 敲除mthfd2的细胞之间的细胞毒性实验,以及来自ot-1小鼠活化脾 细胞与小鼠胰腺癌细胞ova-pan02之间抗原特异性细胞毒性试验。结果 显示,敲除mthfd2后效应细胞的活性显著增加(图3),说明mthfd2 具有免疫抑制作用。
132.进一步地,进行了tcga数据库分析(http://www.tcga.org/),发现 高mthfd2 mrna含量不仅与胰腺癌相关,而且与肾癌、肺癌、乳腺癌 和肝癌患者的预后不良显著相关(图4a)。因此,使用mthfd2/1/1l sirnas对肾癌786-o细胞、肺癌a549细胞、乳腺癌mcf-7细胞、肝癌 hepg2细胞和结肠癌hct-116细胞进行了t细胞毒性分析,在所有这些 癌细胞系中均检测到效应细胞的活性增加(图4b)。这些结果提示 mthfd2在肿瘤发生的中的作用可能是促进肿瘤细胞的免疫逃避。
133.为了探讨mthfd2的代谢功能与pd-l1表达的关系,在mthfd2 敲除的sw1990细胞或正常胰管上皮细胞hpde中过表达失去催化活性 的mthfd2-d168e突变体,发现该突变体不能像野生型mthfd2那样 上调pd-l1的mrna(图5a)和蛋白质(图5b)水平,这表明其催化 活性是调节pd-l1表达的重要因素。此外,pd-l1的mrna和蛋白质的 表达也受到mthfd1l的影响。实施例2:mthfd2可被ifn-γ诱导从而促进本底和ifn-γ诱导的pd-l1 表达
134.将mthfd2敲除的sw1990细胞进行rna测序并分析转录组。msigdb c4(癌症模块)数据库 (https://www.gsea-msigdb.org/gsea/msigdb/collections.jsp#c4)中的 gsea(gene set enrichment analysis)分析显示,“免疫应答”的基因集在 mthfd2敲除组而非对照癌细胞组中富集,提示mthfd2在癌细胞中 具有对免疫系统的抑制作用。此外,还筛选了那些同时在rna测序结果 和tcga胰腺癌临床样本数据库中与mthfd2相关的基因。令人意外的 是,免疫检查点配体pd-l1在两种分析中均显示与mthfd2呈正相关。
135.针对人mthfd2序列设计sirnas,分别命名为simthfd2-1
(ggaugcuucacuuugucaa,seq id no:26),和simthfd2-2 (uggcaaugcuaaugaagaa,seq id no:33)。实验显示,这两 种sirnas均能显著降低pd-l1的mrna水平和蛋白水平。通过向细胞 中导入sirna敲低或敲除mthfd2,检测到pd-l1 mrna(图6a)或 蛋白质(图6b)发生减少。设计3个靶向mthfd2的sgrna并构建克 隆,其中构建ko-1使用的序列(携带克隆用酶切位点)为 caccgctcgcggcagttcggtaaga(seq id no:34),识别序列 为ctcgcggcagttcggtaaga(seq id no:30);构建ko-2使 用的序列为caccggtgtggccgtttgttgcctg(seq id no:35), 识别序列为gtgtggccgtttgttgcctg(seq id no:36);构建 ko-3使用的序列为caccggctgcaggtaagaacacaag(seq idno:37),识别序列为gctgcaggtaagaacacaag(seq id no:38)。 分别构建lenticripsr-sgmthfd2质粒,通过包装慢病毒,感染sw1990 细胞,通过puromycin筛选后,获得3株mthfd2-ko稳定转染细胞系。 结果显示,在敲除mthfd2的细胞中,pd-l1蛋白的表达显著减少(图 6c)。相反,在细胞中过表达mthfd2则显著促进pd-l1 mrna(图7a) 和蛋白质(图7b)的表达。
136.在体内肿瘤组织中,pd-l1通常维持在一个高水平表达,这主要是由 于细胞因子的存在,特别是浸润淋巴细胞分泌的ifn-γ。为了确定 mthfd2是否也参与ifn-γ刺激的pd-l1表达,检测了其在786-o、a549、 mcf-7、hepg2和hct-116细胞中的蛋白水平。结果显示,ifn-γ诱导 的pd-l1蛋白的表达被mthfd2敲低(shmthfd2)显著抑制,而且, 在所有这些癌细胞中ifn-γ单独处理显著促进了mthfd2的表达(图8)。实施例3:通过降低mthfd2表达抑制肿瘤生长
137.肿瘤异种移植的c57bl/6j小鼠和balb/c裸鼠均购自北京维通利华 实验动物技术有限公司。c57bl/6j小鼠和balb/c裸鼠均被放置在无特 定病原体(spf)环境中,光照12小时/黑暗12小时,自由获得食物和水。 将溶于150μl pbs的2*106的慢病毒稳定转染pan02细胞注射到6周龄雄 性裸鼠(每组8只)皮下,左侧和右侧双侧成瘤。同时,将溶于150μl pbs 的5*106的慢病毒稳转株pan02细胞注射到6周龄雄性c57bl/6j小鼠(每 组8只)皮下。该慢病毒表达如seq id no:31所示的shrna,识别序列 如seq id no:32所示。采用公式“体积=(宽^2)
×
长/2”每7天计算一次肿 瘤体积。
138.在裸鼠模型中,靶向小鼠mthfd2的shrna能够显著抑制肿瘤生 长(图9),抑瘤率约为37%。但在含有成熟淋巴细胞的c57小鼠中,其 抑制肿瘤生长的百分率(图10)大大高于在裸鼠模型中,抑瘤率约为80%。 实施例4:通过溶瘤病毒导入shmthfd2
139.由genewiz直接合成靶向mthfd2的shmthfd2表达盒(表达 ccggggaugcuucacuuugucaacucgaguugacaaagugaag caucc,seq id no:39),通过腺病毒穿梭载体(pshuttle-sp-e1a (
△
24bp)-e1b)携带。然后利用穿梭载体和大肠杆菌bj5183株中腺病毒 骨架质粒的同源重组产生腺病毒质粒。在hek-293细胞中被包装和扩增 病毒,然后采用离子交换色谱和分子筛色谱进行纯化。使用快速滴度腺病 毒滴度免疫测定试剂盒(cell biolabs,san diego,ca,usa)测定病毒滴度。
140.用空载病毒和携带shmthfd2的溶瘤腺病毒感染sw1990细胞和人 t细胞。使用pd-l1(cst,1:1000)、mthfd2(cst,1:1000)、β-actin抗 体(sigma,1:5000)对细胞裂解液进行免疫印迹分析;用乳酸脱氢酶(ldh) 释放法测定感染t细胞和感染sw1990细胞的细胞毒性。
141.结果表明,携带人shmthfd2的重组溶瘤腺病毒可抑制mthfd2 和pd-l1在sw1990细胞(图11a)和t细胞(图11b)中的表达水平, 但并不影响免疫细胞mthfd2的表达。
实施例5:与免疫细胞联用治疗癌症
142.m-nsg(nod-prkdcscidil2rgem1/smoc)小鼠来自上海模式生物 中心。m-nsg小鼠(每组8只)被放置在无特定病原体(spf)环境中,光 照12小时/黑暗12小时,自由获得食物和水。侧翼皮下注射5
×
106个 sw1990细胞建立肿瘤模型。当平均肿瘤体积达到100mm3后,每只小鼠 注射2
×
107人pbmc(peripheral blood mononuclear cell)。4天后,每3 天分别向每组小鼠肿瘤内注射盐水、含1.5
×
10
10
个空载病毒颗粒、含 1.5
×
10
10
个携带mthfd2 shrna的溶瘤腺病毒(实施例4构建)。每4 天测量肿瘤体积,在第28天收集肿瘤异种移植物。
143.sw1990细胞和cd8 t细胞分别感染重组溶瘤腺病毒后,过夜共培 养16h,检测sw1990培养上清中ldh的释放。结果显示,将上述重组 溶瘤腺病毒与免疫细胞联用治疗癌症时,重组溶瘤腺病毒显著加剧了t 细胞诱导的细胞死亡(图12)。
144.在nsg小鼠上通过静脉注射人pmbc重建人源免疫系统,然后在该 模型上种植人异种移植瘤中来进一步验证这一策略。与生理盐水或对照空 载溶瘤腺病毒相比,携带shmthfd2的重组溶瘤腺病毒在体内具有更强 的肿瘤杀伤作用(图13)。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。