1.本发明涉及预防与治疗高草酸尿症相关疾病的药物领域,具体涉及一种含草酸脱羧酶与枸橼酸盐或枸橼酸盐和枸橼酸的混合物的组合物,及其在降低尿液中草酸浓度、减少尿液中草酸钙微晶体、以及防止含草酸钙泌尿结石形成与生长等方面的应用。
背景技术:
2.草酸(oxalic acid)又名乙二酸,是人体内的一种代谢终产物,无法被进一步代谢分解,主要通过肾脏以尿液形式排出体外。人类和其他哺乳动物在食用富含草酸盐的食物时,在人体的血液和尿液中容易引起草酸盐浓度的升高,当其与钙离子结合后会生成低溶解度的草酸钙,草酸钙在尿液中过饱和会结晶析出,进而成长为结石,草酸钙是泌尿系结石的主要成分。此外,体内血液或尿液中高浓度的草酸盐还与其他多种病理有关,例如,高草酸尿症,心脏传导障碍、孤独症(autism spectrum disorder)、慢性肾病、肾炎、肾衰竭等。目前临床中,一些早期发现的小结石(最大直径《0.6cm),可以通过大量饮水,服用利尿消炎等辅助排石中药,并配合运动进行排石治疗。对于较大的泌尿系结石,一般临床上的治疗方案主要为外科手术,如体外超声波碎石、微创手术取石或碎石、及开放手术取石等。现有治疗手段不仅对身体与肾脏带来创伤,还存在着复发率高、手术费昂贵(平均2.0-4.0万元/次手术)等问题;更严重的是,结石复发病人反复使用上述手段,会带来更大创伤,并可能最终导致肾功能衰竭。众多的泌尿系统结石患者,占用了大量的医疗资源,同时高昂的医疗费用,也给我国医保支付也带来了巨大的压力。因此,开发一种无创伤的治疗与防止结石复发的药物变得十分迫切。
3.另外,泌尿结石最常见的临床症状除了高草酸尿症外,还常常伴发有低枸橼酸尿症。研究发现,泌尿系结石患者中70%的人伴随有尿枸橼酸排泄量异常,具体表现为尿液枸橼酸排泄量明显下降。尿液中枸橼酸根离子可以与尿液中的钙离子形成络合稳定态,从而减少钙离子与草酸根离子形成难溶的草酸钙晶体,抑制结石生成。同时,临床研究显示,多数泌尿结石并非单一成分,而是多成分为主,许多草酸钙的结石中,会混有尿酸钠,磷酸钙,尿蛋白等成分,即临床上讲的异质成核。口服枸橼酸盐,可以提高尿液的 ph,从而增加尿酸的溶解度,减少尿液中的尿酸钠结晶,因此,枸橼酸盐可以防止由单钠尿酸盐引起的异质成核结石。口服补充枸橼酸盐可以提高尿液中的枸橼酸浓度,但是也伴随着副作用,因为其会升高尿液的ph值。当尿液的ph值高于7.0时,会增加含钙结石(例如:磷酸钙结石)的发病风险,因此,在服用枸橼酸盐药物期间,每天都需要多次监测尿液ph值,从而防止出现尿液ph偏高的情况。
4.市场上已经有用枸橼酸钾或枸橼酸氢钾钠为主要成分的预防和维持治疗泌尿系结石的产品(友来特,逍遥柠,杰石同及urocit-k),但是仅靠枸橼酸的作用,并不能降低尿液中的草酸含量,因此,低剂量枸橼酸盐治疗草酸钙结石的效果不佳,当服用剂量较大(每天6-10g以上)时,会出现的诸多副作用,如腹泻、恶心、胃及腹部疼痛等,患者的体验和依从度很差。临床数据显示,此类药物的不良反应率高达10%,致使25%的服药人员不能坚持完
整治疗疗程(penniston kl,urology,2007;70:856-860)。
5.正在临床试验的口服草酸脱羧酶类药品,需要非常大的剂量,如:每天剂量高达 37500酶活力单位,约1克以上纯酶,生产成本非常高,会导致上市后的售价昂贵,并且,降低尿草酸幅度不是很大(craig b.langman等,am j nephrol,2016,44:150
–
158)。究其原因,本技术的发明人发现,胃部的强酸性ph对草酸脱羧酶发挥降解草酸的作用形成巨大的挑战。
6.因此,现在临床上亟需能够有效地防治高草酸尿症、副作用低、成本低的药物。
技术实现要素:
7.针对现有产品的不足,发明人对现有的几种不同特性的草酸脱羧酶与枸橼酸盐或枸橼酸盐和枸橼酸的混合物按照一定的比例进行了复配,探索了在模拟胃液条件下有效降解饮食中草酸的方案。通过将这些有效方案与增加尿液中枸橼酸含量及适当提高尿液 ph等因素综合考虑,发明人惊奇地发现,枸橼酸盐可在胃液中起到缓冲胃酸的作用,形成枸橼酸-枸橼酸盐-盐酸的缓冲体系,且该缓冲体系恰好在草酸脱羧酶最适酶活的ph 下(ph 3.0-5.0)具有较强的缓冲能力,从而利于草酸脱羧酶发挥最佳的酶活力,较单独使用草酸脱羧酶时的降解草酸效果更优。同时,口服枸橼酸盐,可以提高尿液的ph,从而增加尿酸的溶解度,减少尿液中的尿酸钠结晶,防止由单钠尿酸盐引起的异质成核结石;口服枸橼酸盐还可提高尿液中的枸橼酸浓度,抑制草酸钙微晶体形成,进一步降低了在草酸钙浓度不是非常高的情况下生长结石的几率,也降低了草酸脱羧酶降低尿草酸幅度不足情况下的结石生长风险。
8.本发明提供如下技术方案:
9.第一方面,本发明提供了一种组合物,有效成分包含:a)草酸脱羧酶,和b)枸橼酸组分。
10.所述组合物能防治高草酸尿症或能抑制泌尿系统的含草酸钙结石生长。所述泌尿系统指肾脏、输尿管、膀胱和尿道中的一个或多个脏器或部位。
11.优选地,本发明的组合物中,所述的草酸脱羧酶为重组表达草酸脱羧酶或提取的天然草酸脱羧酶。例如,可以为重组表达的枯草杆菌草酸脱羧酶a、重组表达茶树菇草酸脱羧酶b、提取纯化的杨树菇草酸脱羧酶c、重组表达的金针菇草酸脱羧酶d、重组表达的蓝细菌草酸脱羧酶e、提取纯化的云芝草酸脱羧酶f或重组表达的金福菇草酸脱羧酶g等中的一种、两种或更多种。
12.优选地,本发明的组合物中,所述枸橼酸组分是指枸橼酸盐或枸橼酸盐和枸橼酸的混合物,其中枸橼酸盐包含但不限于枸橼酸钾、枸橼酸镁、枸橼酸钙、枸橼酸钾镁、枸橼酸钠、枸橼酸氢钾钠中的一种、两种、三种或更多种直至全部。
13.优选地,本发明的组合物中,所述的草酸脱羧酶的含量为50-90000u/g组合物,或 1-800mg/g组合物。
14.优选地,本发明的组合物中,所述的枸橼酸组分的含量为10mg-990mg/g组合物。
15.优选地,本发明的组合物中,当所述枸橼酸组分为枸橼酸和枸橼酸盐的混合物时,二者的重量比不受特别地限制,可以为6:39-4:1,优选地为8:37-1:4。
16.优选地,本发明的组合物中,所述枸橼酸组分为以下的组合:枸橼酸:枸橼酸钾:枸
橼酸镁=8:27:10;枸橼酸:枸橼酸钙=6:39;枸橼酸:枸橼酸钾=4:1;枸橼酸:枸橼酸钾:枸橼酸钠=5:14:16;枸橼酸:枸橼酸钾:枸橼酸镁:枸橼酸钙:枸橼酸钠=1:1:1:1:1。
17.优选地,本发明的组合物中,所述有效成分占组合物总重量的20-85%。
18.优选地,本发明的组合物还含有赋形剂。
19.进一步优选地,所述赋形剂可为稀释剂、填充剂、结合剂、崩解剂、润滑剂、溶剂或其他食品学或药学上可接受的赋形剂。
20.优选地,本发明的组合物可以为溶液、悬浮液、乳剂、粉末、锭剂、丸剂、糖浆、口含锭、片剂、口嚼胶、浓浆以及胶囊或其他食品学或药学上可接受的剂型。
21.第二方面,本发明提供上述组合物在制备预防、治疗或缓解高草酸尿症,低枸橼酸尿症以及含草酸钙结石相关疾病的药物中的应用。
22.第三方面,本发明提供上述组合物在制备具有降低尿液中草酸浓度、减少尿液中草酸钙微晶体、以及防止含草酸钙泌尿结石形成与生长功能的食品中的应用;
23.优选地,上述应用中所述的食品,包括普通食品、保健食品或特殊医学用途配方食品。
24.本发明的有益效果:
25.为了更好的解决草酸钙在尿液中过饱和结晶析出导致泌尿结石疾病的难题,本技术人首次提出了将草酸脱羧酶与枸橼酸组分联合使用的复方制剂。本发明人通过一系列的筛选优化,摸索出兼顾草酸脱羧酶活力与枸橼酸组分含量的组合物,可在胃环境下增加草酸脱羧酶的稳定性,提升草酸脱羧酶的活力与延长有效作用时间,降低草酸脱羧酶的有效剂量。
26.本制剂服用方便,既能增加尿液枸橼酸浓度,又具有降低尿草酸的效果,两者相辅相成,协同作用,提升防治含草酸钙泌尿结石的效果。较市场上的枸橼酸盐制剂具有显著的优势,大幅度降低枸橼酸组分的服用剂量,较低的枸橼酸组分剂量能显著降低其副作用,给患者带来更好的治疗效果的同时,提高了治疗体验质量和依从度。同时,该复合制剂,较正在临床试验中的纯草酸脱羧酶药物剂型,达到同等效果所需草酸脱羧酶的剂量更低,因而可以降低生产成本,降低结石患者的治疗经济负担,缓解医保压力,是对人民生命健康和社会都有巨大价值。
附图说明
27.图1示出了多种草酸脱羧酶的ph特性。
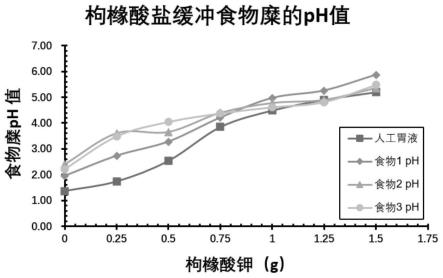
28.图2示出了枸橼酸盐组合物缓冲胃食糜的ph。
29.图3示出了尿液草酸钙结晶图。
具体实施方式
30.下文将结合具体实施例对本发明的技术方案做更进一步的详细说明。应当理解,下列实施例仅为示例性地说明和解释本发明,而不应被解释为对本发明保护范围的限制。凡基于本发明上述内容所实现的技术均涵盖在本发明旨在保护的范围内。
31.除非另有说明,以下实施例中使用的原料和试剂均为市售商品,或者可以通过已知方法制备。
32.定义与说明:
33.如本文所用,术语“含有”或“包括”包括了“包含”、“基本上由
……
构成”、和“由
……
构成”。
34.如本文所用,术语“基本上由
……
构成”指在组合物中,除了含有必要成分或必要组份之外,还可含有少量的且不影响有效成分的次要成分和/或杂质。例如,可以含有甜味剂以改善口味以及其他本领域常用的添加剂。
35.如本文所用,术语“有效量”是指可对人和/或动物产生功能或活性的且可被人和/ 或动物所接受的量。
36.如本文所用,“重量份”或“重量份数”可互换使用,所述的重量份可以是任何一个固定的以毫克、克数或千克数表示重量(如1mg、1g、2g、5g、或1kg等)。例如,一个由1重量份组分a和9重量份组分b构成的组合物,可以是1克组分a 9克组分b,也可以是10克组分a 90克组分b等构成的组合物。在所述组合物,某一组分的百分比含量=(该组分的重量份数/所有组分的重量份数之和)
×
100%。因此,由1重量份组分a 和9重量份组分b构成的组合物中,组分a的含量为10%,组分b为90%。
37.其中,如本文所用,术语“药学上可接受的”或“食品学上可接受的”的成分是适用于人和/或动物而无过度不良副反应(如毒性、刺激和变态反应)的,即有合理的效益/ 风险比的物质。
38.如本文所用,术语“药学上可接受的载体”指用于治疗剂给药的载体,包括各种赋形剂和稀释剂。该术语指这样一些药剂载体:它们本身并不是必要的活性成分,且施用后没有过分的毒性。合适的载体是本领域普通技术人员所熟知的。在r e m i n g t o n's pharmaceutical sciences(mack pub.co.,n.j.1991)中可找到关于药学上可接受的赋形剂的充分讨论。在组合物中药学上可接受的载体可含有液体,如水、盐水、甘油和乙醇,等。另外,这些载体中还可能存在辅助性的物质,如填充剂、崩解剂、润滑剂、助流剂、泡腾剂、润湿剂或乳化剂、矫味剂、ph缓冲物质等。
39.所述的“药学上可接受的载体”或“食品学上可接受的载体”还包括具有预防泌尿系统的结石的成分,例如但不限于,柠檬汁或粉,橙汁或粉、蔓越莓汁或粉,维生素 b6,含醋酸饮料等。
40.除非另外定义或由背景清楚指示,否则在本公开中的全部技术与科学术语具有如本公开所属领域的普通技术人员通常理解的相同含义。
41.实施例1.不同草酸脱羧酶的酶学性质特性
42.本实施例中所述的草酸脱羧酶可参照专利《一种用丝状真菌宿主细胞表达的重组草酸脱羧酶》(cn 108588060a)、《一种草酸脱羧酶及草酸脱羧酶的重组表达方法》 (cn105695441a)、《糖基化草酸脱羧酶及其制备和应用》(cn107868776a)、《草酸脱羧酶的制备及其制品和应用》(cn107868775a),《含金福菇草酸脱羧酶的干粉和菌粉的制备方法》(cn102697040b)以及其他相关的专利及科学论文中的制备方法进行制备。实施例中用到的草酸脱羧酶仅作为发明方案展示,不作为发明方案的限制,其他方式制备的草酸脱羧酶经常规优化也是可以适用的。
43.草酸脱羧酶的活力采用如下方法检测,具体检测步骤如下:将1.0ml 5mm(毫摩尔浓度)草酸盐溶液(含25mm枸橼酸盐缓冲液,ph值为3.0;其中枯草芽孢杆菌的草酸脱羧酶活
力测定时枸橼酸盐缓冲液的ph是4.0),在37℃预热10分钟后,加入0.01-0.1ml (根据酶浓度及酶活力确定加入体积)含草酸脱羧酶的溶液或悬浮液开始反应。反应10 分钟后,加入50μl 2.5m(摩尔浓度)硫酸使酶失活。迅速离心并取上清液,经0.45μ m滤膜过滤后用hplc测定残留草酸盐浓度。hplc的测试条件如下:色谱柱采用sepax 公司的carbomix h-np 10;流动相为2.5mm硫酸;流速0.6ml/min;柱温55℃;检测波长为210nm。一个酶活力单位(u)定义为在测试条件下,每分钟降解1个微摩尔草酸盐所需的酶量。
44.分别配制ph1.5-7.0的含草酸测试缓冲液(草酸终浓度为5mm),测试各种草酸脱羧酶在不同ph下的活力,以每一种草酸脱羧酶的最适ph的活力定义为100%,计算其在不同ph下的相对酶活力。各种草酸脱羧酶的酶学性质如表1所示,其在不同ph条件下的相对酶活力见图1。
45.表1.不同草酸脱羧酶的酶学性质
46.草酸脱羧酶最适ph酶活力(u/mg蛋白)枯草杆菌草酸脱羧酶a(重组表达)4.220重组表达茶树菇草酸脱羧酶b(重组表达)3.050杨树菇草酸脱羧酶c(提取纯化)3.045金针菇草酸脱羧酶d(重组表达)3.533蓝细菌草酸脱羧酶e(重组表达)2.5120云芝草酸脱羧酶f(提取纯化)2.710金福菇草酸脱羧酶g(重组表达)3.075
47.结果显示,不同草酸脱羧酶的酶活力的最适ph有所差异,从2.5-4.2不等,酶活力从10u/mg-120u/mg不等,且部分草酸脱羧酶具有一定的耐酸稳定性。
48.实施例2.草酸脱羧酶与枸橼酸组分的配方优化
49.人在空腹状态下,胃中的胃液量约为20-100ml,为酸性最强状态(ph约1.5),当人进食后,胃液与食物混合,胃中内容物的ph会升高,当ph》4.0时,胃蛋白酶活力下降,进而刺激胃壁增加胃酸分泌,胃内容物一般在ph2.0-5.5波动(李晓华,武警医学院学报, 2002)。本专利申请人以实施例1中制备的各种草酸脱羧酶为材料,经过大量的筛选和优化,以筛选能够相互兼容且能增强草酸脱羧酶在消化道中的稳定性或者提高活力的组方。本实施例提供的是不同来源的草酸脱羧酶与不同比例的枸橼酸组分(包含枸橼酸盐或枸橼酸盐和枸橼酸的混合物)复配方中有代表性的一部分组方,考察其对草酸脱羧酶活力的影响,评估组方的可行性。从表2中组合物的酶活力测试结果与实施例1中各种草酸脱羧酶的活力的比较中可以看出,优选的枸橼酸组分对草酸脱羧酶的活力影响比较小。
50.表2.草酸脱羧酶与枸橼酸组分的配方(质量百分比)
[0051][0052][0053]
实施例3.含草酸脱羧酶和枸橼酸组分的组合物在人工胃液中的酶活力
[0054]
按照《中国药典(2020版)》配制人工胃液,加入实施例2中的不同组合物,测试在人工胃液中的草酸脱羧酶的降草酸活力。由于人在禁食空腹状态、不同程度的排空状态及进食后饱腹状态下的ph是有明显差异的,本实施例在中国药典人工胃液配方的基础上用naoh调整ph后分别配制了ph 1.5-5.5的人工胃液,并分别测试了实施例2中的组合物1、2、5和6的效果。
[0055]
根据研究报道,人在空腹时,胃中的胃酸残留量约50-100ml,饮食后胃液分泌量会根据食物量有所增加,全天的总胃酸量在500-1500ml,最高约500ml/餐,但进食后,食物与胃液混合后,会部分中和酸性,因而ph通常在ph 2.0-5.5。
[0056]
本实施例的测试,分别选取ph1.5和ph5.5两个ph的100ml人工胃液进行测试。具体操作方案如下,将人工胃液(约ph 1.4-1.5)用naoh调节至ph 5.5,并分别加入草酸钠至终浓度为5mm。在ph 1.5和5.5的含草酸的人工胃液中分别加入测试组合物,测试物加入量如
表3所示,快速混合均匀后测试ph,同时在37℃下孵育反应5分钟,加入2ml的 2.5m硫酸终止反应,样品过0.45μm滤膜后,用hplc检测草酸剩余量,评价不同组合物在人工胃液中的降草酸效果。
[0057]
结果(表3)显示,组合物1(仅含草酸脱羧酶a)加入到ph 1.5胃液后,ph在1.65左右,草酸无降解,显示组合物1在ph 1.65的胃液环境中无草酸降解活性,而组合物2(含草酸脱羧酶a和枸橼酸钾)加入到的ph 1.5胃液后,胃液ph上升为3.73,96%草酸被降解,显示组合物2在ph1.5的胃液环境中有较高的草酸降解活性;组合物5(仅含草酸脱羧酶e)加入到ph 5.5胃液后,ph仍然在5.5左右,草酸无降解,显示组合物5在ph5.5的胃液环境中无草酸降解活性,而组合物6(含草酸脱羧酶e,枸橼酸钾与枸橼酸)加入到的ph5.5胃液后,ph下降为3.25左右,83%草酸被降解,显示组合物6在ph 5.5的胃液环境中有较高的草酸降解活性。以上的研究结果说明含有枸橼酸组分的组合物可以缓冲人工胃液的ph 至3.0-4.0左右,从而提升草酸脱羧酶在人工胃液中的活力。
[0058]
表3.不同的含草酸脱羧酶与枸橼酸组分的组合物在人工胃液中的降解草酸效果
[0059][0060]
实施例4.含草酸脱羧酶与枸橼酸组分的组合物在模拟胃中食糜中的ph缓冲作用及其降草酸活力
[0061]
本实施例提供的是含草酸脱羧酶与枸橼酸组分的组合物对模拟胃中食物糜的ph调节效果并测试实施例2中的优选的含草酸脱羧酶与枸橼酸组分的组合物在模拟胃食物糜中的草酸降解能力。测试的食物配方如表4-6所示,套餐一(表4)以荤食为主,套餐二(表5)以素食为主,套餐三(表6)以常规西餐为主。所述食物的材料均采购自当地菜市场或者超市,在实验室自行烹饪为测试食物。将三种套餐的中食物各自混匀,模拟空腔咀嚼次数在食物料理器中切碎搅拌5-10秒制成食物糜,在每份食物糜中加入人工胃液500ml,用玻璃棒搅拌均匀后,测定ph值,然后均分为200g/份。取各食物的对照份样品,在37℃恒温磁力搅拌状态下,分别逐步加入枸橼酸钾,并监测食物糜的 ph值,绘制枸橼酸钾添加量与食物糜ph的关系图,结果(图2)显示,枸橼酸钾可以较好的缓冲胃酸,在ph3.0-5.0形成相对稳定的缓冲体系。
[0062]
3种食物分别各取8份200g食物糜,按照实施例2中的组合物2与组合物8配方中枸橼酸钾的含量换算为组合物添加量(具体见表7),加入到3种食物糜中,37℃下搅拌均匀并孵育30min,取10g食物糜加入1ml 2.5m硫酸终止反应,离心取上清液测定草酸含量,以原始食物糜的草酸含量作为对照,评估组合物2与8对食物糜中草酸的降解率,结果如表7所示。结果显示:在3种配方食物的相同ph食物糜中,组合物8明显优于组合物2,说明不同ph酶活特性的草酸脱羧酶的组合,会克服单一草酸脱羧酶的最适酶活ph范围较窄的不足,在模拟胃食物糜中具有更好的降草酸效果。随着组合物 2和8添加量增加,食物糜的ph逐步上升,食物糜中草酸脱羧酶的含量也随之上升,因而其草酸的降解率逐步提高。
[0063]
表4.模拟胃中食糜的食物配方(一)
[0064][0065][0066]
表5.模拟胃中食糜的食物配方(二)
[0067][0068]
表6.模拟胃中食糜的食物配方(三)
[0069][0070][0071]
表7.组合物2和8在不同食物食糜中的草酸降解量
[0072][0073]
实施例5.一种含草酸脱羧酶和枸橼酸组分的咀嚼片的制备
[0074]
本实施例提供一种含有草酸脱羧酶和枸橼酸组分的咀嚼片的制备方法,所述草酸脱羧酶粉可为实施例1中含任一种或多种草酸脱羧酶与辅料的组合物。咀嚼片配方以质量百分比计如下:枸橼酸14.5%,枸橼酸钾33.5%,茶树菇草酸脱羧酶b粉35%;羧甲基纤维素14.5%,硬脂酸镁2.5%。将各物料粉碎过60目筛网备用,按照配方称取对应的物料,进行混合均匀,将混合好的物料倒入压片机料筒进行压片,调整冲压压力,使咀嚼片的硬度在8-10kg,片重约1-2g/片,在洁净环境下分装至双层泡罩板或者高密度聚乙烯瓶中(高密度聚乙烯瓶中需加入干燥剂包)。该咀嚼片产品的草酸脱羧酶活力大于 5000u/g咀嚼片。
[0075]
实施例6.一种含草酸脱羧酶和枸橼酸组分的泡腾片的制备
[0076]
本实施例提供一种含草酸脱羧酶和枸橼酸组分的泡腾片的制备方法,所述草酸脱羧酶粉可为实施例1中含任一种或多种草酸脱羧酶与辅料的组合物。泡腾片配方(质量百分
比)如下:将枯草杆菌草酸脱羧酶a粉25%,枸橼酸33.5%,碳酸氢钠35%,交联聚维酮5%,硬脂酸镁1.5%。将各物料粉碎过60目筛网备用,按照配方称取对应的物料,进行混合均匀,将混合好的物料倒入压片机料筒进行压片,调整冲压压力,使硬度在 10-15kg,片重约2g/片,生产环境的相对湿度《40%。在洁净环境下分装至双层泡罩板或者高密度聚乙烯瓶中(高密度聚乙烯瓶中需加入干燥剂包)。该泡腾片的草酸脱羧酶活力大于2000u/g泡腾片。
[0077]
实施例7.一种含草酸脱羧酶和枸橼酸组分的胃溶胶囊的制备
[0078]
本实施例提供一种含草酸脱羧酶和枸橼酸组合物的胃溶胶囊的制备方法,所述草酸脱羧酶粉可为实施例1中含任一种或多种草酸脱羧酶与辅料的组合物。胃溶胶囊配方(质量百分比)如下:复合草酸脱羧酶粉(该复合粉含枯草芽孢杆菌草酸脱羧酶a粉25%,茶树菇草酸脱羧酶b粉45%,蓝细菌草酸脱羧酶e粉30%)76.0%,枸橼酸钾13.5%,枸橼酸4%,枸橼酸镁5%,硬脂酸镁1.5%。将各物料粉碎后过60目筛网备用,按照配方称取对应的物料,进行混合均匀,灌入胃溶空心胶囊壳中,0.3-0.6g/胶囊,用双层铝塑泡罩板封装。该胶囊的草酸脱羧酶活力大于10000u/g胶囊。
[0079]
实施例8:一种含草酸脱羧酶和枸橼酸组分的速溶颗粒(粉)剂的制备
[0080]
本实施例提供一种含草酸脱羧酶和枸橼酸组合物的速溶颗粒或粉的制备方法,所述草酸脱羧酶粉可为实施例1中含任一种或多种草酸脱羧酶与辅料的组合物。速溶颗粒的具体配方(质量百分比)如下:茶树菇草酸脱羧酶b粉5%,枸橼酸钾60%,甘露醇19.9%,抗性糊精15%,甜橙香精粉末0.1%。将各物料过60目筛网备用,按照配方称取对应的物料,进行混合均匀,进行湿法制粒(20目筛),40℃减压干燥至水分《5.0%,铝箔袋封装,5g/袋。该速溶颗粒的草酸脱羧酶活力大于500u/g颗粒。服用时采用温开水(《40℃) 溶解,随餐服用。
[0081]
实施例9.在高草酸尿症犬模型中降低尿液草酸钙结晶的效果观察
[0082]
36只比格犬,雄性,体重7~8kg,购买自湖北安陆瑞科森实验动物有限公司,饲养于标准独立犬笼中,正常饮食适应3~5天后,收集尿液至的预加酸化剂的尿液收集桶中(加3m盐酸10ml/桶),测定24h尿草酸总量,确定无尿草酸异常后,随机分为 6组。除空白组外,其余5组,喂食含有菠菜粉的饮食(100g犬粮 15g菠菜粉/餐,2 餐/天,喂食时间8:00与20:00)进行高草酸尿症建模,建模期(1-14天)的后2天(第 13和14天)收集尿液,测尿草酸,评估建模的效果。在高草酸饮食建模的基础上,分别给予相应的测试物(表8,剂量为2g/次,2次/天,给药时间为8:00和20:00,随餐服用)进行干预(15-28天),并分别在27-28天,收集尿液至预加盐酸的尿液收集桶中,测定24h尿草酸总量和尿枸橼酸总量。分别在第8-14天,22-28天,每天早上8:00-9:00 收集约15ml的新鲜尿液至普通收集桶中,用于尿液草酸钙微晶体的测试和ph测定。尿草酸测定采用草酸测定试剂盒(草酸氧化酶法,武汉康复得生物科技股份有限公司自制) 测定,尿枸橼酸测定采用枸橼酸检测试剂盒(货号:k-citr,购自爱尔兰megazyme 公司),操作步骤参照试剂盒说明书。尿液草酸钙微晶体测试方法,取10ml尿液于尿沉渣离心管中,3000g离心5分钟,弃去上清液,吸取底部尿液20微升点样到尿沉渣计数板,在显微镜400倍视野下观察,观测视野中出现草酸钙晶体频率(草酸钙晶体如图 3所示);尿液ph测定采用赛多利斯pb-10型号的ph计测定。结果表明,草酸脱羧酶 (测试物1)可以显著降低尿液中的草酸排泄量,枸橼酸盐(测试物2)可以增加尿液中的枸橼酸排泄量和尿液ph,含草酸脱羧酶与枸橼酸盐的组合物(测试物3)干预后, 24h尿草酸排泄量得到明显下降,同时24h尿枸橼酸排泄量得到提升。与高草酸尿症模型组相比,3种测试物均显著降低
了尿液中出现草酸钙微晶体的频率,可以用来防止含草酸钙的结石复发。令人惊奇的是,同时降低了枸橼酸盐剂量和草酸脱羧酶的剂量的测试物4,也具有显著的降低尿草酸排泄量和增加尿枸橼盐量的效果,其出现结晶尿的频率比原剂量枸橼酸盐组(测试物2)还要低,这说明枸橼酸盐和草酸脱羧酶的复合制剂具有显著的协同作用,可以显著降低草酸脱羧酶和枸橼酸盐的使用剂量。
[0083]
表8.测试组合物配方
[0084]
成分测试物1测试物2测试物3测试物4茶树菇草酸脱羧酶b33%-33%12%枸橼酸-8%8%4%枸橼酸钾-27%27%13.5%枸橼酸镁-10%10%5%微晶纤维素67%55%22%65.5
[0085]
表9.尿草酸与尿枸橼酸的检测结果
[0086][0087][0088]
注:*:干预期与建模期相比,p《0.05
[0089]
表10.尿液微晶体和ph的检测结果
[0090][0091]
注:根据michel daudon的研究结果显示,当尿液中出现草酸钙晶体的频率》50%以上时,结石的复发风险高(michel daudon等,kidney international,vol.67(2005),pp.1934
–
1943)。*:干预期与建模期相比,p《0.05。
[0092]
实施例10.口服草酸脱羧酶组合物对结石患者尿草酸以及草酸钙结石复发的影响
[0093]
根据专利cn107868776a工艺制备的富含草酸脱羧酶的食用菌粉,与枸橼酸钾盐,甜橙果粉等辅料在符合食品生产卫生规范(gb 14881—2013)的工厂中制备为固体饮料,在
含草酸钙肾结石患者中进行了降尿草酸和防止结石复发的效果测试。
[0094]
招募了150名超声波碎石后的草酸钙结石患者(测试者入组需提供碎石后的诊断报告,如b超或x光检测报告,草酸钙结石成分分析报告),随机分为5组(每组30人,各组男女比例相当),对照组不做干预,第一组给予测试物1(含枸橼酸盐与含草酸脱羧酶菌粉的固体饮料,5g/袋,含1.6g枸橼酸钾盐与1600u草酸脱羧酶菌粉),剂量为 1袋/次,2次/天;第二组组给予测试物2(含草酸脱羧酶菌粉固体饮料,5g/袋,含1600u 草酸脱羧酶菌粉),剂量为1袋/次,2次/天;第三组给予测试物3(枸橼酸钾片(1.08g/ 片,3片/次,2次/天),第四组给予2倍剂量的测试物1(2袋/次,2次/天),分别进行干预,干预期为12个月,分别在干预前,干预一周(第7天),干预一个月(第30 天),干预六个月(第180天),干预12个月(第360天)(具体时间点根据测试者时间安排,前后变动不超过15天),收集24h尿液,测定24h尿草酸,24h尿枸橼酸;在第一个月,第三个月,第六个月,以及第12个月最后1周时,连续收集晨尿尿液(起床后第一次尿液),采用尿液微晶体医用放大镜(武汉康复得生物科技股份有限公司研发)测定尿液微晶体的出现频率。干预期结束后,测试者通过b超或者x光影像学检查(与干预前的结果相比,结石复发包括新增结石,已有结石增大,或复发结石后就诊等状况中的任意一种),以评估测试物对泌尿结石的影响。结果如表11-14所示,草酸脱羧酶与枸橼酸组分的组合物制剂可以降低结石患者的尿草酸排泄量,同时提高尿枸橼酸含量;草酸钙微晶体检测和结石复发检测的结果显示,该组合物防治草酸钙结石疾病效果显著,是一种新型的无创伤的防治含草酸钙泌尿结石的新方式。
[0095]
表11.结石患者干预前后的尿草酸变化
[0096][0097]
注:*:干预期与干预前相比,p《0.05。
[0098]
表12.结石患者干预前后的尿枸橼酸变化
[0099][0100]
注:*:干预期与干预前相比,p《0.05。
[0101]
表13.结石患者干预前后的尿草酸微晶体频率
[0102][0103]
注*:干预期与干预前相比,p《0.05。
[0104]
表14.结石患者干预前后的结石复发率
[0105][0106][0107]
以上,对本发明的实施方式进行了说明。但是,本发明不限定于上述实施方式。凡在本发明的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。