1.本技术涉及一种抗流感、解热抗炎的中药组合物的质量控制方法,属于中药分析技术领域。
背景技术:
2.流感(influenza)是由流感病毒引起的急性发热性呼吸道传染病,经飞沫传播,临床典型表现为突起畏寒、高热、头痛、全身酸痛、疲弱乏力等全身中毒症状,而呼吸道症状较轻。本病常呈自限性,病程一般为3-4天。婴幼儿、老年人、有心肺疾病及其他慢性疾病患者或免疫功能低下者可并发肺炎,预后较差。正常机体在下丘脑体温调节中枢的控制下,产热和散热往往保持动态平衡,当身体处于致热原作用时,动态平衡失衡就会导致发热。发热实际上是一种机体保护自身生理功能正常运转的机制。当体温升高,一些病原微生物活动会变得不那么活跃并且繁殖减慢。人体免疫系统应答显著增强。但是长时间的发热,会造成很严重的后果。因此对于发热的治疗也显得尤为重要。另外炎症也是流感中常见的症状,炎症是机体组织受到各种刺激、损伤后所产生的一种重要的防御机制,炎症反应是机体最基本的抗损伤反应,急性炎症通常具有红、肿、热、病、机能障碍等变化。
3.本技术发明人已于2022年05月17日申请抗流感、解热抗炎的中药组合物的发明专利,申请号为202210535773.4。虽然提供了上述中药组合物的配方和制备方法,但需要对方法制备的产品进行质量控制,以保证产品质量的稳定性和可控性,同时由于中药产品质控的特殊性,又特别要求该质控方法具有专属性。
技术实现要素:
4.为了解决上述问题,提供了一种抗流感、解热抗炎的中药组合物的质量控制方法,该方法基于色谱峰峰面积及分离度,选定了11个色谱峰作为用于抗流感、解热抗炎的中药组合物质量评价,有利于全面监控产品的质量,避免了质量控制的单一性和片面性,客观、全面、准确性好并且可重复,对控制该抗流感、解热抗炎的中药组合物的质量与保证临床疗效具有重要意义。
5.根据本技术的一个方面,提供了一种抗流感、解热抗炎的中药组合物的质量控制方法,按照重量份数计,所述中药组合物包括以下原料制备而成:忍冬藤12-60份、大青叶12-60份、板蓝根12-60份、蒲公英12-60份、锦灯笼3-15份和龙脷叶3-15份,包括以下步骤:
6.(1)供试品溶液的制备:取适量抗流感、解热抗炎的中药组合物样品,研细后加入甲醇进行超声处理,再加入甲醇,过滤即得;
7.(2)对照品溶液的制备:取马钱苷对照品适量,精密称定,与甲醇混合即得;
8.(3)测定:分别精密吸取对照品溶液和供试品溶液,注入液相色谱仪,测定得指纹图谱。
9.优选地,步骤(3)中分别精密吸取对照品溶液和供试品溶液各10μl,注入液相色谱仪,测定。
10.可选地,步骤(1)中为取适量抗流感、解热抗炎的中药组合物样品,混匀,研细,取1g,精密称定,置具塞锥形瓶中,精密加入体积分数为10%甲醇20ml,称定重量,超声处理30分钟,放冷,再称定重量,用体积分数为10%甲醇补足减失的重量,摇匀,滤过,即得。
11.可选地,步骤(2)中为取马钱苷对照品适量,精密称定,加甲醇制成每1ml含马钱苷30μg的溶液,即得。
12.可选地,步骤(3)中的色谱条件为:以十八烷基硅烷键合硅胶为填充剂色谱柱;以甲醇为流动相a,0.1%磷酸水溶液为流动相b。
13.可选地,步骤(3)中的梯度洗脱条件为:
14.0-15分钟,流动相a为0%,流动相b为100%;15-35分钟,流动相a为0%-5%,流动相b为100%-95%;35-40分钟,流动相a为5%-10%,流动相b为95%-90%;40-100分钟,流动相a为10%-20%,流动相b为90%-80%;100-110分钟,流动相a为20%,流动相b为80%;110-120分钟,流动相a为20%-25%,流动相b为80%-75%;120-125分钟,流动相a为25%,流动相b为75%;125-180分钟,流动相a为25%-60%,流动相b为75%-40%;180-190分钟,流动相a为60%-90%,流动相b为40%-10%;190-200分钟,流动相a为90%,流动相b为10%。
15.可选地,步骤(3)中的检测波长为250nm。
16.可选地,步骤(3)中的柱温为35℃。
17.可选地,按中药色谱指纹图谱相似度评价系统计算供试品指纹图谱与对照品指纹图谱的相似度,相似度大于0.90为合格产品。
18.本技术的有益效果包括但不限于:
19.1.根据本技术的抗流感、解热抗炎的中药组合物的质量控制方法,该方法基于色谱峰峰面积及分离度,选定了11个色谱峰作为用于抗流感、解热抗炎的中药组合物质量评价,有利于全面监控产品的质量,避免了质量控制的单一性和片面性,客观、全面、准确性好并且可重复,对控制该抗流感、解热抗炎的中药组合物的质量与保证临床疗效具有重要意义。
20.2.根据本技术的抗流感、解热抗炎的中药组合物的质量控制方法,通过限定流动相的种类和波长,使最终色谱峰较丰富,分离度较好,基线平稳。
21.3.根据本技术的抗流感、解热抗炎的中药组合物的质量控制方法,通过考察完整性、精密度、重复性、稳定性和耐用性,方法学结果表明,该方法有较好的灵敏度、准确度和精密度,测定结果准确可靠,可有效评价抗流感、解热抗炎的中药组合物的产品质量。
附图说明
22.此处所说明的附图用来提供对本技术的进一步理解,构成本技术的一部分,本技术的示意性实施例及其说明用于解释本技术,并不构成对本技术的不当限定。在附图中:
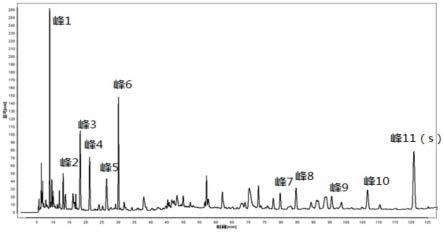
23.图1为本技术实施例1供试品指纹图谱;其中,峰3:尿苷;峰4:鸟苷;峰6:腺苷;峰9:绿原酸;峰11(s):马钱苷;
24.图2为本技术实施例2涉及的不同流动相(有机相)比较供试品hplc色谱图-甲醇;
25.图3为本技术实施例2涉及的不同流动相(有机相)比较供试品hplc色谱图-乙腈;
26.图4为本技术实施例2涉及的不同流动相(水相)比较供试品hplc色谱图-0.1%磷
酸;
27.图5为本技术实施例2涉及的不同流动相(水相)比较供试品hplc色谱图-0.4%磷酸;
28.图6为本技术实施例2涉及的不同流动相(水相)比较供试品hplc色谱图-0.1%甲酸;
29.图7为本技术实施例2涉及的不同流动相(水相)比较供试品hplc色谱图-0.2%甲酸;
30.图8为本技术实施例3涉及的不同波长比较供试品hplc色谱图-210nm;
31.图9为本技术实施例3涉及的不同波长比较供试品hplc色谱图-230nm;
32.图10为本技术实施例3涉及的不同波长比较供试品hplc色谱图-250nm;
33.图11为本技术实施例3涉及的不同波长比较供试品hplc色谱图-280nm;
34.图12为本技术实施例3涉及的不同波长比较供试品hplc色谱图-300nm;
35.图13为本技术实施例3涉及的不同波长比较供试品hplc色谱图-320nm;
36.图14为本技术实施例3涉及的不同波长比较供试品hplc色谱图-350nm;
37.图15为本技术实施例5涉及的hplc指纹图谱完整性色谱图。
具体实施方式
38.下面结合实施例详述本技术,但本技术并不局限于这些实施例。
39.除非另行定义,文中所使用的所有专业与科学用语与本领域熟练人员所熟悉的意义相同。本发明所使用的试剂或原料均可通过常规途径购买获得,如无特殊说明,本发明所使用的试剂或原料均按照本领域常规方式使用或者按照产品说明书使用。此外,任何与所记载内容相似或均等的方法及材料皆可应用于本发明方法中。本专利中所述的较佳实施方法与材料仅作示范之用。
40.其中,本技术中涉及甲醇的百分比,若无特殊说明,均为体积分数。
41.实施例1
42.本实施例的抗流感、解热抗炎的中药组合物的质量控制方法包括以下步骤:
43.(1)供试品溶液的制备:取适量抗流感、解热抗炎的中药组合物样品,混匀,研细,取1g,精密称定,置具塞锥形瓶中,精密加入体积分数为10%甲醇20ml,称定重量,超声处理30分钟,放冷,再称定重量,用体积分数为10%甲醇补足减失的重量,摇匀,滤过,即得;
44.(2)对照品溶液的制备:取马钱苷对照品适量,精密称定,加甲醇制成每1ml含马钱苷30μg的溶液,即得;
45.(3)测定:分别精密吸取对照品溶液和供试品溶液各10μl,注入液相色谱仪,测定得指纹图谱。
46.1.色谱条件与系统适用性试验:以十八烷基硅烷键合硅胶为填充剂(agilent polaris 3柱,柱长为250mm,柱内径为4.6mm,粒径为3μm);以甲醇为流动相a,0.1%磷酸为流动相b,按表1中的条件进行梯度洗脱;检测波长为250nm,柱温35℃。
47.表1梯度洗脱条件
48.时间(分钟)流动相a(%)流动相b(%)0~150100
15~350
→
5100
→
9535~405
→
1095
→
9040~10010
→
2090
→
80100~1102080110~12020
→
2580
→
75120~1252575125~18025
→
6075
→
40180~19060
→
9040
→
10190~2009010
49.本实施例供试品指纹图谱中,分别呈现与参照物色谱保留时间相应的色谱峰。按中药色谱指纹图谱相似度评价系统计算供试品指纹图谱与对照指纹图谱的相似度不得低于0.90,本实施例测定的供试品指纹图谱如图1所示。
50.2.仪器与试药
51.仪器:agilent 1260高效液相色谱仪(安捷伦科技有限公司);
52.色谱柱:agilent polaris 3(4.6*250mm,3μm)sn:614035;
53.试剂:甲醇(色谱纯,月旭,批号:0100812);甲醇(分析纯,天津富宇精细化工有限公司,批号:20211223);磷酸(分析纯,烟台远东精细化工有限公司,批号:20200323);
54.研究用样品:抗流感、解热抗炎的中药组合物试样品(山东宏济堂制药集团股份有限公司,批号:2201001、2202001、2202002、2202003)。
55.实施例2流动相的选择
56.筛选甲醇和乙腈作为有机相,水相分别选用了0.1%磷酸、0.4%磷酸、0.1%甲酸和0.2%甲酸。结果表明有机相选用甲醇,水相选用0.1%磷酸条件下,色谱峰较丰富,分离度较好,基线平稳,因此选择甲醇为有机相,0.1%磷酸作为水相。具体结果见图2-图7。
57.实施例3波长的选择
58.采用dad检测器,进行全波长扫描,并对比不同采集波长下色谱信息,结果显示250nm波长下色谱峰丰富,色谱峰分离度和峰形较好,基线较稳,优于其它波长,因此选用250nm作为检测波长。结果见图8~图14。
59.实施例4供试品制备方法的选择
60.1.提取方式考察
61.取抗流感、解热抗炎的中药组合物试样品颗粒适量,分别进行加热回流和超声处理,测定各标识峰峰面积,结果表明,超声和回流提取所获得的指纹图谱所呈现的物质信息基本相同,且各峰峰面积差异不大,考虑到超声提取方式更为简便,故选择提取方式为超声提取。具体实验数据见表2所示。
62.表2提取方式考察
[0063][0064]
2.提取溶剂考察
[0065]
取抗流感、解热抗炎的中药组合物试样品颗粒,混匀,研细,取1g,精密称定,置具塞锥形瓶中,平行制备6份,分别加入纯化水、10%甲醇、25%甲醇、50%甲醇、75%甲醇和纯甲醇各20ml,称定重量,超声处理30分钟,放冷,再称定重量,用相同的溶剂补足减失的重量,摇匀,滤过,即得。通过比较得出,纯水与10%甲醇的溶剂相较其他溶剂色谱峰多,且两者之间差异不大,从稳定性的角度优选10%甲醇作为溶剂。具体数据详见表3。
[0066]
表3提取溶剂考察
[0067][0068]
3.提取时间考察
[0069]
分别设置超声时间分别为20分钟、30分钟、40分钟,考察各标识峰峰面积,结果表明,20分钟、30分钟和40分钟所获得的指纹图谱所呈现的物质信息基本相同,优选超声时间为30分钟。具体数据详见表4。
[0070]
表4提取时间考察
[0071][0072]
4.供试品取样量考察
[0073]
分别取约0.5g、1.0g、1.5g抗流感、解热抗炎的中药组合物试样品颗粒,测定各标识峰峰面积,结果表明,折合成相同取样量后进行峰面积进行比较,标识峰峰面积基本相同,最终选择称样量为1.0g。具体数据详见表5。
[0074]
表5供试品取样量考察
[0075][0076]
实施例5方法学验证
[0077]
1.完整性试验
[0078]
按实施例1方法制备供试品,对抗流感、解热抗炎的中药组合物的指纹图谱方法进行完整性考察,洗脱梯度如表6所示。
[0079]
表6指纹图谱完整性试验梯度条件
[0080]
时间(分钟)流动相a(%)流动相b(%)0~15010015~350
→
5100
→
9535~405
→
1095
→
9040~10010
→
2090
→
80100~1102080110~12020
→
2580
→
75120~1252575125~18025
→
6075
→
40180~19060
→
9040
→
10
190~2009010200~4009010
[0081]
由结果可知,200分钟内均有色谱峰出现,但色谱峰集中在125分钟内,且占总峰面积90%以上,125分钟之后色谱信息较少,因此选择保留时间为125分钟。结果见图15。
[0082]
2.仪器精密度试验
[0083]
按实施例1供试品溶液制备方法制备供试液,平行进样6次,注入高效液相色谱仪测定。以峰11作为参照峰,计算其余各标识峰相对峰面积和相对保留时间,并计算rsd。结果显示:11个标识峰的相对保留时间rsd≤0.37%,相对峰面积rsd≤1.54%,该方法的仪器精密度良好,详见表7-表10。
[0084]
表7 hplc指纹图谱仪器精密度考察保留时间
[0085][0086][0087]
表8 hplc指纹图谱仪器精密度考察相对保留时间
[0088][0089]
表9 hplc指纹图谱仪器精密度考察峰面积
[0090][0091]
表10 hplc指纹图谱仪器精密度考察相对峰面积
[0092][0093]
3.重复性试验
[0094]
取6份抗流感、解热抗炎的中药组合物样品颗粒,按供试品溶液的制备方法制备供试液,注入agilent高效液相色谱仪测定。6份样品的称样量分别为1.0002、1.0049、1.0038、1.0064、1.0025、1.0038g,以峰11为参照峰,计算其余各标识峰相对峰面积和相对保留时间,并计算rsd。结果显示:11个共有峰的相对保留时间rsd≤0.47%,相对峰面积rsd≤1.51%,该方法的重复性良好,详见表11-表14。
[0095]
表11 hplc指纹图谱重复性试验保留时间
[0096][0097]
表12 hplc指纹图谱重复性试验相对保留时间
[0098][0099]
表13 hplc指纹图谱重复性考察峰面积
[0100][0101]
表14 hplc指纹图谱重复性考察相对峰面积
[0102][0103][0104]
4.稳定性试验
[0105]
分别在0h、4h、8h、12h、24h、48h测定同一供试品溶液,记录各标识峰保留时间和峰面积,并计算相对保留时间、相对峰面积、rsd值。结果显示:11个标识峰相对保留时间的rsd≤0.49%,相对峰面积的rsd≤3.07%,供试品溶液在48小时内稳定性良好,详见表15-表18。
[0106]
表15 hplc指纹图谱稳定性考察保留时间
[0107][0108]
表16 hplc指纹图谱稳定性考察相对保留时间
[0109][0110]
表17 hplc指纹图谱稳定性考察峰面积
[0111][0112]
表18 hplc指纹图谱稳定性考察相对峰面积
[0113][0114]
5.耐用性试验
[0115]
(1)不同柱温考察
[0116]
同一份抗流感、解热抗炎的中药组合物样品颗粒,按供试品溶液制备方法制备供试液,分别设置柱温为33℃、35℃、37℃,进行指纹图谱检测。以峰11为参照峰,计算其余各峰相对峰面积和相对保留时间,并计算rsd。结果显示:11个标识峰的相对保留时间rsd≤1.67%,相对峰面积rsd≤3.47%,该方法对不同柱温耐用性良好,详见表19-表22。
[0117]
表19如意解表方hplc指纹图谱不同柱温耐用性考察的保留时间
[0118][0119]
表20 hplc指纹图谱不同柱温耐用性考察的相对保留时间
[0120][0121]
表21 hplc指纹图谱不同柱温耐用性考察的峰面积
[0122][0123]
表22 hplc指纹图谱不同柱温耐用性考察的相对峰面积
[0124][0125]
(2)不同进样量考察
[0126]
按实施例1供试品溶液制备方法制备供试液,分别设置进样量为5μl、10μl、15μl,注入高效液相色谱仪检测。以峰11为参照峰,计算其余各峰相对峰面积和相对保留时间,并计算rsd。结果显示:11个标识峰的相对保留时间rsd≤0.29%,相对峰面积rsd≤1.76%,该方法对不同进样量耐用性良好,详见表23-表26。
[0127]
表23 hplc指纹图谱不同进样量耐用性考察的保留时间
[0128][0129]
表24 hplc指纹图谱不同进样量耐用性考察的相对保留时间
[0130][0131]
表25 hplc指纹图谱不同进样量耐用性考察的峰面积
[0132][0133]
表26 hplc指纹图谱不同进样量耐用性考察的相对峰面积
[0134][0135]
上述试验表明,本技术较好的稳定性、准确度和精密度,测定结果准确可靠,可有效评价抗流感、解热抗炎的中药组合物的产品质量。
[0136]
以上所述,仅为本技术的实施例而已,本技术的保护范围并不受这些具体实施例的限制,而是由本技术的权利要求书来确定。对于本领域技术人员来说,本技术可以有各种更改和变化。凡在本技术的技术思想和原理之内所作的任何修改、等同替换、改进等,均应包含在本技术的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。