1.本发明属于药物化学技术领域,涉及黄嘌呤醛化合物的新应用,具体为含茶碱乙醛或其水合物的药物组合物及其制备方法和应用。
背景技术:
2.氧化应激被认为是促氧化剂和抗氧化剂之间缺乏平衡引起的,一定数量的ros是细胞信号传导和维持氧化还原稳态所必须的,但过度的ros/rns产生会破坏生物体的防御系统,这被称为氧化应激。内源性和外源性ros的持续攻击会导致关键生物分子的构象和氧化状态发生改变改变,如氧化应激对关键生物分子产生的氧化修饰有:脂质过氧化、蛋白质羰基化、羰基(醛/酮)加合物形成、硝化、磺化氧化、dna损伤(如链断裂或核碱基氧化)等。抗氧化剂是指一种能够阻止或延缓氧化的化合物,其作用机制可以分为多种,如通过抑制自由基物种的形成来防止氧化过程。这些抗氧化剂的作用非常迅速,可以中和任何可能导致产生其他自由基的自由基或任何可能转化为自由基的化学物质,如还原型烟酰胺腺嘌呤二核苷酸(nadh),其自身的还原作用能直接清除掉部分自由基,实验也证实nadh能清除神经细胞中的过氧化氢,帮助预防神经退行性疾病。自由基清除抗氧化剂也是抗氧化应激的一种机制,这种机制中ros的清除是通过电子转移来发挥的,一般为亲水性抗氧化剂(抗坏血酸、谷胱甘肽、尿酸)以及亲脂性抗氧化剂(α-生育酚和泛醇)。自由基损伤后修复也一种抗氧化机制,而此类抗氧化剂也也称为“从头”抗氧化剂。该组由修复受损dna、脂质和蛋白质的酶组成。如上述提到的nadh可释放出生物氢,为atp合成供应能量之后被氧化为烟酰胺腺嘌呤二核苷酸(nad
),补充细胞nad
库。nad
作为dna修复酶聚[adp-核糖]聚合酶1(parp1)的唯一辅酶,是参与dna修复的必需物质。而机体对于自由基也有适应性机制,及在机体中,自由基产生的信号诱导足够的抗氧化剂合成和运输到适当的位点。
[0003]
氧化应激也与多种疾病息息相关,如肺ros的形成是哮喘分子机制的一个组成部分,介导炎症反应的氧化剂激活了促炎细胞因子和趋化因子基因以便促进粘附分子的上调和促炎介质的释放,进而ros伴随产生。此外,ros可改变内皮细胞的形态和功能特性,如增加通透性和粘附分子的表达,导致炎症细胞和内皮细胞之间的粘附相互作用,更有助于炎症症状的表现。同时,ros也可调节转录因子的表达,如上皮细胞中的核因子-кb(nf-кb)和激活蛋白-1(ap-1),许多促炎细胞因子、酶和粘附分子的基因表达可能是由这些转录因子激活引起的,进而诱导炎症反应,这就表明,ros的分子机制与哮喘症状的表达之间存在动态关系。而氧化应激在眼部疾病发病机制中也发挥了极大的作用,如年龄相关性黄斑变性白内障、葡萄膜炎、过早视网膜病变、角膜炎和眼部炎症。氧化蛋白水平升高与这些疾病相关的高炎症活动有关。由于持续暴露于大气中的氧气以及抗氧化剂在泪膜中的不稳定性而导致其支持不足,可在眼表面诱导增强的ros生成。而无论是在急性心肌梗死的缺血再灌注(ir)期间,还是在心肌梗死后的慢性重塑过程中,氧化应激均会严重损害心脏。线粒体内产生的活性氧(ros)是导致ir损伤的机制的特定驱动因素,包括诱导线粒体通透性转变或线粒体内结构和分子的氧化损伤。
[0004]
甲基黄嘌呤是一种分子化合物,这类化合物这对慢性阻塞性肺病,肺气肿和慢性支气管炎有治疗作用,其具有收缩支气管,促进气流,减轻炎症和放松气道等作用,而研究表明甲基黄嘌呤类药物还具有抗氧化应激的作用,如咖啡因是羟自由基和烷氧基的有效清除剂,可通过减少脂质过氧化来防止细胞损伤,其对阿尔茨海默病及晶状体免受ros光化学损伤的保护作用已被证实,而ta,与之具有类似的母核结构,因此,具有同等的抗氧化应激作用,对于醛的安全性来说,一般仅α-β不饱和醛可与dna形成加和物,进而产生毒性作用,如4-羟基壬烯醛(4-hne),但ta没有上述高反应性醛的结构特点,所以ta没有与高反应性醛相关的毒性。而多索茶碱的体内外抗炎作用也均被证实。但是现有技术中并未发现ta及其黄嘌呤醛类化合物等可通过醛的歧化反应产生对抗氧化应激的作用,ros激发机制的炎症损伤几乎是所有氧化应激损伤的重要过程,无论其是何种起因。而所述药物组合物用于治疗ros引起的氧化应激性脏器损伤如急性缺血性心肌梗死,心肌缺血再灌注损伤、炎性疾病、哮喘等的原理在于:ta与醛氧化酶(aldhs)、nad
的基本反应是,黄嘌呤醛类化合物(如茶碱乙醛、ta)主要经和aldhs(如aldh1a1和aldh2)催化,与nad
发生氧化代谢反应、生成相应的氧化产物(taa)。此时,黄嘌呤醛类化合物ta主要作为氢供体将氢转移至nad
上以生成nadh,进而发挥抗氧化作用,表明该组合本身就是一种极具开发潜力的抗氧化应激药物组合。
技术实现要素:
[0005]
解决的技术问题:为了克服现有技术的不足,本发明开发了与以往黄嘌呤类药物作用机制完全不同的全新抗氧化应激作用的药物组合物,该组合可直接生产抗氧化剂还原型烟酰胺腺嘌呤二核苷酸(nadh);该抗氧化剂无论在体内外模型中均具有抗哮喘、抗氧还应激等作用,可应用于许多相关性疾病,如内外源性哮喘、支气管哮喘、炎症因子升高为特征的气道上皮损伤和炎性哮喘亚型,或高氧化应激状态的疾病,如急性缺血性心肌梗死、心肌缺血再灌注损伤等。同时简化组合物配方、降低其副作用和毒性,提高其药效;鉴于此,本发明提供了含ta或其水合物的药物组合物及其制备方法和应用。
[0006]
技术方案:含茶碱乙醛(ta)或其水合物的药物组合物,所述药物组合物包括摩尔质量比为(1~2):(0.5~1):(2~5)的ta或其水合物、烟酰胺腺嘌呤二核苷酸(nad
)和醛脱氢酶(aldhs);
[0007]
其中,茶碱乙醛结构式为:
[0008]
茶碱乙醛水合物结构式为:
[0009]
aldhs为aldh1a1或aldh2。
[0010]
以上所述的含ta或其水合物的药物组合物的制备方法,所述方法采用溴代乙醛缩二甲醇亲电进攻茶碱的咪唑环,再用硫酸氢钾脱甲基后得到ta和其水合物,具体步骤如下:
[0011]
s1、7-(2,2-二甲氧基乙基)-1,3-二甲基-3,7-二氢-1h-嘌呤-2,6-二酮的合成
[0012]
以茶碱(tp)为反应底物,tp与溴代乙醛缩二甲醇的摩尔比为1:1~5,其中优选为1:1.3~1.6、tp与碳酸钾的摩尔比为1:1~10,其中优选为1:2~3、tp与碘化钾的摩尔比为1:0.1~3,其中优选为1:0.5~1、tp与三乙胺的摩尔比为1:1~6,其中优选为1:2~2.5、茶碱的质量与n,n-二甲基甲酰胺(dmf)的体积比为1g:3~30ml,其中优选为1g:(8~10)ml,油浴反应后旋蒸去除dmf,加水、二氯甲烷(dcm)萃取,洗涤、干燥过夜,抽滤、蒸干得棕色固体,然后分散于乙醚中打浆,抽滤得灰白色固体;
[0013]
s2、(2,2-二羟乙基)-1,3-二甲基-3,7-二氢-1h-嘌呤-2,6-二酮的合成
[0014]
向s1产物中加入硫酸氢钾、丙酮,水。所述s1产物与硫酸氢钾的摩尔比为1:2~15,其中优选为1:7~10,所述s1产物的质量与丙酮的体积比为1g:8~35ml,其中优选为1g:(15~20)ml,所述s1产物的质量与水的体积比为1g:5~50ml,其中优选为1g:(7.5~10)ml,油浴反应后冷却、抽滤,滤液蒸干、水重结晶得白色固体;
[0015]
s3、根据摩尔质量比(1~2):(0.5~1):(2~5)混合ta或其水合物、nad 和aldhs,制备获得含ta或其水合物的药物组合物。
[0016]
所述的药物、药物组合在制备抗氧化应激药物中的应用,包括摩尔质量比(1~2):(0.5~1):(2~5)的ta或其水合物:nad :aldh1a1重组单酶,主要用于ros引起的氧化应激性脏器损伤、炎性疾病、哮喘药物中的应用。
[0017]
优选的,所述的药物、药物组合在制备抗氧化应激药物中的应用,包括摩尔质量比2:1:5的ta或其水合物:nad
:aldh1a1重组单酶,主要用于ros引起的高氧化应激状态的疾病,如急性缺血性心肌梗死、心肌缺血再灌注损伤。
[0018]
优选的,如作为治疗氧化应激引起的抗缺水型干眼症,氧化应激引起的白内障的局部用药滴剂时,药物组合物包括茶碱乙醛、nad
,aldhs,其摩尔配比为(1~2):(0.5~1):(2~5),主要应用于由于ros引起的眼疾,如干眼症和白内障。
[0019]
优选的,所述的药物、药物组合在制备抗炎药物中的应用,包括摩尔质量比(1~2):(0.5~1):(2~5)的ta或其水合物:nad
:aldh1a1重组单酶,主要用于tnf-α升高的炎性疾病。
[0020]
优选的,所述的药物、药物组合及联用用药在制备抗哮喘药物中的应用,包括摩尔质量比2:1:5的ta或其水合物:nad
:aldh1a1重组单酶,主要用于反复发作的喘息、气急、胸闷或遗传导致的哮喘。
[0021]
优选的,所述的药物、药物组合在制备降低气道高反应性药物、减轻肺组织炎性程度药物、抑制肺部肥大细胞活化药物中的应用,其特征在于,包括摩尔质量比2:1:5的ta或其水合物:nad
:aldh1a1重组单酶,主要用于因气道炎症而处于过度反应状态,表现出敏感过强的支气管平滑肌收缩反应,引起气道狭窄和气道阻力增加,从而引发咳嗽、胸闷、呼吸困难和喘息等症状的疾病,如支气管哮喘。
[0022]
优选的,所述的药物、药物组合及联用用药在制备用于缓解外源性及内源性过敏性哮喘的药物中的应用,其特征在于,包括摩尔质量比2:(0.5~1):5的ta或其水合物:nad
:aldh1a1重组单酶,主要用于接触螨虫、花粉等过敏原诱发的急性哮喘,及感染导致的发
热、乏力等,这些症状会使呼吸调节异常,最后出现神经源性炎症,从而导致哮喘的发作。
[0023]
优选的,所述的药物、药物组合及联用用药在抑制血清中的ige水平和细胞因子il-4、il-5、il-13等水平升高的药物中的应用,其特征在于,包括摩尔质量比2:0.5:5的ta或其水合物:nad
:aldh1a1重组单酶,主要用于th2细胞活化及肥大细胞活化导致的il-4、il-5、il-13、ige水平升高为特征的气道上皮损伤及哮喘亚型。
[0024]
优选的,所述药物、药物组合是将ta、nad
和aldh1a1,与药学上可接受的辅料制成药物制剂。
[0025]
优选的,所述的药物制剂是滴剂、乳膏、凝胶、片剂、胶囊剂、喷雾剂、口服液或注射剂。
[0026]
优选的,其注射剂的制备方法如下:取各化合物1~10g,精密称定,置于烧杯中,加入50%乙醇50ml,加入羟丙基β环糊精70g,充分搅拌至完全溶解,再搅拌1h,于旋转蒸发器上减压浓缩至干燥,过60目筛,即得,配方中各化合物单独制备成等摩尔浓度的制剂,使用时按所需比例调整用量。
[0027]
优选的,其口服固体制剂制备方法如下:取各药物组合物1-10g,精密称定,置于烧杯中,加入50%乙醇50ml,加入7倍量的羟丙基-β-环糊精,充分搅拌至完全溶解,再搅拌1h,于旋转蒸发器上减压浓缩至干燥,过80目筛,即得。配方中各化合物单独制备成等摩尔浓度的制剂,使用时按所需比例调整用量。称取干燥粉碎过筛的羟丙基-β-环糊精80g,加入淀粉50g,微晶纤维素20g,硬脂酸镁2.5g,混合均匀,
[0028]
优选的,所述的药物制剂是眼部局部用药滴剂,药物组合物包括ta、nad
、催化重组单酶aldh1a1,摩尔比为(1~2):(0.5~1):(2~5);将组合物至于一个粘性载体内,该载体包括去离子水溶液,0.01%的乙二胺四乙酸,氯化钠和氢氧化钠以调节眼药水粘度和ph值维持在7.4,1%抗坏血酸,抗坏血酸可作为该混合物的抗氧化防腐剂。
[0029]
有益效果:(1)本发明所述药物组合物通过黄嘌呤醛代谢反应增加细胞内抗氧化物nadh的生成,进而多通路的抑制氧化应激的发生和发展,可应用于制备ros所致的高氧化应激性脏器损伤,如心肌缺血再灌注损伤、眼疾、炎症、哮喘等的药物领域,本发明丰富了制备抗氧化应激、抗炎等相关药物类型,为氧化应激性脏器损伤、炎性疾病的药物制备提供了全新的选择和策略;(2)所述药物组合物成分简单、副作用下、毒性低。
附图说明
[0030]
图1为ta及其水合物的1hnmr谱图
[0031]
图2为ta在hepg2细胞上的毒性评价,结果显示在48h内,5-60μm的ta对hepg2细胞的存活率均无影响。
[0032]
图3为等摩尔的ta和nad
或nad
、aldh1a1合用(1:1:1)可显著增加细胞内的nadh含量。
[0033]
图4为ta的抗炎活性评价,表明lps组的tnf-α可显著升高,表明模型成功,而10μmta 20μm nad
20μm aldh1a1组的tnf-α释放明显降低,表明ta、nad
、aldh1a1(1:2:2)的联用可抑制lps诱导的tnf-α释放。
[0034]
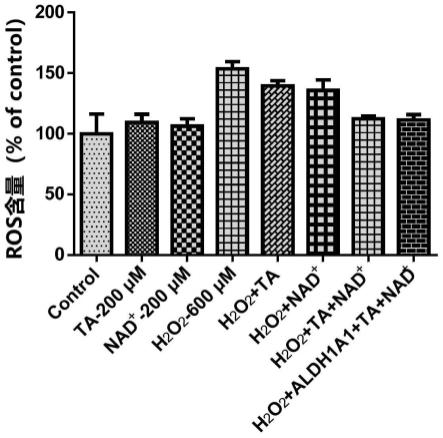
图5为ta的抗氧化应激作用评价,ta和nad 或nad 、aldh1a1合用可抑制h2o2诱导的细胞内ros含量。
[0035]
图6为哮喘大鼠各给药组血清中ige的检测结果,表明模型组ige明显升高,而给药组有所降低,表明ta和nad
或nad
、aldh1a1合用可抑制哮喘大鼠血清中ige的释放
[0036]
图7为哮喘大鼠各给药组血清中il-5的检测结果,表明ta和nad
或nad
、aldh1a1合用可明显抑制哮喘大鼠血清中il-5的释放。
[0037]
图8为哮喘大鼠各给药组肺泡灌洗液中il-5的检测结果,表明ta和nad
或nad
、aldh1a1合用可明显抑制哮喘大鼠balf中il-5的释放。
[0038]
图9为干眼症小鼠各给药组角膜上皮细胞凋亡的检测结果,表明ta、nad
和aldh1a1重组单酶(1~2):(0.5~1):(2~5)的联用可抑制哮喘小鼠因氧化应激引起的干眼症。
具体实施方式
[0039]
以下实施例进一步说明本发明的内容,但不应理解为对本发明的限制。在不背离本发明精神和实质的情况下,对本发明方法、步骤或条件所作的修改和替换,均属于本发明的范围。若未特别指明,实施例中所用的技术手段为本领域技术人员所熟知的常规手段。
[0040]
实施例1
[0041]
含茶碱乙醛或其水合物的药物组合物,所述药物组合物包括摩尔质量比为(1~2):(0.5~1):(2~5)的茶碱乙醛或其水合物、nad
和aldhs;
[0042]
其中,茶碱乙醛结构式为:
[0043]
茶碱乙醛水合物结构式为:
[0044]
aldhs为aldh1a1或aldh2。
[0045]
以上所述的含ta或其水合物的药物组合物的制备方法,所述方法采用溴代乙醛缩二甲醇亲电进攻茶碱的咪唑环,再用硫酸氢钾脱甲基后得到ta和其水合物,具体步骤如下:
[0046]
s1、7-(2,2-二甲氧基乙基)-1,3-二甲基-3,7-二氢-1h-嘌呤-2,6-二酮的合成
[0047]
以茶碱(tp)为反应底物,tp与溴代乙醛缩二甲醇的摩尔比为1:1~5,其中优选为1:1.3~1.6、tp与碳酸钾的摩尔比为1:1~10,其中优选为1:2~3、tp与碘化钾的摩尔比为1:0.1~3,其中优选为1:0.5~1、tp与三乙胺的摩尔比为1:1~6,其中优选为1:2~2.5、茶碱的质量与n,n-二甲基甲酰胺(dmf)的体积比为1g:3~30ml,其中优选为1g:(8~10)ml,油浴反应后旋蒸去除dmf,加水、二氯甲烷(dcm)萃取,洗涤、干燥过夜,抽滤、蒸干得棕色固体,然后分散于乙醚中打浆,抽滤得灰白色固体;
[0048]
s2、(2,2-二羟乙基)-1,3-二甲基-3,7-二氢-1h-嘌呤-2,6-二酮的合成
[0049]
向s1产物中加入硫酸氢钾、丙酮,水。所述s1产物与硫酸氢钾的摩尔比为1:2~15,
其中优选为1:7~10,所述s1产物的质量与丙酮的体积比为1g:8~35ml,其中优选为1g:(15~20)ml,所述s1产物的质量与水的体积比为1g:5~50ml,其中优选为1g:(7.5~10)ml,油浴反应后冷却、抽滤,滤液蒸干、水重结晶得白色固体。氢谱有关资料如下:1h-nmr(400mhz,cdcl3),δ:7.95(s,1h),6.17(s,2h),5.05(t,j=4.8hz,1h),4.16(d,j=5.4hz,2h),3.43(s,3h),3.23(s,3h).图谱如图1所示。
[0050]
实施例2
[0051]
实施例1所述的药物组合物可显著增加细胞内nadh含量,进而达到抗氧化应激或抗炎的作用,其结果如下:
[0052]
(1)ta的毒性评价(cck8实验)
[0053]
hepg2细胞计数后按照5x104个/ml的密度铺于96孔板中,培养24h后用无菌pbs洗净完全培养基,加入5-60μm基础培养基配置的ta溶液,并于加药48h后采用cck8发检测其细胞存活率,并对茶碱乙醛的毒性做出评价。
[0054]
(2)ta、nad 及aldh1a1重组单酶组合使用可增加细胞内nadh含量
[0055]
hepg2细胞计数后按照5x105个/ml的密度铺于6孔板中,培养24h后用无菌pbs洗净完全培养基,加入基础培养基配置的含100μm的ta、100μm的nad
、100μm的aldh1a1及三者的混合药物溶液,并于加药48h后采用nad
/nadh检测试剂盒(碧云天,s0175)提取细胞中的nadh,并对其含量进行检测。
[0056]
(3)ta药物组合的抗炎活性评价
[0057]
raw264.7细胞计数后按照1x106个/ml的密度铺于6孔板中,培养4h后更换基础培养基及继续培养2h,然后分别加入10μm的ta、20μm的nad
、20μm的aldh1a1继续培养4h,4h结束后,各组分别加入lps(终浓度为100ng/ml),细胞继续培养4h,后收集细胞培养上清,采用elisa试剂盒测定上清中tnf-α释放水平
[0058]
(4)ta和nad
或nad
、aldh1a1合用可减少细胞内ros含量
[0059]
hepg2细胞计数后按照5x105个/ml的密度铺于6孔板中,培养24h后用无菌pbs洗净完全培养基,分别加入基础培养基配置的含200μm的ta、200μm的nad
、600μm的h2o2、200μm ta 600μm h2o2、200μm nad
600μm h2o2、200μm ta 200μm nad
600μm h2o2和200μm ta 200μm nad
200μm aldh1a1 600μm h2o2,并于加药48h后采用荧光探针dcfh-da对细胞内的ros含量进行检测。
[0060]
实施例3 ta和nad
或nad
、aldh1a1合用对哮喘大鼠的治疗
[0061]
大鼠适应性喂养1周,按体质量由小到大编号,采用完全随机法分为正常组、模型组、ta组、nad
组、模型 ta醛组、模型 ta nad
组、模型 aldh1a1、ta nad
组,每组各10只。
[0062]
哮喘模型制备于正式开始实验的第1d及第8d,给予模型组、ta组、nad
组、模型 ta组、模型 ta nad
组大鼠腹腔注射卵蛋白(ova)混合液1ml(ova 100mg、氢氧化铝100mg加生理盐水1ml,对其进行致敏,2周后(即第15天)将大鼠置于透明密闭容器中用2%ova雾化吸入15min,诱发哮喘发作,隔天1次,引喘2周。正常组以1ml生理盐水代替ova腹腔注射,第15天给予生理盐水雾化吸入15min,隔天1次。引喘开始后,正常组及模型组每天静脉注射等量生理盐水,ta组、nad
组、模型 ta组、模型 ta nad
组在每次ova激发前30min给予ta或ta和aldh1a1、nad
组合物溶液尾静脉注射(ta剂量:30mg/kg、nad
剂量:30mg/kg、aldh1a1剂量:60mg/ml)。最后一次激发24小时候处死大鼠,以研究ta及ta和aldh1a1、nad
组合物对哮喘
大鼠的治疗作用。
[0063]
末次雾化激发24h后以10%水合氯醛(10ml/kg)腹腔注射麻醉大鼠,眼眶静脉取血,静置后,4℃离心(3000rpm/min)10min,分离血清,分装后置于-80℃备用。喉镜行气管插管,将其与肺功能仪固定,进行肺功能测定,结果如表1所示,肺功能结果表示,同control组比较,ova模型组大鼠i(气道高反应性)、rn(中心气道阻力)和g(组织阻尼)均升高,而给予ta、nad
或与aldh1a1的组合后,其有所降低,而crs(动态顺应性)在各组之间则无明显变化,表明ta和nad
或aldh1a1、nad
的联合给药明显改善了气道高反应性、同时降低了中心气道的阻力及组织阻尼。
[0064]
表1大鼠肺功能检测结果
[0065][0066]
收集各组大鼠肺泡灌洗液(balf),elisa法测定balf中细胞因子的含量。大鼠眼眶取血,elisa法测定血清中细胞因子的含量。各给药组血清中ige的检测结果如图6,表明模型组ige明显升高,而给药组有所降低,表明ta和nad
或nad
、aldh1a1合用可抑制哮喘大鼠血清中ige的释放。各给药组血清和balf中il-5的检测结果如图7和8所示,表明ta和nad
或nad
、aldh1a1合用可明显抑制哮喘大鼠血清和balf中ige的释放。
[0067]
实施例4 ta眼药水对干眼症小鼠的治疗
[0068]
小鼠适应性喂养1周,将60只小鼠按体质量由小到大编号,采用完全随机法分为空白对照组、空白ta组、空白nad 组、ded模型组、ded模型 nad 组、ded模型 ta组、ded模型 ta眼药水组,每组各3只。(其中ta:200μm、nad
:200μm、aldh1a1单酶:0.05mg/ml)
[0069]
ded小鼠模型制备于正式开始实验的第1w及第6w,给予ded模型组、ded模型 ta组、ded模型 nad 组、ded模型 ta眼药水组双眼滴加浓度为0.2%苯扎氯铵溶液(每眼5μl,每日1次,连续滴眼6周),采用泪液检测滤纸检测小鼠的泪液分泌量以评价干眼症模型成功与否。
[0070]
模型成功后,空白对照组给予空白基质溶液、空白ta组给予空白基质溶液 ta、空白nad
组给予空白基质溶液 nad
,ded模型组给予空白基质溶液,ded模型 nad
组给药空白基质溶液和nad
,ded模型 ta组给药空白基质溶液和ta,ded模型 ta眼药水组给药ta眼药水(所有实验,每眼5μl,每日3次,连续6天)。为了避免由于测试试剂的蒸发而造成误差,所有测试试剂都是通过移液器直接涂抹在角膜顶点。处死动物后剖取角膜,收集的组织样本来评估为对药物治疗的组织学变化。由氧化应激和炎症引起的干眼症会导致泪液渗透压升高然后引发角膜上皮细胞凋亡,我们实验发现,相比较空白组,在ded模型中用过ta眼药水治疗后也能明显减少角膜上皮细胞的凋亡(相对ded组的tunel的细胞核染色比例下降)。详
见图9
[0071]
星号表示治疗组与ded组(*p《0.05,**p《0.005,***p《0.001)相比有统计学意义的差异。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。