一种靶向g-四链体多肽类pet显像剂及其制备方法与应用
技术领域
1.本发明属于制药领域,具体涉及一种靶向g-四链体多肽类pet显像剂及其制备方法与应用。
背景技术:
2.恶性肿瘤(癌症)作为全球最大的公共卫生问题之一,传统的癌症治疗方法主要包括手术治疗、化学治疗及放射治疗等。对于非实体瘤、全身广泛转移的癌症存在不能进行有效的手术治疗及放疗,同时化疗的方法也存在副作用大、特异性差、疗效低等问题,难以满足临床治疗的需求。针对特定致癌基因、蛋白或受体的分子靶向治疗相较普通化疗具有特异性强、疗效显著,同时副作用明显小的优点,现已逐渐成为临床肿瘤治疗的重要手段之一。近年来,抗肿瘤新药物的研发已经取得了较大进展,大量新靶点及新靶点药物被开发应用,其中以g-四链体为靶点的抗肿瘤药物的研究引起了人们的广泛关注。
3.g-四链体(g-quadruplex)是一种可以在富含鸟嘌呤(g)的核酸序列中形成的一种非典型结构,dna单链通过g碱基间的氢键作用形成平面的g-四分体,两层或以上的四分体经过π-π堆积最终形成g-四链体螺旋结构。人体大约有70万个可以形成g-四链体的基因序列,主要包括端粒末端、基因的突变热点区、基因的启动子区(如:bcl-2、c-myc、c-myb、c-kit、kras、vegf和vegfr),涵盖了衰老、凋亡、生长因子及其受体、转录调控因子、信号转导因子相关的基因,在细胞衰老、增殖、凋亡及肿瘤形成中起着重要作用。在肿瘤组织中,当特异性配体与这些基因序列形成的g-四链体结合后,导致相应生化过程发生变化(如端粒酶活性被抑制、癌基因转录水平下调等),从而达到抗肿瘤的效果,这些可能的生物学功能和其独特的结构特征,使g-四链体成为一个抗肿瘤药物的重要靶点。
4.正电子发射计算机断层显像(positron emission tomography pet)已被广泛用于多种疾病的诊断与鉴别诊断、疗效评价、脏器功能研究和新药开发等方面。临床应用最多的广谱肿瘤显像剂
18
f-fdg在肿瘤检测中存在常出现假阳性、不能区分肿瘤和炎症等问题,虽然目前多种新型特异性靶点(如psma、fap、egfr等)的pet显像剂被开发研究及应用,更多的新靶点也在被尝试开发相关pet显像剂,但这类pet显像剂依然存在易出现假阳性、不能区分肿瘤和炎症等问题。g-四链体的靶点性质决定了靶向g-四链体的特异性pet/ct显像具有实时、无创、在体明确肿瘤病灶分布,能进行实体瘤的早期诊断、肿瘤分期、术前定位、术后对比及疗效监测,可用于制定个性化治疗方案,指导手术或靶向治疗的潜力。同时以g-四链体为靶点的pet显像在指导此类新型肿瘤药物的研发、药效评估、敏感人群筛选等方面有重要的研究及应用前景,因此开发一种新型的靶向g-4链体的相关pet探针对生物学功能显像具有重要的意义。
技术实现要素:
5.为了克服上述现有技术存在的问题,本发明的目的之一在于提供一种靶向g-四链体多肽类pet显像剂;本发明的目的之二在于提供这种靶向g-四链体多肽类pet显像剂的制
备方法;本发明的目的之三在于提供这种靶向g-四链体多肽类pet显像剂的应用。
6.为了实现上述目的,本发明所采取的技术方案是:
7.本发明第一方面提供一种靶向g-四链体多肽类pet显像剂,所述靶向g-四链体多肽类pet显像剂的结构如式(i)或式(ⅱ)所示:
[0008][0009]
式(i)中,r1表示金属离子螯合基团,m表示放射性金属核素,n选自正整数;
[0010]
式(ⅱ)中,r2表示金属离子螯合基团,a表示放射性金属核素,b选自正整数。
[0011]
优选的,所述放射性金属核素m
n
或a
b
分别独立选自
68
ga
3
、[al
18
f]
2
、
64
cu
2
、
177
lu
3
;进一步优选的,所述放射性金属核素m
n
或a
b
分别独立选自
68
ga
3
、[al
18
f]
2
、
64
cu
2
。
[0012]
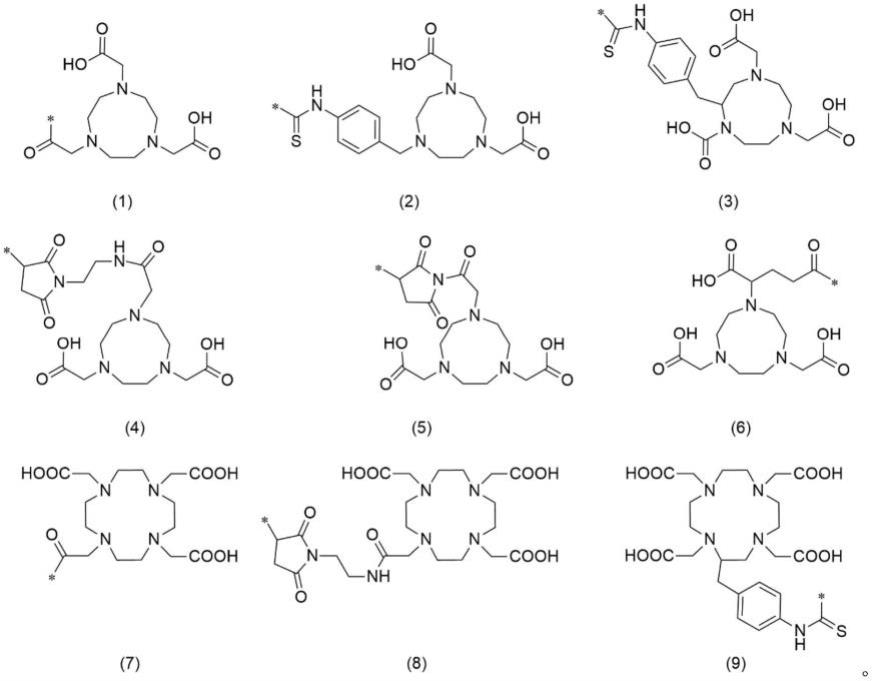
优选的,所述金属离子螯合基团r1或r2分别独立选自如式(1)-式(9)所示的结构:
[0013][0014]
优选的,所述式(1)为1,4,7-三氮杂环九烷基-4,7-二乙酸基-1-乙酰基(-nota)。
[0015]
优选的,所述式(2)为1-(4-异硫氰基苄基)-1,4,7-三氮杂环九烷基-4,7-二乙酸(p-scn-bn-noda)。
[0016]
优选的,所述式(3)为2-(4-异硫氰基苄基)-1,4,7-三氮杂环九烷-1,4,7-三乙酸(p-scn-bn-nota)。
[0017]
优选的,所述式(4)为1-(2-(2-(2,5-二氧代-1-吡咯烷基)乙氨基)酰乙基)-1,4,7-四氮杂环九烷-4,7-二乙酸(mai-noda)。
[0018]
优选的,所述式(5)为1-(2-(2,5-二氧代-1-吡咯烷基)酰乙基)-1,4,7-四氮杂环九烷-4,7-二乙酸。
[0019]
优选的,所述式(6)为2-((4,7-二羧甲基)-1,4,7三氮杂环九烷)基戊二酸。
[0020]
优选的,所述式(7)为1,4,7,10-四氮杂环十二烷基-4,7,10-三乙酸基-1-乙酰基(-dota)。
[0021]
优选的,所述式(8)为1-(2-(2-(2,5-二氧代-1-吡咯烷基)乙氨基)酰乙基)-1,4,7,10-四氮杂环九烷-4,7,10-三乙酸(mai-noda)。
[0022]
优选的,所述式(9)为2-(4-异硫氰基苄基)-1,4,7,10-四氮杂环十二烷-1,4,7,10-四乙酸(p-scn-bn-dota)。
[0023]
优选的,所述靶向g-四链体多肽类pet显像剂包括如下所示结构的化合物;
[0024]
[0025][0026]
优选的,所述多肽结构中氨基酸为l型氨基酸。
[0027]
优选的,所述多肽的氨基酸序列为krivklikkwlr。
[0028]
本发明第二方面提供根据本发明第一方面所述靶向g-四链体多肽类pet显像剂的制备方法,包括以下步骤:
[0029]
将pet显像剂前体与放射性金属核素在缓冲溶液中反应,得到所述的靶向g-四链体多肽类pet显像剂。
[0030]
优选的,所述缓冲溶液包括醋酸钠、醋酸铵、醋酸钾、盐酸、醋酸中的至少一种;进一步优选的,所述缓冲溶液为醋酸钠。
[0031]
优选的,所述缓冲溶液的浓度为0.05mol/l-0.7mol/l;进一步优选的,所述缓冲溶液的浓度为0.1mol/l-0.6mol/l。
[0032]
优选的,所述反应在ph值为3.5-7.0条件下进行;进一步优选的,所述反应在ph值为4.0-5.5条件下进行。
[0033]
优选的,所述反应的温度为80℃-120℃;进一步优选的,所述反应的温度为90℃-110℃。
[0034]
优选的,所述反应的时间为8min-40min;进一步优选的,所述反应的时间为10min-30min。
[0035]
优选的,所述反应后还包括将靶向g-四链体多肽类pet显像剂分离提纯的步骤。
[0036]
优选的,所述分离提纯包括使用hlb小柱或sep-pak c18小柱将靶向g-四链体多肽类pet显像剂分离纯化。
[0037]
本发明第三方面提供根据本发明第一方面所述靶向g-四链体多肽类pet显像剂在生物学功能显像中的应用。
[0038]
优选的,所述生物学功能显像包括疾病生物学功能显像。
[0039]
优选的,所述疾病包括肿瘤。
[0040]
优选的,所述肿瘤包括脑胶质瘤、肺癌或乳腺癌中的至少一种。
[0041]
本发明的有益效果是:
[0042]
本发明公开了一种靶向g-四链体多肽类pet显像剂,该pet显像剂是优良的药代动力学新型探针,其结构包括多肽、金属螯合基团和放射性金属核素,其制备方法简便快捷,产率较高,该pet显像剂稳定性好、水溶性强,体内血液清除快,主要经肾脏、肝脏代谢,能靶向特异性摄取于肿瘤部位,该pet显像剂可广泛应用于生物学功能显像中。
附图说明
[0043]
图1为前体nota-kr12c的hplc图谱。
[0044]
图2为前体nota-kr12c的高分辨质谱图。
[0045]
图3为靶向g-四链体多肽类pet显像剂[
18
f]alf-nota-kr12c的放射性hplc图谱。
[0046]
图4为靶向g-四链体多肽类pet显像剂[
68
ga]nota-kr12c的放射性hplc图谱。
[0047]
图5为[
18
f]alf-nota-kr12c注射液在体外pbs 2h时的放射性hplc图谱。
[0048]
图6为[
18
f]alf-nota-kr12c注射液在体内血清1h时的放射性hplc图谱。
[0049]
图7为[
18
f]alf-nota-kr12c在昆明鼠体内60分钟的生物分布图。
[0050]
图8为[
18
f]alf-nota-kr12c在u87荷瘤鼠中120分钟内不同时间点mico-pet/ct显像图。
[0051]
图9为[
18
f]alf-nota-kr12c在脏器不同时间点%id/g值随时间变化图。
[0052]
图10为[
18
f]alf-nota-kr12c在u87荷瘤鼠中60分钟mico-pet/ct显像图和竞争抑制显像图。
64
cucl2溶液(约5mci),用0.1mol/l乙酸钠缓冲溶液调节ph值至4.0-6.5,100℃加热反应10min~30min。冷却并加入注射用水4ml混匀,转移至hlb柱。用10ml
×
2注射用水冲洗hlb柱并吹干。然后,用1ml乙醇洗脱产品并用生理盐水将其稀释成含5%乙醇的产品溶液,得到符合要求的[
64
cu]nota-kr12c(r为2-(4-异硫氰基苄基)-1,4,7-三氮杂环九烷-1,4,7-三乙酸(p-scn-bn-nota))注射液。[
64
cu]nota-kr12c未校正放射化学产率为70%~95%,总放射合成时间为30min。
[0066]
实施例4
[0067]
前体dota-kr12c的制备步骤如下:
[0068]
采用l型氨基酸为原料,通过固相多肽合成法合成kr12c多肽,金属离子螯合基团为1,4,7,10-四氮杂环十二烷基-4,7,10-三乙酸基-1-乙酰基(-dota),在n端的赖氨酸(lys)的侧链氨基与dota连接,利用制备型hplc分离纯化收集产品峰后冻干即得dota-kr12c前体。
[0069]
靶向g-四链体多肽类pet显像剂[
68
ga]dota-kr12c的制备步骤如下:
[0070]
在含50μl前体dota-kr12c溶液(金属离子螯合基团为2,4,7,10-四氮杂环十二烷基-4,7,10-三乙酸基-1-乙酰基(-dota),1μg/μl)的反应管中加入0.25mol/l乙酸钠溶液900μl。从
68
ge/
68
ga发生器中用0.05mol/l盐酸4ml洗脱
68
gacl3至上述反应管中,混匀,溶液ph为4.0,100℃加热反应10-30min左右。冷却并加入注射用水5ml混匀,转移至hlb柱。用10ml
×
2注射用水冲洗hlb柱并吹干。然后,用乙醇1ml洗脱产品并用生理盐水将其稀释成含5%乙醇的产品溶液,得到符合要求的[
68
ga]dota-kr12c(r为1,4,7,10-三氮杂环十二烷基-4,7,10-三乙酸基-n-乙酰基)注射液。[
68
ga]dota-kr12c未校正放射化学产率为70%~95%,总放射合成时间为30min。
[0071]
实施例5
[0072]
靶向g-四链体多肽类pet显像剂[
64
cu]dota-kr12c的制备步骤如下:
[0073]
在反应管中依次加入50μl实施例4制备的dota-kr12c(金属离子螯合基团为2,4,7,10-四氮杂环十二烷基-4,7,10-三乙酸基-1-乙酰基(-dota),1μg/μl)和1.0ml 64
cucl2溶液(约5mci),用0.1mol/l乙酸钠缓冲溶液调ph至4.0-6.5,100℃反应10min~30min。冷却并加入注射用水4ml混匀,转移至hlb柱。用10ml
×
2注射用水冲洗hlb柱并吹干。然后,用乙醇1ml洗脱产品并用生理盐水将其稀释成含5%乙醇的产品溶液,得到符合要求的[
64
cu]dota-kr12c注射液。[
64
cu]dota-kr12c未校正放射化学产率为80%~95%。
[0074]
性能检测
[0075]
1.放射化学纯度和稳定性的测定
[0076]
用高效液相色谱(hplc)测定药物注射液的放射化学纯度及稳定性。hplc分析条件:分析柱为zorbax eclipse xdb-c18柱;流动相:a相为0.1%三氟乙酸(tfa)的水溶液,b相为0.1%tfa的乙腈溶液。淋洗梯度为:0-2min,a相85%,b相15%,流速1ml/min;2min-20min,a相降至5%,b相升至95%,流速1ml/min;20min-22min,a相升至85%,b相降至15%,流速1ml/min;22min-30min,a相85%,b相15%,流速1ml/min。紫外检测波长220nm,放射性检测器为lablogic systems ltd。
[0077]
为了检测显像剂在体外的稳定性,分别测试[
18
f]alf-nota-kr12c在pbs(ph=7.4)与小鼠血清中的稳定性。
[0078]
取2ml pbs(ph=7.4)缓冲液与50μci显像剂充分混合,在孵箱中37℃孵育2h,取少量溶液,通过hplc检测显像剂稳定性,以上实验重复4次。图5为[
18
f]alf-nota-kr12c注射液在体外pbs 2h时的放射性hplc图谱。
[0079]
取体重22g左右昆明鼠,尾静脉注射[
18
f]alf-nota-kr12c注射液300μci,正常摄取1h后,摘眼取血1.5ml,12000转/分下离心5min,取上清液进行hplc分析,流动相每0.5分钟收集一管,然后利用伽马计数器测定放射性计数,通过origin作图得到探针体内血液中稳定性hplc图。图6为[
18
f]alf-nota-kr12c注射液在体内血清1h时的放射性hplc图谱。
[0080]
图5和图6结果表面[
18
f]alf-nota-kr12c在体外(pbs)、体内(血清)中均100%以原型稳定存在。
[0081]
2.酯水分配系数测试
[0082]
取10μl配制好的[
18
f]alf-nota-kr12c注射液于装有1ml正辛醇与990μl水的2.5ml离心管中,密闭置于干式恒温器中常温震荡10min,静置10min使两相分层,用移液器从两相中分别各取500μl置于γ计数管中,用γ计数器测定计数。平行进行两批次实验,每批重复三次。根据公式1计算得到log p值。
[0083][0084]
公式1中,counts in water表示水相中放射性计数;counts in 1-octanol表示正辛醇相中放射性计数;log取以10为底的对数。
[0085]
通过放射性技术方法测定[
18
f]alf-nota-kr12c的脂水分配系数log p为-2.409
±
0.173,说明显像剂为水溶性物质,具有较好的亲水特性,预测体内摄取与显像剂主要经肾脏代谢,其他软组织摄取可能较低,显像背景摄取比较低。
[0086]
3.[
18
f]alf-nota-kr12c体内生物分布测试
[0087]
实施例1制备得到的靶向egfr的多肽类pet显像剂[
18
f]alf-nota-kr12c后,在4只正常昆明鼠中分别经尾静脉注射30μci显像剂后,正常饲养摄取1h后,处死小鼠,取血及脑、心、肺、肝脏、肾脏等主要脏器与组织称重并进行γ计数,研究显像剂在小鼠体内的生物分布情况。图7为[
18
f]alf-nota-kr12c在昆明鼠体内60分钟的生物分布图。结果显示药物主要经肾脏代谢,血液清除速度快,骨中放射性不高,药物在体内不脱氟。
[0088]
4.micro pet/ct显像测试
[0089]
micro-pet/ct显像研究利用siemens inveon micro-pet/ct,采集工作站为inveon acquirision workplace(iaw)2.2,数据分析工作站为inveon research workplace(irw)。取脑胶质瘤u87、宫颈癌细胞hela以5
×
106/只的密度进行裸鼠皮下接种,待肿瘤直径生长至10mm-15mm时,进行显像剂研究。
[0090]
动态显像:取u87荷瘤鼠经10%水合氯醛麻醉后固定于扫描床上,并建立好方法让床位位于pet视野,取[
18
f]alf-nota-kr12c注射液200μci左右,经尾静脉注射,注射的同时点击“start”按钮,持续扫描120分钟。
[0091]
静态显像:取[
18
f]alf-nota-kr12c注射液200μci左右,经尾静脉注射入u87或hela荷瘤鼠体内,常规摄取40分钟后注射0.1ml 10%水合氯醛,之后行常规pet/ct显像。
[0092]
抑制显像:其他操作同“动态显像”“静态显像”,在注射药物中加入250μg kr12c多
肽。
[0093]
图8为[
18
f]alf-nota-kr12c在u87荷瘤鼠中120分钟内不同时间点mico-pet/ct显像图,其中,图8上方依次为肿瘤部位横断面的ct图、15min pet图、30min pet图、60min pet图、90min pet图、120min pet图;图8下方依次为肿瘤部位冠状面ct图、15min pet图、30min pet图、60min pet图、90min pet图、120min pet图。图9为[
18
f]alf-nota-kr12c在脏器不同时间点%id/g值随时间变化图。图10为[
18
f]alf-nota-kr12c在u87荷瘤鼠中60分钟mico-pet/ct显像图和竞争抑制显像图,其中,左上方为摄取ct图,右上方为摄取pet图,左下方为抑制ct图,右下方为抑制pet图。图11是[
18
f]alf-nota-kr12c在hela荷瘤鼠中60分钟mico-pet/ct显像图和竞争抑制显像图,其中,左上方为摄取ct图,右上方为摄取pet图,左下方为抑制ct图,右下方为抑制pet图。
[0094]
pet显像结果表明:[
18
f]alf-nota-kr12c在u87和hela荷瘤鼠肿瘤中具有较高摄取,同时肿瘤部位摄取量明显高于肌肉、肺、肠等脏器或组织。动态显像显示探针体内血液清除快,主要经肾脏、肝脏代谢,各脏器的时间动态图发现肿瘤/肌肉比值在60分钟左右时较高,故最佳显像时间选择60分钟,60分钟抑制显像结果发现,肿瘤/肌肉比明显下降,表明探针在肿瘤部位为特异性摄取。显像结果表明显像剂可特异性摄取于肿瘤部位,具有较好的应用前景。
[0095]
本实施例以kr12c多肽结构为药效基团,连接一金属离子螯合基团构建前体,利用放射性金属核素m
n
标记构建如[m
n
]nota-kr12c或[m
n
]dota-kr12c的探针,结构如式(i)所示,以获得一类特异性靶向g-四链体多肽类pet显像剂;
[0096][0097]
式(i)中,r1表示金属离子螯合基团,m表示放射性金属核素,n选自正整数。
[0098]
本技术实施例还可以在kr12c多肽赖氨酸(lys)n端修饰一个半胱氨酸(cys)后,将半胱氨酸的巯基侧链与金属离子螯合基团(如nota或dota类似物)反应构建前体,然后与放射性金属核素a
b
在缓冲溶液中反应,得到[a
b
]nota-kr12c或[a
b
]dota-kr12c,如式(ⅱ)所示的靶向g-四链体多肽类pet显像剂;
[0099][0100]
式(ⅱ)中,r2表示金属离子螯合基团,a
b
表示放射性金属核素,b选自正整数。
[0101]
[m
n
]nota-kr12c、[m
n
]dota-kr12c、[a
b
]nota-kr12c或[a
b
]dota-kr12c探针具备成为诊断恶性肿瘤的有用工具的条件,为治疗方案的确定及疗效监测提供有力影像学佐证。
[0102]
上述实例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其它的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。