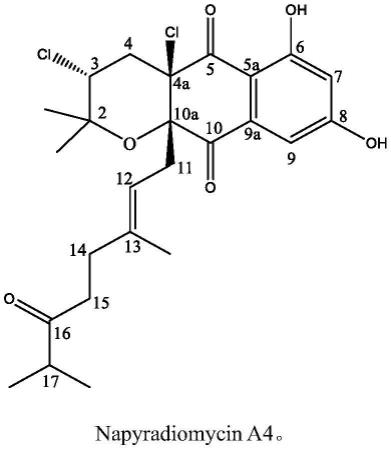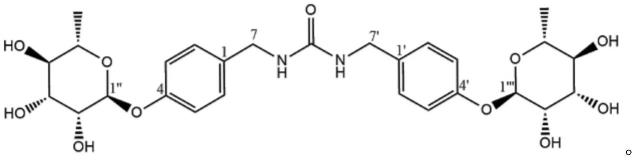
1.本发明涉及医用药物技术领域,具体为一种具有抗流感病毒活性的辣木籽提取物。
背景技术:
2.辣木籽为辣木科(moringaceae)辣木属(moringa adans)植物辣木树的种子,具有广泛的食用和药用价值。辣木籽原产于印度,已有近千年的栽种和食用历史,在非洲、热带、亚热带地区均有种植。上世纪初从缅甸引种到我国云南省芒市,开始大面积种植,近年来我国长江以南各省区均对其开展了大量种植。国内外研究表明,辣木籽中含有丰富的油脂、蛋白质、维生素等营养物质,此外还含有黄酮、酚酸、生物碱、异硫氰酸盐、硫代氨基甲酯天然活性成分,具有降低血脂、血糖、增强人体免疫、杀菌、抗病毒等生理功能。抗病毒研究方面,国外有文献报道辣木籽叶提取物对带状疱疹病毒、艾滋病毒和乙肝病毒表现出较好的抑制作用,但关键活性成分不清楚。
3.流感病毒是对人类健康威胁最大的呼吸道病毒,每年导致数百万人发生上呼吸道感染。由于流感病毒的高突变率以及病毒之间的重组,目前主要治疗和预防流感病毒的两类化学药物m2离子通道阻滞剂和神经氨酸酶抑制剂均面临着严峻的耐药形势,如l26f、v27a、s31n等流感病毒突变株对金刚烷胺类m2离子通道阻滞剂表现出严重耐药;h1n1或h5n1的h274y亚型、h3n2-e119v亚型等流感病毒对奥司他韦、帕拉米韦等神经氨酸酶抑制剂出现耐药。已有抗流感药物难以应对多变的流感病毒。疫苗虽是针对人类预防和治疗病毒感染的核心药物,但某些人畜共患的冠状病毒,针对人的疫苗也无法根除,同时流感病毒极高的基因重配效率使其对疫苗也表现出逃逸现象。因此,新型作用机制抗流感病毒药物的研发尤为迫切。
技术实现要素:
4.本发明的目的在于克服上述背景技术困难,解决流感病毒的高突变率以及病毒之间的重组,导致目前主要治疗和预防流感病毒的化学药物面临着严峻的耐药形势,疫苗对人畜共患的冠状病毒也无法根除,提供一种具有抗流感病毒活性的辣木籽提取物。
5.为达到上述目的,采用的技术方案为:一种具有抗流感病毒活性的辣木籽提取物,所述辣木籽提取物命名为moringa a,其化学结构为:
[0006][0007]
进一步的,所述辣木籽提取物moringa a是从辣木籽甲醇提取物-丙酮萃取相中获得。
[0008]
进一步的,所述辣木籽提取物moringa a的制备方法:30kg干燥辣木籽粉碎至细
粉,用甲醇回流提取2次,每次2h;合并滤液后用布氏漏斗抽滤合并,减压回收甲醇,烘箱干燥后得辣木籽粗提物;将所得粗提物用甲醇溶解后与10倍量80-100目硅胶进行拌样,减压旋干成粉末,经硅胶柱层析(80-100目),将不同极性成分分开,依次用石油醚、氯仿、乙酸乙酯、丙酮和甲醇5种溶剂洗脱;收集丙酮洗脱液,减压回收丙酮,得丙酮洗脱部位fr.d;fr.d 经硅胶柱层析(1:100上样),用氯仿-甲醇-水(7:3:0.5)于冷库(4℃)洗脱,可得30个流分;取第11个流分,经硅胶柱色谱(200-300目)、sephadex lh-20柱色谱、反相键合相色谱(ods)以及制备型高效液相(hplc)等分离手段进行分离纯化。
[0009]
进一步的,一种具有抗流感病毒活性的辣木籽提取物抗病毒活性的测试方法,包括以下步骤:步骤一、选定测试仪器,选定胎牛血清、dmem高糖培养基、0.25%trypsin-edta、双抗、 dmso、cck-8和1%豚鼠红细胞为测试试剂,制备测试药物moringaa,选定测试细胞为raw264.7 和mdck细胞,选定测试病毒株为influenza a/weiss/43(pr8,h1n1);步骤二、药物配制,精密称取步骤一制备的moringaa约10mg,用无血清dmem培养基配制成100μm浓度的溶液, 4℃冰箱保存待用;步骤三、将冻存的raw264.7细胞进行复苏,将raw264.7巨噬细胞加入含 10%胎牛血清的rpmi1640培养基,置于95%湿度、5%co2、37℃的细胞培养箱中培养,取传代的细胞,弃掉培养基,终止培养,经处理后在显微镜下(100
×
)计数四角大方格内的细胞总数,倒置显微镜下观察细胞,处于对数生长期且状态良好时将细胞冻存;步骤四、病毒扩增,采用mdck细胞为宿主对h1n1病毒进行扩增;步骤五、raw264.7细胞接种及加样,细胞存活率检测;步骤六、moringaa体外抗h1n1活性测试。
[0010]
进一步的,所述步骤五,取生长状态良好的raw264.7细胞,消化后加10%fbs的无酚红 dmem高糖培养基制成细胞悬液,稀释细胞浓度至1
×
105个/ml,接种到96孔培养板,每孔 150μl,置于37℃、5%co2的孵箱中培养;24h后,移去上清液,受试药物组分别加入含有1 μm、2μm、4μm、8μm、16μm、32μm、64μm、128μm、256μm、512μm的含moringaa 培养基;溶剂组为5
‰
的dmso;同时设置空白对照组;以上各组细胞各设置3个复孔,在37℃、 5%co2的条件下继续培养24h;moringaa孵育细胞24h后,向各实验组细胞中加入10ml cck-8 溶液,在培养箱中反应4h,反应结束后于450nm波长处测定各实验组细胞吸光度值,计算细胞存活率。
[0011]
进一步的,所述步骤六包括(1)取生长状态良好的raw264.7细胞,消化后加含10%胎牛血清的rpmi1640培养基制成细胞悬液,并稀释细胞浓度至1
×
105个/ml接种到96孔培养板,每孔150μl,置于37℃、5%co2的孵箱中培养;24h后,移除培养板中各孔上清液,加入新鲜rpmi1640完全培养基,同时向各培养孔中接种10μl h1n1病毒液,对照组加入等体积培养基,继续培养24h;(2)按授试药物将细胞分为正常组(control)、病毒组(virus)、奥司他韦组(ost)、moringa(ma)高、中、低剂量组,给药剂量分别为10、5、1μm,每组6 个复孔;移除各实验组细胞上清液,按受试药物相应加入含药培养基;h1n1组和空白对照组加入等体积培养基,然后在37℃、5%co2的条件下继续培养24h;(3)24h后,将各实验组培养上清液对应收集于u型96孔板,每孔收集50μl;然后向u型96孔板中加入50μl1%的豚鼠红细胞,测定各实验组凝血滴度(hemagglutination,ha),结果以ha/50μl计。
[0012]
采用上述方案的有益效果为:经过moringaa对raw264.7巨噬细胞增殖的影响的具体测试,得知这种具有抗流感病毒活性的辣木籽提取物moringaa对raw264.7细胞无明显毒性, moringaa可显著减少流感病毒引起的细胞病变效应,moringaa可显著抑制流感病毒;所述 moringaa对h1n1型流感病毒具有显著抑制作用;所述moringaa对h1n1感染的宿主细
胞具有显著的保护作用。
附图说明
[0013]
图1为本发明一种具有抗流感病毒活性的辣木籽提取物moringaa对raw264.7细胞存活率的影响viability(%)-log
10
[μm ma]。
[0014]
图2为本发明一种具有抗流感病毒活性的辣木籽提取物moringaa对raw264.7细胞存活率的影响viability(%)-moringaa(μμ)。
[0015]
图3为本发明一种具有抗流感病毒活性的辣木籽提取物moringaa对宿主细胞具有显著的保护作用viability(%)-nc vc ost ma(μm)。
[0016]
图4为本发明一种具有抗流感病毒活性的辣木籽提取物moringaa对宿主细胞具有显著的保护作用。
[0017]
图5为本发明一种具有抗流感病毒活性的辣木籽提取物moringaa对流感病毒表现出显著抑制作用ha(unit/50μl)-nc vc ost ma(μm)。
[0018]
图6为本发明一种具有抗流感病毒活性的辣木籽提取物moringaa对流感病毒表现出显著抑制作用。
具体实施方式
[0019]
下面结合本发明的具体实施例,对本发明的技术方案进行清楚、完整地描述。所描述的实施例仅仅是本发明一部分实施例,而不是全部。基于本发明中的实施例,本领域技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
[0020]
实施例一:
[0021]
如图1至6所示,一种具有抗流感病毒活性的辣木籽提取物,所述辣木籽提取物命名为 moringa a,其化学结构为:
[0022][0023]
优选的,所述辣木籽提取物moringa a是从辣木籽甲醇提取物-丙酮萃取相中获得。
[0024]
优选的,所述辣木籽提取物moringa a的制备方法:30kg干燥辣木籽粉碎至细粉,用甲醇回流提取2次,每次2h;合并滤液后用布氏漏斗抽滤合并,减压回收甲醇,烘箱干燥后得辣木籽粗提物;将所得粗提物用甲醇溶解后与10倍量80-100目硅胶进行拌样,减压旋干成粉末,经硅胶柱层析(80-100目),将不同极性成分分开,依次用石油醚、氯仿、乙酸乙酯、丙酮和甲醇5种溶剂洗脱;收集丙酮洗脱液,减压回收丙酮,得丙酮洗脱部位fr.d;fr.d经硅胶柱层析(1:100上样),用氯仿-甲醇-水(7:3:0.5)于冷库(4℃)洗脱,可得30个流分;取第11个流分,经硅胶柱色谱(200-300目)、sephadex lh-20柱色谱、反相键合相色谱(ods) 以及制备型高效液相(hplc)等分离手段进行分离纯化。
[0025]
实施例二:
[0026]
如图1至6所示,一种具有抗流感病毒活性的辣木籽提取物抗病毒活性的测试方法,包括以下步骤:
[0027]
步骤一、选定测试仪器,多功能酶标仪:mk3型美国thermofisher公司。倒置显微镜: ckx53型,日本olympus公司。三目生物显微镜:cx31型,日本olympus公司。co2细胞恒温培养箱:forma-311型,美国thermofisher公司。超净工作台:heraguard eco型,美国 thermofisher公司。低温离心机:s400-rt33d-e10ff型,美国thermofisher公司。电子天平:bp221s型,由德国sartorius生产。微量旋涡混合仪:wh-2型,由上海沪西分析仪器厂生产。高速微量离心机:lg15-w型,由北京医用离心机厂生产。低速离心机:dd-5m型,由湘仪离心机仪器有限公司生产。可调移液器:5、10、20、500、1000μl型,由芬兰thermoelect公司生产。数显恒温水浴锅:hh-4型,河南省巩义市祥和商贸有限公司生产。-80℃低温冰箱:ctr-21型,美国thermofisher仪器有限公司生产。台式冷冻离心机:so-micro 21 型,美国thermo公司生产。水平摇床:ts-2型,海门市其林贝尔仪器公司生产。
[0028]
选定测试试剂,胎牛血清,批号:10099-141,购自gibco公司。dmem高糖培养基,批号: c11995,购自gibco公司。0.25%trypsin-edta(25200-056),购自gibco公司。双抗,批号:15140-122,购自gibco公司。dmso,批号:d2650,100ml,购自日本duojindo公司。 cck-8,货号:ck04,购自日本duojindo公司。1%豚鼠红细胞,货号:sbj-rbc-gp001,购自南京森贝伽生物科技有限公司。
[0029]
制备测试药物moringaa,制备方法:30kg干燥辣木籽粉碎至细粉,用甲醇回流提取2次,每次2h。合并滤液后用布氏漏斗抽滤合并,减压回收甲醇,烘箱干燥后得辣木籽粗提物。将所得粗提物用甲醇溶解后与10倍量80-100目硅胶进行拌样,减压旋干成粉末,经硅胶柱层析(80-100目),将不同极性成分分开,依次用石油醚、氯仿、乙酸乙酯、丙酮和甲醇5种溶剂洗脱。收集丙酮洗脱液,减压回收丙酮,得丙酮洗脱部位fr.d。fr.d经硅胶柱层析(1:100 上样),用氯仿-甲醇-水(7:3:0.5)于冷库(4℃)洗脱,可得30个流分。取第11个流分,经硅胶柱色谱(200-300目)、sephadex lh-20柱色谱、反相键合相色谱(ods)以及制备型高效液相(hplc)等分离手段进行分离纯化,即可得到纯度很高的化合物moringa a。
[0030]
选定测试细胞,raw264.7,货号:zq0098,购自上海中乔新舟生物科技有限公司。mdck 细胞,货号:cl-0154,购自武汉普诺赛生命科技有限公司。
[0031]
选定测试病毒株,influenza a/weiss/43(pr8,h1n1)病毒株由武汉病毒研究所提供。
[0032]
步骤二、药物配制,精密称取步骤一制备的moringaa约10mg,用无血清dmem培养基配制成100μm浓度的溶液,4℃冰箱保存待用。
[0033]
步骤三、细胞培养:细胞复苏,从-80℃冰箱中取出冻存的raw264.7细胞,立即放于37℃水浴快速摇动至完全融化,1000rpm离心5min,弃掉冻存液,加入1ml含10%胎牛血清的 rpmi1640培养基,轻轻吹打使细胞混合均匀,转入培养瓶中,缓慢加入培养基,轻轻摇动培养瓶使培养基与细胞混合均匀,置co2培养箱中培养。
[0034]
细胞培养,将raw264.7巨噬细胞加入含10%胎牛血清的rpmi1640培养基,置于95%湿度、 5%co2、37℃的细胞培养箱中培养。倒置显微镜下观察细胞,处于对数生长期即融合达到80%以上,用细胞刮刮下、传代。
[0035]
细胞计数,取传代的细胞,弃掉培养基,终止培养,将1ml 0.25%胰蛋白酶溶液加
u型96孔板中加入50μl1%的豚鼠红细胞,测定各实验组凝血滴度(hemagglutination,ha),结果以ha/50μl计。
[0048]
实施例三:
[0049]
如图1至6所示,测试结果:
[0050]
一、moringaa对raw264.7细胞无明显毒性。
[0051]
采用1-512μm梯度浓度的moringaa与raw264.7细胞共孵育24h,结果显示,随着浓度增大,moringaa对raw264.7细胞表现出抑制作用,其cc50和logcc50值分别为72.44μm、 1.86。
[0052]
从图3可知,与正常组细胞比较,流感病毒感染组细胞存活率极显著下降(p《0.01);与流感病毒感染组比较,moringaa高、中、低剂量组细胞存活率均有极显著增大(p《0.01)。从图4可以看出,流感病毒感染组细胞表现出明显的细胞病变和死亡,而moringaa治疗组细胞病变效应显著减轻,表明moringaa对宿主细胞具有良好的保护作用。
[0053]
二、moringaa可显著抑制流感病毒。
[0054]
从图5可知,与正常组比较,流感病毒组红细胞凝血滴度显著增大(p《0.01);与流感病毒组比较,moringaa高、中、低剂量组红细胞凝血滴度均有极显著减少(p《0.01)。表明 moringaa可显著抑制流感病毒的活性。
[0055]
三、结论。
[0056]
(1)moringaa对h1n1型流感病毒具有显著抑制作用。
[0057]
(2)moringaa对h1n1感染的宿主细胞具有显著的保护作用。
[0058]
对于本领域技术人员而言,显然本发明不限于上述示范性实施例的细节,而且在不背离本发明的精神或基本特征的情况下,能够以其他的具体形式实现本发明。因此,无论从哪一点来看,均应将实施例看作是示范性的,而且是非限制性的,本发明的范围由所附权利要求而不是上述说明限定,因此旨在将落在权利要求的等同要件的含义和范围内的所有变化囊括在本发明内。
[0059]
此外,应当理解,虽然本说明书按照实施方式加以描述,但并非每个实施方式仅包含一个独立的技术方案,说明书的这种叙述方式仅仅是为清楚起见,本领域技术人员应当将说明书作为一个整体,各实施例中的技术方案也可以经适当组合,形成本领域技术人员可以理解的其他实施方式。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。