1.本发明属于药物和/或化妆品领域,具体涉及牛蒡子苷元在用于制备祛痘药物和/或化妆品中的用途。
背景技术:
2.青春痘,又称痤疮,是一种常见的累及毛囊、皮脂腺的皮肤病,好发于面、胸背部等富含皮脂腺的部位。多国健康监测系统统计数据显示,人群中约有85%在12~24岁期间出现青春痘,发病率有逐年增高的趋势。其发病原因有很多,一般认为青春期雄性激素分泌增加,引起皮脂腺增生,皮脂分泌增多,同时使毛囊、皮脂腺导管角化栓塞,皮脂游积于毛囊形成脂栓。在厌氧环境下,痤疮丙酸杆菌等厌氧菌大量增生繁殖,产生溶脂酶,分离皮脂产生游离脂肪酸,导致毛囊壁损伤破裂,游积的皮脂进入真皮内,从而引起毛囊周围程度不等。
3.针对上述不同的发病环节,目前青春痘的治疗方法也有多样,主要包括局部药物治疗(维酸类乳膏、过氧化苯甲酰、抗生素制剂等)、口服药物治疗(如抗生素、抗雄激素类、维酸类等)及多种光疗法(蓝光、红光、光动力疗法等),然而药物仍是目前治疗青春痘的首要方法。皮脂腺是涉及青春痘发病的重要器官,皮脂腺活性的增加导致的皮脂分泌过多是青春痘发生的主要原发因素,故抑制皮脂腺的活性,控制皮脂分泌是有效治疗青春痘的重要途径。现今认为异维酸是最有效的皮脂腺抑制剂,能针对青春痘发病的多个环节发挥作用,具有缩小皮脂腺组织、抑制皮脂腺活性、减少皮脂分泌和上皮细胞角化以及抑制痤疮丙酸杆菌的作用,被认为是目前祛痘治疗的一线药物。但研究发现长期系统应用异维酸可能会引起脑损害、皮肤屏障功能异常、肠粘膜损害、致畸、精神心理问题等多种副作用的发生,因此在临床应用中存在一定的局限性。而且青春痘病程较长,停药复发率高,往往需要长期服药治疗,因此青春痘的治疗仍然是一个颇为棘手的问题,寻找到有效并且相对安全的治疗青春痘的药物具有显著的实际意义。
4.牛蒡子为菊科二年生草本植物牛蒡的干燥成熟果实,又名大力子、鼠粘子、恶实等。牛蒡子属于常用中药,中医认为它具有疏散风热、宣肺透疹、利咽散结、解毒消肿之功效,用于风热感冒、咳嗽痰多、麻疹、风疹、咽喉肿痛、痄腮丹毒、痈肿疮毒。西医认为它除了具有利尿、消积、祛痰止泄等药理作用外,还用于便秘、高血压、高胆固醇症的食疗。
5.牛蒡子主要含有木脂素类化合物,以牛蒡子苷和牛蒡子苷元为主。根据实验研究发现,牛蒡子苷元比牛蒡子苷具有更强的生理活性,牛蒡子苷在体内被分解为牛蒡子苷元而产生众多药理作用。目前,已有文献报道牛蒡子苷元具有如下药理活性:1)抗病毒作用,包括hiv-1与流感病毒;2)诱导肿瘤细胞凋亡的作用;3)肾病及糖尿病、糖尿病并发症治疗作用;4)热休克反应抑制作用;5)神经保护作用;6)扩张血管作用;7)血小板活化因子拮抗作用;8)抗老年性痴呆的作用;9)抑制k 挛缩的作用等。
6.现有技术中并没有牛蒡子苷元对青春痘治疗作用的研究报道。
技术实现要素:
7.为了解决现有技术中存在的问题,本发明提供了牛蒡子苷元用于制备祛痘的药物和/或化妆品中的用途。本发明揭示了牛蒡子苷元可有效抑制皮脂腺的增殖,对青春痘有显著的治疗效果。本发明的牛蒡子苷元用于祛痘时,治疗效果显著,安全无毒,具有很好的应用前景。
8.发明人通过大量的试验研究发现,牛蒡子苷元对皮脂腺细胞增殖有显著的抑制,能够改善金黄地鼠皮脂腺增厚、腺体排列紧密的组织形态。牛蒡子苷元对新西兰兔耳廓痤疮模型有明显的治疗作用。临床试验表明牛蒡子苷元能够有效治疗青春痘。因此,牛蒡子苷元可在制备祛痘药物和/或化妆品中发挥重要作用。
9.本发明所述的牛蒡子苷元在制备祛痘药物中的用途,所述的牛蒡子苷元的药物剂型为其外用制剂。
10.优选地,所述的外用制剂为其散剂、软膏剂、凝胶剂、乳膏剂、喷雾剂或贴剂。
11.其中,所述外用制剂的给药形式为皮肤给药。
12.本发明所述的牛蒡子苷元的化妆品可以是本领域各种类型的化妆品,如香皂、洗面奶、爽肤水、精华、乳液或膏霜。
13.在本发明中,所述的牛蒡子苷元在所述药物和/或化妆品中的含量为0.0125-99.00wt%,优选地为0.01%-10wt%,更为优选地为0.05%-2wt%。
14.在本发明的药物和/或化妆品中,以及在本发明的药物或/和化妆品的组合物中还包括可以根据需要加入其他药物成份或有效成份,以作为有效成份的联合使用,例如,可以加入维生素e、氨基酸、血液流通促进剂、细胞活化因子等。所述的这些其他药物成份或有效成份可以使用,也可以不使用,其使用与否取决于制备的需要。
15.在本发明的药物和/或化妆品中,以及在本发明的药物或/和化妆品的组合物中,也包括加入选自常规的外用药物和/或化妆品的助剂,如胶凝剂、增稠剂、表面活性剂、防腐剂、抗氧化剂、乳化剂、保湿剂、润滑剂、湿润剂、粘合剂、防腐剂、杀菌剂、香精等。所述的这些助剂可以使用,也可以不使用,可以使用一种,也可以使用多种,其使用与否和使用的多少取决于制备剂型的需要。
16.本发明的牛蒡子苷元用于制备祛痘药物和/或化妆品,相对于现有技术中的方案,具有以下特点和优点:
17.(1)研究的原创性:本发明人在国内外首先发现牛蒡子苷元具有很强的祛痘作用,牛蒡子及其组份的祛痘作用迄今尚未见报道。本研究成果具有原创性。
18.(2)研究的创新性:本发明人打破常规,勇于创新,发掘中草药宝库,研发外用有效、高效无毒、价格便宜、特异性高的牛蒡子苷元祛痘药物和/或化妆品。
19.(3)发明的实用性:本发明人的研究工作已证明牛蒡子苷元具有较强的祛痘作用,而且外用有效、高效无毒。
20.综上所述,本研究集理论创新、应用创新、技术创新为一体。这一创新项目在祖国传统医学的二次开发和研究中具有前瞻性、先导性和探索性的前沿技术,能为青春痘治疗另辟蹊径。
具体实施方式
21.以下通过具体实施例进一步说明本发明的发明内容,但应该理解,本发明实施例并不以任何方式限制本发明。
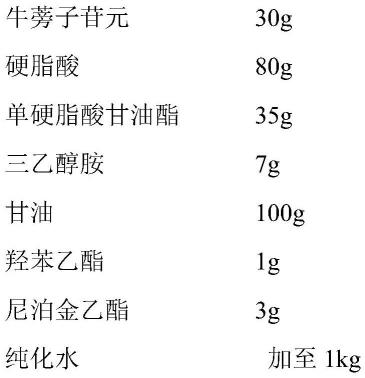
22.实施例1牛蒡子苷元乳膏
[0023][0024]
制备方法:取处方量的硬脂酸、单硬脂酸甘油酯、尼泊金乙酯,置水浴中加热熔融,80℃水浴中保温,制得油相;另取三乙醇胺、甘油、羟苯乙酯及水,混匀,于80℃水浴中保温,制得水相。将油相缓慢加入水相中,搅拌下加入牛蒡子苷元,冷却至室温,即得。
[0025]
实施例2牛蒡子苷元乳膏
[0026][0027]
制备方法:取处方量的硬脂酸、单硬脂酸甘油酯、尼泊金乙酯,置水浴中加热熔融,80℃水浴中保温,制得油相;另取三乙醇胺、甘油、羟苯乙酯及水,混匀,于80℃水浴中保温,制得水相。将油相缓慢加入水相中,搅拌下加入牛蒡子苷元,冷却至室温,即得。
[0028]
实施例3牛蒡子苷元凝胶
[0029][0030]
制备方法:将卡波姆溶于适量的纯化水中,放置24h溶胀完全,加入三乙醇胺;另取丙二醇和甘油,加入到溶胀好的卡波姆中混匀,制得卡波姆凝胶;最后取牛蒡子苷元、羟苯乙酯,聚乙烯吡咯烷酮加入适量的纯化水,加热使其溶解,冷却,加入上述卡波姆凝胶中,搅匀,加纯化水至全量,混匀,即得。
[0031]
实施例4牛蒡子苷元凝胶
[0032][0033]
制备方法:将卡波姆溶于适量的纯化水中,放置24h溶胀完全,加入三乙醇胺;另取丙二醇和甘油,加入到溶胀好的卡波姆中混匀,制得卡波姆凝胶;最后取牛蒡子苷元、羟苯乙酯,聚乙烯吡咯烷酮加入适量的纯化水,加热使其溶解,冷却,加入上述卡波姆凝胶中,搅匀,加纯化水至全量,混匀,即得。
[0034]
实施例5牛蒡子苷元软膏
[0035][0036]
制备方法:将十八醇、白凡士林、液体石蜡置于适当的容器中,加热至70℃熔化。另取月桂醇硫酸钠、尼泊金乙酯、甘油及纯化水混合溶解并加热至同样温度。将油相缓慢加入水相中,搅拌下加入牛蒡子苷元,冷却至室温,即得。
[0037]
实施例6牛蒡子苷元软膏
[0038][0039]
制备方法:将十八醇、白凡士林、液体石蜡置于适当的容器中,加热至70℃熔化。另取月桂醇硫酸钠、尼泊金乙酯、甘油及纯化水混合溶解并加热至同样温度。将油相缓慢加入水相中,搅拌下加入牛蒡子苷元,冷却至室温,即得。
[0040]
实施例7爽肤水
[0041][0042]
制备工艺:
[0043]
1.将a相各组分混合加热到85℃,充分溶解搅拌均匀;预先将c互相溶解;
[0044]
2.将a相冷却到45度,加入b、c相;
[0045]
3.搅拌均匀后出料,ph控制在5.5-7.0。
[0046]
实施例8润肤乳
[0047][0048]
制备工艺:
[0049]
1.先把卡波941分散在甘油中,再分散在水中并同时升高温度到85℃,然后加入b相其他组分,搅拌均匀;
[0050]
2.将a相于85℃溶解完全,搅拌均匀;
[0051]
3.将a相加入b相中搅拌均质(约4分钟),消泡冷却至45℃;
[0052]
4.加入c相各组分,搅拌均匀出料。ph值控制在5.5-7.0。
[0053]
实施例9本发明牛蒡子苷元对皮脂腺细胞的生长增殖的影响
[0054]
药物配制:将牛蒡子苷元用dmso溶解,配制为终浓度0.8、1.6、3.125、6.25、12.5、25、50umol/l。以含0.2%dmso不含待检药物的培养基作为阴性对照。
[0055]
将sz95细胞以2000个/孔的密度接种96孔板,培养24小时后,加入不同浓度的牛蒡子苷元及阴性对照,继续培养72小时和96小时,加入mtt检测细胞的生长增殖情况。在酶联免疫仪上测定吸光度值(a值),波长为490nm。
[0056]
结果如表1所示,牛蒡子苷元对sz95细胞增殖抑制呈现时间和剂量依赖性。牛蒡子苷元作用72h、96h后,对sz95细胞增殖均有显著的抑制作用。
[0057]
表1牛蒡子苷元对sz95细胞增殖的影响(a值,n=6)
[0058]
药物浓度(umol/l)72h96h0.80.521
±
0.0450.691
±
0.0431.60.516
±
0.0490.751
±
0.0513.1250.498
±
0.0520.513
±
0.039
**
6.250.384
±
0.051
*
0.395
±
0.037
**
12.50.361
±
0.019
**
0.346
±
0.023
**
250.285
±
0.026
**
0.371
±
0.031
**
500.234
±
0.020
**
0.196
±
0.026
**
阴性对照组0.495
±
0.0770.751
±
0.067
[0059]
与阴性对照组相比,
*
p《0.05,
**
p《0.01。
[0060]
实施例10牛蒡子苷元对金黄地鼠皮脂腺斑组织形态的影响
[0061]
金黄地鼠侧腹皮脂腺斑包含有毛囊、大量皮脂腺及黑素团块等重要结构,在解剖学特征上以及对激素刺激的反应上与人相似,是目前作为筛选和研究药物抗皮脂腺增生活性的理想动物模型。研究表明,金黄地鼠背部皮脂腺最大横径(dt)
×
最大纵径(dl)的数值变化与皮脂腺斑的真实体积大小变化呈正相关,因此,本实验选用金黄地鼠背部皮脂腺斑作为动物模型。
[0062]
成年雄性金黄地鼠56只,体质量(100
±
20)g,金黄地鼠随机分成7组,每组8只。适应性饲养3天后开始实验。于第4天实验开始时金黄地鼠用乙醚麻醉后,用剃毛器剃尽金黄地鼠背部毛,用游标卡尺测量背部右侧斑块的最大横径(dt)和最大纵径(dl)。分组及给药如下:
[0063]
牛蒡子苷元高剂量组:实施例1牛蒡子苷元乳膏,浓度为3%;
[0064]
牛蒡子苷元低剂量组:实施例3牛蒡子苷元凝胶,浓度为1%;
[0065]
双氯芬酸组:双氯芬酸钠凝胶,浓度为1%;
[0066]
酮洛芬组:酮洛芬凝胶,浓度为2.5%;
[0067]
吡罗昔康组:吡罗昔康软膏,浓度为1%;
[0068]
吲哚美辛组:吲哚美辛凝胶,浓度为1%。
[0069]
正常对照组:溶媒浓度为1%。正常对照组涂抹溶媒,其余各组分别涂擦相应药物于金黄地鼠的皮脂腺斑处,每天2次,连续28d。
[0070]
于实验第31天取材,取材前禁食24h,脱颈椎处死金黄地鼠,用游标卡尺测量背部右侧斑块dt和dl。然后切除皮脂腺斑组织,放入装有固定液的玻璃瓶中固定。将标本制成切片,厚度6μm,于光镜下对皮脂腺斑进行组织学观察。
[0071]
观察指标:(1)皮脂腺面积,用最大横径(dt)
×
最大纵径(dl)表示;
[0072]
(2)皮脂腺斑厚度,重叠腺叶<2为薄;2≤重叠腺叶《4为中;重叠腺叶≥4为厚。
[0073]
采用spss 15.0软件包对结果进行t检验。
[0074]
实验结果如下:
[0075]
(1)金黄地鼠背部皮脂腺斑面积比较
[0076]
治疗前地鼠背部皮脂腺斑面积比较,差异无统计学意义(p>0.05);实验结束,与对照组比较,牛蒡子苷元低剂量组、高剂量组金黄地鼠背部皮脂腺斑面积明显缩小(p<0.01),其余各组组与对照组比较,差异无统计学意义(p>0.05),见表2。
[0077]
表2牛蒡子苷元对金黄地鼠背部皮脂腺斑面积比较
[0078][0079][0080]
与正常对照组比较,
*
p<0.05,
**
p<0.01。
[0081]
(2)金黄地鼠背部皮脂腺斑厚度比较
[0082]
牛蒡子苷元低剂量组、高剂量组地鼠背部皮脂腺斑厚度薄于对照组(p<0.01),其余各组组与对照组比较,差异无统计学意义(p>0.05),见表3。
[0083]
表3牛蒡子苷元对金黄地鼠背部皮脂腺斑厚度比较
[0084]
组别n厚(只)中(只)薄(只)正常对照组8521牛蒡子苷元低剂量组8323
**
牛蒡子苷元高剂量组8314
**
双氯芬酸组8512酮洛芬组8521吡罗昔康组8422吲哚美辛组8431
[0085]
与正常对照组比较,
*
p<0.05,
**
p<0.01。
[0086]
(3)组织学观察
[0087]
光镜下,牛蒡子苷元低剂量组、高剂量组金黄地鼠皮脂腺厚度较薄,多为1~2层,皮脂腺排列松散,腺叶较小,且液化小囊形成数目较多。对照组金黄地鼠皮脂腺呈分叶状分布,排列较紧较厚(重叠腺叶数≥4个),部分腺叶大而饱满。
[0088]
综上,牛蒡子苷元对皮脂腺分泌具有抑制作用,能够改善皮脂腺增厚、腺体排列紧密的组织形态。
[0089]
实施例11本发明牛蒡子苷元对兔耳廓痤疮模型的影响
[0090]
建立油酸/痤疮丙酸杆菌致兔耳痤疮模型。新西兰兔48只,适应性饲养1周后,按体重随机分为造模组42只、正常对照组6只。对造模组42只新西兰兔造模:在新西兰兔右耳内
侧面耳管开口处备皮2cm
×
2cm范围,每日涂抹油酸1次,0.5ml/次,连续2周,并在涂抹油酸的第12天,在耳廓皮内注射痤疮丙酸杆菌备用液200μl,注射后第3天取2只新西兰兔造模处皮肤活检、病理切片观察,确定模型形成。
[0091]
将42只新西兰兔模型随机分为7组。分组及给药如下,
[0092]
模型对照组:溶媒浓度为1%;
[0093]
牛蒡子苷元高剂量组:实施例1牛蒡子苷元乳膏,浓度为3%;
[0094]
牛蒡子苷元低剂量组:实施例3牛蒡子苷元凝胶,浓度为1%;
[0095]
双氯芬酸组:双氯芬酸钠凝胶,浓度为1%;
[0096]
酮洛芬组:酮洛芬凝胶,浓度为2.5%;
[0097]
吡罗昔康组:吡罗昔康软膏,浓度为1%;
[0098]
吲哚美辛组:吲哚美辛凝胶,浓度为1%。
[0099]
正常对照组:溶媒浓度为1%。正常对照组和模型对照组涂抹溶媒,其余各组分别涂擦相应药物于兔的右外耳道,每天2次,连续14d。
[0100]
末次药物治疗给药后18h将兔处死,取兔右耳涂油酸处及对照组兔耳同一部位取皮肤组织活检,以10%中性甲醛固定,石蜡包埋,切片,he染色,在光镜下观察组织学改变。
[0101]
根据毛囊扩张程度、角化物质多少及其病理变化分为4级:
[0102]
0级,皮肤表层、皮脂腺、毛囊、真皮均未见明显病理改变,即0分;
[0103]
级,皮肤表层复层鳞状上皮增厚、血管扩张、炎细胞浸润,即1分;
[0104]
级,皮肤表层复层鳞状上皮明显增厚,真皮层有脓肿形成,脓肿周围管扩张、充血、胶原纤维增生,有大量的炎细胞浸润,即2分;
[0105]
级,皮肤表层复层鳞状上皮明显增厚,真皮层有脓肿形成,在皮肤表面破溃,脓肿周围管扩张、充血、胶原纤维增生,有大量的炎细胞浸润,即3分。
[0106]
采用spss 15.0软件包对结果进行t检验。
[0107]
实验结果如下:
[0108]
正常对照组新西兰兔耳廓表皮、肌肉、皮脂腺、软骨均未见明显病变。模型对照组表皮角化过度,表皮和毛囊上皮的颗粒层增厚,棘层肥厚,相邻扩张的毛囊互相融合,毛囊口及漏斗部充满角化物质,皮下均有多个脓肿形成,周围组织毛细血管扩张、充血、渗出,组织水肿明显,肌肉变性断裂等。
[0109]
表4牛蒡子苷元对兔耳廓痤疮模型的病理组织学分级比较
[0110]
[0111][0112]
与模型对照组比较,
*
p<0.05,
**
p<0.01。
[0113]
由表4可知,与模型对照组比较,牛蒡子苷元高、低剂量组兔耳病理评分明显降低,有显著性差异(p<0.01)。本研究表明本发明牛蒡子苷元对油酸/痤疮丙酸杆菌致引起的新西兰兔耳廓痤疮模型有明显的治疗作用。
[0114]
双氯芬酸组、酮洛芬组、吡罗昔康组、吲哚美辛组与模型对照组相比,兔耳病理评分并无显著性差异。
[0115]
实施例12本发明牛蒡子苷元对于青春痘治疗的临床试验
[0116]
1、一般资料
[0117]
发明人2016年1月-2016年10月间共收集240例门诊就诊的青春痘患者,将患者随机分为6组:牛蒡子苷元1组、牛蒡子苷元2组、双氯芬酸组、酮洛芬组、吡罗昔康组、吲哚美辛组。
[0118]
牛蒡子苷元1组:40例,其中男性24例,女性16例,年龄14~28岁,平均为(21.7
±
2.4)岁,病程1~4年,平均为(2.5
±
1.4)年。
[0119]
牛蒡子苷元2组:40例,其中男性25例,女性15例,年龄15~29岁,平均为(22.4
±
2.3)岁,病程2~5年,平均为(2.7
±
1.4)年。
[0120]
双氯芬酸组:40例,其中男性22例,女性18例,年龄16~27岁,平均为(23.5
±
2.2)岁,病程2~5年,平均为(2.6
±
1.2)年。
[0121]
酮洛芬组:40例,其中男性25例,女性15例,年龄15~27岁,平均为(22.3
±
2.1)岁,病程2~5年,平均为(2.5
±
1.3)年。
[0122]
吡罗昔康组:40例,其中男性24例,女性16例,年龄14~28岁,平均为(21.5
±
2.3)岁,病程1~4年,平均为(2.4
±
1.1)年。
[0123]
吲哚美辛组:40例,其中男性23例,女性17例,年龄15~28岁,平均为(23.7
±
2.1)岁,病程2~5年,平均为(2.6
±
1.2)年。
[0124]
6组患者在年龄、性别以及病程等方面比较无显著性差异,具有可比性。
[0125]
2、试验方法
[0126]
牛蒡子苷元1组患处涂抹牛蒡子苷元凝胶(按本发明实施例3制得,牛蒡子苷元浓度为1%),每日2次。疗程4周。
[0127]
牛蒡子苷元2组患处涂抹牛蒡子苷元润肤乳(按本发明实施例8制得,牛蒡子苷元浓度为2%),每日2次。疗程4周。
[0128]
双氯芬酸组患处涂抹双氯芬酸钠凝胶,浓度为1%,每日2次。疗程4周。
[0129]
酮洛芬组患处涂抹酮洛芬凝胶,浓度为2.5%,每日2次。疗程4周。
[0130]
吡罗昔康组患处涂抹吡罗昔康软膏,浓度为1%,每日2次。疗程4周。
[0131]
吲哚美辛组患处涂抹吲哚美辛凝胶,浓度为1%,每日2次。疗程4周。
[0132]
治愈患者一个疗程后即可停止治疗,停药后继续观察治愈者3个月,记录复发情况。
[0133]
复发率=复发例/治愈例*100%。
[0134]
3、疗效标准与治疗结果
[0135]
3.1疗效标准
[0136]
治愈:患者症状消失,95%以上皮损消退,或不存在皮损,仅留有色素沉着;
[0137]
显效:患者症状明显减轻,70%~95%皮损消失,有色素沉着;
[0138]
有效:患者症状与治疗前相比较有一定程度改善,50%~70%皮损消失,有色素沉着;
[0139]
无效:患者临床症状与治疗前相比较未发生明显变化,仅有小于50%的皮损消退,有色素沉着。
[0140]
3.2治疗统计结果见表5。
[0141]
表5各组疗效比较
[0142]
组别n治愈显效有效无效总有效率(%)复发例牛蒡子苷元1组4022142295%1(5%)牛蒡子苷元2组4020161392.5%2(10%)双氯芬酸组400233512.5%-酮洛芬组40012377.5%-吡罗昔康组400133610%-吲哚美辛组400233512.5%-[0143]
由表5数据可知,本发明的牛蒡子苷元外用能够有效治疗青春痘,愈后复发率低。
[0144]
本发明的牛蒡子苷元外用安全性高,不良反应少。
[0145]
表6各组不良反应比较
[0146]
组别n不良反应例牛蒡子苷元1组402例红斑牛蒡子苷元2组400双氯芬酸组405例(2例皮炎、3例红斑伴有瘙痒)酮洛芬组407例(3例红斑、4例干燥)吡罗昔康组405例(2例皮炎、3例光敏性)吲哚美辛组406例(3例红斑伴有瘙痒、3例皮炎)
[0147]
双氯芬酸组、酮洛芬组、吡罗昔康组、吲哚美辛组患者用药部位有红斑、瘙痒、干燥、光敏性和皮炎等不良反应。而本发明牛蒡子苷元外用组用药部位仅个别患者出现极轻微的红斑,其安全性更高。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。