1.本发明涉及生物医药领域,具体涉及一种抗炎抗氧化的药物组合物及其制备方法与应用。
背景技术:
2.炎症是多种疾病的基本病理过程,是机体为自我保护而做出的防御性反应,包括微生物对组织的渗透、细胞因子和免疫信号分子之间的调控、微生物和凋亡细胞的清除、损伤组织的愈合等过程。如果无法在炎症过程中进行及时的打断和协助修复,炎症会造成机体受损。因此,能够高效治疗炎症损伤的策略,在包括关节炎、炎症性肠病等长期炎症及急性胰腺炎、肺炎等短期炎症性疾病中得到了广泛研究。
3.抗炎细胞因子作为炎症反应及组织修复过程中参与调控的保护性因子,被广泛用于多种疾病的治疗研究。为了提高治疗效果,近年来各种纳米药物载体如纳米囊泡、聚合物胶束等已被开发研究用来递送细胞因子。在一些研究当中,利用可生物降解的控释聚酯,以聚(d-乳酸)和聚乳酸-乙醇酸聚合物的形式,形成保护性纳米材料,用于il-10的靶向输送(acs nano,2016,10,5280-5292)。此外,有研究者利用小鼠血清白蛋白和小鼠il-4形成重组融合物,通过靶向新生儿fc受体实现il-4在次级淋巴器官中的长期驻留(nat biomed eng,2021,5,387-398)。人们还设计了一种超声响应的纳米脂质体,将il-4屏蔽在含有声敏剂原卟啉ix的脂质体中,然后通过生物正交点击反应将其与膜融合制造血小板膜装饰的m0小胶质细胞(通过代谢方法进行标记)连接起来,通过超声刺激il-4释放从而启动小胶质细胞的特定m2极化,达到治疗效果(angew chem int ed engl,2021,60(10),5083-5090)。但目前,这些递送手段的治疗作用都相对单一,无法同时做到精准控释和协同治疗,且药物在体内循环易变性而丧失生物活性,这些问题限制了上述纳米载药体系的实际应用。
技术实现要素:
4.本发明要解决的技术问题是提供一种抗炎抗氧化的药物组合物及其制备方法与应用,利用氨基苯硼酸键合的透明质酸作为载体,与由多酚类物质与蛋白质类药物聚合得到的药物复合物反应得到药物组合物,该药物组合物可保护功能性蛋白质药物的活性并靶向识别炎症组织,响应炎症部位的高浓度活性氧,释放蛋白药物及多酚物质,实现在损伤部位准确高效给药,同时发挥抗炎、抗氧化的协同疗效,促进损伤组织的修复。
5.为解决上述技术问题,本发明提供以下技术方案:
6.本发明第一方面提供了一种抗炎抗氧化的药物组合物,所述药物组合物由纳米药物载体及其包载的药物复合物组成;所述纳米药物载体由氨基苯硼酸与透明质酸脱水缩合得到,所述药物复合物由多酚类物质与蛋白质类药物通过非共价键聚合得到。
7.进一步地,药物组合物中,所述纳米药物载体与药物复合物中抗炎蛋白质类药物的摩尔比为1:0.5~4,例如1:2。
8.进一步地,所述多酚类物质选自表没食子儿茶素没食子酸酯、花青素、单宁酸中的
一种或多种。
9.进一步地,所述蛋白质类药物包含至少一种抗炎蛋白质类药物,所述抗炎蛋白质类药物为白细胞介素4、白细胞介素10、白细胞介素13或白细胞介素22。
10.进一步地,所述药物复合物由多酚类物质与蛋白质类药物通过氢键和疏水作用聚合得到。
11.进一步地,所述纳米药物载体的制备方法包括以下步骤:
12.(1)将透明质酸溶解于1-乙基-3-(3-二甲基氨丙基)-碳化二亚胺和n-羟基琥珀酰亚胺的混合溶液中,搅拌得到混合物;
13.(2)将氨基苯硼酸溶解于溶剂中,加入步骤(1)制备的混合物中,在20~30℃搅拌反应12~36h,将反应后的溶液经去离子水透析后冻干,得到所述纳米药物载体。
14.进一步地,所述1-乙基-3-(3-二甲基氨丙基)-碳化二亚胺(edc)和n-羟基琥珀酰亚胺(nhs)的混合溶液中edc、nhs浓度相同,为30~50mm,例如40mm。
15.进一步地,所述氨基苯硼酸为3-氨基苯硼酸,所述透明质酸与3-氨基苯硼酸的投料摩尔比为1:20~100,例如1:40。
16.进一步地,步骤(2)中,所述溶剂为50%的乙醇。
17.进一步地,步骤(2)中,所述去离子水透析的截留分子量为3.5kda。
18.进一步地,所述药物复合物的制备方法具体为:将多酚类物质与蛋白类药物溶于超纯水中,在20~30℃搅拌反应0.5~2h,纯化得到所述药物复合物。
19.进一步地,所述蛋白质类药物与多酚类物质的投料摩尔比为1:20~100。
20.进一步地,所述蛋白质类药物与多酚类物质的投料摩尔比优选1:50。
21.本发明第二方面提供了一种第一方面所述的药物组合物的制备方法,将纳米药物载体溶解于超纯水中,再加入药物复合物搅拌反应,反应结束后纯化得到所述药物组合物。
22.进一步地,将药物复合物滴加到溶解纳米药物载体的超纯水中,进行搅拌反应。
23.进一步地,所述搅拌反应的温度为20~30℃,搅拌反应的时间为0.5~2h。
24.本发明首先将3-氨基苯硼酸与透明质酸通过氨基与羧基的脱水缩合反应制备得到纳米药物载体,将多酚类物质与蛋白质类药物通过非共价键聚合形成药物复合物,然后利用纳米药物载体中苯硼酸的硼酸基团与多酚类物质的酚羟基反应形成硼酸酯键,构筑得到一种核壳结构的药物组合物。
25.本发明第三方面提供了一种第一方面所述的药物组合物在制备抗炎和/或抗氧化药物中的应用。
26.炎症过程中,损伤组织会表达过量活性氧,大量聚集的炎症细胞还能产生可以水解多酚的酯酶;本发明在纳米药物中引入活性氧和酯酶响应结构硼酸酯键、多酚,利用炎症部位的高表达的活性氧和酯酶的特征,使纳米药物可在损伤部位精准靶向、有效控释,清除损伤部位活性氧的同时释放蛋白质药物,促使蛋白质活性恢复,实现损伤组织的抗炎,促进快速修复,同时避免蛋白质类活性药物在体内循环时变性而丧失活性,提高药物的生物利用度。
27.本发明的有益效果在于:
28.1.本发明利用氨基苯硼酸键合的透明质酸作为纳米载体,通过硼酸酯键连接由多酚类物质与蛋白质类药物聚合得到的药物复合物,得到纳米药物组合物;该纳米药物组合
物可以同时递送多酚类物质及蛋白质类药物,并且可防止活性药物在体内循环时发生降解而失去活性,包含活性氧和酯酶响应结构硼酸酯键、多酚的药物组合物可准确识别炎症组织,减少其在正常组织中的富集;本发明制备的药物组合物到达炎症组织部位,在炎症组织高表达的活性氧以及酯酶作用下,连接纳米载体和药物复合物的硼酸酯键发生断裂,消耗活性氧的同时释放药物复合物,进一步清除损伤部位的活性氧,而活性恢复的抗炎蛋白质在损伤组织部位发挥抗炎作用,在抗炎、抗氧化的协同疗效下,促进损伤组织的快速修复。
29.2.本发明提供的一种药物组合物,制备方法简单、反应条件温和,且过程无需其它物质参与,可保证药物的纯净;此外,本发明通过体外以及动物体内试验,验证了该药物组合物具有良好的稳定性,在递送过程中可极大的保留药物的活性,可增强药物在炎症组织中的富集,有效保护细胞免于氧化应激损伤,实现药物在损伤部位的精准控释;该抗炎纳米药物组合物表现出良好体内抗炎疗效的同时无明显的毒副作用,具有良好的生物安全性,在制备抗炎和/或抗氧化药物方面具有良好的应用前景。
附图说明
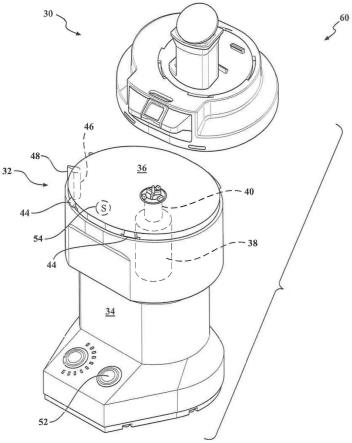
30.图1为实施例一制备的纳米药物载体的核磁谱图;
31.图2为实施例二制备的药物组合物的透射电镜图,标尺为500nm;
32.图3为实施例二制备的药物复合物、药物组合物在血清中粒径随时间的变化情况;
33.图4为实施例二制备的药物复合物、药物组合物水解释放药物后,蛋白质的生物活性恢复情况;
34.图5为药物组合物在h2o2预处理后,纳米药物载体从药物组合物上的脱落情况;
35.图6为药物组合物在模拟炎症微环境下的水解情况;
36.图7为药物组合物对hiec细胞的抗氧化应激作用;
37.图8为药物组合物在正常小鼠及重症急性胰腺炎小鼠模型中的主要器官的离体荧光成像(8a)及荧光强度(8b);
38.图9为小鼠重症急性胰腺炎模型中不同组别血浆内淀粉酶活性水平结果图;
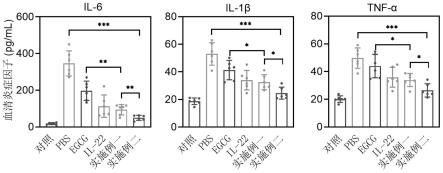
39.图10为小鼠重症急性胰腺炎模型中不同组别血浆内促炎细胞因子(il-6,il-1β及tnf-α)水平结果图;
40.图11为小鼠重症急性胰腺炎模型中不同组别胰腺组织匀浆氧化应激指标mpo(11a)和h2o2水平结果图(11b);
41.图12为小鼠重症急性胰腺炎模型中不同组别胰腺组织切片he染色图。
具体实施方式
42.下面结合附图和具体实施例对本发明作进一步说明,以使本领域的技术人员可以更好地理解本发明并能予以实施,但所举实施例不作为对本发明的限定。
43.除非另有定义,本文所使用的所有的技术和科学术语与属于本发明的技术领域的技术人员通常理解的含义相同。本文中在本发明的说明书中所使用的术语只是为了描述具体的实施例的目的,不是旨在于限制本发明。本文所使用的术语“及/或”包括一个或多个相关的所列项目的任意的和所有的组合。
44.实施例一
45.本实施例涉及一种抗炎抗氧化的药物组合物的制备,其中多酚类物质为表没食子儿茶素没食子酸酯(egcg),蛋白质类药物为牛血清白蛋白(bsa),具体的制备过程如下所示:
46.(1)纳米药物载体的制备:将透明质酸(ha,0.4g,0.01mmol)溶解在去离子水(50ml)中,向其中加入edc/nhs混合溶液(20ml,5mmol),在室温条件下搅拌反应1h后,将溶于乙醇的3-氨基苯硼酸(apba,20ml,v/v=1/1)溶液滴加到上述溶液中并在室温条件下搅拌反应24h。将得到的溶液在去离子水中透析3天(mwco=3.5kda),经冷冻干燥后得到白色固体状产物为纳米药物载体;对产物进行核磁表征,表征结果如图1所示。
47.(2)药物复合物的制备:将bsa(4mg/ml)溶于超纯水中,得到bsa溶液,将egcg(1.4mg/ml)溶于超纯水中,得到egcg溶液;然后按照egcg与bsa的摩尔比为50:1的比例混合两种溶液,并在室温条件下搅拌反应1h,得到药物复合物。
48.(3)药物组合物的制备:将步骤(1)制备得到的纳米药物载体溶于超纯水中(2.5mg/ml),随后,将步骤(2)制备得到的药物复合物按照抗炎蛋白质类药物与苯硼酸修饰的透明质酸的摩尔比为1:2的比例缓慢滴加到苯硼酸修饰的透明质酸溶液中并在室温条件下搅拌1h,得到药物组合物。
49.实施例二
50.本实施例涉及一种抗炎抗氧化的药物组合物的制备,其中多酚类物质为表没食子儿茶素没食子酸酯(egcg),蛋白质类药物为bsa与重组小鼠白介素22(il-22),具体的制备过程如下所示:
51.(1)纳米药物载体的制备:将透明质酸(ha,0.4g,0.01mmol)溶解在去离子水(50ml)中,向其中加入edc/nhs混合溶液(20ml,5mmol),在室温条件下搅拌反应1h后,将溶于乙醇的3-氨基苯硼酸(apba,20ml,v/v=1/1)溶液滴加到上述溶液中并在室温条件下搅拌反应24h。将得到的溶液在去离子水中透析3天(mwco=3.5kda),经冷冻干燥后得到白色固体状产物为纳米药物载体。
52.(2)药物复合物的制备:将bsa(4mg/ml)与il-22(1μg/ml)溶于超纯水中,得到含有il-22的bsa溶液,将egcg(1.4mg/ml)溶于超纯水中,得到egcg溶液;然后按照egcg与bsa的摩尔比为50:1的比例混合两种溶液,并在室温条件下搅拌反应1h,得到药物复合物。
53.(3)药物组合物的制备:将步骤(1)制备得到的纳米药物载体溶于超纯水中(2.5mg/ml),随后,将步骤(2)制备得到的药物复合物按照抗炎蛋白质类药物与苯硼酸修饰的透明质酸的摩尔比为1:2的比例缓慢滴加到苯硼酸修饰的透明质酸溶液中并在室温条件下搅拌1h,得到药物组合物。
54.对制备的药物组合物进行透射电镜表征,结果如图2所示,制备得到的药物组合物是由纳米药物载体包载药物复合物得到的一种核-壳结构的纳米复合物,其大小均一、分散良好。
55.性能测试
56.(1)药物组合物稳定性的研究
57.为了研究药物组合物的稳定性,按照实施例二制备的药物复合物和药物组合物在含有10%fbs的dmem中以37℃水浴孵育24h,在不同时间点测量粒径来评估其稳定性。
58.粒径随时间的变化如图3所示,实施例二中制备的药物组合物的粒径随时间的变
化不大,具有良好的血清稳定性,而没有纳米药物载体包覆的药物复合物的粒径逐渐增加至300nm;该结果说明纳米药物载体对药物复合物具有良好的屏蔽作用,阻止了egcg和il-22与血清中其他物质相互作用,从而加强了药物组合物内部的稳定性。
59.(2)药物组合物解离后蛋白质活性恢复情况的研究
60.通过酶联免疫吸附试验测定药物组合物解离后的蛋白质活性恢复情况,在实施例二新鲜配制的药物组合物、药物复合物中分别加入tween 20(5μg/ml)并在37℃水浴孵育4h。相同浓度的il-22溶液接受同样的处理后作为阳性对照。酶标仪测定各孔吸光度(570nm)。最终结果以阳性对照的吸光度为100%,计算其他组的il-22活性。
61.测试及计算结果如图4,完全解离后的药物组合物中,il-22的活性仍然高达87.8%。该结果说明本发明制备的药物组合物在解离释放后可继续发挥良好的蛋白质药物活性,为后续的治疗效果提供保障。
62.(3)药物组合物的h2o2响应性释放能力的研究
63.通过荧光共振能量转移技术监测h2o2触发的纳米药物载体表面脱落情况。使用cy3荧光素标记纳米药物载体,得到cy3-纳米药物载体,使用cy5荧光素标记bsa,得到cy5-bsa,然后使用实施例一中方法得到药物组合物。在0.2mm h2o2下孵育30分钟后,在580-800nm(λex=550nm)的范围内读取荧光光谱。
64.测试结果如图5所示,没有h2o2的pbs中,cy3-纳米药物载体与内核所含的cy5-bsa距离较近,能够产生fret效应,而当处于0.2mm h2o2中时,在562nm处观察到cy3荧光的恢复,说明cy3-纳米药物载体与cy5-bsa之间距离增大,这表明该药物组合物具有良好的h2o2响应性释放能力。
65.(4)h2o2及酯酶响应性的蛋白质药物释放的研究
66.为了研究h2o2及酯酶响应性的蛋白质药物的释放,使用cy5荧光素标记bsa,得到cy5-bsa,然后使用实施例一中方法得到药物组合物。将溶液置于透析袋(mwco=100kda)中,在有或没有h2o2(0.2mm)及酯酶(30u/ml)的pbs缓冲液(30ml)中于37℃孵育。在预定的时间间隔内,取出释放介质(200μl),并补充相同体积的新鲜介质。酶标仪测定释放介质中荧光强度,并计算累积释放量。
67.计算结果如图6所示,在0.2mm h2o2中,药物组合物的降解率较之pbs中明显增大,从19%升至66%,进一步说明了纳米材料有很好的活性氧响应性。在只有酯酶的情况下,药物组合物的降解率仅为26%,与其在pbs中的降解率差异不大,而在酯酶与h2o2的共同孵育下,其降解率最高,达到85%,这说明,纳米药物载体能很好的屏蔽内部药物复合物,当h2o2促使硼酸酯键断裂后,暴露的内核可进一步被酯酶水解,从而释放药物。
68.(5)药物组合物抗氧化能力的研究
69.将人肠上皮细胞(hiec细胞)接种到96孔板中(1
×
105细胞/孔),培养24h。加入egcg或药物组合物,再加入h2o2使其终浓度为0.2mm,处理24h。再将培养基换成含有10%fbs的dmem,加入mtt(5mg/ml,20μl/孔),37℃条件下孵育4h。吸去培养基,加入二甲基亚砜(dmso,100μl/孔),室温震荡20分钟混匀,酶标仪测定570nm处的吸光度。以pbs处理的细胞存活率作为100%,计算各复合物处理后的细胞存活率(%)从而间接测定该体系对氧化应激诱导的细胞凋亡的抑制作用。
70.测试结果如图7所示,pbs组的细胞存活率明显低于对照组,存活率仅为50%,药物
组合物组的细胞存活率比之pbs组明显提高,这说明药物组合物能有效保护细胞免于氧化应激损伤。
71.(6)药物组合物对炎症部位靶向能力的研究
72.使用cy5荧光素标记bsa,得到cy5-bsa,然后使用实施例一中方法得到药物组合物。采用牛磺胆酸钠逆行注射胰管方法构建小鼠重症急性胰腺炎模型。为了考察该体系的损伤部位靶向性,c57bl/6雄性小鼠分为2组,每组3只。一组作为正常对照,另一组建立小鼠重症急性胰腺炎模型,24h后将药物组合物通过尾静脉注射到小鼠体内。给药后4h处死小鼠,采集主要器官(心脏、肝脏、脾脏、肺、肾脏、胰腺和结肠),在荧光成像系统下观察药物组合物在主要器官的富集情况。
73.结果如图8所示,给药4h后,如图8a所示,药物组合物可以大量滞留在sap模型小鼠的胰腺和结肠部位,对照组及模型组小鼠不同器官的荧光强度总结于图8b中,模型组小鼠的胰腺和结肠部位的荧光强度分别是对照组小鼠的2.3倍和1.5倍,该现象说明本发明制备的药物组合物具有良好的炎症部位靶向能力。
74.(7)药物组合物在体内抗炎效果的研究
75.将c57bl/6雄性小鼠随机分为6组,每组6只。分别为(1)对照组,(2)pbs组,(3)egcg组,(4)il-22组,(5)实施例一组和(6)实施例二组。对照组接受与牛磺胆酸钠造模组相同的手术处理,但不给与牛磺胆酸钠。其他5组给与牛磺胆酸钠(3.5%,50μl)逆行胰胆管给药进行重症急性胰腺炎造模,分别在造模第-48(造模前第48h)、-24、0(造模时)、2和4h通过尾静脉注射200μl的pbs、egcg、ril-22、实施例一所得药物组合物或实施例二所得药物组合物,其中il-22蛋白剂量为10μg/kg,bsa 10mg/kg,egcg为3.5mg/kg。造模后24h对小鼠进行摘眼球采血,处死后收集组织。相关试剂盒根据说明书检测血清淀粉酶,以及采用相关试剂盒检测胰腺组织匀浆液中氧化应激相关指标mpo、h2o2水平,并通过elisa法测定il-6、il-1β、tnf-α,对小鼠胰腺进行h&e染色,观察组织学损伤情况并对胰腺进行病理学评分,上述检测结果如图9~12所示。
76.图9、10分别为不同组别血浆内淀粉酶活性和促炎细胞因子(il-6,il-1β及tnf-α)水平结果图,由图可知,注射实施例一、实施例二制备的药物组合物可有效降低重症急性胰腺炎小鼠模型的血清淀粉酶和促炎细胞因子(il-6,il-1β及tnf-α)水平,缓解疾病严重程度;图11为不同组别胰腺组织匀浆氧化应激指标mpo(图11a)和h2o2(图11b)水平结果图,由图可知,注射药物组合物可降低氧化应激相关指标mpo及h2o2水平,进一步验证了本发明制备的药物组合物具有良好的抗氧化性;图12为不同组别胰腺组织切片he染色图,he染色后可见pbs组胰腺组织弥漫性坏死,存在大片状坏死,仅残留腺叶轮廓,少数正常腺泡呈孤岛状分布,伴有腺泡细胞间隙弥漫性扩张,坏死区域可见大量炎性细胞浸润,并可见多个出血灶。与自由药物egcg组、il-22组相比,药物组合物能更显著地减轻上述病变,说明药物组合物可有效缓解胰腺的组织损伤。
77.此外,在24h的观察期内,药物组合物给药后小鼠主要器官切片的h&e染色结果没有显示异常,表明其系统在给药后并没有出现明显的副作用。且药物组合物给药组的血常规和血生化没有明显变化,具有良好的生物安全性。由上述体内、外实验结果可知,本发明制备的抗炎抗氧化的纳米药物组合物具有良好的体内抗炎疗效,且无明显的毒副作用。
78.以上所述实施例仅是为充分说明本发明而所举的较佳的实施例,本发明的保护范
围不限于此。本技术领域的技术人员在本发明基础上所作的等同替代或变换,均在本发明的保护范围之内。本发明的保护范围以权利要求书为准。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。