产品品质属性测量
1.相关申请的交叉引用
2.本技术要求2019年9月23日提交的美国临时专利申请序列号62/904,682的优先权,该申请的全部内容通过引用结合于此。
技术领域
3.本公开涉及用于样品的产品品质属性测量的系统和方法,所述样品包括从连续生物制造系统收获的样品。
背景技术:
4.含有编码重组蛋白质的核酸的哺乳动物细胞通常用于生产在治疗上或商业上重要的蛋白质。集成连续生物制造是降低与基于此类蛋白质的疗法相关的成本的重要方面。监测系统用于生物制造,以评估各种生物产品和工艺条件。
技术实现要素:
5.治疗性蛋白质物质和其他生物分子的集成连续生物制造为将来生产拯救生命的药物和促进依赖于此类生物分子的可用性的疗法的广泛采用提供了巨大的希望。具有各种配置的双柱和多柱色谱系统可用于工业规模的生物制造。在这种系统中,对来自色谱系统的洗脱物的分析可用于确定各种产品品质属性,以监测和调节各种生物工艺条件。
6.本公开的特征在于用于确定生物样品中分析物的一种或多种产品品质属性的方法和系统,所述生物样品包括从生物反应器收获的样品和串联或并联引入系统的离线样品。可以测量多种产品品质属性,包括但不限于分析物浓度、分析物电荷变化或异质性、分析物聚集、和分析物完整性或纯度。所述系统可以包括具有不同类型色谱柱的样品分析仪,所述不同类型的色谱柱专用于特定产品品质属性的测量。测量的产品品质属性可用于对生物制造工艺相关参数和操作提供反馈和控制。
7.在一个方面,本公开的特征在于用于测量生物样品的分析物的产品品质属性的系统,所述系统的特征在于:第一流动控制装置;样品纯化装置,其与所述第一流动控制装置流体连通;第二流动控制装置,其与所述第一流动控制装置、所述样品纯化装置、以及第一和第二样品分析仪流体连通,其中所述第一样品分析仪包括第一色谱柱;和控制单元,其联接到所述第一和第二流动控制装置,并且被配置成使得在所述系统的操作期间,所述控制单元:(a)调节所述第一流动控制装置的配置,以将来自所述第一流动控制装置的生物样品的一部分引导到所述样品纯化装置中或所述第二流动控制装置中,使得所述生物样品的所述部分被所述第二流动控制装置接收;(b)调节所述第二流动控制装置的配置,以将所述生物样品的所述部分引导至所述第一和第二样品分析仪中的一者;并且(c)基于所述第一和第二样品分析仪中的所述一者对所述生物样品的所述部分的分析,确定所述生物样品的分析物的产品品质属性。
8.所述系统的实施方案可包括以下特征中的任何一个或多个。
9.所述第一色谱柱可以是阳离子交换色谱柱、尺寸排阻色谱柱、或反相色谱柱。所述样品纯化装置可以包括亲和色谱柱。
10.所述第二样品分析仪可以包括定量检测器,其被配置成生成代表所述生物样品中分析物的量的电信号。所述第一色谱柱可以与所述定量检测器流体连通,并且所述定量检测器可以配置成生成代表来自所述第一色谱柱的洗脱物流中的分析物的量的电信号。
11.所述第一样品分析仪可以包括定量检测器,所述定量检测器与所述第一色谱柱流体连通并被配置成生成代表来自所述第一色谱柱的洗脱物流中的分析物的量的电信号。所述第二样品分析仪可以包括第二色谱柱,并且所述第二色谱柱可以不同于所述第一色谱柱,并且可以是阳离子交换色谱柱、尺寸排阻色谱柱、反相色谱柱、和亲水相互作用色谱柱中的一种。
12.所述第二流动控制装置可以与包括第三色谱柱的第三样品分析仪流体连通,并且所述第三色谱柱可以不同于所述第一和第二色谱柱,并且可以是阳离子交换色谱柱、尺寸排阻色谱柱、反相色谱柱、和亲水相互作用色谱柱中的一种。
13.所述第二流动控制装置可以与四个另外的样品分析仪流体连通,所述四个另外的样品分析仪中的每一个的特征在于其包括的色谱柱不同于所述第一色谱柱并且不同于所述四个另外的样品分析仪中的其他样品分析仪的色谱柱。
14.所述分析物的产品品质属性可以是所述生物样品中所述分析物的浓度、所述生物样品中所述分析物聚集的度量、所述生物样品中所述分析物的电荷变化或异质性的度量、或者所述生物样品中所述分析物的纯度或完整性的度量。
15.所述亲和色谱柱可以是蛋白a色谱柱、蛋白g色谱柱、和受体结合柱中的一种。所述分析物可以包括所述生物样品中的蛋白质(例如抗体)。
16.所述系统可以包括柱管理器,其与所述第一和第二样品分析仪以及所述第二流动控制装置流体连通,并且联接到所述控制单元,其中所述控制单元被配置为调节所述柱管理器的配置,以将所述生物样品的所述部分引导到所述第一和第二样品分析仪中的一者中。
17.所述系统可以包括柱管理器,其与所述第一、第二、和第三样品分析仪以及所述第二流动控制装置流体连通,并且联接到所述控制单元,其中所述控制单元可以被配置为调节所述柱管理器的配置,以将所述生物样品的所述部分引导到所述第一、第二、第三和第四样品分析仪中的一者中。
18.所述生物样品的所述部分可以是第一部分,并且所述产品品质属性可以是第一产品品质属性,并且所述控制单元可以被配置成使得在所述系统的操作期间,所述控制单元:(d)调节所述第一流动控制装置的配置,以将来自所述第一流动控制装置的所述生物样品的第二部分引导到所述样品纯化装置中或所述第二流动控制装置中,使得所述生物样品的所述第二部分被所述第二流动控制装置接收;(e)调节所述第二流动控制装置的配置,以将所述生物样品的所述第二部分引导至没有接收所述生物样品的所述第一部分的所述第一和第二样品分析仪中的一者;并且(f)基于接收了所述生物样品的所述第二部分的所述第一和第二样品分析仪中的所述一者对所述生物样品的所述第二部分的分析,确定所述生物样品的所述分析物的第二产品品质属性。所述第一和第二产品品质属性可以是不同的,并且所述第一和第二产品品质属性可以各自选自所述生物样品中所述分析物的浓度、所述生
物样品中所述分析物聚集的度量、所述生物样品中所述分析物的电荷变化或异质性的度量、以及所述生物样品中所述分析物的纯度或完整性的度量。
19.所述生物样品的所述部分可以是第一部分,并且所述产品品质属性可以是第一产品品质属性,并且所述控制装置可以被配置为对所述生物样品的另一部分重复步骤(a)-(c),以确定所述生物样品的所述分析物的两个不同的产品品质属性。
20.所述生物样品的所述部分可以是第一部分,并且所述产品品质属性可以是第一产品品质属性,并且所述控制装置可以被配置为对所述生物样品的其他两个部分重复步骤(a)-(c),以确定所述生物样品的所述分析物的三个不同的产品品质属性。
21.所述生物样品的所述部分可以是第一部分,并且所述产品品质属性可以是第一产品品质属性,并且所述控制装置可以被配置为对所述生物样品的其他三个部分重复步骤(a)-(c),以确定所述生物样品的所述分析物的四个不同的产品品质属性。
22.所述产品品质属性可以各自选自所述生物样品中所述分析物的浓度、所述生物样品中所述分析物聚集的度量、所述生物样品中所述分析物的电荷变化或异质性的度量、以及所述生物样品中所述分析物的纯度或完整性的度量。
23.所述系统可以包括采样装置,其联接到所述控制单元,并且被配置为接收所述生物样品,并且将所述生物样品的所述部分递送到所述第一流体控制装置。所述采样装置可以包括容器接口,所述容器接口被配置为将所述生物样品接收在容器中。所述采样装置可以包括被配置成接收所述生物样品的流体通道,并且所述控制单元可以被配置成使得在所述系统的操作期间,所述控制单元向所述采样装置发送信号以使所述采样装置将所述生物样品的所述部分从所述流体通道排放到所述第一流动控制装置中。
24.所述系统可以包括泵,其与所述第二流动控制装置、所述第一和第二样品分析仪、以及分别与所述第一和第二样品分析仪相关联的第一和第二缓冲液储器流体连通,其中所述控制单元和泵被配置成使得在所述系统的操作期间,当所述生物样品的所述部分被引导到所述第一和第二样品分析仪中的一者中时,所述泵将缓冲溶液从对应的相关联的缓冲液储器递送到所述第一和第二样品分析仪中的所述一者。
25.所述系统可以包括泵,其与所述第二流动控制装置,所述第一、第二和第三样品分析仪,以及分别与所述第一、第二和第三样品分析仪相关联的第一、第二和第三缓冲液储器流体连通,其中所述控制单元和泵被配置成使得在所述系统的操作期间,当所述生物样品的所述部分被引导到所述第一、第二和第三样品分析仪中的一者中时,所述泵将缓冲溶液从对应的相关联的缓冲液储器递送到所述第一、第二和第三样品分析仪中的所述一者。
26.所述系统可以包括泵,其与所述第二流动控制装置、所述第一样品分析仪、以及与所述第一样品分析仪相关联的缓冲液储器流体连通,其中所述第一色谱柱是阳离子交换柱,并且其中所述控制单元和泵被配置成使得在所述系统的操作期间,所述泵向所述第一色谱柱递送乙酸盐缓冲液,以沿着所述第一色谱柱传播所述生物样品的所述部分。所述乙酸盐缓冲液可以具有4.0或更低的ph。
27.所述生物样品可以是从生物反应器中提取的收获培养基。所述生物样品可以是来自生物制造系统的中间溶液或产品溶液。所述生物样品可以是细胞培养物的一部分。
28.所述定量检测器可以包括二极管阵列检测器、被配置为测量所述生物样品的所述部分的吸光度信息的光谱检测器、荧光检测器、和/或质谱检测器。
29.所述系统的实施方案还可以包括本文描述的任何其他特征,包括在不同实施方案中各自公开的特征的任何组合,除非另有明确说明。
30.在另一方面,本公开的特征在于用于测量生物样品的分析物的多个产品品质属性的系统,所述系统的特征在于第一流动控制装置;样品纯化装置,其包括与所述第一流动控制装置流体连通的纯化色谱柱;第二流动控制装置,其与所述第一流动控制装置和所述样品纯化装置流体连通;第一样品分析仪,其包括与所述第二流动控制装置流体连通的第一色谱柱;第二样品分析仪,其包括与所述第二流动控制装置流体连通的第二色谱柱;第三样品分析仪,其包括与所述第二流动控制装置流体连通的第三色谱柱;第四样品分析仪,其包括定量检测器;和控制单元,其联接到所述第一和第二流动控制装置,并且被配置成使得在所述系统的操作期间,所述控制单元:(a)调节所述第一流动控制装置的配置,以将来自所述第一流动控制装置的生物样品的第一部分引导到所述样品纯化装置中或所述第二流动控制装置中,使得所述生物样品的所述部分被所述第二流动控制装置接收;(b)调节所述第二流动控制装置的配置,以将所述生物样品的所述第一部分引导至所述第一、第二、第三、和第四样品分析仪中的一者;(c)基于所述第一、第二、第三和第四样品分析仪中的所述一者对所述生物样品的所述部分的分析,确定所述生物样品的分析物的第一产品品质属性;并且(d)对所述生物样品的另外三个部分重复步骤(a)-(c),调节所述第二流动控制装置的配置,使得所述生物样品的每个部分被引导至所述样品分析仪中不同的样品分析仪,以确定所述生物样品的所述分析物的总共四个产品品质属性。
31.所述系统的实施方案可包括以下特征中的任何一个或多个。
32.所述四个产品品质属性可以各不相同。所述第一、第二和第三色谱柱可以是各不相同的类型的柱。所述第一色谱柱可以是阳离子交换柱,所述第二色谱柱可以是尺寸排阻柱,所述第三色谱柱可以是反相柱或亲水相互作用柱。
33.所述第一样品分析仪可以确定关于所述生物样品中所述分析物的电荷变化或异质性的度量的信息,所述第二样品分析仪可以确定关于所述生物样品中所述分析物的聚集的度量的信息,所述第三样品分析仪可以确定关于所述生物样品中所述分析物的纯度或完整性的度量的信息,并且所述第四样品分析仪可以确定关于所述生物样品中所述分析物的浓度的信息。
34.所述四个产品品质属性可以包括所述生物样品中所述分析物的电荷变化或异质性的度量、所述生物样品中所述分析物的聚集的度量、所述生物样品中所述分析物的纯度或完整性的度量、以及所述生物样品中所述分析物的浓度。所述第一色谱柱可以是阳离子交换色谱柱,所述第二色谱柱可以是尺寸排阻色谱柱,并且所述第三色谱柱可以是反相色谱柱。
35.所述样品纯化装置可以包括亲和色谱柱。所述分析物可以包括所述生物样品中的蛋白质。所述蛋白质可以包括所述生物样品中的抗体。
36.所述系统可以包括柱管理器,其与所述第一、第二、和第三样品分析仪以及所述第二流动控制装置流体连通,并且联接到所述控制单元,其中所述控制单元被配置为调节所述柱管理器的配置,以将所述生物样品的所述部分引导到所述第一、第二、和第三样品分析仪中的一者中。所述系统可以包括采样装置,其联接到所述控制单元,并且被配置为接收所述生物样品,并且将所述生物样品的所述部分递送到所述第一流体控制装置。
37.所述定量检测器可以包括二极管阵列检测器、被配置为测量所述生物样品的所述部分的吸光度信息的光谱检测器、荧光检测器、和质谱检测器中的一种。
38.所述系统的实施方案还可以包括本文描述的任何其他特征,包括在不同实施方案中各自公开的特征的任何组合,除非另有明确说明。
39.在另一方面,本公开的特征在于用于测量生物样品的分析物的产品品质属性的方法,所述方法包括通过从正在操作的生物反应器或者从与所述正在操作的生物反应器流体连通的纯化设备中提取生物样品来获得所述生物样品,将所述生物样品的第一部分引导至第一样品分析仪,并通过在所述第一样品分析仪中分析所述生物样品的所述第一部分来获得关于所述生物样品的分析物的第一产品品质属性的信息,将所述生物样品的第二部分引导至第二样品分析仪,并通过在所述第二样品分析仪中分析所述生物样品的所述第二部分来获得关于所述生物样品的分析物的第二产品品质属性的信息,其中所述第一和第二产品品质属性不同,并且其中所述第一和第二产品品质属性中的至少一者包括所述生物样品中所述分析物的电荷变化或异质性的度量、所述生物样品中所述分析物的聚集的度量、所述生物样品中所述分析物的纯度或完整性的度量、以及所述生物样品中所述分析物的浓度。
40.所述方法的实施方案还可以包括本文描述的任何其他特征,包括在不同实施方案中各自公开的特征的任何组合,除非另有明确说明。
41.定义
42.术语“单元操作”是本领域的术语,意指可以在从液体培养基制造治疗性蛋白质药物的工艺中执行的功能步骤。例如,操作单元可以是过滤(例如,从含重组治疗性蛋白质的流体中去除污染细菌、酵母、病毒或分枝杆菌和/或颗粒物质)、捕获、去除表位标签、纯化、保持或储存、精制、病毒灭活、调节含重组治疗性蛋白质的流体的离子浓度和/或ph和去除不需要的盐。
43.术语“色谱的循环”或“色谱循环”是本领域的术语,意指使用单一色谱柱在一轮色谱分析中进行的所有步骤。例如,色谱循环可以包括用缓冲液平衡色谱柱、使包含重组蛋白质的样品通过色谱柱、从色谱柱洗脱重组蛋白质、以及通过使变性缓冲液通过色谱柱来洗涤色谱柱的步骤。本文描述了在色谱分析循环中执行的步骤的另外的例子。色谱循环中进行的步骤的进一步例子也是本领域公知的。
44.术语“捕获”意指执行来从液体培养基或稀释的液体培养基中存在的一种或多种其他组分(例如培养基蛋白质或哺乳动物细胞中存在或从哺乳动物细胞分泌的一种或多种其他组分(例如,dna、rna或其他蛋白质))部分纯化或分离(例如,按重量计至少或约5%(例如,至少或约10%、15%、20%、25%、30%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%或至少或约95%)纯)、浓缩、并稳定重组治疗性蛋白质的步骤。典型地,使用结合重组治疗性蛋白质的树脂进行捕获(例如,通过使用亲和色谱)。本文描述了用于从液体培养基或稀释的液体培养基捕获重组治疗性蛋白质的非限制性方法,并且其他方法是本领域中已知的。可以使用至少一个色谱柱和/或色谱膜(例如,本文所述的任何色谱柱和/或色谱膜)从液体培养基捕获重组治疗性蛋白质。
45.术语“纯化”意指执行来使重组治疗性蛋白质与含重组治疗性蛋白质的流体中存在的一种或多种其他杂质(例如,主要杂质)或组分(例如液体培养基蛋白质或哺乳动物细胞中存在或从哺乳动物细胞分泌的一种或多种其他组分(例如,dna、rna或其他蛋白质、内
毒素、病毒等))分离的步骤。例如,可以在初始捕获步骤期间或之后执行纯化。可以使用树脂、膜或结合重组治疗性蛋白质或污染物的任何其他固体支持物(例如,通过使用亲和色谱、疏水相互作用色谱、阴离子或阳离子交换色谱或分子筛色谱)执行纯化。可以使用至少一个色谱柱和/或色谱膜(例如,本文所述的任何色谱柱或色谱膜)从含重组治疗性蛋白质的流体纯化重组治疗性蛋白质。
46.术语“精制”是本领域的术语,并且意指执行来从接近最终所需纯度的含重组治疗性蛋白质的流体去除残留的痕量或少量污染物或杂质的步骤。例如,可以通过使含重组治疗性蛋白质的流体通过一个或多个色谱柱或一个或多个膜吸收器来执行精制,所述色谱柱或膜吸收器选择性地结合含重组治疗性蛋白质的流体中存在的靶重组治疗性蛋白质或少量的污染物或杂质。在此种例子中,一个或多个色谱柱或一个或多个膜吸收器的洗脱物/滤液含有重组治疗性蛋白质。
47.术语“过滤”意指从液体(例如,本文所述的任何系统或工艺中的液体培养基或流体)去除至少部分(例如,至少80%、90%、95%、96%、97%、98%或99%)不期望的生物污染物(例如,哺乳动物细胞、细菌、酵母细胞、病毒或分枝杆菌)和/或颗粒物质(例如,沉淀的蛋白质)。
48.术语“洗脱物/滤液”是本领域的术语,并且意指从色谱柱或色谱膜释放出的流体,所述流体包含可检测量的重组治疗性蛋白质。
49.术语“分离”或“分离的”在某些上下文中意指从滤液(例如,使用目前描述的方法生成的滤液)中存在的一种或多种其他组分中至少部分纯化或纯化(例如,按重量计,至少或约5%,例如至少或约10%、15%、20%、25%、30%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、或至少或约95%的纯度)重组蛋白质,例如滤液中存在的dna、rna和/或其他蛋白质的一种或多种组分。本文描述了从滤液中分离蛋白质的非限制性方法,其他方法是本领域已知的。
50.术语“整合工艺”意指使用协同作用以实现特定结果的结构元件进行的工艺(例如,从液体培养基中生成治疗性蛋白质药物)。
51.术语“连续工艺”意指将流体连续馈送通过系统的至少一部分的工艺。例如,在本文所述的任何示例性连续生物制造系统中,当系统操作时,将含有重组治疗性蛋白质的液体培养基连续送入系统,并将治疗性蛋白质药物物质从系统中送出。在另一个例子中,连续工艺是从生物反应器通过第一mccs连续馈送含有重组治疗性蛋白质的液体培养基的工艺。连续工艺的另一个例子是通过第一和第二mccs连续地从生物反应器馈送含有重组治疗性蛋白质的液体培养基的工艺。另外的例子包括通过第一mccs连续馈送含有重组治疗性蛋白质的液体培养基的工艺,通过第一和第二mccs连续馈送含有重组治疗性蛋白质的液体培养基的工艺,或通过第二mccs连续馈送含有重组治疗性蛋白质的流体的工艺。
52.术语“生物制造系统(biological manufacturing system或bio-manufacturing system)”是指用于生产生物药物的系统。
53.术语“生物药物”意指从活生物体或其产品中制成或获得的用于预防、诊断或治疗病理的任何治疗性物质。因此,生物药物或生物制药是使用生物技术生产的医学药物,例如,用于治疗或体内诊断目的的蛋白质(例如,重组治疗性蛋白质)或核酸(dna、rna或反义寡核苷酸)。
54.术语“多柱色谱系统”或“mccs”意指具有总共两个或更多个互连或切换的色谱柱和/或色谱膜的系统。多柱色谱系统的非限制性例子是周期性逆流色谱系统(pcc),其包含总共两个或更多个互连或切换的色谱柱和/或色谱膜。本文描述了多柱色谱系统的其他例子,并且其是本领域中已知的。
55.术语“哺乳动物细胞”意指来自或源自任何哺乳动物(例如,人、仓鼠、小鼠、绿猴、大鼠、猪、母牛或兔)的任何细胞。在一些实施方案中,哺乳动物细胞可以是例如永生化细胞、分化细胞或未分化细胞。
56.术语“细胞培养物”意指悬浮在液体培养基(例如本文所述的任何液体培养基)中的多种哺乳动物细胞(例如本文所述的任何哺乳动物细胞)。细胞培养物可以具有大于约0.1x106个细胞/ml的细胞密度(例如,大于约1.0x106个细胞/ml,大于约5.0x106个细胞/ml,大于约10x106个细胞/ml,大于约15x106个细胞/ml,大于约20x106个细胞/ml,大于约25x106个细胞/ml,大于约30x106个细胞/ml,大于约35x106个细胞/ml,大于约40x106个细胞/ml,大于约45x106个细胞/ml,大于约50x106个细胞/ml,大于约55x106个细胞/ml,大于约60x106个细胞/ml,大于约65x106个细胞/ml,大于约70x106个细胞/ml,大于约75x106个细胞/ml,大于约80x106个细胞/ml,大于约85x106个细胞/ml,大于约90x106个细胞/ml,大于约95x106个细胞/ml,大于约100x106个细胞/ml)。
57.术语“培养”或“细胞培养”意指在一组受控的物理条件下,哺乳动物细胞在液体培养基中的维持或生长。
58.术语“液体培养基”意指含有足够的营养物质以使哺乳动物细胞在体外培养基中生长的流体。例如,液体培养基可以包含以下一种或多种:氨基酸(例如20种氨基酸)、嘌呤(例如次黄嘌呤)、嘧啶(例如胸苷)、胆碱、肌醇、硫胺素、叶酸、生物素、钙、烟酰胺、吡哆醇、核黄素、胸苷、氰钴胺素、丙酮酸、硫辛酸、镁、葡萄糖、钠、钾、离子、铜、锌、硒和其他必需的痕量金属以及碳酸氢钠。液体培养基可以含有来自哺乳动物的血清。在某些情况下,液体培养基不含来自哺乳动物的血清或其他提取物(确定成分的液体培养基)。液体培养基可以含有痕量金属、哺乳动物生长激素和/或哺乳动物生长因子。本文描述了液体培养基的非限制性例子,另外的例子在本领域中是已知的,并且是可商购的。
59.术语“免疫球蛋白质”意指包含具有至少15个氨基酸(例如,至少20、30、40、50、60、70、80、90或100个氨基酸)的氨基酸序列(例如,可变结构域序列、框架序列、或恒定结构域序列)的免疫球蛋白质的多肽。免疫球蛋白质可以例如包括至少15个氨基酸的轻链免疫球蛋白质,例如至少15个氨基酸的重链免疫球蛋白质。免疫球蛋白质可以是分离的抗体(例如,igg、ige、igd、iga、或igm)。免疫球蛋白质可以是igg的一个亚类(例如,igg1、igg2、igg3或igg4)。免疫球蛋白质可以是抗体片段,例如fab片段、f(ab')2片段或scfv片段。免疫球蛋白质还可以是双特异性抗体或三特异性抗体,或二聚体、三聚体或多聚体抗体,或双抗体,或免疫球蛋白质还可以是包含至少一个免疫球蛋白质结构域的经工程化蛋白质(例如融合蛋白质)。本文描述了免疫球蛋白质的非限制性例子,并且免疫球蛋白质的其他例子是本领域中已知的。
60.术语“重组治疗性蛋白质”或“重组蛋白质”是指通过重组dna技术获得的任何治疗性蛋白质。如本文所用,“重组治疗性蛋白质”包括例如抗体或抗体片段、酶、工程蛋白质、或免疫原性蛋白质或蛋白质片段。
61.术语“蛋白质片段”或“多肽片段”意指多肽序列的一部分,其长度为至少或约4个氨基酸、至少或约5个氨基酸、至少或约6个氨基酸、至少或约7个氨基酸、至少或约8个氨基酸、至少或约9个氨基酸、至少或约10个氨基酸、至少或约11个氨基酸、至少或约12个氨基酸、至少或约13个氨基酸、至少或约14个氨基酸、至少或约15个氨基酸、至少或约16个氨基酸、至少或约17个氨基酸、至少或约18个氨基酸、至少或约19个氨基酸或至少或约20个氨基酸,或长度为超过20个氨基酸。可以使用本文描述的任何工艺生产重组蛋白质片段。
62.术语“工程化蛋白质”意指不是由生物体(例如哺乳动物)内存在的内源性核酸天然编码的多肽。工程化蛋白质的例子包括酶(例如,具有一个或多个使工程化酶的稳定性和/或催化活性增加的氨基酸取代、缺失、插入或添加)、融合蛋白质、抗体(例如,二价抗体、三价抗体或双抗体)和包含至少一个重组支架序列的抗原结合蛋白质。
63.术语“分泌的蛋白质”或“分泌的重组蛋白质”意指如下蛋白质(例如,重组蛋白质),其在哺乳动物细胞内翻译时最初包含至少一个分泌信号序列,并且在哺乳动物细胞中至少部分通过酶促切割分泌信号序列而至少部分分泌到细胞外空间(例如,液体培养基)中。“分泌的”蛋白质不需要完全从细胞中解离以被认为是分泌的蛋白质。
64.术语“灌注生物反应器”意指在第一液体培养基中含有多个细胞(例如,哺乳动物细胞)的生物反应器,其中存在于所述生物反应器中的细胞的培养包括定期或连续去除所述第一液体培养基并且同时或此后不久将基本上相同体积的第二液体培养基添加至所述生物反应器中。在一些例子中,在培养时间段内经递增的时间段(例如,约24小时的时间段、约1分钟与约24小时之间的时间段或大于24小时的时间段)去除和添加的第一液体培养基的体积存在递增变化(例如,增加或减少)(例如,培养基的每天再馈送速率)。每天去除和更换的培养基分数可以根据培养的特定细胞、初始接种密度和特定时间的细胞密度而变化。“rv”或“反应器体积”意指培养过程开始时存在的培养基的体积(例如,接种后存在的培养基的总体积)。
65.术语“补料分批生物反应器”是本领域的术语,并且意指在第一液体培养基中含有多个细胞(例如,哺乳动物细胞)的生物反应器,其中存在于所述生物反应器中的细胞的培养包括在不从所述细胞培养物大量或显著地去除所述第一液体培养基或第二液体培养基的情况下将第二液体培养基定期或连续添加至所述第一液体培养基中。所述第二液体培养基可以与所述第一液体培养基相同。在补料分批培养的一些例子中,所述第二液体培养基是所述第一液体培养基的浓缩形式。在补料分批培养的一些例子中,将所述第二液体培养基作为干粉添加。
66.除非另有定义,否则本文所使用的所有技术和科学术语均具有与本公开文本所属领域的一般技术人员所通常理解的含义相同的含义。下文描述了合适的方法和材料,但是在本文主题的实践或测试中可使用与本文所述类似或等同的方法和材料。本文提及的所有出版物、专利申请、专利以及其他参考文献都通过引用整体并入。如有冲突,以本说明书(包括定义)为准。另外,材料、方法以及例子仅为说明性的而不旨在进行限制。
67.在附图及下文描述中陈述一或多个实施方案的细节。从具体实施方式、附图说明及权利要求书,其他特征和优点将显而易见。
附图说明
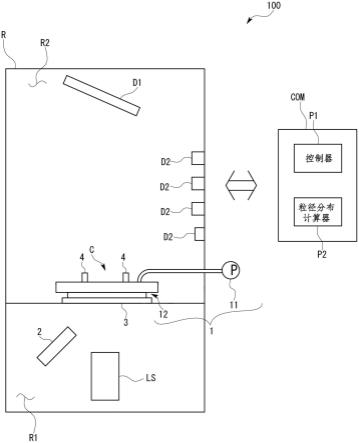
68.图1是用于确定生物样品的分析物的产品品质属性的系统的例子的示意图。
69.图2是样品管理器的例子的示意图。
70.图3是示出用于确定生物样品的分析物的产品品质属性的一组示例性步骤的流程图。
71.图4a-4c是示出流动控制装置的示例性配置的示意图。
72.图5a是示出多个样品的效价色谱图的曲线图。
73.图5b是示出多个样品的计算质量负荷和浓度的表格。
74.图6a是示出多个样品的效价色谱图的曲线图。
75.图6b是具有不同样品的测量峰信息的一组表格。
76.图7是示出一组样品的测量色谱图的曲线图。
77.图8是示出生物制造系统的例子的示意图。
78.图9是示出三柱切换技术的例子的示意图。
79.图10是比较治疗性单克隆抗体100l生物反应器的三种效价方法(mimics-mpqa-蓝色;cedex
tm
生物分析仪-红色;octet-绿色)的曲线图。mimics-mpqa上绘制的所有数据点都是冷冻收获。数据缺口代表未分析的样品。
80.图11是比较治疗性单克隆抗体3l生物反应器(v09)的三种效价方法(mimics-mpqa-蓝色;cedex
tm
生物分析仪-红色;octet-绿色)的曲线图。mimics-mpqa上绘制的所有数据点都是冷冻收获。数据缺口代表未分析的样品。
81.图12是比较治疗性单克隆抗体3l生物反应器(v12)的三种效价滴定方法(mimics-mpqa-蓝色;cedex
tm
生物分析仪-红色;octet-绿色)的曲线图。mimics-mpqa上绘制的所有数据点都是冷冻收获。数据缺口代表未分析的样品。
82.图13是用于比较治疗性单克隆抗体100l生物反应器的两种聚集方法(mimics-mpqa和离线方法)的曲线图。该图比较了两种测定结果:单体百分比和高分子量(hmw)百分比。mimics-mpqa上绘制的所有数据点均来自冷冻收获。数据缺口代表未分析的样品。
83.图14是用于比较治疗性单克隆抗体3l生物反应器(v09)的两种聚集方法(mimics-mpqa和离线方法)的曲线图。该图比较了两种测定结果:单体百分比和高分子量(hmw)百分比。mimics-mpqa上绘制的所有数据点均来自冷冻收获。数据缺口代表未分析的样品。
84.图15是用于比较治疗性单克隆抗体3l生物反应器(v12)的两种聚集方法(mimics-mpqa和离线方法)的曲线图。该图比较了两种测定结果:单体百分比和高分子量(hmw)百分比。mimics-mpqa上绘制的所有数据点均来自冷冻收获。数据缺口代表未分析的样品。
85.图16是比较来自治疗性单克隆抗体的所有生物反应器(100l、3l v09、3l v12)的两种纯度方法(mimics-mpqa和离线方法)总%纯度的曲线图。mimics-mpqa上绘制的所有数据点均来自冷冻收获。数据缺口代表未分析的样品。
86.图中相同的符号表示相同的元件。
具体实施方式
87.引言
88.工业规模的生物制造可以在双柱和多柱色谱系统中以各种配置进行。在这些复杂
系统中,产品产量、品质和废品率是大量与工艺相关的参数和步骤的函数。在制造治疗性蛋白质和其他具有商业价值的生物分子期间,产品结果可受这些参数和步骤的强烈影响。因此,适当控制此类参数和步骤是大规模制造的重要方面。例如,在pct专利申请公开号wo 2014/137903中公开了生物制造系统的特征和方面,将该申请的全部内容通过引用并入本文。
89.通过监测生物反应器收获、中间溶液流和/或产品,有助于对生物制造参数进行适当控制,包括自动控制。常规监测技术包括,例如,uv吸光度测量。
90.不幸的是,由于温度、湿度、环境光强度和局部样品不均匀性等因素,这些方法可能会在几天的测量周期内发生漂移。此外,这种方法可能不允许计算或以其他方式确定多个量。在复杂的生物制造环境中,通常评估多个量,以便为工艺参数的调节提供合适的反馈信息。
91.本公开的特征在于可用于确定多个产品品质属性的值的系统和方法。所述系统可以实施为二维色谱系统。沿着系统的第一维,可以任选地使用样品纯化装置纯化生物样品的一部分,该样品纯化装置可以包括色谱柱。沿着系统的第二维,样品的该部分然后可以被引导到多个不同的样品分析仪中的一者,以确定样品的产品品质属性。样品的其他部分可被引导至不同的样品分析仪,以确定样品的不同产品品质属性。
92.产品品质属性分析系统
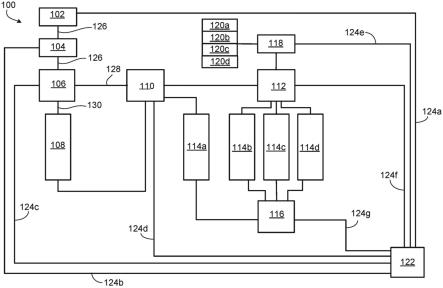
93.图1是示出用于测量多个产品品质属性的测量系统100的例子的示意图。系统100包括样品管理器102、第一泵104(例如,二元泵)、第一流动控制装置106、样品纯化装置108、第二流动控制装置110、柱管理器112、多个样品分析仪114a-114d、检测器116、第二泵118(例如,四元泵)、溶剂/缓冲液储器120a-120d、和控制单元122。样品管理器102、泵104、第一流动控制装置106、第二流动控制装置110、柱管理器112和检测器116可以通过通信线路124a-124g连接到控制单元122。
94.在操作期间,样品管理器102接收用于分析的生物样品。样品管理器102可以以各种方式实施。例如,在一些实施方案中,样品管理器包括容器接收器,其被配置成将样品接收在容器中。合适的容器包括例如小瓶、试管和其他密封或未密封的容器。在某些实施方案中,样品可以由单孔或多孔板承载,并且容器接收器被配置成接收这样的板。样品管理器102可以任选地包括用于将部分生物样品转移到第一流动控制装置106中的转移机构。合适的转移机构包括但不限于基于注射筒的样品注射装置和单通道或多通道流体转移装置。合适的样品管理器的例子包括带流通针(flow through needle)的沃特世h类样品管理器(waters h class sample manager)和沃特世工艺样品管理器(waters process sample manager)(均可从waters corp.,milford,ma获得)。
95.在某些实施方案中,样品管理器102从与生物反应器、流体导管或生物制造系统的另一部件流体连通的采样装置接收生物样品。例如,生物样品可以直接从生物反应器中收获(因此对应于生长培养基的收获样品),或者可以是从生物制造系统的另一个位置提取的溶液或培养基。
96.图2是被配置成直接从采样装置接收生物样品的样品管理器102的例子的示意图。样品管理器102包括入口202、保持导管204和经由控制线路124c联接到控制单元122的闸阀206。生物样品通过入口202被引入样品管理器102,并且样品在被递送到保持导管204内的
第一流动控制装置106之前被维持。为了将一部分样品递送到第一流动控制装置106中,控制单元122向闸阀206发送信号。闸阀206打开,将一部分样品从保持导管204排入出口导管208。样品的排出部分然后被泵送(例如,通过第一泵104)到第一流动控制装置106。
97.通常,样品管理器102可以接收多种不同的生物样品。在一些实施方案中,如上所述,生物样品对应于来自生物反应器的生长培养基的收获部分。在某些实施方案中,生物样品对应于从生物制造系统中的另一位置提取的工艺流体或介质,例如在生物制造系统中的纯化阶段之前或之后取样的含产品或中间体的溶液。
98.在某些实施方案中,系统100可用于确定细胞系开发的产品品质属性,并且生物样品对应于细胞培养物的一部分、细胞培养基、细胞的流体悬浮液,或其中存在细胞、细胞分解产物、细胞代谢物和/或细胞培养物杂质的另一种类型的样品。
99.系统100确定由样品管理器102接收的生物样品中的一种或多种分析物的产品品质属性。一般来说,可以为各种不同类型的分析物确定属性。例如,在一些实施方案中,系统100确定蛋白质分析物的产品品质属性,所述蛋白质分析物包括但不限于抗体(包括单特异性、双特异性和三特异性抗体)、非抗体蛋白质、融合蛋白质、和/或fab片段。
100.在一些实施方案中,所述分析物是重组治疗性蛋白质。可使用本文公开的系统和方法分析的重组治疗性蛋白质的非限制性例子包括免疫球蛋白质(包括轻链和重链免疫球蛋白质、抗体或抗体片段(例如,本文所述的任何抗体片段))、酶(例如,半乳糖苷酶(例如,α-半乳糖苷酶)、myozyme或cerezyme)、蛋白质(例如,人促红细胞生成素、肿瘤坏死因子(tnf)或干扰素α或β)或免疫原性或抗原性蛋白质或蛋白质片段(例如,用于疫苗的蛋白质)。重组治疗性蛋白质可以是包含至少一种多功能重组蛋白质支架的工程化抗原结合多肽(参见,例如,gebauer等人在current opin.chem.biol.13:245-255,2009中;和美国专利申请第2012/0164066号中描述的重组抗原结合蛋白(通过引用将其全部内容结合于此))。
101.作为抗体的重组治疗性蛋白质的非限制性例子包括:帕尼单抗(panitumumab)、奥马珠单抗(omalizumab)、阿巴伏单抗(abagovomab)、阿昔单抗(abciximab)、阿克托单抗(actoxumab)、阿达木单抗(adalimumab)、阿德木单抗(adecatumumab)、阿非莫单抗(afelimomab)、阿夫土珠单抗(afutuzumab)、(alacizumab)、阿拉赛珠单抗(alacizumab)、阿仑单抗(alemtuzumab)、阿利库单抗(alirocumab)、阿妥莫单抗(altumomab)、阿玛妥昔单抗(amatuximab)、阿玛妥昔单抗(amatuximab)、安那莫单抗(anatumomab)、(anrukinzumab)、阿泊珠单抗(apolizumab)、(arcitumomab)、阿替努单抗(atinumab)、托珠单抗(tocilizumab)、巴西利单抗(basilizimab)、贝妥莫单抗(bectumomab)、贝利木单抗(belimumab)、贝伐单抗(bevacizumab)、贝西洛索单抗(besilesomab)、贝佐妥单抗(bezlotoxumab)、比西单抗(biciromab)、康纳单抗(canakinumab)、赛妥珠单抗(certolizumab)、西妥昔单抗(cetuximab)、(cixutumumab)、达克珠单抗(daclizumab)、(denosumab)、登苏单抗(densumab)、依库珠单抗(eculizumab)、依决洛单抗(edrecolomab)、依法珠单抗(efalizumab)、依芬古单抗(efungumab)、(epratuzumab)、厄马索单抗(ertumaxomab)、伊瑞西珠单抗(etaracizumab)、芬妥木单抗(figitumumab)、戈利木单抗(golimumab)、替伊莫单抗(ibritumomab tiuxetan)、伊戈伏单抗(igovomab)、英妥组单抗(imgatuzumab)、英夫利昔(infliximab)、伊诺莫单抗(inolimomab)、奥英妥珠单抗(inotuzumab)、拉贝珠单抗(labetuzumab)、罗氏单抗(lebrikizumab)、(moxetumomab)、那
他珠单抗(natalizumab)、奥滨尤妥珠单抗(obinutuzumab)、奥戈伏单抗(oregovomab)、帕利珠单抗(palivizumab)、帕尼单抗(panitumumab)、帕妥珠单抗(pertuzumab)、兰尼单抗(ranibizumab)、利妥昔单抗(rituximab)、托珠单抗(tocilizumab)、托西莫单抗(tositumomab)、tralokinumab、tucotuzumab、曲妥珠单抗(trastuzumab)、veltuzumab、扎鲁木单抗(zalutumumab)、和zatuximab。
102.可以分析的重组治疗性蛋白质的其他非限制性实例包括:阿糖苷酶α、拉罗尼酶、阿巴西普、加硫酶、促黄体素α、抗嗜血因子、agalsidase beta、干扰素β-1a、阿法达贝泊汀(darbepoetin alfa)、替奈普酶、依那西普、凝血因子ix、卵泡刺激素、干扰素β-1a、伊米苷酶、阿法链道酶、阿法依泊汀、胰岛素或胰岛素类似物、美卡舍明、因子viii、因子viia、抗凝血酶iii、蛋白质c、人血清蛋白、促红细胞生成素、颗粒集落刺激因子、粒细胞巨噬细胞集落刺激因子、白细胞介素-11、拉罗尼酶、idursuphase、加硫酶(galsulphase)、α-1蛋白酶抑制剂、乳糖酶、腺苷脱氨酶、组织纤溶酶原激活剂、促甲状腺素α(如)和阿替普酶。可通过本发明方法生产的重组蛋白质的其他例子包括酸性α-葡糖苷酶、alglucosidase阿尔法(如and )、α-l-艾杜糖醛酸酶(如)、艾杜糖醛酸硫酸酯酶、乙酰肝素n-硫酸酯酶、半乳糖-6-硫酸酯酶、酸性β-半乳糖苷酶、β-葡糖苷酶、n-乙酰葡糖胺-1-磷酸转移酶、α-n-乙酰半乳糖胺酶、酸性脂肪酶、溶酶体酸神经酰胺酶、酸性鞘磷脂酶、β-葡萄糖苷酶(如and )、半乳糖神经酰胺酶、α-半乳糖苷酶-a(如)、酸性β-半乳糖苷酶、β-半乳糖苷酶、神经氨酸酶、己糖胺酶a、和己糖胺酶b。
103.如上所述,在一些实施方案中,分析物是细胞的组分,并且本文所述的方法和系统可用于细胞系工艺开发。这种细胞的例子包括但不限于细菌(例如,革兰氏阴性细菌)、酵母(例如,酿酒酵母(saccharomyces cerevisiae)、巴斯德毕赤酵母(pichia pastoris)、多形汉逊酵母(hansenula polymorpha)、乳酸克鲁维酵母(kluyveromyces lactis)、粟酒裂殖酵母(schizosaccharomyces pombe)、解脂耶氏酵母(yarrowia lipolytica)或解腺嘌呤阿氏酵母(arxula adeninivorans)),或哺乳动物细胞。哺乳动物细胞可以是悬浮生长的细胞或贴壁细胞。哺乳动物细胞的非限制性例子包括:中国仓鼠卵巢(cho)细胞(例如,cho dg44细胞或cho-k1细胞)、sp2.0、骨髓瘤细胞(例如ns/0)、b细胞、杂交瘤细胞、t细胞、人胚肾(hek)细胞(例如,hek 293e和hek293f)、非洲绿猴肾上皮细胞(vero)细胞和马丁达比犬(madin-darby canine)(可卡犬(cocker spaniel))肾上皮细胞(mdck)。
104.哺乳动物细胞可以包含编码重组治疗性蛋白质的重组核酸(例如,稳定地整合在哺乳动物细胞基因组中的核酸)。编码示例性重组治疗性蛋白质的重组核酸的非限制性例子如下所述,所述重组治疗性蛋白质是可以使用本文所述方法产生的重组治疗性蛋白质。在一些情况下,在生物反应器(例如,本文所述的任何生物反应器)中培养的哺乳动物细胞来自更大的培养物。
105.可以使用分子生物学和分子遗传学中已知的多种方法将编码重组治疗性蛋白质的核酸导入哺乳动物细胞。非限制性例子包括转染(例如,脂质转染)、转导(例如慢病毒、腺病毒或逆转录病毒感染)和电穿孔。在一些情况下,编码重组治疗性蛋白质的核酸不能稳定地整合到哺乳动物细胞的染色体中(瞬时转染),而在其他情况下,核酸是整合的。可选地或
另外地,编码重组治疗性蛋白质的核酸可以存在于质粒和/或哺乳动物人工染色体(例如,人类人工染色体)中。可替代地或另外,可以使用病毒载体(例如慢病毒、逆转录病毒或腺病毒载体)将核酸引入细胞中。核酸可以与启动子序列(例如,强启动子,诸如β-肌动蛋白质启动子和cmv启动子,或诱导型启动子)可操作地连接。如果需要,包含核酸的载体还可以包含选择性标记(例如,赋予哺乳动物细胞潮霉素、嘌呤霉素或新霉素抗性的基因)。
106.在一些实施方案中,重组治疗性蛋白质是一种分泌蛋白质,由哺乳动物细胞释放到细胞外介质中。例如,编码可溶性重组治疗性蛋白质的核酸序列可以包含编码重组治疗性蛋白质的n端或c端分泌信号肽的序列,该序列被哺乳动物细胞中存在的酶切割,随后释放到细胞外介质中。
107.在样品管理器102接收到生物样品后,样品由第一泵104通过导管126输送到第一流动控制装置106。第一流动控制装置106通过控制线路124b连接到控制单元122。通常,生物样品可以通过第一流动控制装置106递送到多个不同的输出端。在第一配置中,第一流动控制装置106通过导管128将生物样品直接递送到第二流动控制装置110。在另一种配置中,第一流动控制装置106通过导管130将生物样品递送到样品纯化装置108。控制单元122被配置成调节第一流动控制装置106的配置,以根据生物样品的期望分析模式将生物样品导向任一目的地。
108.第一流动控制装置106可以以各种方式实施。在一些实施方案中,例如,第一流动控制装置106可以实施为多路阀。合适的阀包括,例如,idex mx系列ii的2位、6端口ultralife转换阀(可从idex corp.,lake forest,il获得)。在某些实施方案中,第一流动控制装置106可以被实施为具有输入和/或输出歧管和可电控的流量调节器的多通道流体装置。
109.当生物样品被引导至样品纯化装置108时,在系统100中分析样品之前,生物样品至少被部分纯化。纯化可以以多种方式进行,但通常包括从样品中去除一种或多种非分析物组分。可选地,或者另外,生物样品的纯化也可以包括样品中分析物的浓缩,以及样品中一种分析物与另外一种或多种分析物的分离。
110.样品纯化装置108可以以各种方式实施。在一些实施方案中,例如,样品纯化设备108被实施为色谱设备,并且以一个或多个色谱柱为特征。用于样品纯化装置108的合适色谱柱包括例如亲和色谱柱。术语“亲和色谱”是指一种基于亲和力捕获和分离分析物分子(例如重组蛋白质分析物)的色谱类型。亲和色谱是指使用亲和色谱树脂(例如,包括蛋白质配体(例如,蛋白a或蛋白g))的亲和色谱树脂)。在一些实施方案中,亲和色谱包括假亲和色谱树脂。在一些实施方案中,亲和色谱树脂包括辅因子配体、底物配体、金属配体、产物配体或适体配体。通常,亲和色谱树脂可以包括对任何生物分析物具有亲和力的任何受体或配体,包括dna、寡核苷酸。在一些实施方案中,亲和色谱树脂可以包括来自驼科的单结构域抗体片段,用于基因治疗载体的纯化。作为另一个例子,亲和色谱柱可以是腺相关病毒(aav)亲和色谱柱。
111.亲和色谱树脂的非限制性例子可以包含蛋白质或肽配体(例如,约5个氨基酸至约100个氨基酸之间、约5个氨基酸至约90个氨基酸之间、约5个氨基酸至约80个氨基酸之间、约5个氨基酸至约70个氨基酸之间、约5个氨基酸至约60个氨基酸之间、约5个氨基酸至约50个氨基酸之间、约5个氨基酸至约40个氨基酸之间、约5个氨基酸至约30个氨基酸之间、或约
5个氨基酸至约20个氨基酸之间)、酶的小分子底物或辅因子、适体、抑制剂(例如竞争性蛋白质抑制剂)或金属。
112.蛋白a亲和色谱树脂的非限制性例子有:ge mabselect suretm(一种高度交联的琼脂糖树脂,粒径为85μm,环氧官能团将蛋白a连接到琼脂糖上)、jjsr lifesciences amsphere proa jwt203(一种多孔的聚甲基丙烯酸酯树脂,粒径约为50μm,环氧官能团将蛋白a连接到聚甲基丙烯酸酯上)、和kaneka kancap a(一种高度交联的纤维素,粒径为65-85μm,通过还原胺化将蛋白a连接到纤维素上)。
113.对于亲和色谱柱,例如蛋白a柱,亲和色谱循环中的步骤可以包括以下步骤:用包含分析物的流体加载亲和柱,例如蛋白a色谱柱,洗涤柱以除去不需要的生物材料(例如污染蛋白质和/或小分子),洗脱结合到柱上的靶重组蛋白质,并使柱再平衡。
114.色谱循环中的任何单个步骤都可以包括单一缓冲液或多种缓冲液(例如,两种或更多种缓冲液),并且色谱循环中的任何单个步骤中的一个或多个可以包括缓冲液梯度。单个色谱循环的各种熟知方面的任何组合可以以任何组合形式用于这些方法中,例如,一种或多种不同色谱树脂、一种或多种流速、一种或多种缓冲液、柱的一种或多种空隙体积、柱的一种或多种床体积、每个步骤中使用的缓冲液的一种或多种体积、包含靶蛋白质的流体的一种或多种体积以及每个步骤中使用的一种或多种缓冲液的数量和类型。
115.在一些实施方案中,蛋白a柱可以加载有ph约7(例如,约ph 7.0至约ph 7.1、约ph 7.2、约ph 7.3、约ph 7.4、约ph 7.5、约ph 7.6、约ph 7.7、约ph 7.8或约ph 7.9)的1x磷酸盐缓冲盐水(pbs)。在一些实施方案中,蛋白a柱可以加载ph约7.2的1x pbs。
116.在一些实施方案中,蛋白a柱用缓冲液洗脱,所述缓冲液包括约50mm至约200mm的柠檬酸磷酸盐(例如,约50mm至约190mm,约50mm至约180mm,约50mm至约170mm,约50mm至约160mm,约50mm至约150mm,约50mm至约140mm,约50mm至约130mm,约50mm至约120mm,约50mm至约110mm,约50mm至约100mm,约50mm至约90mm,约50mm至约80mm,约50mm至约70mm,约50mm至约60mm,约75mm至约200mm,约75mm至约190mm,约75mm至约180mm,约75mm至约170mm,约75mm至约160mm,约75mm至约150mm,约75mm至约140mm,约75mm至约130mm,约75mm至约120mm,约75mm至约110mm,约75mm至约100mm,约75mm至约90mm,约75mm至约80mm,约100mm至约200mm,约100mm至约190mm,约100mm至约180mm,约100mm至约170mm,约100mm至约160mm,约100mm至约150mm,约100mm至约140mm,约100mm至约130mm,约100mm至约120mm,约100mm至约110mm,约125mm至约200mm,约125mm至约190mm,约125mm至约180mm,约125mm至约170mm,约125mm至约160mm,约125mm至约150mm,约125mm至约140mm,约125mm至约130mm,约150mm至约200mm,约150mm至约190mm,约150mm至约180mm,约150mm至约170mm,约150mm至约160mm,约175mm至约200mm,约175mm至约190mm,约175mm至约180mm,或约180mm至约200mm),约50mm至约200mm的nacl(例如,约50mm至约190mm,约50mm至约180mm,约50mm至约170mm,约50mm至约160mm,约50mm至约150mm,约50mm至约140mm,约50mm至约130mm,约50mm至约120mm,约50mm至约110mm,约50mm至约100mm,约50mm至约90mm,约50mm至约80mm,约50mm至约70mm,约50mm至约60mm,约75mm至约200mm,约75mm至约190mm,约75mm至约180mm,约75mm至约170mm,约75mm至约160mm,约75mm至约150mm,约75mm至约140mm,约75mm至约130mm,约75mm至约120mm,约75mm至约110mm,约75mm至约100mm,约75mm至约90mm,约75mm至约80mm,约100mm至约200mm,约100mm至约190mm,约100mm至约180mm,约100mm至约170mm,约100mm至约160mm,
约100mm至约150mm,约100mm至约140mm,约100mm至约130mm,约100mm至约120mm,约100mm至约110mm,约125mm至约200mm,约125mm至约190mm,约125mm至约180mm,约125mm至约170mm,约125mm至约160mm,约125mm至约150mm,约125mm至约140mm,约125mm至约130mm,约130mm至约200mm,约130mm至约190mm,约130mm至约180mm,约130mm至约170mm,约130mm至约160mm,约130mm至约150mm,约140mm至约200mm,约140mm至约190mm,约140mm至约180mm,约140mm至约170mm,约140mm至约160mm,约140mm至约150mm,约150mm至约200mm,约150mm至约190mm,约150mm至约180mm,约150mm至约170mm,约150mm至约160mm,约175mm至约200mm,约175mm至约190mm,约175mm至约180mm,或约180mm至约200mm),酸碱度约ph 2至约ph 4(例如,约ph 2至约ph 3.8,约ph 2至约ph 3.6,约ph 2至约ph 3.8,约ph 2至约ph 3.6,约ph 2至约ph 3.4,约ph 2至约ph 3.2,约ph 2至约ph 3.0,约ph 2至约ph 2.8,约ph 2至约ph 2.6,约ph 2至约ph 2.4,约ph 2至约ph 2.2,约ph 3至约ph 4,约ph 3至约ph 3.8,约ph 3至约ph 3.6,约ph 3至约ph 3.4,或约ph 3至约ph 3.2)。
117.在一些实施方案中,用约10mm至约100mm(例如,10mm至约90mm,约10mm至约80mm,约10mm至约70mm,约10mm至约60mm,约10mm至约50mm,约10mm至约40mm,约10mm至约30mm,约10mm至约20mm,约15mm至约100mm,约15mm至约90mm,约15mm至约80mm,约15mm至约70mm,约15mm至约60mm,约15mm至约50mm,约15mm至约40mm,约15mm至约30mm,约15mm至约20mm,约20mm至约100mm,约20mm至约90mm,约20mm至约80mm,约20mm至约70mm,约20mm至约60mm,约20mm至约50mm,约20mm至约40mm,约20mm至约30mm,约20mm至约25mm,约30mm至约100mm,约30mm至约90mm,约30mm至约80mm,约30mm至约70mm,约30mm至约60mm,约30mm至约50mm,约30mm至约40mm,约40mm至约100mm,约40mm至约90mm,约40mm至约80mm,约40mm至约70mm,约40mm至约60mm,约40mm至约50mm,约50mm至约100mm,约50mm至约90mm,约50mm至约80mm,约50mm至约70mm,约50mm至约60mm,约60mm至约100mm,约60mm至约90mm,约60mm至约80mm,约60mm至约70mm,约70mm至约100mm,约70mm至约90mm,约70mm至约80mm,约80mm至约100mm,约80mm至约90mm,或约90mm至约100mm)的乙酸钠,以约ph 2至约ph 4(例如,约ph 2至约ph 3.8,约ph 2至约3.75,约ph 2至约ph 3.6,约ph 2至约ph 3.8,约ph 2至约ph 3.6,约ph 2至约ph 3.4,约ph 2至约ph 3.2,约ph 2至约ph 3.0,约ph 2至约ph 2.8,约ph 2至约ph 2.6,约ph 2至约ph 2.4,约ph 2至约ph 2.2,约ph 3至约ph 4,约ph 3至约ph 3.8,约ph 3至约ph 3.75,约ph 3至约ph 3.6,约ph 3至约ph 3.4,或约ph 3至约ph 3.2)洗脱蛋白a柱。
118.使用这种类型的色谱柱进行的色谱分析可以包括,例如,通常进行加载、洗涤、洗脱和再生色谱柱的顺序色谱步骤。本文描述的分配给每个顺序色谱步骤的任何示例性流速、缓冲液体积和/或时间长度可用于这些不同的顺序色谱步骤中的任何一个。
119.在一些实施方案中,在例如约5分钟至约90分钟之间(例如,约10分钟至约90分钟之间,约15分钟至80分钟之间,约20分钟至80分钟之间,约30分钟至约80分钟之间,约40分钟至约80分钟之间以及约50分钟至80分钟之间)加载包含能够捕获分析物的树脂的单个色谱柱或单个色谱膜。
120.在将分析物加载到柱上之后,用至少一种洗涤缓冲液洗涤柱。至少一种(例如,两种、三种或四种)洗涤缓冲液用于从柱中洗脱所有不是分析物的化合物,同时不干扰分析物与树脂的相互作用。
121.洗涤缓冲液可以以约0.1ml/分钟至约25ml/分钟之间(例如,约0.2ml/分钟至约
20ml/分钟之间,约0.5ml/分钟至约20ml/分钟之间,约0.2ml/分钟至约15ml/分钟之间,约0.5ml/分钟至约15ml/分钟之间,约0.5ml/分钟至约10ml/分钟之间,约0.5ml/分钟至约14ml/分钟之间,约1.0ml/分钟至约25.0ml/分钟之间,约1.0ml/分钟至约15.0ml/分钟之间)的流率通过柱。
122.使用的洗涤缓冲液的体积(例如,当使用超过一种洗涤缓冲液时使用的洗涤缓冲液的组合总体积)可以是例如约1x柱体积(cv)至约15x cv之间(例如,约1x cv至约14x cv之间,约1x cv至约13x cv,约1x cv至约12x cv,约1x cv至约11x cv,约2x cv至约11x cv,约3x cv至约11x cv,约4x cv至约11x cv,约5x cv至约11x cv,或约5x cv至约10x cv)。洗涤的总时间可以是例如约2分钟至约3小时之间(例如,约2分钟至约2.5小时之间,约2分钟至约2.0小时之间,约5分钟至约1.5小时之间,约10分钟至约1.5小时之间,约10分钟至约1.25小时之间,约20分钟至约1.25小时之间或约30分钟至约1小时之间)。
123.洗涤柱后,通过使洗脱缓冲液通过柱,从柱中洗脱分析物。洗脱缓冲液可以以约0.2ml/分钟至约25ml/分钟之间(例如,约0.1ml/分钟至约20ml/分钟之间,约0.5ml/分钟至约20ml/分钟之间,约0.2ml/分钟至约15ml/分钟之间,约0.5ml/分钟至约15ml/分钟之间,约0.5ml/分钟至约10ml/分钟之间,约0.5ml/分钟至约6.0ml/分钟之间,约1.0ml/分钟至约5.0ml/分钟之间,约0.5ml/分钟至约14ml/分钟之间,约1.0ml/分钟至约25.0ml/分钟之间,约1.0ml/分钟至约15.0ml/分钟之间)的流率通过柱。用于从柱中洗脱分析物的洗脱缓冲液的体积可以是例如约1x柱体积(cv)至约15x cv(例如,约1x cv至约14x cv之间,约1x cv至约13x cv,约1x cv至约12x cv,约1x cv至约11x cv,约2x cv至约11x cv,约3x cv至约11x cv,约4x cv至约11x cv,约5x cv至约11x cv,或约5x cv至约10x cv)。洗脱的总时间可以是例如约0.1分钟至约3小时之间(例如,约2分钟至约2.5小时之间、约2分钟至约2.0小时之间、约2分钟至约1.5小时之间、约2分钟至约1.5小时之间、约2分钟至约1.25小时之间、约2分钟至约1.25小时之间、约2分钟至约1小时之间、约2分钟与约40分钟之间、约10分钟与约40分钟之间、约20分钟与约40分钟之间、约0.1分钟至约10分钟之间)。
124.可以使用的洗脱缓冲液的非限制性例子取决于捕获机制和/或分析物。例如,洗脱缓冲液可以包含不同浓度的盐(例如,增加的盐浓度)、不同的ph(例如,增加或减少的盐浓度)或将与分析物竞争结合树脂的分子。这种洗脱缓冲液的例子如上所述。
125.分析物从色谱柱上洗脱后,可以使用再生缓冲液平衡色谱柱。再生缓冲液可以以例如约0.1ml/分钟至约25ml/分钟之间(例如,约0.2ml/分钟至约20ml/分钟之间,约0.5ml/分钟至约20ml/分钟之间,约0.2ml/分钟至约15ml/分钟之间,约0.5ml/分钟至约15ml/分钟之间,约0.5ml/分钟至约10ml/分钟之间,约0.5ml/分钟至约6.0ml/分钟之间,约1.0ml/分钟至约5.0ml/分钟之间,约0.5ml/分钟至约14ml/分钟之间,约1.0ml/分钟至约25.0ml/分钟之间,约5.0ml/分钟至约15.0ml/分钟之间,或约1.0ml/分钟至约15.0ml/分钟之间)的流率通过柱。
126.用于平衡柱的再生缓冲液的体积可以是例如约1x柱体积(cv)至约15x cv(例如,约1x cv至约14x cv之间,约1x cv至约13x cv,约1x cv至约12x cv,约1x cv至约11x cv,约2x cv至约11x cv,约3x cv至约11x cv,约2x cv至约5x cv,约4x cv至约11x cv,约5x cv至约11x cv,或约5x cv至约10x cv)。
127.在一些实施方案中,样品纯化装置108包括单个亲和色谱柱。在某些实施方案中,
样品纯化装置108包括多个亲和色谱柱。当使用多个柱时,柱可以不同(例如,包括不同的色谱树脂),或者可以相同。此外,多个柱可以用相同的溶剂和缓冲液、或者用不同的溶剂和/或缓冲液加载和/或洗脱。多柱样品纯化装置中的每个柱可以包括本文所述的任何一种或多种色谱树脂,并且可以用本文所述的任何一种或多种不同溶剂和缓冲液加载和/或洗脱。
128.如上所述,生物样品直接从第一流动控制装置106或通过样品纯化装置108被递送到第二流动控制装置110。第二流动控制装置110接收生物样品,并根据在控制线路124d上传输的来自控制单元122的控制信号,沿着多个流动路径中的一者引导生物样品。第二流动控制装置110通常可以以与上述第一流动控制装置106相同的方式实施。
129.通常,第二流动控制装置110将生物样品导向多个样品分析仪中的一个,如图1所示。通常,系统100可以包括2个或更多个样品分析仪(例如,3个或更多个、4个或更多个、5个或更多个、6个或更多个、7个或更多个、8个或更多个、10个或更多个、15个或更多个、甚至还要更多个)。每个样品分析仪与生物样品的分析物的一个产品品质属性的测量相关联。在图1中,以举例的方式示出了四个不同的样品分析仪114a-114d。然而,应当理解,系统100可以包括任意数量的样品分析仪,这取决于要测量的产品品质属性的数量。
130.在一些实施方案中,特定的样品分析仪不包括色谱柱。例如,在图1中,样品分析仪114a不包括色谱柱。生物样品可以从第二流动控制装置110直接递送到样品分析仪114a。更具体地,当要测量与样品分析器114a相关联的产品品质属性时,控制单元122向第二流动控制装置110发送控制信号,调节第二流动控制装置110的配置并使生物样品被递送到样品分析器114a。针对生物样品中的分析物,测量与样品分析仪114a相关的产品品质属性。
131.在某些实施方案中,特定的样品分析仪包括色谱柱。例如,在图1中,样品分析器114b-114d各自包括色谱柱。如上所述,为了将生物样品递送到这种样品分析仪,可以在控制单元122的控制下直接从第二流动控制装置110递送样品。
132.可选地,在一些实施方案中,系统100可选地包括柱管理器112,该柱管理器从第二流动控制装置110接收生物样品并将其引导到样品分析仪中。柱管理器在包括多个具有色谱柱的样品分析仪的系统中特别有用。如图1所示,柱管理器112可以通过控制线路124f联接到控制单元122。为了将生物样品导入与待测量的特定产品品质属性相关联的样品分析仪,控制单元122可以向柱管理器112发送控制信号,调节柱管理器112的配置以将生物样品导入样品分析仪的流动路径。
133.柱管理器112可以可选地通过第二泵118与一个或多个储器(为了说明的目的,在图1中示出为四个容器120a-120d)流体连通,第二泵也可以可选地通过控制线路124e联接到控制单元122。当生物样品被导入特定的样品分析仪时,控制单元122还向第二泵118发送控制信号,使第二泵118将合适的加载缓冲液、洗脱缓冲液或其他合适的溶剂或溶液的流导入特定的样品分析仪。尽管在图1中以举例的方式示出了四个储器,但是通常应当理解,第二泵118可以与2个或更多个储器流体连通(例如,3个或更多个、4个或更多个、5个或更多个、6个或更多个、8个或更多个、10个或更多个、15个或更多个、20个或更多个或者甚至还要更多个)。
134.第二泵通常可以以多种方式实施。例如,在一些实施方案中,合适的第二泵118是具有另外的溶剂选择阀改进的沃特世h类生物四元泵(waters h-class bio quaternary pump)(waters corp.,milford,ma)。
135.在生物样品被加载到选定的色谱样品分析仪的柱上之后,柱被展开并洗脱,洗脱物被分析以提供关于与生物样品的分析物的样品分析仪相关的产品品质属性的信息。
136.洗脱物的分析可以多种方式进行。在一些实施方案中,例如,系统100包括与样品分析仪的色谱柱的出口流体连通的检测器116。检测器116检测洗脱物中的分析物,并通过控制线路124g向控制单元122提供测量信息。控制单元122使用测量信息(其通常对应于色谱图和/或色谱信息,例如检测到的峰高、面积和时间)来确定生物样品的分析物的特定产品品质属性的值。
137.系统100通常可以使用多种检测器。在一些实施方案中,检测器116对应于光电二极管阵列检测器。系统100中使用的合适的二极管阵列检测器包括但不限于沃特世光电二极管阵列检测器(waters photodiode array detector)(waters corp.,milford,ma)。
138.也可以使用其他类型的检测器。例如,在一些实施方案中,检测器116对应于测量生物样品吸光度(例如,在电磁光谱的紫外、可见和红外区域中的至少一个中)的吸收光谱仪。在某些实施方案中,检测器116可以被实施为荧光检测器,并且包括用于将照明光引导到生物样品上的光源,以及用于测量来自样品的荧光发射的检测元件。在一些实施方案中,检测器116可以被实施为质谱检测器,其中生物样品被电离,并且离子的分布通过质量来解析,以确定生物样品的丰度信息。在某些实施方案中,检测器116可以被实施为多角度光散射检测器或折射角检测器。
139.在一些实施方案中,每个基于柱的样品分析仪可以与不同的专用检测器流体连通。在某些实施方案中,如图1所示,两个或更多基于柱的样品分析仪可以与公共检测器流体连通。也就是说,检测器116可以在两个或多个样品分析仪之间共享,因为系统100一次只分析生物样品的一部分。
140.在一些实施方案中,检测器116有效地用作样品分析仪。例如,在图1中,样品分析仪114a可以包括在第二流动控制装置110和检测器116之间延伸的流体导管。当样品被递送到样品分析器114a中时,样品简单地通过流体导管传播,并且随后被检测器116直接分析。
141.总体而言,在系统100中,每个样品分析仪专用于测量生物样品中分析物的特定产品品质属性。待确定的特定产品品质属性由控制单元122选择,控制单元122调节第二流动控制装置110的配置,以将一部分生物样品引导至样品分析仪中的一者。
142.系统100通常可以被配置成测量任意数量的产品品质属性,这取决于系统中存在的样品分析仪的数量。例如,在某些实施方案中,系统100可以测量生物样品中分析物的2个或更多个(例如,3个或更多个、4个或更多个、5个或更多个、6个或更多个、7个或更多个、8个或更多个、10个或更多个、12个或更多个、15个或更多个、20个或更多个、甚至还要更多个)产品品质属性。
143.产品品质属性
144.如上所述,系统100可用于测量生物样品中分析物的多种产品品质属性。根据系统100中存在的样品分析仪的性质,可以测量多种产品品质属性。
145.(a)浓度或效价
146.在一些实施方案中,系统100包括测量生物样品中分析物的浓度或效价的样品分析仪。分析物的浓度或效价可以通过上述任何不同类型的检测器直接在生物样品中测量。因此,例如,为了测量图1中生物样品的浓度或效价,生物样品的一部分可以直接从第二流
动控制装置110递送到检测器116,即样品分析仪可以有效地是在第二流动控制装置110和检测器116之间延伸的流体导管。
147.(b)电荷变化或异质性
148.在一些实施方案中,系统100包括测量生物样品中分析物的电荷变化或异质性的样品分析仪。电荷变化/异质性可以通过例如样品分析仪来确定,该分析仪包括用于对样品中的分析物进行阳离子交换色谱的阳离子交换柱。
149.术语“阳离子交换色谱”是指一种离子交换色谱,它使用带负电荷的离子交换树脂根据电荷差异分离分子。在一些实施方案中,阳离子交换色谱柱是强阳离子交换色谱柱,例如hitrap sp hp阳离子交换色谱柱、mono s阳离子交换色谱柱、thermo mabpac强阳离子交换色谱柱。
150.使用阳离子交换色谱柱(例如强阳离子交换色谱柱)的色谱循环,其中分析物在加载步骤中结合到色谱树脂上,可以包括以下步骤:用包含分析物的流体加载柱,洗涤柱以除去不需要的生物材料,洗脱结合到柱上的分析物,并使柱再平衡。在某些实施方案中,使用阳离子交换色谱柱的色谱循环,其中不需要的生物材料在加载步骤中结合到色谱树脂上,而分析物不结合,可以包括以下步骤:用包含目标蛋白质的流体加载柱,在流通中收集靶重组蛋白质,并使柱再平衡。
151.色谱循环中的任何单个步骤都可以包括单一缓冲液或多种缓冲液(例如,两种或更多种缓冲液),并且色谱循环中的任何单个步骤中的一个或多个可以包括缓冲液梯度。单个色谱循环的各种熟知方面的任何组合可以以任何组合形式用于这些方法中,例如,一种或多种不同色谱树脂、一种或多种流速、一种或多种缓冲液、柱的一种或多种空隙体积、柱的一种或多种床体积、每个步骤中使用的缓冲液的一种或多种体积、包含靶蛋白质的流体的一种或多种体积以及每个步骤中使用的一种或多种缓冲液的数量和类型。
152.在一些实施方案中,阳离子交换柱加载有约50mm至约120mm的柠檬酸磷酸盐(例如,约50mm、约60mm、约70mm、约80mm、约90mm、约100mm、约110mm、或约120mm)、约100mm至约150mm的nacl(例如,约100mm、约110mm、约120mm、约130mm、约140mm、或约150mm),酸碱度在约ph 3至约ph 4(例如,约ph 3.2、约ph 3.4、约ph 3.6、约ph 3.8、或约ph 4)。
153.在一些实施方案中,用约10mm至约100mm(例如,10mm至约90mm,约10mm至约80mm,约10mm至约70mm,约10mm至约60mm,约10mm至约50mm,约10mm至约40mm,约10mm至约30mm,约10mm至约20mm,约15mm至约100mm,约15mm至约90mm,约15mm至约80mm,约15mm至约70mm,约15mm至约60mm,约15mm至约50mm,约15mm至约40mm,约15mm至约30mm,约15mm至约20mm,约20mm至约100mm,约20mm至约90mm,约20mm至约80mm,约20mm至约70mm,约20mm至约60mm,约20mm至约50mm,约20mm至约40mm,约20mm至约30mm,约20mm至约25mm,约30mm至约100mm,约30mm至约90mm,约30mm至约80mm,约30mm至约70mm,约30mm至约60mm,约30mm至约50mm,约30mm至约40mm,约40mm至约100mm,约40mm至约90mm,约40mm至约80mm,约40mm至约70mm,约40mm至约60mm,约40mm至约50mm,约50mm至约100mm,约50mm至约90mm,约50mm至约80mm,约50mm至约70mm,约50mm至约60mm,约60mm至约100mm,约60mm至约90mm,约60mm至约80mm,约60mm至约70mm,约70mm至约100mm,约70mm至约90mm,约70mm至约80mm,约80mm至约100mm,约80mm至约90mm,或约90mm至约100mm)的乙酸钠,以约ph 2至约ph 4(例如,约ph 2至约ph 3.8,约ph 2至约3.75,约ph 2至约ph 3.6,约ph 2至约ph 3.8,约ph 2至约ph 3.6,约ph 2
8.4,约ph 8至约ph 8.2,约ph 9至约ph 10,约ph 9至约ph 9.8,约ph 9至约ph 9.6,约ph 9至约ph 9.4,约ph 9至约ph 9.2,或约ph 9.4至约ph 10)洗脱。
156.(c)聚集
157.在一些实施方案中,系统100包括测量生物样品中分析物聚集的样品分析仪。聚集的程度可以通过例如样品分析仪来确定,该分析仪包括用于对样品中的分析物进行尺寸排阻色谱分析的尺寸排阻柱。
158.术语“尺寸排阻色谱柱”或“分子筛色谱”是指其中分析物和其他组分通过尺寸和/或分子量来分离的色谱柱。在一些实施方案中,尺寸排阻色谱柱用于分离蛋白质聚集体,例如蛋白质多聚体(例如二聚体和三聚体)。尺寸排阻色谱柱的非限制性例子包括:sephadex g-10、sephadex g-25、sephadex g-50、sephadex g-75、sephadex g-100、sephadex g-150、sephadex g-200、sepharose 2b、sepharose 4b、sepharose 6b、bio-gel p-300和waters beh sec 200a。
159.在一些实施方案中,尺寸排阻柱加载有ph约7(例如,约ph 7.0至约ph 7.1、约ph 7.2、约ph 7.3、约ph 7.4、约ph 7.5、约ph 7.6、约ph 7.7、约ph 7.8或约ph 7.9)的1x磷酸盐缓冲盐水(pbs)。在一些实施方案中,尺寸排阻柱在约7.2的ph下加载1x pbs。
160.(d)完整性或纯度
161.在一些实施方案中,系统100包括测量生物样品中分析物的完整性或纯度的样品分析仪。完整性或纯度可以通过例如样品分析仪来确定,该分析仪包括用于对样品中的分析物进行反相色谱分析的反相柱。
162.术语“反相色谱”或“疏水色谱”是指包括疏水固定相的色谱类型。反相色谱柱的非限制性例子是本领域已知的,包括例如sepax opalshell-c18。疏水配体的非限制性例子包括脂肪族,例如c2、c4、c8、c10、c12、c16和c18,以及多苯基。
163.使用反相色谱柱的色谱循环可以包括以下步骤:用包含分析物的流体加载柱,洗涤柱以除去不需要的生物材料,洗脱结合到柱上的分析物,并使柱再平衡。
164.色谱循环中的任何单个步骤都可以包括单一缓冲液或多种缓冲液(例如,两种或更多种缓冲液),并且色谱循环中的任何单个步骤中的一个或多个可以包括缓冲液梯度。单个色谱循环的各种熟知方面的任何组合可以以任何组合形式用于这些方法中,例如,一种或多种不同色谱树脂、一种或多种流速、一种或多种缓冲液、柱的一种或多种空隙体积、柱的一种或多种床体积、每个步骤中使用的缓冲液的一种或多种体积、包含靶蛋白质的流体的一种或多种体积以及每个步骤中使用的一种或多种缓冲液的数量和类型。
165.在一些实施例中,反相柱用水中约0.01%至约1%(例如约0.01%至约0.8%,约0.01%至约0.6%,约0.01%至约0.5%,约0.01%至约0.4%,约0.01%至约0.2%,约0.01%至约0.1%,约0.02%至约1%,约0.02%至约0.8%,约0.02%至约0.6%,约0.02%至约0.5%,约0.02%至约0.4%,约0.02%至约0.2%,约0.02%至约0.1%,约0.05%至约1%,约0.05%至约0.8%,约0.05%至约0.6%,约0.05%至约0.5%,约0.05%至约0.4%,约0.05%至约0.2%,约0.05%至约0.1%,约0.06%至约1%,约0.06%至约0.8%,约0.06%至约0.6%,约0.06%至约0.5%,约0.06%至约0.4%,约0.06%至约0.2%,约0.06%至约0.1%,约0.08%至约1%,约0.08%至约0.8%,约0.08%至约0.6%,约0.08%至约0.5%,约0.08%至约0.4%,约0.08%至约0.2%,约0.08%至约1%,约0.1%至约1%,
约0.1%至约0.8%,约0.1%至约0.6%,约0.1%至约0.5%,约0.1%至约0.4%,约0.1%至约0.2%,约0.2%至约1%,约0.2%至约0.8%,约0.2%至约0.6%,约0.2%至约0.5%,约0.2%至约0.4%,约0.4%至约1%,约0.4%至约0.8%,约0.4%至约0.6%,约0.4%至约0.5%,约0.5%至约1%,约0.5%至约0.8%,约0.5%至约0.6%,约0.6%至约1%,约0.6%至约0.8%,或约0.8%至约1%)的三氟乙酸(tfa)洗脱。
166.在一些实施例中,反相柱用在约1:10至约10:120的异丙醇(ipa):乙腈(acn)(例如,约1:50、1:90、1:100、1:120、10:50、10:90或10:120)中约0.01%至约1%(例如约0.01%至约0.8%,约0.01%至约0.6%,约0.01%至约0.5%,约0.01%至约0.4%,约0.01%至约0.2%,约0.01%至约0.1%,约0.02%至约1%,约0.02%至约0.8%,约0.02%至约0.6%,约0.02%至约0.5%,约0.02%至约0.4%,约0.02%至约0.2%,约0.02%至约0.1%,约0.05%至约1%,约0.05%至约0.8%,约0.05%至约0.6%,约0.05%至约0.5%,约0.05%至约0.4%,约0.05%至约0.2%,约0.05%至约0.1%,约0.06%至约1%,约0.06%至约0.8%,约0.06%至约0.6%,约0.06%至约0.5%,约0.06%至约0.4%,约0.06%至约0.2%,约0.06%至约0.1%,约0.08%至约1%,约0.08%至约0.8%,约0.08%至约0.6%,约0.08%至约0.5%,约0.08%至约0.4%,约0.08%至约0.2%,约0.08%至约1%,约0.1%至约1%,约0.1%至约0.8%,约0.1%至约0.6%,约0.1%至约0.5%,约0.1%至约0.4%,约0.1%至约0.2%,约0.2%至约1%,约0.2%至约0.8%,约0.2%至约0.6%,约0.2%至约0.5%,约0.2%至约0.4%,约0.4%至约1%,约0.4%至约0.8%,约0.4%至约0.6%,约0.4%至约0.5%,约0.5%至约1%,约0.5%至约0.8%,约0.5%至约0.6%,约0.6%至约1%,约0.6%至约0.8%,或约0.8%至约1%)的三氟乙酸(tfa)洗脱。
167.在一些实施方案中,反相柱用在约10:90至约1:80的异丙醇(ipa):乙腈(acn)中约0.01%至约0.2%(例如,约0.01%、约0.02%、约0.04%、约0.05%、约0.06%、约0.08%、约0.1%、约0.12%、约0.14%、约0.15%、约0.16%、约0.18%或约0.2%)的三氟乙酸(tfa)洗脱。
168.在一些实施方案中,用约10mm至约100mm(例如,10mm至约90mm,约10mm至约80mm,约10mm至约70mm,约10mm至约60mm,约10mm至约50mm,约10mm至约40mm,约10mm至约30mm,约10mm至约20mm,约15mm至约100mm,约15mm至约90mm,约15mm至约80mm,约15mm至约70mm,约15mm至约60mm,约15mm至约50mm,约15mm至约40mm,约15mm至约30mm,约15mm至约20mm,约20mm至约100mm,约20mm至约90mm,约20mm至约80mm,约20mm至约70mm,约20mm至约60mm,约20mm至约50mm,约20mm至约40mm,约20mm至约30mm,约20mm至约25mm,约30mm至约100mm,约30mm至约90mm,约30mm至约80mm,约30mm至约70mm,约30mm至约60mm,约30mm至约50mm,约30mm至约40mm,约40mm至约100mm,约40mm至约90mm,约40mm至约80mm,约40mm至约70mm,约40mm至约60mm,约40mm至约50mm,约50mm至约100mm,约50mm至约90mm,约50mm至约80mm,约50mm至约70mm,约50mm至约60mm,约60mm至约100mm,约60mm至约90mm,约60mm至约80mm,约60mm至约70mm,约70mm至约100mm,约70mm至约90mm,约70mm至约80mm,约80mm至约100mm,约80mm至约90mm,或约90mm至约100mm)的乙酸钠,以约ph 2至约ph 4(例如,约ph 2至约ph 3.8,约ph 2至约3.75,约ph 2至约ph 3.6,约ph 2至约ph 3.8,约ph 2至约ph 3.6,约ph 2至约ph 3.4,约ph 2至约ph 3.2,约ph 2至约ph 3.0,约ph 2至约ph 2.8,约ph 2至约ph 2.6,约ph 2至约ph 2.4,约ph 2至约ph 2.2,约ph 3至约ph 4,约ph 3至约ph 3.8,约ph 3
至约ph 3.75,约ph 3至约ph 3.6,约ph 3至约ph 3.4,或约ph 3至约ph 3.2)洗脱反相柱。
169.(e)抗体还原
170.在一些实施方案中,系统100包括样品分析仪,其测量生物样品中抗体分析物的还原。在生物制造生产平台中,抗体产物的还原性降解是一个问题,并且本文所述的系统可用于测量抗体的还原,以对制造工艺参数进行反馈调节。抗体还原可以通过例如样品分析仪来确定,该分析仪包括用于对样品中的分析物进行反相色谱分析的反相柱。本文讨论的任何反相柱树脂、缓冲液、ph值和其他操作条件都可以与样品分析仪中的反相色谱结合使用。
171.在一些实施方案中,亲水性相互作用色谱柱可用于测量样品分析物的产品品质属性。在某些实施方案中,疏水相互作用色谱柱可用于测量产品品质属性,例如氧化分析。在一些实施方案中,凝集素柱可用于获得与糖基化信息相关的产品品质属性。
172.在某些实施方案中,酶色谱柱可用于进行肽图谱绘制,以测量产品品质属性。反相色谱分离可用于分离肽分析物进行分析。
173.使用系统100的产品品质属性的分析通常可以接近实时地完成,以提供及时的控制反馈,用于多种生物制造工艺条件和参数的调节。在一些实施方案中,例如,从在合适的样品分析仪上初始引入样品的一部分到确定属性值,可以在10分钟或更短时间内(例如,9分钟或更短时间、8分钟或更短时间、7分钟或更短时间、6分钟或更短时间、5分钟或更短时间、4分钟或更短时间、3分钟或更短时间、2分钟或更短时间、1分钟或更短时间)确定生物样品的分析物的浓度或效价属性。
174.在某些实施方案中,从在合适的样品分析仪上初始引入样品的一部分到确定属性值,可以在70分钟或更短时间内(例如,65分钟或更短时间、60分钟或更短时间、55分钟或更短时间、50分钟或更短时间、45分钟或更短时间、40分钟或更短时间、35分钟或更短时间、30分钟或更短时间)确定生物样品的分析物的电荷变化或异质性属性。
175.在一些实施方案中,从在合适的样品分析仪上初始引入样品的一部分到确定属性值,可以在30分钟或更短时间内(例如,28分钟或更短时间、26分钟或更短时间、24分钟或更短时间、22分钟或更短时间、20分钟或更短时间、18分钟或更短时间、16分钟或更短时间、14分钟或更短时间、12分钟或更短时间、10分钟或更短时间)确定生物样品的分析物的聚集属性。
176.在某些实施方案中,从在合适的样品分析仪上初始引入样品的一部分到确定属性值,可以在30分钟或更短时间内(例如,28分钟或更短时间、26分钟或更短时间、24分钟或更短时间、22分钟或更短时间、20分钟或更短时间、18分钟或更短时间、16分钟或更短时间、14分钟或更短时间、12分钟或更短时间、10分钟或更短时间)确定生物样品的分析物的完整性或纯度属性。
177.对于一个分析周期,其中确定了分析物的上述四个产品品质属性中的每一个的值,从最初将生物样品的第一部分引入第一样品分析仪到确定第四属性的值,经过的时间间隔可以是150分钟或更少(例如,130分钟或更少、110分钟或更少、105分钟或更少、100分钟或更少、95分钟或更少、90分钟或更少、80分钟或更少、70分钟或更少、60分钟或更少)。
178.图3是流程图300,其包括用于确定生物样品的分析物的产品品质属性的一系列示例性步骤。在第一步骤302中,在样品管理器中接收样品。如上所述,样品可以离线接收在小瓶、孔板或其他容器中,从其中提取并注入第一流动控制装置106。样品也可以从在线采样
装置接收,并保持在流体回路或通道中,生物样品的一部分从该流体回路或通道注射到第一流动控制装置106中。
179.接下来,在步骤304中,将一部分生物样品注射到第一流动控制装置106中。在步骤306中,可以任选地纯化所注射的样品部分。无论是否纯化,该部分生物样品都被递送到第二流动控制装置110,随后在步骤308中从第二流动控制装置递送到与感兴趣的产品品质属性相关联的样品分析仪。
180.在步骤310中,在样品分析仪中,分析生物样品的该部分,以确定样品中分析物的相关产品品质属性值。在确定了产品品质属性值之后,如果还没有确定样品分析周期的所有产品品质属性值(见步骤312),则控制返回到步骤304,并且将生物样品的另一部分注射到第一流动控制装置106中。
181.或者,如果在步骤312中已经确定了所有的产品品质属性值,则属性的值可以可选地由控制单元122传输到主控制器,用于调节一个或多个生物制造工艺参数。分析循环然后在步骤316处结束。
182.将生物样品从第一流动控制装置106直接递送到第二流动控制装置110或通过样品纯化装置108递送到第二流动控制装置110的方法取决于流动控制装置的性质等。图4a-4c示出了当第一和第二流动控制装置被实施为多路阀时,在第一和第二流动控制装置之间递送生物样品的例子。
183.图4a是第一流动控制装置106的示意图,其配置被调节为处于第一位置,其中端口1和2连接,端口3和4连接,并且端口5和6连接。生物样品从样品管理器102注入端口2。端口2连接到端口1,端口1又连接到第二流动控制装置110和柱管理器112。结果,样品被直接递送到第二流动控制装置110,而不经过样品纯化装置108。
184.图4b和图4c是示出第一和第二流动控制装置106和110的示意图,所述第一和第二流动控制装置被配置成将生物样品递送到样品纯化装置108。在图4b中,第一流动控制装置的配置使得该装置处于第二位置,端口2和3连接,端口4和5连接,端口1和6连接。第二流动控制装置配置在第一位置,端口1和2连接,端口3和4连接,端口5和6连接。此外,样品纯化装置108连接在端口1和4之间,端口3连接到废弃物容器,端口2连接到第一流动控制装置的端口3。图4b所示的配置用于将生物样品加载到样品纯化装置108的柱上,加载缓冲液通过第一流动控制装置的端口1引入。
185.一旦生物样品被加载到样品纯化装置柱上,如图4c所示调节第一和第二流动控制装置的配置,以从样品纯化装置柱洗脱生物样品。在该配置中,第二流动控制装置被调节为不同的配置,其中端口2和3被连接,端口4和5被连接,并且端口1和6被连接。此外,第二流动控制装置110的端口6连接到第一流动控制装置106的端口1。为了从样品纯化装置柱中洗脱分析物,洗脱缓冲液被递送到第二流动控制装置的端口5,洗脱的分析物被递送到第二流动控制装置,然后进入与第二流动控制装置流体连通的样品分析仪中的一者。
186.根据本文所述的系统和方法分析生物样品以确定产品品质属性的值在各种方面都是有利的。例如,所描述的系统可以在整个工艺开发(例如,从细胞系开发到药物产品开发)中作为许多不同产品品质属性的单一收集平台,保持收集方法中的数据连续性和一致性。
187.此外,产品品质属性的测量可以用于光谱模型验证和正在进行的模型验证。例如,
使用周期性测量的产品品质属性,可以通过验证使用在线ftir和/或拉曼测量的化学计量方法的预测准确性来维护光谱模型。
188.本文所述系统的自动化特性可用于消除繁琐、重复的分析步骤,否则这些步骤将手动执行,从而节省时间并降低操作员错误影响测量属性的值的可能性。同样,整合样品纯化可以在线进行,大大减少了获得更纯生物样品所需的时间量。
189.本文所述的系统和方法可用于在制造系统中靠近生物反应器的位置直接分析收获的培养基。在一些实施方案中,关于所测量的产品品质属性的信息的反馈(例如,通过控制单元122)可以提供对制造工艺参数的更直接和及时的控制,该控制可以被调节以增加产品产量、降低废品率,并且以其他方式提高生物制造工艺的效率。
190.除了直接评估生物反应器管理的产品品质属性的应用之外,属性值还可用于细胞系工艺开发。例如,本文所述的方法可用于确定单克隆抗体治疗剂的产品品质属性,以分析和比较不同的克隆。
191.生物制造系统的集成与调节
192.本文公开的系统可与生物制造系统整合,以便为各种生物产品的合成和纯化工艺中的各种组分与步骤提供反馈控制。
193.用于制造治疗性蛋白质药物和其他物质的集成与全连续工艺可包括,例如,提供含有基本上无细胞的重组治疗性蛋白质的液体培养基,然后将该液体培养基进料到第一多柱色谱系统(mccs1)中。下一步骤涉及使用mccs1在该液体培养基中捕获重组治疗性蛋白质,然后将含有重组治疗性蛋白质的mccs1洗脱物连续进料到第二多柱色谱系统(mccs2)中,并使用mccs2对该蛋白质进行纯化和精处理。来自mccs2的所得洗脱物被认为是治疗性蛋白质药品。该工艺是整合的,并且可以从液体培养基连续运行到来自mccs2的洗脱物(即治疗性蛋白质药品)。
194.生物制造系统通常用于进行上述工艺。例如,此类系统可包括mccs1(其包括入口)和mccs2(其包括出口)。在这些系统中,第一与第二mccs彼此流体连通。这些系统还被配置为使得流体可被传送进入入口、通过第一mccs和第二mccs,并通过出口离开该制造系统。
195.此类系统可以从液体培养基中提供连续的、具有时效性的治疗性药品的生产。例如,在将含有治疗性蛋白质的流体(例如,液体培养基)进料到第一mccs与从第二mccs的出口洗脱治疗性蛋白质药品(含有治疗性蛋白质)之间的经过时间可以是例如约4小时与约48小时之间。
196.图8是示出生物制造系统的例子的示意图。系统1包括第一mccs,即四柱周期逆流色谱系统(pccs)2,其中四柱pccs 2的四个柱中的三个(柱3、4和5)进行从含有重组治疗性蛋白质的流体(例如,基本无哺乳动物细胞的液体培养基)中捕获重组治疗性蛋白质的单元操作,并且pccs 2的柱中的一个(柱6)进行灭活洗脱物中存在的病毒的单元操作,该洗脱物来自含有重组治疗性蛋白质的pccs 2的柱3、4和5。柱3、4和5可含有利用蛋白a结合捕获机制的树脂。柱6能够将ph为约3.75的流体保持约1小时。pccs 1还具有入口7。入口7可以是,例如,接受流体进入pccs 1的孔口。
197.系统1还包括第二mccs(其为pccs 8),所述第二mccs包括三个色谱柱9、10和11以及一个色谱膜12。pccs 8中的柱9、10和11可含有阳离子交换树脂。pccs 8中的色谱膜12可以包含阳离子交换树脂。pccs 8还具有设置在pccs 8中的柱9、10和11与pccs 8中的色谱膜
12之间的流体导管13。pccs 8还具有与流体导管13处于流体连通的在线缓冲液调节储器14,并且配置为使得容纳于在线缓冲调节储器14内的缓冲液被引入存在于流体导管13中的流体中。pccs 8还包括出口15。出口15可以是例如允许流体从pccs 8排出的孔口。
198.系统1可进一步包括设置在pccs 2与pccs 8之间的流体导管16。系统1还可包括与流体导管16处于流体连通的在线缓冲调节储器17,其被配置为使得容纳于在线缓冲调节储器17内的缓冲液可被引入存在于流体导管16中的流体中。系统1还可包括设置在流体导管16中的过滤器18,以过滤存在于流体导管16中的流体。系统1还可包括断流槽19,所述断流槽被设置在流体导管16中并且被配置为容纳流体导管16中的任何不能容易地进料到pccs 8中的流体。
199.系统1可进一步包括与入口7处于流体连通的泵系统20。泵系统20可包括用于将流体推入入口7的泵21。系统1还可包括设置在泵21与入口7之间的流体导管22。系统1还可包括设置在流体导管22中的过滤器23,以过滤存在于流体导管22中的流体(例如,液体培养基)。系统1还可包括设置在流体导管22中的断流槽24,其被配置为使得断流槽24与流体导管22处于流体连通并且能够存储存在于流体导管22中的不能进入入口7的任何流体。
200.系统1还可包括生物反应器25和设置在生物反应器25与泵21之间的流体导管26。过滤系统27可以设置在流体导管26中,以对存在于流体导管26中的液体培养基进行过滤(例如,从中除去细胞)。
201.第一mccs(pccs 2)包括入口,通过该入口,流体(例如,基本上无细胞的液体培养基)可被传送进入第一mccs。该入口可以是本领域已知的用于此类目的的任何结构。它可包括,例如,允许插入流体导管的螺纹、肋材或密封件,这样使得在将流体导管插到入口中之后,流体将通过入口进入第一mccs而没有大量流体从入口渗出。
202.第一mccs包括至少两个色谱柱、至少两个色谱膜,或者至少一个色谱柱和至少一个色谱膜,以及入口。例如,第一mccs可包括总共四个色谱柱,或者三个色谱柱与一个色谱膜,或本文所述的任何其他的示例性mccs,或者具有本文所述的mccs的任何示例性特征(以任意组合)中的一个或多个。
203.存在于第一mccs中的一个或多个色谱柱和/或一个或多个色谱膜可含有各种树脂中的一种或多种。例如,包含于在第一mccs中存在的一个或多个色谱柱和/或一个或多个色谱膜中的一个或多个中的树脂可以是利用捕获机制(例如,蛋白a结合捕获机制、蛋白g结合捕获机制、抗体或抗体片段结合捕获机制、底物结合捕获机制、辅因子结合捕获机制、适配体结合捕获机制、和/或标签结合捕获机制)的树脂。包含于第一mccs的一个或多个色谱柱和/或一个或多个色谱膜中的一个或多个中的树脂可以是阳离子交换树脂、阴离子交换树脂、分子筛树脂或疏水性相互作用树脂、或其任意组合。可用于纯化重组治疗性蛋白质的树脂的其他例子是本领域已知的,并且可包含于在第一mccs中存在的一个或多个色谱柱和/或一个或多个色谱膜中的一个或多个中。存在于第一mccs中的一个或多个色谱柱和/或色谱膜可含有相同的和/或不同的树脂(例如,本文所述的或本领域已知的用于重组蛋白质纯化的任何树脂)。
204.存在于第一mccs中的两个或更多个色谱柱和/或色谱树脂可以进行一种或多种单元操作(例如,捕获重组治疗性蛋白质、纯化重组治疗性蛋白质、精处理重组治疗性蛋白质、灭活病毒、调节含有重组治疗性蛋白质的流体的离子浓度和/或ph、或过滤含有重组治疗性
蛋白质的流体)。在非限制性例子中,第一mccs可进行从流体(例如液体培养基)中捕获重组治疗性蛋白质并且灭活存在于含有重组治疗性蛋白质的流体中的病毒的单元操作。第一mccs可进行本文描述的或本领域已知的两个或更多个单元操作的任意组合。
205.存在于第一mccs中的一个或多个色谱柱和/或一个或多个色谱膜可以通过切换机制(例如,柱切换机制)相对于彼此连接或移动。第一mccs还可包括一个或多个(例如,两个、三个、四个或五个)泵(例如,自动化的,例如自动蠕动泵)。柱切换事件可通过检测经过第一mccs的流体(例如,进入和/或来自第一mccs中的一个或多个色谱柱和/或色谱膜中的一个或多个的输入和/或洗脱物)中的重组治疗性蛋白质的水平、特定的液体(例如缓冲液)体积或特定的经过时间来触发。柱切换通常是指允许mccs中至少两个不同的色谱柱和/或色谱膜(例如,mccs(例如,第一或第二mccs)中存在的两个或更多个不同的色谱柱和/或色谱膜)在工艺的至少部分期间基本上同时地通过不同步骤(例如,平衡、加载、洗脱或洗涤)的机制。
206.作为第一mccs的pccs 2可包括四个色谱柱,其中前三个柱进行从流体(例如液体培养基)中捕获重组治疗性蛋白质的单元操作,并且pccs的第四个柱进行在含有重组治疗性蛋白质的流体中灭活病毒的单元操作。作为第一mccs的pccs可以使用柱切换机制。pcc系统可采用改进的系统(ge healthcare,piscataway,nj),所述系统能够运行多达例如四、五、六、七或八个柱或更多柱。
207.柱切换事件可通过检测流体中的特定蛋白质或其他物质的浓度来触发,所述流体从pccs 2或pccs 8的一个柱中洗脱出、流动通过在mccs中的过滤器、包含在mccs的断流槽中、或流动通过mccs中的导管(例如,在mccs 1与mccs 2之间)。本文公开的测量系统可用于测量此类蛋白质的浓度,并将该浓度信息传递至系统1中的控制器,该控制器在系统1中启动诸如柱切换、过滤和流体传输等事件。
208.第一mccs可配备:一个或多个(例如,两个、三个、四个、五个、六个、七个、八个、九个或十个)被配置为获得工艺流体的红外光谱信息的测量系统(例如,系统100),一个或多个(例如,两个、三个、四个、五个、六个、七个、八个、九个或十个)阀,一个或多个(例如,两个、三个、四个、五个、六个、七个、八个、九个、或十个)ph计,和/或一个或多个(例如,两个、三个、四个、五个、六个、七个、八个、九个或十个)电导率计。第一mccs还可配备执行操作系统的控制器,该操作系统利用软件(例如,基于unicorn的软件(ge healthcare,piscataway,nj)或实施类似功能的其他软件)来确定何时应发生柱切换(例如,基于来自红外光谱测量的浓度信息、液体体积或经过时间)并影响(触发)柱切换事件。测量系统可任选地放置在第一mccs中的一个或多个色谱柱和/或一个或多个色谱膜中的一个或多个(例如,两个、三个、四个、五个、六个、七个、八个、九个或十个)的入口处,和/或在第一mccs中的一个或多个色谱柱和/或一个或多个色谱膜中的一个或多个的出口处。
209.第一mccs可进一步包括一个或多个(例如,两个、三个、四个、五个、六个、七个、八个、九个、十个、十一个、十二个、十三个、十四个、十五个、十六个、十七个、十八个、十九个、二十个、二十一个、二十二个、二十三个或二十四个)在线缓冲液调节储器和/或缓冲液储器。在其他例子中,第一mccs可包括一个或多个(例如,两个、三个、四个、五个或六个)断流槽,所述一个或多个断流槽可容纳不能容易地进入第一mccs中的一个或多个色谱柱和/或色谱膜的流体。本文所述的系统可在第一和/或第二mccs中含有一个或多个断流槽(例如,
本文所述的断流槽)。本文所述的系统的其他例子不包括在第一mccs或第二mccs中的断流槽,或者在整个系统中不包括断流槽。所述系统的其他例子包括在整个系统中最多一个、两个、三个、四个或五个断流槽。
210.在一些实施方案中,第一mccs可以包括病毒灭活装置。例如,参考图8,在某些实施方案中,第一mccs包括病毒灭活装置6(即,代替上述柱6)。病毒灭活装置6被配置为灭活生物制造工艺中使用的病毒和病毒载体。在一些实施方案中,例如,病毒灭活装置6包括混合器皿。可替代地,在某些实施方案中,例如,装置6包括活塞流灭活系统。这些病毒灭活装置的各个例子有助于从第一mccs中的工艺流体中消除活性病毒和病毒载体。
211.第二mccs包括至少两个色谱柱,至少两个色谱膜,或者至少一个色谱柱与至少一个色谱膜,以及出口。例如,第二mccs可包括总共四个色谱柱,三个色谱柱与一个色谱膜,或本文所述的任何其他的示例性mccs,或者可以具有本文所述的mccs的任何示例性特征(以任意组合)中的一个或多个。存在于第二mccs中的一个或多个色谱柱和/或一个或多个色谱膜可具有以下的一种或多种:本文所述的任何形状、尺寸、体积(床体积)和/或单元操作。包含于在第二mccs中存在的一个或多个色谱柱和/或一个或多个色谱膜中的一个或多个中的树脂可以是利用捕获机制(例如,蛋白a结合捕获机制、蛋白g结合捕获机制、抗体或抗体片段结合捕获机制、底物结合捕获机制、辅因子结合捕获机制、标签结合捕获机制、和/或适配体结合捕获机制)的树脂。有用的树脂包括,例如,阳离子交换树脂、阴离子交换树脂、分子筛树脂、和疏水性相互作用树脂。存在于第二mccs中的一个或多个色谱柱和/或色谱膜可含有相同的和/或不同的树脂(例如,本文所述的或本领域已知的用于重组蛋白质纯化的任何树脂)。
212.存在于第二mccs中的一个或多个色谱柱和/或一个或多个色谱膜可进行一个或多个单元操作(例如,本文所述的任何单元操作或本文所述的单元操作的任何组合)。在非限制性例子中,第二mccs可进行从流体中纯化重组治疗性蛋白质并且精处理存在于含有重组治疗性蛋白质的流体中的重组治疗性蛋白质的单元操作。在其他非限制性例子中,第二mccs可以进行纯化存在于流体中的重组治疗性蛋白质、精处理存在于流体中的重组治疗性蛋白质、以及过滤含有重组治疗性蛋白质的流体的单元操作。在另一个例子中,第二mccs可以进行纯化存在于流体中的重组治疗性蛋白质、精处理存在于流体中的重组治疗性蛋白质、过滤含有重组治疗性蛋白质的流体、以及调节含有重组治疗性蛋白质的流体的离子浓度和/或ph的单元操作。第二mccs可进行本文描述的或本领域已知的两个或更多个单元操作的任何组合。
213.第二mccs还可包括一个或多个(例如,两个、三个、四个或五个)泵(例如,自动化的,例如自动蠕动泵)。
214.存在于第二mccs中的一个或多个色谱柱和/或一个或多个色谱膜可以通过切换机制(例如,柱切换机制)相对于彼此连接或移动。柱切换事件可以通过检测重组治疗性蛋白质或其他物质的水平(经红外光谱测量并使用如上所讨论的化学计量模型对其进行分析以确定经过第二mccs的流体(例如,进入和/或来自第二mccs中的一个或多个色谱柱和/或色谱膜中的一个或多个的输入和/或洗脱物)中的重组治疗性蛋白质的水平)、特定的液体(例如缓冲液)体积或特定的经过时间来触发。
215.形成第二mccs的pccs 8可含有三个柱(进行从流体中纯化重组治疗性蛋白质的单
元操作)和一个色谱膜(进行精处理在流体中存在的重组治疗性蛋白质的单元操作)。例如,进行从流体中纯化重组治疗性蛋白质的单元操作的三个柱可含有例如阳离子交换树脂,并且进行精处理的单元操作的色谱膜可含有阳离子交换树脂。作为第二mccs的pccs可以使用柱切换机制。例如,pccs可利用能够运行多至例如四个、五个、六个、七个或八个柱、或者更多柱的改良的系统(ge healthcare,piscataway,nj)。
216.与第一mccs类似,第二mccs也可配备:一个或多个(例如,两个、三个、四个、五个、六个、七个、八个、九个或十个)红外光谱测量系统,一个或多个(例如,两个、三个、四个、五个、六个、七个、八个、九个或十个)阀,一个或多个(例如,两个、三个、四个、五个、六个、七个、八个、九个、或十个)ph计,和/或一个或多个(例如,两个、三个、四个、五个、六个、七个、八个、九个或十个)电导率计。一个或多个测量系统将测量的流体中的蛋白质或其他物质的浓度信息传输到控制器,该控制器使用浓度信息来确定是否触发柱切换事件。第二mccs可配备由接收浓度信息的控制器执行的操作系统,所述操作系统利用软件(例如,基于unicorn的软件,ge healthcare,piscataway,nj)来确定何时应发生柱切换事件(例如,基于红外光谱测量、液体体积或经过时间)并启动柱切换事件。在第二mccs包括一个或多个红外光谱测量系统的例子中,测量系统可任选地放置在第二mccs中的一个或多个色谱柱和/或一个或多个色谱膜中的一个或多个(例如,两个、三个、四个、五个、六个、七个、八个、九个或十个)的入口处,和/或在第二mccs中的一个或多个色谱柱和/或一个或多个色谱膜中的一个或多个的出口处。
217.第二mccs可进一步包括一个或多个(例如,两个、三个、四个、五个、六个、七个、八个、九个、十个、十一个、十二个、十三个、十四个、十五个、十六个、十七个、十八个、十九个、二十个、二十一个、二十二个、二十三个或二十四个)在线缓冲液调节储器和/或缓冲液储器。在其他例子中,第二mccs可包括一个或多个(例如,两个、三个、四个、五个或六个)断流槽(例如,本文所述的任何断流槽),所述一个或多个断流槽可容纳不能容易地进入第二mccs中的一个或多个色谱柱和/或色谱膜的流体。
218.第二mccs包括出口,治疗性蛋白质药品可以通过所述出口离开系统。出口可包括,例如,允许插入流体导管的螺纹、肋材或密封件,或设计用于容纳或储存治疗性蛋白质药品的小瓶。出口可含有可用于将无菌小瓶或其他此类储存容器密封在出口上的表面,以允许重组蛋白质药品直接流入无菌小瓶或储存容器中。
219.本文所述的任何流体导管可以是例如由例如聚乙烯、聚碳酸酯或塑料制成的管。设置在第一mccs与第二mccs之间的流体导管可以进一步包括以下任何组合中的一个或多个:一个或多个在线缓冲液调节储器,其与流体导管处于流体连通并且被定位为使得储存于一个或多个在线缓冲液调节储器中的缓冲液被添加到存在于流体导管中的流体中;断流槽(例如,本文所述的任何一个或多个断流槽),其与流体导管处于流体连通并且被定位为使得其可以容纳存在于流体导管中的不能容易地进料到第二mccs的任何多余流体;以及一个或多个过滤器,其被设置于流体导管中使得它们能够对存在于流体导管中的流体进行过滤(例如,除去细菌)。任何在线缓冲液调节储器可含有例如体积在约0.5l与50l之间的缓冲液(例如,在为或低于50℃、37℃、25℃、15℃或10℃的温度下)。
220.本文所述的系统可任选地包括设置在第二mccs中的最终色谱柱或色谱膜与出口之间的流体导管。本文所述的系统可以进一步包括一个或多个过滤器,所述一个或多个过
滤器与设置在第二mccs中的最终色谱柱或色谱膜与出口之间的流体导管处于流体连接,使得过滤器可以从存在于流体导管中的流体除去例如沉淀材料、微粒物质或者细菌,所述流体导管设置在第二mccs中的最终色谱柱或色谱膜与出口之间。
221.本文提供的系统的一些例子还包括与第一mccs的入口处于流体连接的生物反应器。本文所述或本领域中已知的任何示例性生物反应器都可以用于本发明的系统中。
222.本文提供的系统的一些例子还包括泵系统。泵系统可以包括以下中的一个或多个:一个或多个(例如,两个、三个、四个、五个、六个、七个、八个、九个或十个)泵(例如,本文所述或本领域中已知的任何泵),一个或多个(例如,两个、三个、四个或五个)过滤器(例如,本文所述或本领域中已知的任何过滤器),一个或多个(例如,两个、三个、四个、五个、六个、七个、八个、九个或十个)uv检测器,以及一个或多个(例如,两个、三个、四个或五个)断流罐(例如,本文所述的任何断流罐)。本文提供的系统的一些例子进一步包括设置在泵与第一mccs的入口之间的流体导管(例如,本文所述的或本领域已知的任何示例性流体导管)。在一些例子中,此特定流体导管可包括一个或多个(例如,两个、三个或四个)泵(例如,本文所述的或本领域已知的任何泵)和/或一个或多个(例如,两个、三个或四个)断流槽(例如,本文所述的任何示例性断流槽),其中这些泵和/或断流槽与存在于流体导管中的流体处于流体连接。
223.本文所述的系统的一些例子进一步包括连接到在泵与入口之间的流体导管的另一个流体导管,其中另一个流体导管的一端流体地连接到生物反应器,并且另一端流体地连接到在泵与入口之间的流体导管。该另外的流体导管可包括过滤器,该过滤器能够从取自生物反应器(例如,atf细胞保留系统)的液体培养基中除去细胞。
224.前述生物制造系统允许连续生产治疗性蛋白质药品。例如,本文提供的系统允许重组治疗性蛋白质(自起始材料,例如起始液体培养基)的产率百分比大于约70%、大于约80%、大于约82%、大于约84%、大于约86%、大于约88%、大于约90%、大于约92%、大于约94%、大于约96%、或大于约98%。本文所述的系统还可导致重组治疗性蛋白质(自起始材料,例如起始液体培养基)的产率百分比为约80%至约90%之间、约82%至约90%之间、约84%至约90%之间、约84%至约88%之间、约84%至约94%之间、约82%至约92%之间、或约85%至约95%之间。
225.本文描述的系统还可导致如下治疗性蛋白质药品的产生,其含有的重组治疗性蛋白质的浓度大于约1.0mg/ml,例如,大于约15mg/ml、大于约20mg/ml、大于约25mg/ml、大于约30mg/ml、大于约35mg/ml、大于约40mg/ml、大于约45mg/ml、大于约50mg/ml、大于约55mg/ml、大于约60mg/ml、大于约65mg/ml、大于约70mg/ml、大于约75mg/ml、大于约80mg/ml、大于约85mg/ml、大于约90mg/ml、大于约100mg/ml、大于约125mg/ml、或大于约150mg/ml。
226.如上所述,在一些实施方案中,第一和/或第二mccs可以是周期逆流色谱系统(pccs)。pccs可以例如包括两个或更多个色谱柱(例如,三个柱或四个柱),将其切换以允许从两个或更多个色谱柱连续洗脱重组治疗性蛋白质。pccs可包括两个或更多个色谱柱,两个或更多个色谱膜,或者至少一个色谱柱与至少一个色谱膜。柱操作通常由加载、洗涤、洗脱以及再生步骤组成。在pccs中,将多个柱用于以循环方式离散地且连续地运行相同的步骤。由于柱是串联操作的,因此经过一个柱的流和来自所述柱的洗液由另一个柱捕获。pccs的该独特特征允许树脂的加载接近其静态结合能力而不是动态结合能力,这在分批模式色
谱期间是典型的。
227.用于含有三个柱的pccs中的三柱切换技术的例子示出于图9。一个循环被定义为三个完整的柱操作,其产生来自柱切换技术中使用的三个柱中的各个的洗脱池。一旦完成循环中的所有步骤,循环重新开始。由于连续循环与洗脱,进入pccs的流体被连续地处理,而重组治疗性蛋白质从各个柱的洗脱是离散的和周期性的。
228.为了从pccs循环中的一个步骤前进到另一个步骤,正如图9中所示出的示例性循环,采用柱切换策略。柱切换方法在图9所示出的示例性pccs系统的三柱中采用每柱两个自动切换操作,其中第一个与初始产品穿透有关,而第二个与柱饱和相符。确定何时应发生柱切换操作是基于有关在来自pccs的各个色谱柱的洗脱物中重组治疗性蛋白质的浓度的信息。
229.如上所述,合适的样品分析仪可用于测定来自pccs柱的洗脱物中重组治疗性蛋白质的浓度。浓度信息,其作为生物制造系统的反馈控制而发挥作用,被控制单元122传输至mccs控制器,其在确定切换被授权之后启动柱切换。
230.例如,在柱加载期间,该pcc控制系统可以使用上面讨论的红外光谱测量系统确定从柱洗脱的治疗性蛋白质物质的基线浓度(其通常为零浓度)。在活性洗脱期间,当蛋白质物质穿透时,测量的蛋白质浓度增加(例如,高于基线浓度)。系统继续监测渐增的蛋白质浓度,并且当浓度达到预定的阈值时,来自柱1的流被引导到柱2上而不是到废弃物。名义上,这发生在时间t1。
231.随着继续向柱1内进料,柱1最终几乎被蛋白质产品饱和。此时,测量的洗脱物中蛋白质浓度已达到另一个预定值,其发生在时间t2。此时,mccs控制器将入口进料切换到柱2。
232.无论进料产品浓度和容量如何,上述柱切换策略都允许对柱进行均匀加载。可以基于检测到的在来自各个柱的洗脱物中的重组蛋白质水平实施柱的类似切换。柱切换还可以基于通过第一或第二mccs中的一个或多个色谱柱和/或色谱膜的流体(例如,缓冲液)的经过时间或量。
233.本文公开的测量系统除了提供反馈信息以控制柱切换事件之外,还可以提供用于调节各种其他生物制造步骤和操作参数的反馈信息。此类调节的一个例子是在生物制造工艺的各个阶段控制性调节缓冲液浓度。
234.通常,在本文所述的任何工艺中使用两个或更多个mccs期间,可采用一个或多个(例如,三个、四个、五个、六个、七个、八个、九个、十个、十一个、十二个、十三个、十四个、十五个、十六个、十七个、十八个、十九个、二十个、二十一个、二十二个、二十三个或二十四个)不同类型的缓冲液。如本领域已知的,在本文所述的工艺中使用的用于两个或更多个mccs中的一种或多种类型的缓冲液将取决于:存在于该两个或更多个mccs(例如,第一mccs和第二mccs)的一个或多个色谱柱和/或一个或多个色谱膜中的树脂,重组治疗性蛋白质,和单元操作(例如,本文所述的任何示例性单元操作)-其通过该两个或更多个mccs的特定的一个或多个色谱柱和/或一个或多个色谱膜进行。在本文所述的任何工艺中使用两个或更多个mccs期间,所采用的缓冲液的体积和类型也可以由本领域技术人员确定(例如,下面将更详细地讨论)。例如,可以选择在本文所述的任何工艺中使用两个或更多个mccs期间所采用的缓冲液的体积和一个或多个类型,以优化重组蛋白质药物产品中的以下中的一个或多个:重组治疗性蛋白质的总产量、重组治疗性蛋白质的活性、重组治疗性蛋白质的纯度水
平、以及从含有重组治疗性蛋白质的流体中除去生物污染物(例如,不存在活性病毒、分枝杆菌、酵母菌、细菌或哺乳动物细胞)。
235.调节含有重组治疗性蛋白质的流体的离子浓度和/或ph的单元操作可以使用mccs(例如,第一和/或第二mccs)来进行,该mccs包括并利用缓冲液调节储器(例如,在线缓冲液调节储器)以将新的或另外的缓冲溶液添加到含有重组治疗性蛋白质的流体中(例如在单个mccs中的柱之间,或在倒数第二个mccs(例如第一mccs)中的最后一个柱之后并且在将含有重组治疗性蛋白质的流体进料到下一个mccs(例如第二mccs)的第一个柱之前。在线缓冲液调节储器可以是任何尺寸(例如,大于100ml)并且可以含有任何缓冲溶液(例如具有以下中的一个或多个的缓冲溶液:与含有重组治疗性蛋白质的流体相比升高或降低的ph;与含有重组治疗性蛋白质的流体相比增加或减少的离子(例如盐)浓度;和/或增加或减少的试剂浓度,该试剂与重组治疗性蛋白质竞争地结合于存在于mccs(例如第一或第二mccs)的至少一个色谱柱或至少一个色谱膜中的树脂)。
236.在一些实施方案中,mccs控制器对添加到工艺流体的缓冲溶液的量的确定是基于生物样品中分析物的浓度或效价信息。例如,用于此类测量的溶质可以是缓冲溶液组分或工艺流体组分,其浓度与流体缓冲液组成、工艺流体的ph、和/或工艺流体的离子强度有关。将组分的浓度信息的测量作为反馈信息提供给mccs控制器,其使用反馈信息来确定将一种或多种缓冲溶液在何时和以多少量排放到工艺流体中。红外光谱测量系统通常可以定位在生物制造系统中的任何位置,用于测量工艺流体以向mccs控制器提供与缓冲液相关的反馈信息。
237.在某些实施方案中,工艺流体的抗体浓度信息可用于控制将细胞培养物引入生物反应器的速率。具体而言,通过确定从生物反应器收获的工艺流体中的抗体浓度值,mccs控制器可以调节细胞培养物流出到生物反应器中的速率。以这种方式的调节允许控制源自生物反应器的细胞密度和比生产率的容积生产率。对于固定的灌注速率,此类调节允许控制工艺流体中的抗体浓度,使得mccs 1每单位时间将接收近似恒定量的产品。换言之,调节这种性质可用于确保生物反应器内的产品生成速率在特定时间段内保持近似恒定。
238.在一些实施方案中,与工艺流体相关的某些质量属性的确定可由mccs控制器使用以确定生物制造系统是否在可接受的参数范围内操作,或者在操作期间,系统是否在一个或多个可接受的参数范围之外。
239.对于一个或多个品质属性中的各个品质属性,可通过校准程序建立可接受的值的范围。这些范围有效地为系统建立了操作条件,在该操作条件下生物产品以可接受的速率和纯度水平生成,而副产品及其他不希望的物质的产量处于可接受的低水平。当系统在一个或多个范围之外操作时,产品产量和/或纯度可能会降低,不希望的物质产生的速率/量可能会增加,试剂消耗速率可能会增加,和/或其他不希望的效果或情况可能发生。
240.在系统内的一个或多个位置处为工艺流体确定的品质属性可用于确保系统在这些操作参数的可接受范围内操作。如果一个或多个品质属性的确定值落在确立的可接受范围之外,则mccs控制器识别出存在潜在的故障状况。
241.为了解决故障状况,mccs控制器(或连接至mccs控制器的另一个系统控制器)可调节生物制造系统的任何操作参数以修改其操作,从而也调节质量属性值,使得它们落在可接受的范围内。这种性质的纠正措施确保了基于由确定的品质属性值提供的反馈,系统可
主动地保持在确立的一组或一系列操作条件内。
242.在某些实施方案中,如果mccs控制器(或连接至mccs控制器的另一个系统控制器)确定系统离其可接受的操作条件范围太远以致于将系统返回到可接受的条件范围会是困难的或者甚至不可能的,或者会导致其他不希望的后果,则控制器可将控制信号传输至生物反应器以中止生产并将其内容物排放到废弃物中。在此类案例中,生产工艺偏离系统的可接受的操作条件范围太远,有效的纠正措施是不切实际或不可能的。通过简单地排出生物反应器的内容物,系统可以通过重新开始生产工艺节省相当多的时间,而不是试图调节可能已经无可挽回地偏离可接受条件范围的正在进行的生产工艺。
243.此外,可以基于一种或多种生物反应器培养基组分(例如葡萄糖浓度、谷氨酰胺浓度、乳酸浓度和铵离子浓度)的测量值向mccs控制器(或另一种系统控制器)提供反馈,然后该控制器可用于调节反应器条件以确保细胞活力、产品产量以及其他性能指标被维持在目标范围内。控制器可以基于生物反应器培养基组分的值,以类似于基于产品品质属性和其他测量的量值实行的调节的方式调节任何一个或多个工艺参数。
244.硬件和软件实现
245.控制单元122可以被配置成执行本文描述的任何控制功能,并且可以以硬件、软件或者硬件和软件的组合来实现。控制单元122通常包括连接到存储器单元、存储装置、输出装置(例如显示器)和人机接口装置(例如键盘、鼠标、触摸板、触敏显示器)的至少一个电子处理器。控制单元122沿着本文所示的一些或全部控制线从系统部件接收作为电信号的信息,并且沿着控制线将电控制信号传输到系统部件。
246.本文描述的方法步骤和控制功能可以使用标准或专有编程语言在计算机程序中实现。这样的程序被设计成由控制单元122(例如,控制单元的电子处理器)执行,并且使得控制单元执行所描述的步骤和功能。每个程序可以存储在计算机可读存储介质(例如,光学、磁性、固态、可重写或其他永久存储介质)上。可用于向控制单元122提供指令的专有编程语言的一个例子是软件套件(waters corp.,milford,ma)。
247.实施例
248.提供以下实施例以进一步说明前述公开文本的各个方面,但除非另有明确说明,否则不旨在以另外的方式限制权利要求的任何特征,或限制实施方案的任何方面。
249.实施例1.
250.系统100用于分析来自以强化灌注工艺运行的灌注生物反应器的抗tgfβ。所述系统包括工艺样品管理器(process sample manager,psm)、色谱柱加热器(column heater,ch)、包含两个1位9端口阀门的色谱柱管理器(column manager,cm)、二元泵(binary pump,bsm)、在“d”线上增加了溶剂选择阀的四元泵(quaternary pump,qsm)、pda检测器(pda)、装有一个5ml不锈钢样品保持回路的一个2位10端口色谱柱选择阀(均从waters corp.,milford,ma获得)、以及两个idex辅助2位6端口切换阀。
251.生物反应器的收获物使用连接到液体处理器(其从obtained from gilson,middleton,wi获得)的mast(模块化自动采样技术)(其从lonza,basel,switzerland获得)自动采样。mast系统通过容积泵抽取约40ml的收获物,以在将10ml收获物放入液体处理器平台上的12ml透明玻璃瓶之前清空线路。然后,液体处理器通过将材料重新注入连接液体处理器和抽吸装置的peek管道传输线路,将7.5ml的收获物传输至系统100。将样品直接转
移到5ml样品保持回路中,在那里保持样品直到进行样品分析。一旦样品转移完成,主计算机向控制单元122发送信号,以初始化3软件中指定的方法集。
252.本例的方法设置运行包括回路加载功能、在两个质量负荷下在样品纯化装置的蛋白a(pro a)柱上的两次注射、在2个质量负荷下在尺寸排阻柱上的两次注射、在常用系统部件的分离技术(pro a和尺寸排阻色谱(sec))之间的中间水洗方法,以及最后用20%甲醇清洗循环并完成分段,以确保循环处于正确位置以接受更多样品。需要注意的是,每当提到二级柱(如sec)时,除非另有说明,应假设该方法包含pro a的在线纯化。
253.对于每次注射,从保持回路中抽取1ml的收获物,并转移到50μl样品注射回路中,以便在系统上进行全回路注射。为了测试不同的质量负荷,进行了全环注射以及使用1x磷酸盐缓冲盐水(pbs)ph 7.2的缓冲液在线1:2稀释。
254.效价分析的样品纯化在thermo poros a 2.1x30mm、20μm的柱(即蛋白a亲和柱)上进行。表1和表2示出了第一泵和第二泵的梯度细节。
255.表1:效价分析的第一(二元)泵方法参数
[0256][0257]
表2:效价分析的第二(四元)泵方法参数
[0258][0259]
对于表1中所示的方法,缓冲液a是ph为7.2的1x杜氏磷酸盐缓冲盐水,缓冲液b是ph 8.0的20mm磷酸钠、1m氯化钠和7.5%异丙醇。对于表2所示的方法,缓冲液a是ph为3.2的0.1m磷酸-柠檬酸盐、0.14m氯化钠。
[0260]
所述系统被配置成将纯化的样品直接导向检测器116(pda检测器),而不经过任何基于柱的样品分析仪。在280nm的吸光度下监测分离。蛋白a柱在室温下保持在周围环境中。在pda检测器中检测后,对测得的色谱图进行积分,以计算在约2.5分钟时对应于洗脱蛋白质的峰在曲线下的面积。单克隆抗体的面积随后通过使用校准曲线进行定量,该校准曲线由柱上50μg至2μg的质量负荷相对于面积绘制而成。
[0261]
图5a是示出纯样品和1:2稀释样品的效价色谱图的曲线图,图5b是示出在每个稀释比率下6次不同运行的计算质量负荷和浓度的表。数据示出了运行之间极好的再现性,无论是在视觉上还是在计算结果中。
[0262]
使用尺寸排阻分离法在waters uplc beh sec 4.6x300mm,1.7μm,和柱上进行聚集分析。表3和表4示出了第一泵和第二泵的梯度细节。
[0263]
表3:用于聚集分析的第一(二元)泵方法参数
[0264][0265][0266]
表4:用于聚集分析的第二(四元)泵方法参数
[0267][0268]
对于表3中所示的方法,缓冲液a是ph为7.2的1x杜氏磷酸盐缓冲盐水,缓冲液b是ph 8.0的20mm磷酸钠、1m氯化钠和7.5%异丙醇。对于表4所示的方法,缓冲液a是ph为3.2的0.1m磷酸-柠檬酸盐和0.14m氯化钠,缓冲液b是ph为7.2的1x杜氏磷酸盐缓冲盐水。
[0269]
色谱柱管理器被配置为使用尺寸排阻色谱柱将样品导入样品分析仪。在280纳米的吸光度下监测分析物和其他组分的分离。当蛋白a柱处于环境中时,尺寸排阻柱在30cm的柱加热器中保持在25℃。在pda检测器116中检测时,记录的色谱被积分以计算对应于高分子量物质(主峰之前)、主要物质和低分子量物质(主峰之后)的峰在曲线下的面积。
[0270]
图6a是示出纯样品和1:2稀释样品的效价色谱图的曲线图,而图6b示出了具有在两次稀释的每一次中6种不同样品的测量峰信息的表。数据示出了运行之间极好的再现性,无论是在视觉上还是在计算结果中。质量负荷之间的峰百分比存在一些差异,这可能是由柱本身造成的。
[0271]
图7是示出来自实验的测量色谱图的曲线图,其中总共12个样品每1.5小时获得一次样品。对于这些实验,只有1个质量负荷被递送到蛋白a和尺寸排阻色谱柱:在样品管理器上用ph为7.2的1x pbs进行1:2的在线稀释。效价和聚集产品品质属性在12个样品中表现出优异的重现性。
[0272]
对于反相分析,使用水中(流动相a)的0.1%三氟乙酸,10%异丙醇、90%乙腈(流动相b)中的0.1%三氟乙酸和20mm乙酸钠ph 3.75(蛋白a柱洗脱物)在waters bioresolve polyphenyl 2.1x100mm,2.7μm,柱上进行分离。对于强阳离子交换分析,分离在
thermo mabpac scx-10rs,2.1x150mm,5μm柱上进行。流动相为20mm乙酸钠ph 3.75(流动相a和蛋白a洗脱物)和20mm乙酸三酯,25mm氯化钠ph 9.8(流动相b)。目前,这种方法使用梯度曲率来创建最佳峰分辨率的“s”形梯度。
[0273]
上述方法用于在线分析样品。如上所述,系统100还可以使用例如样品管理器流通针模块(可从waters corp.,milford,ma获得)来分析离线样品。使用流通针头,直接从小瓶或孔板中注射样品。注射量可根据需要在1μl至100μl之间变化这种灵活性允许在不进行在线稀释的情况下改变柱上的质量负荷。此外,在所述系统版本中没有样品保持回路,因为所有样品体积都包含在小瓶或孔板中,并且每个小瓶允许多次注射。
[0274]
实施例2.mimics-mpqa在工艺开发和中试规模生物反应器的在线工艺监测中的应用
[0275]
实验概述
[0276]
mimics-mpqa平台应用于抗转tgfβ单克隆治疗抗体的100l规模运行。收获样品在mimics-mpqa平台上运行,以收集3个属性的在线产品品质信息:效价、聚集和纯度/完整性。
[0277]
分析的样品是来自100l生物反应器和2个卫星3l生物反应器的收获材料(后atf)。对于分析,蛋白a亲和柱用于效价测定,蛋白a柱与大小排阻(sec)柱串联用于聚集分析,蛋白a柱与反相(rp)柱串联用于纯度/完整性信息。测试在4周的时间内进行,在此期间,每个队列中所有反应堆的样品在大约4个收获日的时间段内运行。在分析期间,一旦消耗掉,系统流动相根据需要被替换。
[0278]
对于每个生物反应器测试的每个收获日,将0.75ml材料转移到自动进样器小瓶中,并置于mimics-mpqa系统中。每个样品在系统上注射1个分析周期,以定量3个目标属性。注射体积保持在20μl,但每个柱上的质量负荷是不同的,根据以前的开发经验,通过应用范围从1:2到1:10的不同在线稀释因子来瞄准每个方法的线性区域。简而言之,pro a柱上的负载目标为10-25μg,sec柱上的负载目标为20-50μg,rp柱上的负载目标为3-7μg。
[0279]
对于pro a效价方法,在整个活动开始时运行一条标准曲线,并在pro a缓冲液更换后的第二个时间点再次运行,在整个活动中总共运行2条标准曲线。标准曲线是通过在线稀释2.5mg/ml的储备抗tgfβ构建的,以在柱上产生2-50μg的曲线。
[0280]
用于标准曲线的库存先前在之前的运行中进行了稀释,并保存在-80℃的亚液体中,用于mimics-mpqa活动。
[0281]
结果
[0282]
从pro a定量中捕获的数据也与两种离线定量效价测量进行了比较:通过使用pro a生物传感器尖端在octet上测量的效价和通过cedex
tm
生物分析仪测量的效价。图10-12展示了与100l和3l生物反应器的离线方法相比,mimics-mpqa效价的可比性。
[0283]
总的来说,这三种方法的趋势是一致的。将mimics-mpqa数据与cedex
tm
生物分析仪方法进行比较时,所有运行的%差异小于10%,这是一种可接受的分析方法的cv。cedex
tm
生物分析仪通常是用于每日上游工艺监测的效价测量方法。mimics-mpqa与该技术的可比性为哺乳动物培养的效价测定提供了一个正交工具。mimics-mpqa的另一个优点是,当离线执行测试时,减少了对样品的手动操作和样品存储的潜在偏差。
[0284]
将本实验中捕获的聚合数据与为正常流程监测而运行的离线sec方法进行了比较。每个生物反应器的数据如图13-15所示。
[0285]
总体而言,离线分析方法和mimics-mpqa之间的趋势是可比较的。这两种方法示出,在整个活动中,聚合水平都低于2.5%。mimics-mpqa系统允许为该活动获取比离线分析中正常测试更多的数据点。这种增加的采样允许更深入地观察整个活动期间的聚集波动。
[0286]
从mimics-mpqa分析中获得的纯度数据也与用于工艺监测的离线纯度方法进行了比较,如图16所示。离线方法基于ce-sds方法,该方法与mimics-mpqa进行的纯度测量正交。
[0287]
如图16所示,与离线方法相比,mimics-mpqa系统提供了总体更低的绝对百分比纯度。尽管百分比存在绝对差异,但两种方法的总体趋势是一致的。
[0288]
总的来说,mimics-mpqa系统成功地以在线监测模式应用于抗tgfβ的100l中试规模生物反应器项目。与离线分析相比,所述系统允许增加采样,这进一步允许在活动工艺中更好地理解流程。此外,效价和聚集方法与离线分析相比具有很高的可比性,与分析实验室获得的结果相比,提供了对现场分析的信心。mimics-mpqa系统还允许减少样品消耗和更快的通量,因为在分析之前不需要预先纯化蛋白a,因为这一步骤是mimics-mpqa整体工作流程的一部分。最后,所述系统能够以最小的事故运行4周,进一步加强了对仪器鲁棒性和柱稳定性的理解。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。