蛋变态反应的抗原
1.本技术是中国专利申请201780034053.7的分案申请,原申请201780034053.7的申请日为2017年06月02日,其名称为“蛋变态反应的抗原”。
技术领域
2.本发明涉及蛋变态反应的新型抗原。本发明还涉及蛋变态反应的诊断试剂盒、诊断用组合物以及诊断方法。本发明还涉及包含该抗原的药物组合物、去除或降低了该抗原的蛋、蛋加工品或者产生该蛋或由该蛋孵化的鸟。本发明还涉及去除或降低了该抗原的蛋加工品的制造方法。本发明进而还涉及用于判断对象物中有无蛋抗原的检测仪。
背景技术:
3.变态反应患者的血清和组织中产生了针对特定抗原(以下,也称为变应原)特异的ige抗体。通过该ige抗体与特定抗原的相互作用产生的生理学结果,引起了变态反应。抗原广义上是指引起变态反应症状的食品/食材等;狭义上是指特异的ige抗体所结合的、食品/食材等所包含的蛋白质(以下,也称为变应原成分)。
4.现有的变态反应检测试剂中,大多是简单地将变应原候补食品/食材等磨碎而制成抗原试剂(专利文献1)。因此,现有的抗原试剂中所包含的变应原成分中,对于与ige抗体的结合,只有在超过可判定阳性反应阈值的含量时,才能在变态反应检查中检测出阳性反应,是诊断效率还不能说是充分高的状态。
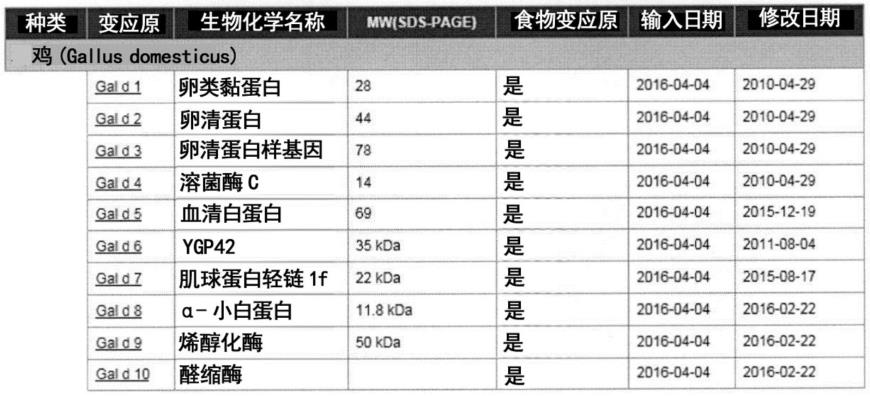
5.关于蛋变应原,现在已知有以下表中所示的物质(非专利文献1)。
6.[表1]
[0007][0008]
变应原候补的食品/食材中,启示了几种变应原成分,作为检测试剂盒而被商品化,但为了提高变态反应检测的可靠度,需要网罗地限定变应原成分,但利用上述变应原成分的测定进行的患者检测率还不充分。鉴定蛋的新型变应原不仅需要提高诊断试剂的精度,作为低变应原食品、低变应原食材、治疗药的靶标也是非常重要的。
[0009]
另一方面,关于蛋白质的分离/纯化,近年来、作为从少量样品中对多种蛋白质进
行分离纯化的方法,使用了第一维进行等电点电泳、第二维进行sds-page(十二烷基硫酸钠-聚丙烯酰胺凝胶电泳)的二维电泳法。申请人等到目前为止,开发出了分离能力高的二维电泳法(专利文献2~5)。
[0010]
现有技术文献
[0011]
专利文献
[0012]
专利文献1:日本特开2002-286716
[0013]
专利文献2:日本特开2011-33544
[0014]
专利文献3:日本特开2011-33546
[0015]
专利文献4:日本特开2011-33547
[0016]
专利文献5:日本特开2011-33548
[0017]
非专利文献
[0018]
非专利文献1:allergen nomenclature,who/iuis allergen nomenclature sub-committee,[平成28年5月31日検索],
インターネット
<url:http://www.allergen.org/search.php?allergenname=&allergensource=gallus domesticus&taxsource=&taxorder=&foodallerg=all&bioname=>
技术实现要素:
[0019]
发明要解决的问题
[0020]
本发明提供蛋变态反应的新型抗原。本发明还提供蛋变态反应的诊断方法和诊断试剂盒。本发明还涉及包含该抗原的药物组合物、去除或降低了该抗原的蛋、蛋加工品或者产生该蛋或由该蛋孵化的鸟。本发明进一步提供用于判断对象物中有无蛋抗原的检测仪。
[0021]
用于解决问题的方案
[0022]
本发明人等为了解决上述问题,对于蛋变态反应的原因的抗原鉴定进行了深入研究。结果成功地鉴定出患有蛋变态反应的患者血清中ige抗体所特异地结合的新型的抗原。基于该见解完成了本发明。
[0023]
即,一实施方式中,本发明如下。
[0024]
[1]一种蛋变态反应的诊断试剂盒,其包含以下(1)~(3)的蛋白质中的至少一种作为抗原:
[0025]
(1)(1a)包含卵黄原蛋白-3(vitellogenin-3)的c末端部分的蛋白质或其突变体,其是作为蛋变态反应的抗原的、以下(1a-a)~(1a-e)中的任一蛋白质:
[0026]
(1a-a)含有在序列号2中缺失、置换、插入或附加有1个或多个氨基酸的氨基酸序列的蛋白质;
[0027]
(1a-b)含有与序列号2所示的氨基酸序列的同一性(identity)为70%以上的氨基酸序列的蛋白质;
[0028]
(1a-c)含有由在序列号1中缺失、置换、插入或附加有1个或多个核苷酸的碱基序列编码的氨基酸序列的蛋白质;
[0029]
(1a-d)含有由与序列号1所示的碱基序列的同一性为70%以上的碱基序列编码的氨基酸序列的蛋白质;或
[0030]
(1a-e)含有由下述核酸编码的氨基酸序列的蛋白质,所述核酸和由与序列号1所
示的碱基序列互补的碱基序列构成的核酸在严格的条件下杂交;或者
[0031]
(1b)含有选自由序列号2~11组成的组中的氨基酸序列中的至少一种的蛋白质;
[0032]
(2)(2a)包含卵黄原蛋白-3(vitellogenin-3)的c末端部分的蛋白质或其突变体,其是作为蛋变态反应的抗原的、以下(2a-a)~(2a-e)中的任一蛋白质:
[0033]
(2a-a)含有在序列号13中缺失、置换、插入或附加有1个或多个氨基酸的氨基酸序列的蛋白质;
[0034]
(2a-b)含有与序列号13所示的氨基酸序列的同一性为70%以上的氨基酸序列的蛋白质;
[0035]
(2a-c)含有由在序列号12中缺失、置换、插入或附加有1个或多个核苷酸的碱基序列编码的氨基酸序列的蛋白质;
[0036]
(2a-d)含有由与序列号12所示的碱基序列的同一性为70%以上的碱基序列编码的氨基酸序列的蛋白质;或
[0037]
(2a-e)含有由下述核酸编码的氨基酸序列的蛋白质,所述核酸和由与序列号12所示的碱基序列互补的碱基序列构成的核酸在严格的条件下杂交;或者
[0038]
(2b)含有选自由序列号9~11、13、14和16组成的组中的氨基酸序列中的至少一种的蛋白质;
[0039]
(3)(3a)包含卵黄原蛋白-1(vitellogenin-1)的中央部分或卵黄脂磷蛋白-1(lipovitellin-1)的c末端部分的蛋白质、或其突变体,其是作为蛋变态反应的抗原的、以下(3a-a)~(3a-e)的任一蛋白质:
[0040]
(3a-a)含有在序列号18中缺失、置换、插入或附加有1个或多个氨基酸的氨基酸序列的蛋白质;
[0041]
(3a-b)含有与序列号18所示的氨基酸序列的同一性为70%以上的氨基酸序列的蛋白质;
[0042]
(3a-c)含有由在序列号17中缺失、置换、插入或附加有1个或多个核苷酸的碱基序列编码的氨基酸序列的蛋白质;
[0043]
(3a-d)含有由与序列号17所示的碱基序列的同一性为70%以上的碱基序列编码的氨基酸序列的蛋白质;或
[0044]
(3a-e)含有由下述核酸编码的氨基酸序列的蛋白质,所述核酸和由与序列号17所示的碱基序列互补的碱基序列构成的核酸在严格的条件下杂交;或者
[0045]
(3b)含有选自由序列号18~45组成的组中的氨基酸序列中的至少一种的蛋白质。
[0046]
[2]一种蛋变态反应的诊断用组合物,其包含上述[1]中作为(1)~(3)限定的蛋白质中的至少一种作为抗原。
[0047]
[3]一种提供用于诊断对象的蛋变态反应的指标的方法,其包括以下工序:
[0048]
(i)使由对象得到的试样与抗原接触,此处,该试样是包含有ige抗体的溶液;
[0049]
(ii)对由对象得到的试样中的ige抗体与该抗原的结合进行检测;
[0050]
(iii)检测到对象的ige抗体与该抗原结合时,提供对象为蛋变态反应的指标;
[0051]
此处,该抗原是上述[1]中作为(1)~(3)限定的蛋白质的至少一种。
[0052]
[4]一种药物组合物,其包含上述[1]中作为(1)~(3)限定的蛋白质的至少一种。
[0053]
[5]根据上述[4]所述的药物组合物,其用于治疗蛋变态反应。
[0054]
[6]一种蛋、蛋加工品或鸟,其特征在于,其为去除或降低了抗原的蛋、蛋加工品或者产生该蛋或由该蛋孵化的鸟,该抗原为上述[1]中作为(1)~(3)限定的蛋白质的至少一种。
[0055]
[7]一种用于判断对象物中有无蛋抗原的检测仪,其特征在于,其包含与上述[1]中作为(1)~(3)限定的蛋白质的至少一种结合的抗体。
[0056]
[8]一种用于判断对象物中有无蛋变态反应的抗原的检测仪,其特征在于,其包含具有与序列号1、12或17所示的碱基序列的至少一个互补的碱基序列的引物。
[0057]
[9]一种蛋变态反应的诊断试剂盒,其包含以下(4)~(10)的蛋白质中的至少一种作为抗原:
[0058]
(4)(4a)包含卵黄原蛋白-3(vitellogenin-3)的蛋白质或其突变体,其是作为蛋变态反应的抗原的、以下(4a-a)~(4a-e)中的任一蛋白质:
[0059]
(4a-a)含有在序列号47中缺失、置换、插入或附加有1个或多个氨基酸的氨基酸序列的蛋白质;
[0060]
(4a-b)含有与序列号47所示的氨基酸序列的同一性为70%以上的氨基酸序列的蛋白质;
[0061]
(4a-c)含有由在序列号46中缺失、置换、插入或附加有1个或多个核苷酸的碱基序列编码的氨基酸序列的蛋白质;
[0062]
(4a-d)含有由与序列号46所示的碱基序列的同一性为70%以上的碱基序列编码的氨基酸序列的蛋白质;或
[0063]
(4a-e)含有由下述核酸编码的氨基酸序列的蛋白质,所述核酸和由与序列号46所示的碱基序列互补的碱基序列构成的核酸在严格的条件下杂交;或者
[0064]
(4b)含有选自由序列号47~57组成的组中的氨基酸序列中的至少一种的蛋白质;
[0065]
(5)(5a)包含卵黄原蛋白-2前体(vitellogenin-2precursor)的蛋白质或其突变体,其是作为蛋变态反应的抗原的、以下(5a-a)~(5a-e)中的任一蛋白质:
[0066]
(5a-a)含有在序列号59中缺失、置换、插入或附加有1个或多个氨基酸的氨基酸序列的蛋白质;
[0067]
(5a-b)含有与序列号59所示的氨基酸序列的同一性为70%以上的氨基酸序列的蛋白质;
[0068]
(5a-c)含有由在序列号58中缺失、置换、插入或附加有1个或多个核苷酸的碱基序列编码的氨基酸序列的蛋白质。
[0069]
(5a-d)含有由与序列号58所示的碱基序列的同一性为70%以上的碱基序列编码的氨基酸序列的蛋白质;或
[0070]
(5a-e)含有由下述核酸编码的氨基酸序列的蛋白质,所述核酸和由与序列号58所示的碱基序列互补的碱基序列构成的核酸在严格的条件下杂交;或者
[0071]
(5b)含有选自由序列号59~104组成的组中的氨基酸序列中的至少一种的蛋白质;
[0072]
(6)(6a)卵黄原蛋白-2前体(vitellogenin-2precursor)或其突变体,其是作为蛋变态反应的抗原的、以下(6a-a)~(6a-e)中的任一蛋白质:
[0073]
(6a-a)含有在序列号106中缺失、置换、插入或附加有1个或多个氨基酸的氨基酸
序列的蛋白质;
[0074]
(6a-b)含有与序列号106所示的氨基酸序列的同一性为70%以上的氨基酸序列的蛋白质;
[0075]
(6a-c)含有由在序列号105中缺失、置换、插入或附加有1个或多个核苷酸的碱基序列编码的氨基酸序列的蛋白质;
[0076]
(6a-d)含有由与序列号105所示的碱基序列的同一性为70%以上的碱基序列编码的氨基酸序列的蛋白质;或
[0077]
(6a-e)含有由下述核酸编码的氨基酸序列的蛋白质,所述核酸和由与序列号105所示的碱基序列互补的碱基序列构成的核酸在严格的条件下杂交;或者
[0078]
(6b)含有选自由序列号106~150组成的组中的氨基酸序列中的至少一种的蛋白质;
[0079]
(7)(7a)载脂蛋白b前体(apolipoprotein b precursor)或其突变体,其是作为蛋变态反应的抗原的、以下(7a-a)~(7a-e)中的任一蛋白质:
[0080]
(7a-a)含有在序列号152中缺失、置换、插入或附加有1个或多个氨基酸的氨基酸序列的蛋白质;
[0081]
(7a-b)含有与序列号152所示的氨基酸序列的同一性为70%以上的氨基酸序列的蛋白质;
[0082]
(7a-c)含有由在序列号151中缺失、置换、插入或附加有1个或多个核苷酸的碱基序列编码的氨基酸序列的蛋白质;
[0083]
(7a-d)含有由与序列号151所示的碱基序列的同一性为70%以上的碱基序列编码的氨基酸序列的蛋白质;或
[0084]
(7a-e)含有由下述核酸编码的氨基酸序列的蛋白质,所述核酸和由与序列号151所示的碱基序列互补的碱基序列构成的核酸在严格的条件下杂交;或者
[0085]
(7b)含有选自由序列号152~235组成的组中的氨基酸序列中的至少一种的蛋白质;
[0086]
(8)(8a)载脂蛋白b前体(apolipoprotein b precursor)或其突变体,其是作为蛋变态反应的抗原的、以下(8a-a)~(8a-e)中的任一蛋白质:
[0087]
(8a-a)含有在序列号237中缺失、置换、插入或附加有1个或多个氨基酸的氨基酸序列的蛋白质;
[0088]
(8a-b)含有与序列号237所示的氨基酸序列的同一性为70%以上的氨基酸序列的蛋白质;
[0089]
(8a-c)含有由在序列号236中缺失、置换、插入或附加有1个或多个核苷酸的碱基序列编码的氨基酸序列的蛋白质;
[0090]
(8a-d)含有由与序列号236所示的碱基序列的同一性为70%以上的碱基序列编码的氨基酸序列的蛋白质;或
[0091]
(8a-e)含有由下述核酸编码的氨基酸序列的蛋白质,所述核酸和由与序列号236所示的碱基序列互补的碱基序列构成的核酸在严格的条件下杂交;或者
[0092]
(8b)含有选自由序列号237~249组成的组中的氨基酸序列中的至少一种的蛋白质;
[0093]
(9)(9a)载脂蛋白b前体(apolipoprotein b precursor)或其突变体,其为作为蛋变态反应的抗原的、以下(9a-a)~(9a-e)中的任一蛋白质:
[0094]
(9a-a)含有在序列号251中缺失、置换、插入或附加有1个或多个氨基酸的氨基酸序列的蛋白质;
[0095]
(9a-b)含有与序列号251所示的氨基酸序列的同一性为70%以上的氨基酸序列的蛋白质;
[0096]
(9a-c)含有由在序列号250中缺失、置换、插入或附加有1个或多个核苷酸的碱基序列编码的氨基酸序列的蛋白质;
[0097]
(9a-d)含有由与序列号250所示的碱基序列的同一性为70%以上的碱基序列编码的氨基酸序列的蛋白质;或
[0098]
(9a-e)含有由下述核酸编码的氨基酸序列的蛋白质,所述核酸和由与序列号250所示的碱基序列互补的碱基序列构成的核酸在严格的条件下杂交;或者
[0099]
(9b)含有选自由序列号251~260组成的组中的氨基酸序列中的至少一种的蛋白质;
[0100]
(10)(10a)卵黄原蛋白-2前体(vitellogenin-2precursor)或其突变体,其是作为蛋变态反应的抗原的、以下(10a-a)~(10a-e)中的任一蛋白质:
[0101]
(10a-a)含有在序列号262中缺失、置换、插入或附加有1个或多个氨基酸的氨基酸序列的蛋白质;
[0102]
(10a-b)含有与序列号262所示的氨基酸序列的同一性为70%以上的氨基酸序列的蛋白质;
[0103]
(10a-c)含有由在序列号261中缺失、置换、插入或附加有1个或多个核苷酸的碱基序列编码的氨基酸序列的蛋白质;
[0104]
(10a-d)含有由与序列号261所示的碱基序列的同一性为70%以上的碱基序列编码的氨基酸序列的蛋白质;或
[0105]
(10a-e)含有由下述核酸编码的氨基酸序列的蛋白质,所述核酸和由与序列号261所示的碱基序列互补的碱基序列构成的核酸在严格的条件下杂交;或者
[0106]
(10b)含有选自由序列号262~271组成的组中的氨基酸序列中的至少一种的蛋白质。
[0107]
[10]一种蛋变态反应的诊断用组合物,其包含上述[9]中作为(4)~(10)限定的蛋白质的至少一种作为抗原。
[0108]
[11]一种提供用于诊断对象的蛋变态反应的指标的方法,其包括以下工序:
[0109]
(i)使由对象得到的试样与抗原接触,此处,该试样是包含有ige抗体的溶液;
[0110]
(ii)对由对象得到的试样中的ige抗体与该抗原的结合进行检测;
[0111]
(iii)检测到对象的ige抗体与该抗原结合时,提供对象为蛋变态反应的指标;
[0112]
此处,该抗原是上述[9]中作为(4)~(10)限定的蛋白质的至少一种。
[0113]
[12]一种药物组合物,其包含上述[9]中作为(4)~(10)限定的蛋白质的至少一种。
[0114]
[13]根据上述[12]所述的药物组合物,其用于治疗蛋变态反应。
[0115]
[14]一种蛋、蛋加工品或鸟,其特征在于,其为去除或降低了抗原的蛋、蛋加工品
或者产生该蛋或由该蛋孵化的鸟,该抗原是上述[9]中作为(4)~(10)限定的蛋白质的至少一种。
[0116]
[15]一种用于判断对象物中有无蛋抗原的检测仪,其特征在于,其包含与上述[9]中作为(4)~(10)限定的蛋白质的至少一种结合的抗体。
[0117]
[16]一种用于判断对象物中有无蛋变态反应的抗原的检测仪,其特征在于,其包含具有与序列号46、58、105、151、236、250或261所示的碱基序列的至少一个互补的碱基序列的引物。
[0118]
[17]一种去除或降低了抗原的蛋加工品的制造方法,其具有如下步骤:在该加工品的制造过程中确认抗原被去除或降低了,
[0119]
此处,该抗原是上述[1]中作为(1)~(3)限定的蛋白质的至少一种、或者上述[9]中作为(4)~(10)限定的蛋白质的至少一种。
[0120]
[18]一种源自蛋的抗原,其是上述[1]中作为(1)~(3)限定的蛋白质的至少一种、或者上述[9]中作为(4)~(10)限定的蛋白质的至少一种,并且成为蛋变态反应的原因。
[0121]
发明的效果
[0122]
通过本发明,能够提供蛋变态反应的新型的抗原。本发明中,鉴定出了引起蛋变态反应的新型的抗原(变应原成分),因此能够提供蛋变态反应的高灵敏度的诊断方法和诊断试剂盒、包含该抗原的药物组合物、去除或降低了该抗原的蛋、蛋加工品或者产生该蛋或由该蛋孵化的鸟、去除或降低了该抗原的蛋加工品的制造方法、以及用于判断对象物中有无蛋抗原的检测仪。
附图说明
[0123]
图1是表示对于鸡蛋(生的蛋)的蛋黄所包含的蛋白质利用二维电泳的蛋白质的泳动图的凝胶照片。照片左侧的条带是分子量标记物的条带,照片左侧的数值是各分子量标记物的分子量(kda)。照片上部的数值表示等电点。
[0124]
图2是对于鸡蛋(生的蛋)的蛋黄所包含的蛋白质的二维电泳图,使用蛋变态反应患者1的血清进行免疫印迹的照片。
[0125]
图3是表示对于鸡蛋(生的蛋)的蛋黄所包含的蛋白质的二维电泳图的凝胶照片。蛋变态反应患者1的血清特异地进行了反应的斑点1、2和3分别用方框围起来表示。
[0126]
图4是对于鸡蛋(生的蛋)的蛋黄所包含的蛋白质的二维电泳图,使用蛋变态反应患者2的血清进行免疫印迹的照片。蛋变态反应患者2的血清特异地进行了反应的斑点4~8分别用方框围起来表示。
[0127]
图5是对于鸡蛋(生的蛋)的蛋黄所包含的蛋白质的二维电泳图,使用蛋变态反应患者3的血清进行免疫印迹的照片。蛋变态反应患者3的血清特异地进行了反应的斑点9和10分别用方框围起来表示。
[0128]
图6是对于鸡蛋(生的蛋)的蛋黄所包含的蛋白质的二维电泳图,使用蛋变态反应患者4的血清进行免疫印迹的照片。蛋变态反应患者4的血清特异地进行了反应的斑点11用方框围起来表示。
具体实施方式
[0129]
以下具体地对本发明进行说明,但本发明不限于这些内容。
[0130]
本说明书中,只要没有特别的定义,与本发明相关联而使用的科学术语和技术术语为本领域技术人员通常理解的意思。
[0131]
本说明书中变态反应是指:在对某抗原敏感的生物体中,该抗原再次进入时产生的、对生物体表现出不舒服的过敏反应的状态。食物中的大多变态反应疾病,在血液和组织中产生对抗原特异的ige抗体。ige抗体与肥大细胞或嗜碱性粒细胞结合。对该ige抗体特异的抗原再次进入变态反应疾病患者的体内时,该抗原与结合有肥大细胞或嗜碱性粒细胞的ige抗体组合,然后该ige抗体在细胞表面交联,产生ige抗体-抗原相互作用的生理学效果。作为它们的生理学的效果,可列举出组胺、5-羟色胺、肝素、嗜酸性粒细胞趋化因子或各种白三烯等的释放。这些释放物质引起由ige抗体与特定抗原组合产生的变态反应。由特定抗原产生的变态反应通过上述路径来实现。
[0132]
本说明书中,蛋是指鸟类的蛋、优选指代鸡蛋。
[0133]
本说明书中,蛋变态反应是指:具有将蛋所包含的蛋白质等作为抗原而产生的变态反应的状态。蛋变态反应是指:与蛋所包含的抗原接触时或者摄取该抗原时能够产生变态反应。通常将摄取食物时产生的变态反应特别地称为食物变态反应。蛋变态反应也可以是食物变态反应。
[0134]
本说明书中,抗原是指引起变态反应的物质,也被称为变应原成分。抗原优选为蛋白质。
[0135]
本说明书中,蛋白质是具有天然氨基酸通过肽键连接而成的结构的分子。对于蛋白质所包含的氨基酸的个数没有特别的限定,有时将2~50个左右的氨基酸通过肽键连接而成的蛋白质称为肽。另外,关于氨基酸,在可能存在旋光异构体的情况下,只要没有特别明示则表示l体。本说明书中使用的蛋白质或肽的氨基酸序列的标记法如下:基于标准的用法和本领域中惯用的标记法,氨基酸用一文字标记表示,左方向是氨基末端方向并且右方向是羧基末端方向。
[0136]
抗原的限定
[0137]
对于蛋所包含的蛋白质,利用上述的手法对于蛋变态反应的抗原进行限定。具体而言,将生的鸡蛋分为蛋黄和蛋白,分别对于其中所包含的蛋蛋白质按照下述条件供于二维电泳。
[0138]
第一维电泳作为等电点电泳用凝胶使用凝胶长度5~10cm范围内并且凝胶的ph范围为3~10、凝胶相对于泳动方向的ph梯度在将凝胶的全长设为1、至ph5为止的凝胶长度设为a、ph5~7的凝胶长度设为b、ph7以上的凝胶长度设为c时,a为0.15~0.3的范围内、b为0.4~0.7的范围内、c为0.15~0.3范围内的凝胶,具体而言,使用ge healthcare bioscience(以下,简称为ge公司)制的ipg凝胶immobiline drystrip(ph3-10nl)进行等电点泳动。电泳仪使用ge公司制的ipgphor。将电泳仪电流值的上限设定为每1根凝胶75μa,将电压程序如下进行设置:(1)以300v恒定电压升压至750vhr为止,从而进行恒定电压工序(该工序结束前的泳动30分钟的电流変化幅度为5μa);(2)缓缓地使电压从300vhr升压至1000v为止;(3)进一步,缓缓地使电压从4500vhr升压至5000v为止;(4)之后,以5000v恒定电压直至vhr成为12000,进行第一维的等电点电泳。
[0139]
第二维电泳使用:泳动方向基端部的凝胶浓度被设定为3~6%且泳动方向前端侧部分的凝胶浓度被设定为高于泳动方向基端部凝胶浓度的聚丙烯酰胺凝胶,具体而言,使用life technologies公司制的nupage 4-12%bris-tris gels ipg well mini 1mm进行sds-page。电泳仪使用life technologies公司制的xcell surelock mini-cell。作为泳动缓冲液,使用50mm mops、50mm tris碱、0.1%(w/v)sds、1mm edta,在200v恒定电压下进行约45分钟泳动。
[0140]
结果可知,对于鸡蛋的蛋白质在上述的条件下进行二维电泳时的凝胶中,斑点1~3的抗原与、蛋变态反应的被诊断为食物依赖性运动引起的变态反应症(food-dependent exercise-induced anaphylaxis)的患者的ige抗体特异地结合。另外可知,蛋的其他变态反应患者中,斑点4~11的抗原与该患者的ige抗体特异地结合(图4~6)。
[0141]
抗原
[0142]
(1)斑点1的抗原
[0143]
对于斑点1,利用质谱分析进行序列鉴定的结果,检测到了序列号3~11的氨基酸序列。
[0144]
另外,对于斑点1,将由质谱分析装置得到的质谱数据(序列号3~11)与ncbi的蛋白质数据进行对照并解析,鉴定为卵黄原蛋白-3(vitellogenin-3)的c末端部分(氨基酸序列:序列号2、编码其的碱基序列:序列号1)。
[0145]
因此,本技术中,斑点1的抗原为以下(1a-a)~(1a-e)和(1b)中的任一者。
[0146]
(1a-a)含有在序列号2中缺失、置换、插入或附加有1个或多个氨基酸的氨基酸序列的蛋白质。
[0147]
(1a-b)含有与序列号2所示的氨基酸序列的同一性为70%以上、优选为75%以上、80%以上、85%以上、90%以上、95%以上、97%以上、98%以上、99%以上的氨基酸序列的蛋白质。
[0148]
(1a-c)含有由在序列号1中缺失、置换、插入或附加有1个或多个核苷酸的碱基序列编码的氨基酸序列的蛋白质。
[0149]
(1a-d)含有由与序列号1所示的碱基序列的同一性为70%以上、优选为75%以上、80%以上、85%以上、90%以上、95%以上、97%以上、98%以上、99%以上的碱基序列编码的氨基酸序列的蛋白质。
[0150]
(1a-e)含有由下述核酸编码的氨基酸序列的蛋白质,所述核酸和由与序列号1所示的碱基序列互补的碱基序列构成的核酸在严格的条件下杂交。
[0151]
(1b)含有选自由序列号2~11组成的组中的氨基酸序列中的至少一种的蛋白质、优选为包含该氨基酸序列的至少2、3、4、5、6、7、8、9种或所有序列的蛋白质。进而优选:含有选自由序列号2、4和序列号9~11组成的组中的氨基酸序列中的至少一种的蛋白质、优选为包含该氨基酸序列的至少2、3、4种或所有序列的蛋白质。其中,序列号3~11中的任一者所示的氨基酸序列任选缺失、置换、插入或附加有1个或多个氨基酸。
[0152]
上述(1a-a)~(1a-e)和(1b)的蛋白质还可以是:上述“抗原的限定”项目中记载的条件下进行二维电泳时的凝胶中,作为分子量20kda~40kda、优选为分子量30kda~35kda以及等电点4.0~10.0、优选为4.0~9.0的斑点出现的蛋白质。
[0153]
(2)斑点2的抗原
[0154]
对于斑点2,利用质谱分析进行序列鉴定的结果,检测到了序列号9~11、14、16的氨基酸序列。
[0155]
另外,对于斑点2,将由质谱分析装置得到的质谱数据(序列号9~11、14、16)与ncbi的蛋白质数据进行对照并解析,鉴定为卵黄原蛋白-3(vitellogenin-3)的c末端部分(氨基酸序列:序列号13、编码其的碱基序列:序列号12)。
[0156]
因此,本技术中,斑点2的抗原为以下(2a-a)~(2a-e)和(2b)中的任一者。
[0157]
(2a-a)含有在序列号13中缺失、置换、插入或附加有1个或多个氨基酸的氨基酸序列的蛋白质。
[0158]
(2a-b)含有与序列号13所示的氨基酸序列的同一性为70%以上、优选为75%以上、80%以上、85%以上、90%以上、95%以上、97%以上、98%以上、99%以上的氨基酸序列的蛋白质。
[0159]
(2a-c)含有由在序列号12中缺失、置换、插入或附加有1个或多个核苷酸的碱基序列编码的氨基酸序列的蛋白质。
[0160]
(2a-d)含有由与序列号12所示的碱基序列的同一性为70%以上、优选为75%以上、80%以上、85%以上、90%以上、95%以上、97%以上、98%以上、99%以上的碱基序列编码的氨基酸序列的蛋白质。
[0161]
(2a-e)含有由下述核酸编码的氨基酸序列的蛋白质,所述核酸和由与序列号12所示的碱基序列互补的碱基序列构成的核酸在严格的条件下杂交。
[0162]
(2b)含有选自由序列号9~11、13、14和16组成的组中的氨基酸序列中的至少一种的蛋白质、优选为包含该氨基酸序列的至少2、3、4、5种或所有序列的蛋白质。进而优选:含有选自由序列号9~11、13和16组成的组中的氨基酸序列中的至少一种的蛋白质、优选为包含该氨基酸序列的至少2、3、4种或所有序列的蛋白质。其中,序列号9~11、13、14、16中的任一者所示的氨基酸序列任选缺失、置换、插入或附加有1个或多个氨基酸。
[0163]
上述(2a-a)~(2a-e)和(2b)的蛋白质还可以是:上述“抗原的限定”项目中记载的条件下进行二维电泳时的凝胶中,作为分子量30kda~60kda、优选为分子量35kda~40kda附近以及等电点5.0~10.0、优选为6.0~9.0的斑点出现的蛋白质。
[0164]
(3)斑点3的抗原
[0165]
对于斑点3,利用质谱分析进行序列鉴定的结果,检测到了序列号19~45的氨基酸序列。
[0166]
另外,对于斑点3,将由质谱分析装置得到的质谱数据(序列号19~45)与uniprot的蛋白质数据进行对照并解析,鉴定为卵黄原蛋白-1(vitellogenin-1)的中央部分或其蛋白质的n末端侧的能够利用切断得到的卵黄脂磷蛋白-1(lipovitellin-1)的c末端部分(氨基酸序列:序列号18、编码其的碱基序列:序列号17)。
[0167]
因此,本技术中,斑点3的抗原为以下(3a-a)~(3a-e)和(3b)中的任一者。
[0168]
(3a-a)含有在序列号18中缺失、置换、插入或附加有1个或多个氨基酸的氨基酸序列的蛋白质。
[0169]
(3a-b)含有与序列号18所示的氨基酸序列的同一性为70%以上、优选为75%以上、80%以上、85%以上、90%以上、95%以上、97%以上、98%以上、99%以上的氨基酸序列的蛋白质。
[0170]
(3a-c)含有由在序列号17中缺失、置换、插入或附加有1个或多个核苷酸的碱基序列编码的氨基酸序列的蛋白质。
[0171]
(3a-d)含有由与序列号17所示的碱基序列的同一性为70%以上、优选为75%以上、80%以上、85%以上、90%以上、95%以上、97%以上、98%以上、99%以上的碱基序列编码的氨基酸序列的蛋白质。
[0172]
(3a-e)含有由下述核酸编码的氨基酸序列的蛋白质,所述核酸和由与序列号17所示的碱基序列互补的碱基序列构成的核酸在严格的条件下杂交。
[0173]
(3b)含有选自由序列号18~45组成的组中的氨基酸序列中的至少一种的蛋白质、优选为包含该氨基酸序列的至少2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27种或所有序列的蛋白质。进而优选为:含有选自由序列号18、19、22~31、33~35、37、39、40、42、43和45组成的组中的氨基酸序列中的至少一种的蛋白质、优选为包含该氨基酸序列的至少2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20种或所有序列的蛋白质。其中,序列号18~45中的任一者所示的氨基酸序列任选缺失、置换、插入或附加有1个或多个氨基酸。
[0174]
上述(3a-a)~(3a-e)和(3b)的蛋白质还可以是:上述“抗原的限定”项目中记载的条件下进行二维电泳时的凝胶中,作为分子量35kda~60kda、优选为分子量40kda~50kda附近以及等电点5.0~10.0、优选为6.0~9.0的斑点出现的蛋白质。
[0175]
(4)斑点4的抗原
[0176]
对于斑点4,利用质谱分析进行序列鉴定的结果,检测到了序列号48~57的氨基酸序列。
[0177]
另外,对于斑点4,将由质谱分析装置得到的质谱数据(序列号48~57)与ncbi的蛋白质数据进行对照并解析,鉴定为卵黄原蛋白-3(vitellogenin-3)(氨基酸序列:序列号47、编码其的碱基序列:序列号46)。
[0178]
因此,本技术中,斑点4的抗原为以下(4a-a)~(4a-e)和(4b)中的任一者。
[0179]
(4a-a)含有在序列号47中缺失、置换、插入或附加有1个或多个氨基酸的氨基酸序列的蛋白质。
[0180]
(4a-b)含有与序列号47所示的氨基酸序列的同一性为70%以上、优选为75%以上、80%以上、85%以上、90%以上、95%以上、97%以上、98%以上、99%以上的氨基酸序列的蛋白质。
[0181]
(4a-c)含有由在序列号46中缺失、置换、插入或附加有1个或多个核苷酸的碱基序列编码的氨基酸序列的蛋白质。
[0182]
(4a-d)含有由与序列号46所示的碱基序列的同一性为70%以上、优选为75%以上、80%以上、85%以上、90%以上、95%以上、97%以上、98%以上、99%以上的碱基序列编码的氨基酸序列的蛋白质。
[0183]
(4a-e)含有由下述核酸编码的氨基酸序列的蛋白质,所述核酸和由与序列号46所示的碱基序列互补的碱基序列构成的核酸在严格的条件下杂交。
[0184]
(4b)含有选自由序列号47~57组成的组中的氨基酸序列中的至少一种的蛋白质、优选为包含该氨基酸序列的至少2、3、4、5、6、7、8、9、10种或所有序列的蛋白质。进而优选:含有选自由序列号47、50、51、53和54组成的组中的氨基酸序列中的至少一种的蛋白质、优
选为包含该氨基酸序列的至少2、3、4种或所有序列的蛋白质。其中,序列号47~57中的任一者所示的氨基酸序列任选缺失、置换、插入或附加有1个或多个氨基酸。
[0185]
上述(4a-a)~(4a-e)和(4b)的蛋白质还可以是:上述“抗原的限定”项目中记载的条件下进行二维电泳时的凝胶中,作为分子量20kda~50kda、优选为分子量25kda~40kda、更优选为分子量30kda~35kda附近、以及等电点3.0~8.0、优选为3.5~7.0、进而优选为4.0~6.0的斑点出现的蛋白质。
[0186]
(5)斑点5和6的抗原
[0187]
对于斑点5和6,利用质谱分析进行序列鉴定的结果,检测到了序列号60~104的氨基酸序列。
[0188]
另外,对于斑点5和6,将由质谱分析装置得到的质谱数据(序列号60~104)与ncbi的蛋白质数据进行对照并解析,鉴定为卵黄原蛋白-2前体(vitellogenin-2 precursor)(氨基酸序列:序列号59、编码其的碱基序列:序列号58)。
[0189]
因此,本技术中,斑点5和6的抗原为以下(5a-a)~(5a-e)和(5b)中的任一者。
[0190]
(5a-a)含有在序列号59中缺失、置换、插入或附加有1个或多个氨基酸的氨基酸序列的蛋白质。
[0191]
(5a-b)含有与序列号59所示的氨基酸序列的同一性为70%以上、优选为75%以上、80%以上、85%以上、90%以上、95%以上、97%以上、98%以上、99%以上的氨基酸序列的蛋白质。
[0192]
(5a-c)含有由在序列号58中缺失、置换、插入或附加有1个或多个核苷酸的碱基序列编码的氨基酸序列的蛋白质。
[0193]
(5a-d)含有由与序列号58所示的碱基序列的同一性为70%以上、优选为75%以上、80%以上、85%以上、90%以上、95%以上、97%以上、98%以上、99%以上的碱基序列编码的氨基酸序列的蛋白质。
[0194]
(5a-e)含有由下述核酸编码的氨基酸序列的蛋白质,所述核酸和由与序列号58所示的碱基序列互补的碱基序列构成的核酸在严格的条件下杂交。
[0195]
(5b)含有选自由序列号59~104组成的组中的氨基酸序列中的至少一种的蛋白质、优选为包含该氨基酸序列的至少2、3、4、5、6、7、8、9、10、15、20、25、30、35、40、45种序列或所有序列的蛋白质。进而优选为:含有选自由序列号59、60、63、65、68、69、71、73、75~79、81、83~88、91~94、96~99和101~103组成的组中的氨基酸序列中的至少一种的蛋白质、优选为包含该氨基酸序列的至少2、3、4、5、6、7、8、9、10、15、20、25、30种或所有序列的蛋白质。其中,序列号59~104中的任一者所示的氨基酸序列任选缺失、置换、插入或附加有1个或多个氨基酸。
[0196]
上述(5a-a)~(5a-e)和(5b)的蛋白质还可以是:上述“抗原的限定”项目中记载的条件下进行二维电泳时的凝胶中,作为分子量80kda~260kda、优选为分子量90kda~200kda、更优选为分子量110kda~160kda附近、以及等电点1.0~8.0、优选为2.0~7.0、进而优选为3.0~6.0的斑点出现的蛋白质。
[0197]
(6)斑点7的抗原
[0198]
对于斑点7,利用质谱分析进行序列鉴定的结果,检测到了序列号107~150的氨基酸序列。
[0199]
另外,对于斑点7,将由质谱分析装置得到的质谱数据(序列号107~150)与ncbi的蛋白质数据进行对照并解析,鉴定为卵黄原蛋白-2前体(vitellogenin-2 precursor)(氨基酸序列:序列号106、编码其的碱基序列:序列号105)。
[0200]
因此,本技术中,斑点7的抗原为以下(6a-a)~(6a-e)和(6b)中的任一者。
[0201]
(6a-a)含有在序列号106中缺失、置换、插入或附加有1个或多个氨基酸的氨基酸序列的蛋白质。
[0202]
(6a-b)含有与序列号106所示的氨基酸序列的同一性为70%以上、优选为75%以上、80%以上、85%以上、90%以上、95%以上、97%以上、98%以上、99%以上的氨基酸序列的蛋白质。
[0203]
(6a-c)含有由在序列号105中缺失、置换、插入或附加有1个或多个核苷酸的碱基序列编码的氨基酸序列的蛋白质。
[0204]
(6a-d)含有由与序列号105所示的碱基序列的同一性为70%以上、优选为75%以上、80%以上、85%以上、90%以上、95%以上、97%以上、98%以上、99%以上的碱基序列编码的氨基酸序列的蛋白质。
[0205]
(6a-e)含有由下述核酸编码的氨基酸序列的蛋白质,所述核酸和由与序列号105所示的碱基序列互补的碱基序列构成的核酸在严格的条件下杂交。
[0206]
(6b)含有选自由序列号106~150组成的组中的氨基酸序列中的至少一种的蛋白质、优选为包含该氨基酸序列的至少2、3、4、5、6、7、8、9、10、15、20、25、30、35、40、44种序列或所有序列的蛋白质。进而优选为:含有选自由序列号106、108、110、111、113、114、116、117、120~124、126~131、133、134、136~138、140~143、145~147和149组成的组中的氨基酸序列中的至少一种的蛋白质、优选为包含该氨基酸序列的至少2、3、4、5、6、7、8、9、10、15、20、25、30、31种或所有序列的蛋白质。其中,序列号106~150中的任一者所示的氨基酸序列任选缺失、置换、插入或附加有1个或多个氨基酸。
[0207]
上述(6a-a)~(6a-e)和(6b)的蛋白质还可以是:上述“抗原的限定”项目中记载的条件下进行二维电泳时的凝胶中,作为分子量110kda~300kda、优选为分子量130kda~280kda、更优选为分子量160kda~260kda附近、以及等电点3.0~8.0、优选为3.5~7.0、进而优选为4.0~6.0的斑点出现的蛋白质。
[0208]
(7)斑点8的抗原
[0209]
对于斑点8,利用质谱分析进行序列鉴定的结果,检测到了序列号153~235的氨基酸序列。
[0210]
另外,对于斑点8,将由质谱分析装置得到的质谱数据(序列号153~235)与ncbi的蛋白质数据进行对照并解析,鉴定为载脂蛋白b前体(apolipoprotein b precursor)(氨基酸序列:序列号152、编码其的碱基序列:序列号151)。
[0211]
因此,本技术中,斑点8的抗原为以下(7a-a)~(7a-e)和(7b)中的任一者。
[0212]
(7a-a)含有在序列号152中缺失、置换、插入或附加有1个或多个氨基酸的氨基酸序列的蛋白质。
[0213]
(7a-b)含有与序列号152所示的氨基酸序列的同一性为70%以上、优选为75%以上、80%以上、85%以上、90%以上、95%以上、97%以上、98%以上、99%以上的氨基酸序列的蛋白质。
[0214]
(7a-c)含有由在序列号151中缺失、置换、插入或附加有1个或多个核苷酸的碱基序列编码的氨基酸序列的蛋白质。
[0215]
(7a-d)含有由与序列号151所示的碱基序列的同一性为70%以上、优选为75%以上、80%以上、85%以上、90%以上、95%以上、97%以上、98%以上、99%以上的碱基序列编码的氨基酸序列的蛋白质。
[0216]
(7a-e)含有由下述核酸编码的氨基酸序列的蛋白质,所述核酸和由与序列号151所示的碱基序列互补的碱基序列构成的核酸在严格的条件下杂交。
[0217]
(7b)含有选自由序列号152~235组成的组中的氨基酸序列中的至少一种的蛋白质、优选为包含该氨基酸序列的至少2、3、4、5、6、7、8、9、10、15、20、25、30、35、40、45、50、55、60、65、70、75、80、83种序列或所有序列的蛋白质。进而优选为:含有选自由序列号152、154、157~160、163、164、167~172、174、175、177、178、180、182~185、187、189、190、192、194~196、198~200、203~207、209、211、212、214~216、220~229、231和232组成的组中的氨基酸序列中的至少一种的蛋白质、优选为包含该氨基酸序列的至少2、3、4、5、6、7、8、9、10、15、20、25、30、35、40、45、50、55种或所有序列的蛋白质。其中,序列号152~235中的任一者所示的氨基酸序列任选缺失、置换、插入或附加有1个或多个氨基酸。
[0218]
上述(7a-a)~(7a-e)和(7b)的蛋白质还可以是:上述“抗原的限定”项目中记载的条件下进行二维电泳时的凝胶中,作为分子量160kda~550kda、优选为分子量180kda~400kda、更优选为分子量200kda~300kda附近、以及等电点3.0~8.0、优选为3.5~7.0、进而优选为4.0~6.0的斑点出现的蛋白质。
[0219]
(8)斑点9的抗原
[0220]
对于斑点9,利用质谱分析进行序列鉴定的结果,检测到了序列号238~249的氨基酸序列。
[0221]
另外,对于斑点9,将由质谱分析装置得到的质谱数据(序列号238~249)与ncbi的蛋白质数据进行对照并解析,鉴定为载脂蛋白b前体(apolipoprotein b precursor)(氨基酸序列:序列号237、编码其的碱基序列:序列号236)。
[0222]
因此,本技术中,斑点9的抗原为以下(8a-a)~(8a-e)和(8b)中的任一者。
[0223]
(8a-a)含有在序列号237中缺失、置换、插入或附加有1个或多个氨基酸的氨基酸序列的蛋白质。
[0224]
(8a-b)含有与序列号237所示的氨基酸序列的同一性为70%以上、优选为75%以上、80%以上、85%以上、90%以上、95%以上、97%以上、98%以上、99%以上的氨基酸序列的蛋白质。
[0225]
(8a-c)含有由在序列号236中缺失、置换、插入或附加有1个或多个核苷酸的碱基序列编码的氨基酸序列的蛋白质。
[0226]
(8a-d)含有由与序列号236所示的碱基序列的同一性为70%以上、优选为75%以上、80%以上、85%以上、90%以上、95%以上、97%以上、98%以上、99%以上的碱基序列编码的氨基酸序列的蛋白质。
[0227]
(8a-e)含有由下述核酸编码的氨基酸序列的蛋白质,所述核酸和由与序列号236所示的碱基序列互补的碱基序列构成的核酸在严格的条件下杂交。
[0228]
(8b)含有选自由序列号237~249组成的组中的氨基酸序列中的至少一种的蛋白
质、优选为包含该氨基酸序列的至少2、3、4、5、6、7、8、9、10、11、12种或所有序列的蛋白质。进而优选:含有选自由序列号237~239、241、242、244和246~249组成的组中的氨基酸序列中的至少一种的蛋白质、优选为包含该氨基酸序列的至少2、3、4、5、6、7、8、9种或所有序列的蛋白质。其中,序列号237~249中的任一者所示的氨基酸序列任选缺失、置换、插入或附加有1个或多个氨基酸。
[0229]
上述(8a-a)~(8a-e)和(8b)的蛋白质还可以是:上述“抗原的限定”项目中记载的条件下进行二维电泳时的凝胶中,作为分子量20kda~50kda、优选为分子量25kda~45kda、更优选为分子量30kda~40kda附近、以及等电点7.0~11.0、优选为8.0~10.0、进而优选为9.0~10.0的斑点出现的蛋白质。
[0230]
(9)斑点10的抗原
[0231]
对于斑点10,利用质谱分析进行序列鉴定的结果,检测到了序列号252~260的氨基酸序列。
[0232]
另外,对于斑点10,将由质谱分析装置得到的质谱数据(序列号252~260)与ncbi的蛋白质数据进行对照并解析,鉴定为载脂蛋白b前体(apolipoprotein b precursor)(氨基酸序列:序列号251、编码其的碱基序列:序列号250)。
[0233]
因此,本技术中,斑点10的抗原为以下(9a-a)~(9a-e)和(9b)中的任一者。
[0234]
(9a-a)含有在序列号251中缺失、置换、插入或附加有1个或多个氨基酸的氨基酸序列的蛋白质。
[0235]
(9a-b)含有与序列号251所示的氨基酸序列的同一性为70%以上、优选为75%以上、80%以上、85%以上、90%以上、95%以上、97%以上、98%以上、99%以上的氨基酸序列的蛋白质。
[0236]
(9a-c)含有由在序列号250中缺失、置换、插入或附加有1个或多个核苷酸的碱基序列编码的氨基酸序列的蛋白质。
[0237]
(9a-d)含有由与序列号250所示的碱基序列的同一性为70%以上、优选为75%以上、80%以上、85%以上、90%以上、95%以上、97%以上、98%以上、99%以上的碱基序列编码的氨基酸序列的蛋白质。
[0238]
(9a-e)含有由下述核酸编码的氨基酸序列的蛋白质,所述核酸和由与序列号250所示的碱基序列互补的碱基序列构成的核酸在严格的条件下杂交。
[0239]
(9b)含有选自由序列号251~260组成的组中的氨基酸序列中的至少一种的蛋白质、优选为包含该氨基酸序列的至少2、3、4、5、6、7、8、9种或所有序列的蛋白质。进而优选:含有选自由序列号251~254、256、257和260组成的组中的氨基酸序列中的至少一种的蛋白质、优选为包含该氨基酸序列的至少2、3、4、5、6种或所有序列的蛋白质。其中,序列号251~260中的任一者所示的氨基酸序列任选缺失、置换、插入或附加有1个或多个氨基酸。
[0240]
上述(9a-a)~(9a-e)和(9b)的蛋白质还可以是:上述“抗原的限定”项目中记载的条件下进行二维电泳时的凝胶中,作为分子量20kda~50kda、优选为分子量25kda~45kda、更优选为分子量30kda~40kda附近、以及等电点7.0~11.0、优选为8.0~10.0、进而优选为9.0~10.0的斑点出现的蛋白质。
[0241]
(10)斑点11的抗原
[0242]
对于斑点11,利用质谱分析进行序列鉴定的结果,检测到了序列号263~271的氨
基酸序列。
[0243]
另外,对于斑点11,将由质谱分析装置得到的质谱数据(序列号263~271)与ncbi的蛋白质数据进行对照并解析,鉴定为卵黄原蛋白-2前体(vitellogenin-2precursor)(氨基酸序列:序列号262、编码其的碱基序列:序列号261)。
[0244]
因此,本技术中,斑点11的抗原为以下(10a-a)~(10a-e)和(10b)中的任一者。
[0245]
(10a-a)含有在序列号262中缺失、置换、插入或附加有1个或多个氨基酸的氨基酸序列的蛋白质。
[0246]
(10a-b)含有与序列号262所示的氨基酸序列的同一性为70%以上、优选为75%以上、80%以上、85%以上、90%以上、95%以上、97%以上、98%以上、99%以上的氨基酸序列的蛋白质。
[0247]
(10a-c)含有由在序列号261中缺失、置换、插入或附加有1个或多个核苷酸的碱基序列编码的氨基酸序列的蛋白质。
[0248]
(10a-d)含有由与序列号261所示的碱基序列的同一性为70%以上、优选为75%以上、80%以上、85%以上、90%以上、95%以上、97%以上、98%以上、99%以上的碱基序列编码的氨基酸序列的蛋白质。
[0249]
(10a-e)含有由下述核酸编码的氨基酸序列的蛋白质,所述核酸和由与序列号261所示的碱基序列互补的碱基序列构成的核酸在严格的条件下杂交。
[0250]
(10b)含有选自由序列号262~271组成的组中的氨基酸序列中的至少一种的蛋白质、优选为包含该氨基酸序列的至少2、3、4、5、6、7、8、9种或所有序列的蛋白质。进而优选:含有选自由序列号262~265、268和269组成的组中的氨基酸序列中的至少一种的蛋白质、优选为包含该氨基酸序列的至少2、3、4、5种或所有序列的蛋白质。其中,序列号262~271中的任一者所示的氨基酸序列任选缺失、置换、插入或附加有1个或多个氨基酸。
[0251]
上述(10a-a)~(10a-e)和(10b)的蛋白质还可以是:上述“抗原的限定”项目中记载的条件下进行二维电泳时的凝胶中,作为分子量15kda~40kda、优选为分子量17kda~35kda、更优选为分子量20kda~30kda附近、以及等电点6.0~11.0、优选为7.0~10.0、进而优选为8.0~10.0的斑点出现的蛋白质。
[0252]
上述(1)~(3)、(4)~(10)的作为抗原的蛋白质中还包含有:该蛋白质的氨基酸残基通过磷酸化、糖链修饰、氨基酰化、开环、脱氨基化等被修饰而成的蛋白质。
[0253]
优选的是,上述(1)~(3)、(4)~(10)的作为抗原的蛋白质是蛋变态反应的抗原。
[0254]
本说明书中,氨基酸序列中,“缺失、置换、插入或附加有1个或多个氨基酸”这样的情况是指:在成为对象的氨基酸序列中,缺失有1个或多个氨基酸(例如,相对于氨基酸序列的全长为30%、优选为25%、20%、15%、10%、5%、3%、2%或1%的氨基酸)、或者置换为其他氨基酸、或者插入有其他氨基酸、和/或附加其他氨基酸而成的氨基酸序列。
[0255]
上述中,置换优选为保守的置换。保守的置换是指将特定的氨基酸残基用具有類似物理化学特征的残基进行置换;只要是不使原序列结构相关的特征实质上变化就可以为任意的置换,例如,置换氨基酸只要不破坏原序列中存在的螺旋、或者不破坏作为原序列特征的其他种类的二次结构就可以为任意的置换。以下,关于氨基酸残基的保守的置换,根据能够置换的残基分类而例示,但作为能够置换的氨基酸残基不限定于以下记载的物质。
[0256]
a组:亮氨酸、异亮氨酸、缬氨酸、丙氨酸、蛋氨酸
[0257]
b组:天冬氨酸、谷氨酸
[0258]
c组:天冬酰胺、谷氨酰胺
[0259]
d组:赖氨酸、精氨酸
[0260]
e组:丝氨酸、苏氨酸
[0261]
f组:苯丙氨酸、酪氨酸
[0262]
非保守的置换的情况下,也可以将上述种类中的、某一个成员替换为其他种类成员。例如,为了排除预料之外的糖链修饰,也可以将上述b、d、e组的氨基酸置换成除此以外组的氨基酸。或者,为了防止三维结构的蛋白质中被折叠,可以缺失半胱氨酸或者置换为其他氨基酸。或者,为了保持亲水性/疏水性平衡,或者为了容易地进行合成,为了提高亲水度而考虑与氨基酸相关的作为疏水性/亲水性指标的氨基酸的亲水指数(hydropathy index)(j.kyte和r.doolittle,j.mol.biol.,vol.157,p.105-132,1982),也可以置换氨基酸。
[0263]
本说明书中,2个氨基酸序列的同一性%可以通过视觉的检查和数学计算来确定。另外,也可以使用计算机程序确定同一性%。作为这样的计算机程序,可列举出例如:blast和clustalw等。特别是,利用blast程序进行的同一性检索的各种条件(参数)可以按照altschul等(nucl.acids.res.,25,p.3389-3402,1997)记载的、从美国国立生物技术信息中心(ncbi)、dna data bank of japan(ddbj)网站等公开得到(blast手册、altschul等ncb/nlm/nih bethesda,md 20894;altschul等)。另外,也可以使用遗传信息处理软件genetyx ver.7(genetyx)、dinasis pro(hitachi soft,ltd.)、vector nti(infomax)等程序来决定。
[0264]
本说明书中,碱基序列中,“缺失、置换、插入或附加有1个或多个核苷酸”这样的情况是指:在成为对象的碱基序列中,缺失有1个或多个核苷酸(例如,相对于碱基序列的全长为30%、优选为25%、20%、15%、10%、5%、3%、2%或1%的氨基酸)、或者置换为其他核苷酸、或者插入有其他核苷酸、和/或附加其他核苷酸而成的碱基序列。通过上述核苷酸的缺失、置换、插入或附加,优选在编码氨基酸的序列中不产生移码。
[0265]
本说明书中,2个碱基序列的同一性%可以通过视觉的检查和数学计算来确定。另外,也可以使用计算机程序确定同一性%。作为这样的序列比较计算机程序,可以使用例如:从美国国立医学图书馆的网站:https://blast.ncbi.nlm.nih.gov/blast.cgi能够利用的blastn程序(altschul et al.(1990)j.mol.biol.215:403-10),并使用默认参数(default parameter)来确定。
[0266]
本说明书中“严格条件下”是指中等程度或高度严格的条件下进行杂交。具体而言,作为中等程度严格的条件,例如可以由具有一般技术的本领域技术人员基于dna的长度容易地决定。基本的条件如sambrook等,molecular cloning:a laboratory manual,第3版,第6-7章,cold spring harbor laboratory press,2001所示。优选的是,中等程度严格的条件作为杂交条件可列举出:1
×
ssc~6
×
ssc、42℃~55℃的条件;更优选为1
×
ssc~3
×
ssc、45℃~50℃的条件;最优选为2
×
ssc、50℃的条件。杂交溶液中包含例如约50%甲酰胺的情况下,可以采用比上述温度低5~15℃的温度。洗涤条件可列举出:0.5
×
ssc~6
×
ssc、40℃~60℃。在杂交和洗涤时,通常加入0.05%~0.2%、优选约0.1%sds。作为高度严格的条件,还可以例如由本领域技术人员基于dna的长度容易地决定。通常,作为高度严格(high stringent)的条件,包括比中等程度严格的条件温度更高和/或盐浓度更低的杂交
和/或洗涤。例如,作为杂交条件,可列举出:0.1
×
ssc~2
×
ssc、55℃~65℃的条件;更优选为0.1
×
ssc~1
×
ssc、60℃~65℃的条件;最优选为0.2
×
ssc、63℃的条件。作为洗涤条件,可列举出:0.2
×
ssc~2
×
ssc、50℃~68℃、更优选为0.2
×
ssc、60~65℃。
[0267]
抗原也可以通过组合本领域技术人员公知的蛋白质纯化方法由蛋(优选为鸡蛋)进行分离/纯化来得到。或者,抗原也可以通过本领域技术人员公知的基因重组技术表达抗原作为重组蛋白质,然后通过本领域技术人员公知的蛋白质纯化方法进行分离/纯化来得到。
[0268]
作为蛋白质的纯化方法,可列举出例如:盐析、溶剂沉淀法等利用溶解度的方法;透析、超滤、凝胶过滤、sds-page等利用分子量的差的方法;离子交换色谱、羟磷灰石色谱等利用荷电的方法;亲和色谱等利用特异的亲和性的方法;反相高效液相色谱等利用疏水性的差的方法;等电点电泳等利用等电点的差的方法等。
[0269]
利用基因重组技术制备蛋白质可以如下进行:制备包含编码抗原的核酸的表达载体,将该表达载体通过基因导入或转化导入至适宜的宿主细胞中,在适合于重组蛋白质表达的条件下培养该宿主细胞,然后对该宿主细胞中表达的重组蛋白质进行回收。
[0270]“载体”是能够用于将与之连接的核酸导入宿主细胞内的核酸;“表达载体”是能够引导被载体导入的核酸所编码的蛋白质表达的载体。作为载体包括质粒载体、病毒载体等。本领域技术人员可以根据使用的宿主细胞的种类选择适合于重组蛋白质表达的表达载体。
[0271]“宿主细胞”是通过载体进行了基因导入或接受了转化的细胞。宿主细胞可以由本领域技术人员根据使用的载体适宜选择。宿主细胞可以来自例如大肠杆菌(e.coli)等原核生物。使用大肠杆菌这样的原核细胞作为宿主时,为了使原核细胞内的重组蛋白质的表达变得容易,本发明的抗原优选包含n末端蛋氨酸残基。该n末端蛋氨酸也可以在表达后从重组蛋白质切离。或者,可以是酵母等单细胞真核生物;植物细胞、动物细胞(例如,人细胞、猿猴细胞、仓鼠细胞、大鼠细胞、小鼠细胞或昆虫细胞)等来自真核生物的细胞、蚕。
[0272]
表达载体向宿主细胞的基因导入或转化可以通过本领域技术人员公知的方法适宜进行。另外,本领域技术人员会根据宿主细胞的种类适宜选择适合于表达重组蛋白质的条件来培养宿主细胞,从而能够表达重组蛋白质。然后,对表达重组蛋白质的宿主细胞进行均质化处理,对由得到的均质混合物纯化成上述蛋白质的方法进行适宜组合,由此能够分离/纯化作为重组蛋白质表达的抗原。
[0273]
诊断试剂盒/诊断方法
[0274]
本发明是提供用于诊断对象的蛋变态反应的指标的方法,其包括以下的工序:
[0275]
(i)使由对象得到的试样与抗原接触,此处,该试样是包含有ige抗体的溶液;
[0276]
(ii)对由对象得到的试样中的ige抗体与该抗原的结合进行检测;
[0277]
(iii)检测到对象ige抗体与该抗原结合时,提供对象为蛋变态反应的指标;
[0278]
此处,该抗原为作为上述(1)~(3)、(4)~(10)的抗原而限定的蛋白质的至少一种。
[0279]
由对象得到的试样是指包含有由对象采集的ige抗体的溶液。这样的溶液中包含有例如血液、唾液、痰、鼻涕、尿、汗、泪。在与抗原接触之前,也可以对由对象得到的试样实施用于提高试样中ige抗体浓度的前处理。作为试样的前处理,也可以包括例如由血液得到血清、血浆。另外,也可以进一步对作为与抗原结合部分的fab部分进行纯化。在特别优选的
方式中,上述工序(i)通过使由对象得到的血清中的ige抗体与抗原接触来进行。
[0280]
ige抗体可以是ige抗体自身,也可以是ige抗体所结合的肥大细胞等。
[0281]
由对象得到的试样与抗原的接触以及它们的结合的检测可以通过已知的方法来进行。作为这样的方法,可以使用利用例如:elisa(酶联免疫吸附试验,enzyme-linked immunosorvent assay)、夹层免疫测定法(sandwich immunoassays)、蛋白质免疫印迹法、免疫沉淀法、免疫层析法进行的检测。这些均是使抗原与对象ige抗体接触而结合,使之作用于对于与抗原特异地结合的ige抗体进行酶标记而成的二次抗体,加入酶的底物(通常为显色或发光试剂)而检测出酶反应的产物,由此能够检测抗原与对象ige抗体结合的方法。或者为检测被荧光标记的二次抗体的方法。或者,也可以使用表面等离子共振(spr)等能够评价抗原与ige抗体结合的测定方法进行检测。也可以混合多种抗原特异的ige抗体。
[0282]
抗原也可以是分离的抗原被固定于载体的状态。该情况下,上述工序(i)和(ii)中可以利用elisa、夹层免疫测定法、免疫层析法、表面等离子共振;另外,上述工序(i)中,由对象得到的试样与固定了抗原的面接触来进行。所分离的抗原可以通过组合本领域技术人员公知的蛋白质纯化方法由蛋(优选为鸡蛋)分离/纯化来得到,或者也可以通过基因重组技术来制备。另外,也可以是抗体被固定的状态。
[0283]
抗原也可以是被固定于载体的状态。该情况下,在上述工序(i)和(ii)中,可以利用流式细胞仪等,可以通过激光确认结合有抗体的抗原的存在。可列举出例如嗜碱性粒细胞激活试验(bat)等。另外,也可列举出通过使抗原与试样中的血细胞进一步接触来确认是否使组胺游离的组胺游离试验(hrt)。
[0284]
另外,抗原也可以由通过二维电泳分离的状态转印、通过蛋白质免疫印迹进行检测。二维电泳通过第一维进行等电点电泳、第二维进行sds-page(sds-聚丙烯酰胺凝胶电泳),由此分离蛋白质试样的方法。该情况下,二维电泳的条件只要是能够分离本发明抗原的条件就没有特别的限定。例如,可以利用上述“抗原的限定”项目中记载的二维电泳的条件。或者,也可以参考上述专利文献1~4的记载设定电泳条件,例如,满足选自由以下组成的组中的至少一个条件下进行二维电泳:
[0285]
(a)作为第一维等电点电泳凝胶,在凝胶长度为5~10cm的范围内且凝胶的ph范围为3~10、将相对于泳动方向的凝胶的ph梯度直至ph5为止的凝胶长度设为a、ph5~7的凝胶长度设为b、ph7以上的凝胶长度设为c的情况下,满足“a<b”和“b>c”的关系;
[0286]
(b)在(a)的情况下,将凝胶的全长设为1时,a为0.15~0.3的范围内、b为0.4~0.7的范围内、c为0.15~0.3的范围内;
[0287]
(c)在第一维的等电点电泳中,对于每1根包含被检体的凝胶施加100v~600v范围内值的恒定电压进行恒定电压工序,在每泳动30分钟的泳动变化幅度为5μa范围内之后,开始由前述恒定电压使电压上升的电压上升工序;
[0288]
(d)在(c)的情况下,将电压上升工序的最终电压设为3000v~6000v的范围内;
[0289]
(e)第一维等电点电泳凝胶的长边方向的凝胶长度设为5~10cm、第二维电泳凝胶的泳动方向基端部的凝胶浓度设为3~6%;以及
[0290]
(f)在(e)的情况下,将第二维电泳凝胶的泳动方向前端侧部分的凝胶浓度设定为高于泳动方向基端部的凝胶浓度。
[0291]
上述(1)~(3)、(4)~(10)的抗原为与蛋变态反应患者的ige抗体特异结合的抗
原。因此,检测到对象的ige抗体与该抗原结合的情况下,提供对象为蛋变态反应的指标。
[0292]
本发明还提供包含上述(1)~(3)、(4)~(10)的抗原的至少一种的蛋变态反应的诊断试剂盒。本发明的诊断试剂盒可以在上述提供用于诊断蛋变态反应指标的方法或下述诊断方法中应用。本发明的诊断试剂盒除了包含上述(1)~(3)、(4)~(10)的抗原的至少一种之外,还可以包含被酶标记的抗ige抗体以及成为该酶底物的显色底物或发光底物。另外,也可以使用被荧光标记的抗ige抗体。本发明的诊断试剂盒中,也可以以抗原被固定化于载体的状态提供。本发明的诊断试剂盒还可以与关于用于诊断的步骤的说明书、包含该说明的方法包一起提供。
[0293]
在另外的方式中,上述的診断试剂盒包含:蛋变态反应的伴侣诊断药物。伴侣诊断药物是指用于以下用途的物质:期待医药品效果的患者的特定或医药品的具有重度副作用风险的患者的特定、或者为了最优化使用了医药品的治疗而研究该医药品的反应性。此处,治疗的最优化包括例如:用法容量的确定、给药中止的判断、使用何种变应原成分来确认是否获得免疫耐受。
[0294]
本发明还提供包含上述(1)~(3)、(4)~(10)抗原的至少一种的蛋变态反应的诊断用组合物。本发明的诊断用组合物可以用于下述的诊断方法中。本发明的诊断用组合物还可以根据需要包含通常与本发明的抗原一起使用的、药学上允许的载体、添加剂。
[0295]
一方式中,本发明为诊断对象的蛋变态反应的方法,其包括以下工序:
[0296]
(i)使由对象得到的试样与抗原接触;
[0297]
(ii)对由对象得到的试样中的ige抗体与该抗原的结合进行检测;
[0298]
(iii)检测到对象的ige抗体与该抗原结合的情况下,判断对象为蛋变态反应;
[0299]
此处,该抗原为作为上述(1)~(3)、(4)~(10)的抗原而限定的蛋白质的至少一种。其中,(i)和(ii)的各工序按照对于提供用于诊断蛋变态反应指标的方法的各工序的说明来进行。
[0300]
在另一个方式中,本发明提供诊断对象的蛋变态反应的方法,其包括对对象给予上述(1)~(3)、(4)~(10)的抗原的至少一种。该方法也可以以特征在于对皮肤施用抗原的皮肤测试的形式进行。皮肤测试中包含如下形式:对皮肤上施用诊断用组合物之后、以不出血程度地轻微抓伤,使皮肤浸透抗原再观察皮肤反应的点刺试验(prick test);施用了诊断用组合物的基础上轻挠皮肤再观察反应的划痕试验(scratch test);对皮肤施用霜、软膏等形式的诊断用组合物再观察反应的肤斑试验(patch test);对皮内给予抗原再观察反应的皮内测试;等。在施用了抗原部分的皮肤出现肿胀等皮肤反应的情况下,诊断为该对象具有蛋变态反应。此处,对皮肤施用的抗原的量也可以为例如每1次100μg以下的用量。
[0301]
在变态反应的诊断中,经常进行的是以限定抗原为目的的负荷试验。上述(1)~(3)、(4)~(10)的抗原的至少一种可以作为诊断蛋变态反应的负荷试验的有效成分来使用。此处,作为负荷试验中使用的抗原蛋白质,可以为表达纯化的蛋白质,也可以为例如在稻子中转化杉木花粉抗原的基因,并且在米内使该抗原蛋白质表达的花粉米那样的、在食品/食材中表达的蛋白质。
[0302]
另外,在另一个方式中,本发明提供蛋变态反应的诊断中使用的上述(1)~(3)、(4)~(10)的抗原的至少一种。此处,也包含将上述(1)~(3)、(4)~(10)抗原的至少一种与已知的抗原混合来提供。
[0303]
进而在另一个实施方式中,本发明提供上述(1)~(3)、(4)~(10)的抗原的至少一种在制备蛋变态反应的诊断药物中的应用。
[0304]
药物组合物/治疗方法
[0305]
本发明提供包含上述(1)~(3)、(4)~(10)的抗原的至少一种的药物组合物。
[0306]
一个方式中,上述的药物组合物用于治疗蛋变态反应。
[0307]
本发明还提供治疗蛋变态反应的方法,其包括:对于需要治疗蛋变态反应的患者,给予上述(1)~(3)、(4)~(10)的抗原的至少一者。
[0308]
在另一个方式中,本发明提供蛋变态反应的治疗中使用的上述(1)~(3)、(4)~(10)的抗原的至少一种。进而在另一个实施方式中,本发明提供上述(1)~(3)、(4)~(10)的抗原的至少一种在制备蛋变态反应的治疗药物中的应用。
[0309]
在变态反应的治疗中,经常进行的是目的在于通过对患者给予抗原来诱导免疫耐受的、脱敏治疗法。上述(1)~(3)、(4)~(10)的抗原的至少一种可以作为治疗蛋变态反应的脱敏治疗法的有效成分来使用。此处,作为脱敏治疗法中使用的抗原蛋白质,可以为表达纯化的蛋白质,也可以为例如在稻子中转化杉木花粉抗原的基因,并且在米内使该抗原蛋白质表达的花粉米那样的、在食品/食材中表达的蛋白质。
[0310]
本发明的药物组合物可以通过通常的给药途径进行给药。通常的给药途径包括例如:经口、舌下、经皮、皮内、皮下、血液内、鼻腔内、肌肉内、腹腔内、直肠内的给药。
[0311]
本发明的药物组合物可以使用根据需要与本发明的抗原一起通过常规方法添加了通常使用的药学上允许的佐剂、赋形剂、或者各种添加剂(例如稳定剂、助溶剂、乳浊化剂、缓冲剂、储存剂、着色剂等)而成的药物组合物。药物组合物的剂型可以由本领域技术人员根据给药途径而适宜选择。也可以是例如:片剂、胶囊剂、糖浆剂、舌下片、注射剂、鼻腔内喷雾剂、膏剂、溶液剂、霜剤、露剂等形式。本发明的药物组合物的给药量、给药次数和/或给药期间可以由医师根据给药途径、症状、年龄、体重等患者的特性等适宜选择。例如是成人的情况下,也可以以每1次100μg以下的用量给药。给药间隔可以是例如每天1次、每周1次、每月2次或者3个月1次左右。给药期间可以为例如数周~数年。在给药期间内,也可以是梯度地增加给药量的给药方法。
[0312]
检测仪
[0313]
本发明提供一种检测仪,其包含针对上述(1)~(3)、(4)~(10)的抗原的至少一种的抗体。
[0314]
该抗体可以通过常规方法来制作。例如,对兔子等哺乳动物用上述(1)~(3)、(4)~(10)的抗原进行免疫来制作。该抗体可以为ige抗体、多克隆抗体、单克隆抗体、或者它们的抗原结合片段(例如、fab、f(ab’)2、fab’)。
[0315]
另外,上述检测仪中,该抗体可以以与载体结合的形式提供。载体只要是在抗体与抗原结合的检测中能够利用的载体,就没有特别的限定。可以利用本领域技术人员公知的任意载体。
[0316]
作为用于检查是否含有抗原的方法,可列举出例如以下的方法。
[0317]
·
使包含制作的ige抗体的检测仪与由食品/食材等得到的试样接触,例如使用elisa法等检测该ige抗体与试样中的抗原的结合,在检测到该ige抗体与抗原结合的情况下,判断为对象食品/食材等中残留有该抗原的方法等。
[0318]
·
使滤纸等包裹食品/食材,使之与抗体溶液反应来检测其中所包含的抗原的方法。
[0319]
本发明另外的实施方式中包含用于判断对象物中有无蛋变态反应的抗原的检测仪,其特征在于,其包含具有与序列号1、12、17、46、58、105、151、236、250或261所示的碱基序列的至少一个部分互补的碱基序列的引物。非限定地,上述引物具有例如:与序列号1、12、17、46、58、105、151、236、250或261所示的碱基序列的至少一个序列的一部分3’末端或中央部分的序列的、优选12个碱基、15个碱基、20个碱基、25个碱基互补的碱基序列。特别是在将mrna作为对象的情况下,具有poly(a)tail(多腺嘌呤尾)的互补引物。在优选的方式中,包含上述引物的检测仪进一步包含含有序列号1、12、17、46、58、105、151、236、250或261所示的碱基序列的至少一个序列的5’末端部分的碱基序列、优选由12个碱基、15个碱基、20个碱基、25个碱基构成的碱基序列的引物。
[0320]
例如,以由蛋或鸟得到的dna或mrna作为模板、使用所述互补的引物,用包含rt-pcr的pcr(聚合酶链式反应,polymerase chain reaction)对cdna进行扩增,将所扩增的cdna的序列与序列号1、12、17、46、58、105、151、236、250或261进行比较,从而判断抗原的有无。用pcr进行扩增的方法可例示出race法等。此时,在扩增的cdna与序列号1、12、17、46、58、105、151、236、250或261的比较中,编码相同氨基酸的点突变存在的情况下;或者、扩增的cdna的碱基序列中即便存在有对于序列号1、12、17、46、58、105、151、236、250或261的碱基序列的碱基插入、缺失、置换或添加时,编码该cdna的氨基酸序列相对于序列号2、13、18、47、59、106、152、237、251或262的氨基酸序列的同一性为70%以上、优选为80、90、95、98、99%以上时,判断为抗原存在。
[0321]
一个方式中,上述检测仪可以用来检测在食材(蛋或鸟)中或食品生产线中等对象物中是否含有抗原。上述检测仪可以由制造业者用在生产线和出厂前产品的质量检查;也可以由品尝者自己用来检查对象食品/食材是否含有抗原。
[0322]
去除抗原的食品等
[0323]
本发明提供特征在于去除或降低了上述(1)~(3)、(4)~(10)的抗原的至少一种的蛋、蛋加工品或者产生该蛋或由该蛋孵化的鸟。
[0324]
对于蛋、蛋加工品或者产生该蛋或由该蛋孵化的鸟而言,对于本发明的去除或降低抗原的方法没有限定。抗原的去除或降低不限定于本发明抗原的去除或降低,可以使用任意的方法来进行。
[0325]
例如,去除或降低了本发明抗原的蛋可以使用基因敲除技术来制备本发明的抗原的表达被敲除了的蛋。
[0326]
基因敲除技术可以使用本领域技术人员公知的方法的任一项。例如,oishi,et al.(scientific reports,vol.6,article number:23980,2016,doi:10.1038/srep23980)记载了作为基因组编辑技术的、将crisper/cas9应用于鸡的原始生殖细胞,从而得到卵类黏蛋白(ovomucoid)基因缺失个体。也可以利用同样的方法得到本发明的去除了抗原的蛋。另外,也可以与不含有抗原或抗原含量少的鸟或蛋通过人工授精进行交配,从而得到本发明的去除/降低了抗原的鸟或蛋。鸟或蛋的人工交配可以通过常规方法进行。
[0327]
本发明的去除或降低了抗原的蛋加工品也可以是以去除或降低了本发明抗原的蛋作为原料的加工品。将通常的蛋作为原料的情况下,在蛋加工品的制备前或制备后进行
本发明的去除或降低抗原的处理。在以通常的蛋作为原料的蛋加工品中,作为本发明的去除或降低抗原的方法,可列举出:高压处理和利用中性盐溶液的洗脱、高温蒸汽等去除食品/食材中的蛋白质成分的方法;通过热处理和酸处理进行水解、变性、氨基酸变性(侧链的化学修饰/脱离等)的方法。
[0328]
本发明的去除或降低了抗原的鸟也可以是由去除或降低了本发明抗原的蛋孵化、成长的鸟。鸟包括雏鸟、幼鸟、少鸟、成鸟和老鸟的各成长阶段的鸟。本说明书中,鸟是指属于鸟类的动物、优选为鸡。
[0329]
去除抗原的蛋加工品的制造方法
[0330]
本发明为去除或降低了抗原的蛋加工品的制造方法,其具有如下步骤:在该加工品的制造过程中确认抗原被去除或降低了,
[0331]
此处,该抗原是上述(1)~(3)、(4)~(10)的抗原的至少一种。
[0332]
去除或降低了抗原的蛋加工品的制造过程中,确认去除或降低了抗原的步骤可以通过上述“检测仪”的项目中记载的方法确认是否含有抗原来进行。
[0333]
另外,去除或降低了抗原的蛋加工品的制造可以通过上述“去除抗原的食品等”项目中记载的方法来进行。
[0334]
实施例
[0335]
以下,对于本发明的实施例进行说明。本发明的技术范围不限定于这些实施例。
[0336]
实施例1:蛋白质图谱的确认
[0337]
使用下述二维电泳方法,检测蛋所包含的蛋白质。
[0338]
蛋白质的提取
[0339]
将生的鸡蛋分为蛋白和蛋黄。
[0340]
蛋白和蛋黄中所包含的蛋白质的提取和纯化如下进行。向蛋白中加入增溶剂而提取蛋白质之后,添加水或尿素缓冲液而得到蛋白质提取液。尿素缓冲液的组成如下。
[0341]
30mm tris
[0342]
2m 硫脲
[0343]
7m 尿素
[0344]
4%(w/v)chaps:
[0345]
3-[3-(胆酰胺丙基)二甲氨基]丙磺酸内盐
[0346]
适量的稀盐酸
[0347]
加入蒸馏水将整体调节为100ml。ph为8.5。
[0348]
之后,以蛋白质重量计各混合25μg来得到提取液。向蛋黄中添加表面活性剂缓冲液(mammalian lysis buffer(mcli),sigma公司)作为增溶剂来提取蛋白质。
[0349]
之后,使用2d-cleanup试剂盒(ge公司制)进行2次沉淀操作。第1次的沉淀操作向回收的上述蛋白质提取液中加入tca(三氯乙酸)进行沉淀,对该操作所产生的沉淀(tca沉淀)进行回收。第2次沉淀操作通过向回收的前述tca沉淀中加入丙酮进行沉淀,对该操作得到的沉淀(被检体)进行回收。
[0350]
被检体溶液的制备
[0351]
将得到的被检体的一部分(以蛋白质重量计50μg)溶解于第一维等电点电泳用凝胶的溶胀用缓冲液destreak rehydration solution(ge公司制)150μl中,作为第一维等电
gels。另外,制备以下的组成的泳动用缓冲液并使用。
[0377]
50mm mops
[0378]
50mm tris碱
[0379]
0.1%(w/v)sds
[0380]
1mm edta
[0381]
另外,本实施例中,使用在泳动用缓冲液中溶解0.5%(w/v)的琼脂糖s(nippon gene co.,ltd制)和适量的bpb(溴酚蓝)而成的粘接用琼脂糖溶液。
[0382]
将sds-page的孔中充分地用上述泳动用缓冲液进行清洗之后,去除该洗涤中使用的缓冲液。接着,向孔中添加充分溶解的粘接用琼脂糖溶液。接着,使进行了sds平衡化的凝胶浸渍于琼脂糖中,用镊子使进行了sds平衡化的凝胶与第二维泳动用凝胶密合。在该两凝胶密合的状态下确认到琼脂糖充分地凝固,以200v恒定电压进行约45分钟泳动。
[0383]
凝胶的荧光染色
[0384]
使用sypro ruby(life technologies公司制)进行凝胶的荧光染色。
[0385]
首先,将所使用的密闭容器事先用98%(v/v)的乙醇充分地进行清洗。进行2次如下处理:从sds-page仪器将泳动后的第二维泳动用凝胶卸下,放置于洗净的密闭容器中,在含有50%(v/v)甲醇和7%(v/v)乙酸的水溶液中浸渍30分钟的处理。之后,将该水溶液置换为水,浸渍10分钟。接着,将第二维泳动用凝胶浸渍于40ml的sypro ruby中,在室温下振荡一晩。接着,去除sypro ruby,将第二维泳动用凝胶用水洗涤之后,用含有10%(v/v)甲醇和7%(v/v)乙酸的水溶液振荡30分钟。进一步,将该水溶液置换为水,振荡30分以上。
[0386]
解析
[0387]
将实施了上述一系列处理的第二维泳动用凝胶供于使用了typhoon9400(ge公司制)的荧光图像的扫描中。对于蛋黄所包含的蛋白质,将2维电泳的结果示于图1中(对于蛋白的结果没有显示)。凝胶的照片的左侧可见分子量标记物的带,带的位置表示特定的分子量(kda)。
[0388]
实施例2:用免疫印迹确认抗原(1)
[0389]
用免疫印迹确认抗原是如下进行的:将实施例1中记载的步骤进行至“第二维的sds-page”为止,之后进行以下的“向膜的转印”、“免疫印迹”、“解析”的操作。
[0390]
向膜的转印
[0391]
向膜的转印使用以下的转印装置和转印用缓冲液进行。
[0392]
转印装置:xcell surelock mini-cell和xcell ii blot module(life technologies公司制)
[0393]
转印用缓冲液:将nupage transfer缓冲液(
×
20)(life technologies公司制)用milliq水稀释20倍然后使用。
[0394]
具体而言,按照以下的步骤,将二维电泳凝胶中的蛋白质转印到膜(pvdf膜)。
[0395]
(1)将pvdf膜浸渍于100%甲醇中,然后浸渍于milliq水中,然后转移至转印用缓冲液中,进行pvdf膜的亲水化处理。
[0396]
(2)按照海绵、滤纸、第二维sds-page结束后的凝胶、亲水化处理后的pvdf膜、滤纸、海绵的顺序进行设置,在转印装置中、30v恒定电压下通电1小时。
[0397]
免疫印迹
[0398]
作为第一抗体使用具有蛋变态反应的患者(患者1)的血清或者非蛋变态反应被检者血清进行膜的免疫印迹。该蛋变态反应的患者是被诊断为由鸡蛋导致的食物依赖性运动引起的变态反应症(fdeia)的患者。需要说明的是,对于该患者而言,在穿刺试验中,生的蛋、煮蛋和温泉蛋均显示为阴性;在特异的ige抗体检查中,对于蛋白、蛋黄、卵类黏蛋白显示为阴性。
[0399]
膜的免疫印迹按照以下的步骤进行。
[0400]
(1)将转印的膜在5%脱脂奶/pbst溶液(包含0.1%非离子表面活性剂tween 20的pbs缓冲液)中、室温下振荡1小时。
[0401]
(2)作为第一抗体,在5%血清/5%脱脂奶/pbst溶液中、室温下静置1小时。
[0402]
(3)用pbst溶液进行洗涤(5分钟
×
3次)。
[0403]
(4)作为第二抗体将抗人ige-hrp(西洋山葵过氧化酶)在用5%脱脂奶/pbst溶液稀释了5000倍的溶液中、室温下静置1小时。
[0404]
(5)用pbst溶液进行洗涤(5分钟
×
3次)。
[0405]
(6)在pierce western blotting substrate plus(thermo公司制)中静置5分钟。
[0406]
解析
[0407]
将实施了上述一系列处理的膜供于使用了typhoon9500(ge公司制)的荧光图像的扫描中。
[0408]
将使用了蛋变态反应患者血清的免疫印迹与作为对照的使用了非蛋变态反应被检者血清的免疫印迹进行比较。对于生的蛋黄所包含的蛋白质使用了蛋变态反应患者血清的免疫印迹(图2)中,与使用了非蛋变态反应被检者的血清的情况不同,并且检测到与公知的鸡蛋变应原蛋白质不同的3个斑点。
[0409]
上述3个斑点的分子量和等电点分别如下(图3)。
[0410]
斑点1:分子量20~40kda、pi4.0~10.0
[0411]
斑点2:分子量30~60kda、pi5.0~10.0
[0412]
斑点3:分子量35~60kda、pi5.0~10.0
[0413]
实施例3:质谱分析和抗原的鉴定(1)
[0414]
对于实施例2的产生3个斑点的抗原,利用质谱分析进行氨基酸序列的鉴定。
[0415]
具体而言,按照以下的步骤进行蛋白质的提取和质谱分析。
[0416]
(1)对于生的鸡蛋的蛋黄,按照实施例1和2的步骤进行蛋白质提取、2维电泳和膜转印,用0.008%直接蓝(direct blue)/40%乙醇/10%乙酸进行振荡而染色。
[0417]
(2)之后,用40%乙醇/10%乙酸进行5分钟的处理3次进行脱色,用水洗涤5分钟之后进行风干。
[0418]
(3)将目标的斑点用干净的裁刀切取,加入至离心试管中。用50μl的甲醇进行膜亲水处理之后,用100μl的水洗涤2次之后离心除去,加入20μl的20mm nh4hco3·
50%乙腈。
[0419]
(4)加入1pmol/μl赖氨酸-肽链内切酶(wako)1μl,在37℃下静置60分钟之后,将溶液回收至新的离心试管中。对膜加入20μl的20mm nh4hco3·
70%乙腈,在室温下浸渍10分钟,进一步进行回收。用0.1%甲酸、4%乙腈10μl溶解,转移至试管中。
[0420]
(5)对回收的溶液进行减压干燥之后,用a液(0.1%甲酸、4%乙腈溶液)15μl进行溶解,进行质谱分析(esi-tof6600,ab sciex公司制)。
[0421]
(6)基于由质谱仪得到的质谱数据的蛋白质鉴定通过搜索ncbi或uniprot来进行。
[0422]
结果
[0423]
对于各斑点进行了质谱分析的结果,检测到以下的氨基酸序列。
[0424]
斑点1:序列号3~11所示的氨基酸序列
[0425]
斑点2:序列号9~11、14、16所示的氨基酸序列
[0426]
斑点3:序列号19~45所示的氨基酸序列
[0427]
进一步,对于各斑点,针对斑点1和斑点2,将由质谱仪得到的质谱数据用ncbi进行解析;针对斑点3,将由质谱仪得到的质谱数据用uniprot进行解析,结果鉴定出各斑点为以下的蛋白质。
[0428]
斑点1:卵黄原蛋白-3(vitellogenin-3)(氨基酸序列:ncbi登陆号xp_015146355、编码其的碱基序列:genbank登陆号xm_015290869.1)的c末端部分(氨基酸序列:序列号2、编码其的碱基序列:序列号1)
[0429]
斑点2:卵黄原蛋白-3(vitellogenin-3)(氨基酸序列:ncbi登陆号xp_015146355、编码其的碱基序列:genbank登陆号xm_015290869.1)的c末端部分(氨基酸序列:序列号13、编码其的碱基序列:序列号12)
[0430]
斑点3:卵黄原蛋白-1(vitellogenin-1)(氨基酸序列:uniprot登录号p87498、编码其的碱基序列:ena(embl)登录号d89547.1)的中央部分、或者、卵黄脂磷蛋白-1(lipovitellin-1)的c末端部分(氨基酸序列:序列号18、编码其的碱基序列:序列号17)
[0431]
实施例4:用免疫印迹确认抗原(2)
[0432]
与实施例2同样地,使用別的蛋变态反应患者3名(患者2、患者3、患者4)的血清,用免疫印迹进行抗原确认。对于生的蛋黄所包含的蛋白质使用了蛋变态反应患者血清的免疫印迹(对于患者2是图4、对于患者3是图5、对于患者4是图6)中,与使用了非蛋变态反应被检者的血清的情况不同,并且检测到与公知的鸡蛋变应原蛋白质不同的斑点。具体而言,对于患者2检测到斑点4~8;对于患者3检测到斑点9和10;对于患者4检测到斑点11。
[0433]
上述斑点4~11的分子量和等电点分别如下(图4~6)。
[0434]
斑点4:分子量20~50kda、pi3.0~8.0
[0435]
斑点5、6:分子量80~260kda、pi1.0~8.0
[0436]
斑点7:分子量110~300kda、pi3.0~8.0
[0437]
斑点8:分子量160~550kda、pi3.0~8.0
[0438]
斑点9:分子量20~50kda、pi7.0~11.0
[0439]
斑点10:分子量20~50kda、pi7.0~11.0
[0440]
斑点11:分子量15~40kda、pi6.0~11.0
[0441]
实施例5:质谱分析和抗原的鉴定(2)
[0442]
与实施例3同样地,对于实施例4的产生斑点4~11的抗原,利用质谱分析进行氨基酸序列的鉴定。
[0443]
对于各斑点进行了质谱分析的结果,检测到以下的氨基酸序列。
[0444]
斑点4:序列号48~57所示的氨基酸序列
[0445]
斑点5、6:序列号60~104所示的氨基酸序列
[0446]
斑点7:序列号107~150所示的氨基酸序列
[0447]
斑点8:序列号153~235所示的氨基酸序列
[0448]
斑点9:序列号238~249所示的氨基酸序列
[0449]
斑点10:序列号252~260所示的氨基酸序列
[0450]
斑点11:序列号263~271所示的氨基酸序列
[0451]
进一步,对于各斑点,将由质谱仪得到的质谱数据用ncbi进行解析的结果,鉴定出各斑点为以下的蛋白质。
[0452]
斑点4:卵黄原蛋白-3(vitellogenin-3)(氨基酸序列:ncbi登陆号xp_015146355、编码其的碱基序列:genbank登陆号xm_015290869.1)(氨基酸序列:序列号47、编码其的碱基序列:序列号46)
[0453]
斑点5、6:卵黄原蛋白-2前体(vitellogenin-2precursor)(氨基酸序列:ncbi登录号np_001026447.1、编码其的碱基序列:genbank登录号nm_001031276.1)(氨基酸序列:序列号59、编码其的碱基序列:序列号58)
[0454]
斑点7:卵黄原蛋白-2前体(vitellogenin-2precursor)(氨基酸序列:ncbi登录号np_001026447.1、编码其的碱基序列:genbank登录号nm_001031276.1)(氨基酸序列:序列号106、编码其的碱基序列:序列号105)
[0455]
斑点8:载脂蛋白b前体(apolipoprotein b precursor)(氨基酸序列:ncbi登录号np_001038098.1、编码其的碱基序列:genbank登录号nm_001044633.1)(氨基酸序列:序列号152、编码其的碱基序列:序列号151)
[0456]
斑点9:载脂蛋白b前体(apolipoprotein b precursor)(氨基酸序列:ncbi登录号np_001038098.1、编码其的碱基序列:genbank登录号nm_001044633.1)(氨基酸序列:序列号237、编码其的碱基序列:序列号236)
[0457]
斑点10:载脂蛋白b前体(apolipoprotein b precursor)(氨基酸序列:ncbi登录号np_001038098.1、编码其的碱基序列:genbank登录号nm_001044633.1)(氨基酸序列:序列号251、编码其的碱基序列:序列号250)
[0458]
斑点11:卵黄原蛋白-2前体(vitellogenin-2precursor)(氨基酸序列:ncbi登录号np_001026447.1、编码其的碱基序列:genbank登录号nm_001031276.1)(氨基酸序列:序列号262、编码其的碱基序列:序列号261)
[0459]
产业上的可利用性
[0460]
本发明提供蛋变态反应的新型抗原、蛋变态反应的诊断方法和诊断试剂盒、包含该抗原的药物组合物、去除或降低了该抗原的蛋或蛋加工品或者产生该蛋或由该蛋孵化的鸟、以及去除或降低了该抗原的蛋加工品的制造方法。本发明还能够提供用于判断对象物中有无蛋抗原的检测仪。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。