1.本发明涉及医学技术领域,尤其是涉及一种用于无创评估乳腺癌前哨淋巴结转移的靶向分子探针。
背景技术:
2.乳腺癌是全球发病率最高的恶性肿瘤,严重影响广大女性的身心健康。前哨淋巴结活检 (sentinel lymph node biopsy,slnb)是早期乳腺癌腋窝分期的主要手段,需切除前哨淋巴结(sentinel lymph node,sln)行病理检查判断是否转移。然而,slnb可能导致淋巴水肿、手臂麻木等后遗症,且研究表明约70%行slnb患者无转移,应避免slnb。目前临床常用的淋巴结示踪剂如亚甲蓝、icg等均只能起到示踪作用,评估淋巴结的转移状态仍需依靠病理活检。如何无创评估sln转移,避免过度活检是亟待解决的临床需求。
3.分子影像技术运用影像学手段在细胞和分子水平对生物活动过程进行无创定性和定量分析,可以探测小至1mm肿瘤病灶,并具备高特异性、高灵敏度和超高图像分辨率的特性。研究发现,近红外荧光成像技术,用于术中导航,具备实时、灵敏、动态、无创地反映目标病灶等特点,有助于术者辨别目标病灶,提高术中诊疗的精准度。相比近红外一区(the secondnear-infrared window,nir
‑ⅰ
,700-900nm)和nir
‑ⅱ
a区(1300-1400nm)荧光成像存在荧光穿透深度有限,信噪不高等问题,nir
‑ⅱ
b荧光具有“组织透明窗口”的独特性,在组织中具有更低的散射和吸收,能够进一步提高成像的空间分辨率和组织穿透深度。目前的nir
‑ꢀⅱ
区的显像剂主要有小分子染料、单臂碳纳米管、量子点、稀土纳米材料这几类。而稀土纳米材料由于其出色的光稳定性,丰富可调的光谱特性及低毒性备受关注。但单纯纳米探针缺乏靶向性,仅依赖epr效应难以精准定位肿瘤。cxcr4是恶性肿瘤研究的重要靶点,它是一种七次跨膜蛋白,在乳腺癌及乳腺癌转移淋巴结部位高表达。
技术实现要素:
4.本发明的第一目的在于针对现有技术存在的上述缺点与不足,提供基于nir
‑ⅱ
b区荧光成像,实时、精准、无创,具有良好靶向性的一种用于无创评估乳腺癌前哨淋巴结转移的靶向分子探针。
5.本发明的第二目的在于提供所述靶向分子探针的制备方法。
6.本发明的第三目的在于提供所述靶向分子探针在制备用于无创评估乳腺癌sln转移状态的示踪剂中应用。
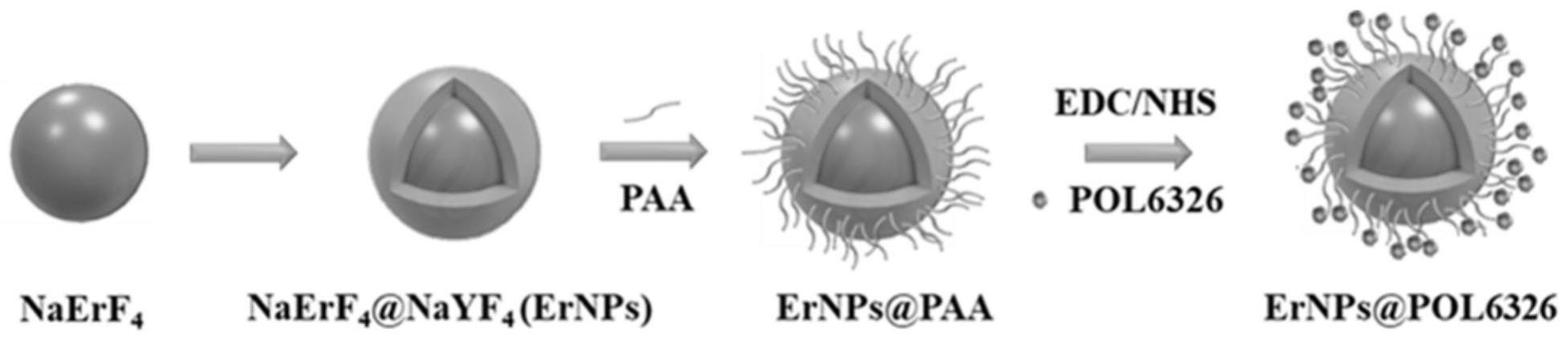
7.所述靶向分子探针为乳腺癌特异靶向分子探针ernps@pol6326,以特异性识别乳腺癌细胞的balixafortide作为靶向肽,偶联生物相容性好、nir
‑ⅱ
b发光的稀土纳米颗粒;
8.所述靶向分子探针以稀土纳米颗粒naerf4为内核,表面覆盖nayf4,合成稀土核壳纳米颗粒naerf4@nayf4(ernps),在nayf4层的外表面通过修饰paa以提供羧基,通过edc/nhs活化羧基,偶联靶向cxcr4的肿瘤特异性导向肽balixafortide(pol6326),从而合成nir
‑ⅱ
b 发光的稀土纳米探针ernps@pol6326。
9.所述靶向分子探针ernps@pol6326的制备方法,包括以下步骤:
10.1)高温共沉淀合成法合成naerf4核;
11.2)外延生长法合成稀土核壳纳米材料naerf4@nayf4(ernps);
12.3)酸洗法去除ernps上的油酸配体,增加材料的亲水性;
13.4)ernps表面修饰聚丙烯酸(paa);
14.5)edc/nhs活化ernps@paa上的羧基后连接靶标pol6326。
15.在步骤1)中,所述高温共沉淀合成法合成naerf4核的具体步骤可为:
16.在容器中加入油酸(oa)和十八烯(ode),再加入er(ch3coo)3混合搅拌,在室温下抽真空;升温至110~150℃反应后冷却至40~60℃;加入0.7~0.9m氟化铵甲醇溶液、0.4~0.6m 氢氧化钠甲醇溶液反应;打开容器的玻璃塞,升温至100~150℃,完全去除甲醇;然后抽真空通n2,再升温至280~320℃反应;冷却至室温,加入过量乙醇,离心去上清,再加入环己烷和乙醇(1︰2)洗涤,再次离心;分散在环己烷中。
17.在步骤2)中,所述外延生长法合成稀土核壳纳米材料naerf4@nayf4(ernps)的具体步骤可为:
18.在容器中加入油酸(oa)和十八烯(ode),再加入y(ch3coo)3混合搅拌,在室温下抽真空后,升温至110~150℃反应;然后冷却至40~60℃;加入步骤1)合成的naerf4核心颗粒,再加入0.7~0.9m氟化铵甲醇溶液、0.4~0.6m氢氧化钠甲醇溶液,40~60℃反应;打开容器的玻璃塞,升温至100~150℃,完全去除甲醇;再次抽真空,通n2,升温至280~320℃反应;然后冷却至室温,加入过量乙醇,离心,去上清,加入环己烷和乙醇(1︰2)洗涤,再次离心后分散在环己烷中。
19.在步骤3)中,所述酸洗法去除ernps上的油酸配体的具体步骤可为:
20.ernps离心后弃去上清,加入5ml ph=1的盐酸在超声清洗仪中重悬,采用磁力搅拌器充分搅拌50min后,滴加适量乙醚,于通风橱内室温静置萃取;弃去上层乙醚,再次滴加适量乙醚,于通风橱内室温静置萃取;弃去上层乙醚,离心,超纯水洗涤、离心3次;在超纯水中重悬。
21.在步骤4)中,所述ernps表面修饰聚丙烯酸paa的具体步骤可为:
22.按去除油酸配体后的ernps︰聚丙烯酸(paa)为1︰2的比例称取聚丙烯酸,充分溶解在2~4ml超纯水中,加入步骤3)去除油酸配体后的ernps,超声,离心去上清,超纯水洗涤,沉淀在5ml超纯水中重悬,得ernps@paa。
23.在步骤5)中,所述edc/nhs活化ernps@paa上的羧基后连接靶标pol6326的具体步骤可为:
24.取1ml步骤4)中合成的ernps@paa溶解到的mes缓冲液中,加入10~20mg edc搅拌 0.5~1h;加入10~20mg nhs试剂,搅拌1~2h;离心后,弃去上清,0.9%生理盐水重悬;加入pol6326,4℃搅拌24h;离心弃上清,用0.9%生理盐水洗涤、离心,分散到1ml的0.9%生理盐水里,得到目标探针ernps@pol6326。
25.所述靶向分子探针ernps@pol6326可在制备用于无创评估乳腺癌sln转移状态的示踪剂中使用。
26.所述应用的具体方法可为:
27.在局部注射所述靶向分子探针ernps@pol6326时,探针可通过淋巴管进入前哨淋
巴结。当前哨淋巴结无乳腺癌癌转移时,分子探针ernps@pol6326无法长时间滞留在前哨淋巴结中。当前哨淋巴结出现乳腺癌癌转移时,分子探针ernps@pol6326可通过结合癌细胞表面的cxcr4 受体而滞留在前哨淋巴结中。所述探针在808nm激光的激发下于nir
‑ⅱ
b区有一个强的发射光,通过近红外二b区成像观察前哨淋巴结的荧光信号强度,当出现强荧光时可认为前哨淋巴结存在癌转移。故而基于近红外二b区成像可判定乳腺癌前哨淋巴结是否有转移,实现术前无创实时判断前哨淋巴结的转移状态,避免过度活检。
28.与现有技术相比,本发明的有益效果在于:
29.本发明提出的nir
‑ⅱ
b区荧光成像无创评估乳腺癌sln转移状态方法解决一直困扰临床医生的不必要slnb导致过度治疗的问题,准确、实时、无创判断乳腺癌sln转移状态进而避免了过度活检。nir
‑ⅱ
b区荧光成像系统因其高信噪比、成像空间分辨率和大穿透深度、实时、可视化的特点在无创评估乳腺癌sln转移状态方法手术中独具优势。
30.通过nir
‑ⅱ
b荧光成像可视化乳腺癌转移sln,实现实时、精准、无创的评估乳腺癌sln 的转移状态,辅助乳腺癌术中腋窝淋巴结分期,在nir
‑ⅱ
b区荧光成像引导下可视化乳腺癌 sln转移状态,避免不必要slnb,提高患者的生活质量,对改善患者预后具有重要临床意义。
31.本发明进一步通过paa修饰偶联靶向cxcr4的肿瘤特异性导向肽巴利沙福balixafortide (pol6326),构建形成特异靶向肿瘤组织高亲和性分子探针,探针具有良好的靶向性,实现无创精准评估乳腺癌sln转移状态,辅助术中腋窝淋巴结分期。
附图说明
32.图1为ernps@pol6326探针的合成示意图。
33.图2为ernps@pol6326探针的电镜图、发射光谱及穿透深度。
34.图3为ernps@pol6326探针的细胞靶向性、时间和浓度依赖性。
35.图4为ernps@pol6326探针的动物靶向性。
36.图5为ernps@pol6326探针识别淋巴结转移的可行性。
具体实施方式
37.为了使本发明的目的及优点更加清楚明白,以下结合附图及实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
38.本发明的目的旨在以特异性识别乳腺癌balixafortide作为靶向肽,偶联生物相容性好、 nir
‑ⅱ
b发光的稀土纳米颗粒,制备乳腺癌特异靶向分子探针naerf4@nayf4@pol6326,通过 nir
‑ⅱ
b荧光成像可视化乳腺癌转移sln,实现实时、精准、无创的评估sln的转移状态,指导乳腺癌术中腋窝淋巴结分期。
39.本发明的首要目的在于提供一种肿瘤靶向稀土纳米颗粒,该纳米材料在808nm激光的激发下于nir
‑ⅱ
b区有一个强的发射光,利用其光谱特性作为分子探针用于乳腺癌sln转移状态的无创评估,进而建立精准有效的乳腺癌转移sln识别方法。
40.所述靶向分子探针为乳腺癌特异靶向分子探针ernps@pol6326,以特异性识别乳腺癌细胞的balixafortide作为靶向肽,偶联生物相容性好、nir
‑ⅱ
b发光的稀土纳米颗粒。
41.所述靶向分子探针以稀土纳米颗粒naerf4为内核,表面覆盖nayf4,合成稀土核壳纳米颗粒naerf4@nayf4(ernps),在nayf4层的外表面通过修饰paa以提供羧基,通过edc/nhs活化羧基,偶联靶向cxcr4的肿瘤特异性导向肽balixafortide(pol6326),从而合成nir
‑ⅱ
b 发光的稀土纳米探针ernps@pol6326(合成路线示意图参见图1)。
42.本发明实施例所述靶向分子探针ernps@pol6326的合成方法,包括以下步骤:
43.1)高温共沉淀合成法合成naerf4核
44.取三口烧瓶,加入3~8ml油酸(oa)和10-15ml十八烯(ode),再加入er(ch3coo)3(1 mmol,0.3444g)混合搅拌,在室温下抽真空;升温至110~150℃,反应至液体澄清无固体颗粒;冷却至40~60℃;加入0.7~0.9m氟化铵甲醇溶液、0.4~0.6m氢氧化钠甲醇溶液各 5ml,40~60℃反应20-30min;打开三口烧瓶的玻璃塞,升温至100~150℃,完全去除甲醇;抽真空通n2,3次;升温至280~320℃,反应1.5~2h;冷却至室温,加入过量乙醇,离心6000~8000rpm,5~15min;弃去上清,加入环己烷和乙醇(1︰2)洗涤两次,离心 6000-8000rpm,5~15min;分散在2~10ml的环己烷中。
45.2)外延生长法合成稀土核壳纳米材料naerf4@nayf4(ernps)
46.取三口烧瓶,加入3~8ml油酸(oa)和10~15ml十八烯(ode),再加入y(ch3coo)3(0.5 mmol,0.1333g)混合搅拌,在室温下抽真空;升温至110~150℃,反应至液体澄清无固体颗粒;冷却至40~60℃;加入上述合成的核心颗粒2.5ml,搅拌均匀;加入0.7~0.9m氟化铵甲醇溶液、0.4~0.6m氢氧化钠甲醇溶液各2.5ml,40~60℃反应20~30min;打开三口烧瓶的玻璃塞,升温至100~150℃,完全去除甲醇;抽真空通n2,3次;升温至280-320℃,反应1.5~2h;冷却至室温,加入过量乙醇,离心6000~8000rpm,5~15min;弃去上清,加入环己烷和乙醇(1︰2)洗涤两次,离心6000~8000rpm,5~15min;分散在2~10ml 的环己烷中。
47.3)酸洗法去除ernps上的油酸配体,增加材料的亲水性
48.5ml ernps离心后加入5ml ph=1的盐酸在超声清洗仪中重悬;在磁力搅拌器上充分搅拌30~60min;到时间后,边滴加适量乙醚边搅拌,加完后关闭磁力搅拌器,于通风橱内室温静置萃取5~10min;弃去上层的乙醚,在磁力搅拌器搅拌条件下滴加适量乙醚,加完后关闭磁力搅拌器,于通风橱内室温静置萃取5~10min;弃去上层乙醚,10000~15000rpm 离心10~20min,超纯水洗涤、离心3次;在5ml超纯水中重悬。
49.4)ernps表面修饰聚丙烯酸(paa)
50.按去除油酸的ernps︰聚丙烯酸(paa)1︰2的比例称取聚丙烯酸,充分溶解在2~4ml 超纯水中;加入上述去除油酸配体后的ernps;超声3~12h;10000~15000rpm离心10~ 20min后,弃去上清,超纯水洗涤3次,每次10~20min;沉淀在5ml超纯水中重悬,得到ernps@paa。
51.5)edc/nhs活化ernps@paa上的羧基后连接靶标pol6326
52.0.1mmol ernps@paa溶解到适量mes缓冲液(0.1m,ph=5);加入10~20mg edc搅拌0.5~ 1h;加入10~20mg nhs试剂,搅拌1~2h;10000~15000rpm离心10~20min后,弃去上清,5ml 0.9%生理盐水重悬;加入过量的pol6326,4℃搅拌24h;10000~15000rpm离心 10-20min后,弃上清,用0.9%生理盐水洗涤、离心,3次;分散到1ml的0.9%生理盐水里。得到目标探针ernps@pol6326。
53.以下给出一个具体实施例。
54.一、高温共沉淀合成法合成naerf4核
55.1、取100ml三口烧瓶,加入5ml油酸(oa)和15ml十八烯(ode),再加入er(ch3coo)3(1 mmol,0.3444g)混合搅拌,在室温下抽真空10min;
56.2、升温至120℃,反应20min;
57.3、冷却至50℃;
58.4、加入0.8m氟化铵甲醇溶液、0.5m氢氧化钠甲醇溶液各5ml,50℃反应30min;
59.5、打开三口烧瓶的玻璃塞,升温至100℃,30min去除甲醇;
60.6、抽真空通n2,3次;
61.7、升温至300℃,反应1.5h;
62.8、冷却至室温,加入过量乙醇,离心6000rpm,10min;
63.9、弃去上清,加入环己烷和乙醇(1︰2)洗涤两次,离心6000rpm,10min;
64.10、分散在5ml的环己烷中。
65.二、外延生长法合成稀土核壳纳米材料naerf4@nayf4(ernps)
66.1、取100ml三口烧瓶,加入4.5ml油酸(oa)和10.5ml十八烯(ode),再加入 y(ch3coo)3(0.5mmol,0.1333g)混合搅拌,在室温下抽真空10min;
67.2、升温至120℃,反应20min;
68.3、冷却至50℃;
69.4、加入上述合成的核心颗粒2.5ml,搅拌均匀;加入0.8m氟化铵甲醇溶液、0.5m氢氧化钠甲醇溶液各2.5ml,50℃反应30min;
70.5、打开三口烧瓶的玻璃塞,升温至100℃,30min去除甲醇;
71.6、抽真空通n2,3次;
72.7、升温至300℃,反应1.5h;
73.8、冷却至室温,加入过量乙醇,离心6000rpm,10min;
74.9、弃去上清,加入环己烷和乙醇(1︰2)洗涤两次,离心6000rpm,10min;
75.10、分散在5ml的环己烷中。
76.三、酸洗法去除ernps上的油酸配体,增加材料的亲水性
77.1、5ml ernps离心后加入5ml ph=1的盐酸在超声清洗仪中重悬;
78.2、在磁力搅拌器上充分搅拌50min;
79.3、到时间后,边滴加2ml乙醚边搅拌,加完后关闭磁力搅拌器,于通风橱内室温静置萃取10min;
80.4、弃去上层的乙醚,在磁力搅拌器搅拌条件下滴加2ml乙醚,加完后关闭磁力搅拌器,于通风橱内室温静置萃取10min;
81.5、弃去上层乙醚,15000rpm离心10min,超纯水洗涤、离心3次;
82.6、在5ml超纯水中重悬。
83.四、ernps表面修饰聚丙烯酸(paa)
84.1、按材料︰聚丙烯酸(paa)1︰2的比例称取聚丙烯酸,充分溶解在2~4ml超纯水中;
85.2、加入上述去除油酸配体后的ernps;
86.3、超声6h;
87.4、15000rpm离心15min后,弃去上清,超纯水洗涤3次,每次10min;
88.5、沉淀在5ml超纯水中重悬,得到ernps@paa。
89.五、edc/nhs活化ernps@paa上的羧基后连接靶标pol6326
90.1、0.1mmol ernps@paa溶解到5ml的mes缓冲液(0.1m,ph=5)
91.2、加入10mg edc搅拌0.5h;
92.3、加入10mg nhs试剂,搅拌1h;
93.4、15000rpm离心15min后,弃去上清,5ml 0.9%生理盐水重悬;
94.5、加入1mg的pol6326,4℃搅拌24h;
95.4、15000rpm离心10min,弃上清,用0.9%生理盐水洗涤、离心,3次;
96.5、分散到1ml的0.9%生理盐水里。得到目标探针ernps@pol6326。
97.六、ernps@pol6326用于无创评估乳腺癌sln转移状态
98.1.构建乳腺癌淋巴结转移模型小鼠,于最佳显影时间肿瘤侧与正常对照测足垫注射最佳浓度的ernps@pol6326;在最佳观察时间,采用小动物nir
‑ⅱ
荧光成像系统进行成像;对比观察两侧荧光信号的差异,成像结束后取小鼠淋巴结组织,置于小动物nir
‑ⅱ
荧光成像系统下检测离体淋巴结的荧光强度,之后进行组织病理学检查。
99.2.术后组织标本的体外分析:将上述取下的淋巴结组织切片进行he染色。将染色后的切片通过显微数字切片扫描系统motic采集图像,并进行病理学分析。将上述在体、离体荧光分布及he染色结果进行对比,分析转移侧淋巴结及正常淋巴结中荧光信号、组织病理,建立起荧光信号与病理诊断的一致性。
100.3.统计两组间差异,分析nir
‑ⅱ
b荧光成像评估乳腺癌sln转移状态可靠性与安全性,探讨其用于无创评估乳腺癌sln转移的可行性。建立实时、精准、无创判定乳腺癌sln转移的新方法。
101.图2显示成功构建ernps@pol6326探针,其在电镜下粒径较为均一,修饰靶向肽前后光谱特性一致,且发光元件ernps与临床常用的icg相比,具有更大的穿透深度和更高的分辨率。
102.图3显示所合成的探针连上荧光染料罗丹明,用于孵育乳腺癌细胞4t1细胞,使用共聚焦显微镜检测,发现探针具有良好的靶向性,且呈浓度和时间依赖性,且探针与乳腺癌细胞 mda-mb-231细胞,mcf-7细胞共孵育后发现探针也具有良好的靶向性。
103.图4显示乳腺癌移植瘤小鼠模型尾静脉注射探针后,nir
‑ⅱ
b荧光成像发现ernps@ pol6326相较于ernps@paa具有良好的肿瘤富集效果,在注射后36h具有最大的信噪比。而且其在肿瘤中的富集效果可被游离的pol6326阻断。
104.图5显示乳腺癌淋巴结转移小鼠模型足垫注射探针后,nir
‑ⅱ
b荧光成像发现ernps@ pol6326相较于ernps@paa具有良好的转移前哨淋巴结富集效果。而且小鼠双侧足垫注射 ernps@pol6326后,与健侧淋巴结相比,有转移的淋巴结部位(包括前哨淋巴结和第二站淋巴结及腹股沟淋巴结和骶部淋巴结)出现强荧光,在注射后48h荧光信号最强。且病理也证实有强荧光信号的淋巴结就是转移的淋巴结。
105.上述实施例仅为本发明的较佳实施例,不能被认为用于限定本发明的实施范围。凡依本发明申请范围所作的均等变化与改进等,均应仍归属于本发明的专利涵盖范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。