1.本发明涉及用于检测前列腺癌的方法、用于可靠的前列腺癌分级的方法、用于确定前列腺癌进展的方法、用于界定晚期前列腺癌的方法、以及用于基于生物标志物的检测来治疗前列腺癌患者的方法。
背景技术:
2.前列腺癌是发达国家男性中最常见的癌症形式,预计到2030年,这种疾病的发病率将在全球范围内翻一番。例如,2016年,超过19,300名澳大利亚男性被诊断患有前列腺癌,超过3,000名患者死亡,使这种疾病成为该国癌症相关死亡的最大原因之一。在国际上,每年有超过1,000,000名前列腺癌患者确诊,并且超过300,000名患者死亡,使得其成为全球关注的卫生保健问题。
3.前列腺特异性抗原(psa)测试目前用于前列腺癌筛查,然而,这种测定存在许多缺点,包括高百分比的假阳性和假阴性结果。psa也不能在诊断时区分侵袭性或生长较慢的癌症,并导致不必要的活检和过度治疗。最近有人建议放弃这种方法,尤其是对老年男性。
4.直肠指检是检查前列腺异常的一种替代方法,但是这种检查受到不能评估整个腺体和不能在一定程度上评估肿瘤大小的限制。
5.一旦怀疑是前列腺癌,可以进行活检以确认诊断并对癌症进行分级,但是组织的组织学评估和gleason/epstein分级,特别是操作者之间的可靠性存在明显的问题。尽管较高的gleason分级/epstein评分预示着较差的患者预后,但迄今为止,尚未发现与患者预后直接相关的组织病理学的具体方面。
6.因此,迫切需要更特异和/或更准确的前列腺癌检测方法,以帮助诊断/预后,并能够选择最合适的治疗干预。早期准确的检测显著降低了前列腺癌的死亡率,使得改进的诊断和预后方法成为一个重要的目标。
7.鉴于当前前列腺癌诊断/预后技术的缺陷,利用生物标志物辅助检测前列腺癌的能力将是非常有利的。然而,与前列腺癌相关的临床相关生物标志物的鉴定仍然是有问题的,并且可能需要生物标志物的组合来解决当前的问题。
8.因此,仍然需要鉴定更可靠的方法来检测前列腺癌以及癌症到晚期的进展,以便更好地帮助当前和未来的治疗方案。
技术实现要素:
9.本公开基于确定三种特异性内体生物标志物的组合可用于在受试者中检测前列腺癌和/或确定这种癌症的进展程度。
10.本公开的某些实施方案提供了检测受试者中前列腺癌的方法,所述方法包括检测来自受试者的生物样品中至少以下三种内体生物标志物appl1(衔接蛋白,与ph结构域和亮氨酸拉链1相互作用的磷酸酪氨酸,appl1)、sortilin-1(sort1)和syndecan-1(sdc1)与参照相比的改变的存在、水平、分泌和分布中的一种或多种。
11.在一个实施方案中,参照是正常或良性前列腺组织或正常血液或血浆样品。参照也可以是临界值。
12.在一个实施方案中,该方法包括检测appl1、sort1和sdc1的升高水平。
13.在一个实施方案中,该方法包括检测appl1和sdc1的升高水平。
14.在一个实施方案中,受试者是已经进行psa测试的人。
15.本公开的某些实施方案提供了检测受试者中前列腺癌的方法,所述方法包括检测来自受试者的生物样品中至少以下三种内体生物标志物appl1、sort1和sdc1与参照相比的升高水平。
16.本公开的某些实施方案提供了检测和测量受试者中前列腺癌严重程度的方法,该方法包括检测来自受试者的生物样品中至少以下三种内体生物标志物appl1、sort1和sdc1与参照相比的改变的存在、水平、分泌和分布中的一种或多种。
17.本公开的某些实施方案提供了检测和测量受试者中前列腺癌严重程度的方法,该方法包括检测来自受试者的生物样品中以下三种内体生物标志物appl1、sort1和sdc1的组合与参照相比的升高水平。
18.本公开的某些实施方案提供了监测受试者中前列腺癌进展的方法,该方法包括检测来自受试者的生物样品中至少以下三种内体生物标志物appl1、sort1和sdc1与参照相比的改变的存在、水平、分泌和分布中的一种或多种。
19.在一个实施方案中,该方法包括推荐受试者进行主动监测。受试者可以是被发现与参照相比appl1和sort1水平升高和syndecan-1水平降低的人。
20.本公开的某些实施方案提供了推荐受试者进行主动监测的方法,该方法包括检测来自受试者的生物样品中至少以下三种内体生物标志物appl1、sort1和sdc1与参照相比的改变的存在、水平、分泌和分布中的一种或多种。受试者可以是被发现与参照相比appl1和sort1水平升高和syndecan-1水平降低的人。
21.本发明的某些实施方案提供了检测受试者中前列腺癌的方法,该方法包括:
22.●
从受试者获得生物样品;
23.●
处理生物样品以允许检测至少以下三种内体标志物:appl1、sort1和sdc1;
24.●
在每种生物标志物中,检测经处理的样品中所选生物标志物的改变的存在、水平、分泌和分布中的一种或多种;和
25.●
识别受试者中的前列腺癌和/或癌症进展。
26.本发明的某些实施方案提供了用于检测受试者中前列腺癌的方法,该方法包括:
27.●
从受试者获得生物样品;
28.●
处理生物样品以允许检测至少以下三种内体标志物:appl1、sort1和sdc1;
29.●
在每种生物标志物中,比较所选标志物的存在、水平、分泌和分布;任选地与一种或多种已知指示受试者中存在或不存在前列腺癌的其他标志物进行比较;和
30.●
识别受试者中的前列腺癌。
31.本发明的某些实施方案提供了检测受试者中前列腺癌的方法,该方法包括:
32.●
处理来自所述受试者的生物样品以允许检测至少以下三种内体标志物:appl1、sort1和sdc1;
33.●
比较所选标志物的存在、水平、分泌和分布;任选地与一种或多种已知指示受试
者中存在或不存在前列腺癌的其他标志物一起使用;和
34.●
识别受试者中的前列腺癌和/或癌症进展。
35.本发明的某些实施方案提供了检测受试者中前列腺癌的方法,该方法包括:
36.●
从受试者获得生物样品;
37.●
处理生物样品以允许检测至少以下三种内体标志物:appl1、sort1和sdc1;和
38.●
检测经处理的样品中这些选定的标志物的改变的存在、水平、分泌和分布中的一种或多种;和
39.●
识别受试者中的前列腺癌和/或癌症进展,
40.●
其中根据生物标志物模式有效地治疗受试者的前列腺癌。
41.本公开的某些实施方案提供了在受试者中筛查前列腺癌的方法,该方法包括检测来自受试者样品的至少以下三种内体标志物:appl1、sort1和sdc1。
42.本发明的某些实施方案提供了在受试者中筛查前列腺癌并确定其进展的方法,该方法包括检测来自受试者样品的至少以下三种内体标志物:appl1、sort1和sdc1,其中所选标志物的改变的存在、水平、分泌和分布中的一种或多种指示受试者中的前列腺癌和/或其进展。
43.本发明的某些实施方案提供了用于诊断(或检测)和治疗受试者中前列腺癌的方法,该方法包括:
44.●
从受试者中检测appl1、sort1和sdc1;和
45.●
基于检测到的所选标志物的存在、水平、分泌和分布中的一种或多种,用癌症疗法治疗受试者。
46.本发明的某些实施方案还提供了包含一种或多种抗体或其片段的组合物,所述抗体或其片段结合从患有前列腺癌的受试者获得的生物样品中的至少以下三种内体生物标志物appl1、sort1和sdc1。所述一种或多种抗体或其片段可以与可检测标记结合。本文还提供了制备这种组合物的方法。
47.本发明的某些实施方案提供了确定受试者中存在前列腺癌的可能性的方法,该方法包括检测来自受试者的生物样品中至少以下三种内体生物标志物appl1、sort1和sdc1与参照相比的改变的存在、水平、分泌和分布中的一种或多种。
48.本发明的某些实施方案提供了鉴定可能对癌症治疗有反应的患有前列腺癌的受试者的方法,该方法包括检测来自受试者的生物样品中至少以下三种内体生物标志物appl1、sort1和sdc1与参照相比的改变的存在、水平、分泌和分布中的一种或多种。
49.本文还提供了将患有前列腺癌的受试者分为对癌症治疗可能有反应者或无反应者的方法,该方法包括检测来自受试者的生物样品中至少以下三种内体生物标志物appl1、sort1和sdc1与参照相比的升高水平。
50.本发明的某些实施方案提供了预测癌症治疗后受试者中前列腺癌复发风险的方法,该方法包括检测来自受试者的生物样品中至少以下三种内体生物标志物appl1、sort1和sdc1与参照相比的改变的存在、水平、分泌和分布中的一种或多种。
51.本发明的某些实施方案提供了用于实施本文所述的诊断/预后方法的试剂盒。
52.本文公开了其他实施方案。
附图说明
53.下面的附图说明了某些实施方案。应该理解,下面的描述仅仅是为了描述特定的实施方案,而不是为了限制该描述。
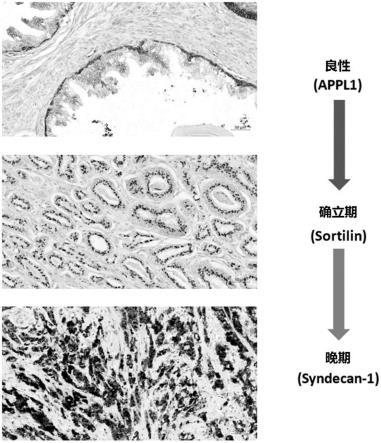
54.图1.appl1定义了具有强烈基底细胞层染色的良性组织,但是随着癌症的发展显示出向细胞核或细胞质分布的转变;sortilin-1在确立期癌组织中具有极化分布;syndecan-1检测到晚期癌症表型。良性和前列腺癌组织中的例子。
55.图2.通过ihc使用appl1生物标志物绘制癌症图,其可靠地检测和可视化前列腺癌以确认诊断。
56.图3.appl1绘制了前列腺切除术患者组织中癌症的分布图。appl1对良性组织中的基底细胞层强烈染色,并且在确立期癌组织中表达量增加并且改变为分布到细胞的细胞质中。appl1对具有细胞质分布的晚期癌组织强烈染色。表显示appl1在前列腺癌检测中具有非常高的灵敏度和特异性。
57.图4.sortilin-1定义了确立期癌症,并在确立期癌症中被检测为强烈的颗粒状染色模式,其变得弥散,并且在晚期癌组织中表达较少。癌组织的强烈颗粒状sotilin-1染色与gleason分级6/isup分级组1一致,并定义了应进行主动监测的患者(注意,其中在癌症中不存在明显的syndecan-1染色)。表显示sortilin-1在前列腺癌检测中的灵敏度和特异性。
58.图5.syndecan-1定义了晚期癌症。syndecan-1在来自良性组织的基底细胞中具有强染色模式(类似于appl1),在pin组织中消失,并且随着其转变为更晚期的癌症表型而在确立期癌症中变得明显。syndecan-1可检测迁移的癌细胞和晚期癌组织的口袋(pocket)。表显示syndecan-1在晚期前列腺癌的检测中具有高灵敏度和特异性。
59.图6.syndecan-1定义了迁移的癌细胞,甚至是上图中可见的晚期癌症的小口袋,以及下图中可见的癌症的另一个小口袋的放大图。
60.图7.appl1定义了前列腺癌结构以确认诊断。appl1在pin组织中的表达增加(箭头),在癌组织中具有细胞质分布,并且与确立期癌症相比,在晚期癌症中的表达增加。
61.图8.sortilin-1定义了具有强烈颗粒状染色模式的确立期前列腺癌,这在癌形成时的pin组织中也是明显的。在晚期癌症中,sortilin-1的表达降低,并且染色模式为更少颗粒状且更分散。
62.图9.syndecan-1定义了晚期前列腺癌,其具有非常强的染色模式,当其发展到更晚期时,这在某些确立期癌症区域中也是明显的。
63.图10.由appl1、sortilin-1和syndecan-1指导的潜在患者管理的复合图像描述。
64.图11.appl1(ev1)和syndecan-1(ev3)清楚地描绘了良性组织中的基底细胞标记,并且仅限于没有sortilin-1(ev2)染色。在临床实践中,appl1(ev1)可用于提供组织的整体情况,在这种情况下组织不存在癌症,并且sortilin-1(ev2)和syndecan-1(ev3)可用于确定,癌症存在或者在这种情况下良性组织存在,不存在确立期和晚期癌症。
65.图12.在isup分级组1患者组织中,appl1(ev1)清楚地描绘了局部癌症,sortilin-1(ev2)显示出强烈的极化标记,而syndecan-1(ev3)具有最少染色或没有染色。在临床实践中,appl1(ev1)可用于提供癌症的整体情况,sortilin-1(ev2)和ev3可用于确定存在/不存在确立期癌症(在该患者中sortilin-1(ev2)阳性)和晚期癌症(在该情况中syndecan-1(ev3)阴性)。
66.图13.在isup分级组2患者组织中,appl1(ev1)标志癌症,并且存在sortillin-1(ev2)极化的标记/gleason分级3的区域,或具有筛状腺体的强syndecan-1(ev3)标记/gleason分级4的组织。在临床实践中,appl1(ev1)可用于提供癌症的整体情况,sortillin-1(ev2)和syndecan-1(ev3)可用于确定确立期癌症(在该患者中sortillin-1(ev2)阳性)和晚期癌症(在该情况中syndecan-1(ev3)阳性)的存在/不存在/相对量。
67.图14.在isup分级组3患者组织中,appl1(ev1)绘制了具有sortilin-1(ev2阳性)/gleason 3标记的区域和sortilin-1(ev2)低强度染色和强syndecan-1(ev3阳性)/gleason 4标记的较大核心的癌症区域。
68.图15.在isup分级组4患者组织中,appl1(ev1)绘制了癌症的多个结,并且通常在多个区域中存在具有最少sortilin-1(ev2)染色和大量syndecan-1(ev3阳性染色)/gleason分级4标记的不良形成的癌腺。
69.图16.在isup分级组5患者组织中,在多个区域和节中存在强appl1(ev1)和强syndecan-1(ev3)标记,具有最少sortilin-1(ev2)标记。
70.图17.在isup分级组5患者组织中,在多个区域和节中存在强appl1(ev1),并且在索(cord)、癌袋(pocket of cancer)、迁移的癌细胞和高强度局灶性syndecan-1(ev3)染色的区域中存在强syndecan-1(ev3)标记。
71.图18.定义前列腺癌发病机理的精确生物标志物。该表总结了appl1、sortilin-1和syndecan-1生物标志物的临床效用。
72.图19.与h&e isup分级分组相比,使用appl1、sortilin-1和syndecan-1的ihc能够对前列腺癌患者(n=114名前列腺癌患者)进行更可靠的isup分级分组。
73.图20.与h&e isup分级分组(p=0.001)相比,通过ihc isup分级分组(p=0.0002)在预测生化复发方面有显著改善。n=144名前列腺癌患者。
74.图21.ihc isup分级分组对临床复发(转移)的显著预测,但不适用于h&e isup分级分组。n=114名前列腺癌患者。
75.图22.用ihc预测临床复发。只有具有cr的前列腺癌患者具有高appl1、低sortilin-1和高syndecan-1标记。没有sortilin-1的患者表现出50个月的临床复发,而具有少量sortilin-1的患者表现出高达150个月的临床复发。图的底部显示了来自具有临床复发的典型前列腺癌患者的appl1(ev1)、sortilin-1(ev2)和syndecan-1(ev3)染色模式。
76.图23.由h&e进行的患者isup分级分组与由ihc进行的使用sortilin-1(ev2)和syndecan-1(ev3)的isup分级分组的比较。绿框显示了通过两种技术明确识别的病理学一致的病例;绿框左侧的白框显示了根据h&e被过度报告的前列腺癌患者病例,或绿框右侧显示了报告不足的前列腺癌患者病例。解释的这些变化导致可靠性的提高(图19)和识别生化复发(bcr,图20)和临床复发(cr,图21)的能力的增加。
77.图24.经验证的appl1免疫测定用于检测患者血浆样品中的前列腺癌。appl1显示出前列腺癌和对照人血浆样品的显著分离。
78.图25.示意图显示了具有蛋白核心和潜在蛋白水解剪切位点和碳水化合物侧链的syndecan-1的结构。
79.图26.针对syndecan-1的市售抗体和针对syndecan-1的envision sciences单克隆抗体的ihc的比较。
80.图27.比较前列腺癌患者穿刺活检和前列腺切除术切片中的appl1、sortillin-1和syndecan-1ihc,证明在两种组织样品中对发病机理的检测是等效的。
81.图28.使用appl1、sortillin-1和syndecan-1ihc确定前列腺癌患者是否适合主动监测的实例。
82.图29.针对sortillin-1的envision sciences单克隆抗体的比较表明,只有seq id no:4准确描绘了前列腺癌患者组织样品中的发病机理。使用肽序列wvsknfggkweeihk(seq id no:4)和ekdytiwlahstdpe(seq id no:5)产生(genscript,piscataway,nj 08854,usa.)抗sortilin-1小鼠单克隆抗体。
具体实施方式
83.本公开基于确定至少三种特异性鉴定的内体标志物的组合可用于前列腺癌的检测、诊断和预后,特别是可用于确定受试者中癌症的进展和严重程度,因此将有助于医生推荐的治疗过程。
84.本公开的某些实施方案提供了用于检测受试者中前列腺癌的方法。本公开的某些实施方案提供了用于确定受试者中前列腺癌进展的方法。本公开的某些实施方案提供了基于至少三种选定的内体标志物的诊断和预后来治疗受试者中前列腺癌的方法,所述内体标志物具体为appl1(衔接蛋白,磷酸酪氨酸与ph结构域和亮氨酸拉链1相互作用,appl1)、sortilin-1(sort1)和syndecan-1(sdc1)。本文公开了其他实施方案。
85.本公开的某些实施方案提供了检测受试者中前列腺癌的方法,所述方法包括检测来自受试者的生物样品中至少以下三种内体生物标志物appl1(衔接蛋白,磷酸酪氨酸与ph结构域和亮氨酸拉链1相互作用,appl1)、sortilin-1(sort1)和syndecan-1(sdc1)与参照相比的改变的存在、水平、分泌和分布中的一种或多种。
86.某些公开的实施方案具有一个或多个优点的组合。例如,本文公开的实施方案的一些优点包括以下一个或多个:鉴定了一类新的三种特异性标志物,它们相互作用用于前列腺癌的诊断和/或预后;和附加的一种或多种标志物,在一些情况下,所述标志物可附加地用于前列腺癌的诊断和预后。
87.这些标志物可以在生物样品中,例如在组织样品、或组织活检、或血液/血浆样品或尿液样品中容易地被检测到。
88.三种生物标志物appl1、sortilin-1和syndecan-1在组织样品或组织活检中用于癌症检测和分级的效用/优势:-89.●
appl1和syndecan-1分布的组合可用于定义癌症的发作(pin组织形成)。在pin组织中,appl1经历了从清晰界定的基底细胞染色到细胞质分布的分布变化,在选定的细胞中经常伴有核内含物的染色。syndecan-1在良性组织中具有非常强的基底细胞染色模式,但随着pin组织的形成而消失。
90.●
appl1和syndecan-1的这种组合有效地鉴定了组织/活检样品中的前列腺癌起始。appl1在组织中的表达随着确立期癌症(establishment cancer)的形成而增加,而sortilin-1在确立期癌症中表现出特定的极化分布。这种生物标志物的组合识别患有gleason评分≤6(gleason分级/gg 3 3)的癌症或isup分级组1的患者,并且在这一阶段,癌症将具有最少或没有syndecan-1染色。
91.●
这三种生物标志物的组合有效地识别了癌症进展的早期阶段。appl1对于扫描大面积的组织以绘制癌症图并识别癌症及其边界是最佳的,并且基质不被染色(无背景);但与紧密排列的gleason 3级腺体相比,很难区分腺体是否为筛状/融合腺体。syndecan-1为这种染色提供了证实,并且经常以与appl1相同的方式分布,尽管它更加明显和颗粒化。然而,sortilin-1清楚地区分了组织/活检样品中的筛状腺体和融合腺体。sortilin-1对于这种可视化是最佳的,因为染色是极性的,并且细胞和边界被更好地区分,与融合/筛状腺体相比,可以清楚地显示分离的gleason 3级腺体。在细胞增殖形成融合腺体/片的gleason 4/5级癌症中,appl1不能区分融合腺体和细胞片,而syndecan-1表明融合腺体的存在,并与sortilin-1结合证实了这种形态。因为appl1使基质染色,并且在所有组织样品/活检芯(core)中出现更多的片状,而sortilin-1和syndecan-1没有,所以用这种生物标志物的组合可以清楚地区分间隙(指示融合的腺体)或基质(指示片状)。虽然这三种生物标志物有相当多的共染色,但是较高量的appl1和syndecan-1以及减少的sortilin-1表明晚期癌症;对于临床复发(转移)风险高的患者,观察到强appl1染色和强syndecan-1染色的特定模式,但很少或没有sortilin-1染色。appl1(由于其强度随着癌症进展到晚期而增加)和syndecan-1(由于其在晚期癌症和迁移的癌细胞中的高强度染色)的组合能够有效检测晚期癌症;这与sortilin-1的表达相平衡,以决定癌症的进展程度。三种生物标志物appl1、sortilin-1和syndecan-1的组合使得:-92.■
更准确的癌症检测,有助于对先前分级的gleason评分≤6或isup分级组1的患者进行最佳癌症识别。这对于评估适合主动监测的患者尤其重要,其中患者应仅为gleason评分≤6或isup等级组1;这可以通过appl1和sortilin-1染色来识别,而没有任何syndecan-1染色的迹象(即syndecan-1准确地识别甚至很小的癌块并表明晚期癌症表型)。
93.■
sortilin-1和syndecan-1的组合和相对比例确定了癌症的进展程度,并可用于更可靠地确定isup分级组1-5(sortilin-1仅用于isup-1,syndecan-1的量增加用于其他分级分组;和appl1染色的强度用于确认进展)。
94.■
在远离主要发病机理的地方检测癌症的存在;即远离癌症的主要病理或起源的癌症迹象
95.■
gleason评分7(gg 3 4或4 3)或isup分级组2和组3患者晚期癌症的更明确鉴定
96.■
对有临床复发风险的患者的特异性识别。
97.●
前列腺癌患者组织中三种生物标志物appl1、syndecan-1和sortilin-1的最佳检测涉及针对每种蛋白质的特定线性序列的单克隆抗体的产生:-98.■
来自appl1蛋白的特定线性序列,包括但不限于:
99.srliaassrpnqassegqfvvl(seq id no:9)
100.■
来自sortilin-1蛋白的特定线性序列,包括但不限于:
101.englwvsknfggkweeihka(seq id no:10)
102.■
来自syndecan-1蛋白的特定线性序列,包括但不限于:
103.epkqanggayqkptkqeefya(seq id no:11)。
104.本文的方法可适用于样品的高通量分析。
105.此外,本公开的某些实施方案至少部分基于这样的认识,即在前列腺癌细胞和组织中发生内体的细胞生物学的独特变化。这种变化涉及特异性地内化到早期内体中的细胞
表面蛋白,并涉及早期内体和循环内体囊泡机制。该途径中特定蛋白质的表达具有准确描述前列腺癌发病机理的能力,为此特定目的,已经从超过20种生物标志物的组中选择了三种特定的生物标志物。由于这三种生物标志物的相互关联的生物学和不同的功能特性,它们需要协同使用以充分描述发病机理并告知癌症进展和预后。这为前列腺癌细胞/组织中的这些内体相关生物标志物提供了一组独特的变化,并且通过这三种生物标志物的组合,当与对照组织相比时,有效地鉴定了前列腺癌组织中的关键变化。这些生物标志物对前列腺癌的高灵敏度和特异性,特别是当联合使用时(≥95%),是提供这种水平的明确可视化的第一组生物标志物。在包括血液和尿液在内的其他患者样品中检测到这三种内体生物标志物是由这些蛋白质的已知生物学所暗示的,并且已经由体外前列腺癌细胞的释放所证实。此外,三种生物标志物的比率提供了对患者临床复发/转移发作的风险评估,使得能够对治疗干预提出具体建议。
106.三种生物标志物appl1、sortilin-1和syndecan-1中每一种的生物学都与致病过程密切相关,并代表其他生物学的关键控制点。appl1是一种转录因子,也参与内体运输和再循环,并控制生长因子摄取和信号传导。appl1的转录因子活性尤其在pin组织中是明显的,在该组织中,它对很大比例(20-30%)的细胞核进行染色,并且可能参与调节基因表达。sortilin-1是glut4囊泡生物发生的关键分子,也与glut1相互作用,以共同调节糖代谢和warburg效应。glut4囊泡生物发生和运输过程的所有元件都受雄激素调节(例如as160)。sortilin-1还结合并调节脂蛋白脂肪酶(lpl)、氧固醇结合蛋白(osbp)和前颗粒蛋白(pgrn/grn),并且当下调时,它释放这些配体蛋白来驱动晚期癌症,这涉及脂质代谢、血管生成和syndecan-1生物学。syndecan-1增强了晚期信号传导和生长因子生物学,并且还结合β3整联蛋白,β3整联蛋白被认为驱动血小板相互作用和免疫遮盖(immune cloaking);并且还激活生存素以限制细胞凋亡。syndecan-1通过其肝素和硫酸软骨素侧链与细胞外基质分子如纤连蛋白(fn1)、玻连蛋白(vtn)、层粘连蛋白和胶原结合,在附着扩散和组织侵袭中发挥作用。因此,前列腺癌发病机理的三个关键控制点由appl1、sortilin-1和syndecan-1描述,并代表更广泛的致病过程,其涉及上述其他生物标志物,这些生物标志物与炎症、迁移、信号传导、免疫遮盖和血管生成一起参与糖和脂质代谢。在某些实施方案中,上文列出的其他生物标志物被认为是appl1、sortilin-1和syndecan-1的替代物。
107.在一个实施方案中,本文定义的方法可包括检测appl1蛋白、sort1蛋白和sdc1蛋白。所述方法可包括检测appl1蛋白的变体、sort1蛋白的变体和/或sdc1蛋白的变体。
108.在一个实施方案中,本文定义的方法可包括检测appl1核酸、sort1核酸和sdc1蛋白核酸。核酸可以是mrna。
109.本公开的某些实施方案提供了检测受试者中前列腺癌的方法,所述方法包括检测来自受试者的生物样品中至少以下三种内体生物标志物appl1、sort1和sdc1与参照相比的升高水平。
110.本公开的某些实施方案提供了检测和测量受试者中前列腺癌严重程度的方法,该方法包括检测来自受试者的生物样品中至少以下三种内体生物标志物appl1、sort1和sdc1与参照相比的改变的存在、水平、分泌和分布中的一种或多种。
111.例如,该方法能够检测前列腺癌并区分前列腺上皮内瘤(pin)、原发性(或确立期)前列腺癌和转移性前列腺癌,以确定前列腺癌的严重程度。该方法可以例如将转移性前列
腺癌与pin和原发性前列腺癌区分开来。
112.本公开的某些实施方案提供了检测和测量受试者中前列腺癌严重程度的方法,该方法包括检测来自受试者的生物样品中以下三种内体生物标志物:appl1、sort1和sdc1的组合与参照相比的升高水平。
113.本公开的某些实施方案提供了监测受试者中前列腺癌进展的方法,该方法包括检测来自受试者的生物样品中至少以下三种内体生物标志物appl1、sort1和sdc1与参照相比的改变的存在、水平、分泌和分布中的一种或多种。
114.例如,该方法能够区分前列腺上皮内瘤(pin)、原发性前列腺癌和转移性前列腺癌,以确定前列腺癌的进展。
115.在一些实施方案中,该方法包括检测包含seq id no:1、seq id no:2和/或seq id no:3的氨基酸序列的appl1多肽。
116.在一些实施方案中,该方法包括检测包含seq id no:4的氨基酸序列的sort1多肽。
117.在一些实施方案中,该方法包括检测包含seq id no:6或8的氨基酸序列的sdc1多肽。
118.在某些实施方案中,前列腺癌选自前列腺上皮内瘤(pin)、原发性前列腺癌和转移性前列腺癌。考虑了其他形式和/或等级的前列腺癌。本发明能够提供这种癌症的区分,以帮助医生推荐有益的和靶向的治疗,从而改善患者的预后。pin被定义为先前存在的良性前列腺腺泡或导管内的上皮细胞的肿瘤性生长(即已经发展超过增生)。我们知道pin满足从恶性前状态转化为癌症(增生转化为瘤形成)的许多要求。此外,高级别pin(hgpin)被更广泛地接受为已经转变为前列腺癌瘤形成/恶性肿瘤,或者随着癌症通过导管或进入其他组织发展而形成。可以用前列腺癌患者组织中的生物标志物作为导管中的“罗马桥(roman bridges)”,或者用导管和组织区域中非常强的appl1/syndecan-1染色来对hgpin进行可视化。因此,生物标志物识别从增生到瘤形成/前列腺癌的转变。
119.在这点上,通常gleason分级系统目前用于评估前列腺癌。基于与肿瘤样品的各种特征相关的“gleason”模式和分配给肿瘤样品模式的次级的组合,将“得分”分配给前列腺癌。gleason评分为2-6被认为是低侵袭性的癌症,并被划分为isup分级组1。在这些癌症局限于前列腺的患者中,可以建议对患者进行主动监测。晚期癌症的不同阶段被定义为:gleason评分为7被认为是中间(intermediate)至中等(moderate)侵袭性,现在被分为isup 2(gg 3 4)和isup 3(gg 4 3)分级组;gleason评分为8-10或isup 4/5被认为是高侵袭性的癌症。在某些实施方案中,前列腺癌是具有任何前述评分的gleason评分或isup分级分组的癌症,并且生物标志物可以比标准h&e组织学更准确地定义这些评分。
120.目前gleason分级/isup分级分组和h&e组织学的可靠性存在非常显著的问题:1)大量gleason评分≤6或isup分级组1的患者患有晚期癌症;2)具有gleason评分7的患者或isup组2和3的患者具有可变的预后,并且不容易识别哪些患者需要主动干预和主动监测/观察等待;3)取样误差或活检过程遗漏了癌症,使得难以确认诊断和进行分级/预测预后,并且重复活检是常见的;4)当早期检测到患者且癌症较小且局限(如下所述的1期)时,更难以定义gleason分级;5)使用gleason分级或isup分级分组不可能准确预测哪些患者将具有临床复发/转移。我们的技术的优势在于,我们具有三种生物标志物的组,其能够精确检测
癌症,并能够区分确立期癌症和晚期癌症,从而有助于更准确的gleason分级/isup分级分组,提供晚期癌症的最佳检测,并能够识别具有临床复发风险的患者。
[0121]“epstein”分级系统在epstein ji,zelefsky mj,sjoberg dd,et al.a contemporary prostate cancer grading system:a validated alternative to the gleason score,eur urol(2015)中进行了讨论,在此引用作为参考;并且被国际泌尿病理学学会同意用作isup分级分组。
[0122]
如上所述,当前gleason分级系统的问题可以总结如下:
[0123]
1.gleason评分2-6目前不再被指定(现在是isup分级组1),并且被定义为gleason评分6的某些模式现在被分级为7(isup分级组2),因此导致目前gleason评分6的癌症比历史评分6的癌症具有更好的预后。
[0124]
2.尽管3 4=7比4 3=7和8比9-10具有非常不同的预后,但gleason评分组合成3级分组(6,7,8-10)用于预后和治疗目的。此外,这些现在被指定为isup分级组2-5,但是尽管这在一定程度上增加了可靠性,但是基于用h&e定义晚期癌症的能力,这仍然是不理想的,h&e不是癌症特异性染色,只是形态学染色。
[0125]
3.在实践中,最低的gleason评分现在被指定为6或iusp分级组1,即使它在主要和次要癌症区域的评分为1-5。这导致部分患者有一个合乎逻辑但不正确的假设,即他们的癌症处于中等水平,这加剧了他们对癌症诊断的恐惧,认为癌症是严重的,从而导致治疗是必要的这一预期。
[0126]
为了部分解决gleason分级和gleason评分的上述缺陷,基于对》20,000例接受根治性前列腺切除术治疗的前列腺癌病例和》5,000例接受放射疗法治疗的前列腺癌病例的研究,开发了isup 5级分级组系统(参见不同模式的合成照片)。
[0127]
■
分级组1(gleason评分≤6)-只有单个分离的良好形成的腺体
[0128]
■
分级组2(gleason评分3 4=7)-主要是良好形成的腺体,较少组成部分为不良形成/融合/筛状的腺体
[0129]
■
分级组3(gleason评分4 3=7)-主要为不良形成/融合/筛状的腺体,较少组成部分为良好形成的腺体
[0130]
■
分级组4(gleason评分8)
[0131]-仅不良形成/融合/筛状的腺体或
[0132]-主要是良好形成的腺体,较少组成部分缺少腺体或
[0133]-绝大多数缺少腺体,较少组成部分为良好形成的腺体
[0134]
■
分级组5(gleason评分9-10)-缺乏腺体形成(或伴有坏死),有或没有不良形成/融合/筛状的腺体
[0135]
对于具有》95%的不良形成/融合/筛状的腺体或在核心或rp处缺少腺体的病例,《5%的良好形成的腺体的组成部分不计入等级
[0136]
不良形成/融合/筛状的腺体也可能是较小的组成部分
[0137]
1.根治性前列腺切除术isup分级组1-5的5年无生化复发(bcr)进展概率为96%、88%、63%、48%和26%;这分别意味着bcr仍然分别发生在这些分级组的4%、12%、37%、52%和74%中。此外,这些分级分组数字没有定义临床复发/转移,仅与bcr相关。
[0138][0139]
2.这5个isup分级组也可以预测随后进行根治性前列腺切除术或放射治疗的活检分级。
[0140]
3.新系统将前列腺癌的分级提炼到最低数目的分级,每个分级都有独特的预后,但在可靠性和解释方面仍然存在问题。然而,由于与gleason的原始分级系统相比,在标准和报告方面存在显著差异,我们已将新提出的分级组视为新的分级系统。
[0141]
尽管目前采用的isup分级分组系统(在美国/欧洲部分地区也称为epstein分级系统)具有以下优点:
[0142]
1.比传统的gleason评分系统更准确的分级分层
[0143]
2.简化的分级系统为5个,而不是根据不同gleason模式组合有多个可能的评分
[0144]
3.最低分级为1,而不是现行实践的gleason评分6,有可能减少惰性前列腺癌的过度治疗
[0145]
使用上述术语的新分级系统已在2016年被世界卫生组织(who)接受。
[0146]
前列腺癌也可以通过阶段来分类,阶段是癌症已经发展或已经包含在前列腺内的程度的量度。在第1阶段,癌症是局灶性的,并且包含在前列腺内。在第2阶段,癌症更大,并且可能在前列腺的两个叶中,但仍然局限于器官。在第3阶段中,癌症已经扩散到前列腺之外(例如,破坏包膜或沿着前列腺的导管向下延伸),并且可能已经侵入邻近的淋巴腺或精囊。在第4阶段,癌症已经扩散到其他器官或骨骼,这被称为转移。在某些实施方案中,前列腺癌是具有任何上述分期的癌症。我们的生物标志物的优势在于,与h&e染色相比,它们提供了最佳的癌症检测,并提供了改善的癌症(包括确立期癌症和晚期癌症)可视化,这使得能够更好地可视化癌症的位置、扩散和发病机理。
[0147]
应当理解的是,虽然参考检测人类受试者中的前列腺癌对本公开进行了描述,但是本公开考虑了检测动物受试者中的前列腺癌,因此也考虑了本公开的兽医应用。
[0148]
在某些实施方案中,受试者患有前列腺癌。前列腺癌的例子如本文所述。
[0149]
在某些实施方案中,受试者是患有前列腺癌的可能性或风险增加的受试者。在某些实施方案中,受试者是易患前列腺癌的受试者。在某些实施方案中,受试者是具有一种或多种与前列腺癌相关的风险因素的受试者。在某些实施方案中,受试者是患有前列腺癌的可能性或风险未知的受试者。
[0150]
在某些实施方案中,受试者是具有测量的或已知的psa水平的受试者。psa水平的实例如本文所述,例如,如本文实施例6中所述。在某些实施方案中,受试者是具有一个或多个附图和/或实施例中描述的一个或多个特征的受试者。
[0151]
术语“相关标志物”是指在一种或多种特定组织、细胞、细胞器和/或细胞区室中富集的任选的其他生物标志物,因此可以与其他标志物一起使用,以进一步帮助鉴定组织、细胞、细胞器和/或细胞区室。
[0152]
所选择的生物标志物包括至少以下三种:appl1、sortilin-1和syndecan-1,和/或编码上述蛋白质之一的基因/mrna、上述蛋白质/基因/mrna之一的片段、上述蛋白质/基因/mrna之一的衍生物和上述蛋白质/基因/mrna之一的加工的形式。考虑了与关键蛋白质appl1(例如,appl2、rab5、egfr、rab21、ocrl、gipc1、肌球蛋白vi)、sortilin-1(例如,glut-4、glut-1、lpl、osbp、pgrn、nts、rap)、syndecan-1(例如,syntenin-1、生存素、itgb3、itgb5、pdgf、igf1r、vegf’s、fn1、vtn、层粘连蛋白、bmp’s、pai-1、fgf’s)相互作用的其他相关生物标志物。
[0153]
应当理解,本公开的所选标志物在本文中指代所选标志物的人类形式。然而,应当理解,也考虑了等同或协同标志物的检测和/或使用。检测标志物的方法是本领域已知的。通常,在取自受试者的样品或样品的加工形式中检测受试者中存在的标志物。例如,检测蛋白质和rna的方法是已知的,并且通常可以使用市售产品来进行。包括用于蛋白质和rna检测、提取和分离的方法在内的一般方法是已知的,描述于例如ausubel等,current protocols of molecular biology,john wiley and sons(1997),其全部内容在此引入作为参考。
[0154]
检测蛋白质标志物的方法是已知的,包括例如免疫检测方法,如免疫结合、免疫印迹(例如蛋白质分析)、免疫沉淀、免疫电泳、免疫染色、免疫组织化学、分光光度法、酶测定法、质谱法和显微镜检查。考虑了其他方法。
[0155]
检测核酸的方法是已知的,包括微阵列分析、印迹(northern、southern)、原位杂交、rt-pcr、终点茎环实时rt-pcr、mir-q rt-pcr、(a)尾通用逆转录、rna扩增图谱、基于克隆的方法、基于纳米颗粒的方法、夹板连接(splinted ligation)方法、挂锁探针(padlock-probe)和滚环扩增、基于珠子的流式细胞术方法、生物发光rna检测方法、分子信标方法、核酶方法和定量lna-elf-fish方法。考虑了其他方法。
[0156]
在某些实施方案中,rna标志物的检测包括逆转录。逆转录rna的方法是本领域已知的。在某些实施方案中,rna标志物的检测包括核酸的扩增。核酸扩增的方法是本领域已知的。在某些实施方案中,rna标志物的检测包括聚合酶链式反应。在某些实施方案中,聚合酶链式反应包括定量聚合酶链式反应。
[0157]
在某些实施方案中,rna标志物的检测包括核酸与一种或多种靶核酸的结合或杂交。在某些实施方案中,rna标志物的检测包括核酸与一种或多种靶核酸的结合,所述靶核酸与固体基质如芯片结合。将核酸结合到靶核酸上,包括结合到与固体基质结合的核酸上
的方法是已知的。
[0158]
在某些实施方案中,所选标志物的检测包括聚合酶链式反应。在某些实施方案中,聚合酶链式反应包括定量聚合酶链式反应。
[0159]
在某些实施方案中,对所选标志物的检测包括免疫学检测。在某些实施方案中,免疫学检测包括elisa或免疫测定、用抗体染色、免疫组织化学和/或流式细胞术检测。涉及免疫学检测的方法是本领域已知的。
[0160]
在某些实施方案中,本文所述的方法包括检测所选标志物的存在、水平、表达、分泌和分布中的一种或多种。
[0161]
在某些实施方案中,所选标志物的改变的存在、改变的水平、改变的表达、改变的分泌和改变的分布中的一种或多种指示受试者中的前列腺癌。
[0162]
在某些实施方案中,内体标志物的水平增加和/或分泌增加指示受试者中的前列腺癌。在某些实施方案中,内体标志物的水平降低和/或分泌减少表明受试者患有前列腺癌。
[0163]
在某些实施方案中,内体生物标志物是蛋白质或核酸(如mrna)。
[0164]
在某些实施方案中,mrna标志物水平的增加指示受试者中的前列腺癌。在某些实施方案中,mrna标志物水平的降低指示受试者中的前列腺癌。
[0165]
在某些实施方案中,内体标志物的水平增加和/或分泌增加指示受试者中的前列腺癌。
[0166]
在某些实施方案中,该方法检测appl1蛋白和/或mrna水平的增加、appl1蛋白分泌的增加、sortilin-1蛋白和/或mrna分泌的增加以及syndecan-1蛋白和/或mrna的增加。在某些实施方案中,该方法检测低或高水平的appl1蛋白、高或低水平的sortilin-1和低或高水平的syndecan-1和/或mrna,其指示受试者中的前列腺癌。这三种生物标志物的所有组合都被考虑用于定义前列腺癌的致病过程。
[0167]
在某些实施方案中,一种或多种标志物的改变的存在、改变的水平、改变的表达、改变的分泌和改变的分布是与非恶性组织、前列腺上皮内瘤、原发性前列腺癌和转移性前列腺癌中的一种或多种相比。
[0168]
在某些实施方案中,与参照相比,appl1水平的增加、sortilin-1水平的增加或减少以及syndecan-1水平的增加指示受试者中的前列腺癌。在某些实施方案中,与参照相比,appl1、sortilin-1和syndecan-1水平的增加指示受试者中的前列腺癌。
[0169]
在某些实施方案中,与参照相比,appl1、sortilin-1和syndecan-1水平的增加指示受试者中的确立期前列腺癌。
[0170]
在某些实施方案中,与参照相比,appl1水平的增加、sortilin-1水平的降低和syndecan-1水平的增加指示受试者中的晚期前列腺癌(或转移性前列腺癌)。在一个实施方案中,本文定义的方法可以区分转移性前列腺癌和非转移性前列腺癌。
[0171]
在某些实施方案中,与非恶性组织相比,appl1蛋白或mrna在原发性前列腺癌中增加,与非恶性组织相比,sortilin-1蛋白或mrna在原发性前列腺癌中增加或减少,与非恶性组织相比,syndecan-1蛋白或mrna在原发性前列腺癌中增加。
[0172]
在某些实施方案中,与原发性或建立期前列腺癌相比,在转移性前列腺癌中,appl1蛋白或mrna增加,sortilin-1蛋白或mrna减少,而syndecan-1蛋白或mrna增加。
[0173]
在某些实施方案中,与参照相比,appl1分布的改变表明受试者中存在前列腺癌(如确立期前列腺癌或晚期前列腺癌)。所述分布的改变可以是,例如,从参照中的基底细胞染色到前列腺癌样品中的伴有核内含物染色的细胞质分布的变化。
[0174]
在某些实施方案中,与参照相比,syndecan-1分布的改变表明受试者中存在前列腺癌(如前列腺上皮内瘤(pin)、原发性前列腺癌或转移性前列腺癌)。所述分布的改变可以是,例如,从参照中基底细胞染色模式到前列腺癌样品中基底细胞染色模式消失的变化。
[0175]
在某些实施方案中,sortilin-1中的颗粒状染色模式指示前列腺上皮内瘤(pin)或确立期前列腺癌的存在。在一个实施方案中,sortilin-1水平与参照相比降低表明晚期癌症的存在。在一个实施方案中,sortilin-1分布的改变表明晚期癌症的存在。例如,改变的分布可以是更少颗粒和更分散的染色模式。
[0176]
术语“升高的水平”可以指与参照相比水平增加至少1.1倍、1.2倍、1.3倍、1.4倍、1.5倍、1.6倍、1.7倍、1.8倍、1.9倍、2倍、3倍、4倍、5倍、6倍、7倍、8倍、9倍、10倍、11倍、12倍、13倍、14倍、15倍、16倍、17倍、18倍、19倍、20倍、21倍、22倍、23倍、24倍、25倍、26倍、27倍、28倍、29倍、30倍、31倍、32倍、33倍、34倍、35倍、36倍、37倍、38倍、39倍、40倍、41倍、42倍、43倍、44倍、45倍、46倍、47倍、48倍、49倍、50倍、51倍、52倍、53倍、54倍、55倍、56倍、57倍、58倍、59倍、60倍、61倍、62倍、63倍、64倍、65倍、66倍、67倍、68倍、69倍、70倍、71倍、72倍、73倍、74倍、75倍、76倍、77倍、78倍、79倍、80倍、81倍、82倍、83倍、84倍、85倍、86倍、87倍、88倍、89倍、90倍、91倍、92倍、93倍、94倍、95倍、96倍、97倍、98倍、99倍或100倍或介于任意两者之间的任何值。
[0177]
本发明的某些实施方案提供了确定受试者中存在前列腺癌的可能性的方法,该方法包括检测来自受试者的生物样品中至少以下三种内体生物标志物appl1、sort1和sdc1与参照相比的改变的存在、水平、分泌和分布中的一种或多种。
[0178]
短语“存在前列腺癌的可能性”是指受试者中存在前列腺癌的可能性有多大。三种内体生物标志物appl1、sortilin-1和syndecan-1中的至少一组的水平升高指示受试者中存在前列腺癌的可能性(即机会或风险)。这可能是,例如,受试者中存在前列腺癌的可能性大于10%、20%、30%、40%、50%、60%、70%、80%、90%或99%。
[0179]
在某些实施方案中,本文所述的方法包括从受试者获得生物样品。
[0180]
在某些实施方案中,本文所述的方法包括处理生物样品以允许检测所选标志物。在某些实施方案中,本文所述的方法包括处理生物样品以允许检测本文所述的标志物,并检测经处理的样品中的标志物。在某些实施方案中,本文所述的方法包括从受试者获得生物样品,并处理该生物样品以允许检测所选择的标志物。
[0181]
术语“生物样品”是指从受试者获得的样品和/或其加工和/或处理形式。例如,生物样品可以是未处理的、稀释的、衍生物、提取物、经处理的形式、预清除的、过滤的、脱盐的、浓缩的、稀释的、缓冲的、离心的、诱导的、预处理的、经处理以从样品中去除一种或多种成分或杂质的、切片的、固定化的、粘附到载玻片上的、或其合适的组合。在某些实施方案中,直接在样品中检测选定的标志物。在某些实施方案中,在加工和/或处理后,在样品中检测选定的标志物。在某些实施方案中,在检测所选标志物之前和/或在检测所选标志物的同时,对样品进行加工和/或处理。
[0182]
生物样品的例子包括一种或多种生物流体,例如血液、血浆、尿液、羊水、眼泪、唾
液、毛发、皮肤,以及一种或多种组织样品或活检。考虑了其他类型的生物样品。
[0183]
在某些实施方案中,生物样品包括血液样品、血浆样品、血清样品、活检和前列腺组织样品中的一种或多种。
[0184]
在某些实施方案中,生物样品包括活检或组织样品。
[0185]
某些实施方案提供了检测所选标志物的原位水平。
[0186]
在某些实施方案中,所选标志物包括一种或多种血液标志物、血浆标志物和/或血清标志物。某些实施方案提供了检测选定标志物的循环水平。
[0187]
在某些实施方案中,所述检测包括定性确定。在某些实施方案中,所述检测包括定性确定所选标志物是否具有改变的存在、改变的水平、改变的表达、改变的分泌和改变的分布中的一种或多种。在某些实施方案中,所述检测包括定量确定所选标志物是否具有改变的存在、改变的水平、改变的表达、改变的分泌和改变的分布中的一种或多种。
[0188]
在某些实施方案中,所述检测包括定性确定。在某些实施方案中,所述检测包括所选标志物是否存在的定性测定。在某些实施方案中,所述检测包括所选标志物水平的定量评估。例如,某些方法允许量化所选标志物的浓度。计算或确定标志物浓度的方法是本领域已知的。
[0189]
本公开的某些实施方案包括检测两种或更多种选定的生物标志物。本公开的某些实施方案包括检测三种或更多种选定的生物标志物。本公开的某些实施方案包括检测四种或更多种选定的生物标志物。
[0190]
在某些实施方案中,本公开的方法包括检测两种或更多种选定的生物标志物。在某些实施方案中,该方法包括检测三种或更多种选定的生物标志物。在某些实施方案中,该方法包括检测四种或更多种选定的生物标志物。
[0191]
在某些实施方案中,本文所述的方法包括确定一种选定的标志物与另一种选定的标志物的水平之比。
[0192]
在某些实施方案中,生物标志物比率的改变指示受试者中的前列腺癌。在某些实施方案中,与非恶性组织相比,改变的比率指示受试者中的前列腺癌。不同类型前列腺组织之间的其他比较形式如本文所述。
[0193]
在某些实施方案中,与非恶性组织相比,appl1、sortilin-1和syndecan-1生物标志物的比率改变指示受试者中的前列腺癌。在某些实施方案中,与sortilin-1相比,appl1和syndecan-1的比率增加指示受试者中的晚期前列腺癌。
[0194]
在某些实施方案中,本公开的方法包括检测除所选生物标志物之外的一种或多种其他生物标志物。
[0195]
在某些实施方案中,如本文所述,本公开的方法提供了一种或多种生物标志物、对照生物标志物和/或参照标志物的用途。
[0196]
在一个实施方案中,参照是正常或良性前列腺组织或正常血液或血浆样品。正常或良性前列腺组织可以是来自相同受试者或不同受试者(即健康受试者)的组织。正常血液或血浆样品可以是来自不同受试者(即健康受试者)的样品。该参照也可以是截断值(例如预定的截断值)。
[0197]
生物标志物的存在、水平、表达、分泌和分布的改变通常与一种或多种相应生物标志物,例如一个或多个对照受试者和/或一个或多个已知患有前列腺癌的受试者中的一种
或多种相应蛋白质或mrna的水平相关。
[0198]
在某些实施方案中,本文所述的方法包括将所选生物标志物的存在、水平、表达、分泌和分布与一种或多种已知指示受试者中前列腺癌和/或已知指示不存在癌症的其他生物标志物进行比较。
[0199]
在某些实施方案中,本文所述的方法包括将所选生物标志物的存在、水平、表达、分泌和分布与一种或多种参照和/或对照生物标志物进行比较。
[0200]
在某些实施方案中,本文所述的方法包括将所选生物标志物的存在和/或水平与一种或多种与前列腺癌风险改变相关的其他生物标志物和/或一种或多种已知指示受试者中前列腺癌存在或不存在的其他生物标志物的存在和/或水平进行比较。
[0201]
在某些实施方案中,参照生物标志物包括内源性标志物。在某些实施方案中,参照标志物包括外源性生物标志物。例如,样品可以掺有外源性参照生物标志物。
[0202]
在某些实施方案中,本公开的方法包括处理生物样品以允许检测所选择的生物标志物。在某些实施方案中,本公开的方法包括处理从受试者获得的生物样品,以允许检测所选择的生物标志物。受试者如本文所述。
[0203]
在某些实施方案中,本文所述的方法和试剂盒包括使用一种或多种试剂来处理用于分析的样品。
[0204]
在某些实施方案中,本文所述的方法还包括获得与受试者的一个或多个临床特征相关的信息,并使用该信息结合所选标志物的存在、水平、分泌和分布中的一种或多种来检测受试者中的前列腺癌。在某些实施方案中,所述一个或多个临床特征包括年龄、体重指数、吸烟、遗传和癌症和/或前列腺癌家族史中的一个或多个。
[0205]
在某些实施方案中,本文所述的方法还包括获得与受试者的一个或多个临床特征相关的信息,并使用该信息结合所选标志物的存在、水平、表达分泌和分布中的一种或多种来检测受试者中的前列腺癌或不存在前列腺癌。
[0206]
在某些实施方案中,本文所述的方法包括使用计算机处理器装置处理与所选标志物的存在、水平、分泌和分布中的一种或多种相关的数据,以产生受试者中前列腺癌存在的可能性和/或风险。计算机处理器装置的例子是已知的。
[0207]
在某些实施方案中,该方法具有0.60或更高的检测灵敏度。
[0208]
在某些实施方案中,该方法具有0.70或更高的检测灵敏度。
[0209]
在某些实施方案中,该方法具有0.80或更高的检测灵敏度。
[0210]
在某些实施方案中,该方法具有0.90或更高的检测灵敏度。
[0211]
在某些实施方案中,该方法具有0.95或更高的检测灵敏度。
[0212]
在某些实施方案中,该方法具有0.60或更高的检测特异性。
[0213]
在某些实施方案中,该方法具有0.70或更高的检测特异性。
[0214]
在某些实施方案中,该方法具有0.80或更高的检测特异性。
[0215]
在某些实施方案中,该方法具有0.90或更高的检测特异性。
[0216]
在某些实施方案中,该方法具有0.95或更高的检测特异性。
[0217]
本发明的某些实施方案提供了检测受试者中前列腺癌的方法,该方法包括:
[0218]
●
从受试者获得生物样品;
[0219]
●
处理生物样品以允许检测至少以下三种内体标志物:appl1、sort1和sdc1;
[0220]
●
在每种生物标志物中,检测经处理的样品中所选生物标志物的改变的存在、水平、分泌和分布中的一种或多种;和
[0221]
●
识别受试者中的前列腺癌和/或癌症进展。
[0222]
本发明的某些实施方案提供了用于检测受试者中前列腺癌的方法,该方法包括:
[0223]
●
从受试者获得生物样品;
[0224]
●
处理生物样品以允许检测至少以下三种内体标志物:appl1、sort1和sdc1;
[0225]
●
在每种生物标志物中,比较所选标志物的存在、水平、分泌和分布;任选地与一种或多种已知指示受试者中存在或不存在前列腺癌的其他标志物一起使用;和
[0226]
●
识别受试者中的前列腺癌。
[0227]
本发明的某些实施方案提供了检测受试者中前列腺癌的方法,该方法包括:
[0228]
●
处理来自所述受试者的生物样品以允许检测至少以下三种内体标志物:appl1、sort1和sdc1;
[0229]
●
比较所选标志物的存在、水平、分泌和分布;任选地与一种或多种已知指示受试者中存在或不存在前列腺癌的其他标志物一起使用;和
[0230]
●
识别受试者中的前列腺癌和/或癌症进展。
[0231]
本发明的某些实施方案提供了检测受试者中前列腺癌的方法,该方法包括:
[0232]
●
从受试者获得生物样品;
[0233]
●
处理生物样品以允许检测至少以下三种内体标志物:appl1、sort1和sdc1;和
[0234]
●
检测经处理的样品中这些选定的标志物的改变的存在、水平、分泌和分布中的一种或多种;和
[0235]
●
识别受试者中的前列腺癌和/或癌症进展,
[0236]
●
其中根据生物标志物模式有效地治疗受试者的前列腺癌。
[0237]
在一个实施方案中,该方法包括推荐受试者进行主动监测。受试者可以是被发现具有与参照相比升高水平的appl1和sort1和降低水平的syndecan-1的人。
[0238]
在某些实施方案中,本文所述的方法用于诊断受试者中的前列腺癌,筛查受试者中的前列腺癌,评估预后,确定前列腺癌的转移潜能,鉴定患有前列腺癌的受试者,鉴定易患前列腺癌的受试者,确定受试者中前列腺癌的复发率,确定受试者中前列腺癌的死亡风险,对前列腺癌进行分层,区分受试者中患有前列腺癌和未患前列腺癌,确定前列腺癌是否为器官局限型癌,区分前列腺癌与良性前列腺增生、前列腺炎和前列腺炎性病况中的一种或多种,确定致病性进展,评估前列腺癌是缓慢生长的、惰性的还是侵袭性的,排除受试者中前列腺癌的存在,鉴定适于接受前列腺癌治疗和/或手术的受试者,和确定受试者患有前列腺癌的可能性或风险。
[0239]
本公开的某些实施方案提供了一种检测受试者中前列腺癌的方法,该方法基本上如本文参考任何所附实施例和/或附图所述。
[0240]
本公开的某些实施方案提供了用于鉴定患有或易患前列腺癌的受试者的方法或试剂盒。
[0241]
在某些实施方案中,该方法还包括首先鉴定受试者中psa的表达水平,并基于受试者中psa的表达水平对标志物的表达进行分层。psa水平如本文所述。
[0242]
在某些实施方案中,psa是指示前列腺癌低风险的水平。在某些实施方案中,psa水
平低于10ng/ml。
[0243]
本发明的某些实施方案提供了预测癌症治疗后受试者中前列腺癌复发风险的方法,该方法包括检测受试者的生物样品中至少以下三种内体生物标志物appl1、sort1和sdc1与参照相比的改变的存在、水平、分泌和分布中的一种或多种。
[0244]
本发明的某些实施方案提供了预测癌症治疗后受试者中前列腺癌复发时间的方法,该方法包括检测受试者的生物样品中至少以下三种内体生物标志物appl1、sort1和sdc1与参照相比的改变的存在、水平、分泌和分布中的一种或多种。
[0245]
复发风险可能是低、中或高复发风险。
[0246]
高水平的appl1和syndecan-1以及最低限度的sortilin-1或没有sortilin-1可预测约50个月内临床复发的风险。高水平的appl1和syndecan-1以及少量的sortilin-1可预测超过约120个月的临床复发风险。高水平的appl1、syndecan-1和sortilin-1可预测受试者不太可能具有临床复发。
[0247]
本公开的某些实施方案提供了用于实施本文所述方法的试剂盒。试剂盒可包含一种或多种本文所述的组分、试剂和/或说明书。试剂可以包括一种或多种能够结合appl1、sort1和sdc1的抗体。
[0248]
在某些实施方案中,试剂盒包含一种或多种试剂和/或说明书,用于确定所选生物标志物的存在、水平、表达、分泌和分布。
[0249]
该试剂盒可以包含能够结合seq id no:1、seq id no:2或seq id no:3中任何一个的氨基酸序列的抗体或其片段。
[0250]
该试剂盒可以包含能够结合seq id no:4的氨基酸序列的抗体或其片段。
[0251]
该试剂盒可以包含能够结合seq id no:6或8的氨基酸序列的抗体或其片段。
[0252]
本发明的某些实施方案还提供了包含一种或多种抗体或其片段的组合物,所述抗体或其片段结合三种内体生物标志物appl1、sort1和sdc1中的至少一组以及从患有前列腺癌的受试者获得的生物样品。所述一种或多种抗体或其片段可以与可检测标记结合。本文还提供了制备这种组合物的方法。
[0253]
本公开的某些实施方案提供了一种治疗前列腺癌的方法。
[0254]
本发明的某些实施方案提供了用于诊断(或检测)和治疗受试者中前列腺癌的方法,该方法包括:
[0255]
●
从受试者中检测appl1、sort1和sdc1;和
[0256]
●
基于检测到的所选标志物的存在、水平、分泌和分布中的一种或多种,用癌症疗法治疗受试者。
[0257]
本发明的某些实施方案提供了一种治疗受试者中前列腺癌的方法,该方法包括:
[0258]
●
从受试者中检测appl1、sort1和sdc1;和
[0259]
●
基于检测到的所选标志物的存在、水平、分泌和分布中的一种或多种,用癌症疗法治疗受试者。
[0260]
本发明的某些实施方案提供了确定受试者中存在前列腺癌的可能性和治疗受试者的方法,该方法包括检测来自受试者的生物样品中至少以下三种内体生物标志物appl1、sort1和sdc1与参照相比的改变的存在、水平、分泌和分布中的一种或多种;和治疗被发现有可能存在前列腺癌的受试者。
[0261]
本发明的某些实施方案提供了鉴定可能对癌症治疗有反应的患有前列腺癌的受试者的方法,该方法包括检测受试者的生物样品中至少以下三种内体生物标志物appl1、sort1和sdc1与参照相比的改变的存在、水平、分泌和分布中的一种或多种。
[0262]
本文还提供了将患有前列腺癌的受试者分层为对癌症治疗可能有反应者或无反应者的方法,该方法包括当与参照比较时,检测来自受试者的生物样品的三种内体生物标志物appl1、sort1和sdc1的至少一组的升高的水平。
[0263]
术语“治疗(treating)”以及相关术语如“treatment”和“treat”是指在改善受试者的病况、改善、阻止、抑制、减轻和/或减缓受试者的一种或多种症状的发展、受试者的部分或完全稳定、一种或多种症状的消退、或受试者的疾病、病况或状态的治愈方面获得所需的效果。
[0264]
在某些实施方案中,治疗包括手术干预、放射治疗和治疗剂的施用中的一种或多种。
[0265]
本文所用的“癌症治疗”也可以指手术干预、放射治疗和治疗剂的施用中的一种或多种来治疗受试者。合适的疗法还可包括使用雄激素剥夺疗法(adt)(如亮丙瑞林、戈舍瑞林、曲普瑞林、组氨瑞林、地加瑞克(degerelix)或手术阉割)或雄激素受体(ar)拮抗剂(如mdv3100、arn-509、氟他胺、比卡鲁胺、尼鲁米特或醋酸环丙孕酮)或化疗药物。某些化疗药物针对前列腺癌使用是众所周知的。这些包括卡培他滨、卡铂、环磷酰胺(cytoxan)、卡巴他赛、柔红霉素、多西他赛(taxotere)、阿霉素(adriamycin)、表阿霉素(ellence)、氟尿嘧啶(也称为5-氟尿嘧啶或5-fu)、吉西他滨、艾瑞布林、伊沙匹隆、甲氨蝶呤、丝裂霉素c、米托蒽醌、紫杉醇(taxol)、噻替派、长春新碱、长春瑞滨。
[0266]
在某些实施方案中,本发明的方法涉及在用于评估ar治疗干预、非ar治疗选择、ar治疗监测以及pet扫描和放射治疗的适用性的伴随诊断中的使用。
[0267]
如本文所述,本公开的某些实施方案提供了一种通过基于检测到的所选标志物的存在、水平、表达、分泌和分布中的一种或多种对受试者进行手术干预来治疗前列腺癌的方法。前列腺癌的手术干预方法是本领域已知的。
[0268]
如本文所述,本公开的某些实施方案提供了一种通过基于检测到的所选标志物的存在、水平、表达、分泌和分布中的一种或多种向受试者施用有效量的治疗剂来治疗前列腺癌的方法。前列腺癌的药物干预方法是本领域已知的。
[0269]
如本文所述,本公开的某些实施方案提供了一种通过基于检测到的所选标志物的存在、水平、表达、分泌和分布中的一种或多种进行放疗来治疗前列腺癌的方法。前列腺癌的放射治疗方法是本领域已知的。
[0270]
在某些实施方案中,如本文所述,当所选标志物的存在、水平、表达、分泌和分布存在中的一种或多种指示前列腺癌的存在和/或前列腺癌的可能性或风险增加时,进行治疗。
[0271]
在某些实施方案中,所选生物标志物的改变的存在、水平、表达分泌和分布水平中的一种或多种指示受试者适合接受治疗。存在、水平、表达、分泌和分布的改变如本文所述。
[0272]
在某些实施方案中,所选生物标志物水平的增加指示受试者适合接受治疗。在某些实施方案中,所选标志物水平的降低指示受试者适合接受治疗。在某些实施方案中,所选生物标志物的下调指示受试者适合接受治疗。在某些实施方案中,所选生物标志物的上调指示受试者适合接受治疗。在某些实施方案中,一种所选生物标志物的下调和/或另一种所
选生物标志物的上调指示受试者适合接受治疗。
[0273]
本公开的某些实施方案提供了在受试者中筛查前列腺癌的方法,该方法包括检测来自受试者样品的至少以下三种内体标志物:appl1、sort1和sdc1。
[0274]
本发明的某些实施方案提供了在受试者中筛查前列腺癌并确定其进展的方法,该方法包括检测来自受试者样品的至少以下三种内体标志物:appl1、sort1和sdc1,其中所选标志物的改变的存在、水平、分泌和分布中的一种或多种指示受试者中的前列腺癌和/或其进展。
[0275]
如本文所述,本公开的某些实施方案提供了如下方法:诊断受试者中的前列腺癌,筛查受试者中的前列腺癌,评估预后,确定前列腺癌的转移潜能,鉴定患有前列腺癌的受试者,鉴定易患前列腺癌的受试者,确定受试者中前列腺癌的复发率,确定受试者中前列腺癌的死亡风险,对前列腺癌进行分层,区分受试者中患有前列腺癌和未患前列腺癌,确定前列腺癌是否为器官局限型癌,区分前列腺癌与良性前列腺增生、前列腺炎和前列腺炎性病况中的一种或多种,确定致病性进展,评估前列腺癌是缓慢生长的、惰性的还是侵袭性的,排除受试者中前列腺癌的存在,鉴定适于接受前列腺癌治疗和/或手术的受试者,和确定受试者患有前列腺癌的可能性或风险。
[0276]
本公开的某些实施方案提供了在受试者中区分前列腺癌与良性前列腺增生、前列腺炎和前列腺炎性病况中的一种或多种的方法或试剂盒。
[0277]
本公开的某些实施方案提供了确定受试者中前列腺癌的致病进展的方法或试剂盒。
[0278]
本公开的某些实施方案提供了评估受试者中的前列腺癌是缓慢生长的、惰性的还是侵袭性的方法或试剂盒。
[0279]
本公开的某些实施方案提供了排除受试者中前列腺癌存在的方法或试剂盒。
[0280]
本公开的某些实施方案提供了一种鉴定适于接受前列腺癌治疗和/或手术的受试者的方法或试剂盒。
[0281]
本公开的某些实施方案提供了确定受试者患有前列腺癌的可能性或风险的方法或试剂盒。
[0282]
本公开的某些实施方案提供了鉴定用于前列腺癌诊断和/或预后的选定标志物的方法或试剂盒。本公开的某些实施方案提供了一种筛选用于前列腺癌诊断和/或预后的选定标志物的方法。
[0283]
本公开的某些实施方案提供了分离的和/或纯化的抗体,和/或其抗原结合片段。抗体及其片段如本文所述。抗体及其抗原结合片段可用于例如检测前列腺癌,例如用于本文所述的试剂盒中。
[0284]
术语“抗体”应理解为是指具有结合另一分子的抗原区域的能力的免疫球蛋白分子,包括单克隆抗体、多克隆抗体、多价抗体、嵌合抗体、多特异性抗体、双抗体和免疫球蛋白分子的片段或其组合,其具有以所需亲和力结合另一分子的抗原区域的能力,包括fab、fab’、f(ab’)2、fv、单链抗体(scfv)或多肽,其包含足以赋予特异性抗原结合的免疫球蛋白(或免疫球蛋白变体)的至少一部分,例如包含一个或多个互补决定区(cdr)的分子。
[0285]
在某些实施方案中,抗体(或其抗原结合片段)对抗原具有至少106m-1
、至少107m-1
、至少108m-1
、至少109m-1
、至少10
10
m-1
、至少10
11
m-1
或至少10
12
m-1
的亲和力。
[0286]
可以使用本领域已知的方法产生抗体。为了产生抗体,可以通过注射适当的抗原来免疫各种宿主,包括山羊、兔子、大鼠、小鼠、人和其他。根据宿主的种类,可以使用各种佐剂来增强免疫反应。这种标准佐剂包括弗氏佐剂、矿物凝胶如氢氧化铝和表面活性物质如溶血卵磷脂、普朗尼克多元醇、聚阴离子、肽、油乳剂、钥孔血蓝蛋白和二硝基酚。
[0287]
在某些实施方案中,抗体是多克隆抗体。生产和分离多克隆抗体的方法是已知的。一般来说,多克隆抗体是由b淋巴细胞产生的。典型地,多克隆抗体直接从被免疫的受试者,例如从被免疫的动物获得。免疫方法是本领域已知的。
[0288]
在某些实施方案中,抗体是单克隆抗体。可以使用通过培养中的连续分离细胞产生抗体分子的技术来制备单克隆抗体。这些技术包括但不限于杂交瘤技术、人b细胞杂交瘤技术和ebv杂交瘤技术。制备单克隆抗体的方法包括例如kohler et al.(1975)nature 256:495-497(在此引入作为参考);kozbor et al.(1985)j.immunol.methods 81:31-42(在此引入作为参考);cote et al.(1983)proc.natl.acad.sci 80:2026-2030(在此引入作为参考);和cole et al.(1984)mol.cell biol.62:109-120(在此引入作为参考)。
[0289]
在某些实施方案中,抗体和/或其抗原结合片段包含分离的抗体。在某些实施方案中,抗体和/或其抗原结合片段包含纯化的抗体。生产和分离多克隆和单克隆抗体的方法是已知的。
[0290]
术语“分离的”是指已经从其自然环境中分离出来的物种,例如核酸、多肽或抗体。本公开的某些实施方案提供了本文所述的分离的核酸、多肽、蛋白质或抗体。
[0291]
分离的核酸、多肽或抗体可以被部分或基本上纯化。在一些情况下,分离的实体处于基本上未纯化的状态,与多种其他物种相结合。在一些情况下,分离的实体处于基本上纯化的状态,基本上不含与它在自然界中或体内相结合的其他物质。术语“纯化的”是指经过某种形式的处理以增加所需物种的比例的物种。本公开的某些实施方案提供了如本文所述的纯化的核酸、多肽、蛋白质或抗体。
[0292]
在某些实施方案中,抗体具有选自由igg1、igg2a、igg2b、igg3、igm和iga组成的组的同种型。
[0293]
在某些实施方案中,抗体和/或其抗原结合片段是小鼠抗体和/或其抗原结合片段、人抗体和/或其抗原结合片段、或人源化抗体和/或其抗原结合片段。考虑了其他类型的抗体(或其抗原结合片段)。
[0294]
人源化抗体或适于不被其他哺乳动物排斥的抗体可以通过本领域已知的合适方法,包括例如表面重建或cdr移植来产生。在表面重建技术中,结合分子建模、统计分析和诱变来调整可变区的非cdr表面,以与靶宿主的已知抗体的表面相似。用于抗体表面重建的策略和方法以及用于降低不同宿主体内抗体免疫原性的其他方法是已知的,例如美国专利5,639,641中所述。抗体的人源化形式也可以通过cdr移植,即通过将例如小鼠抗体的互补决定区替换到人框架结构域中来制备。
[0295]
对抗体进行人源化的方法是已知的。例如,抗体可以如美国专利号6,180,370(在此引入作为参考);wo 92/22653(在此引入作为参考);wright et al.(1992)critical rev.in immunol.12(3,4):125-168(在此引入作为参考);和gu et al.(1997)thrombosis and hematocyst 77(4):755-759)(在此引入作为参考)中所述产生。
[0296]
人源化抗体通常具有恒定区和可变区,而不是基本上或仅仅源自人抗体的互补决
定区(cdr)和基本上或仅仅源自目的非人抗体的cdr。
[0297]
为生产“嵌合抗体”而开发的技术可以通过合适的方法进行,所述生产“嵌合抗体”例如是将小鼠抗体基因与人抗体基因拼接以获得具有适当抗原特异性和生物学活性的分子。例如,嵌合抗体可以如morrison,s.l.et al.(1984)proc.natl.acad.sci 81:6851-6855(在此引入作为参考);neuberger,m.s.et al.(1984)nature 312:604-608(在此引入作为参考);和takeda,s.et al.(1985)nature 314:452-454(在此引入作为参考)中所述制备。
[0298]
免疫测定可用于筛选以鉴定具有所需特异性的抗体和/或其抗原结合片段。
[0299]
抗体分子及其抗原结合片段也可以通过本领域已知的方法重组产生,例如通过在大肠杆菌表达系统中表达。例如,美国专利4,816,567(在此引入作为参考)中描述了一种生产重组抗体的方法。抗原结合片段也可以通过例如本领域已知的噬菌体展示技术或使用肽库来产生。
[0300]
本公开的某些实施方案提供了针对本文所述的多肽的分离的或纯化的抗体,或其抗原结合片段。
[0301]
本公开的某些实施方案还提供了如本文所述的多肽或蛋白质。
[0302]
在某些实施方案中,本文所述的多肽(或蛋白质)是分离的多肽。在某些实施方案中,本文所述的多肽(或蛋白质)是纯化的多肽。在某些实施方案中,本文所述的多肽(或蛋白质)是非天然存在的多肽。在某些实施方案中,本文所述的多肽(或蛋白质)是重组的多肽。在某些实施方案中,本文所述的多肽(或蛋白质)是合成的多肽。考虑了其他类型的多肽。
[0303]
术语蛋白质、多肽或氨基酸序列的“变体”包括例如一种或多种氨基酸插入变体、氨基酸缺失变体、氨基酸取代变体和氨基酸修饰变体(天然的和/或合成的)。
[0304]
例如,氨基酸插入变体可包含(任何所需长度的)氨基和/或羧基末端融合,以及在特定氨基酸序列中插入单个或两个或更多个氨基酸。在氨基酸序列变体具有插入的情况下,可以将一个或多个氨基酸残基插入氨基酸序列的特定位点,尽管随机插入并适当筛选所得产物也是可能的。
[0305]
氨基酸缺失变体的特征在于从序列中去除一个或多个氨基酸。氨基酸取代变体的特征在于序列中至少一个残基被去除,另一个残基被插入其位置。
[0306]
变体中的氨基酸变化可以是非保守的和/或保守的氨基酸变化,即取代带相似电荷或不带电荷的氨基酸。保守的氨基酸变化包括取代其侧链相关的氨基酸家族中的一个。天然存在的氨基酸一般分为四类:酸性(天冬氨酸、谷氨酸)、碱性(赖氨酸、精氨酸、组氨酸)、非极性(丙氨酸、缬氨酸、亮氨酸、异亮氨酸、脯氨酸、苯丙氨酸、蛋氨酸、色氨酸)和不带电荷的极性(甘氨酸、天冬酰胺、谷氨酰胺、胱氨酸、丝氨酸、苏氨酸、酪氨酸)氨基酸。苯丙氨酸、色氨酸和酪氨酸有时被共同归为芳香族氨基酸。
[0307]
借助于已知的肽合成技术,例如通过固相合成和类似方法或通过重组dna操作,可以容易地制备本文所述的多肽和氨基酸变体。在sambrook,j,fritsch,e.f.and maniatis,t.molecular cloning:a laboratory manual 2nd.ed.cold spring harbor laboratory press,new york.(1989)(通过引用并入本文),以及ausubel et al.,current protocols in molecular biology(2011),john wiley&sons,inc.(通过引用并入本文)中详细描述了
用于制备具有取代、插入或缺失的蛋白质和肽的dna序列的操作。
[0308]
术语“衍生物”是指一个物种的修饰形式。例如,多肽或蛋白质的衍生物是指多肽或蛋白质的修饰形式。这种修饰包括化学修饰,并且包括与蛋白质或肽相关的任何分子(例如碳水化合物、脂质和/或蛋白质或肽)的单个或多个取代、缺失和/或添加。术语“衍生物”也延伸至所述蛋白质和肽的所有功能性化学等价物。
[0309]
分离和/或生产多肽和蛋白质的方法是已知的,并且如sambrook,j,fritsch,e.f.and maniatis,t.molecular cloning:a laboratory manual 2nd.ed.cold spring harbor laboratory press,new york.(1989)(通过引用并入本文),以及ausubel et al.,current protocols in molecular biology(2011),john wiley&sons,inc.(通过引用并入本文)中一般性描述的。
[0310]
本公开的某些实施方案提供了检测appl1蛋白或其片段的方法,该方法包括使用如本文所述的抗体。
[0311]
本公开的某些实施方案提供了包含本文所述抗体的试剂盒。该试剂盒可包含一种或多种本文所述的其他试剂。
[0312]
本公开的某些实施方案提供了产生本文所述抗体的杂交瘤。生产杂交瘤和单克隆抗体的方法是本领域已知的。
[0313]
产生杂交瘤的典型方案如下:首先将动物(例如小鼠)暴露于选定的抗原。通常这是通过一系列的抗原注射来完成的,历时数周。一旦从哺乳动物的脾脏中分离出脾细胞,b细胞可以与永生化骨髓瘤细胞融合。通常选择骨髓瘤细胞以确保它们自身不分泌抗体,并且它们缺乏次黄嘌呤-鸟嘌呤磷酸核糖转移酶(hgprt)基因,使它们对hat培养基敏感。例如,可以使用聚乙二醇或仙台病毒完成融合。
[0314]
融合细胞在hat培养基中孵育大约10到14天。氨基蝶呤阻断允许核苷酸合成的途径,并且未融合的骨髓瘤细胞死亡,因为它们不能通过从头或补救途径产生核苷酸,因为它们缺乏hgprt。去除未融合的骨髓瘤细胞是必要的,因为它们具有生长超过其他细胞的潜力,特别是弱确立的杂交瘤。未融合的b细胞会死亡,因为它们的寿命很短。这样,只有b细胞-骨髓瘤杂交体存活,因为来自b细胞的hgprt基因是有功能的。这些细胞产生抗体,并且是永生的。然后将孵育的培养基稀释到多孔板中,达到每个孔仅含有一个细胞的程度。由于孔中的抗体由相同的b细胞产生,它们将指向相同的表位,因此是单克隆抗体。
[0315]
下一阶段是快速初级筛选过程,该过程仅鉴定和选择那些产生具有适当特异性的抗体的杂交瘤。然后孵育杂交瘤培养物上清液、二级酶标志物的缀合物和生色或荧光底物,有色产物的形成指示阳性杂交瘤。或者,也可以使用免疫细胞化学筛选或流式细胞术。
[0316]
产生所需抗体的b细胞可以被克隆以产生许多相同的子克隆。含有白细胞介素-6的补充培养基对这一步是必不可少的。一旦杂交瘤菌落确立,它将在培养基如rpmi-1640(含抗生素和胎牛血清)中持续生长并产生抗体。
[0317]
最初用多孔板培养杂交瘤,筛选后,换成更大的组织培养瓶。这维持了杂交瘤的健康,并提供了用于冷冻保存的足够的细胞和用于后续研究的上清液。培养物上清液可产生1至60μg/ml的单克隆抗体,其保持在-20℃或更低,直到需要。
[0318]
通过使用培养物上清液或纯化的免疫球蛋白制剂,可以在反应性、特异性和交叉反应性方面对潜在的产生单克隆抗体的杂交瘤进行进一步分析。
[0319]
最后,标准技术可用于重组dna技术、寡核苷酸合成、抗体生产、肽合成、组织培养和转染。酶促反应和纯化技术可以根据制造商的说明书或者如本领域通常完成的或者如本文所述进行。前述技术和程序通常可以根据本领域已知的常规方法来执行,并且如在本说明书全文中引用和讨论的各种一般和更具体的参考文献中所述。参见例如sambrook et al.molecular cloning:a laboratory manual(2d ed.,cold spring harbor laboratory press,cold spring harbor,n.y.(1989)),在此引入作为参考。
[0320]
示例性实施方案通过以下实施例来说明。应该理解,下面的描述仅仅是为了描述特定的实施方案,而不是为了限制上面的描述。
[0321]
本公开的某些实施方案提供了结合人appl1蛋白的氨基酸序列中的表位的分离的和/或纯化的抗体,其包含一种或多种assrpnqasseg(seq id no:1)、sqseesdlgeggkkr(seq id no:2)、vpdpdptkfpvnrn(seq id no:3)和/或该蛋白质的同源物、直系同源物或旁系同源物的等同区域。
[0322]
本公开的某些实施方案提供了结合人sortilin-1蛋白的氨基酸序列中的表位的分离的和/或纯化的抗体,其包含一种或多种wvsknfggkweeihk(seq id no:4)、ekdytiwlahstdpe(seq id no:5)和/或该蛋白质的同源物、直系同源物或旁系同源物的等同区域。
[0323]
本公开的某些实施方案提供了结合人syndecan-1蛋白的氨基酸序列中的表位的分离的和/或纯化的抗体,其包含一种或多种epkqanggayqkptk(seq id no:6)、shphrdmqpghhets(seq id no:7)、tprprettqlpt(seq id no:8)和/或该蛋白质的同源物、直系同源物或旁系同源物的等同区域。
[0324]
本公开的某些实施方案提供了检测appl1蛋白或其片段的方法,该方法包括使用如本文所述的appl1抗体。
[0325]
本公开的某些实施方案提供了检测sortilin-1蛋白或其片段的方法,该方法包括使用如本文所述的sortilin-1抗体。
[0326]
本公开的某些实施方案提供了检测syndecan-1蛋白或其片段的方法,该方法包括使用如本文所述的syndecan-1抗体。
[0327]
本公开的某些实施方案提供了检测受试者中前列腺癌的方法,该方法包括使用如本文所述的抗appl1抗体和/或抗sortilin-1抗体和/或抗syndecan-1抗体。
[0328]
本文公开了其他实施方案。
[0329]
在某些实施方案中,抗体或其抗原结合片段产生于一种或多种多肽,所述多肽由assrpnqasseg(seq id no:1)、wvsknfggkweeihk(seq id no:4)和epkqanggayqkptk(seq id no:6)的氨基酸序列、任何前述氨基酸序列的抗原性片段和/或任何前述氨基酸序列或其抗原性片段的变体组成。
[0330]
本公开的某些实施方案还提供了如本文所述的多肽或蛋白质。
[0331]
本公开的某些实施方案提供了由一种或多种下列氨基酸序列:assrpnqasseg(seq id no:1)、wvsknfggkweeihk(seq id no:4)和epkqanggayqkptk(seq id no:6)、任何前述氨基酸序列的片段、任何前述氨基酸序列的抗原性片段和/或任何前述氨基酸序列的变体或其抗原性片段组成的多肽。在某些实施方案中,所述多肽是分离的多肽。这些多肽,例如,可用于产生抗体。
[0332]
本公开的某些实施方案提供了包含一种或多种下列氨基酸序列:assrpnqasseg(seq id no:1)、wvsknfggkweeihk(seq id no:4)和epkqanggayqkptk(seq id no:6)、任何前述氨基酸序列的片段、任何前述氨基酸序列的抗原性片段和/或任何前述氨基酸序列的变体或其抗原性片段的非天然存在的多肽。在某些实施方案中,所述多肽是分离的多肽。这些多肽,例如,可用于产生抗体。
[0333]
本公开的某些实施方案提供了结合人appl1蛋白的氨基酸序列中的表位的分离的和/或纯化的抗体,其包含一种或多种assrpnqasseg(seq id no:1)、sqseesdlgeggkkr(seq id no:2)、vpdpdptkfpvnrn(seq id no:3)和/或该蛋白质的同源物、直系同源物或旁系同源物的等同区域。用于鉴定相关靶标的等效结合区的方法是本领域已知的。
[0334]
本公开的某些实施方案提供了结合人sortilin-1蛋白的氨基酸序列中的表位的分离的和/或纯化的抗体,其包含一种或多种wvsknfggkweeihk(seq id no:4)、ekdytiwlahstdpe(seq id no:5)和/或该蛋白质的同源物、直系同源物或旁系同源物的等同区域。用于鉴定相关靶标的等效结合区的方法是本领域已知的。
[0335]
本公开的某些实施方案提供了结合人syndecan-1蛋白的氨基酸序列中的表位的分离的和/或纯化的抗体,其包含一种或多种epkqanggayqkptk(seq id no:6)、shphrdmqpghhets(seq id no:7)、tprprettqlpt(seq id no:8)和/或该蛋白质的同源物、直系同源物或旁系同源物的等同区域。用于鉴定相关靶标的等效结合区的方法是本领域已知的。
[0336]
在某些实施方案中,本文所述的多肽(或蛋白质)是分离的多肽。在某些实施方案中,本文所述的多肽(或蛋白质)是纯化的多肽。在某些实施方案中,本文所述的多肽(或蛋白质)是非天然存在的多肽。在某些实施方案中,本文所述的多肽(或蛋白质)是重组的多肽。在某些实施方案中,本文所述的多肽(或蛋白质)是合成的多肽。考虑了其他类型的多肽。
[0337]
术语多肽或氨基酸序列的“变体”包括例如一种或多种氨基酸插入变体、氨基酸缺失变体、氨基酸取代变体和氨基酸修饰变体(天然的和/或合成的)。例如,氨基酸插入变体可包含(任何所需长度的)氨基和/或羧基末端融合以及在特定氨基酸序列中插入单个或两个或更多个氨基酸。在氨基酸序列变体具有插入的情况下,可以将一个或多个氨基酸残基插入氨基酸序列的特定位点,尽管随机插入并适当筛选所得产物也是可能的。
[0338]
氨基酸缺失变体的特征在于从序列中去除一个或多个氨基酸。氨基酸取代变体的特征在于序列中至少一个残基被去除,另一个残基被插入其位置。
[0339]
实施例
[0340]
实施例1
–
用常规光学显微镜检查解释组织免疫化学
[0341]
(i)抗体试剂
[0342]
使用肽序列assrpnqasseg(seq id no:1)、sqseesdlgeggkkr(seq id no:2)和vpdpdptkfpvnrn(seq id no:3)产生(genscript,piscataway,nj 08854,usa.)抗appl1小鼠单克隆抗体。
[0343]
使用肽序列wvsknfggkweeihk(seq id no:4)和ekdytiwlahstdpe(seq id no:5)产生(genscript,piscataway,nj 08854,usa.)抗sortilin-1小鼠单克隆抗体。
[0344]
使用肽序列epkqanggayqkptk(seq id no:6)、shphrdmqpghhets(seq idno:7)和
tprprettqlpt(seq id no:8)产生(genscript,piscataway,nj 08854,usa.)抗syndecan-1小鼠单克隆抗体。
[0345]
(ii)方法
[0346]
组织学样品的制备:
[0347]
块制备-将石蜡包埋的块以2μm切片,漂浮(42℃的反渗透纯水)到涂布的super frost plus载玻片上并风干。然后将切片在60℃下烘烤1小时,并在4℃下储存。切下连续切片用于所有分析,第一个切片用常规苏木精和伊红染色(如下所述),最后一个切片用于阴性对照。
[0348]
切片在切片机hm325或徕卡histo core autocut切片机上切割。
[0349]
(a)苏木精和伊红(h&e)染色
[0350]
试剂:
[0351]
●
埃利希氏(ehrlich’s)苏木精
[0352]
●
伊红溶液
[0353]
○
95%乙醇
[0354]
○
1%伊红y水溶液(e4009,sigma-aldrich)
[0355]
○
1%荧光桃红(phloxine)(p2759,sigma-aldrich)
[0356]
○
冰醋酸(0.05%(v/v)
[0357]
●
酸性酒精
[0358]
○
70%乙醇中的1%盐酸(30%原液)
[0359]
●
氨水
[0360]
○
0.04%氨水
[0361]
方案:
[0362]
使用自动化的st5010徕卡自动染色机xl对h&e切片进行染色,如下表所示。然后用厚度为1.5(170μm)的盖玻片滑动覆盖切片。
[0363]
[0364][0365]
(b)免疫组织化学方案。
[0366]
将切片浸入干净的二甲苯中5分钟。排出多余的二甲苯,并将切片浸入100%乙醇中。搅动切片,然后检查剩余的蜡(白色)。浸泡切片1分钟;沥干,再放入90%乙醇中1分钟。浸入流动的自来水中2分钟。如果蜡或乙醇残留,则会观察到流动的伪影。
[0367]
抗原修复;hier
–
热诱导表位修复:将切片浸入ph 6的柠檬酸盐缓冲液或ph 9的tris edta中。确保架子中的最后一个切片面向其他切片,以避免在加热过程中损坏该切片。如果只使用一个的话,包括另外250ml的水作为散热器。大火加热4分钟,直到沸腾,然后继续中火加热15分钟。取出整个容器,放入冷水浴中30分钟。在1xtbs中清洗切片5分钟。
[0368]
在tbs中使用新鲜制备的3%h2o2淬灭内源性过氧化物酶5分钟。在1xtbs中清洗切片2分钟。切片周围用dako pap笔涂抹。不要让切片变干。
[0369]
将第一抗体涂在切片上。确保溶液完全到达pap笔,以防止干燥。在室温下,在潮湿的室内孵育切片1小时。如有必要,用石蜡薄膜覆盖。
[0370]
在1xtbs中清洗切片3次,每次2分钟。
[0371]
将显色试剂涂在切片上。确保溶液完全到达pap笔,以防止干燥。在室温下,在潮湿的室内孵育切片30分钟。如有必要,用石蜡薄膜覆盖。
[0372]
在1xtbs中清洗切片3次,每次2分钟。
[0373]
配制dab溶液
–
在最后2分钟的清洗过程中,在1ml底物溶液中滴入1滴dab试剂。在室温下,将这种dab溶液涂抹在切片上,持续正好10分钟。立即用蒸馏水清洗切片。继续用蒸馏水洗涤2分钟。
[0374]
在埃利希氏苏木精中对细胞核进行反染1分钟。反染后,立即将切片浸入流动的ro水中,直到紫色变透明。
[0375]
用70%酒精中的1%酸对苏木精染色进行分色。将切片浸入酸性酒精中1-2秒钟,然后立即在流动的ro水中清洗。
[0376]“蓝色”在0.04%氨水中持续1分钟。并在水中清洗。
[0377]
在乙醇浓度的系列梯度中脱水,在二甲苯中清洁并封固在pix中:将切片浸入90%乙醇中10秒并搅拌,将切片转移到100%乙醇中再持续10秒。在二甲苯中清洁切片15秒钟,并使用24x50mm盖玻片和pix封固剂进行封固。允许在室温下过夜干燥或在固态加热板上以60℃干燥。
[0378]
ii)生物标志物的评估
[0379]
(a)首先,在低倍(4x)放大下评估appl1染色切片。这可能会突出癌症区域及其边界。在低倍下,伴有appl1的癌症区域是明显的,并且在晚期癌症区域中染色强度可能增加(图2、3、7、10,和图11-17的更大的图)。
[0380]
(b)接下来,同时使用sortilin-1和syndecan-1,分别对低级别(gleason 3级)和高级别(gleason 4级)癌症区域进行评分
[0381]
iii)组织免疫化学的解释
[0382]
(a)sortilin-1染色在低级别癌症(gleason 3级)中呈现强染色,有时在高级别癌症(》gleason 3级;图1、4、8、10和图12-16)区域中可能会出现染色减少。在低级别癌症区域,sortilin-1染色极性很强,分布在核上位置(图1、4、8、10、12-14)。sortilin-1染色强度的丧失和染色极性的丧失有时可能表明进展为更晚期的癌症(》gleason 3级)。
[0383]
(b)使用syndecan-1的低倍放大检测良性腺体,其具有强基底细胞染色(图5、9、10)以及在分泌上皮细胞层和pin组织中没有染色或具有弱染色(图9、10)。syndecan-1染色在gleason 4级和gleason 5级癌症区域中呈现中度至高度染色强度。当向gleason 4级发展时,可以在确立期癌症区域中检测到syndecan-1(图9、10、14)。具有迁移前沿的晚期癌症区域可能显示出syndecan-1的强特征性染色,同时也突出了单个癌细胞(图9、10、16、17)。syndecan-1强染色出现在高级别晚期癌症区域(图9、10、14、15、16、17)。
[0384]
实施例2-基于生物标志物的诊断/预后潜力的前列腺癌诊断和治疗选择
[0385]
三种生物标志物appl1、sortilin-1和syndecan-1描绘了前列腺癌发病机理,后两种识别了前列腺癌的两个不同的代谢阶段。生物标志物appl1可用于准确确认前列腺癌的诊断(≥95%的灵敏度和特异性;例如参见图3),而另外两种生物标志物为癌症进展的特定阶段提供了高特异性(分别参见例如图4和图5),并可用于预后(在图18中用图19-23中的临床实践应用的例子进行了总结)。sortilin-1在确立期癌症中具有特定的极化分布和增加的表达,并且可用于识别适合主动监测的患者;其中仅限于没有syndecan-1染色(参见病例研究图12)。syndecan-1可检测晚期癌症,联合appl1、sortilin-1和syndecan-1可用于将组织病理学与患者预后(生化和临床复发)联系起来,为预后提供可靠的方法(图12-18、20-22)。
[0386]
(i)方法
–
如实施例1
[0387]
(ii)appl1提供卓越的癌症可视化
[0388]
appl1绘制了前列腺切除术患者组织中癌症的分布(见图2、3和病例研究图12-17)。appl1显示了在癌组织中的细胞质分布,并且从确立期到晚期癌症表达增加,晚期癌症存在更高强度的染色(例如图3),这也显示了细胞质分布(图2、3和7)。因此,基于特定的生物标志物分布,appl1生物标志物能够准确地区分良性组织和癌组织。这使得能够非常精确地识别癌组织(参见病例研究图12-17),便于容易地对癌症分布进行可视化和限定前列腺
癌的边界(图2、3)。该生物标志物有效地绘制了癌症区域(例如图2;虚线)并且能够准确确认患者组织样品中前列腺癌的诊断(图3)。在临床实践中,这使得病理学家能够可靠地确认癌症的存在(图18、19)并观察其扩散程度(图2和病例研究图12-17)。因为生物标志物与致病过程相关联,所以它提供了癌症的完整图像视图。appl1对良性组织中的基底细胞层强烈染色(图3、7、10、11),并且在确立期癌组织中表达量增加并且改变为分布到细胞的细胞质中(例如图3)。appl1对晚期癌组织进行强烈染色(例如图3、7、10、15-17)。appl1显示出高灵敏度和特异性,并且几乎是独一无二的,因为在临床实践中很少有生物标志物对任何癌症达到这种性能(图3中的表格显示了appl1的数据)。
[0389]
(iii)sortilin-1定义了癌症确立,并且在晚期癌症中倾向于具有较低的表达和不同的分布
[0390]
sortilin-1在良性组织中具有最低表达至无表达,除非癌细胞开始形成pin组织(图8);然后该生物标志物的表达增加,并显示在确立期癌症中的极化分布(图1、4、8、10和病例研究图13)。sortilin-1在早期或确立期癌症中具有非常特征性的极化分布(例如,图4、8),并且该途径的所有元件都受雄激素调节,包括glut-4转运蛋白。sortilin-1控制这一关键途径的生物发生,特别是glut-4/glut-1囊泡形成,这有效地可视化了使用无氧糖酵解代谢或“所谓的”warburg代谢的癌细胞。在晚期癌症中,sortilin-1显示出表达降低,并且分布没有极化(例如,图4、8)。生物标志物表达的这种变化表明癌组织正在从葡萄糖代谢转换到脂质代谢,sortilin-1整体参与了这种转换过程。sortilin-1在先前已被证明为gleason 3级的癌组织中均匀表达,因此非常适合用于识别属于isup分级组1且适合主动监测的癌症患者(例如,案例研究图12)。
[0391]
(iv)syndecan-1定义晚期前列腺癌。
[0392]
syndecan-1在基底细胞中有非常强的表达,这类似于appl1,但随着pin组织的形成而消失(图5、9和10)。在早期或确立期癌症中,syndecan-1生物标志物具有有限的表达,除非癌细胞正在向更基于脂质的代谢转变(例如,图5、9和病例研究图14)。虽然代谢的转换是通过减少sortilin-1的量来控制的,但这释放了刺激脂质代谢的酶和生长因子。syndecan-1发出这种变化的信号,并增强生长因子信号传导,刺激影响细胞迁移的信号传导级联,增强血小板结合和免疫遮盖,并直接参与晚期癌症的过程。这使得syndecan-1能够用于特异性地绘制晚期癌症,识别多个淋巴结并清楚地描述癌症在哪里破坏了包膜(例如,图5,和病例研究图15-17)。因此,该生物标志物可以准确地检测晚期癌症,并且syndecan-1和sortilin-1的量的平衡使得在临床实践中能够进行更准确的gleason分级/isup分级分组(参见图18-22)。
[0393]
(v)生物标志物的组合;appl1、sortilin-1和syndecan-1提供可靠的前列腺癌评估。
[0394]
appl1以≥95%的灵敏度和特异性定义癌症的程度,以准确确认患者组织样品中前列腺癌的诊断(见图3、18、19)。在临床实践中,使用appl1生物标志物以及sortilin-1和syndecan-1来绘制感兴趣区域的特定分级(参见病例研究图12-17),但是appl1表达的增加也给出了癌症进展的明确指示(例如,图3、7和病例研究图15-17)。使用h&e组织学染色的gleason分级的可靠性仅为中等,kappa值《0.600,而isup分级分组将kappa值增加至0.728,这是相当大的,但是通过使用sortilin-1和syndecan-1ihc,isup分级分组的可靠性显著增
加至kappa值0.814;这处于几乎完美的范围内(图19)。随着癌症检测和分级可靠性的提高,患者分级分组发生了非常显著的变化(图23)。这项新技术将为临床医生和患者提供前所未有的建议,通过提供准确的诊断和预后、改善主动监测的选择并首次识别出需要立即干预的高转移风险患者,从而进行挽救生命的治疗干预。
[0395]
(vi)生物标志物的组合;appl1、sortilin-1和syndecan-1可以帮助指定isup分级分组
[0396]
使用h&e的isup分级分组具有预测生化复发(bcr;p=0.001)的显著能力,但是生物标志物sortilin-1和syndecan-1显著增加了检测bcr(p=0.0002)的能力(图20)。更重要的是,虽然基于h&e的isup分级分组不能预测临床复发(cr),但通过使用具有sortilin-1和syndecan-1生物标志物的ihc进行isup分级,这导致预测cr的显著能力(图21)。appl1、sortilin-1和syndecan-1的组合也显示了生物标志物表达的特定模式,并且当组合使用时,生物标志物能够预测临床复发的时间(图22)。高水平的appl1和最低的sortilin-1或没有sortilin-1以及高水平的syndecan-1生物标志物染色描绘了在约50个月内达到临床复发的患者,而具有高appl1和syndecan-1和少量sortilin-1的患者在约120个月后达到临床复发(图22)。sortilin-1水平高的患者不会出现临床复发。这项技术首次预测了与转移和存活直接相关的临床复发,并对患者管理具有深远的意义。
[0397]
实施例3
–
syndecan-1肽;基于对患者组织中的晚期癌症的最佳检测,epkqanggayqkptk(sedq id no.6)是产生针对syndecan-1的抗体的最佳肽。
[0398]
syndecan-1(sdc1)是一种跨膜蛋白聚糖,其包含硫酸乙酰肝素和硫酸软骨素链。syndecan-1由310个氨基酸长的核心蛋白组成,该核心蛋白由细胞外结构域(胞外域)、跨膜结构域和胞质结构域组成(图25)。它在调节许多重要过程,包括生长因子摄取、细胞粘附、细胞迁移、内吞作用、外泌体(exosome)生物发生和纤维化中发挥重要作用。syndecan-1有两种形式:膜结合的和可溶的。可溶形式是从细胞表面脱落的含有蛋白聚糖链的胞外域。人syndecan-1的蛋白水解通过不同的蛋白酶发生在许多特定位点(图25):膜相关基质金属蛋白酶mt1-mmp导致在gly82-leu83和gly245-leu246处的裂解;凝血酶在arg126-glu127(ettql)处裂解;纤溶酶在arg230-asn231(nqspv)处裂解;mmp2在gly82-leu83(leata)处裂解,mmp3在asp236-gln237(qgatg)和gly245-leu246(lldip)二者处裂解。
[0399]
针对肽epkqanggayqkptk(sedq id no.6)的syndecan-1抗体是一种独特且新颖的抗体,其针对syndecan-1的细胞质区域,允许对膜相关syndecan-1蛋白进行不同的检测,从而允许对晚期前列腺癌进行检测(参见例如图9、10、14-17)。
[0400]
实施例4-也可以在血浆中检测生物标志物appl1、sortilin-1和syndecan-1。
[0401]
(i)appl1、sortilin-1和syndecan-1提供了检测前列腺癌组织中发病机理的关键方面的一组全面的生物标志物,但也可以在血液中检测(例如,图24中的appl1),首次给出了一组直接报告独立于活检的主要发病机理的癌症生物标志物;没有其他前列腺癌生物标志物可以达到这一重要结果。我们已经开发、验证并测试了一种appl1免疫测定法,该方法在血浆中显示出高灵敏度(≥95%)和高特异性(≥93%)用于检测前列腺癌(图24)。
[0402]
(ii)方法
[0403]
用于确定衔接蛋白,磷酸酪氨酸与ph结构域和亮氨酸拉链1相互作用(appl-1)的方法具有三明治形式。msd标准结合板用抗appl-1抗体包被,然后被封闭以使非特异性结合
最小化。加入人血浆样品,孵育平板。血浆中存在的appl-1被固定化的包被抗体结合,未结合的物质被洗去。通过随后添加磺基标记的抗appl-1(seq id no.2)抗体来检测appl-1。通过加入read缓冲液产生电化学发光信号,并在msd quickplex sq 120上测量信号。产生的信号与存在的分析物的量成比例,并根据每个板上存在的校准曲线进行插值。
[0404]
(iii)试剂:
[0405]
●
吐温-20
–
sigma aldrich cat.#p1379;牛血清白蛋白(bsa)
–
sigma aldrich cat.#a7030;pbs
–
sigma aldrich cat.#p5368,p3813,p38135;使用pro uv/di水净化系统(sartorius)的超纯水;msd gold读取缓冲液
–
cat.#r92tg;对照基质(control matrix):人血浆k2edta个体并混合储存在标称-20℃或-80℃;包被缓冲液:pbs,1x(磷酸盐缓冲盐水);洗涤缓冲液(wb):pbs/t(含有0.05%吐温20的1x pbs);检测缓冲液(ab):1%bsa在pbst中:msd gold读取缓冲液:提供即用。
[0406]
●
包被抗体溶液(appl1(seq id no.1)抗体,2.00μg/ml)。如下所述,通过在包被缓冲液中稀释抗appl1(seq id no.1)抗体来制备包被抗体溶液。
[0407][0408]
●
检测抗体溶液(appl1(seq id no.2)抗体-stag,125ng/ml)。如下,通过在检测缓冲液中稀释抗appl1(seq id no.2)抗体-stag来制备检测抗体溶液。appl1(seq id no.2)抗体-stag以400μg/ml(det)提供。
[0409][0410]
●
校准曲线样品:如下,通过将appl-1蛋白加样到冰上的检测缓冲液来制备校准曲线。
[0411][0412]
●
质量/阳性对照样品:通过将appl-1蛋白加样到冰上的检测缓冲液来制备缓冲液质量对照样品。缓冲液质量对照样品将在分析当天新鲜制备。
[0413][0414]
●
血浆质量对照样品:通过筛选单一或合并的血浆并合并所有具有可检测水平的appl-1的血浆以产生具有内源性appl-1水平的新的库来制备血浆质量对照样品(pqc)。血浆质量对照品将在冰上的检测缓冲液中稀释。
[0415]
●
选择性样品的制备:如下表所示,通过将appl-1蛋白加样到冰上的单一人血浆来制备选择性样品。选择性样品可以预先制备,并在标称-80℃下以一次性使用的等分试样冷冻储存,或者在分析当天新鲜制备。
[0416]
[0417][0418]
●
平行样品的制备:通过在冰上连续稀释超高浓度人血浆来制备平行样品。平行样品将在分析当天新鲜制备。
[0419]
[0420][0421]
(iv)样品制备
[0422]
●
在分析之前,所有血浆样品将在冰上在检测缓冲液中进行五分之一的推荐样品稀释,如下所示。
[0423][0424]
(v)检测程序
[0425]
●
平板涂布:向平板的每个孔中加入50μl涂布溶液。轻轻敲击板的侧面,使溶液分布在整个板上。密封并在标称4℃下孵育14-24小时。
[0426]
●
板封闭:从冰箱(标称4℃)中取出板,用3x350μl洗涤缓冲液清洗。在纸巾上轻轻拍干。向板的每个孔中加入150μl封闭缓冲液。密封并在室温下孵育(无摇动)至少60分钟。
[0427]
●
样品制备:在冰上制备样品(包括校准曲线、qc和任何所需的验证样品)。将所有血浆样品按五分之一(1 in 5)稀释。
[0428]
●
样品孵育:用3x350μl洗涤缓冲液洗涤。在纸巾上轻轻拍干。使用多通道移液器,将50μl每种样品从管中一式两份直接添加到板上。密封并在室温下振荡(450rpm)孵育90
±
10分钟。
[0429]
检测:按照alm第2.5.7节制备检测抗体溶液。用3x350μl的洗涤缓冲液清洗平板。在纸巾上轻轻拍干。向板的每个孔中加入50μl检测溶液。密封并在室温下振荡(450rpm)孵育60
±
10分钟。
[0430]
平板读数:使用msd洗涤程序,用3x350μl洗涤缓冲液洗涤。在纸巾上轻轻拍干。向msd板的每个孔中加入150μl gold读取缓冲液。在加入读取缓冲液的10分钟内,在msd板读取器上进行。
[0431]
实施例5
–
通过lc/ms/ms测定人血浆中的syndecan-1
[0432]
(i)样品制备和提取程序:
[0433]
●
允许血浆在标称4℃/冰浆下解冻。将25μl空白样品、校准曲线样品、qc样品和受试者样品(按处理顺序)等分到1.5ml微量离心管中。用力涡旋血浆样品,使其混合。向每个孔中加入50μl消化缓冲液(db,50mm碳酸氢铵)。向任何空白样品中加入10ul ppds。向每个孔中加入10ul工作is溶液(wis,10ng/ml sil-79)(空白除外)。短暂涡旋混合,例如2*1秒,中间暂停,让液体沉淀在底部。
[0434]
●
酶消化前置于冰浆中平衡。就在第一次加入之前,新鲜制备10.0mg/ml的胰蛋白酶溶液(ts)。将1.0ml(注意:调整td(胰蛋白酶稀释液)的体积,使其与胰蛋白酶的实际重量完全匹配,从而得到10.0mg/ml)冷td加入到在5ml蛋白低结合eppendorf小瓶中的预称重的冷冻的约10mg胰蛋白酶中。短暂涡旋溶解。储存在冰浆中。注:胰蛋白酶稀释液-1mm hcl,20mm cacl2在milliq水中。向上述制备的样品中加入10.00μl新鲜制备的ts。在处理下一个样品之前,对每个样品执行以下所有步骤。
[0435]
●
以20为一批添加ts,即在完成向该批第一个样品添加ts后≥10分钟,开始添加ths(胰蛋白酶终止溶液)。涡旋2次,中间有停顿,让液体排到底部。向制备好的样品中加入10.00μl ths。涡旋2次,中间有停顿,让液体排到底部。
[0436]
●
使用multipette,向每个eppendorf小瓶中加入1.0ml licl-4deg,涡旋2次,并置于-80
°
冰箱中至少30分钟。
[0437]
●
冲洗:从冷藏室中取出所需的spe溶液,使其达到室温。从-80储存中取出稀释的经消化的血浆,放入冰浆中解冻。启动微量离心机,平衡至4度,准备旋转。cba
–
安捷伦结合洗脱cba柱,100mg,1ml,40um。样式:直筒柱。part#12102011。允许所有添加到spe柱中的溶液仅通过重力流动。如果流动明显停止,则使用50ml注射器轻轻推动,并记录观察结果。使用multipette,将1.0ml的tb(tris缓冲液,0.1m tris缓冲液,ph 8.7)添加到每个cba柱中。然后,将1.0ml的f1(冲洗#1,30%乙腈/1%tfa)添加到每个cba柱中。向每个cba柱中加入1.0ml f2(冲洗#2,80%乙腈/1%tfa)。
[0438]
●
调节:使用multipette,向每个cba柱中加入1.0ml甲醇。使用multipette,将1.0ml甲醇分三组添加到cba柱中,并用力推动以排出任何残留空气。确保cba吸附剂床不会排出任何液体,即始终保持液面高于吸附剂床顶部玻璃料(frit)。
[0439]
●
平衡:使用multipette,向每个cba柱中加入1.0ml licl-rt(100mm licl,室温下使用)。使用multipette,向每个cba柱中加入1.0ml licl-rt(100mm licl,室温下使用)。
[0440]
●
样品装载:涡旋稀释的经消化的血浆,暂停,重复,确保空气涡旋到达底部以完全混合。在13.2k和4度下旋转10分钟。放置微量离心管,铰合部(hinge)朝外。放回冰浆中。继续装载样品,不得无故拖延。将cba柱从spe歧管转移到单独标记的15ml蓝色顶部falcon
管中。取出1.0ml上清液。将微量离心管倾斜45度,铰合部朝上。小心地从离底部最远的液体顶部除去上清液,以确保没有ppt被取样(可能会堵塞spe柱)。
[0441]
●
洗涤:向每个cba柱中加入1.0ml licl-rt(100mm licl,室温下使用)。向每个cba柱中加入1.0ml10-tris(10%tb/90%100mm licl)。
[0442]
●
丢弃:使用multipette,将200ul的50-tris(50%tb/50%100mm licl)添加到每个cba柱中。
[0443]
●
洗脱:将10μl keeper(keeper-未稀释的血浆沉淀溶液)添加到用于捕获洗脱步骤的10ml管的底部。将cba柱从15ml蓝色顶部falcon pp管转移至10ml管。使用multipette,将250ul 50-tris添加到每个cba柱中。使用multipette,将250ul 50-tris添加到每个cba柱中。取出spe柱,密封在50ml蓝色falcon管中,储存在4度。确保在从10ml黄色顶部洗脱管中取出spe柱之前抖掉所有悬滴。涡旋洗脱管3次,中间有明显的停顿,以便每次将所有液体排到底部。将500ul洗脱液转移至0.5ml锥形pp hplc小瓶并加盖。检查每个小瓶的锥形底部,确保没有任何气泡。如果有起泡,用手指轻敲小瓶底部,直到气泡释放出来。
[0444]
实施例6-基于mrna表达变化的前列腺癌诊断
[0445]
前列腺癌存在的诊断可基于本文所述任何标志物的的一种或多种mrna的mrna表达水平、本文所述标志物蛋白的水平、本文所述标志物蛋白的分泌、本文所述生物流体中标记物蛋白的存在中的一种或多种,或基于本文所述任何标志物蛋白的组织或活检样品的免疫组织学。
[0446]
可以使用的选定的标志物的例子包括一种或多种下列蛋白质或它们的mrna:组织蛋白酶b,capthesin d,α-半乳糖苷酶,rab7,limp-1,limp-2,tfr1,tfr2,stamp2,sort1(sortilin),appl1,eea-1,lamp-1,rab4,appl2,rab5,rab11,rab21,肌球蛋白vi,ocrl,gipc1,mpr,pap,肌动蛋白,glut1,glut4,lpl,osbp,pgrn/grn,nts,rap,m6pr,igfr2,myo1b,pdcd6ip,sdcbp,sdc1,生存素,itgb3,itgb5,stx7,stx12,egfr,pdgf,vegf’s,fn1,vtn,pai-1,层粘连蛋白,bmp’s,fgf1,fgf2,fgf3,fgfr1,fgfr2,fgfr3,nox2和nox4。
[0447]
例如,可以使用空心针通过直肠取出前列腺组织的圆柱形样品(活检),并制备一部分样品用于组织学和免疫组织化学。如果前列腺被手术切除,病理学家可以准备前列腺组织的切片用于分析。
[0448]
可以选择appl1作为合适的标志物,并如实施例1中所述使用免疫组织化学进行分析,以使用appl1特异性抗体确定appl1的分布。appl1绘制了癌症图,描绘了癌症边缘,并显示了随着癌症在分级分组中的进展,肿瘤块内的染色显著增加。这种染色将指示前列腺癌的存在,并且具有高灵敏度和特异性,适于在临床实践中确认诊断。
[0449]
基于使用本文所述的选定的标志物的检测,除了本文所述的选定的标志物的预后价值之外,或与此结合,根据癌症的诊断和/或预后和复发程度,可获得多种治疗选择:
[0450]
(i)低复发风险:
[0451]
对临床分期为t1-t2a、gleason评分为2-6、psa《10ng/ml、预期寿命《10年的患者的治疗包括主动监测。
[0452]
对预期寿命≥10年的患者的治疗包括主动监测,或如果预测淋巴结转移的概率≥2%,则包括根治性前列腺切除术(rp),伴有或不伴有盆腔淋巴结清扫(plnd);rp是局部前列腺癌的标准疗法,包括切除前列腺和精囊,无论有或没有盆腔淋巴结;这可以使用开放式
id 6、7和8)进行的免疫组织化学比较表明,只有两种envision sciences单克隆抗体可以准确描述患者组织样品中前列腺癌的发病机理。针对syndecan-1的商用抗体和envision sciences seq id no:7不能定义前列腺癌与良性组织相比的发病机理(图26)。相比之下,两种envision sciences单克隆抗体(seq id no:6和8)准确检测到晚期前列腺癌,并可以区分良性和癌组织(图2)。因此,尽管抗体针对相同的靶蛋白,但是在syndecan-1上只有两个特定的线性序列能够描述前列腺癌患者组织样品中的发病机理。
[0470]
在使用本文所述的envision sciences单克隆抗体进行晚期癌症检测的基础上,除了本文所述的选定的标志物的预后价值之外,或与此结合,根据癌症的诊断和/或预后和复发程度,可获得多种治疗选择。
[0471]
参考用其它syndecan-1抗体获得的现有技术,很明显只有由两种envision sciences单克隆抗体检测的特定线性序列能够准确描述前列腺癌发病机理。尽管已经参考特定实施例描述了本公开,但是本领域技术人员将会理解,本公开可以以许多其他形式实施。
[0472]
实施例8
–
生物标志物appl1、sortillin-1和syndecan-1在穿刺活检切片和前列腺切除切片中同样适用。
[0473]
appl1、sortilin-1和syndecan-1提供了一组全面的生物标志物,可以在不同的前列腺癌组织样品(包括穿刺活检和前列腺切除术)中同样好地检测发病机理的关键方面。图27显示appl1、sortilin-1和syndecan-1在描述穿刺活检和前列腺切除术样品中的发病机理方面具有相似的能力。图27中描绘的病理学表明了用appl1和sortilin-1而不是syndecan-1进行ihc检测,并且是被推荐进行主动监测的患者的代表。适用于主动监测的患者的第二个例子如图28所示,再次表明了appl1和sortilin-1而不是syndecan-1。生物标志物sortilin-1和syndecan-1可以清楚地识别适合主动监测的isup分级组1(确立期癌症)的患者(图27,28)。尽管已经参考特定实施例描述了本公开,但是本领域技术人员将会理解,本公开可以直接应用于不同患者前列腺组织样品中的前列腺癌病理检测。
[0474]
实施例9-使用抗wvsknfggkweeihk(seq id no:4)和ekdytiwlahstdpe(seq id no:5)的sortilin-1抗体,证明只有一个特异性表位检测确立期前列腺癌的发病机理。
[0475]
(i)sortilin-1肽wvsknfggkweeihk(seq id no:4)的使用是基于确立期癌症的最佳检测的用于产生针对sortilin-1的抗体的最佳肽。针对肽wvsknfggkweeihk(seq id no:4)的sortilin-1抗体是一种独特的新型抗体,其针对sortilin-1的细胞外区域,允许在确立期前列腺癌中明确检测sortilin-1蛋白(图29)。这种抗体在良性分泌细胞(点状和核上)中具有最低限度的标记,并且它不标记基底细胞(图29)。在确立期前列腺癌中,sortilin-1抗体在分泌细胞(点状和核上)中是丰富的。在晚期癌症中,sortilin-1标记是颗粒状的,不再位于核上,有一些细胞质分布。
[0476]
(ii)sortilin-1肽;ekdytiwlahstdpe(seq id no:5)是另一种用于产生sortilin-1抗体的肽。针对肽ekdytiwlahstdpe(seq id no:5)的抗sortilin-1单克隆抗体也针对sortilin-1的细胞外区域,但不能有效地识别确立期或晚期前列腺癌(图29)。这种抗体不标记良性腺体中的分泌细胞和基底细胞;而在确立期和晚期前列腺癌中,这种抗体具有细胞质分布,它对于检测前列腺癌发病机理不是最佳的(图29)。
[0477]
sortilin-1肽;基于对确立期癌症的最佳检测,wvsknfggkweeihk(seq id no:4)
是针对sortilin-1的抗体产生的最佳肽,这在研究前列腺癌患者组织中的sortilin-1的任何现有技术中并非显而易见。
[0478]
在本说明书中对任何现有技术的引用不是也不应该被认为是对该现有技术在任何国家构成公知常识的一部分的承认或任何形式的暗示。
[0479]
在整个说明书中,除非上下文另有要求,否则词语“包括”或诸如“包含”或“含有”的变体将被理解为暗示包括所陈述的元素或整体或元素或整体的组,但不排除任何其他元素或整体或元素或整体的组。
[0480]
如本文所用,单数形式“一个”、“一种”和“该”包括复数方面,除非上下文已经另外指明。
[0481]
本文描述的所有方法可以以任何合适的顺序执行,除非本文另有说明或与上下文明显矛盾。本文提供的任何和所有实施例或示例性语言(例如,“诸如”)的使用仅旨在更好地阐明示例性实施方案,而不是对所要求保护的发明的范围进行限制,除非另有要求。说明书中的任何语言都不应被解释为将任何未要求保护的元素指示为必要的。
[0482]
本文提供的描述涉及可以共享共同特性和特征的几个实施方案。应当理解,一个实施方案的一个或多个特征可以与其他实施方案的一个或多个特征相结合。此外,实施方案的单个特征或特征的组合可以构成另外的实施方案。
[0483]
本文使用的主题标题仅仅是为了便于读者参考,而不应该用来限制整个公开内容或权利要求中的主题。主题标题不应用于解释权利要求的范围或权利要求的限制。
[0484]
尽管已经参照特定的实施例描述了本公开,本领域技术人员将会理解,本公开可以以许多其他形式来体现。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。