载体组合物及其用于治疗溶酶体贮积症的方法
1.相关申请本技术要求于2019年7月2日提交的临时申请ussn 62/869,781以及于2019年7月2日提交的ussn 62/869,808的权益,所述临时申请的内容通过引用以其整体并入本文。
2.序列表的并入于2020年7月1日创建且大小为611 kb,命名为“m6pt-002/01wo_seqlist.txt”的文本文件的内容在此通过引用以其整体并入。
技术领域
3.所公开的公开内容涉及用于治疗溶酶体贮积症的组合物和方法。更具体地,所公开的公开内容涉及使用改善的基因疗法和改善的酶替代疗法(ert)治疗溶酶体病症的领域。
背景技术:
4.溶酶体贮积症(lsd)涉及起因于溶酶体功能缺陷的遗传性代谢病症。目前,已鉴定了约50种不同的lsd,但这些中的少数(少于10种)据报道具有治疗。因此,本领域存在用于lsd的安全有效治疗的未满足需求。本公开内容通过酶替代疗法(ert)或基因疗法,对于这种未满足的需求提供了两种解决方案。
技术实现要素:
5.本公开内容提供了包含载体的组合物,所述载体包含编码启动子的序列、编码溶酶体酶的第一多核苷酸序列和编码修饰的n-乙酰葡糖胺-1-磷酸转移酶(glcnac-1 ptase,ptase)的第二多核苷酸序列,其中所述启动子能够驱动哺乳动物细胞中的表达,并且其中所述启动子与第一多核苷酸和第二多核苷酸可操作地连接。
6.在本公开内容的组合物的一些实施方案中,载体进一步包含编码内部核糖体进入位点(ires)的序列。在一些实施方案中,编码ires的序列位于编码溶酶体酶的序列和编码修饰的glcnac-1 ptase的序列之间。在一些实施方案中,载体从5’到3’包含编码修饰的glcnac-1 ptase的序列、编码ires的序列和编码溶酶体酶的序列。在一些实施方案中,载体从5’到3’包含编码溶酶体酶的序列、编码ires的序列和编码修饰的glcnac-1 ptase的序列。
7.在本公开内容的组合物的一些实施方案中,载体进一步包含编码切割位点的序列。在一些实施方案中,切割位点包含编码2a自切割肽的序列。
8.在本公开内容的组合物的一些实施方案中,载体是表达载体。在一些实施方案中,表达载体包含质粒。
9.在本公开内容的组合物的一些实施方案中,载体是递送载体。在一些实施方案中,递送载体包含病毒载体。在一些实施方案中,病毒载体包含aav载体或慢病毒载体。在一些实施方案中,aav载体包含分离自或衍生自血清型aav1、aav2、aav3、aav4、aav5、aav6、aav7、
aav8或aav9的aav的序列。在一些实施方案中,递送载体包含非病毒载体。在一些实施方案中,非病毒载体包含脂质体、脂质纳米颗粒(lnp)、胶束、聚合物囊泡(polymersome)、纳米颗粒、聚合物纳米颗粒或外来体。
10.在本公开内容的组合物的一些实施方案中,载体是病毒载体。在一些实施方案中,病毒载体包含aav载体或慢病毒载体。在一些实施方案中,aav载体包含分离自或衍生自血清型aav1、aav2、aav3、aav4、aav5、aav6、aav7、aav8或aav9的aav的序列。在本公开内容的组合物的一些实施方案中,载体是非病毒载体。在一些实施方案中,非病毒载体包含脂质体、脂质纳米颗粒(lnp)、胶束、聚合物囊泡、纳米颗粒、聚合物纳米颗粒或外来体。
11.在本公开内容的组合物的一些实施方案中,载体是病毒载体。在一些实施方案中,载体是慢病毒载体。在一些实施方案中,载体是腺病毒载体或腺伴随病毒(aav)载体。在一些实施方案中,aav载体包含选自aav1、aav2、aav3、aav4、aav5、aav6、aav7、aav8和aav9的血清型。在一些实施方案中,aav载体包含编码衣壳的序列,所述衣壳分离自或衍生自选自aav1、aav2、aav3、aav4、aav5、aav6、aav7、aav8和aav9的一种或多种血清型。在一些实施方案中,aav载体包含编码至少一个反向末端重复(itr)的序列,所述反向末端重复分离自或衍生自选自aav1、aav2、aav3、aav4、aav5、aav6、aav7、aav8和aav9的一种或多种血清型。
12.在本公开内容的组合物的一些实施方案中,载体是双顺反子载体。
13.在本公开内容的组合物的一些实施方案中,载体是多顺反子载体。
14.在本公开内容的组合物的一些实施方案中,启动子包含普遍存在的启动子。在一些实施方案中,启动子能够驱动哺乳动物细胞中的表达。在一些实施方案中,启动子能够驱动人细胞中的表达。
15.在本公开内容的组合物的一些实施方案中,启动子包括细胞类型特异性启动子。在一些实施方案中,启动子能够驱动哺乳动物细胞中的表达。在一些实施方案中,启动子能够驱动人细胞中的表达。在一些实施方案中,启动子能够驱动神经细胞中的表达,所述神经细胞包括但不限于神经元或神经胶质细胞。在一些实施方案中,启动子能够驱动肌细胞中的表达,所述肌细胞包括但不限于平滑肌细胞、横纹肌细胞或心肌细胞。在一些实施方案中,启动子能够驱动肺细胞中的表达。在一些实施方案中,启动子能够驱动骨细胞中的表达。在一些实施方案中,启动子能够驱动血细胞中的表达,所述血细胞包括但不限于红血细胞、白血细胞、其祖细胞或造血干细胞。在一些实施方案中,启动子能够驱动免疫细胞中的表达,所述免疫细胞包括但不限于t细胞、b细胞或巨噬细胞。在一些实施方案中,启动子能够驱动脾或胰腺细胞中的表达。在一些实施方案中,启动子能够驱动肾细胞中的表达。
16.在本公开内容的组合物的一些实施方案中,启动子是人嗜t淋巴细胞病毒i型(htlv-i)启动子。
17.在本公开内容的组合物的一些实施方案中,启动子是cbh启动子。在一些实施方案中,cbh启动子包含与修饰的鸡β-肌动蛋白启动子融合的cmv早期增强子。
18.在本公开内容的组合物的一些实施方案中,启动子是cef或hcefi启动子。在一些实施方案中,hcefi启动子包含与人ef1a启动子可操作连接的人cmv增强子。在一些实施方案中,hcefi启动子包含seq id no: 161的序列。
19.在本公开内容的组合物的一些实施方案中,启动子包含组成型启动子。在一些实施方案中,组成型启动子包含巨细胞病毒(cmv)启动子。
20.在本公开内容的组合物的一些实施方案中,载体包含seq id no: 1的核酸序列。
21.在本公开内容的组合物的一些实施方案中,编码修饰的glcnac-1 ptase的多核苷酸包含seq id no: 4的核酸序列。
22.在本公开内容的组合物的一些实施方案中,溶酶体酶涉及如表1a、表1b或表1c中列出的至少一种溶酶体贮积症(lsd)。
23.在本公开内容的组合物的一些实施方案中,溶酶体酶包含表1a、表1b或表1c中列出的至少一种溶酶体酶。
24.在本公开内容的组合物的一些实施方案中,溶酶体酶选自β-葡糖脑苷脂酶(gcase/gba,由gba基因编码)、半乳糖神经酰胺酶(galc)、α-半乳糖苷酶(由gla基因编码)、α-n-乙酰氨基葡糖苷酶(naglu)、酸性α-葡糖苷酶(gaa)和溶酶体酸性α-甘露糖苷酶(laman)。
25.在本公开内容的组合物的一些实施方案中,溶酶体酶包含β-葡糖脑苷脂酶(gcase/gba)。在一些实施方案中,编码溶酶体酶的多核苷酸包含seq id no: 5的核酸序列。
26.在本公开内容的组合物的一些实施方案中,溶酶体酶包含半乳糖神经酰胺酶(galc)。在一些实施方案中,编码溶酶体酶的多核苷酸包含seq id no: 6的核酸序列。在一些实施方案中,编码溶酶体酶的多核苷酸包含seq id no: 23的核酸序列。
27.在本公开内容的组合物的一些实施方案中,溶酶体酶包含α-半乳糖苷酶(gla)。在一些实施方案中,编码溶酶体酶的多核苷酸包含seq id no: 7的核酸序列。
28.在本公开内容的组合物的一些实施方案中,溶酶体酶包含α-n-乙酰氨基葡糖苷酶(naglu)。在一些实施方案中,编码溶酶体酶的多核苷酸包含seq id no: 8的核酸序列。
29.在本公开内容的组合物的一些实施方案中,溶酶体酶包含酸性α-葡糖苷酶(gaa)。在一些实施方案中,编码溶酶体酶的多核苷酸包含seq id no: 9的核酸序列。
30.在本公开内容的组合物的一些实施方案中,溶酶体酶包含溶酶体酸性α-甘露糖苷酶(laman)。在一些实施方案中,编码溶酶体酶的多核苷酸包含seq id no: 10的核酸序列。
31.本公开内容提供了治疗溶酶体贮积症(lsd)的方法,该方法包括向受试者施用有效量的本公开内容的组合物,其中所述组合物增加导致lsd的溶酶体酶的磷酸化,从而治疗lsd。本公开内容提供了治疗溶酶体贮积症(lsd)的方法,该方法包括向受试者施用有效量的本公开内容的组合物,其中所述组合物增加导致lsd的溶酶体酶的n联寡糖磷酸化,从而治疗lsd。在一些实施方案中,受试者呈现lsd的体征或症状。在一些实施方案中,受试者已被诊断有lsd。
32.本公开内容提供了预防溶酶体贮积症(lsd)发生或发作的方法,该方法包括向受试者施用有效量的本公开内容的组合物,其中所述组合物增加导致lsd的溶酶体酶的磷酸化,从而预防受试者中的lsd发生。在一些实施方案中,受试者处于lsd发生或发作的风险中。在一些实施方案中,受试者呈现lsd的体征或症状。
33.本公开内容提供了改善导致溶酶体贮积症(lsd)的溶酶体酶的磷酸化的方法,该方法包括向受试者施用有效量的本公开内容的组合物,其中所述组合物增加溶酶体酶的磷酸化。在一些实施方案中,受试者呈现lsd的体征或症状。在一些实施方案中,受试者处于lsd发生或发作的风险中。在一些实施方案中,受试者已被诊断有lsd。
34.本公开内容提供了改善导致溶酶体贮积症(lsd)的溶酶体酶的磷酸化的方法,该方法包括使有效量的本公开内容的组合物与细胞接触,其中所述组合物增加溶酶体酶的磷酸化。在一些实施方案中,细胞是在体外或离体的。在一些实施方案中,细胞是在体内的。在一些实施方案中,受试者包含细胞。在一些实施方案中,受试者呈现lsd的体征或症状。在一些实施方案中,受试者处于lsd发生或发作的风险中。在一些实施方案中,受试者已被诊断有lsd。
35.在本公开内容的方法的一些实施方案中,溶酶体酶涉及如表1a、表1b或表1c中列出的至少一种溶酶体贮积症(lsd)。
36.在本公开内容的方法的一些实施方案中,溶酶体酶是如表1a、表1b或表1c中列出的至少一种。
37.在本公开内容的方法的一些实施方案中,溶酶体酶包含β-葡糖脑苷脂酶(gcase/gba)、半乳糖神经酰胺酶(galc)、α-半乳糖苷酶(gla)、α-n-乙酰氨基葡糖苷酶(naglu)、酸性α-葡糖苷酶(gaa)和溶酶体酸性α-甘露糖苷酶(laman)中的一种或多种。
38.在本公开内容的方法的一些实施方案中,施用包含全身施用途径。在一些实施方案中,全身施用途径是肠内、肠胃外、经口、肌内(im)、皮下(sc)、静脉内(iv)、动脉内(ia)、脊柱内、心室内、鞘内、脑室内。
39.在本公开内容的方法的一些实施方案中,施用包含局部施用途径。
40.在本公开内容的方法的一些实施方案中,受试者是人。在一些实施方案中,受试者是男性。在一些实施方案中,受试者是女性。
附图说明
41.为了说明本公开内容的目的,在附图中描绘了本公开内容的某些实施方案。然而,本公开内容并不限于附图中描绘的实施方案的精确布置和手段。
42.专利或申请文件含有至少一幅彩色绘图。本专利或专利申请公开的带有彩色附图的副本将在请求和支付必要费用后由专利局提供。
43.图1a-1c是描绘s1-s3双顺反子载体的一系列图解和图。图1a:cmv-s1s3载体。图1b:pll01: pcmv-mcs-ires-s1s3载体。图1c:说明cmv-s1s3和pll01的表达水平的图(cpm:每分钟计数)。
44.图2a-2c是描绘在s1-s3双顺反子载体中生成gba双顺反子表达质粒的一系列图解和直方图。图2a:pll11: pcmv-hgba-ires-s1s3载体。图2b:条件培养基中的gba活性。图1c:说明ptase活性百分比的直方图。
45.图3a-3c是显示双顺反子表达增加gba酶的磷酸化的一系列图和直方图。
46.图4a-4d是显示双顺反子表达增加gaa酶的磷酸化的一系列图解、图和直方图。
47.图5a-5d是显示双顺反子表达增加galc酶的磷酸化的一系列图解、图和直方图。
48.图6a-6d是显示双顺反子表达增加naglu酶的磷酸化的一系列图解、图和直方图。
49.图7a-7d是显示双顺反子表达增加gla酶的磷酸化的一系列图解、图和直方图。
50.图8a-8d是显示双顺反子表达增加laman酶的磷酸化的一系列图解、图和直方图。
51.图9a-9e是证实本公开内容的s1-s3 ptase双顺反子载体在戈谢病(a-c)的治疗中显著增加gba酶的ci-mpr结合及其细胞摄取的一系列图。图d和e证实gba酶中的单一点突变
增加其稳定性,但不影响其与ci-mpr的结合。
52.图10a-10c是证实本公开内容的s1-s3 ptase双顺反子载体在庞贝病的治疗中显著增加gaa酶的ci-mpr结合及其细胞摄取的一系列图。
53.图11a-11c是证实本公开内容的s1-s3 ptase双顺反子载体在克拉伯病的治疗中显著增加galc酶的ci-mpr结合及其细胞摄取的一系列图。
54.图12a-12c是证实本公开内容的s1-s3 ptase双顺反子载体在mps iiib疾病的治疗中显著增加naglu酶的ci-mpr结合及其细胞摄取的一系列图。
55.图13a-13c是证实本公开内容的s1-s3 ptase双顺反子载体在法布里病的治疗中显著增加gla酶的ci-mpr结合及其细胞摄取的一系列图。
56.图14a-14c是证实本公开内容的s1-s3 ptase双顺反子载体在α-甘露糖苷贮积症的治疗中显著增加laman酶的ci-mpr结合及其细胞摄取的一系列图。
57.图15a-15b是证实由aav9载体递送的本公开内容的s1-s3 ptase双顺反子载体可以用作粘脂质贮积病的治疗中的基因疗法的示意图解和图。
58.图16a-16b是描绘在20周龄的gaucher
d409v/null
小鼠的肝、肺和脾中观察到的葡萄糖神经酰胺水平升高的一对图。在组织匀浆中确定gba的天然底物葡糖脑苷脂的累积。gc在肺中的累积是具有统计学和治疗价值的结果,其是目前护理标准的已知的未满足需求。通过加入200
ꢀµ
l甲醇/acn/h2o (v:v:v=85:10:5),以800 rpm混合5分钟,随后以3220 g 4℃离心15分钟,提取20
ꢀµ
l等份试样的组织匀浆,并且适当的对照是葡萄糖神经酰胺;3). 回收50
ꢀµ
l上清液,用氮干燥并且用甲醇/acn/h2o (v:v:v=85:10:5)重悬浮,并且直接进样用于lc-ms/ms分析。
59.图17a-17c是证实与伊米苷酶相比,gcase
m6p
在gba
d409v/null
小鼠模型中具有更长的半衰期和更大的组织摄取的一系列图。使用标准护理、伊米苷酶和纯化的gba (其通过利用编码s1-s3 ptase和gba的天然变体的双顺反子载体在expi293细胞中的瞬时共表达产生),执行戈谢d409v/null小鼠模型中的pk/pd研究。这种gcase变体在中性和弱碱性条件下具有更大的稳定性。简言之,3只动物接受了~ 1.5 mg/kg重组gcase的尾静脉注射。对于血清药代动力学数据,在2、10、20、40和60分钟收集血浆样品。使用合成底物4-甲基伞形酮-β-d-吡喃葡糖苷(4mu-glc)测量活性。通过将2分钟时间点设定为100%活性,并且随后的时间点是t=2分钟时间点的百分比,使各个动物中的活性标准化。在s1-s3 ptase的存在下表达的稳定gcase似乎具有更长的半衰期。这种更长的半衰期是具有更大稳定性的酶和不同清除途径的组合。为了确定多少gcase由组织吸收,在酶注射后2小时,回收组织、匀浆化并使用4mu-glc底物测量活性。如通过用于蛋白质测定的bca方法确定的,活性针对匀浆中的总蛋白质进行标准化。在显示的组织摄取数据中,观察到具有适当磷酸化的稳定gcases的真正优点。对于所有评估的组织,在利用双顺反子s1-s3 ptase载体平台s1’s3 ptase表达的稳定gcase中,发现更多活性。这在其中伊米苷酶具有很少活性的肺、肌肉和脑中最为显著。当将组织和血清数据放在一起时,具有更高n联寡糖磷酸化的更稳定gcase的优点对于将更多酶递送到受影响的组织是显而易见的。这是第一次已以这些剂量将显著量的gcase递送到肺、肌肉和心脏。
60.图18a-18e是一系列照片和条形图,其证实在gba
d409v/null
小鼠模型中,gcase
m6p ert比伊米苷酶更好地减少组织巨噬细胞(抗cd68染色)。使用标准护理、cerezyme和纯化的
gba (m0111) (其利用双顺反子载体在expi293细胞中瞬时共表达,所述双顺反子载体编码s1s3 ptase以及在中性和弱碱性条件下具有报道的更大稳定性的gba的天然变体),执行d409v戈谢小鼠模型中的功效研究。~20周龄的戈谢小鼠每周用~1.5 mg/kg)酶治疗一次,共4周。4周后,收获肝和肺组织并在4%多聚甲醛-pbs,ph 7.4中固定,用于使用cd68抗体的免疫组织化学。与目前护理标准相比,m0111具有更大的功效,如通过如经由cd68 ab显现的受影响组织中的巨噬细胞减少所证明的。
61.图19a-19c是一系列照片,其证实在gba
d409v/null
小鼠模型中,gcase
m6p ert比伊米苷酶更好地减少戈谢贮存细胞的数目和大小(苏木精和伊红(h&e)染色)。使用标准护理、cerezyme和纯化的gba (其利用双顺反子载体在expi293细胞中瞬时共表达,所述双顺反子载体编码s1-s3 ptase以及在中性和弱碱性条件下具有报道的更大稳定性的gba的天然变体),执行d409a戈谢小鼠模型中的功效研究。~20周龄的戈谢小鼠每周用~1.5 mg/kg酶治疗一次,共4周。4周后,收获肝和肺组织并在4%多聚甲醛-pbs,ph 7.4中用于福尔马林固定,用于苏木精和伊红(h&e)染色。与目前护理标准相比,gcase
m6p
具有更大的功效,如通过如经由h&e染色显现的受影响组织中的贮存细胞减少所证明的。
62.图20a-20b是证实在gba
d409v/null
小鼠模型中,gcase
m6p ert比伊米苷酶更好地减少累积底物的一对图。~20周龄的戈谢小鼠每周用~1.5 mg/kg酶治疗一次,共4周。收集组织样品并匀浆化用于糖基神经酰胺分析。在组织匀浆中确定gcase的天然底物葡糖脑苷脂的累积。具有重要价值的是在肺中的gc累积,其是目前护理标准的已知的未满足需求。通过加入200
ꢀµ
l甲醇/acn/h2o (v:v:v=85:10:5),以800 rpm混合5分钟,随后以3220 g 4℃离心15分钟,提取20
ꢀµ
l等份试样的组织匀浆,并且适当的对照是葡萄糖神经酰胺。回收50
ꢀµ
l上清液,用氮干燥并且用甲醇/acn/h2o (v:v:v=85:10:5)重悬浮,并且直接进样用于lc-ms/ms分析。对于测量的两种神经酰胺,与伊米苷酶相比,gcase
m6p
治疗的动物在ert疗法之后具有较低的水平。
63.图21a-21d是显示体内aav介导的基因疗法研究用于治疗戈谢病的结果的一系列图。为了确定用具有三种不同启动子的稳定gba s1-s3 ptas转基因的双顺反子表达的aav9基因疗法的效应,15周龄的gba
d409v/null
小鼠用中等剂量的aav9-稳定的gba s1-s3 ptase,5e11vg进行给药。为了确定多少gba由组织生成,在aav9注射后2周,回收组织、匀浆化并使用4mu-glc底物测量活性。如通过用于蛋白质测定的bca方法确定的,活性针对匀浆中的总蛋白质进行标准化。
64.图22a-22c是描绘使用溶酶体α-甘露糖苷酶(laman)作为ert的体外研究结果的一系列图。
65.图23a-23b是描绘laman酶表达、纯化和表征的照片和相应的数据表。两种laman制剂伴随(m0611)或不伴随编码s1-s3 ptase的双顺反子载体在expi293细胞中瞬时共表达。两者均通过利用hpc4亲和标签进行纯化。通过测量以剂量依赖性方式与固定的不依赖于阳离子的甘露糖6-磷酸受体结合的laman的量,证实了磷酸化的显著增加。所结合的laman的量基于其使用其合成底物4-甲基伞形酮-α-d-吡喃甘露糖苷(4mu-man)的活性。通过添加的甘露糖6-磷酸阻断结合的能力,确认了经由磷酸化的寡糖的结合特异性。值得注意的是,即使在m6p的存在下,laman m6p (m0611)也结合受体的能力。选择laman m6p (m0611,p-0030)和laman (p-0031)用于体内动物研究。
66.图23c是描绘laman m6p (m0611)酶表达、纯化和表征的图。两种laman制剂伴随或不伴随编码ptase的s1-s3变体的双顺反子载体在expi293细胞中瞬时共表达。两者均通过利用hpc4标签进行纯化。通过测量以剂量依赖性方式与固定的不依赖于阳离子的甘露糖6-磷酸受体结合的laman的量,证实了磷酸化的显著增加。所结合的laman的量通过使用合成底物4-甲基伞形酮-α-d-吡喃甘露糖苷(4mu-man)的活性进行确定。通过添加的甘露糖6-磷酸阻断结合的能力,确认了经由磷酸化的寡糖的结合特异性。值得注意的是,即使在m6p的存在下,m0611也结合受体的能力。选择laman m6p (m0611,p-0030)和laman (p-0031)用于体内动物研究。
67.图24a-24b是证实用于酶替代疗法的laman和laman
m6p
酶在野生型小鼠中的生物分布的一对图。为了评估laman和laman
m6p (与s1-s3 ptase共表达的laman)之间的组织摄取差异,经由尾静脉将2 mg/kg的每种制剂注射到野生型小鼠(n=4)内。在给药后2和8小时,回收组织、匀浆化并使用4mu-man底物测量活性。如通过用于蛋白质测定的bca方法确定的,活性针对匀浆中的总蛋白质进行标准化。在组织摄取数据中观察到laman
m6p (与s1s3 ptase共表达的laman)的优点。对于肝、脾、心脏、肺和脑,在2小时的组织中存在更大的活性。除了肺之外,这一趋势在8小时也是如此。这可能是在分析这种组织时观察到的高变化的结果。这种观察的唯一例外是肾。从所有样品中扣除内源性laman活性。在用我们的laman
m6p
酶注射的小鼠的大多数组织中,检测到更高的laman酶活性。
68.图25a-25b是证实用于酶替代疗法的αlaman和laman
m6p
酶在野生型小鼠中的生物分布的一对图。为了评估laman和laman
m6p (与s1-s3 ptase共表达的laman)之间的组织摄取差异,经由尾静脉将10 mg/kg的每种制剂注射到野生型小鼠(n=4)内。在给药后2和8小时,回收组织、匀浆化并使用4mu-man底物测量活性。如通过用于蛋白质测定的bca方法确定的,活性针对匀浆中的总蛋白质进行标准化。在组织摄取数据中观察到laman
m6p (与s1-s3 ptase共表达的laman)的优点。对于肝、脾、心脏、肺和脑,在2小时的组织中存在更大的活性。除了肾之外,这一趋势在8小时也是如此。这可能是在分析这种组织时观察到的高变化的结果。
69.图26a-26b是描绘用于粘脂质贮积症基因疗法(gtx)的aav9设计和体外测试的示意图解和图。293t细胞用各种m0021 (aav9-cagp-s1-s3)病毒进行转导,并且在ptase活性测定法前培养2天。
70.图27a-27b是证实m0021治疗降低ml ii小鼠中的血清溶酶体酶水平的一对图。为了确定s1-s3 ptase基因疗法的效应,34周龄的雌性小鼠用中等剂量的m0021 (aav9-cagp-s1-s3) ,4e12 vg (2e13 vg/kg)进行给药。ml ii的表型之一是由于其无法靶向细胞内的溶酶体,溶酶体酶的血清水平升高。当在接受疗法仅1周后的血清中,存在laman和manb活性的降低时,观察到令人鼓舞的结果。这个结果很重要,因为它证实了影响所描述的mlii小鼠模型表型的能力。
71.图28a-28c是证实m0021治疗增加ml ii中的溶酶体酶的磷酸化的一系列图。为了进一步理解关于s1-s3 ptase基因疗法在降低laman和manb的血清活性方面的影响,使用较早描述的固定化受体结合测定法,评估了血清中发现的酶的ci-mpr结合。简言之,已知的活性以渐增的量加入固定化ci-mpr中。将未结合的酶洗掉,并且使用适当的合成底物man-b-4mu (manb,laman 4mu-man (laman)测量剩余的结合酶。ml ii小鼠的aav9-s1s3基因疗法
增加了溶酶体酶的聚糖磷酸化。在3周后,血清中的总磷酸化的溶酶体酶标准化至正常水平或略微更高。
72.图29a-29c是描绘在戈谢小鼠中注射aav9-htlv-gba
m6p
基因疗法后2周,肺和肝中的酶活性和所选gcase底物的一系列图。aav9-htlv-gba-s1s3也称为aav9-htlv-gba
m6p
,其中m6p表示s1s3构建体。在aav9 htlv-gba或aav9 htlv-gba
m6p (具有含有gba和s1-s3 ptase的双顺反子载体的转基因)之后两周,对于两种构建体,肝中的表达升高(图29a)。当测量肝葡糖基-β-神经酰胺水平时(图29b、c),尽管与aav9 htlv-gba治疗的动物相比,在肝中存在较低的gcase活性,但对于aav9 htlv-gba
m6p
治疗的动物,观察到累积底物的最大减少。这种更大的底物减少伴随更少的活性指示了n联寡糖磷酸化在细胞摄取和溶酶体靶向方面对于基因疗法的重要性。在肺中,aav9治疗动物的gcase活性很低。然而,aav9-htlv-gba
m6p
治疗的动物显示肺中累积的葡糖基-β-神经酰胺水平的显著减少(图29b、c)。对于aav9-htlv-gba治疗的动物,观察到很少减少。这证实了由于有效的细胞摄取和溶酶体靶向,即使在低活性水平下,具有对于ci-mpr具有高亲和力的磷酸化的转基因产物也可以导致有效的疗法。
具体实施方式
73.溶酶体贮积症(lsd)涉及起因于溶酶体功能缺陷的遗传性代谢病症。目前,已鉴定了约50种不同的lsd,但这些中的少数(少于10种)据报道具有治疗。患者目前通过酶替代疗法(ert)的静脉内输注进行治疗,所述酶替代疗法补充患者中缺失的酶,以解决其疾病症状。ert的目标是将足够量的正常酶引入缺陷细胞的溶酶体内,以清除贮存物质并恢复溶酶体功能。为了确保ert有效摄取到受影响的溶酶体内,ert必须含有高水平的甘露糖6-磷酸(m6p)。理想地,lsd患者应该通过施用缺失的酶与高度饱和水平的m6p进行治疗,以使得能够有效递送至溶酶体。然而,这个过程非常具有挑战性,因为使得能够将m6p加入溶酶体中的磷酸化过程是固有地低效的。最近发现的glcnac-1ptase的s1-s3变体显著改善了溶酶体酶的磷酸化过程。另外,需要为患者提供lsd的长期治愈的基因治疗方法。
74.本公开内容提供了用于生成与glcnac-1-磷酸转移酶的s1-s3变体可操作地连接的溶酶体酶的表达载体、组合物和方法。glcnac-1-磷酸转移酶的s1-s3变体显著增加了可操作连接的溶酶体酶进入细胞内和离开血清或肾的转运,用于增加的更新、分布和溶酶体酶促活性。
75.本公开内容提供了用于生成与glcnac-1-磷酸转移酶的s1-s3变体可操作地连接的溶酶体酶的基因治疗载体、组合物和方法。本公开内容证实了s1-s3变体的表达增加了内源性溶酶体酶的摄取、分布和活性。
76.本公开内容提供了通过经由新型双顺反子载体与s1-s3 ptase共表达,用于生成具有适当磷酸化的n联寡糖的溶酶体酶的ert、载体、组合物和方法。s1-s3 ptase和溶酶体酶的双顺反子表达显著增加了所表达的溶酶体酶的m6p含量。具有良好磷酸化的酶允许酶的有效摄取和溶酶体递送。这允许更好的组织分布、细胞摄取、溶酶体靶向和底物减少。本公开内容提供了通过与s1-s3 ptase共表达,用于生成高表达水平或高活性水平的m6p溶酶体酶的基因治疗载体、组合物和方法。ptase的s1-s3变体的双顺反子表达显著增加了溶酶体酶中m6p的含量水平。通过在溶酶体酶的表面上的高m6p,酶可以在体外和体内以增加的
摄取、分布和功效递送到组织细胞。
77.本公开内容的载体、组合物和方法可以用于酶替代疗法(ert)。
78.可替代地或另外,本公开内容的载体、组合物和方法可以用于基因疗法。
79.许多溶酶体酶得到描述并且其在ert和基因疗法两者中的用途得到证实。重要的是,本公开内容的载体、组合物和方法可以与任何溶酶体酶一起使用,以增加溶酶体酶的细胞摄取,并且因而增加一种或多种身体组织中的溶酶体酶活性。
80.在一些实施方案中,包含可操作地连接至溶酶体蛋白的s1-s3 ptase的本公开内容的组合物和方法,在受试者的脾、脑、一个或多个肺、或者一块或多块肌肉中的一种或多种中,增加溶酶体蛋白的摄取和活性。
81.在一些实施方案中,本公开内容的包含s1-s3 glcnac-1-磷酸转移酶的载体、组合物和方法,包括其中双顺反子载体包含编码s1-s3 glcnac-1-磷酸转移酶的序列和编码溶酶体蛋白的序列的那些实施方案,在受试者的脾、脑、一个或多个肺、或者一块或多块肌肉中的一种或多种中,增加所编码的溶酶体蛋白的摄取和活性。
82.示例性实施方案本公开内容提供了包含载体的组合物,所述载体包含编码溶酶体酶的多核苷酸和编码修饰的glcnac-1磷酸转移酶(glcnac-1 ptase)的多核苷酸。
83.本公开内容提供了包含双顺反子载体的组合物,所述双顺反子载体包含编码溶酶体酶的多核苷酸和编码修饰的glcnac-1磷酸转移酶(glcnac-1 ptase)的多核苷酸。
84.在本公开内容的组合物的一些实施方案中,双顺反子载体包含定位于编码修饰的glcnac-1 ptase的多核苷酸之前和编码溶酶体酶的多核苷酸之后的内部核糖体进入位点(ires)。在一些实施方案中,双顺反子载体包含定位于编码修饰的glcnac-1 ptase的多核苷酸之后和编码溶酶体酶的多核苷酸之前的ires。
85.在本公开内容的组合物的一些实施方案中,双顺反子载体包含启动子。在一些实施方案中,双顺反子载体包含组成型启动子。在一些实施方案中,组成型启动子包含巨细胞病毒(cmv)启动子。在一些实施方案中,启动子可操作地连接至编码溶酶体酶的多核苷酸或编码修饰的glcnac-1 ptase的多核苷酸。在一些实施方案中,启动子可操作地连接至编码溶酶体酶的多核苷酸和编码修饰的glcnac-1 ptase的多核苷酸。
86.在本公开内容的组合物的一些实施方案中,双顺反子载体包含seq id no: 1的核酸序列。
87.在本公开内容的组合物的一些实施方案中,编码修饰的glcnac-1磷酸转移酶的多核苷酸包含seq id no: 4的核酸序列。
88.在本公开内容的组合物的一些实施方案中,所编码的溶酶体酶涉及如表1中列出的至少一种溶酶体贮积症(lsd)。在一些实施方案中,所编码的溶酶体酶或其变体引起如表1a、表1b或表1c中列出的至少一种溶酶体贮积症(lsd)。在一些实施方案中,在如表1a、表1b或表1c中列出的至少一种溶酶体贮积症(lsd)中,所编码的溶酶体酶或其变体的活性或功能是降低、抑制或失调的。
89.在本公开内容的组合物的一些实施方案中,溶酶体酶包含表1a、表1b或表1c中列出的溶酶体酶。在一些实施方案中,溶酶体酶包含表1a、表1b或表1c中列出的至少一种溶酶体酶。在一些实施方案中,溶酶体酶包含表1a、表1b或表1c中列出的一种或多种溶酶体酶。
在一些实施方案中,溶酶体酶选自β-葡糖脑苷脂酶(gcase,gba)、半乳糖神经酰胺酶(galc)、α-半乳糖苷酶(gla)、α-n-乙酰氨基葡糖苷酶(naglu)、酸性α-葡糖苷酶(gaa)和溶酶体酸性α-甘露糖苷酶(laman)。在一些实施方案中,溶酶体酶包含β-葡糖脑苷脂酶(gcase,gba)。在一些实施方案中,溶酶体酶包含半乳糖神经酰胺酶(galc)。在一些实施方案中,溶酶体酶包含α-半乳糖苷酶(gla)。在一些实施方案中,溶酶体酶包含α-n-乙酰氨基葡糖苷酶(naglu)。在一些实施方案中,溶酶体酶包含酸性α-葡糖苷酶(gaa)。在一些实施方案中,溶酶体酶包含溶酶体酸性α-甘露糖苷酶(laman)。在一些实施方案中,编码溶酶体酶的多核苷酸包含seq id no: 5-10的核酸序列。
90.本公开内容提供了包含双顺反子载体的组合物,所述双顺反子载体包含组成型启动子、内部核糖体进入位点(ires)和编码修饰的glcnac-1磷酸转移酶(glcnac-1 ptase)的多核苷酸。
91.在本公开内容的组合物的一些实施方案中,组合物进一步包含药学上可接受的载体。
92.在本公开内容的载体的一些实施方案中,载体是病毒载体。在一些实施方案中,病毒载体是腺病毒、腺伴随病毒(aav)、逆转录病毒或慢病毒。在一些实施方案中,病毒载体包含腺病毒。在一些实施方案中,病毒载体包含aav载体。在一些实施方案中,aav载体包含分离自或衍生自血清型aav1、aav2、aav3、aav4、aav5、aav6、aav7、aav8和aav9中的一种或多种aav的序列。在一些实施方案中,aav载体包含分离自或衍生自血清型1的aav (aav1)的序列。在一些实施方案中,aav载体包含分离自或衍生自血清型2的aav (aav2)的序列。在一些实施方案中,aav载体包含分离自或衍生自血清型3的aav (aav3)的序列。在一些实施方案中,aav载体包含分离自或衍生自血清型4的aav (aav4)的序列。在一些实施方案中,aav载体包含分离自或衍生自血清型5的aav (aav5)的序列。在一些实施方案中,aav载体包含分离自或衍生自血清型6的aav (aav6)的序列。在一些实施方案中,aav载体包含分离自或衍生自血清型7的aav (aav7)的序列。在一些实施方案中,aav载体包含分离自或衍生自血清型8的aav (aav8)的序列。在一些实施方案中,aav载体包含分离自或衍生自血清型9的aav (aav9)的序列。
93.在本公开内容的载体的一些实施方案中,载体是表达载体。在一些实施方案中,表达载体包含seq id no: 1的多核苷酸序列。
94.本公开内容提供了包含本公开内容的载体的细胞。在一些实施方案中,细胞是哺乳动物细胞。在一些实施方案中,细胞是灵长类动物细胞。在一些实施方案中,细胞是人细胞。在一些实施方案中,细胞是培养的细胞。在一些实施方案中,细胞是永生化或稳定化的细胞系。在一些实施方案中,细胞是中国仓鼠卵巢(cho)细胞。在一些实施方案中,细胞是人胚肾293 (hek293)细胞。
95.本公开内容提供了包含本公开内容的双顺反子载体的细胞。在一些实施方案中,细胞是哺乳动物细胞。在一些实施方案中,细胞是灵长类动物细胞。在一些实施方案中,细胞是人细胞。在一些实施方案中,细胞是培养的细胞。在一些实施方案中,细胞是永生化或稳定化的细胞系。在一些实施方案中,细胞是中国仓鼠卵巢(cho)细胞。在一些实施方案中,细胞是人胚肾293 (hek293)细胞。
96.本公开内容提供了包含本公开内容的组合物的细胞。在一些实施方案中,细胞是
哺乳动物细胞。在一些实施方案中,细胞是灵长类动物细胞。在一些实施方案中,细胞是人细胞。在一些实施方案中,细胞是培养的细胞。在一些实施方案中,细胞是永生化或稳定化的细胞系。在一些实施方案中,细胞是中国仓鼠卵巢(cho)细胞。在一些实施方案中,细胞是人胚肾293 (hek293)细胞。
97.本公开内容提供了药物组合物,其包含由本公开内容的载体表达的溶酶体酶和药学上可接受的载体。
98.本公开内容提供了治疗溶酶体贮积症(lsd)的方法,该方法包括向受试者施用本公开内容的组合物,从而治疗lsd。
99.本公开内容提供了治疗溶酶体贮积症(lsd)的方法,该方法包括向受试者施用治疗有效量的本公开内容的组合物,其中所述组合物增加溶酶体酶的磷酸化,从而治疗lsd。
100.本公开内容提供了治疗患有溶酶体贮积症(lsd)的受试者的方法,该方法包括向受试者施用本公开内容的药物组合物,从而增加溶酶体酶的磷酸化并治疗受试者。
101.本公开内容提供了预防有需要的受试者中的溶酶体贮积症(lsd)发生的方法,该方法包括向受试者施用本公开内容的药物组合物,从而增加溶酶体酶的磷酸化并预防受试者中的lsd发生。
102.本公开内容提供了改善有需要的受试者中导致溶酶体贮积症(lsd)的溶酶体酶的磷酸化的方法,该方法包括向受试者施用本公开内容的组合物,其中所述组合物增加溶酶体酶的磷酸化。
103.在本公开内容的方法的一些实施方案中,溶酶体酶涉及如表1a、表1b或表1c中列出的至少一种溶酶体贮积症(lsd)。
104.在本公开内容的方法的一些实施方案中,溶酶体酶包含表1a、表1b或表1c中列出的溶酶体贮积症(lsd)。在一些实施方案中,溶酶体酶包含表1a、表1b或表1c中列出的至少一种溶酶体贮积症(lsd)。在一些实施方案中,溶酶体酶包含表1a、表1b或表1c中列出的一种或多种溶酶体贮积症(lsd)。
105.酶替代疗法(ert)本文提供的是包含双顺反子表达载体的组合物,所述双顺反子表达载体包含编码溶酶体酶的多核苷酸和编码修饰的glcnac-1磷酸转移酶(glcnac-1 ptase)的多核苷酸。在一些实施方案中,所公开的双顺反子表达载体包含定位于编码修饰的glcnac-1 ptase的多核苷酸之前和编码溶酶体酶的多核苷酸之后的内部核糖体进入位点(ires)。在其它实施方案中,所公开的双顺反子表达载体包含定位于编码修饰的glcnac-1 ptase的多核苷酸之后和编码溶酶体酶的多核苷酸之前的ires。
106.本文提供的是包含所公开的双顺反子表达载体的哺乳动物细胞。
107.本文提供的是药物组合物,其包含通过如本文公开的双顺反子载体表达的溶酶体酶和药学上可接受的载体。
108.本文提供的是用于治疗患有溶酶体贮积症(lsd)的受试者的方法,以及预防有需要的受试者中的溶酶体贮积症(lsd)发生的方法。
109.基因疗法本文提供的是包含双顺反子病毒载体的组合物,所述双顺反子病毒载体包含编码溶酶体酶的多核苷酸和编码修饰的glcnac-1磷酸转移酶(glcnac-1 ptase)的多核苷酸。在
一些实施方案中,所公开的双顺反子病毒载体包含定位于编码修饰的glcnac-1 ptase的多核苷酸之前和编码溶酶体酶的多核苷酸之后的内部核糖体进入位点(ires)。在其它实施方案中,所公开的双顺反子病毒载体包含定位于编码修饰的glcnac-1 ptase的多核苷酸之后和编码溶酶体酶的多核苷酸之前的ires。在一些实施方案中,病毒载体是腺病毒、腺伴随病毒(aav)、逆转录病毒或慢病毒。
110.本文提供的是通过向受试者施用所公开的双顺反子病毒载体,用于治疗患有溶酶体贮积症(lsd)的受试者的方法、以及预防有需要的受试者中的溶酶体贮积症(lsd)发生的方法。
111.本文进一步提供的是用于改善有需要的受试者中导致lsd的溶酶体酶的磷酸化的方法。
112.本文提供的是使用双顺反子载体用于治疗或预防受试者中的溶酶体贮积症(lsd)的组合物和方法。
113.本公开内容提供了包含双顺反子载体的组合物,所述双顺反子载体包含启动子、内部核糖体进入位点(ires)、编码溶酶体酶的多核苷酸和编码修饰的glcnac-1磷酸转移酶(glcnac-1 ptase)的多核苷酸。本公开内容的方法包括向受试者施用包含如本文公开的双顺反子载体的药物组合物。
114.定义除非另外定义,否则本文使用的所有技术和科学术语都具有与本发明所属领域的普通技术人员通常理解的相同的含义。尽管本文描述了优选的材料和方法,但与本文所述的那些相似或等价的任何方法和材料都可以用于测试本发明的实践中。在描述且请求保护本发明时,将使用下述术语。
115.还应理解,在本文中使用的术语仅用于描述一些实施方案的目的,并不预期是限制性的。
116.如本文使用的,冠词“一个(a)”和“一种(an)”用于指冠词的一个或多于一个(即,至少一个)语法对象。例如,“元件”意指一个元件或多于一个元件。
117.如本文使用的,当提及可测量的值如量、持续时间等等时,术语“约”意欲涵盖相对于指定值
±
20%或
±
10%,更优选
±
5%,甚至更优选
±
1%,并且还更优选
±
0.1%的变化,当此类变化对于执行所公开的方法是适当的时。
118.术语“2a”或“2a肽”或“2a样肽”是自加工的病毒肽。2a肽可以在单个orf转录单位中分开不同的蛋白质编码序列(ryan等人,1991,j gen virol 72:2727-2732)。尽管称为“自切割”肽或蛋白酶位点,但2a序列从一个转录物生成两种蛋白质的机制通过核糖体跳跃而发生,其中正常的肽键在2a处是受损的,导致来自一次翻译事件的两个不连续的蛋白质片段。与2a肽序列连接导致衍生自单个orf的多重不连续的蛋白质(以基本上等摩尔的数量)的细胞表达(de felipe等人,2006,trends biotechnol 24:68-75)。
119.术语“生物”或“生物样品”指从生物体或生物体的组分(例如,细胞)获得的样品。样品可以是任何生物组织或流体。样品通常是“临床样品”,其为衍生自患者的样品。此类样品包括但不限于骨髓、心脏组织、痰、血液、淋巴液、血细胞(例如白细胞)、组织或细针活组织检查样品、尿、腹水和胸膜液、或来自其的细胞。生物样品还可以包括组织切片,例如为了组织学目的而获取的冷冻切片。
120.如本文使用的,术语“衍生物”指定病毒的衍生物可以具有相对于模板病毒核酸或氨基酸序列的核酸或氨基酸序列差异。
[0121]“疾病”是动物的健康状态,其中动物不能维持体内稳态,并且其中如果疾病没有改善,则动物的健康继续恶化。
[0122]
相比之下,动物中的“病症”是这样的健康状态,其中动物能够维持体内稳态,但其中动物的健康状态不如在病症的不存在下有利。如果不予以治疗,病症不一定引起动物的健康状态的进一步下降。
[0123]“表达载体”指包含重组多核苷酸的载体,所述重组多核苷酸包含与待表达的核苷酸序列可操作地连接的表达控制序列。表达载体包含用于表达的足够的顺式作用元件;其它表达元件可以由宿主细胞或在体外表达系统中供应。表达载体包括本领域已知的所有那些表达载体,例如掺入重组多核苷酸的粘粒、质粒(例如,裸露的或包含在脂质体中的)和病毒(例如,慢病毒、逆转录病毒、腺病毒和腺伴随病毒)。在一些实施方案中,所公开的载体在本文中被称为病毒载体。在一些实施方案中,所公开的载体在本文中被称为表达载体。
[0124]
如本文使用的,“更高”指比对照参考高至少10%或更多,例如高20%、30%、40%或50%、60%、70%、80%、90%或更多,和/或是对照参考的1.1倍、1.2倍、1.4倍、1.6倍、1.8倍、2.0倍或更多,以及两者之间的任何和所有整体或部分增量的表达水平。本文公开的高于参考值的表达水平指这样的表达水平(mrna或蛋白质),其高于来自在健康受试者中测量的或者本领域中定义或使用的表达(mrna或蛋白质)的正常或对照水平。
[0125]
如本文使用的,“更低”指比对照参考低至少10%或更多,例如低20%、30%、40%或50%、60%、70%、80%、90%或更多,和/或是对照参考的1/1.1、1/1.2、1/1.4、1/1.6、1/1.8、1/2.0或更少,以及两者之间的任何和所有整体或部分增量的表达水平。本文公开的低于参考值的表达水平指这样的表达水平(mrna或蛋白质),其低于来自在健康受试者中测量的或者本领域中定义或使用的表达(mrna或蛋白质)的正常或对照水平。
[0126]
如本文使用的,术语“对照”或“参考”可以互换使用,并且指用作比较标准的值。
[0127]
如本文使用的,“组合疗法”意指第一种药剂与另一种药剂结合施用。“与
……
组合”或“与
……
结合”指一种治疗模式加上另一种治疗模式的施用。因此,“与
……
组合”指在向个体递送另一种治疗模式之前、期间或之后施用一种治疗模式。此类组合被视为单一治疗方案或方案的部分。例如,本公开内容的载体或包含载体的组合物可以与第二治疗剂组合提供给或施用于受试者。在一些实施方案中,本公开内容的载体和组合物与第二治疗剂同时或序贯地提供给或施用于受试者。在一些实施方案中,本公开内容的载体和组合物与第二治疗剂同时提供给或施用于受试者。在一些实施方案中,本公开内容的载体和组合物与第二治疗剂序贯地提供给或施用于受试者。在一些实施方案中,在第二治疗剂施用之前,向受试者提供或施用本公开内容的载体和组合物。在一些实施方案中,在第二治疗剂施用之后,向受试者提供或施用本公开内容的载体和组合物。在一些实施方案中,第二治疗剂包含本公开内容的组合物的第二载体。在一些实施方案中,第二治疗剂包含本公开内容的溶酶体酶的变体形式,包括编码所述变体形式的本公开内容的载体或组合物。在一些实施方案中,第二治疗剂包含减轻溶酶体贮积症的体征或症状的一种或多种药剂。在一些实施方案中,第二治疗剂包含一种或多种抗炎剂或免疫抑制剂。
[0128]
如本文使用的,术语“可操作地连接的”意指核酸序列的表达在它与之空间连接的
启动子的控制下。启动子可以位于在其控制下的核酸序列的5' (上游)。
[0129]
如本文使用的,“原代细胞”指直接取自活组织(即活组织检查材料)并建立用于在体外生长的细胞,其已经历极少的群体倍增,并且因此与连续致瘤或人工永生化细胞系相比,更能代表细胞由其衍生的组织的主要功能组分和特性。
[0130]
如本文使用的,术语“肽”、“多肽”和“蛋白质”可互换使用,并且指由通过肽键共价连接的氨基酸残基组成的化合物。蛋白质或肽必须含有至少两个氨基酸,并且对可能构成蛋白质或肽序列的最大氨基酸数目没有限制。多肽包括包含通过肽键彼此连接的两个或更多个氨基酸的任何肽或蛋白质。如本文使用的,该术语既指短链,其在本领域中通常也被称为例如肽、寡肽和寡聚体,又指更长的链,其在本领域中一般被称为蛋白质,其中存在许多类型。“多肽”尤其包括例如生物活性片段、基本上同源的多肽、寡肽、同源二聚体、异源二聚体、多肽的变体、修饰的多肽、衍生物、类似物、融合蛋白。多肽包括天然肽、重组肽、合成肽或其组合。
[0131]
如本文使用的,术语“启动子”可以意指能够赋予、激活或增强核酸表达的合成或天然衍生的分子。如本文使用的,启动子被定义为启动多核苷酸序列的特异性转录所需的,由细胞的合成机制或所引入的合成机制识别的dna序列。
[0132]
如本文使用的,术语“启动子/调控序列”意指与启动子/调控序列可操作连接的基因产物表达所需的核酸序列。在一些情况下,这种序列可以是核心启动子序列,而在其它情况下,这种序列还可以包括增强子序列和基因产物表达所需的其它调控元件。例如,启动子/调控序列可以是以组织特异性方式表达基因产物的启动子/调控序列。
[0133]“组成型”启动子是这样的核苷酸序列,当与编码或指定基因产物的多核苷酸可操作地连接时,其促使基因产物在细胞的大多数或所有生理条件下在细胞中产生。
[0134]“诱导型”启动子是这样的核苷酸序列,当与编码或指定基因产物的多核苷酸可操作地连接时,基本上仅当对应于该启动子的诱导物存在于细胞中时,其才促使基因产物在细胞中产生。
[0135]
如本文使用的,术语“rna”被定义为核糖核酸。
[0136]
如本发明的上下文中使用的,术语“治疗”意欲包括用于疾病或病症的治疗性治疗以及预防性或压制性措施。如本文使用的,术语“治疗(treatment)”和相关术语例如“治疗(treat)”和“治疗(treating)”意指疾病状况或其至少一种症状的进展、严重性和/或持续时间的减少。因此,术语
‘
治疗’指可以使受试者受益的任何方案。治疗可以针对现有状况或者可以是预防性的(预防性治疗)。治疗可以包括治愈、缓解或预防效应。本文对“治疗性”和“预防性”治疗的提及在其最广泛的背景下加以考虑。术语“治疗性的”并不一定暗示受试者进行治疗直至完全恢复。类似地,“预防性的”并不一定意指受试者最终并不感染疾病状况。因此,例如,术语治疗包括在疾病或病症发作之前或之后的药剂施用,从而预防或去除疾病或病症的所有体征。作为另一个实例,在疾病的临床表现之后施用药剂以对抗疾病的症状构成疾病的“治疗”。
[0137]
如本文使用的,术语“核酸”指多核苷酸,例如脱氧核糖核酸(dna),以及适当时,核糖核酸(rna)。该术语还应该理解为包括作为等价物的由核苷酸类似物制备的rna或dna类似物,以及如可应用于所述实施方案的,单链(有义或反义)和双链多核苷酸。est、染色体、cdna、mrna和rrna是可以被称为核酸的分子的代表性实例。
[0138]
如本文使用的,术语“药物组合物”指在本发明内有用的至少一种化合物与其它化学组分的混合物,所述化学组分例如载体、稳定剂、稀释剂、佐剂、分散剂、助悬剂、增稠剂和/或赋形剂。药物组合物促进化合物施用于生物体。本领域存在施用化合物的多重技术,其包括但不限于:瘤内、静脉内、胸膜内、经口、气溶胶、肠胃外、眼、肺和局部施用。
[0139]
术语“药学上可接受的载体”包括药学上可接受的盐、药学上可接受的材料、组合物或载体,例如液体或固体填料、稀释剂、赋形剂、溶剂或包封材料,其涉及将本发明的化合物携带或转运到受试者内或至受试者,使得它可以执行其预期功能。通常,此类化合物从一个器官或身体部分携带或转运到另一个器官或身体部分。每种盐或载体必须在与制剂的其它成分相容且对受试者无害的意义上是“可接受的”。可以充当药学上可接受的载体的材料的一些实例包括:糖,例如乳糖、葡萄糖和蔗糖;淀粉,例如玉米淀粉和马铃薯淀粉;纤维素及其衍生物,例如羧甲基纤维素钠、乙基纤维素和乙酸纤维素;粉状黄蓍胶;麦芽;明胶;滑石;赋形剂,例如可可脂和栓剂蜡;油,例如花生油、棉籽油、红花油、芝麻油、橄榄油、玉米油和大豆油;二醇,例如丙二醇;多元醇,例如丙三醇、山梨糖醇、甘露糖醇和聚乙二醇;酯,例如油酸乙酯和月桂酸乙酯;琼脂;缓冲剂,例如氢氧化镁和氢氧化铝;海藻酸;无热原水;等渗盐水;林格氏溶液;乙醇;磷酸盐缓冲溶液;稀释剂;造粒剂;润滑剂;粘合剂;崩解剂;润湿剂;乳化剂;着色剂;释放剂(release agent);包衣剂;甜味剂;调味剂;芳香剂;防腐剂;抗氧化剂;增塑剂;胶凝剂;增稠剂;硬化剂;固化剂;助悬剂;表面活性剂;保湿剂;载体;稳定剂;以及用于药物制剂中的其它无毒的相容物质,或其任何组合。如本文使用的,“药学上可接受的载体”还包括任何和所有包衣、抗菌剂和抗真菌剂以及吸收延迟剂等等,其与化合物的活性相容并且对受试者是生理上可接受的。还可以将补充性活性化合物掺入组合物内。
[0140]
如本文使用的,术语“有效量”或“治疗有效量”意指从本发明的载体生成的病毒颗粒或感染单位的量,其是预防特定疾病状况、或者减少疾病状况或其至少一种症状或与其相关的状况的严重性和/或改善疾病状况或其至少一种症状或与其相关的状况所需的。
[0141]
如本文使用的,“受试者”或“患者”可以是人或非人哺乳动物。非人哺乳动物包括例如家畜和宠物,例如羊科、牛科、猪科、犬科、猫科和鼠科哺乳动物。优选地,受试者是人。
[0142]
范围:本公开内容自始至终,一些实施方案可以以范围形式呈现。应该理解,以范围形式的描述仅仅是为了方便和简洁,而不应解释为对本公开内容的范围的刚性限制。相应地,范围的描述应该被视为已具体公开了所有可能的子范围以及该范围内的各个数值。例如,范围如从1到6的描述应该被视为已具体公开了子范围,例如从1到3、从1到4、从1到5、从2到4、从2到6、从3到6等,以及该范围内的各个数目,例如1、2、2.7、3、4、5、5.3和6。无论范围的广度如何,这都适用。
[0143]
组合物本文提供的是通过向受试者施用包含双顺反子表达载体的药物,用于治疗或预防受试者中的溶酶体贮积症(lsd)的组合物和方法。
[0144]
在一些实施方案中,本公开内容提供了包含双顺反子载体的组合物,所述双顺反子载体包含编码溶酶体酶的多核苷酸和编码修饰的glcnac-1磷酸转移酶(glcnac-1 ptase)的多核苷酸。在一个实施方案中,编码溶酶体酶的多核苷酸和编码修饰的glcnac-1磷酸转移酶(glcnac-1 ptase)的多核苷酸是可操作地连接的。
[0145]
在一些实施方案中,本公开内容提供了包含双顺反子载体的组合物,所述双顺反
子载体包含组成型启动子、内部核糖体进入位点(ires)和编码修饰的glcnac-1磷酸转移酶(glcnac-1 ptase)的多核苷酸。
[0146]
在一些实施方案中,双顺反子载体包含定位于编码修饰的glcnac-1 ptase的多核苷酸之前和编码溶酶体酶的多核苷酸之后的ires。在其它实施方案中,双顺反子载体包含定位于编码修饰的glcnac-1 ptase的多核苷酸之后和编码溶酶体酶的多核苷酸之前的ires。
[0147]
ires的序列可以是本领域已知的序列或其变体。ires变体可以是修饰的或突变的。在一个实施方案中,序列ires包含seq id no: 3。在其它实施方案中,ires的序列与seq id no: 3至少70%、至少75%、至少80%、至少85%、至少90%、至少95%、至少99%相似。
[0148]
在一个实施方案中,溶酶体酶的多核苷酸可操作地连接至编码2a肽的2a dna,其依次又可操作地连接至修饰的glcnac-1磷酸转移酶(glcnac-1 ptase)的多核苷酸。本领域已知的各种2a肽可以用于所公开的双顺反子载体中,包括但不限于t2a、p2a、e2a和f2a。在一些实施方案中,gsg残基的添加可以加入肽的5'端中,以改善切割效率。
[0149]
在一些实施方案中,双顺反子病毒载体包含与编码溶酶体酶的多核苷酸和编码修饰的glcnac-1 ptase的多核苷酸可操作地连接的启动子。
[0150]
在一些实施方案中,双顺反子表达载体包含启动子。
[0151]
启动子可以是组成型、诱导型/阻遏型或细胞类型特异性的。在某些实施方案中,启动子可以是组成型的。用于哺乳动物细胞的组成型启动子的非限制性实例包括cmv、ubc、ef1 a、sv40、pgk、cag、cba/caggs/actb、cbh、mecp2、u6和h1。在一些实施方案中,本文公开的双顺反子载体包含组成型启动子。在一些实施方案中,组成型启动子是巨细胞病毒(cmv)启动子。在一些实施方案中,cmv启动子的多核苷酸包含seq id no: 2的核酸序列。
[0152]
在其它实施方案中,启动子可以是诱导型启动子。诱导型启动子可以选自:四环素、热休克、类固醇激素、重金属、佛波酯、腺病毒e1a元件、干扰素和血清诱导型启动子。
[0153]
在不同的实施方案中,启动子可以是细胞类型特异性的。例如,可以使用用于神经元(例如突触蛋白(syapsin))、星形胶质细胞(例如gfap)、少突胶质细胞(例如髓鞘碱性蛋白)、小胶质细胞(例如cx3cr1)、神经内分泌细胞(例如嗜铬粒蛋白a)、肌细胞(例如结蛋白、mb)、或心肌细胞(例如α肌球蛋白重链启动子)的细胞类型特异性启动子。在一个示例性实施方案中,启动子可以是nrl (视杆光感受器特异性)启动子或hbb (血红蛋白β)启动子。启动子可以进一步包含一个或多个特异性转录调控序列,以进一步增强核酸的表达和/或改变核酸的空间表达和/或时间表达。
[0154]
在载体上发现的增强子序列也调控其中包含的基因的表达。通常,增强子与蛋白质因子结合以增强基因的转录。增强子可能定位于其调控的基因的上游或下游。增强子也可以是组织特异性的,以增强特定细胞或组织类型中的转录。在一个实施方案中,本发明的双顺反子载体包含一种或多种增强子,以加强载体内存在的基因的转录。增强子的非限制性实例包括cmv增强子和sp1增强子。
[0155]
在一些实施方案中,多于一种启动子可以与编码多肽的每种多核苷酸可操作地连接,所述启动子可以是相同的或不同的。启动子与待表达的核酸序列之间的距离可以与该启动子与其控制的天然核酸序列之间的距离大致相同。如本领域已知的,可以适应该距离的变化而不丧失启动子功能。
[0156]
为了评价双顺反子载体内的多肽表达,载体还可以包含可选择标记物基因或报道基因或两者,以促进从寻求通过病毒载体转染或感染的细胞群体中鉴定和选择表达细胞。在一些实施方案中,可选择标记物可以携带在分开的dna片上,并且用于共转染程序中。可选择标记物和报道基因两者均可以由适当的调控序列侧接,以使得能够在宿主细胞中表达。有用的可选择标记物包括例如抗生素抗性基因,例如neo等等。
[0157]
报道基因用于鉴定潜在转染的细胞和评估调控序列的功能性。一般而言,报道基因是不存在于受体生物体或组织中或者不由受体生物体或组织表达并且编码多肽的基因,所述多肽的表达通过一些可容易检测的性质例如酶促活性来体现。在已将dna引入受体细胞内之后,在合适的时间测定报道基因的表达。合适的报道基因可以包括编码萤光素酶、β-半乳糖苷酶、氯霉素乙酰转移酶、分泌性碱性磷酸酶的基因或绿色荧光蛋白基因(例如,ui-tei等人,2000 febs letters 479: 79-82)。合适的表达系统是众所周知的,并且可以使用已知技术进行制备或商业上获得。一般而言,将具有显示报道基因的最高表达水平的最小5'侧翼区的构建体鉴定为启动子。此类启动子区可以与报道基因连接,并且用于评估药剂调节启动子驱动的转录的能力。
[0158]
将基因引入细胞内且在其内表达的方法是本领域已知的。在表达载体的背景下,可以通过本领域的任何方法将载体容易地引入宿主细胞内,所述宿主细胞例如哺乳动物、细菌、酵母或昆虫细胞。例如,可以通过物理、化学或生物手段将表达载体转移到宿主细胞内。
[0159]
用于将多核苷酸引入宿主细胞内的物理方法包括磷酸钙沉淀、脂转染、粒子轰击、显微注射、电穿孔等等。用于产生包含载体和/或外源核酸的细胞的方法是本领域众所周知的。参见例如,sambrook等人(2001,molecular cloning: a laboratory manual,cold spring harbor laboratory,new york)。用于将多核苷酸引入宿主细胞内的优选方法是磷酸钙转染。
[0160]
用于将目的多核苷酸引入宿主细胞内的生物学方法包括dna和rna载体的使用。病毒载体且尤其是逆转录病毒载体,已成为用于将基因插入哺乳动物例如人细胞内的最广泛使用的方法。其它病毒载体可以衍生自慢病毒、痘病毒、单纯疱疹病毒i、腺病毒和腺伴随病毒等等。参见例如,美国专利号5,350,674和5,585,362。
[0161]
用于将多核苷酸引入宿主细胞内的化学手段包括胶体分散系统,例如大分子复合物、纳米胶囊、微球体、珠和基于脂质的系统,包括水包油型乳状液、胶束、混合胶束和脂质体。用作体外和体内递送媒介物的示例性胶体系统是脂质体(例如,人工膜囊泡)。
[0162]
在其中利用非病毒递送系统的一些实施方案中,示例性递送媒介物是脂质体。考虑使用脂质制剂用于将核酸引入宿主细胞内(在体外、离体或在体内)。在一些实施方案中,核酸可以与脂质结合。与脂质结合的核酸可以被封装在脂质体的水性内部,散布在脂质体的脂质双层内,经由与脂质体和寡核苷酸两者结合的连接分子附着到脂质体,在脂质体中截留,与脂质体复合,分散在含有脂质的溶液中,与脂质混合,与脂质组合,作为悬浮液包含在脂质中,含有胶束或与胶束复合,或以其它方式与脂质结合。脂质、脂质/dna或脂质/表达载体相关的组合物并不限于溶液中的任何特定结构。例如,它们可能在双层结构中、作为胶束或具有“坍塌”结构存在。它们也可能简单地散布在溶液中,可能形成在大小或形状方面不均匀的聚集体。脂质是脂肪物质,其可以是天然存在的或合成的脂质。例如,脂质包括天
然存在于细胞质中的脂肪小滴,以及含有长链脂肪族烃及其衍生物例如脂肪酸、醇、胺、氨基醇和醛的化合物类别。
[0163]
适用的脂质可以从商业来源获得。例如,二肉豆蔻基磷脂酰胆碱(“dmpc”)可以从sigma,st. louis,mo获得;磷酸双十六酯(“dcp”)可以从k & k laboratories (plainview,ny)获得;胆固醇(“choi”)可以从calbiochem-behring获得;二肉豆蔻基磷脂酰甘油(“dmpg”)和其它脂质可以从avanti polar lipids,inc. (birmingham,al)获得。脂质在氯仿或氯仿/甲醇中的储备溶液可以在约-20
°
c下贮存。氯仿用作唯一的溶剂,因为它比甲醇更容易蒸发。“脂质体”是通用术语,其涵盖了通过生成封闭的脂质双层或聚集体而形成的各种单层和多层脂质媒介物。脂质体可以表征为具有囊泡结构,其具有磷脂双层膜和内部水性介质。多层脂质体具有由水性介质分开的多重脂质层。它们在磷脂悬浮于过量的水溶液中时自发形成。脂质组分在形成封闭结构之前经历自重排,并且在脂质双层之间截留水和溶解的溶质(ghosh等人,1991 glycobiology 5: 505-10)。然而,还涵盖了在溶液中具有与正常囊泡结构不同的结构的组合物。例如,脂质可能采取胶束结构或仅仅作为脂质分子的不均匀聚集体存在。还考虑的是lipofectamine
ꢀ‑
核酸复合物。
[0164]
不管用于将外源核酸引入宿主细胞内的方法如何,为了确认宿主细胞中重组dna序列的存在,可以执行各种测定法。此类测定法包括例如本领域技术人员众所周知的“分子生物学”测定法,例如dna印迹和rna印迹、rt-pcr和pcr;“生物化学”测定法,例如检测特定肽的存在或不存在,例如通过免疫学手段(elisa和蛋白质印迹)或本文所述的测定法来鉴定落入本公开内容的范围内的药剂。
[0165]
用于基因疗法的载体如本文公开的待用于治疗或预防受试者中的lsd的载体适合于在真核细胞中复制和任选地整合。典型的载体含有可用于调控所需核酸序列表达的转录和翻译终止子、起始序列和启动子。
[0166]
本公开内容的载体还可以用于使用标准基因递送方案的核酸免疫和基因疗法。用于基因递送的方法是本领域已知的。参见例如,通过引用以其整体并入本文的美国专利号5,399,346、5,580,859、5,589,466。在另一个实施方案中,本公开内容提供了基因治疗载体。
[0167]
本公开内容的分离的核酸可以克隆到多种类型的载体内。例如,可以将核酸克隆到包括但不限于以下的载体内:质粒、噬菌粒、噬菌体衍生物、动物病毒和粘粒。目的载体包括表达载体、复制载体、探针生成载体和测序载体。
[0168]
进一步地,载体可以以病毒载体的形式提供给细胞。病毒载体技术是本领域众所周知的,并且例如在sambrook等人(2001,molecular cloning: a laboratory manual,cold spring harbor laboratory,new york)、以及其它病毒学和分子生物学手册中进行描述。可用作载体的病毒包括但不限于逆转录病毒、腺病毒、腺伴随病毒、疱疹病毒和慢病毒。一般而言,合适的载体含有在至少一种生物体中有功能的复制起点、启动子序列、方便的限制性内切核酸酶位点和一种或多种可选择标记物(例如,wo 01/96584;wo 01/29058;和美国专利号6,326,193)。
[0169]
已开发了许多基于病毒的系统,用于将基因转移到哺乳动物细胞内。例如,逆转录病毒提供了用于基因递送系统的方便平台。可以使用本领域已知的技术,将所选基因插入
载体内并且在逆转录病毒颗粒中包装。然后可以分离重组病毒并且在体内或离体递送至受试者的细胞。许多逆转录病毒系统是本领域已知的。在一些实施方案中,使用腺病毒载体。许多腺病毒载体是本领域已知的。在一个实施方案中,使用慢病毒载体。
[0170]
例如,衍生自逆转录病毒如慢病毒的载体是实现长期基因转移的合适工具,因为它们允许转基因的长期、稳定整合及其在子细胞中的繁殖。慢病毒载体具有超过衍生自癌逆转录病毒(例如鼠白血病病毒)的载体的附加优点,因为它们可以转导非增殖细胞,例如肝细胞。它们还具有低免疫原性的附加优点。在一个优选的实施方案中,组合物包括衍生自腺伴随病毒(aav)的载体。腺伴随病毒(aav)载体已成为用于治疗各种病症的强大的基因递送工具。aav载体具有致使其理想地适合基因疗法的许多特征,包括缺乏致病性、最低限度的免疫原性、以及以稳定有效的方式转导有丝分裂后细胞的能力。通过选择aav血清型、启动子和递送方法的适当组合,aav载体内包含的特定基因的表达可以特异性地靶向一种或多种类型的细胞。
[0171]
在一些实施方案中,所公开的双顺反子病毒载体包含腺病毒(例如ad-sye、adsur-sye、ad5/3-mda7/il-24、ad-sb、ad-crispr、溶瘤ad);腺伴随病毒,aav (例如aav-mecp2、aav1、aav5、dual aav9 aav8、aav9、aavrh10、aavhu37);单纯疱疹病毒,hsv (例如hsv1、hsv2、hsv-1、hf10溶瘤hsv-2);逆转录病毒(例如rrv/ toca 511、grv);慢病毒(例如hiv-1、hiv-2);甲病毒(sfv、m1);黄病毒(昆津病毒);弹状病毒(vsv);麻疹病毒(例如mv-edm);新城疫病毒(例如ndv90);美洲蛇鸟微小核糖核酸病毒柯萨奇病毒(例如cvb3、cav21、ev1);或痘病毒(例如panvac、vv、vv-glv-1h153、cpxv)。
[0172]
在一个实施方案中,所公开的双顺反子病毒载体是腺病毒、腺伴随病毒(aav)、甲病毒、黄病毒、单纯疱疹病毒(hsv)、麻疹病毒、弹状病毒、逆转录病毒、慢病毒、新城疫病毒(ndv)、痘病毒或微小核糖核酸病毒。在一个实施方案中,所公开的双顺反子病毒载体是腺病毒、腺伴随病毒(aav)、逆转录病毒或慢病毒。
[0173]
在一个实施方案中,编码溶酶体酶的多核苷酸和编码修饰的glcnac-1 ptase的多核苷酸包含在aav载体内。多于30种天然存在的aav血清型是可用的。aav衣壳中存在许多天然变体,其允许鉴定和使用具有特别适合骨骼肌的性质的aav。aav病毒可以使用常规的分子生物学技术进行改造,使得可优化这些颗粒用于核酸序列的细胞特异性递送、使免疫原性降到最低、调整稳定性和颗粒寿命、有效降解、准确递送至核,仅举几例。
[0174]
aav的使用是dna的外源递送的常见模式,因为它是相对无毒的,提供有效的基因转移,并且可以容易地对于具体目的进行优化。在从人或非人灵长类动物(nhp)中分离且充分表征的aav血清型中,人血清型2是被开发为基因转移载体的第一个aav;它已广泛用于不同靶组织和动物模型中的有效基因转移实验。基于aav2的载体对一些人疾病模型的实验应用的临床试验正在进行中,并且包括用于疾病如囊性纤维化和血友病b的疗法。其它有用的aav血清型包括aav1、aav3、aav4、aav5、aav6、aav7、aav8和aav9。
[0175]
用于组装成载体的期望aav片段包括cap蛋白,包括vpl、vp2、vp3和高变区,rep蛋白,包括rep 78、rep 68、rep 52和rep 40,以及编码这些蛋白的序列。这些片段可以容易地用于各种载体系统和宿主细胞中。此类片段可以单独使用,与其它aav血清型序列或片段组合使用,或者与来自其它aav或非aav病毒序列的元件组合使用。如本文使用的,人工aav血清型包括但不限于具有非天然存在的衣壳蛋白的aav。此类人工衣壳可以通过任何合适的
技术生成,使用与异源序列组合的所选aav序列(例如,vpl衣壳蛋白的片段),所述异源序列可以得自不同的所选aav血清型、相同aav血清型的非邻接部分、非aav病毒来源或非病毒来源。人工aav血清型可以是但不限于嵌合aav衣壳、重组aav衣壳或“人源化
”ꢀ
aav衣壳。因此,适合于表达目的溶酶体酶和修饰的glcnac-1 ptase的示例性aav或人工aav尤其包括aav2/8 (参见美国专利号7,282,199)、aav2/5 (可得自美国国立卫生研究院(national institutes of health))、aav2/9 (国际专利公开号wo2005/033321)、aav2/6 (美国专利号6,156,303)和aavrh8 (国际专利公开号wo2003/042397)。
[0176]
在一个实施方案中,可用于本文所述的组合物和方法中的载体最低限度地含有编码所选aav血清型衣壳,例如aav8衣壳或其片段的序列。在另一个实施方案中,有用的载体最低限度地含有编码所选aav血清型rep蛋白,例如aav8 rep蛋白或其片段的序列。任选地,此类载体可以含有aav cap和rep蛋白两者。在其中提供aav rep和cap两者的载体中,aav rep和aav cap序列均可以具有一种血清型起源,例如,全部aav8起源。可替代地,可以使用这样的载体,其中rep序列来自与提供cap序列的aav血清型不同的aav血清型。在一个实施方案中,rep和cap序列由分开的来源(例如,分开的载体、或宿主细胞和载体)表达。在另一个实施方案中,这些rep序列与不同aav血清型的cap序列在框内融合,以形成嵌合aav载体,例如美国专利号7,282,199中描述的aav2/8。
[0177]
合适的重组腺伴随病毒(aav)通过培养宿主细胞而生成,所述宿主细胞含有编码如本文定义的腺伴随病毒(aav)血清型衣壳蛋白或其片段的核酸序列;功能性rep基因;最低限度地由aav反向末端重复(itr)以及编码溶酶体酶的多核苷酸和编码修饰的glcnac-1 ptase的多核苷酸组成的小基因;以及允许将小基因包装到aav衣壳蛋白内的足够的辅助功能。需要在宿主细胞中培养以将aav小基因包装到aav衣壳中的组分可以反式提供给宿主细胞。可替代地,所需组分(例如,小基因、rep序列、cap序列和/或辅助功能)中的任何一种或多种可以由稳定的宿主细胞提供,所述宿主细胞已使用本领域技术人员已知的方法被改造为含有一种或多种所需组分。
[0178]
最适当地,此类稳定的宿主细胞将含有在组成型启动子的控制下的所需组分。然而,所需组分可能在诱导型启动子的控制下。合适的诱导型和组成型启动子的实例在本文其它地方提供,并且是本领域众所周知的。在另外一个替代方案中,所选的稳定宿主细胞可以含有在组成型启动子的控制下的所选组分、以及在一个或多个诱导型启动子的控制下的其它所选组分。例如,可以生成稳定的宿主细胞,其衍生自293细胞(其含有在组成型启动子的控制下的e1辅助功能),但含有在诱导型启动子的控制下的rep和/或cap蛋白。另外其它的稳定宿主细胞可以由本领域技术人员生成。
[0179]
产生本公开内容的raav所需的小基因、rep序列、cap序列和辅助功能,可以以转移在其上携带的序列的任何遗传元件的形式递送至包装宿主细胞。可以使用任何合适的方法递送所选的遗传元件,所述方法包括本文所述的那些方法和本领域可用的任何其它方法。用于构建本公开内容的任何实施方案的方法是核酸操作技术人员已知的,并且包括遗传工程、重组工程和合成技术(参见例如,sambrook等人,molecular cloning: a laboratory manual,cold spring harbor press,cold spring harbor,n.y)。类似地,生成raav病毒粒子的方法是众所周知的,并且合适方法的选择不是对本公开内容的限制(尤其参见例如,k. fisher等人,1993 j. virol.,70:520-532和美国专利号5,478,745)。
[0180]
除非另有说明,否则本文所述的aav itr和其它所选的aav组分可以容易地选自任何aav血清型中,包括但不限于aav1、aav2、aav3、aav4、aav5、aav6、aav7、aav8、aav9或者其它已知或仍未知的aav血清型。使用本领域技术人员可用的技术,可以容易地从aav血清型中分离这些itr或其它aav组分。此类aav可以从学术、商业或公共来源(例如美国典型培养物保藏中心,manassas,va.)分离或获得。可替代地,aav序列可以通过合成或其它合适的手段,通过参考例如文献或数据库(例如genbank、pubmed等等)中可用的公开序列而获得。
[0181]
在一些实施方案中,双顺反子载体包含seq id no: 1的核酸序列。在其它实施方案中,双顺反子载体包含与seq id no: 1具有至少20%、至少30%、至少40%、至少50%、至少60%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%、至少99%的相似性的序列。
[0182]
在一些实施方案中,所编码的溶酶体酶涉及如下表1a、表1b或表1c中列出的至少一种溶酶体贮积症(lsd)。在其它实施方案中,溶酶体酶是如下表1a、表1b或表1c中列出的至少一种。
[0183]
表1a
ꢀ‑ꢀ
ert实施方案(具有(uniprot登录号)的酶)
表1b
ꢀ‑ꢀ
基因疗法实施方案(具有(uniprot登录号)的酶)
表1c
ꢀ‑ꢀ
溶酶体病症(蛋白质(uniprot登录号)
在一些实施方案中,溶酶体酶选自β-葡糖脑苷脂酶(gba)、半乳糖神经酰胺酶(galc)、α-半乳糖苷酶(gla)、α-n-乙酰氨基葡糖苷酶(naglu)、酸性α-葡糖苷酶(gaa)和溶酶体酸性α-甘露糖苷酶(laman)。在再其它实施方案中,编码溶酶体酶的多核苷酸包含seq id no: 5-10的核酸序列。在其它实施方案中,溶酶体酶由多核苷酸编码,所述多核苷酸与seq id no: 5-10具有至少50%、至少60%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%、至少99%的相似性。
[0184]
在一些实施方案中,s1-s3 ptase由包含seq id no: 4的核酸序列的多核苷酸编码。在其它实施方案中,glcnac-1 ptase由多核苷酸编码,所述多核苷酸与seq id no: 4具有至少50%、至少60%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%、至少99%的相似性。
[0185]
本公开内容还应该解释为包括与本文公开的那些具有基本同源性的任何形式的多肽或多核苷酸。
[0186]
优选地,“基本上同源的”多肽与本文公开的肽的氨基酸序列是约50%同源的,更优选约70%同源的,甚至更优选约80%同源的,更优选约90%同源的,甚至更优选约95%同源的,且甚至更优选约99%同源的。
[0187]
可替代地,可以通过重组手段或从更长的多肽中切割来制备多肽。肽的组成可以通过氨基酸分析或测序来确认。根据本公开内容的多肽的变体可以是(i)其中一个或多个氨基酸残基由保守或非保守的氨基酸残基(优选保守的氨基酸残基)取代,并且此类取代的氨基酸残基可以是或不是由遗传密码编码的氨基酸残基的变体,(ii)其中存在一个或多个修饰的氨基酸残基,例如通过附着取代基进行修饰的残基的变体,(iii)其中多肽是本公开内容的多肽的可变剪接变体的变体,(iv)多肽的片段,和/或(v)其中多肽与另一种多肽融合的变体,所述另一种多肽例如前导序列或分泌序列或者用于纯化(例如,his标签)或用于检测(例如,sv5表位标签)的序列。片段包括经由原始序列的蛋白酶解切割(包括多位点蛋白酶解)生成的多肽。变体可以是翻译后修饰或化学修饰的。根据本文的教导,此类变体被认为在本领域技术人员的范围内。
[0188]
如本领域已知的,通过将一个多肽的氨基酸序列及其保守氨基酸取代与第二个多
肽的序列进行比较,来确定两个多肽之间的“相似性”。变体被定义为包括与原始序列不同的多肽序列,优选在小于40%的残基/目的区段中与原始序列不同,更优选在小于25%的残基/目的区段中与原始序列不同,更优选相差小于10%的残基/目的区段,最优选在仅几个残基/目的区段中与原始蛋白质序列不同,并且同时与原始序列足够同源,以保存原始序列的功能性和/或与泛素或泛素化蛋白质结合的能力。本公开内容包括与原始氨基酸序列至少60%、65%、70%、72%、74%、76%、78%、80%、90%或95%相似或等同的氨基酸序列。使用本领域技术人员广泛已知的计算机算法和方法,来确定两个多肽之间的同一性程度。两个氨基酸序列之间的同一性优选通过使用blastp算法[blast manual,altschul,s.等人,ncbi nlm nih bethesda,md. 20894,altschul,s.等人,j. mol. biol. 215: 403-410 (1990)]进行确定。
[0189]
本文公开的多肽可以是翻译后修饰的。例如,落入本公开内容的范围内的翻译后修饰包括信号肽切割、糖基化、乙酰化、异戊二烯化、蛋白酶解、肉豆蔻酰化、蛋白质折叠和蛋白酶解加工等。一些修饰或加工事件需要引入另外的生物机制。例如,通过将犬微粒体膜或非洲爪蟾卵提取物加入标准翻译反应中,来检查加工事件例如信号肽切割和核心糖基化。
[0190]
本公开内容的多肽可以包括通过翻译后修饰或在翻译过程中引入非天然氨基酸而形成的非天然氨基酸。各种方法可用于在蛋白质翻译过程中引入非天然氨基酸。
[0191]
如本文使用的,术语“功能上等价的”指优选保留本公开内容的溶酶体酶的特定氨基酸序列的至少一种生物学功能或活性的多肽。
[0192]
多肽可以与其它分子例如蛋白质缀合,以制备融合蛋白。这可以例如通过合成n末端或c末端融合蛋白来实现,条件是所得到的融合蛋白保留本公开内容的溶酶体酶的功能性。
[0193]
多肽可以使用常规方法进行磷酸化。在一个实施方案中,由于本文公开的修饰的glcnac-1磷酸转移酶(glcnac-1 ptase),本文公开的溶酶体酶可以进行磷酸化。
[0194]
本文还考虑了肽或嵌合蛋白的环状衍生物。环化可以允许肽或嵌合蛋白采取更有利的构象,用于与其它分子结合。可以使用本领域已知的技术来实现环化。例如,可以在具有游离巯基的两个适当间隔的组分之间形成二硫键,或者可以在一种组分的氨基和另一种组分的羧基之间形成酰胺键。
[0195]
环化也可以使用含有偶氮苯的氨基酸来实现。形成键的组分可以是氨基酸的侧链、非氨基酸组分或两者的组合。在一个实施方案中,环肽可以在右位置中包含β-转角。可以通过在右位置处添加氨基酸pro-gly,将β-转角引入本公开内容的肽内。可能期望产生比如上所述的含有肽键连接的环肽更柔性的环肽。可以通过在肽的右位置和左位置处引入半胱氨酸,并且在两个半胱氨酸之间形成二硫桥,来制备更柔性的肽。两个半胱氨酸这样排列,以便使β-折叠变形且转动。由于二硫键的长度和β-折叠部分中较少数目的氢键,肽是更柔性的。环肽的相对柔性可以通过分子动力学模拟来确定。
[0196]
标签在一个实施方案中,如本文公开的多肽进一步包含标签的氨基酸序列。标签包括但不限于:多组氨酸标签(his标签) (例如h6和h10等)或用于imac系统例如ni2 亲和柱等的其它标签、gst融合物、mbp融合物、链霉抗生物素蛋白标签、细菌酶bira的bsp生物素化靶
序列、以及抗体针对的标签表位(例如尤其是c-myc标签、flag标签、hpc4标签)。如通过本领域技术人员观察到的,标签肽可以用于本公开内容的融合蛋白的纯化、检查、选择和/或显现。在一个实施方案中,标签是检测标签和/或纯化标签。应了解标签序列并不干扰本公开内容的蛋白质的功能。
[0197]
前导序列和分泌序列相应地,本公开内容的多肽可以融合至另一种多肽或标签,例如前导序列或分泌序列或者用于纯化或检测的序列。在一些实施方案中,本公开内容的多肽包含谷胱甘肽-s-转移酶蛋白标签,其对于本公开内容的多肽的快速高亲和力纯化提供了基础。事实上,这种gst融合蛋白可以经由其对于谷胱甘肽的高亲和力从细胞中进行纯化。琼脂糖珠可以与谷胱甘肽偶联,并且此类谷胱甘肽-琼脂糖珠结合gst蛋白。因此,在一个特定实施方案中,多肽可以与固体支持物结合。在一些实施方案中,如果多肽包含gst部分,则多肽与谷胱甘肽修饰的支持物偶联。在一些实施方案中,谷胱甘肽修饰的支持物是谷胱甘肽-琼脂糖珠。另外,在亲和标签和多肽序列之间可以包括编码蛋白酶切割位点的序列,因此允许在与这种特定酶一起温育后去除结合标签,并且因此促进相应目的蛋白质的纯化。
[0198]
本文公开的多肽还可以融合至或整合到靶蛋白和/或能够将嵌合蛋白引导至所需细胞组分或细胞类型或组织的靶向结构域内。嵌合蛋白还可以含有另外的氨基酸序列或结构域。在各种组分来自不同来源,并且因此在自然界中并未一起发现(即是异源的)的意义上,嵌合蛋白是重组的。
[0199]
在本公开内容的组合物的一些实施方案中,多肽包含本公开内容的溶酶体蛋白质的肽模拟物、或编码本公开内容的溶酶体蛋白质的肽模拟物的载体。肽模拟物是基于或衍生自肽和蛋白质的化合物。
[0200]
包含与其它分子缀合的本公开内容的肽或嵌合蛋白的n末端或c末端融合蛋白可以通过以下进行制备:经由重组技术,使肽或嵌合蛋白的n末端或c末端与具有所需生物学功能的所选蛋白质或可选择标记物的序列融合。所得的融合蛋白含有溶酶体酶,其包含与如本文所述的所选蛋白质或标记蛋白融合的肽或嵌合蛋白。可以用于制备融合蛋白的蛋白质的实例包括免疫球蛋白、谷胱甘肽-s-转移酶(gst)、血凝素(ha)和截短的myc。
[0201]
本文公开的多肽和嵌合蛋白可以通过与以下反应而转换成药用盐:无机酸如盐酸、硫酸、氢溴酸、磷酸等,或有机酸如甲酸、乙酸、丙酸、乙醇酸、乳酸、丙酮酸、草酸、琥珀酸、苹果酸、酒石酸、柠檬酸、苯甲酸、水杨酸、苯磺酸和甲苯磺酸。
[0202]
修饰的细胞在一些实施方案中,本公开内容提供了包含本公开内容的载体的细胞。在一些实施方案中,载体是病毒载体(例如,aav或慢病毒载体)。在一些实施方案中,载体是非病毒载体(例如,脂质体、纳米颗粒、脂质纳米颗粒、胶束、聚合物囊泡、外来体)。在一些实施方案中,载体是表达载体。在一些实施方案中,载体含有允许至少两个序列的双顺反子、多顺反子或多重顺反子表达的至少一种元件。在一些实施方案中,载体包含编码本公开内容的溶酶体酶的序列。可替代地或另外,在一些实施方案中,载体包含编码本公开内容的s1s3构建体的序列。在一些实施方案中,溶酶体酶是表1a、表1b或表1c中列出的一种或多种酶。在一些实施方案中,载体包含编码溶酶体酶的核酸序列或氨基酸序列,所述溶酶体酶是表1a、表1b或表1c中列出的一种或多种酶。
sp.)、分枝杆菌属物种(mycobacterium sp.)、放线菌属物种(actinobacteria sp.)、沙门氏菌属物种(salmonella sp.)、志贺氏菌属物种(shigella sp.)、莫拉氏菌属物种(moraxella sp.)、螺杆菌属物种(helicobacter sp)、窄养单胞菌属物种(stenotrophomonas sp.)、微球菌属物种(micrococcus sp.)、奈瑟球菌属物种(neisseria sp.)、蛭弧菌属物种(bdellovibrio sp.)、嗜血杆菌属物种(hemophilus sp.)、克雷伯氏菌属物种(klebsiella sp.)、奇异变形杆菌(proteus mirabilis)、阴沟肠杆菌(enterobacter cloacae)、沙雷氏菌属物种(serratia sp.)、柠檬酸杆菌属物种(citrobacter sp.)、变形杆菌属物种(proteus sp.)、沙雷氏菌属物种、耶尔森氏菌属物种(yersinia sp.)、不动杆菌属物种(acinetobacter sp.)、放线杆菌属物种(actinobacillus sp.)、包特菌属物种(bordetella sp.)、布鲁氏菌属物种(brucella sp.)、二氧化碳嗜纤维菌属物种(capnocytophaga sp.)、心杆菌属物种(cardiobacterium sp.)、艾肯氏菌属物种(eikenella sp.)、弗朗西斯菌属物种(francisella sp.)、嗜血菌属物种(haemophilus sp.)、金氏杆菌属物种(kingella sp.)、巴斯德氏菌属物种(pasteurella sp.)、黄杆菌属物种(flavobacterium sp.)、黄单胞菌属物种(xanthomonas sp.)、伯克霍尔德氏菌属物种(burkholderia sp.)、气单胞菌属物种(aeromonas sp.)、邻单胞菌属物种(plesiomonas sp.)、军团菌属物种(legionella sp.)和α-变形菌如沃尔巴克氏体属物种(wolbachia sp.)、蓝细菌、螺旋体、绿色硫细菌和绿色非硫细菌、革兰氏阴性球菌、苛求的革兰氏阴性杆菌、肠杆菌科-葡萄糖发酵革兰氏阴性杆菌、革兰氏阴性杆菌-非葡萄糖发酵菌、革兰氏阴性杆菌-葡萄糖发酵、氧化酶阳性的。用于蛋白质表达的特别有用的细菌宿主细胞包括革兰氏阴性菌,例如大肠杆菌、荧光假单胞菌(pseudomonas fiuorescens)、pseudomonas haloplanctis、恶臭假单胞菌(pseudomonas putida) ac 10、pseudomonas pseudof lava、汉氏巴尔通体(bartonella henselae)、丁香假单胞菌(pseudomonas syringae)、新月柄杆菌(caulobacter crescentus)、运动发酵单胞菌(zymomonas mobilis)、苜蓿根瘤菌(rhizobium meliloti)、黄色粘球菌(myxococcus xanthus),以及革兰氏阳性菌如枯草芽孢杆菌(bacillus subtilis)、棒状杆菌属、乳脂链球菌(streptococcus cremoris)、变青链球菌(streptococcus lividans)和变青链霉菌(streptomyces lividans)。大肠杆菌是最广泛使用的表达宿主之一。相应地,用于大肠杆菌中的过表达的技术是充分开发的,并且对于本领域技术人员是可容易获得的。
[0212]
进一步地,荧光假单胞菌通常用于重组蛋白的高水平生产(即用于生物治疗剂和疫苗的开发)。
[0213]
在一些实施方案中,宿主细胞是酵母或真菌细胞。用于蛋白质表达的特别有用的真菌宿主细胞包括米曲霉(aspergillis oryzae)、黑曲霉(aspergillis niger)、里氏木霉(trichoderma reesei)、构巢曲霉(aspergillus nidulans)、禾谷镰刀菌(fusarium graminearum)。用于蛋白质表达的特别有用的酵母宿主细胞包括白色假丝酵母(candida albicans)、麦芽糖假丝酵母(candida maltose)、多形汉逊酵母(hansenula polymorpha)、脆壁克鲁维酵母(kluyveromyces fragilis)、乳酸克鲁维酵母(kluyveromyces lactis)、季也蒙毕赤酵母(pichia guillerimondii)、巴斯德毕赤酵母(pichia pastoris)、酿酒酵母(saccharomyces cerevisiae)、粟酒裂殖酵母(schizosaccharomyces pombe)和解脂耶氏酵母(yarrowia lipolytica)。
[0214]
在一些实施方案中,宿主细胞是昆虫细胞。非限制性实例包括草地夜蛾(spodoptera frugiperda)细胞系(例如sf9或sf21)、果蝇细胞系或蚊子细胞系(例如白纹伊蚊(aedes albopictus)衍生的细胞系)。
[0215]
在一些实施方案中,宿主细胞是哺乳动物细胞。用于蛋白质表达的有用的哺乳动物宿主细胞包括中国仓鼠卵巢(cho)细胞、hela细胞、人胚肾293 (hek293)细胞、幼仓鼠肾(bhk)细胞、猴肾细胞(cos)、人肝细胞癌细胞(例如hep g2)、人胚肾细胞、原牛(bos primigenius)和小家鼠(mus musculus)。在一个具体实施方案中,宿主细胞是cho细胞。另外,哺乳动物宿主细胞可以是建立的、商购可得的细胞系(例如,美国典型培养物保藏中心(atcc),manassas,va)。宿主细胞可以是永生化细胞。可替代地,宿主细胞可以是原代细胞。
[0216]
在一些实施方案中,宿主细胞已进行改造,以产生高水平的目的蛋白质。
[0217]
本公开内容的方法在一些实施方案中,本公开内容提供了治疗患有如本文公开的溶酶体贮积症(lsd)的受试者的方法。该方法包括向受试者施用药物组合物,其包含通过如本文其它地方公开的双顺反子载体表达的溶酶体酶,从而增加溶酶体酶的磷酸化并治疗受试者。
[0218]
在一些实施方案中,本公开内容提供了预防有需要的受试者中的溶酶体贮积症(lsd)发生的方法。该方法包括向受试者施用药物组合物,其包含通过如本文其它地方公开的双顺反子载体表达的溶酶体酶,从而增加溶酶体酶的磷酸化并预防受试者中的lsd发生。
[0219]
在一些实施方案中,溶酶体酶涉及如表1中列出的至少一种溶酶体贮积症(lsd)。在其它实施方案中,溶酶体酶是如表1中列出的至少一种。
[0220]
在进一步的实施方案中,施用包含选自肠内、肠胃外、经口、肌内(im)、皮下(sc)、静脉内(iv)和动脉内(ia)的施用途径。可以用于所公开方法的另外施用途径在本文其它地方详细描述。
[0221]
组合疗法当与可用于治疗lsd的至少一种另外的化合物组合时,如本文所述的用于治疗或预防lsd的组合物和方法可能是有用的。另外的化合物可以包含商购可得的化合物,其已知治疗、预防或减少lsd的症状。化合物可以是但不限于本领域已知的ert。
[0222]
药物组合物和制剂本文还提供的是包含通过本公开内容的双顺反子载体表达的溶酶体酶的药物组合物。
[0223]
此类药物组合物为适合施用于受试者的形式,或者药物组合物可以进一步包含一种或多种药学上可接受的载体、一种或多种另外的成分、或这些的一些组合。药物组合物的各种组分可以以生理学上可接受的盐的形式存在,例如与生理学上可接受的阳离子或阴离子组合,如本领域众所周知的。
[0224]
在本公开内容的一些实施方案中,可以施用对于实践本公开内容的方法有用的药物组合物,以递送1 ng/kg/天至100 mg/kg/天的剂量。在本公开内容的一些实施方案中,可以施用对于实践本公开内容有用的药物组合物,以递送1 ng/kg/天至500 mg/kg/天的剂量。本公开内容的药物组合物中的活性成分、药学上可接受的载体和任何另外成分的相对量,取决于所治疗的受试者的身份、尺寸和状况,并且进一步取决于组合物待施用的途径而变。例如,组合物可以包含0.1%至100% (w/w)的活性成分。
[0225]
在本公开内容的一些实施方案中,可以施用对于实践本公开内容的方法有用的药物组合物,以递送1 ng/kg至100 mg/kg的剂量。在本公开内容的一些实施方案中,可以施用对于实践本公开内容有用的药物组合物,以递送1 ng/kg至500 mg/kg的剂量。在本公开内容的一些实施方案中,药物组合物每天、每周、每两周、每月或每年提供一次。本公开内容的药物组合物中的活性成分、药学上可接受的载体和任何另外成分的相对量,取决于所治疗的受试者的身份、尺寸和状况,并且进一步取决于组合物待施用的途径而变。例如,组合物可以包含0.1%至100% (w/w)的活性成分。
[0226]
在本公开内容的方法中有用的药物组合物可以适当地开发用于吸入、经口、直肠、阴道、肠胃外、局部、经皮、肺、鼻内、颊、眼、鞘内、静脉内或其它施用途径。其它考虑的制剂包括投射纳米颗粒(projected nanoparticle)、脂质体制剂、含有活性成分的重密封红细胞和基于免疫学的制剂。施用途径对技术人员是显而易见的,并且取决于许多因素,包括待治疗疾病的类型和严重性、待治疗的兽医或人患者的类型和年龄等等。
[0227]
本文描述的药物组合物的制剂可以通过药理学领域中已知的或以后开发的任何方法进行制备。一般而言,此类制备方法包括将活性成分与载体或者一种或多种其它辅助成分结合的步骤,然后,需要或期望时,将产品成型或包装成所需的单剂量单位或多剂量单位。在一些实施方案中,本文公开的组合物可以作为裸露的rna在天然衣壳、修饰衣壳中配制,或封装在保护包衣中。
[0228]
活性成分的量一般等于将施用于受试者的活性成分的剂量或此类剂量的方便部分,例如此类剂量的一半或三分之一。单位剂型可以用于单次日剂量或多重日剂量之一(例如,每天约1至4次或更多次)。当使用多重日剂量时,每个剂量的单位剂型可以是相同的或不同的。
[0229]
尽管本文提供的药物组合物的描述原则上针对适合于伦理施用于人的药物组合物,但本领域技术人员应理解此类组合物一般适合于施用于所有种类的动物。修饰适合于施用于人的药物组合物以便致使组合物适合于施用于各种动物是充分理解的,并且普通技术的兽医药理学家可以仅通过普通的实验(如果存在的话)来设计且执行此类修饰。本公开内容的药物组合物考虑施用的受试者包括但不限于人和其它灵长类动物,哺乳动物包括商业上有关的哺乳动物例如牛、猪、马、羊、猫和犬。在一个实施方案中,受试者是人或非人哺乳动物,例如但不限于马科动物、羊科动物、牛科动物、猪科动物、犬科动物、猫科动物和鼠科动物。在一个实施方案中,受试者是人。
[0230]
在一个实施方案中,使用一种或多种药学上可接受的赋形剂或载体来配制组合物。在一些实施方案中,本公开内容提供了用于治疗患有lsd的受试者的药物组合物。在一些实施方案中,本公开内容提供了药物组合物,其包含由本公开内容的双顺反子载体表达的溶酶体酶和药学上可接受的载体。
[0231]
有用的药学上可接受的载体包括但不限于甘油、水、盐水、乙醇和其它药学上可接受的盐溶液例如磷酸盐和有机酸的盐。载体可以是溶剂或分散介质,其含有例如水、乙醇、多元醇(例如甘油、丙二醇和液体聚乙二醇等等)、其合适的混合物和植物油。例如,可以通过使用包衣如卵磷脂、在分散体的情况下通过维持所需的粒度、以及通过使用表面活性剂,来维持适当的流动性。可以通过各种抗菌剂和抗真菌剂来实现微生物作用的预防,所述抗菌剂和抗真菌剂例如对羟基苯甲酸酯、三氯叔丁醇、苯酚、抗坏血酸、硫柳汞等等。在一些实
施方案中,优选在组合物中包括等渗剂,例如糖、氯化钠或多元醇如甘露糖醇和山梨糖醇。可以通过在组合物中包括延迟吸收的试剂,例如单硬脂酸铝或明胶,来实现可注射组合物的延长吸收。
[0232]
制剂可以以具有常规赋形剂的混合物采用,所述赋形剂即适合于经口、肠胃外、鼻、静脉内、皮下、肠内或本领域已知的任何其它合适的施用模式的药学上可接受的有机或无机载体物质。药物制剂可以是灭菌的,并且需要时,可以与辅助试剂混合,所述辅助试剂例如润滑剂、防腐剂、稳定剂、润湿剂、乳化剂、影响缓冲液渗透压的盐、着色剂、调味剂和/或芳香物质等等。当需要时,它们也可以与其它活性剂例如其它镇痛剂组合。
[0233]
所公开的组合物可以包含按组合物的总重量计约0.005%至2.0%的防腐剂。防腐剂用于预防在暴露于环境中的污染物的情况下的变质。根据本公开内容有用的防腐剂的实例包括但不限于选自苯甲醇、山梨酸、对羟基苯甲酸酯、咪唑烷基脲及其组合的那些防腐剂。在一些实施方案中,防腐剂是约0.5%至2.0%苯甲醇和0.05%至0.5%山梨酸的组合。
[0234]
组合物可以包括抗氧化剂和螯合剂,其抑制化合物的降解。用于一些化合物的优选抗氧化剂是在0.01%至0.3%的优选范围内的bht、bha、α-生育酚和抗坏血酸,且更优选按组合物的总重量计在按重量计0.03%至0.1%的范围内的bht。优选地,螯合剂以按组合物的总重量计按重量计0.01%至0.5%的量存在。特别优选的螯合剂包括按组合物的总重量计在按重量计约0.01%至0.20%的重量范围内,且更优选在0.02%至0.10%的范围内的依地酸盐(例如依地酸二钠)和柠檬酸。螯合剂可用于螯合组合物中的金属离子,其可能对制剂的贮存期限有害。在一些实施方案中,bht和依地酸二钠分别是用于一些化合物的抗氧化剂和螯合剂,然而,如本领域技术人员已知的,其它合适的和等价的抗氧化剂和螯合剂可以因此进行取代。
[0235]
施用/给药施用方案可能影响有效量的构成。例如,治疗制剂可以在与溶酶体贮积症(lsd)有关的手术干预之前或之后,或在患者被诊断有溶酶体贮积症(lsd)之后不久,施用于患者受试者。进一步地,几个分份剂量以及交错的剂量可以每天或序贯地施用,或者剂量可以连续地输注,或可以是推注。进一步地,可以如通过治疗或预防情形的紧急程度指示的,治疗制剂的剂量可以按比例增加或降低。
[0236]
本公开内容的组合物对患者受试者,优选哺乳动物,更优选人的施用,可以使用已知程序、以有效治疗受试者中的溶酶体贮积症(lsd)的剂量和时间段来进行。达到疗效所需的治疗化合物的有效量可以根据因素而变,所述因素如所采用的特定化合物的活性;施用时间;化合物的排泄率;治疗的持续时间;与该化合物组合使用的其它药物、化合物或材料;疾病或病症的状态,待治疗的患者的年龄、性别、重量、状况、一般健康和既往病史,以及医学领域众所周知的类似因素。可以调整剂量方案以提供最佳治疗应答。例如,可以每天施用几个分份剂量,或者如通过治疗情形的紧急程度指示的,可以按比例减少剂量。本公开内容的治疗化合物的有效剂量范围的非限制性实例为约0.01至50 mg/kg体重/天。
[0237]
化合物可以频繁至每天几次施用于受试者,或者它可以以更不频繁地施用,例如每天一次、每周一次、每两周一次、每月一次,或甚至更不频繁地施用,例如每几个月一次、或甚至一年一次或更少。应理解,在非限制性实例中,每天给药的化合物的量可以每天、每隔一天、每2天、每3天、每4天或每5天进行施用。例如,对于每隔一天施用,5 mg/天的剂量可
以在星期一开始,第一个后续的5 mg/天的剂量在星期三施用,第二个后续的5 mg/天的剂量在星期五施用,依此类推。剂量的频率对技术人员是显而易见的,并且取决于许多因素,例如但不限于待治疗疾病的类型和严重性、以及动物的类型和年龄。本公开内容的药物组合物中的活性成分的实际剂量水平可以变化,以便获得这样的活性成分的量,其对于特定患者、组合物和施用模式有效实现所需治疗应答,而对患者无毒。具有本领域普通技术的医生,例如医师或兽医,可以容易地确定所需药物组合物的有效量且对此开出处方。例如,医师或兽医可以以低于实现所需疗效需要的水平起始在药物组合物中采用的本公开内容的化合物的剂量,并且逐渐增加剂量直至实现所需效应。
[0238]
在一些实施方案中,将化合物配制成剂量单位形式对于施用的容易和剂量的均匀性是尤其有利的。如本文使用的,剂量单位形式指适合作为用于待治疗的患者的单位剂量的物理离散单元;每个单元含有预定数量的治疗化合物,其计算为与所需的药物媒介物结合产生所需的疗效。本公开内容的剂量单位形式由以下决定并直接取决于以下:(a)治疗化合物的独特特性和待实现的特定疗效,和(b)调配/配制此类治疗化合物用于治疗lsd的领域中固有的限制性。
[0239]
施用途径本领域技术人员将认识到,尽管多于一种途径可以用于施用,但特定途径可以提供比另一种途径更直接和更有效的反应。
[0240]
所公开的组合物的施用途径包括吸入、经口、鼻、直肠、肠胃外、舌下、经皮、经粘膜(例如,舌下、舌、(经)颊、(经)尿道、阴道(例如,经阴道和阴道周)、鼻(内)和(经)直肠)、膀胱内、肺内、十二指肠内、胃内、鞘内、大池内(icm)、脊柱内、心室内、脑室内、皮下、肌内、皮内、动脉内、静脉内、支气管内、吸入和局部施用。合适的组合物和剂型包括例如片剂、胶囊、囊片、丸剂、囊形片(gel cap)、含片、分散体、悬浮液、溶液、糖浆剂、颗粒、珠、经皮贴剂、凝胶、粉末、小丸、乳浆剂、锭剂、乳膏、糊剂、硬膏剂、洗剂、盘剂、栓剂、用于鼻或经口施用的液体喷雾剂、用于吸入的干粉或气溶胶化制剂、用于膀胱内施用的组合物和制剂等等。应当理解,可用于本公开内容的制剂和组合物并不限于本文所述的特定制剂和组合物。在一个实施方案中,lsd的治疗包括选自以下的施用途径:吸入、经口、直肠、阴道、肠胃外、局部、经皮、肺、鼻内、颊、眼、肝内动脉、胸膜内、鞘内、瘤内、静脉内及其任何组合。
[0241]
基因疗法施用本领域技术人员认识到不同的递送方法可以用于将载体施用到细胞内。实例包括:(1)利用物理手段例如电穿孔(电)、基因枪(物理力)或施加大量液体(压力)的方法;以及(2)其中载体与另一种实体复合的方法,所述另一种实体例如脂质体、聚集蛋白或转运蛋白分子。
[0242]
此外,实际剂量和时间表可以取决于组合物是否与其它药物组合物组合施用,或者取决于药代动力学、药物处置和代谢的个体间差异而变。类似地,体外应用中的量可以取决于所利用的特定细胞系(例如,基于细胞表面上存在的载体受体的数目、或用于基因转移的特定载体在该细胞系中复制的能力)而变。此外,每个细胞待添加的载体量很可能随着插入载体中的治疗基因的长度和稳定性以及序列的性质而变,且特别是需要凭经验确定的参数,并且可以由于并非本公开内容的方法所固有的因素(例如,与合成相关的成本)进行改变。本领域技术人员可以依照特定情形的紧急程度容易地进行任何必需的调整。
[0243]
含有治疗剂的细胞还可以含有自杀基因,即编码可以用于破坏细胞的产物的基因。在许多基因疗法情形下,期望能够在宿主细胞中表达用于治疗目的的基因,而且还具有随意破坏宿主细胞的能力。治疗剂可以与自杀基因连接,在不存在激活剂化合物的情况下,所述自杀基因的表达不被激活。当其中已引入药剂和自杀基因两者的细胞死亡是需要的时,将活化剂化合物施用于细胞,从而激活自杀基因的表达并杀死细胞。可以使用的自杀基因/前药组合的实例是单纯疱疹病毒-胸苷激酶(hsv-tk)和更昔洛韦、阿昔洛韦;氧化还原酶和放线菌酮;胞嘧啶脱氨酶和5-氟胞嘧啶;胸苷激酶胸苷酸激酶(tdk::tmk)和azt;以及脱氧胞苷激酶和阿糖胞苷。
[0244]
治疗学本公开内容涵盖了治疗被诊断有lsd的受试者或处于发展lds的风险的受试者中的溶酶体酶缺陷的方法。该方法改善溶酶体酶的磷酸化,从而治疗受试者或预防受试者中的lsd发生。进一步地,该方法改善了患者的生活质量。在一个实施方案中,本公开内容的方法包括向受试者施用包含编码溶酶体酶的多核苷酸和编码glcnac-1 ptase的多核苷酸的组合物。
[0245]
核酸序列:pll01双顺反子载体序列(seq id no: 1) (cmv启动子:斜体且加下划线的。ires:粗体且斜体的。s1-s3:粗体且加下划线的。) ꢀꢀ
1 gacggatcgg gagatctccc gatcccctat ggtgcactct cagtacaatc tgctctgatg
ꢀꢀ
61 ccgcatagtt aagccagtat ctgctccctg cttgtgtgtt ggaggtcgct gagtagtgcg 121 cgagcaaaat ttaagctaca acaaggcaag gcttgaccga caattgcatg aagaatctgc 181 ttagggttag gcgttttgcg ctgcttcgcg atgtacgggc cagatatacg cgttgacatt 241 gattattgac tagttattaa tagtaatcaa ttacggggtc attagttcat agcccatata 301 tggagttccg cgttacataa cttacggtaa atggcccgcc tggctgaccg cccaacgacc 361 cccgcccatt gacgtcaata atgacgtatg ttcccatagt aacgccaata gggactttcc 421 attgacgtca atgggtggag tatttacggt aaactgccca cttggcagta catcaagtgt 481 atcatatgcc aagtacgccc cctattgacg tcaatgacgg taaatggccc gcctggcatt 541 atgcccagta catgacctta tgggactttc ctacttggca gtacatctac gtattagtca 601 tcgctattac catggtgatg cggttttggc agtacatcaa tgggcgtgga tagcggtttg 661 actcacgggg atttccaagt ctccacccca ttgacgtcaa tgggagtttg ttttggcacc 721 aaaatcaacg ggactttcca aaatgtcgta acaactccgc cccattgacg caaatgggcg 781 gtaggcgtgt acggtgggag gtctatataa gcagagctct ctggctaact agagaaccca 841 ctgcttactg gcttatcgaa attaatacga ctcactatag ggagacccaa gctggctagc 901 gtttaaactt aagcttggta ccgagctcgg atccactagt ccagtgtggt ggaattctgc 961 agatatccag cacagtggcg gccgctgatt aacctcagga ctagtggtta ttttccacca1021 tattgccgtc ttttggcaat gtgagggccc ggaaacctgg ccctgtcttc ttgacgagca1081 ttcctagggg tctttcccct ctcgccaaag gaatgcaagg tctgttgaat gtcgtgaagg1141 aagcagttcc tctggaagct tcttgaagac aaacaacgtc tgtagcgacc ctttgcaggc1201 agcggaaccc cccacctggc gacaggtgcc tctgcggcca aaagccacgt gtataagata1261 cacctgcaaa ggcggcacaa ccccagtgcc acgttgtgag ttggatagtt gtggaaagag1321 tcaaatggct cacctcaagc gtattcaaca aggggctgaa ggatgcccag aaggtacccc
1381 attgtatggg atctgatctg gggcctcggt gcacatgctt tacatgtgtt tagtcgaggt1441 taaaaaacgt ctaggccccc cgaaccacgg ggacgtggtt ttcctttgaa agtttgttaa1501 catgctgttc aagctcctgc agagacagac ctatacctgc ctgtcccaca ggtatgggct1561 ctacgtgtgc ttcttgggcg tcgttgtcac catcgtctcc gccttccagt tcggagaggt1621 ggttctggaa tggagccgag atcaatacca tgttttgttt gattcctata gagacaatat1681 tgctggaaag tcctttcaga atcggctttg tctgcccatg ccgattgacg ttgtttacac1741 ctgggtgaat ggcacagatc ttgaactact gaaggaacta acagaattaa aaagatcaaa1801 acgtgatcca ttaataccag aatgtcaagg taaacaaaca ccagaaaaag ataaatgtta1861 tagagatgac atctctgcca gtcgttttga agataacgaa gaactgaggt actcattgcg1921 atctatcgag aggcatgcac catgggttcg gaatattttc attgtcacca acgggcagat1981 tccatcctgg ctgaaccttg acaatcctcg agtgacaata gtaacacacc aggatgtttt2041 tcgaaatttg agccacttgc ctacctttag ttcacctgct attgaaagtc acattcatcg2101 catcgaaggg ctgtcccaga agtttattta cctaaatgat gatgtcatgt ttgggaagga2161 tgtctggcca gatgattttt acagtcactc caaaggccag aaggtttatt tgacatggcc2221 tgtgccaaac ggaggtagcg gaggtgatac atttgcagat tccctcagat atgtaaataa2281 aattctaaat agcaagtttg gattcacatc gcggaaagtc cctgctcaca tgcctcacat2341 gattgaccgg attgttatgc aagaactgca agatatgttc cctgaagaat ttgacaagac2401 gtcatttcac aaagtgcgcc attctgagga tatgcagttt gccttctctt atttttatta2461 tctcatgagt gcagtgcagc cactgaatat atctcaagtc tttgatgaag ttgatacaga2521 tcaatctggt gtcttgtctg acagagaaat ccgaacactg gctaccagaa ttcacgaact2581 gccgttaagt ttgcaggatt tgacaggtct ggaacacatg ctaataaatt gctcaaaaat2641 gcttcctgct gatatcacgc agctaaataa tattccacca actcaggaat cctactatga2701 tcccaacctg ccaccggtca ctaaaagtct agtaacaaac tgtaaaccag taactgacaa2761 aatccacaaa gcatataagg acaaaaacaa atataggttt gaaatcatgg gagaagaaga2821 aatcgctttt aaaatgattc gtaccaacgt ttctcatgtg gttggccagt tggatgacat2881 aagaaaaaac cctaggaagt ttgtttgcct gaatgacaac attgaccaca atcataaaga2941 tgctcagaca gtgaaggctg ttctcaggga cttctatgaa tccatgttcc ccataccttc3001 ccaatttgaa ctgccaagag agtatcgaaa ccgtttcctt catatgcatg agctgcagga3061 atggagggct tatcgagaca aattgaagtt ttggacccat tgtgtactag caacattgat3121 tatgtttact atattctcat tttttgctga gcagttaatt gcacttaagc ggaagatatt3181 tcccagaagg aggatacaca aagaagctag tcccaatcga atcagagtat ctagaggagg3241 taagcctatc cctaaccctc tcctcggtct cgattctacg tgagtttaaa cccgctgatc3301 agcctcgact gtgccttcta gttgccagcc atctgttgtt tgcccctccc ccgtgccttc3361 cttgaccctg gaaggtgcca ctcccactgt cctttcctaa taaaatgagg aaattgcatc3421 gcattgtctg agtaggtgtc attctattct ggggggtggg gtggggcagg acagcaaggg3481 ggaggattgg gaagacaata gcaggcatgc tggggatgcg gtgggctcta tggcttctga3541 ggcggaaaga accagctggg gctctagggg gtatccccac gcgccctgta gcggcgcatt3601 aagcgcggcg ggtgtggtgg ttacgcgcag cgtgaccgct acacttgcca gcgccctagc3661 gcccgctcct ttcgctttct tcccttcctt tctcgccacg ttcgccggct ttccccgtca3721 agctctaaat cgggggctcc ctttagggtt ccgatttagt gctttacggc acctcgaccc3781 caaaaaactt gattagggtg atggttcacg tagtgggcca tcgccctgat agacggtttt3841 tcgccctttg acgttggagt ccacgttctt taatagtgga ctcttgttcc aaactggaac
3901 aacactcaac cctatctcgg tctattcttt tgatttataa gggattttgc cgatttcggc3961 ctattggtta aaaaatgagc tgatttaaca aaaatttaac gcgaattaat tctgtggaat4021 gtgtgtcagt tagggtgtgg aaagtcccca ggctccccag caggcagaag tatgcaaagc4081 atgcatctca attagtcagc aaccaggtgt ggaaagtccc caggctcccc agcaggcaga4141 agtatgcaaa gcatgcatct caattagtca gcaaccatag tcccgcccct aactccgccc4201 atcccgcccc taactccgcc cagttccgcc cattctccgc cccatggctg actaattttt4261 tttatttatg cagaggccga ggccgcctct gcctctgagc tattccagaa gtagtgagga4321 ggcttttttg gaggcctagg cttttgcaaa aagctcccgg gagcttgtat atccattttc4381 ggatctgatc aagagacagg atgaggatcg tttcgcatga ttgaacaaga tggattgcac4441 gcaggttctc cggccgcttg ggtggagagg ctattcggct atgactgggc acaacagaca4501 atcggctgct ctgatgccgc cgtgttccgg ctgtcagcgc aggggcgccc ggttcttttt4561 gtcaagaccg acctgtccgg tgccctgaat gaactgcagg acgaggcagc gcggctatcg4621 tggctggcca cgacgggcgt tccttgcgca gctgtgctcg acgttgtcac tgaagcggga4681 agggactggc tgctattggg cgaagtgccg gggcaggatc tcctgtcatc tcaccttgct4741 cctgccgaga aagtatccat catggctgat gcaatgcggc ggctgcatac gcttgatccg4801 gctacctgcc cattcgacca ccaagcgaaa catcgcatcg agcgagcacg tactcggatg4861 gaagccggtc ttgtcgatca ggatgatctg gacgaagagc atcaggggct cgcgccagcc4921 gaactgttcg ccaggctcaa ggcgcgcatg cccgacggcg aggatctcgt cgtgacccat4981 ggcgatgcct gcttgccgaa tatcatggtg gaaaatggcc gcttttctgg attcatcgac5041 tgtggccggc tgggtgtggc ggaccgctat caggacatag cgttggctac ccgtgatatt5101 gctgaagagc ttggcggcga atgggctgac cgcttcctcg tgctttacgg tatcgccgct5161 cccgattcgc agcgcatcgc cttctatcgc cttcttgacg agttcttctg agcgggactc5221 tggggttcga aatgaccgac caagcgacgc ccaacctgcc atcacgagat ttcgattcca5281 ccgccgcctt ctatgaaagg ttgggcttcg gaatcgtttt ccgggacgcc ggctggatga5341 tcctccagcg cggggatctc atgctggagt tcttcgccca ccccaacttg tttattgcag5401 cttataatgg ttacaaataa agcaatagca tcacaaattt cacaaataaa gcattttttt5461 cactgcattc tagttgtggt ttgtccaaac tcatcaatgt atcttatcat gtctgtatac5521 cgtcgacctc tagctagagc ttggcgtaat catggtcata gctgtttcct gtgtgaaatt5581 gttatccgct cacaattcca cacaacatac gagccggaag cataaagtgt aaagcctggg5641 gtgcctaatg agtgagctaa ctcacattaa ttgcgttgcg ctcactgccc gctttccagt5701 cgggaaacct gtcgtgccag ctgcattaat gaatcggcca acgcgcgggg agaggcggtt5761 tgcgtattgg gcgctcttcc gcttcctcgc tcactgactc gctgcgctcg gtcgttcggc5821 tgcggcgagc ggtatcagct cactcaaagg cggtaatacg gttatccaca gaatcagggg5881 ataacgcagg aaagaacatg tgagcaaaag gccagcaaaa ggccaggaac cgtaaaaagg5941 ccgcgttgct ggcgtttttc cataggctcc gcccccctga cgagcatcac aaaaatcgac6001 gctcaagtca gaggtggcga aacccgacag gactataaag ataccaggcg tttccccctg6061 gaagctccct cgtgcgctct cctgttccga ccctgccgct taccggatac ctgtccgcct6121 ttctcccttc gggaagcgtg gcgctttctc atagctcacg ctgtaggtat ctcagttcgg6181 tgtaggtcgt tcgctccaag ctgggctgtg tgcacgaacc ccccgttcag cccgaccgct6241 gcgccttatc cggtaactat cgtcttgagt ccaacccggt aagacacgac ttatcgccac6301 tggcagcagc cactggtaac aggattagca gagcgaggta tgtaggcggt gctacagagt6361 tcttgaagtg gtggcctaac tacggctaca ctagaagaac agtatttggt atctgcgctc
6421 tgctgaagcc agttaccttc ggaaaaagag ttggtagctc ttgatccggc aaacaaacca6481 ccgctggtag cggttttttt gtttgcaagc agcagattac gcgcagaaaa aaaggatctc6541 aagaagatcc tttgatcttt tctacggggt ctgacgctca gtggaacgaa aactcacgtt6601 aagggatttt ggtcatgaga ttatcaaaaa ggatcttcac ctagatcctt ttaaattaaa6661 aatgaagttt taaatcaatc taaagtatat atgagtaaac ttggtctgac agttaccaat6721 gcttaatcag tgaggcacct atctcagcga tctgtctatt tcgttcatcc atagttgcct6781 gactccccgt cgtgtagata actacgatac gggagggctt accatctggc cccagtgctg6841 caatgatacc gcgagaccca cgctcaccgg ctccagattt atcagcaata aaccagccag6901 ccggaagggc cgagcgcaga agtggtcctg caactttatc cgcctccatc cagtctatta6961 attgttgccg ggaagctaga gtaagtagtt cgccagttaa tagtttgcgc aacgttgttg7021 ccattgctac aggcatcgtg gtgtcacgct cgtcgtttgg tatggcttca ttcagctccg7081 gttcccaacg atcaaggcga gttacatgat cccccatgtt gtgcaaaaaa gcggttagct7141 ccttcggtcc tccgatcgtt gtcagaagta agttggccgc agtgttatca ctcatggtta7201 tggcagcact gcataattct cttactgtca tgccatccgt aagatgcttt tctgtgactg7261 gtgagtactc aaccaagtca ttctgagaat agtgtatgcg gcgaccgagt tgctcttgcc7321 cggcgtcaat acgggataat accgcgccac atagcagaac tttaaaagtg ctcatcattg7381 gaaaacgttc ttcggggcga aaactctcaa ggatcttacc gctgttgaga tccagttcga7441 tgtaacccac tcgtgcaccc aactgatctt cagcatcttt tactttcacc agcgtttctg7501 ggtgagcaaa aacaggaagg caaaatgccg caaaaaaggg aataagggcg acacggaaat7561 gttgaatact catactcttc ctttttcaat attattgaag catttatcag ggttattgtc7621 tcatgagcgg atacatattt gaatgtattt agaaaaataa acaaataggg gttccgcgca7681 catttccccg aaaagtgcca cctgacgtc.cmv序列(seq id no: 2)
ꢀꢀ
1 cgttacataa cttacggtaa atggcccgcc tggctgaccg cccaacgacc cccgcccatt 61 gacgtcaata atgacgtatg ttcccatagt aacgccaata gggactttcc attgacgtca121 atgggtggag tatttacggt aaactgccca cttggcagta catcaagtgt atcatatgcc181 aagtacgccc cctattgacg tcaatgacgg taaatggccc gcctggcatt atgcccagta241 catgacctta tgggactttc ctacttggca gtacatctac gtattagtca tcgctattac301 catggtgatg cggttttggc agtacatcaa tgggcgtgga tagcggtttg actcacgggg361 atttccaagt ctccacccca ttgacgtcaa tgggagtttg ttttggcacc aaaatcaacg421 ggactttcca aaatgtcgta acaactccgc cccattgacg caaatgggcg gtaggcgtgt481 acggtgggag gtctatataa gcagagct.ires序列(seq id no: 3)
ꢀꢀ
1 ggttattttc caccatattg ccgtcttttg gcaatgtgag ggcccggaaa cctggccctg 61 tcttcttgac gagcattcct aggggtcttt cccctctcgc caaaggaatg caaggtctgt121 tgaatgtcgt gaaggaagca gttcctctgg aagcttcttg aagacaaaca acgtctgtag181 cgaccctttg caggcagcgg aaccccccac ctggcgacag gtgcctctgc ggccaaaagc241 cacgtgtata agatacacct gcaaaggcgg cacaacccca gtgccacgtt gtgagttgga301 tagttgtgga aagagtcaaa tggctcacct caagcgtatt caacaagggg ctgaaggatg361 cccagaaggt accccattgt atgggatctg atctggggcc tcggtgcaca tgctttacat421 gtgtttagtc gaggttaaaa aacgtctagg ccccccgaac cacggggacg tggttttcct481 ttgaaa.
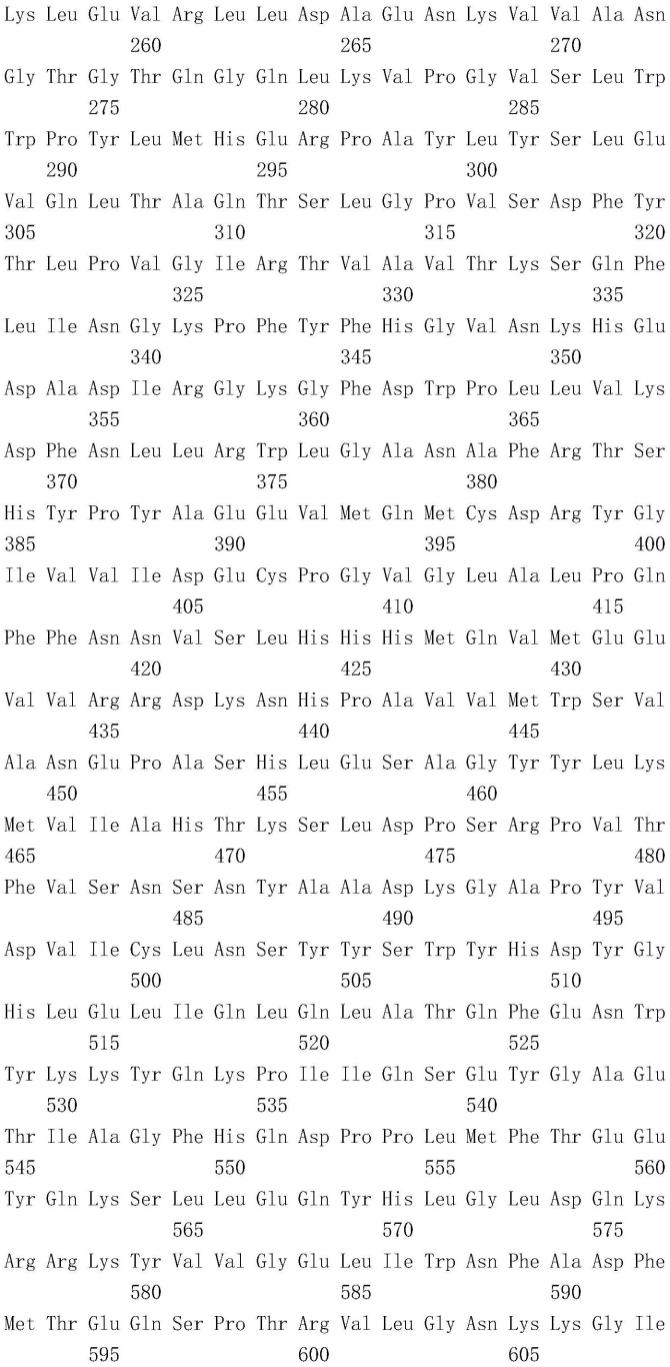
修饰的glcnac-1磷酸转移酶(glcnac-1 ptase),s1-s3序列(seq id no: 4)
ꢀꢀꢀ
1 atgctgttca agctcctgca gagacagacc tatacctgcc tgtcccacag gtatgggctc
ꢀꢀ
61 tacgtgtgct tcttgggcgt cgttgtcacc atcgtctccg ccttccagtt cggagaggtg 121 gttctggaat ggagccgaga tcaataccat gttttgtttg attcctatag agacaatatt 181 gctggaaagt cctttcagaa tcggctttgt ctgcccatgc cgattgacgt tgtttacacc 241 tgggtgaatg gcacagatct tgaactactg aaggaactaa cagaattaaa aagatcaaaa 301 cgtgatccat taataccaga atgtcaaggt aaacaaacac cagaaaaaga taaatgttat 361 agagatgaca tctctgccag tcgttttgaa gataacgaag aactgaggta ctcattgcga 421 tctatcgaga ggcatgcacc atgggttcgg aatattttca ttgtcaccaa cgggcagatt 481 ccatcctggc tgaaccttga caatcctcga gtgacaatag taacacacca ggatgttttt 541 cgaaatttga gccacttgcc tacctttagt tcacctgcta ttgaaagtca cattcatcgc 601 atcgaagggc tgtcccagaa gtttatttac ctaaatgatg atgtcatgtt tgggaaggat 661 gtctggccag atgattttta cagtcactcc aaaggccaga aggtttattt gacatggcct 721 gtgccaaacg gaggtagcgg aggtgataca tttgcagatt ccctcagata tgtaaataaa 781 attctaaata gcaagtttgg attcacatcg cggaaagtcc ctgctcacat gcctcacatg 841 attgaccgga ttgttatgca agaactgcaa gatatgttcc ctgaagaatt tgacaagacg 901 tcatttcaca aagtgcgcca ttctgaggat atgcagtttg ccttctctta tttttattat 961 ctcatgagtg cagtgcagcc actgaatata tctcaagtct ttgatgaagt tgatacagat1021 caatctggtg tcttgtctga cagagaaatc cgaacactgg ctaccagaat tcacgaactg1081 ccgttaagtt tgcaggattt gacaggtctg gaacacatgc taataaattg ctcaaaaatg1141 cttcctgctg atatcacgca gctaaataat attccaccaa ctcaggaatc ctactatgat1201 cccaacctgc caccggtcac taaaagtcta gtaacaaact gtaaaccagt aactgacaaa1261 atccacaaag catataagga caaaaacaaa tataggtttg aaatcatggg agaagaagaa1321 atcgctttta aaatgattcg taccaacgtt tctcatgtgg ttggccagtt ggatgacata1381 agaaaaaacc ctaggaagtt tgtttgcctg aatgacaaca ttgaccacaa tcataaagat1441 gctcagacag tgaaggctgt tctcagggac ttctatgaat ccatgttccc cataccttcc1501 caatttgaac tgccaagaga gtatcgaaac cgtttccttc atatgcatga gctgcaggaa1561 tggagggctt atcgagacaa attgaagttt tggacccatt gtgtactagc aacattgatt1621 atgtttacta tattctcatt ttttgctgag cagttaattg cacttaagcg gaagatattt1681 cccagaagga ggatacacaa agaagctagt cccaatcgaa tcagagta.hgba野生型序列(seq id no: 5):
ꢀꢀꢀ
1 atggagtttt caagtccttc cagagaggaa tgtcccaagc ctttgagtag ggtaagcatc
ꢀꢀ
61 atggctggca gcctcacagg attgcttcta cttcaggcag tgtcgtgggc atcaggtgcc 121 cgcccctgca tccctaaaag cttcggctac agctcggtgg tgtgtgtctg caatgccaca 181 tactgtgact cctttgaccc cccgaccttt cctgcccttg gtaccttcag ccgctatgag 241 agtacacgca gtgggcgacg gatggagctg agtatggggc ccatccaggc taatcacacg 301 ggcacaggcc tgctactgac cctgcagcca gaacagaagt tccagaaagt gaagggattt 361 ggaggggcca tgacagatgc tgctgctctc aacatccttg ccctgtcacc ccctgcccaa 421 aatttgctac ttaaatcgta cttctctgaa gaaggaatcg gatataacat catccgggta 481 cccatggcca gctgtgactt ctccatccgc acctacacct atgcagacac ccctgatgat 541 ttccagttgc acaacttcag cctcccagag gaagatacca agctcaagat acccctgatt 601 caccgagccc tgcagttggc ccagcgtccc gtttcactcc ttgccagccc ctggacatca
ꢀ
661 cccacttggc tcaagaccaa tggagcggtg aatgggaagg ggtcactcaa gggacagccc 721 ggagacatct accaccagac ctgggccaga tactttgtga agttcctgga tgcctatgct 781 gagcacaagt tacagttctg ggcagtgaca gctgaaaatg agccttctgc tgggctgttg 841 agtggatacc ccttccagtg cctgggcttc acccctgaac atcagcgaga cttcattgcc 901 cgtgacctag gtcctaccct cgccaacagt actcaccaca atgtccgcct actcatgctg 961 gatgaccaac gcttgctgct gccccactgg gcaaaggtgg tactgacaga cccagaagca1021 gctaaatatg ttcatggcat tgctgtacat tggtacctgg actttctggc tccagccaaa1081 gccaccctag gggagacaca ccgcctgttc cccaacacca tgctctttgc ctcagaggcc1141 tgtgtgggct ccaagttctg ggagcagagt gtgcggctag gctcctggga tcgagggatg1201 cagtacagcc acagcatcat cacgaacctc ctgtaccatg tggtcggctg gaccgactgg1261 aaccttgccc tgaaccccga aggaggaccc aattgggtgc gtaactttgt cgacagtccc1321 atcattgtag acatcaccaa ggacacgttt tacaaacagc ccatgttcta ccaccttggc1381 cacttcagca agttcattcc tgagggctcc cagagagtgg ggctggttgc cagtcagaag1441 aacgacctgg acgcagtggc actgatgcat cccgatggct ctgctgttgt ggtcgtgcta1501 aaccgctcct ctaaggatgt gcctcttacc atcaaggatc ctgctgtggg cttcctggag1561 acaatctcac ctggctactc cattcacacc tacctgtggc gtcgccagtg a.hgba天然变体序列(seq id no: 162):hgba (k360n)序列。粗体且加下划线的核苷酸在突变位点处。
[0246]
ꢀꢀꢀ
1 atggagtttt caagtccttc cagagaggaa tgtcccaagc ctttgagtag ggtaagcatc
ꢀꢀ
61 atggctggca gcctcacagg tttgcttcta cttcaggcag tgtcgtgggc atcaggtgcc 121 cgcccctgca tccctaaaag cttcggctac agctcggtgg tgtgtgtctg caatgccaca 181 tactgtgact cctttgaccc cccgaccttt cctgcccttg gtaccttcag ccgctatgag 241 agtacacgca gtgggcgacg gatggagctg agtatggggc ccatccaggc taatcacacg 301 ggcacaggcc tgctactgac cctgcagcca gaacagaagt tccagaaagt gaagggattt 361 ggaggggcca tgacagatgc tgctgctctc aacatccttg ccctgtcacc ccctgcccaa 421 aatttgctac ttaaatcgta cttctctgaa gaaggaatcg gatataacat catccgggta 481 cccatggcca gctgtgactt ctccatccgc acctacacct atgcagacac ccctgatgat 541 ttccagttgc acaacttcag cctcccagag gaagatacca agctcaagat acccctgatt 601 caccgagccc tgcagttggc ccagcgtccc gtttcactcc ttgccagccc ctggacatca 661 cccacttggc tcaagaccaa tggagcggtg aatgggaagg ggtcactcaa gggacagccc 721 ggagacatct accaccagac ctgggccaga tactttgtga agttcctgga tgcctatgct 781 gagcacaagt tacagttctg ggcagtgaca gctgaaaatg agccttctgc tgggctgttg 841 agtggatacc ccttccagtg cctgggcttc acccctgaac atcagcgaga cttcattgcc 901 cgtgacctag gtcctaccct cgccaacagt actcaccaca atgtccgcct actcatgctg 961 gatgaccaac gcttgctgct gccccactgg gcaaaggtgg tactgacaga cccagaagca1021 gctaaatatg ttcatggcat tgctgtacat tggtacctgg actttctggc tccagccaac1081 gccaccctag gggagacaca ccgcctgttc cccaacacca tgctctttgc ctcagaggcc1141 tgtgtgggct ccaagttctg ggagcagagt gtgcggctag gctcctggga tcgagggatg1201 cagtacagcc acagcatcat cacgaacctc ctgtaccatg tggtcggctg gaccgactgg1261 aaccttgccc tgaaccccga aggaggaccc aattgggtgc gtaactttgt cgacagtccc1321 atcattgtag acatcaccaa ggacacgttt tacaaacagc ccatgttcta ccaccttggc1381 cacttcagca agttcattcc tgagggctcc cagagagtgg ggctggttgc cagtcagaag
1441 aacgacctgg acgcagtggc actgatgcat cccgatggct ctgctgttgt ggtcgtgcta1501 aaccgctcct ctaaggatgt gcctcttacc atcaaggatc ctgctgtggg cttcctggag1561 acaatctcac ctggctactc cattcacacc tacctgtggc gtcgccagtg a.hgba改造的变体序列(seq id no: 163):hgba (c165s)序列。粗体且加下划线的核苷酸在突变位点处。
[0247]
ꢀꢀꢀ
1 atggagtttt caagtccttc cagagaggaa tgtcccaagc ctttgagtag ggtaagcatc
ꢀꢀ
61 atggctggca gcctcacagg tttgcttcta cttcaggcag tgtcgtgggc atcaggtgcc 121 cgcccctgca tccctaaaag cttcggctac agctcggtgg tgtgtgtctg caatgccaca 181 tactgtgact cctttgaccc cccgaccttt cctgcccttg gtaccttcag ccgctatgag 241 agtacacgca gtgggcgacg gatggagctg agtatggggc ccatccaggc taatcacacg 301 ggcacaggcc tgctactgac cctgcagcca gaacagaagt tccagaaagt gaagggattt 361 ggaggggcca tgacagatgc tgctgctctc aacatccttg ccctgtcacc ccctgcccaa 421 aatttgctac ttaaatcgta cttctctgaa gaaggaatcg gatataacat catccgggta 481 cccatggcca gctccgactt ctccatccgc acctacacct atgcagacac ccctgatgat 541 ttccagttgc acaacttcag cctcccagag gaagatacca agctcaagat acccctgatt 601 caccgagccc tgcagttggc ccagcgtccc gtttcactcc ttgccagccc ctggacatca 661 cccacttggc tcaagaccaa tggagcggtg aatgggaagg ggtcactcaa gggacagccc 721 ggagacatct accaccagac ctgggccaga tactttgtga agttcctgga tgcctatgct 781 gagcacaagt tacagttctg ggcagtgaca gctgaaaatg agccttctgc tgggctgttg 841 agtggatacc ccttccagtg cctgggcttc acccctgaac atcagcgaga cttcattgcc 901 cgtgacctag gtcctaccct cgccaacagt actcaccaca atgtccgcct actcatgctg 961 gatgaccaac gcttgctgct gccccactgg gcaaaggtgg tactgacaga cccagaagca1021 gctaaatatg ttcatggcat tgctgtacat tggtacctgg actttctggc tccagccaaa1081 gccaccctag gggagacaca ccgcctgttc cccaacacca tgctctttgc ctcagaggcc1141 tgtgtgggct ccaagttctg ggagcagagt gtgcggctag gctcctggga tcgagggatg1201 cagtacagcc acagcatcat cacgaacctc ctgtaccatg tggtcggctg gaccgactgg1261 aaccttgccc tgaaccccga aggaggaccc aattgggtgc gtaactttgt cgacagtccc1321 atcattgtag acatcaccaa ggacacgttt tacaaacagc ccatgttcta ccaccttggc1381 cacttcagca agttcattcc tgagggctcc cagagagtgg ggctggttgc cagtcagaag1441 aacgacctgg acgcagtggc actgatgcat cccgatggct ctgctgttgt ggtcgtgcta1501 aaccgctcct ctaaggatgt gcctcttacc atcaaggatc ctgctgtggg cttcctggag1561 acaatctcac ctggctactc cattcacacc tacctgtggc gtcgccagtg a.mgalc序列(seq id no: 6):
ꢀꢀꢀ1ꢀꢀ
atggctaaca gccaacctaa ggcttcccag caacgccaag caaaagtcat gaccgccgcc
ꢀꢀ
61
ꢀꢀ
gcgggctcgg cgagccgtgt tgcggtgccc ttattgttgt gtgcgctgct agtgcccggt 121
ꢀꢀ
ggcgcctacg tgctggacga ctctgacggc ctgggcagag agttcgacgg catcggcgct 181
ꢀꢀ
gtgtctggcg gcggagccac aagcagactg ctggtcaact accccgagcc ctacagaagc 241
ꢀꢀ
gagatcctgg actacctgtt caagcccaac ttcggcgcca gcctgcacat cctgaaggtg 301
ꢀꢀ
gaaatcggcg gcgacggcca gaccaccgac ggcacagagc ccagccacat gcactacgag 361
ꢀꢀ
ctggatgaga actacttcag aggctacgag tggtggctga tgaaggaagc caagaagaga 421
ꢀꢀ
aaccccgaca tcatcctgat gggcctgcct tggagcttcc ccggctggct gggcaagggc 481
ꢀꢀ
ttcagctggc cctacgtgaa cctgcagctg accgcctact acgtcgtgcg gtggattctg
ꢀ
541
ꢀꢀ
ggcgccaagc actaccacga cctggacatc gactacatcg gcatctggaa cgagaggccc 601
ꢀꢀ
ttcgacgcca actacatcaa agaactgagg aagatgctgg attaccaggg cctgcagaga 661
ꢀꢀ
gtgcggatca ttgccagcga caacctgtgg gagcccatca gcagctccct gctgctggac 721
ꢀꢀ
caggacctgt ggaaggtcgt cgacgtgatc ggcgcccact accctggcac ctacaccgtg 781
ꢀꢀ
tggaacgcca agatgagcgg caagaagctg tggtccagcg aggacttcag caccatcaac 841
ꢀꢀ
agcaacgtgg gagccggctg ctggtccaga atcctgaacc agaattacat caacggcaac 901
ꢀꢀ
atgaccagca caatcgcctg gnaacctggn ggccagctac tacgaggact gccctacggc 961
ꢀꢀ
agatccggcc tgatgaccgc ccaggaacct tggagcggcc actacgtggt ggcttcccca1021
ꢀꢀ
atctgggtgt ccgcccacac cacccagttc acccagcctg gctggtacta cctgaaaacc1081
ꢀꢀ
gtgggccacc tggaaaaggg cggcagctac gtggccctga ccgatggcct gggcaacctg1141
ꢀꢀ
accatcatca tcgagacaat gagccaccag cacagcatgt gcatcagacc ctacctgccc1201
ꢀꢀ
tactacaacg tgtcccacca gctggccaca ttcaccctga agggcagcct gagagagatc1261
ꢀꢀ
caggaactgc aggtctggta caccaagctg ggcacccccc agcagagact gcacttcaag1321
ꢀꢀ
cagctggaca ccctgtggct gctggacggc agcggcagct tcaccctgga actggaagag1381
ꢀꢀ
gacgaaatct tcaccctgac cacactgacc accggcagaa agggcagcta ccccccacct1441
ꢀꢀ
cctagcagca agccattccc caccaactac aaggacgact tcaacgtgga ataccccctg1501
ꢀꢀ
ttcagcgagg cccccaactt cgccgaccag accggcgtgt tcgagtacta catgaacaac1561
ꢀꢀ
gaggacagag agcacaggtt caccctgaga caggtgctga accagaggcc catcacctgg1621
ꢀꢀ
gctgccgacg ccagcagcac catctccgtg atcggggacc accactggac caacatgacc1681
ꢀꢀ
gtgcagtgcg acgtgtacat cgagacacct agaagcggcg gagtgtttat cgccggcaga1741
ꢀꢀ
gtgaacaagg gcggcatcct gatcagatcc gctacaggcg tgttcttctg gatcttcgcc1801
ꢀꢀ
aacggcagct acagagtgac cgccgacctg ggcggctgga tcacatacgc ctctggccac1861
ꢀꢀ
gccgacgtga ccgccaagag atggtacacc ctgaccctgg gcatcaaggg ctacttcgcc1921
ꢀꢀ
ttcggcatgc tgaacggcac catcctgtgg aagaacgtgc gcgtgaagta ccccggccac1981
ꢀꢀ
ggctgggctg ccatcggcac ccacacattc gagttcgccc agttcgacaa ctttcgcgtg2041
ꢀꢀ
gaagctgctc gc.hgla序列(seq id no: 7):
ꢀꢀꢀ
1 atgcagctga ggaacccaga actacatctg ggctgcgcgc ttgcgcttcg cttcctggcc
ꢀꢀ
61 ctcgtttcct gggacatccc tggggctaga gcactggaca atggattggc aaggacgcct 121 accatgggct ggctgcactg ggagcgcttc atgtgcaacc ttgactgcca ggaagagcca 181 gattcctgca tcagtgagaa gctcttcatg gagatggcag agctcatggt ctcagaaggc 241 tggaaggatg caggttatga gtacctctgc attgatgact gttggatggc tccccaaaga 301 gattcagaag gcagacttca ggcagaccct cagcgctttc ctcatgggat tcgccagcta 361 gctaattatg ttcacagcaa aggactgaag ctagggattt atgcagatgt tggaaataaa 421 acctgcgcag gcttccctgg gagttttgga tactacgaca ttgatgccca gacctttgct 481 gactggggag tagatctgct aaaatttgat ggttgttact gtgacagttt ggaaaatttg 541 gcagatggtt ataagcacat gtccttggcc ctgaatagga ctggcagaag cattgtgtac 601 tcctgtgagt ggcctcttta tatgtggccc tttcaaaagc ccaattatac agaaatccga 661 cagtactgca atcactggcg aaattttgct gacattgatg attcctggaa aagtataaag 721 agtatcttgg actggacatc ttttaaccag gagagaattg ttgatgttgc tggaccaggg 781 ggttggaatg acccagatat gttagtgatt ggcaactttg gcctcagctg gaatcagcaa 841 gtaactcaga tggccctctg ggctatcatg gctgctcctt tattcatgtc taatgacctc
ꢀ
901 cgacacatca gccctcaagc caaagctctc cttcaggata aggacgtaat tgccatcaat 961 caggacccct tgggcaagca agggtaccag cttagacagg gagacaactt tgaagtgtgg1021 gaacgacctc tctcaggctt agcctgggct gtagctatga taaaccggca ggagattggt1081 ggacctcgct cttataccat cgcagttgct tccctgggta aaggagtggc ctgtaatcct1141 gcctgcttca tcacacagct cctccctgtg aaaaggaagc tagggttcta tgaatggact1201 tcaaggttaa gaagtcacat aaatcccaca ggcactgttt tgcttcagct agaaaataca1261
ꢀꢀ
cagatgt cattaaaaga cttactttaa.hnaglu序列(seq id no: 8):
ꢀꢀꢀ
1 atggaggcgg tggcggtggc cgcggcggtg ggggtccttc tcctggccgg ggccgggggc
ꢀꢀ
61 gcggcaggcg acgaggcccg ggaggcggcg gccgtgcggg cgctcgtggc ccggctgctg 121 gggccaggcc ccgcggccga cttctccgtg tcggtggagc gcgctctggc tgccaagccg 181 ggcttggaca cctacagcct gggcggcggc ggcgcggcgc gcgtgcgggt gcgcggctcc 241 acgggcgtgg cggccgccgc ggggctgcac cgctacctgc gcgacttctg tggctgccac 301 gtggcctggt ccggctctca gctgcgcctg ccgcggccac tgccagccgt gccgggggag 361 ctgaccgagg ccacgcccaa caggtaccgc tattaccaga atgtgtgcac gcaaagctac 421 tctttcgtgt ggtgggactg ggcccgctgg gagcgagaga tagactggat ggcgctgaat 481 ggcatcaacc tggcactggc ctggagcggc caggaggcca tctggcagcg ggtgtacctg 541 gccttgggcc tgacccaggc agagatcaat gagttcttta ctggtcctgc cttcctggcc 601 tgggggcgaa tgggcaacct gcacacctgg gatggccccc tgcccccctc ctggcacatc 661 aagcagcttt acctgcagca ccgggtcctg gaccagatgc gctccttcgg catgacccca 721 gtgctgcctg cattcgcggg gcatgttccc gaggctgtca ccagggtgtt ccctcaggtc 781 aatgtcacga agatgggcag ttggggccac tttaactgtt cctactcctg ctccttcctt 841 ctggctccgg aagaccccat attccccatc atcgggagcc tcttcctgcg agagctgatc 901 aaagagtttg gcacagacca catctatggg gccgacactt tcaatgagat gcagccacct 961 tcctcagagc cctcctacct tgccgcagcc accactgccg tctatgaggc catgactgca1021 gtggatactg aggctgtgtg gctgctccaa ggctggctct tccagcacca gccgcagttc1081 tgggggcccg cccagatcag ggctgtgctg ggagctgtgc cccgtggccg cctcctggtt1141 ctggacctgt ttgctgagag ccagcctgtg tatacccgca ctgcctcctt ccagggccag1201 cccttcatct ggtgcatgct gcacaacttt gggggaaacc atggtctttt tggagcccta1261 gaggctgtga acggaggccc agaagctgcc cgcctcttcc ccaactccac catggtaggc1321 acgggcatgg cccccgaggg catcagccag aacgaagtgg tctattccct catggctgag1381 ctgggctggc gaaaggaccc agtgccagat ttggcagcct gggtgaccag ctttgccgcc1441 cggcggtatg gggtctccca cccggacgca ggggcagcgt ggaggctact gctccggagt1501 gtgtacaact gctccgggga ggcctgcagg ggccacaatc gtagcccgct ggtcaggcgg1561 ccgtccctac agatgaatac cagcatctgg tacaaccgat ctgatgtgtt tgaggcctgg1621 cggctgctgc tcacatctgc tccctccctg gccaccagcc ccgccttccg ctacgacctg1681 ctggacctca ctcggcaggc agtgcaggag ctggtcagct tgtactatga ggaggcaaga1741 agcgcctacc tgagcaagga gctggcctcc ctgttgaggg ctggaggcgt cctggcctat1801 gagctgctgc cggcactgga cgaggtgctg gctagtgaca gccgcttctt gctgggcagc1861 tggctagagc aggcccgagc agcggcagtc agtgaggccg aggccgattt ctacgagcag1921 aacagccgct accagctgac cttgtggggg ccagaaggca acatcctgga ctatgccaac1981 aagcagctgg cggggttggt ggccaactac tacacccctc gctggcggct tttcctggag
2041 gcgctggttg acagtgtggc ccagggcatc cctttccaac agcaccagtt tgacaaaaat2101 gtcttccaac tggagcaggc cttcgttctc agcaagcaga ggtaccccag ccagccgcga2161 ggagacactg tggacctggc caagaagatc ttcctcaaat attacccccg ctgggtggcc2221 ggctcttggt ga.hgaa序列(seq id no: 9):
ꢀꢀꢀ
1 atgggagtga ggcacccgcc ctgctcccac cggctcctgg ccgtctgcgc cctcgtgtcc
ꢀꢀ
61 ttggcaaccg ctgcactcct ggggcacatc ctactccatg atttcctgct ggttccccga 121 gagctgagtg gctcctcccc agtcctggag gagactcacc cagctcacca gcagggagcc 181 agcagaccag ggccccggga tgcccaggca caccccggcc gtcccagagc agtgcccaca 241 cagtgcgacg tcccccccaa cagccgcttc gattgcgccc ctgacaaggc catcacccag 301 gaacagtgcg aggcccgcgg ctgttgctac atccctgcaa agcaggggct gcagggagcc 361 cagatggggc agccctggtg cttcttccca cccagctacc ccagctacaa gctggagaac 421 ctgagctcct ctgaaatggg ctacacggcc accctgaccc gtaccacccc caccttcttc 481 cccaaggaca tcctgaccct gcggctggac gtgatgatgg agactgagaa ccgcctccac 541 ttcacgatca aagatccagc taacaggcgc tacgaggtgc ccttggagac cccgcatgtc 601 cacagccggg caccgtcccc actctacagc gtggagttct ccgaggagcc cttcggggtg 661 atcgtgcgcc ggcagctgga cggccgcgtg ctgctgaaca cgacggtggc gcccctgttc 721 tttgcggacc agttccttca gctgtccacc tcgctgccct cgcagtatat cacaggcctc 781 gccgagcacc tcagtcccct gatgctcagc accagctgga ccaggatcac cctgtggaac 841 cgggaccttg cgcccacgcc cggtgcgaac ctctacgggt ctcacccttt ctacctggcg 901 ctggaggacg gcgggtcggc acacggggtg ttcctgctaa acagcaatgc catggatgtg 961 gtcctgcagc cgagccctgc ccttagctgg aggtcgacag gtgggatcct ggatgtctac1021 atcttcctgg gcccagagcc caagagcgtg gtgcagcagt acctggacgt tgtgggatac1081 ccgttcatgc cgccatactg gggcctgggc ttccacctgt gccgctgggg ctactcctcc1141 accgctatca cccgccaggt ggtggagaac atgaccaggg cccacttccc cctggacgtc1201 cagtggaacg acctggacta catggactcc cggagggact tcacgttcaa caaggatggc1261 ttccgggact tcccggccat ggtgcaggag ctgcaccagg gcggccggcg ctacatgatg1321 atcgtggatc ctgccatcag cagctcgggc cctgccggga gctacaggcc ctacgacgag1381 ggtctgcgga ggggggtttt catcaccaac gagaccggcc agccgctgat tgggaaggta1441 tggcccgggt ccactgcctt ccccgacttc accaacccca cagccctggc ctggtgggag1501 gacatggtgg ctgagttcca tgaccaggtg cccttcgacg gcatgtggat tgacatgaac1561 gagccttcca acttcatcag gggctctgag gacggctgcc ccaacaatga gctggagaac1621 ccaccctacg tgcctggggt ggttgggggg accctccagg cggccaccat ctgtgcctcc1681 agccaccagt ttctctccac acactacaac ctgcacaacc tctacggcct gaccgaagcc1741 atcgcctccc acagggcgct ggtgaaggct cgggggacac gcccatttgt gatctcccgc1801 tcgacctttg ctggccacgg ccgatacgcc ggccactgga cgggggacgt gtggagctcc1861 tgggagcagc tcgcctcctc cgtgccagaa atcctgcagt ttaacctgct gggggtgcct1921 ctggtcgggg ccgacgtctg cggcttcctg ggcaacacct cagaggagct gtgtgtgcgc1981 tggacccagc tgggggcctt ctaccccttc atgcggaacc acaacagcct gctcagtctg2041 ccccaggagc cgtacagctt cagcgagccg gcccagcagg ccatgaggaa ggccctcacc2101 ctgcgctacg cactcctccc ccacctctac acactgttcc accaggccca cgtcgcgggg2161 gagaccgtgg cccggcccct cttcctggag ttccccaagg actctagcac ctggactgtg
2221 gaccaccagc tcctgtgggg ggaggccctg ctcatcaccc cagtgctcca ggccgggaag2281 gccgaagtga ctggctactt ccccttgggc acatggtacg acctgcagac ggtgccagta2341 gaggcccttg gcagcctccc acccccacct gcagctcccc gtgagccagc catccacagc2401 gaggggcagt gggtgacgct gccggccccc ctggacacca tcaacgtcca cctccgggct2461 gggtacatca tccccctgca gggccctggc ctcacaacca cagagtcccg ccagcagccc2521 atggccctgg ctgtggccct gaccaagggt ggggaggccc gaggggagct gttctgggac2581 gatggagaga gcctggaagt gctggagcga ggggcctaca cacaggtcat cttcctggcc2641 aggaataaca cgatcgtgaa tgagctggta cgtgtgacca gtgagggagc tggcctgcag2701 ctgcagaagg tgactgtcct gggcgtggcc acggcgcccc agcaggtcct ctccaacggt2761 gtccctgtct ccaacttcac ctacagcccc gacaccaagg tcctggacat ctgtgtctcg2821 ctgttgatgg gagagcagtt tctcgtcagc tggtgttag.hgaa (seq id no: 164;uniprot登录号p10253-1)
ꢀꢀ
1 mgvrhppcsh rllavcalvs lataallghi llhdfllvpr elsgsspvle ethpahqqga 61 srpgprdaqa hpgrpravpt qcdvppnsrf dcapdkaitq eqceargccy ipakqglqga121 qmgqpwcffp psypsyklen lsssemgyta tltrttptff pkdiltlrld vmmetenrlh181 ftikdpanrr yevpletphv hsrapsplys vefseepfgv ivrrqldgrv llnttvaplf241 fadqflqlst slpsqyitgl aehlsplmls tswtritlwn rdlaptpgan lygshpfyla301 ledggsahgv fllnsnamdv vlqpspalsw rstggildvy iflgpepksv vqqyldvvgy361 pfmppywglg fhlcrwgyss taitrqvven mtrahfpldv qwndldymds rrdftfnkdg421 frdfpamvqe lhqggrrymm ivdpaisssg pagsyrpyde glrrgvfitn etgqpligkv481 wpgstafpdf tnptalawwe dmvaefhdqv pfdgmwidmn epsnfirgse dgcpnnelen541 ppyvpgvvgg tlqaaticas shqflsthyn lhnlygltea iashralvka rgtrpfvisr601 stfaghgrya ghwtgdvwss weqlassvpe ilqfnllgvp lvgadvcgfl gntseelcvr661 wtqlgafypf mrnhnsllsl pqepysfsep aqqamrkalt lryallphly tlfhqahvag721 etvarplfle fpkdsstwtv dhqllwgeal litpvlqagk aevtgyfplg twydlqtvpv781 ealgslpppp aaprepaihs egqwvtlpap ldtinvhlra gyiiplqgpg ltttesrqqp841 malavaltkg geargelfwd dgeslevler gaytqvifla rnntivnelv rvtsegaglq901 lqkvtvlgva tapqqvlsng vpvsnftysp dtkvldicvs llmgeqflvs wc.hlaman序列(seq id no: 10):
ꢀꢀꢀ
1 atgggcgcct acgcgcgggc ttcgggggtc tgcgctcgcg gctgcctgga ctcagcaggc
ꢀꢀ
61 ccctggacca tgtcccgcgc cctgcggcca ccgctcccgc ctctctgctt tttccttttg 121 ttgctggcgg ctgccggtgc tcgggccggg ggatacgaga catgccccac agtgcagccg 181 aacatgctga acgtgcacct gctgcctcac acacatgatg acgtgggctg gctcaaaacc 241 gtggaccagt acttttatgg aatcaagaat gacatccagc acgccggtgt gcagtacatc 301 ctggactcgg tcatctctgc cttgctggca gatcccaccc gtcgcttcat ttacgtggag 361 attgccttct tctcccgttg gtggcaccag cagacaaatg ccacacagga agtcgtgcga 421 gaccttgtgc gccaggggcg cctggagttc gccaatggtg gctgggtgat gaacgatgag 481 gcagccaccc actacggtgc catcgtggac cagatgacac ttgggctgcg ctttctggag 541 gacacatttg gcaatgatgg gcgaccccgt gtggcctggc acattgaccc cttcggccac 601 tctcgggagc aggcctcgct gtttgcgcag atgggcttcg acggcttctt ctttgggcgc 661 cttgattatc aagataagtg ggtacggatg cagaagctgg agatggagca ggtgtggcgg 721 gccagcacca gcctgaagcc cccgaccgcg gacctcttca ctggtgtgct tcccaatggt
ꢀ
781 tacaacccgc caaggaatct gtgctgggat gtgctgtgtg tcgatcagcc gctggtggag 841 gaccctcgca gccccgagta caacgccaag gagctggtcg attacttcct aaatgtggcc 901 actgcccagg gccggtatta ccgcaccaac cacactgtga tgaccatggg ctcggacttc 961 caatatgaga atgccaacat gtggttcaag aaccttgaca agctcatccg gctggtaaat1021 gcgcagcagg caaaaggaag cagtgtccat gttctctact ccacccccgc ttgttacctc1081 tgggagctga acaaggccaa cctcacctgg tcagtgaaac atgacgactt cttcccttac1141 gcggatggcc cccaccagtt ctggaccggt tacttttcca gtcggccggc cctcaaacgc1201 tacgagcgcc tcagctacaa cttcctgcag gtgtgcaacc agctggaggc gctggtgggc1261 ctggcggcca acgtgggacc ctatggctcc ggagacagtg cacccctcaa tgaggcgatg1321 gctgtgctcc agcatcacga cgccgtcagc ggcacctccc gccagcacgt ggccaacgac1381 tacgcgcgcc agcttgcggc aggctggggg ccttgcgagg ttcttctgag caacgcgctg1441 gcgcggctca gaggcttcaa agatcacttc accttttgcc aacagctaaa catcagcatc1501 tgcccgctca gccagacggc ggcgcgcttc caggtcatcg tttataatcc cctggggcgg1561 aaggtgaatt ggatggtacg gctgccggtc agcgaaggcg ttttcgttgt gaaggacccc1621 aatggcagga cagtgcccag cgatgtggta atatttccca gctcagacag ccaggcgcac1681 cctccggagc tgctgttctc agcctcactg cccgccctgg gcttcagcac ctattcagta1741 gcccaggtgc ctcgctggaa gccccaggcc cgcgcaccac agcccatccc cagaagatcc1801 tggtcccctg ctttaaccat cgaaaatgag cacatccggg caacgtttga tcctgacaca1861 gggctgttga tggagattat gaacatgaat cagcaactcc tgctgcctgt tcgccagacc1921 ttcttctggt acaacgccag tataggtgac aacgaaagtg accaggcctc aggtgcctac1981 atcttcagac ccaaccaaca gaaaccgctg cctgtgagcc gctgggctca gatccacctg2041 gtgaagacac ccttggtgca ggaggtgcac cagaacttct cagcttggtg ttcccaggtg2101 gttcgcctgt acccaggaca gcggcacctg gagctagagt ggtcggtggg gccgatacct2161 gtgggcgaca cctgggggaa ggaggtcatc agccgttttg acacaccgct ggagacaaag2221 ggacgcttct acacagacag caatggccgg gagatcctgg agaggaggcg ggattatcga2281 cccacctgga aactgaacca gacggagccc gtggcaggaa actactatcc agtcaacacc2341 cggatttaca tcacggatgg aaacatgcag ctgactgtgc tgactgaccg ctcccagggg2401 ggcagcagcc tgagagatgg ctcgctggag ctcatggtgc accgaaggct gctgaaggac2461 gatggacgcg gagtatcgga gccactaatg gagaacgggt cgggggcgtg ggtgcgaggg2521 cgccacctgg tgctgctgga cacagcccag gctgcagccg ccggacaccg gctcctggcg2581 gagcaggagg tcctggcccc tcaggtggtg ctggccccgg gtggcggcgc cgcctacaat2641 ctcggggctc ctccgcgcac gcagttctca gggctgcgca gggacctgcc gccctcggtg2701 cacctgctca cgctggccag ctggggcccc gaaatggtgc tgctgcgctt ggagcaccag2761 tttgccgtag gagaggattc cggacgtaac ctgagcgccc ccgttacctt gaacttgagg2821 gacctgttct ccaccttcac catcacccgc ctgcaggaga ccacgctggt ggccaaccag2881 ctccgcgagg cagcctccag gctcaagtgg acaacaaaca caggccccac accccaccaa2941 actccgtacc agctggaccc ggccaacatc acgctggaac ccatggaaat ccgcactttc3001 ctggcctcag ttcaatggaa ggaggtggat ggt.hgalc序列(seq id no: 23;genbank登录号:bc036518.2):
ꢀꢀꢀ
1 aaaagctatg actgcggccg cgggttcggc gggccgcgcc gcggtgccct tgctgctgtg
ꢀꢀ
61 tgcgctgctg gcgcccggcg gcgcgtacgt gctcgacgac tccgacgggc tgggccggga 121 gttcgacggc atcggcgcgg tcagcggcgg cggggcaacc tcccgacttc tagtaaatta
ꢀ
181 cccagagccc tatcgttctc agatattgga ttatctcttt aagccgaatt ttggtgcctc 241 tttgcatatt ttaaaagtgg aaataggtgg tgatgggcag acaacagatg gcactgagcc 301 ctcccacatg cattatgcac tagatgagaa ttatttccga ggatacgagt ggtggttgat 361 gaaagaagct aagaagagga atcccaatat tacactcatt gggttgccat ggtcattccc 421 tggatggctg ggaaaaggtt tcgactggcc ttatgtcaat cttcagctga ctgcctatta 481 tgtcgtgacc tggattgtgg gcgccaagcg ttaccatgat ttggacattg attatattgg 541 aatttggaat gagaggtcat ataatgccaa ttatattaag atattaagaa aaatgctgaa 601 ttatcaaggt ctccagcgag tgaaaatcat agcaagtgat aatctctggg agtccatctc 661 tgcatccatg ctccttgatg ccgaactctt caaggtggtt gatgttatag gggctcatta 721 tcctggaacc cattcagcaa aagatgcaaa gttgactggg aagaagcttt ggtcttctga 781 agactttagc actttaaata gtgacatggg tgcaggctgc tggggtcgca ttttaaatca 841 gaattatatc aatggctata tgacttccac aatcgcatgg aatttagtgg ctagttacta 901 tgaacagttg ccttatggga gatgcgggtt gatgacggcc caggagccat ggagtgggca 961 ctacgtggta gaatctcctg tctgggtatc agctcatacc actcagttta ctcaacctgg1021 ctggtattac ctgaagacag ttggccattt agagaaagga ggaagctacg tagctctgac1081 tgatggctta gggaacctca ccatcatcat tgaaaccatg agtcataaac attctaagtg1141 catacggcca tttcttcctt atttcaatgt gtcacaacaa tttgccacct ttgttcttaa1201 gggatctttt agtgaaatac cagagctaca ggtatggtat accaaacttg gaaaaacatc1261 cgaaagattt ctttttaagc agctggattc tctatggctc cttgacagcg atggcagttt1321 cacactgagc ctgcatgaag atgagctgtt cacactcacc actctcacca ctggtcgcaa1381 aggcagctac ccgcttcctc caaaatccca gcccttccca agtacctata aggatgattt1441 caatgttgat tacccatttt ttagtgaagc tccaaacttt gctgatcaaa ctggtgtatt1501 tgaatatttt acaaatattg aagaccctgg cgagcatcac ttcacgctac gccaagttct1561 caaccagaga cccattacgt gggctgccga tgcatccaac acaatcagta ttataggaga1621 ctacaactgg accaatctga ctacaaagtg tgatgtttac atagagaccc ctgacacagg1681 aggtgtgttc attgcaggaa gagtaaataa aggtggtatt ttgattagaa gtgccagagg1741 aattttcttc tggatttttg caaatggatc ttacagggtt acaggtgatt tagctggatg1801 gattatatat gctttaggac gtgttgaagt tacagcaaaa aaatggtata cactcacgtt1861 aactattaag ggtcatttcg cctctggcat gctgaatgac aagtctctgt ggacagacat1921 ccctgtgaat tttccaaaga atggctgggc tgcaattgga actcactcct ttgaatttgc1981 acagtttgac aactttcttg tggaagccac acgctaatac ttaacagggc atcatagaat2041 actctggatt ttcttccctt ctttttggtt ttggttcaga gccaattctt gtttcattgg2101 aacagtatat gaggcttttg agactaaaaa taatgaagag taaaagggga gagaaattta2161 tttttaattt accctgtgga agattttatt agaattaatt ccaaggggaa aactggtgaa2221 tctttaacat tacctggtgt gttccctaac attcaaactg tgcattggcc atacccttag2281 gagtggtttg agtagtacag acctcgaagc cttgctgcta acactgaggt agctctcttc2341 atcttatttg caagcggtcc tgtagatggc agtaacttga tcatcactga gatgtattta2401 tgcatgctga ccgtgtgtcc aagtgagcca gtgtcttcat cacaagatga tgctgccata2461 atagaaagct gaagaacact agaagtagct ttttgaaaac cacttcaacc tgttatgctt2521 tatgctctaa aaagtatttt ttttattttc ctttttaaga tgatactttt gaaatgcagg2581 atatgatgag tgggatgatt ttaaaaatgc ctctttaata aactacctct aacactattt2641 ctgtggtaat agatattagc agattaattg ggttatttgc attatttaat ttttttgatt
2701 ccaagttttg gtcttgtaac cactataact ctctgtgaac atttttccag gtggctggaa2761 gaaggaagaa aacctgatat agccaatgct gttgtagtcg tttcctcagc ctcatctcac2821 tgtgctgtgg tctgtcctca catgtgcact ggtaacagac tcacacagct gatgaatgct2881 tttctctcct tatgtgtgga aggaggggag cacttagaca tttgctaact cccagaattg2941 gatcatctcc taagatgtac ttacttttta aagtccaaat atgtttatat ttaaatatac3001 gtgagcatgt tcatcatgtt gtatgattta tactaagcat taatgtggct ctatgtagca3061 aatcagttat tcatgtaggt aaagtaaatc tagaattatt tataagaatt actcattgaa3121 ctaattctac tatttaggaa tttgtaagag tctaacatag gcttagctac agtgaagttt3181 tgcattgctt ttgaagacaa gaagataagt gctagaataa ataagattac agagaaaatt3241 ttttgttaaa accaagtgat ttccagctga tgtatctaat attttttaaa acgaacatta3301 tagaggtgta atttatttac aataaaatgt tcctacttta aatatacaat tcagtgagtt3361 ttgataaatt gatataccca tgtaaccaac actccagtca agcttcagaa tatttccatc3421 accccagaag gttctcttgt atacctgctc agtcagttcc tttcactccc gattgttggc3481 agccattgat aggaattcta tcactatagg ttagttttct ttgttccaga acatcatgaa3541 agcggcgtca tgtactgtgt attcttatga atggtttctt tccatcagca taatgatttg3601 agatttgtcc atgttgtgtg attcagtggt ttgttccttc ttatttctga agagttttcc3661 attgtatgaa tataccacaa tttgtttcct ccccaccagt ttctgatact acaattaaaa3721 ctgtctacat ttacaaaaaa aaaaaaaaa.cef启动子序列(seq id no: 161):
ꢀꢀ
1 gttacataac ttatggtaaa tggcctgcct ggctgactgc ccaatgaccc ctgcccaatg 61 atgtcaataa tgatgtatgt tcccatgtaa tgccaatagg gactttccat tgatgtcaat121 gggtggagta tttatggtaa ctgcccactt ggcagtacat caagtgtatc atatgccaag181 tatgccccct attgatgtca atgatggtaa atggcctgcc tggcattatg cccagtacat241 gaccttatgg gactttccta cttggcagta catctatgta ttagtcattg ctattaccat301 gggaattcac tagtggagaa gagcatgctt gagggctgag tgcccctcag tgggcagaga361 gcacatggcc cacagtccct gagaagttgg ggggaggggt gggcaattga actggtgcct421 agagaaggtg gggcttgggt aaactgggaa agtgatgtgg tgtactggct ccaccttttt481 ccccagggtg ggggagaacc atatataagt gcagtagtct ctgtgaacat tc。
[0248]
表 2:研究中使用的引物。
引物序列seqidno:限制性酶gba-fctgctagccaccatggagttttcaagtccttc11nheigba-ratagcggccgctcactggcgacgccacaggt12notigaa-fctgctagccaccatgggagtgaggcacccgccctg13nheigaa-ratagcggccgctcaacaccagctgacgagaaactgctc14notigalc-fctgctagccaccatggctaacagccaacctaaggc15nheigalc-ratagcggccgctcagcgagcagcttccacgcgaaagttg16notinaglu-fctgctagccaccatggaagccgtggctgtcgcag17nheinaglu-ratagcggccgctcaccaactaccagccacccatctag18notigla-fctggatccaccatgcagctgaggaacccagaac19bamhigla-ratagcggccgctcaaagtaagtcttttaatgacatctg20notilaman-fctgctagccaccatgggcgcctacgcgcgggcttc21nhei
laman-ratagcggccgctcaaccatccacctccttccattgaac22noti
实施例
[0249]
现在参考下述实施例描述本公开内容。提供这些实施例仅用于说明的目的,并且本公开内容决不应该解释为限于这些实施例,而是应该解释为涵盖由于本文提供的教导而变得显而易见的任何和所有变化。
[0250]
无需进一步描述,认为本领域普通技术人员可以使用先前的描述和下述说明性实施例来制备且利用本公开内容的化合物,并且实践请求保护的方法。因此,下述工作实施例具体指出了本公开内容的优选实施方案,并且不应解释为以任何方式限制本公开内容的剩余部分。
[0251]
现在描述这些实验中采用的材料和方法。
[0252]
细胞系:将hek293t细胞维持在含有0.11 g/l丙酮酸钠和4.5 g/l葡萄糖、补充有110% (vol/vol) fbs (gibco)、100,000 u/l青霉素、100 mg/l链霉素(invitrogen)和2 mm l-谷氨酰胺(invitrogen)的dmem (corning)中。expi293细胞(invitrogen)在expi293表达培养基(invitrogen)中悬浮生长。
[0253]
dna构建体:cmv-s1s3质粒由st. louis的washington university school的stuart kornfeld教授提供。双顺反子载体pll01在如下的两个步骤中创建:在第一步中,从ptase α/β和γ双顺反子构建体(由stuart kornfeld教授提供)扩增486 bp ires序列,并且通过pcr从质粒cmv-s1s3获得s1-s3基因片段。这两个片段随后在第二步中通过重叠延伸pcr连接在一起,以形成ires-s1s3片段。ires-s1s3片段用hpai和pmei限制性酶(neb)进行消化,并且连接到pcdna3.1 ( )载体内。为了生成pll11、pll21、pll31、pll41、pll51和pll61双顺反子质粒,hgba、hgaa、mgalc、hnaglu、hgla和hlaman基因通过其特异性引物(表1)进行扩增并插入双顺反子载体(pll01)内。
[0254]
磷酸转移酶测定法:收获hek293t或expi293细胞,并且在裂解缓冲液(25 mm tris-cl ph 7.2、150 mm nacl、1% triton x-100和蛋白酶抑制剂混合物)中裂解。在75 mm udp-glcnac、1 mci udp-[3h]glcnac和100 mm amm的存在下,使5
ꢀµ
l细胞提取物在磷酸转移酶测定法缓冲液(50 mm tris-cl ph 7.4、10 mm mgcl2、10 mm mncl2、2 mg/ml bsa、2 mm atp)中以50
ꢀµ
l的最终体积在37℃下温育0.5小时。通过添加1 ml 2 mm edta ph 8.0来终止反应,并且使样品经受qae-sephadex层析。
[0255]
酶生产:expi293细胞用空载体、双顺反子质粒或其单一表达质粒进行转染。在2-3天后收获培养基。对于gba的生产,在细胞培养过程中含有30 um异桑叶生物碱(isofagomine)以稳定分泌酶的条件培养基,在pbs缓冲液中在4
°
c下透析过夜,以去除异桑叶生物碱用于酶活性测定法。
[0256]
酶活性测定法:下述底物用于酶活性测定法:4-甲基伞形酮[3-d-吡喃葡糖苷(gcase/gba酶底物,m3633,sigma)、4-甲基伞形酮α-d-吡喃葡糖苷(gaa酶底物,m9766,sigma)、6-十六烷酰基氨基-4-甲基伞形酮[3-d-吡喃半乳糖苷(galc酶底物,eh05989,carbosynth)、4-甲基伞形酮-n-乙酰-α-d-氨基葡糖苷(naglu酶底物,474500,millipore)、4-甲基伞形酮α-d-吡喃半乳糖苷(gla酶底物,m7633,sigma)、以及4-甲基伞形酮α-d-吡喃甘露糖苷(laman酶底物,m3657,sigma)。gba酶活性在具有1 mm gba底物的柠檬酸盐-磷酸
盐缓冲液ph5.0、0.25% tx-100、0.25%牛磺胆酸钠中进行测定。gaa酶活性在具有1 mm gaa底物的柠檬酸盐缓冲液ph4.0、0.25% tx-100中进行。galc酶活性在具有0.1 mm galc底物的柠檬酸盐-磷酸盐缓冲液ph4.0、0.25% tx-100、0.6%牛磺胆酸钠、0.2%油酸中执行。naglu酶活性在具有1 mm naglu底物的柠檬酸盐缓冲液ph4.0、0.25% tx-100中进行测定。gla酶活性在具有1 mm gla底物的柠檬酸盐缓冲液ph4.5、0.25% tx-100中进行测定。laman酶活性在具有1 mm laman底物的柠檬酸盐缓冲液ph4.0、0.25% tx-100中进行测定。
[0257]
ci-mpr结合测定法:在高结合96孔板(costar 3601)中执行ci-mpr结合。板在室温(rt)下用以10
ꢀµ
g/ml的50
ꢀµ
l纯化的牛ci-mpr固定1小时,并且在rt下通过2% bsa再封闭1小时。来自转染的expi293细胞的条件培养基的等分试样用hepes缓冲液(40 mm hepes ph6.8、150 mm nacl、0.05% tween-20)进行稀释,并且与固定的ci-mpr一起在rt下温育1小时,以结合磷酸化的溶酶体酶。在3次洗涤后,通过4-甲基伞形酮法测定溶酶体酶活性。
[0258]
实施例1:用于溶酶体酶表达的含有磷酸转移酶(s1-s3)的空双顺反子载体的生成作为由两种基因(gnptab和gnptg)编码的α2β2γ2六聚体的glcnac-1-磷酸转移酶(glcnac-1-ptase,也称为ptase),涉及经由不依赖于阳离子的甘露糖6-磷酸受体(ci-mpr)的溶酶体靶向所需的磷酸化寡糖的生成。通过与改造的截短的ptase (s1-s3)共转染,所表达的溶酶体酶的磷酸化显著增加。这项研究利用s1-s3构建体用于产生磷酸化的溶酶体酶,用于治疗溶酶体贮积病(lsd,例如但不限于戈谢病、庞贝病和α-甘露糖苷贮积症)。
[0259]
为了产生用于酶替代疗法(ert)的高度磷酸化的治疗性溶酶体酶,使治疗性溶酶体酶和s1-s3在相同细胞中同时共表达。由于s1-s3和溶酶体酶在不同的载体中表达,为了产生高度磷酸化的治疗性溶酶体酶,通过两个步骤生成具有溶酶体酶和s1-s3表达的稳定细胞系:(a)创建表达ptase s1-s3的稳定细胞系;(b)基于s1-s3稳定细胞系,生成向其中添加治疗性溶酶体酶的表达的第二细胞系。为了避免这种两步且耗时的程序,本文公开的是通过引入内部核糖体进入位点(ires)的双顺反子载体,其能够在单个启动子下表达两种分开的基因。
[0260]
双顺反子表达也可以应用于溶酶体贮积病(lsd)的基因疗法。空的双顺反子载体
ꢀ–ꢀ
含有在pcdna3.1 ( )质粒载体中的巨细胞病毒(cmv)启动子下的486bp ires序列和s1-s3基因的pll01 (图1b)。双顺反子载体pll01具有在多克隆位点中的三个独特的限制性酶切割位点,其定位于ires序列的前面,并且允许插入治疗性溶酶体酶基因。为了检查使用双顺反子载体pll01的s1-s3表达,用等量的pcdna3.1 ( )、cmv-s1s3 (图1a)或pll01质粒转染hek293细胞。48小时后,收获细胞并在裂解缓冲液(具有蛋白酶抑制剂混合物的25 mm tris缓冲液ph7.4、150 mm nacl、1% tx-100)中裂解。执行表达pcdna3.1 ( )、cmv-s1s3或pll01的全细胞提取物的磷酸转移酶活性分析,以确定s1-s3的表达。如图1c中所示,与样品cmv-s1s3相比,pcdna3.1 ( )样品中的磷酸转移酶活性是可忽略不计的,但双顺反子载体pll01维持9.3%的活性。
[0261]
实施例2:双顺反子表达增强治疗性溶酶体酶的磷酸化由于双顺反子载体中的s1-s3表达很低(9.3%) (参见实施例1),因此这项研究设计为确定低s1-s3活性是否足以使溶酶体酶磷酸化。在本双顺反子载体中测试了六种不同的溶酶体酶。所述酶如下:酸性β-葡糖苷酶(gba)、酸性α-葡糖苷酶(gaa)、半乳糖神经酰胺酶(galc)、α-n-乙酰氨基葡糖苷酶(naglu)、α-半乳糖苷酶(gla)和酸性α-甘露糖苷酶
(laman)。
[0262]
酸性β-葡糖苷酶(gba):gba是一种溶酶体酶,其在溶酶体中降解其底物葡糖脑苷脂。溶酶体中的gba缺乏引起戈谢病,其是最常见的溶酶体贮积病(lsd)。为了测试本文公开的双顺反子载体中gba的磷酸化,通过经由nhei和noti限制位点,将具有终止密码子的1611 bp人gba cdna序列插入双顺反子空载体
ꢀ‑ꢀ
pll01内,生成gba双顺反子质粒
ꢀ‑ꢀ
pll11 (图2a)。将相同量的pll11和gba质粒连同或不连同cmv-s1s3质粒一起转染到expi293细胞内。48小时后,分别收获细胞和条件培养基。令人惊讶的是,pll11条件培养基中的gba活性为240 nmol/小时/ml,其是通过单独的gba (96 nmol/小时/ml)或gba和s1-s3共转染(90 nmol/小时/ml,图2b)制备的培养基的多于两倍。除gba表达之外,s1-s3表达还通过使用细胞提取物的磷酸转移酶测定法进行定量。与缺乏gba的双顺反子载体pll01类似,与gba&s1-s3的共转染样品相比,pll11样品具有7.5%的磷酸转移酶表达(图2c)。
[0263]
由于s1-s3表达在双顺反子载体中降低,因此确定了低磷酸转移酶表达对gba磷酸化的后果。为此,收获了pll11、单独的gba以及与s1-s3共转染的gba的条件培养基,并且通过执行不依赖于阳离子的甘露糖6-磷酸受体(ci-mpr)结合实验来定量磷酸化程度。在本文公开的双顺反子载体中产生的gba在平台期具有与ci-mpr甚至更高的结合(图3a)。然而,当通过使用线性范围点计算受体结合的百分比时,所公开的双顺反子载体中生成的44%的gba与ci-mpr结合,其与通过与s1-s3的共转染产生的gba相同(43%),并且是通过内源性磷酸转移酶产生的gba的十倍(4.5%,图3b)。
[0264]
滴定已在本领域中广泛用于确定所鉴定的分析物的浓度。滴定结合实验中的ci-mpr浓度。将连续稀释的ci-mpr固定到96孔板中,并且将类似量的通过本文公开的双顺反子载体产生的gba酶或内源性磷酸酶(ptase)加入板内,用于受体结合测定法。如图3c中所示,来自pll11样品的gba的结合取决于ci-mpr的浓度,并且当受体浓度达到15
ꢀµ
g/ml时,它是饱和的,而通过内源性ptase产生的gba的结合保持在低水平下。所述数据指示所公开的双顺反子载体极大地升高了gba酶的磷酸化水平。
[0265]
酸性α-葡糖苷酶(gaa):溶酶体酶gaa对于溶酶体中的糖原降解为葡萄糖是必要的。gaa基因中的突变与溶酶体贮积症
ꢀ‑ꢀ
庞贝病相关。为了创建gaa双顺反子质粒-pll21,扩增含有终止密码子的2859个基对(bp)的人gaa基因片段,并且在通过限制性酶nhei和noti消化后,插入双顺反子载体pll01内(图4a)。序列验证的pll21和gaa质粒在expi293细胞中进行转染。48小时后,收集条件培养基用于gaa活性和ci-mpr结合实验。与gba类似,pll21条件培养基中的gaa活性高于gaa单一表达(图4b)。pll21条件培养基的结合比gaa单一条件培养基更快且更高(图4c)。在1小时的温育时间过程中,来自pll21条件培养基的72.5%的gaa与ci-mpr结合,但来自gaa单一表达的gaa的ci-mpr结合仅为21.5% (图4d)。这些数据提示了,本文公开的双顺反子表达平台可以极大地增加gaa酶的磷酸化。
[0266]
半乳糖神经酰胺酶(galc):在溶酶体中,galc酶通过从神经酰胺衍生物中去除半乳糖,负责半乳糖神经酰胺的分解代谢。galc酶的遗传缺陷导致克拉伯病。为了测试本文公开的双顺反子表达中的galc酶,通过将小鼠galc基因插入载体pll01内,生成双顺反子质粒pll31 (图5a)。在pll31转染的expi293细胞中收获的pll31条件培养基中的galc酶活性类似于单独的galc培养基(0.86 nmol/
µ
l/h相对于0.62 nmol/
µ
l/h,图5b)。ci-mpr受体结合结果显示了,galc与s1-s3的双顺反子表达将其ci-mpr结合从28.4%增加到56.8% (图5c和
d)。
[0267]
α-n-乙酰氨基葡糖苷酶(naglu):naglu基因编码降解溶酶体中的硫酸肝素的酶。naglu酶缺陷导致圣菲利波综合征b型,也称为粘多糖贮积症(mps) iiib。当用于ert的naglu酶在细胞系中产生时,在甘露糖残基中没有任何磷酸基。并且今年早些时候,其ert的临床试验失败。为了在本文公开的双顺反子载体中表达naglu,使用与上文所述相同的程序。将2229 bp人naglu基因插入pll01双顺反子载体内(图6a),并且将naglu双顺反子质粒-pll41和naglu单一表达质粒转染到expi293细胞内。通过使用条件培养基,样品pll41中的naglu活性显示为高于naglu单一表达样品(图6b)。就ci-mpr结合而言,即使我们加入大量酶(高达9 nmol/小时,图6c-6d),从naglu单一表达样品中几乎检测不到任何naglu结合。然而,通过双顺反子载体产生的naglu与高达25%的ci-mpr结合(图6c-6d)。
[0268]
α-半乳糖苷酶(gla):溶酶体酶gla将蜜二糖水解成半乳糖和葡萄糖,并且能够代谢球形三酰神经酰胺(gl-3)。gla酶活性的缺乏引起x连锁病症
ꢀ‑ꢀ
法布里病。为了制备gla双顺反子质粒
ꢀ‑ꢀ
pll51,人gla基因片段和双顺反子载体pll01用bamhi和noti进行消化,并且通过t4连接酶进行连接(图7a)。正确的pll51克隆和gla单一质粒在expi293细胞中进行转染且表达。gla活性测定法和ci-mpr结合实验通过使用其条件培养基进行。如图7b中所示,单独的gla或pll51条件培养基中的gla活性是相似的。使用这两种培养基的滴定曲线提示了,pll51样品比gla样品更多且更快地与ci-mpr结合(图7c)。pll51样品的总体结合百分比为62.1%,其几乎是gla样品的两倍(33.1%,图7d)。
[0269]
酸性α-甘露糖苷酶(laman):遗传病α-甘露糖苷贮积症通过由man2b1基因编码的溶酶体酶laman的缺陷引起。由于人laman酶几乎没有磷酸化,因此hlaman是用于所公开的双顺反子表达的良好候选物。将3033 bp人laman基因插入pll01双顺反子载体内(图8a),并且在expi293细胞中表达用于以后研究。laman双顺反子质粒pll61条件培养基中的laman活性略低于laman单一表达(图8b)。当滴定它们与ci-mpr的结合时,通过使用laman单一表达样品几乎检测不到与ci-mpr结合的laman酶,但发现来自pll61样品的大量laman酶与ci-mpr相互作用(图8c)。使用s1-s3双顺反子表达,laman与ci-mpr的结合从1.6%增加到75.2% (图8d)。
[0270]
上文六种酶可以基于其基础磷酸化水平分成两组。第一组是低磷酸化溶酶体酶(gba、naglu和laman),其是在酶生产过程中野生型ptase的不良底物。第二组是高磷酸化酶(gaa、galc和gla)。所述酶被视为野生型ptase的良好底物,并且接受了相当量的磷酸盐。本文公开的s1-s3的双顺反子表达显示显著增加六种溶酶体酶的磷酸,不依赖于其基础磷酸化水平。鉴于这些发现,本文公开的双顺反子载体pll01可以用于产生高度磷酸化的溶酶体酶,以治疗所有溶酶体贮积病。显然,本文公开的双顺反子载体极大地有利于用于治疗溶酶体贮积症的ert和基因疗法。
[0271]
实施例3:戈谢病的治疗酶替代疗法(ert)包含编码gba的序列和编码s1-s3 ptase的序列的表达载体可以用于治疗或预防戈谢病的体征或症状。下述研究证实了,(gcase/gba)-s1-s3在领域公认的标准的戈谢病小鼠模型中的表达导致(gcase/gba)-s1-s3的表达、v-s1-s3从循环血流转运到细胞内、以及吸收v-s1-s3复合物的细胞中v的活性增加。起因于gba-s1-s3复合物的表达和摄取的
(gcase/gba)活性的少量增加导致小鼠模型中功能的显著功能恢复。
[0272]
利用具有s1-s3 ptase的双顺反子表达载体表达gba,生成具有更高水平的磷酸化寡糖的重组蛋白,其可以用于治疗或预防戈谢病的体征或症状。下述研究证实了,在领域公认的标准的戈谢病小鼠模型中,使用重组蛋白(其使用具有s1-s3 ptase的双顺反子载体表达)的ert导致与目前护理标准相比更长的半衰期、更大的组织摄取、更大的底物减少和更好的组织病理学校正。
[0273]
图16a-16b是描绘在20周龄的gaucher
d409v/null
小鼠的肝、肺和脾中观察到的葡萄糖神经酰胺水平升高的一对图。在组织匀浆中确定gba的天然底物葡糖脑苷脂的累积。gc在肺中的累积是具有统计学和治疗价值的结果,其是目前护理标准的已知的未满足需求。通过加入200
ꢀµ
l甲醇/acn/h2o (v:v:v=85:10:5),以800 rpm混合5分钟,随后以3220 g 4℃离心15分钟;3),提取20
ꢀµ
l等份试样的组织匀浆,并且适当的对照是葡萄糖神经酰胺。回收50
ꢀµ
l上清液,用氮干燥并且用甲醇/acn/h2o (v:v:v=85:10:5)重悬浮,并且直接进样用于lc-ms/ms分析。
[0274]
图17a-17c是证实与伊米苷酶相比,gcase
m6p
在gba
d409v/null
小鼠模型中具有更长的半衰期和更大的组织摄取的一系列图。使用标准护理、伊米苷酶和纯化的gba (其通过利用编码s1-s3 ptase和gba的天然变体的双顺反子载体在expi293细胞中的瞬时共表达产生),执行戈谢d409v/null小鼠模型中的pk/pd研究。这种gcase变体在中性和弱碱性条件下具有更大的稳定性。简言之,3只动物接受了~ 1.5 mg/kg重组gcase的尾静脉注射。对于血清药代动力学数据,在2、10、20、40和60分钟收集血浆样品。使用合成底物4-甲基伞形酮-β-d-吡喃葡糖苷(4mu-glc)测量活性。通过将2分钟时间点设定为100%活性,并且随后的时间点是t=2分钟时间点的百分比,使各个动物中的活性标准化。在s1-s3 ptase的存在下表达的稳定gcase似乎具有更长的半衰期。这种更长的半衰期是具有更大稳定性的酶和不同清除途径的组合。为了确定多少gcase由组织吸收,在酶注射后2小时,回收组织、匀浆化并使用4mu-glc底物测量活性。如通过用于蛋白质测定的bca方法确定的,活性针对匀浆中的总蛋白质进行标准化。在显示的组织摄取数据中,观察到具有适当磷酸化的稳定gcases的真正优点。对于所有评估的组织,在利用双顺反子s1-s3 ptase载体平台s1’s3 ptase表达的稳定gcase中,发现更多活性。这在其中伊米苷酶具有很少活性的肺、肌肉和脑中最为显著。当将组织和血清数据放在一起时,具有更高n联寡糖磷酸化的更稳定gcase的优点对于将更多酶递送到受影响的组织是显而易见的。这是第一次已以这些剂量将显著量的gcase递送到肺、肌肉和心脏。
[0275]
图18a-18e是一系列照片和条形图,其证实在gba
d409v/null
小鼠模型中,gcase
m6p ert比伊米苷酶更好地减少组织巨噬细胞(抗cd68染色)。使用标准护理、cerezyme和纯化的gba (m0111) (其利用双顺反子载体在expi293细胞中瞬时共表达,所述双顺反子载体编码s1s3 ptase以及在中性和弱碱性条件下具有报道的更大稳定性的gba的天然变体),执行d409v戈谢小鼠模型中的功效研究。~20周龄的戈谢小鼠每周用~1.5 mg/kg)酶治疗一次,共4周。4周后,收获肝和肺组织并在4%多聚甲醛-pbs,ph 7.4中固定,用于使用cd68抗体的免疫组织化学。与目前护理标准相比,m0111具有更大的功效,如通过如经由cd68 ab显现的受影响组织中的巨噬细胞减少所证明的。
[0276]
图19a-19c是一系列照片,其证实在gba
d409v/null
小鼠模型中,gcase
m6p ert比伊米
苷酶更好地减少戈谢贮存细胞的数目和大小(苏木精和伊红(h&e)染色)。使用标准护理、cerezyme和纯化的gba (其利用双顺反子载体在expi293细胞中瞬时共表达,所述双顺反子载体编码s1-s3 ptase以及在中性和弱碱性条件下具有报道的更大稳定性的gba的天然变体),执行d409a戈谢小鼠模型中的功效研究。~20周龄的戈谢小鼠每周用~1.5 mg/kg酶治疗一次,共4周。4周后,收获肝和肺组织并在4%多聚甲醛-pbs,ph 7.4中用于福尔马林固定,用于苏木精和伊红(h&e)染色。与目前护理标准相比,gcase
m6p
具有更大的功效,如通过如经由h&e染色显现的受影响组织中的贮存细胞减少所证明的。
[0277]
图20a-20b是证实在gba
d409v/null
小鼠模型中,gcase
m6p ert比伊米苷酶更好地减少累积底物的一对图。~20周龄的戈谢小鼠每周用~1.5 mg/kg酶治疗一次,共4周。收集组织样品并匀浆化用于糖基神经酰胺分析。在组织匀浆中确定gcase的天然底物葡糖脑苷脂的累积。具有重要价值的是在肺中的gc累积,其是目前护理标准的已知的未满足需求。通过加入200
ꢀµ
l甲醇/acn/h2o (v:v:v=85:10:5),以800 rpm混合5分钟,随后以3220 g 4℃离心15分钟,提取20
ꢀµ
l等份试样的组织匀浆,并且适当的对照是葡萄糖神经酰胺。回收50
ꢀµ
l上清液,用氮干燥并且用甲醇/acn/h2o (v:v:v=85:10:5)重悬浮,并且直接进样用于lc-ms/ms分析。对于测量的两种神经酰胺,与伊米苷酶相比,gcase
m6p
治疗的动物在ert疗法之后具有较低的水平。
[0278]
基因疗法具有包含编码gba的序列和编码s1-s3 ptase的序列的双顺反子载体的递送载体可以用于治疗或预防戈谢病的体征或症状。在一些实施方案中,递送载体是病毒载体。在一些实施方案中,病毒载体是aav载体。在一些实施方案中,aav载体是aav1、aav2、aav3、aav4、aav5、aav6、aav7、aav8或aav9载体。在一些实施方案中,病毒载体是慢病毒载体。在一些实施方案中,载体是非病毒载体。在一些实施方案中,非病毒载体是脂质体、lnp、聚合物纳米颗粒、纳米颗粒、胶束、聚合物囊泡或外来体。下述研究证实了,在领域公认的标准的戈谢病小鼠模型中利用双顺反子载体表达gba和s1-s3 ptase导致gba
m6p
的表达、组织和血清中的活性增加以及底物减少。这证实了由于有效的细胞摄取和溶酶体靶向,即使在低活性水平下,具有对于ci-mpr具有高亲和力的磷酸化的转基因产物也可以导致有效的疗法。
[0279]
图21a-21d是显示体内aav介导的基因疗法研究用于治疗戈谢病的结果的一系列图。为了确定用具有三种不同启动子的稳定gba s1-s3 ptas转基因的双顺反子表达的aav9基因疗法的效应,15周龄的gba
d409v/null
小鼠用中等剂量的aav9-稳定的gba s1-s3 ptase,5e11vg进行给药。为了确定多少gba由组织生成,在aav9注射后2周,回收组织、匀浆化并使用4mu-glc底物测量活性。如通过用于蛋白质测定的bca方法确定的,活性针对匀浆中的总蛋白质进行标准化。
[0280]
图29a-29c是描绘在戈谢小鼠中注射aav9-htlv-gba
m6p
基因疗法后2周,肺和肝中的酶活性和所选gcase底物的一系列图。aav9-htlv-gba-s1s3也称为aav9-htlv-gba
m6p
,其中m6p表示s1s3构建体。在aav9 htlv-gba或aav9 htlv-gba
m6p (具有含有gba和s1-s3 ptase的双顺反子载体的转基因)之后两周,对于两种构建体,肝中的表达升高(图29a)。当测量肝葡糖基-β-神经酰胺水平时(图29b和c),尽管与aav9 htlv-gba治疗的动物相比,在肝中存在较低的gcase活性,但对于aav9 htlv-gba
m6p
治疗的动物,观察到累积底物的最大减少。这种更大的底物减少伴随更少的活性指示了n联寡糖磷酸化在细胞摄取和溶酶体靶
向方面对于基因疗法的重要性。在肺中,aav9治疗动物的gcase活性很低。然而,aav9-htlv-gba
m6p
治疗的动物显示肺中累积的葡糖基-β-神经酰胺水平的显著减少(图29b、c)。对于aav9-htlv-gba治疗的动物,观察到少量减少。这证实了由于有效的细胞摄取和溶酶体靶向,即使在低活性水平下,具有对于ci-mpr具有高亲和力的磷酸化的转基因产物也可以导致有效的疗法。
[0281]
实施例4:α-甘露糖苷贮积症的治疗酶替代疗法(ert)包含编码laman的序列和编码s1-s3 ptase的序列的表达载体可以用于治疗或预防α-甘露糖苷贮积症的体征或症状。下述研究证实了,laman-s1-s3在小鼠模型中的表达导致laman-s1-s3的表达、laman-s1-s3从循环血流转运到细胞内、以及吸收laman-s1-s3复合物的细胞中laman的活性增加。起因于laman-s1-s3复合物的表达和摄取的laman的少量增加导致小鼠模型中功能的显著功能恢复。
[0282]
利用具有s1-s3 ptase的双顺反子表达载体表达laman,生成具有更高水平的磷酸化寡糖的重组蛋白,其可以用于治疗或预防α-甘露糖苷贮积症的体征或症状。下述研究证实了,在野生型小鼠中使用重组laman蛋白(其使用具有s1-s3 ptase的双顺反子载体表达)的ert导致组织中更大的摄取和更广泛的分布。
[0283]
图22a-22c是描绘使用溶酶体α-甘露糖苷酶(laman)作为ert的体外研究结果的一系列图。
[0284]
图23a-23b是描绘laman酶表达、纯化和表征的照片和相应的数据表。两种laman制剂伴随(m0611)或不伴随编码s1-s3 ptase的双顺反子载体在expi293细胞中瞬时共表达。两者均通过利用hpc4亲和标签进行纯化。通过测量以剂量依赖性方式与固定的不依赖于阳离子的甘露糖6-磷酸受体结合的laman的量,证实了磷酸化的显著增加。所结合的laman的量基于其使用其合成底物4-甲基伞形酮-α-d-吡喃甘露糖苷(4mu-man)的活性。通过添加的甘露糖6-磷酸阻断结合的能力,确认了经由磷酸化的寡糖的结合特异性。值得注意的是,即使在m6p的存在下,laman m6p (m0611)也结合受体的能力。选择laman m6p (m0611,p-0030)和laman (p-0031)用于体内动物研究。
[0285]
图23c是描绘laman m6p (m0611)酶表达、纯化和表征的图。两种laman制剂伴随或不伴随编码ptase的s1-s3变体的双顺反子载体在expi293细胞中瞬时共表达。两者均通过利用hpc4标签进行纯化。通过测量以剂量依赖性方式与固定的不依赖于阳离子的甘露糖6-磷酸受体友好结合的laman的量,证实了磷酸化的显著增加。所结合的laman的量通过使用合成底物4-甲基伞形酮-α-d-吡喃甘露糖苷(4mu-man)的活性进行确定。通过添加的甘露糖6-磷酸阻断结合的能力,确认了经由磷酸化的寡糖的结合特异性。值得注意的是,即使在m6p的存在下,m0611也结合受体的能力。选择laman m6p (m0611,p-0030)和laman (p-0031)用于体内动物研究。
[0286]
图24a-24b是证实用于酶替代疗法的laman和laman
m6p
酶在野生型小鼠中的生物分布的一对图。为了评估laman和laman
m6p (与s1-s3 ptase共表达的laman)之间的组织摄取差异,经由尾静脉将2 mg/kg的每种制剂注射到野生型小鼠(n=4)内。在给药后2和8小时,回收组织、匀浆化并使用4mu-man底物测量活性。如通过用于蛋白质测定的bca方法确定的,活性针对匀浆中的总蛋白质进行标准化。在组织摄取数据中观察到laman
m6p (与s1s3 ptase
共表达的laman)的优点。对于肝、脾、心脏、肺和脑,在2小时的组织中存在更大的活性。除了肺之外,这一趋势在8小时也是如此。这可能是在分析这种组织时观察到的高变化的结果。这种观察的唯一例外是肾。从所有样品中扣除内源性laman活性。在用我们的laman
m6p
酶注射的小鼠的大多数组织中,检测到更高的laman酶活性。
[0287]
图25a-25b是证实用于酶替代疗法的αlaman和laman
m6p
酶在野生型小鼠中的生物分布的一对图。为了评估laman和laman
m6p (与s1-s3 ptase共表达的laman)之间的组织摄取差异,经由尾静脉将10 mg/kg的每种制剂注射到野生型小鼠(n=4)内。在给药后2和8小时,回收组织、匀浆化并使用4mu-man底物测量活性。如通过用于蛋白质测定的bca方法确定的,活性针对匀浆中的总蛋白质进行标准化。在组织摄取数据中观察到laman
m6p (与s1-s3 ptase共表达的laman)的优点。对于肝、脾、心脏、肺和脑,在2小时的组织中存在更大的活性。除了肾之外,这一趋势在8小时也是如此。这可能是在分析这种组织时观察到的高变化的结果。
[0288]
基因疗法包含编码laman的序列和编码s1-s3修饰的glcnac-1磷酸转移酶(glcnac-1 ptase)的序列的递送载体可以用于治疗或预防α-甘露糖苷贮积症的体征或症状。在一些实施方案中,递送载体是病毒载体。在一些实施方案中,病毒载体是aav载体。在一些实施方案中,aav载体是aav1、aav2、aav3、aav4、aav5、aav6、aav7、aav8或aav9载体。在一些实施方案中,病毒载体是慢病毒载体。在一些实施方案中,载体是非病毒载体。在一些实施方案中,非病毒载体是脂质体、lnp、聚合物纳米颗粒、纳米颗粒、胶束、聚合物囊泡或外来体。下述研究证实了,laman-s1-s3在α-甘露糖苷贮积症的小鼠模型中的表达导致laman-s1-s3的表达、laman-s1-s3从循环血流转运到细胞内、以及吸收laman-s1-s3复合物的细胞中laman的活性增加。起因于laman-s1-s3复合物的表达和摄取的v的少量增加导致小鼠模型中功能的显著功能恢复。
[0289]
可替代地或另外,包含编码s1-s3修饰的glcnac-1磷酸转移酶(glcnac-1 ptase)的序列的递送载体可以用于治疗或预防α-甘露糖苷贮积症的体征或症状。s1-s3的表达可增加内源性laman被身体组织的摄取,从而诱导小鼠模型中功能的显著功能恢复。
[0290]
实施例5:粘脂质贮积症的治疗酶替代疗法(ert)包含编码s1-s3修饰的glcnac-1磷酸转移酶(glcnac-1 ptase)的序列的表达载体可以用于治疗或预防粘脂质贮积症的体征或症状。下述研究证实了,s1-s3的表达导致s1-s3的表达、s1-s3以及一种或多种溶酶体酶从循环血流转运到细胞内、以及吸收s1-s3复合物的细胞中一种或多种溶酶体酶的活性增加。起因于s1-s3复合物和一种或多种溶酶体酶的表达和摄取的s1-s3复合物的少量增加导致功能的显著功能恢复。
[0291]
基因疗法包含编码s1-s3修饰的glcnac-1磷酸转移酶(glcnac-1 ptase)的序列的递送载体可以用于治疗或预防粘脂质贮积症的体征或症状。在一些实施方案中,递送载体是病毒载体。在一些实施方案中,病毒载体是aav载体。在一些实施方案中,aav载体是aav1、aav2、aav3、aav4、aav5、aav6、aav7、aav8或aav9载体。在一些实施方案中,病毒载体是慢病毒载体。在一些实施方案中,载体是非病毒载体。在一些实施方案中,非病毒载体是脂质体、lnp、
聚合物纳米颗粒、纳米颗粒、胶束、聚合物囊泡或外来体。包含编码可溶性s1-s3修饰的glcnac-1磷酸转移酶(glcnac-1 ptase)的序列的递送载体可以用于治疗或预防粘脂质贮积症的体征或症状。包含编码s1-s3修饰的glcnac-1磷酸转移酶(glcnac-1 ptase)的序列的递送载体可以用于治疗或预防粘脂质贮积症的体征或症状。下述研究证实了,s1-s3 ptase的表达导致s1-s3 ptase的表达,s1-s3细胞活性通过增加其n联寡糖磷酸化导致错误运输的溶酶体酶的血清水平的校正,允许有效的靶向溶酶体。
[0292]
可替代地或另外,包含编码s1-s3修饰的glcnac-1磷酸转移酶(glcnac-1 ptase)的序列的递送载体可以用于治疗或预防粘脂质贮积症的体征或症状。s1-s3 ptase的表达可能增加一种或多种内源性溶酶体酶通过身体组织的摄取,从而诱导小鼠模型中功能的显著功能恢复。
[0293]
图26a-26b是描绘用于粘脂质贮积症基因疗法(gtx)的aav9设计和体外测试的示意图解和图。293t细胞用各种m0021 (aav9-cagp-s1-s3)病毒进行转导,并且在ptase活性测定法前培养2天。
[0294]
图27a-27b是证实m0021治疗降低ml ii小鼠中的血清溶酶体酶水平的一对图。为了确定s1-s3 ptase基因疗法的效应,34周龄的雌性小鼠用中等剂量的m0021 (aav9-cagp-s1-s3) ,4e12 vg (2e13 vg/kg)进行给药。ml ii的表型之一是由于其无法靶向细胞内的溶酶体,溶酶体酶的血清水平升高。当在接受疗法仅1周后的血清中,存在laman和manb活性的降低时,观察到令人鼓舞的结果。这个结果很重要,因为它证实了影响所描述的mlii小鼠模型表型的能力。
[0295]
图28a-28c是证实m0021治疗增加ml ii中的溶酶体酶的磷酸化的一系列图。为了进一步理解关于s1-s3 ptase基因疗法在降低laman和manb的血清活性方面的影响,使用较早描述的固定的受体结合测定法,评估了血清中发现的酶的ci-mpr结合。简言之,已知的活性以渐增的量加入固定的ci-mpr中。将未结合的酶洗掉,并且使用适当的合成底物man-b-4mu (manb,laman 4mu-man (laman)测量剩余的结合酶。ml ii小鼠的aav9-s1s3基因疗法增加了溶酶体酶的聚糖磷酸化。在3周后,血清中的总磷酸化的溶酶体酶标准化至正常水平或略微更高。
[0296]
本文引用的每个专利、专利申请和出版物的公开内容均在此通过引用以其整体并入本文。虽然本公开内容已参考具体实施方案进行公开,但显而易见的是,本公开内容的其它实施方案和变化可以通过本领域的其它技术人员进行设计,而不脱离本公开内容的真实精神和范围。所附权利要求预期解释为包括所有此类实施方案和等价变化。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。