cnp变体和其共轭物
1.相关申请的交叉引用
2.本技术要求2019年9月16日提交的美国临时专利申请第62/901,093号、2019年11月13日提交的美国临时专利申请第62/935,050号、2020年1月20日提交的美国临时专利申请第62/963,350号、2020年1月23日提交的美国临时专利申请第62/964,852号和2020年6月12日提交的美国临时专利申请第63/038,667号的优先权,所述申请以全文引用的方式并入本文中。
3.以引用的方式并入以电子方式提交的材料
4.作为本公开的一部分的序列表与说明书同时提交为文本文件。含有序列表的文本文件的名称为“54736_seqlisting.txt”,其创建于2020年8月6日且大小为54,429字节。序列表的主题以全文引用的方式并入本文中。
技术领域
5.一般而言,本公开涉及c型利尿钠肽(c-type natriuretic peptide;cnp)的变体、包括cnp变体的药物组合物和使用方法。cnp变体可用作治疗剂,用于治疗对cnp起反应的疾病,包含(但不限于)骨相关病症,如骨胳发育不良(例如,软骨发育不全)。
背景技术:
6.c型利尿钠肽(cnp)(《生物化学与生物物理研究交流(biochem.biophys.res.commun.)》,168:863-870(1990)(genbank寄存编号np_077720,对于cnp前体蛋白nppc)(《高血压杂志(j.hypertens.)》,10:907-912(1992))为具有17个氨基酸的环结构的肽家族(anp、bnp、cnp)中的小单链肽(levin等人,《新英格兰医学杂志(n.engl.j.med.)》,339:863-870(1998))且在多种生物过程中具有重要角色。cnp与利尿钠肽受体-b(npr-b、gc-b)相互作用以刺激产生环鸟苷单磷酸(cyclic-guanosine monophosphate;cgmp)(《高血压杂志》10:1111-1114(1992))。cnp为广泛表达的,包含表达于中枢神经系统、生殖道、骨和血管内皮中(《高血压(hypertension)》,49:419-426(2007))。
7.在人类中,cnp最初以单链126个氨基酸的前-原多肽形式产生自利尿钠肽前体c(natriuretic peptide precursor c;nppc)基因(《生物化学与生物物理研究交流》,168:863-870(1990))。移除信号肽产生原-cnp,且通过内切蛋白酶弗林蛋白酶(endoprotease furin)进一步裂解产生活性53个氨基酸的肽(cnp-53),其被分泌且通过未知酶再次裂解以产生成熟的22个氨基酸的肽(cnp-22)(wu,《生物化学杂志(j.biol.chem.)》278:25847-852(2003))。cnp-53和cnp-22的不同之处在于其分布,其中cnp-53在组织中占主导地位,而cnp-22主要发现于血浆和脑脊髓液中(j.alfonzo,《受体信号转导研究(recept.signal.transduct.res.)》,26:269-297(2006))。cnp-53和cnp-22均与npr-b类似地结合。
8.cgmp产生介导的下游信号传导影响许多不同生物过程,包含软骨内骨化。举例来
说,小鼠模型中的cnp或npr-b的基因敲除导致矮化表型的动物具有较短的长骨和脊椎。已经鉴别出阻断正常cnp信号传导的人类npr-b突变且其导致侏儒症(olney等人,《临床内分泌与代谢杂志(j.clin.endocrinol.metab.)》91(4):1229-1232(2006);bartels等人,《美国人类遗传学杂志(am.j.hum.genet.)》75:27-34(2004))。相比之下,经工程改造以产生升高含量的cnp的小鼠展现延长的长骨和脊椎。
9.cnp(cnp22)的治疗用途受其短血浆半衰期限制,所述短血浆半衰期已在人类体内显示为2.6分钟(《临床内分泌与代谢杂志》,78:1428-35(1994))。具有更长体内血清半衰期且展示与野生型cnp类似或改良的活性的cnp变体对于可持续治疗策略是重要的。
技术实现要素:
10.本公开涉及在水性介质中具有增加的循环半衰期和稳定性的c型利尿钠肽(cnp)的新颖变体、包括此类cnp变体的药物组合物,以及使用此类cnp变体治疗对cnp起反应的病症的方法,所述病症包含(但不限于)骨相关病症,例如软骨发育不全。
11.在各种实施例中,本公开提供选自由以下组成的群组的c型利尿钠肽(cnp)的变体:pgqehpqarryrgaqrrglsrgcfglkldrigsmsglgc(seq id no:5);pgqehpnarkykgankkglskgcfglkldrigsmsglgc(seq id no:1);pgqehpnarryrganrrglsrgcfglkldrigsmsglgc(seq id no:6);以及pgqehpqarryrgaqrrglsrgcfglkldrigsmsglgc(seq id no:5)。
12.在各种实施例中,本公开提供选自由以下组成的群组的c型利尿钠肽(cnp)的变体:pgqehpqarryrgaqrrglsrgcfglkldrigsmsglgc(seq id no:5);pgqehpnarkykgankkglskgcfglkldrigsmsglgc(seq id no:1);pgqehpnarryrganrrglsrgcfglkldrigsmsglgc(seq id no:6);pgqehpqarryrgaqrrglsrgcfglkldrigsmsglgc(seq id no:5);以及pgqehpqarkykgaqkkglskgcfglkldrigsmsglgc(seq id no:7)。
13.在各种实施例中,变异肽进一步包括乙酰基。在各种实施例中,乙酰基位于肽的n端上。在各种实施例中,肽于c端进一步包括oh或nh2基团。
14.在各种实施例中,变异肽包括共轭部分。在各种实施例中,共轭部分在cnp环状域的残基上或在除所述cnp环状域之外的位点处。在各种实施例中,共轭部分位于赖氨酸残基上。在各种实施例中,共轭部分包括一个或多个酸部分。在各种实施例中,酸部分为疏水性酸。
15.在各种实施例中,共轭部分包括一个或多个与亲水性间隔基连接的酸部分。在各种实施例中,亲水性间隔基为任何氨基酸。在各种实施例中,亲水性间隔基为γ谷氨酸(γglu)。在各种实施例中,亲水性间隔基为oeg(8-氨基-3,6-二氧杂辛酸)。在各种实施例中,亲水性间隔基为γ谷氨酸(γglu)或oeg(8-氨基-3,6-二氧杂辛酸)。在各种实施例中,亲水性间隔基为与一或两个或更多个oeg(8-氨基-3,6-二氧杂辛酸)连接的γ谷氨酸(γglu)。在各种实施例中,酸部分为脂肪酸。示例性脂肪酸包含短链、中链或长链脂肪酸或二羧基脂肪酸。在各种实施例中,脂肪酸为饱和或不饱和的。考虑c-6至c-20脂肪酸,包含(但不限于)c-6、c-8、c-10、c-12、c-14、c-16、c-18或c-20饱和或不饱和脂肪酸。在各种实施例中,脂肪酸为癸酸、十二酸、肉豆蔻酸、棕榈酸、硬脂酸、二十酸或其二酸。
16.在各种实施例中,酸部分和亲水性间隔基具有结构aeea-aeea-γglu-c18da。在各种实施例中,酸部分和亲水性间隔基具有结构:
17.其中表示与cnp变体的连接点。在各种实施例中,表示与可水解连接子的连接点,其中可水解连接子连接至cnp变体。在各种实施例中,可水解连接子能够释放完整cnp变体。
18.在各种实施例中,具有接共轭部分的cnp变体为缓释组合物的组分。在各种实施例中,缓释组合物为延释组合物。在各种实施例中,包括共轭部分和可水解连接子的cnp变体能够释放cnp变体,其中在ph 7至7.6下,(i)第1天释放小于约20%的cnp变体;且(ii)每周释放约90%的cnp变体,或每两周释放约90%的cnp变体,或每月释放约90%的cnp变体。
19.在各种实施例中,(i)在ph 7.0至7.6下,第1天释放小于约25%、约30%、约35%、约40%、约45%、约50%、约55%、约60%、约65%、约70%或约75%的肽;和(ii)在ph 7至7.6下,每周释放约90%的肽、或每两周释放约90%的肽、或每月释放约90%的肽。经进一步考虑(i)在ph 7.0至7.6下,第1天释放小于约25%、约30%、约35%、约40%、约45%、约50%、约55%、约60%、约65%、约70%或约75%的肽;和(ii)在ph 7至7.6下,每周释放约70%、约80%或约90%的肽;或每两周释放约70%、约80%或约90%的肽;或每三周释放约70%、约80%或约90%的肽;或每月释放约70%、约80%或约90%的肽;或可替代地ii)在ph 7至7.6下,每周释放约70%、约75%、约80%、约85%或约90%的肽;或每两周释放约70%、约75%、约80%、约85%或约90%的肽;或每三周释放约70%、约75%、约80%、约85%或约90%的肽;或每月释放约70%、约75%、约80%、约85%或约90%的肽。
20.在各种实施例中,变体具有以下结构:pgqehpqarryrgaqrrglsrgcfglk(aeea-aeea-γglu-c18da)ldrigsmsglgc(seq id no:5)或ac-pgqehpqarryrgaqrrglsrgcfglk(aeea-aeea-γglu-c18da)ldrigsmsglgc-oh(seq id no:8)。
21.在各种实施例中,变体选自由以下组成的群组:
22.ac-pgqehpqarryrgaqrrglsrgcfglkldrigsmsglgc-oh(seq id no:8);
23.ac-pgqehpnarkykgankkglskgcfglkldrigsmsglgc-nh2(seq id no:9);
24.ac-pgqehpnarryrganrrglsrgcfglkldrigsmsglgc-oh(seq id no:10);
25.ac-pgqehpnarryrganrrglsrgcfglkldrigsmsglgc-nh2(seq id no:11);
26.ac-pgqehpqarryrgaqrrglsrgcfglkldrigsmsglgc-nh2(seq id no:12);
27.ac-pgqehpqarkykgaqkkglskgcfglkldrigsmsglgc-nh2(seq id no:13);以及
28.ac-pgqehpqarkykgaqkkglskgcfglkldrigsmsglgc-oh(seq id no:14)。
29.在各种实施例中,变体包括一个或多个连接子基团。在各种实施例中,连接子位于cnp环状域的残基上或位于除所述cnp环状域之外的位点处。在各种实施例中,连接子位于赖氨酸残基上。
30.在各种实施例中,连接子为可水解连接子。
31.在各种实施例中,cnp变体经由连接子连接至共轭部分。在各种实施例中,连接子经由共轭部分的亲水性间隔基连接至共轭部分。在各种实施例中,连接子为氨基乙氧基-2-乙氧基乙酸(aeea)。在各种实施例中,连接子为bicin型连接子或类肽连接子,它是指具有
与bicin(双-2-羟乙基甘氨酰胺)类似的裂解机制,但替代地经由不对称n-烷基肽(即类肽)裂解的连接子。在各种实施例中,连接子为基于非酶β消除的电子连接子。在各种实施例中,电子连接子包括so2部分。如cnp共轭物中所说明的连接子的实例阐述于图1中。还参见santi等人,《美国科学院院刊(proc natl acad sci usa)》109:6211-6216,2012)。
32.在各种实施例中,共轭部分为合成聚合基团。在各种实施例中,变体包括经由可水解连接子与变体偶合的合成聚合基团。在各种实施例中,合成聚合基团包括亲水性聚合物部分。在各种实施例中,亲水性聚合物部分包括聚乙二醇(peg)。在各种实施例中,亲水性聚合物部分包括具有6至20个原子链长的聚乙二醇(peg)。
33.在各种实施例中,变异肽是以合成方式制备的。
34.在各种实施例中,变异肽在约37℃、ph 7.0至7.6下稳定10天。在各种实施例中,变异肽在约37℃、ph 7.0至7.4下稳定至少10天。在各种实施例中,变异肽在约37℃、ph 7.2至7.6下稳定至少10天。
35.在各种实施例中,变异肽对脱酰胺作用为稳定的。在各种实施例中,变异肽对氧化为稳定的。在各种实施例中,变异肽对脱酰胺作用和/或氧化或其组合为稳定的。在各种实施例中,甲硫氨酸被正亮氨酸置换。在各种实施例中,10天后几乎无或无可检测的脱酰胺作用。
36.在各种实施例中,变异肽在约37℃、ph 7.0至7.6下具有约10天的半衰期。在各种实施例中,变异肽在约37℃、ph 7.0至7.4下具有约10天的半衰期。在各种实施例中,变异肽在约37℃、ph 7.2至7.6下具有约10天的半衰期。在各种实施例中,变异肽在约37℃、ph 7.0至7.6下具有至少10天的半衰期。在各种实施例中,变异肽在约37℃、ph 7.0至7.4下具有至少10天的半衰期。在各种实施例中,变异肽在约37℃、ph 7.2至7.6下具有至少10天的半衰期。在各种实施例中,半衰期为至少约15天、16天、17天、18天、19天、20天、21天、22天、23天、24天、25天、30天或更长时间。
37.在各种实施例中,在cgmp分析中,变异肽具有0.1至10nm的ec50。在各种实施例中,在cgmp分析中,变异肽具有0.1至25nm的ec50。
38.在各种实施例中,在生理条件,例如约37℃、ph 7.0至7.6下,在水性介质中10天之后,检测到大于45%的变异肽。在各种实施例中,在生理条件,例如约37℃、ph 7.0至7.6下,在水性介质中10天之后,检测到大于50%、55%、60%、65%、70%、75%、80%、85%、90%或95%的变异肽。
39.在各种实施例中,在37℃、ph 7.4下,在水性介质中10天之后,检测到大于45%的变异肽。在各种实施例中,在37℃、ph 7.4下,在水性介质中10天之后,检测到大于50%、55%、60%、65%、70%、75%、80%、85%、90%或95%的变异肽。
40.在各种实施例中,在生理条件,例如约37℃、ph 7.0至7.6下,在血浆中10天之后,检测到大于45%的变异肽。在各种实施例中,在生理条件,例如约37℃、ph 7.0至7.6下,在血浆中10天之后,检测到大于50%、55%、60%、65%、70%、75%、80%、85%、90%或95%的变异肽。
41.在各种实施例中,在37℃、ph 7.4下,在血浆中10天之后,检测到大于45%的变异肽。在各种实施例中,在37℃、ph 7.4下,在血浆中10天之后,检测到大于50%、55%、60%、65%、70%、75%、80%、85%、90%或95%的变异肽。
42.在各种实施例中,变异肽与脂质、脂肪酸、亲水性间隔基或连接子或任选地与其组合共轭。在各种实施例中,连接子为亲水性聚合物部分。在各种实施例中,亲水性聚合物部分为合成亲水性聚合物部分。
43.在各种实施例中,与pro-gly-cnp37相比,变异肽具有更长的半衰期。在各种实施例中,与cnp-22相比,变异肽具有更长的半衰期。在各种实施例中,与pro-gly-cnp37和/或cnp-22相比,变异肽具有更长的半衰期。在各种实施例中,与体外和/或体内的pro-gly-cnp37和/或cnp-22相比,变异肽具有更长的半衰期。
44.本公开进一步提供一种药物组合物,其包括本文所描述的cnp变体和药学上可接受的赋形剂、载剂或稀释剂。
45.在各种实施例中,组合物为由包括ph为约4至约6的柠檬酸/柠檬酸盐缓冲液或乙酸/乙酸盐缓冲液的配制物制备的冻干配制物。在各种实施例中,冻干配制物是由进一步包括等张调节剂或选自由以下组成的群组的增积剂的配制物制备:甘露糖醇、蔗糖、山梨糖醇、海藻糖、聚山梨醇酯80和其组合。在各种实施例中,所述冻干配制物是由进一步包括选自由以下组成的群组的抗氧化剂的配制物制备:甲硫氨酸、抗坏血酸、抗坏血酸的盐形式、硫甘油和其组合。在各种实施例中,cnp变体组合物以冻干粉末形式供应,用于从0.8mg复原至10mg。在各种实施例中,cnp变体组合物以0.8mg或2mg冻干无防腐剂的复原用粉末形式供应。
46.在各种实施例中,组合物为延释组合物。
47.在各种实施例中,cnp变体为
48.pgqehpnarkykgankkglskgcfglkldrigsmsglgc(pro-gly-cnp-37)(bmn111)(seq id no:1)。
49.还提供一种治疗有需要的个体的骨相关病症或骨胳发育不良的方法,其包括向个体施用包括如本文所描述的cnp变体的组合物。
50.在各种实施例中,骨相关病症或骨胳发育不良选自由以下组成的群组:骨关节炎(osteoarthritis)、低磷酸盐血性佝偻病(hypophosphatemic ricket)、软骨发育不全(achondroplasia)、软骨生成减退(hypochondroplasia)、身材矮小、侏儒症、骨软骨发育不良(osteochondrodysplasias)、致死性发育不良、成骨不全(osteogenesis imperfecta)、软骨成长不全(achondrogenesis)、点状软骨发育异常(chondrodysplasia punctata)、纯合性软骨发育不全(homozygous achondroplasia)、点状软骨发育异常、屈肢骨发育不良(camptomelic dysplasia)、先天性致死型低磷酸酶症(congenital lethal hypophosphatasia)、围产期致死型成骨不全(perinatal lethal type of osteogenesis imperfecta)、短肋多指综合征(short-rib polydactyly syndromes)、软骨生成减退、肢根型点状软骨发育异常(rhizomelic type of chondrodysplasia punctata)、扬森型干骺端发育不良(jansen-type metaphyseal dysplasia)、先天性脊椎骨骺发育不良(spondyloepiphyseal dysplasia congenita)、骨发育不全、畸型发育不良、先天性短股骨、兰格型肢中骨发育不良(langer-type mesomelic dysplasia)、尼维格型肢中骨发育不良(nievergelt-type mesomelic dysplasia)、罗氏综合征(robinow syndrome)、莱因哈特综合征(reinhardt syndrome)、肢端发育不全(acrodysostosis)、周围骨发育障碍、克尼斯特发育不良(kniest dysplasia)、纤维软骨增生症、罗伯茨综合征(roberts syndrome)、肢
端肢中发育不良、小肢、莫奎氏综合征(morquio syndrome)、克尼斯特综合征(kniest syndrome)、后生营养性发育不良和脊椎骨骺干骺端发育不良(spondyloepimetaphyseal dysplasia)。
51.在各种实施例中,cnp变体适用作用于治疗特发性身材矮小和其它骨骼发育不良的生长激素的辅助或替代。
52.在各种实施例中,骨相关病症、骨胳发育不良或身材矮小病症由npr2突变、shox突变(特纳氏综合征/莱里维尔(turner's syndrome/leri weill))或ptpn11突变(努南氏综合征(noonan's syndrome))引起。
53.在各种实施例中,骨相关病症、骨胳发育不良或身材矮小病症由npr2突变、shox突变(特纳氏综合征/莱里维尔)或ptpn11突变(努南氏综合征)或胰岛素生长因子1受体(insulin growth factor 1receptor;igf1r)引起。
54.在各种实施例中,cnp变体适用于治疗生长板病症和身材矮小,包含家族性身材矮小、显性家族性身材矮小(其也称为显性遗传性身材矮小)或特发性身材矮小。在各种实施例中,身材矮小或生长板病症为胶原蛋白(col2a1、col11a1、col9a2、col10)、聚集蛋白聚糖(acan)、印度刺猬因子(indian hedgehog;ihh)、ptpn11、npr2、nppc或fgfr3的突变的结果。
55.在各种实施例中,生长板病症或身材矮小与相关于拉索病(rasopathy)的基因中的一个或多个突变相关。
56.在各种实施例中,骨相关病症、骨胳发育不良或身材矮小病症由拉索病引起。在各种实施例中,拉索病为努南氏综合征、科斯特洛综合征(costello syndrome)、心脸皮肤综合征、1型神经纤维瘤或leopard综合征。
57.在一个实施例中,拉索病为遗传性1型齿龈纤维瘤病。
58.在各种实施例中,cnp变体适用于治疗生长板病症和身材矮小,包含家族性身材矮小、显性家族性身材矮小(其也称为显性遗传性身材矮小)或特发性身材矮小。在各种实施例中,身材矮小或生长板病症为胶原蛋白(col2a1、col11a1、col9a2、col10)、聚集蛋白聚糖(acan)、印度刺猬因子(ihh)、ptpn11、npr2、nppc、fgfr3或胰岛素生长因子1受体(igf1r)的突变的结果。
59.在各种实施例中,生长板病症或身材矮小与相关于拉索病的基因中的一个或多个突变相关。
60.在各种实施例中,cnp变体适用于治疗具有如下的身材矮小的个体:身高sds为小于-1.0、-1.5、-2.0、-2.5或-3.0,且至少一个亲代的身高sds为小于-1.0、-1.5、-2.0或-2.5,任选地其中第二亲代的身高在正常范围内。在各种实施例中,cnp变体适用于治疗具有身高sds为-2.0至-3.0的身材矮小的个体。在各种实施例中,cnp变体适用于治疗具有身高sds为-2.0至-2.5的身材矮小的个体。在各种实施例中,身材矮小与相关于身材矮小的基因中的一个或多个突变相关,如胶原蛋白(col2a1、col11a1、col9a2、col10)、聚集蛋白聚糖(acan)、印度刺猬因子(ihh)、ptpn11、npr2、nppc、fgfr3或胰岛素生长因子1受体(igf1r)或其组合。在各种实施例中,生长板病症或身材矮小与相关于拉索病的基因中的一个或多个突变相关。
61.在各种实施例中,身材矮小为如通过多基因风险评分(prs)所确定的多个基因的突变的结果。在各种实施例中,个体具有npr2的突变和低prs。在各种实施例中,个体具有
fgfr3的突变和低prs。在各种实施例中,个体具有npr2的突变和低prs。在各种实施例中,个体具有igf1r的突变和低prs。在各种实施例中,个体具有nppc的突变和低prs。在各种实施例中,个体具有shox的突变和低prs。在各种实施例中,个体具有fgfr3、igf1r、nppc、npr2和shox中的一或多者的一个或多个突变和低prs。在各种实施例中,prs为1或2。在各种实施例中,prs为1。在各种实施例中,prs为2。如实例4所描述来计算身高的多基因风险评分(prs)。prs 1是指最矮身高,prs 5是指最高身高。
62.在各种实施例中,cnp变体为
63.pgqehpnarkykgankkglskgcfglkldrigsmsglgc(pro-gly-cnp-37)(seq id no:1)。在各种实施例中,肽进一步包括乙酰基。在各种实施例中,乙酰基位于肽的n端上。在各种实施例中,肽于c端进一步包括oh或nh2基团。在各种实施例中,变体包括一个或多个如本文所描述的连接子基团。在各种实施例中,连接子为可水解连接子。
64.在各种实施例中,本公开提供一种在有需要的个体中进行骨延长或增加长骨生长的方法,其包括向个体施用包括本文所描述的cnp变体的组合物,且其中所述施用使骨延长或增加长骨生长。
65.在各种实施例中,组合物经皮下、皮内、关节内、经口或肌肉内施用。
66.在各种实施例中,每日一次、每周一次、每两周一次、每三周一次、每4周一次、每6周一次、每两个月一次、每三个月一次或每六个月一次地施用组合物。
67.在各种实施例中,组合物为延释组合物。
68.经进一步考虑一种治疗cnp反应性病状或病症的方法,其包括向个体施用如本文所描述的cnp变体或组合物,和监测个体的至少一种骨相关或软骨相关的生物标记的含量,其中至少一种骨相关或软骨相关的生物标记的含量增加指示cnp肽或变体对个体或病状或病症的治疗作用。
69.经进一步考虑一种克服由组成性活性突变型成纤维细胞生长因子受体3(fibroblast growth factor receptor 3;fgfr-3)诱导的细胞生长遏制的方法,其包括使表达组成性活性fgfr-3的细胞与如本文所描述的cnp变体或组合物接触。
70.经进一步考虑一种在表达利尿钠肽受体b(npr-b)的细胞中刺激cgmp产生的方法,其包括使表达npr-b的细胞与如本文所描述的cnp变体或组合物接触。
71.在各种实施例中,方法进一步包括调节如本文所描述的cnp肽或变体的施用量或频率,其中i)如果至少一种骨相关或软骨相关的生物标记的含量低于目标含量,则cnp肽或变体的施用量或频率增加;或ii)如果至少一种骨相关或软骨相关的生物标记的含量高于目标含量,则减少cnp肽或变体的施用量或频率。
72.在各种实施例中,至少一种骨相关或软骨相关的生物标记选自由以下组成的群组:cnp、cgmp、ii型胶原蛋白和其片段的前肽、ii型胶原蛋白和其片段、i型胶原蛋白c端肽(ctx)、骨钙化素、增殖细胞核抗原(proliferating cell nuclear antigen;pcna)、i型原胶原的前肽(pinp)和其片段的前肽、i型胶原蛋白和其片段、聚集蛋白聚糖硫酸软骨素(chondroitin sulfate)、胶原蛋白x和碱性磷酸酶。
73.在各种实施例中,cnp变体为
74.pgqehpnarkykgankkglskgcfglkldrigsmsglgc(pro-gly-cnp-37)(seq id no:1)。在各种实施例中,肽进一步包括乙酰基。在各种实施例中,乙酰基位于肽的n端上。在各种实
施例中,乙酰基位于肽序列内的氨基酸侧链上。在各种实施例中,肽在c端进一步包括oh或nh2基团。在各种实施例中,变体包括一个或多个如本文所描述的连接子基团。在各种实施例中,连接子为可水解连接子。
75.还提供一种制备本文所描述的cnp变体的方法,其包括使用fmoc氨基酸于固相树脂上合成肽。
76.在各种实施例中,方法包括通过使树脂与nmp/ac2o/diea(10:1:0.1,v/v/v)反应而使肽乙酰化。
77.在各种实施例中,所述方法包括使肽与任选地存在于赖氨酸残基上的共轭部分共轭。在各种实施例中,所述方法包括使赖氨酸上的保护性氨基裂解、使肽与2
×
fmoc-氨基peg(2)反应,接着与氨基酸反应,接着使脂质或脂肪酸部分共轭。
附图说明
78.图1说明本文所描述的cnp共轭物中的类肽或电子连接子的用途。
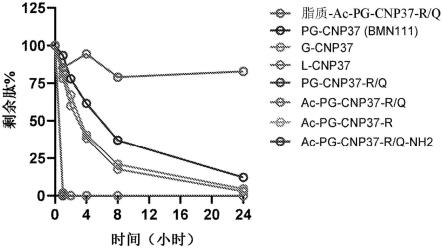
79.图2展示cnp变体于人类血浆中历经24小时的时间段的稳定性。
80.图3展示cnp变体在不同培养条件下的稳定性。
81.图43展示cnp变体(pro-gly-cnp)对携带npr2同型接合或异型接合突变的细胞的作用,如通过cgmp刺激所测量。
82.图5展示转染至rcs细胞中的npr2突变克隆中第一外显子的核苷酸和预测的蛋白质序列。
83.图6展示关于对cnp的反应分析的示例性npr2突变。
84.图7展示fgfr3、igf1r、nppc、npr2和shox中与身材矮小相关的示例性突变。
85.图8说明prs和稀有编码变体对身高的组合影响。图8a.对身高的影响作为定量性状,将样品基于其prs分为五组,水平线表示高度的25%、50%和75%百分位的小提琴图。样品通过误义、功能丧失或无携带状态而分组至五个核心基因中的任一个中。图8b.由对于“特发性身材矮小”或iss的胜算比反映的影响。使用prs=3作为参考相对于其它prs组的iss的胜算。图8c.使用prs=1作为参考相对于核心基因中具有误义和/或功能丧失变体的iss的胜算。图8d.使用prs=1非携带者作为参考相对于核心基因中具有误义和/或功能丧失变体的iss的胜算。图8e.使用prs=2非携带者作为参考相对于核心基因中具有误义和/或功能丧失变体的iss的胜算。图8f.使用prs=3非携带者作为参考相对于核心基因中具有误义和/或功能丧失变体的iss的胜算。g.使用prs=4非携带者作为参考相对于核心基因中具有误义和/或功能丧失变体的iss的胜算。
具体实施方式
86.本公开涉及适用于治疗骨胳发育不良和骨生长病症的稳定cnp变体。
87.如本说明书和随附权利要求书中所使用,除非上下文另外明确规定,否则不定冠词“一(a/an)”以及定冠词“所述(the)”包含复数以及单数指示物。
88.术语“约(about)”或“大致(approximately)”意指如由本领域普通技术人员所测定的特定值的可接受误差,其部分取决于如何测量或测定所述值。在某些实施例中,术语“约”或“大致”意指在1、2、3或4个标准差内。在某些实施例中,术语“约”或“大致”意指在给
定值或范围的30%、25%、20%、15%、10%、9%、8%、7%、6%、5%、4%、3%、2%、1%、0.5%或0.05%内。当术语“约”或“大致”冠于一系列两个或更多个数值中的第一数值之前时,应理解术语“约”或“大致”适用于所述系列中的数值中的每一个。
89.术语“c型利尿钠肽”或“cnp”是指在c末端具有17个氨基酸的环结构的较小单链肽(genbank寄存编号np_077720,对于cnp前体蛋白nppc)和其变体。17-聚体cnp环结构也称为cnp 17、cnp环或cnp环状域。cnp包含活性53个氨基酸的肽(cnp-53)和成熟22个氨基酸的肽(cnp-22),以及两个肽之间的不同长度的肽。
90.在各种实施例中,“cnp变体”与野生型nppc在相同数目的氨基酸残基上为至少约40%、50%、60%、70%、75%、80%、85%、90%或95%同源。经进一步考虑cnp变异肽可包括约1至约53、或1至39、或1至38、或1至37、或1至35、或1至34、或1至31、或1至27、或1至22、或10至35、或约15至约37个nppc多肽残基。在一个实施例中,cnp变体可包括具有1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35,36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52或53个源自nppc多肽的氨基酸的序列。
91.术语“共轭部分”是指与变异肽共轭的部分。共轭部分包含脂质、脂肪酸、亲水性间隔基、合成聚合物、连接子或任选地包含其组合。
92.术语“有效量”是指足以对个体的健康状况、病变或疾病产生所要结果或足以用于诊断目的的剂量。所要结果可包括剂量的接受者的主观或客观改善。“治疗有效量”是指可有效产生所预期的对健康有益的效果的药剂量。在任何个别情况下的适当“有效”量可由本领域普通技术人员使用常规实验来测定。应理解,针对任何具体患者的特定剂量水准和剂量频率可变化且将取决于多种因素,包含所采用的特定化合物的活性;生物可用性、代谢稳定性、分泌速率以及所述化合物的作用时间长度;化合物的施用模式和施用时间;患者的年龄、体重、总体健康状况、性别以及饮食;以及特定病状的严重程度。
[0093]“基本上纯的”或“经分离的”意指目标物质为存在的主要物质(即,按摩尔计,比组合物中的任何其它个别大分子物质更丰富),且基本上纯化的部分为其中目标物质占所存在的所有大分子物质的至少约50%(按摩尔计)的组合物。在一个实施例中,基本上纯的组合物意指所关注的物质以摩尔计或重量计占存在于组合物中的大分子物质的至少约70%、75%、80%、85%、90%、95%、98%或更多。如果组合物基本上由单一大分子物质组成,则将目标物质纯化至基本均质(通过习知检测方法无法检测到组合物中的污染物质)。出于此定义的目的,溶剂物质、小分子(《500道尔顿)、稳定剂(例如bsa)和元素离子物质不视为大分子物质。在一个实施例中,本公开的化合物为基本上纯的或经分离的。在另一实施例中,本公开的化合物相对于其生产中所使用的大分子起始物质为基本上纯的或经分离的。在又另一实施例中,本公开的药物组合物包括与一种或多种药学上可接受的赋形剂、载剂或稀释剂且任选地与另一生物活性剂掺合的基本上纯的或经分离的cnp变体。
[0094]“治疗”是指防治性治疗或治疗性治疗或诊断性治疗。在某些实施例中,“治疗”是指出于治疗、预防或诊断目的而向个体施用化合物或组合物。
[0095]“预防性”治疗为出于降低产生病变的风险的目的,向未展现疾病的病征或仅展现疾病的早期病征的个体施用治疗。本公开的化合物或组合物可作为预防性治疗提供以减少产生病变的可能性或最小化病变(如果产生)的严重程度。
[0096]“治疗性”治疗为出于减轻或消除病变的病征或症状的目的,向展现那些病征或症状的个体施用治疗。病征或症状可为生物化学、细胞、组织学、功能或物理、主观或客观的。本公开的化合物还可作为治疗性治疗给出或针对诊断提供。
[0097]“诊断”意指鉴别病理学病状的存在、程度和/或性质。诊断方法在其特异性和选择性方面不同。尽管特定诊断方法可能不提供病状的确定诊断,但如果所述方法提供辅助诊断的正向指示,则其为足够的。
[0098]“骨相关或软骨相关的生物标记”或“骨相关或软骨相关的标记”是指含量与例如软骨转换、软骨形成、软骨生长、骨再吸收、骨形成、骨生长或其组合相关联而增加或减少的生长因子、酶、蛋白质或其它可检测的生物物质或部分。此类生物标记可在施用如本文所描述的cnp变体之前、期间和/或之后测量。示例性骨相关或软骨相关的生物标记包含(但不限于)cnp、cgmp、ii型胶原蛋白和其片段的前肽、ii型胶原蛋白和其片段、i型胶原蛋白和其片段的前肽、i型胶原蛋白和其片段、骨钙化素、增殖细胞核抗原(pcna)、聚集蛋白聚糖硫酸软骨素、胶原蛋白x和碱性磷酸酶。可测量任何适当生物样品中的软骨相关和骨相关的生物标记,包含(但不限于)组织、血液、血清、血浆、脑脊髓液、滑液和尿液。在一些实施例中,在来自进行体内功效/药效学研究的动物和/或来自离体研究的经调节的培养基的血液、血浆或血清中测量生物标记。
[0099]“药物组合物”或“配制物”是指适用于个体动物(包含人类和哺乳动物)中的医药用途的组合物。药物组合物包括治疗有效量的cnp变体、任选的另一生物活性剂以及任选的药学上可接受的赋形剂、载剂或稀释剂。在一实施例中,药物组合物涵盖包括一种或多种活性成分和构成载剂的一种或多种惰性成分的组合物,以及直接或间接由任何两种或更多种成分的组合、复合或聚集或由一种或多种以上成分的解离或由一种或多种成分的其它类型的反应或相互作用而产生的任何产物。因此,本公开的药物组合物涵盖通过将本公开的化合物与药学上可接受的赋形剂、载剂或稀释剂掺和制得的任何组合物。
[0100]“药学上可接受的载剂”是指标准医药学载剂、缓冲剂和其类似者中的任一者,如磷酸盐缓冲盐水溶液、5%右旋糖水溶液和乳液(例如油/水或水/油乳液)。赋形剂的非限制性实例包含佐剂、粘合剂、填充剂、稀释剂、崩解剂、乳化剂、润湿剂、润滑剂、助滑剂、甜味剂、调味剂和着色剂。适合的医药学载剂、赋形剂和稀释剂描述于《雷明顿氏医药科学(remington's pharmaceutical sciences)》,第19版(马克出版公司(mack publishing co.),easton,1995)中。优选医药学载剂视活性剂的预期施用模式而定。典型施用模式包含经肠(例如,经口)或非经肠(例如,皮下、肌肉内、静脉内或腹膜内注射;或局部、经皮或经粘膜施用)。
[0101]“药学上可接受的盐”为可配制成用于医药学用途的化合物的盐,包含(但不限于)金属盐(例如钠、钾、镁、钙等)以及氨或有机胺的盐。
[0102]“药学上可接受的”或“药理学上可接受的”意指不为生物学上或以其它方式非所要的物质,即可在不导致任何非所要生物效应的情况下或在不以有害方式与含有其的组合物的任何组分或与存在于个体身体的上或的中的任何组分相互作用的情况下向个体施用的物质。
[0103]“生理条件”是指动物(例如人类)体内的条件。生理条件包含(但不限于)体温以及具有生理离子强度、ph和酶的水性环境。生理条件还涵盖特定个体体内与大部分个体中存
在的“正常”条件不同的条件,例如与大致37℃的正常人体体温不同或与大致7.4的正常人类血液ph不同。
[0104]“生理ph”或“生理范围内的ph”意指大致7.0至8.0(包含端点)范围内,更典型地在大致7.2至7.6(包含端点)范围内的ph。
[0105]
如本文所用,术语“个体”涵盖哺乳动物和非哺乳动物。哺乳动物的实例包含(但不限于)哺乳动物类的任何成员:人类、非人类灵长类动物,如黑猩猩以及其它猿和猴物种;农畜,如牛、马、绵羊、山羊、猪;家畜,如兔子、狗和猫;实验室动物,包含啮齿动物,如大鼠、小鼠和天竺鼠,和类似动物。非哺乳动物的实例包含(但不限于)鸟类、鱼和类似动物。术语并不指示特定年龄或性别。在各种实施例中,个体为人类。在各种实施例中,个体为儿童或青少年。在各种实施例中,个体为婴儿。在各种实施例中,个体年龄大于3个月、大于2个月、大于1个月或大于6个月。
[0106]
c型利尿钠肽变体
[0107]
c型利尿钠肽(cnp)(《生物化学与生物物理研究交流》,168:863-870(1990)(genbank寄存编号np_077720,对于cnp前体蛋白nppc)(《高血压杂志》,10:907-912(1992))为具有17个氨基酸的环结构的肽家族(anp、bnp、cnp)中的小单链肽(levin等人,《新英格兰医学杂志》,339:863-870(1998))且在多种生物过程中具有重要角色。cnp与利尿钠肽受体-b(npr-b、gc-b)相互作用以刺激产生环鸟苷单磷酸(cgmp)(《高血压杂志》10:1111-1114(1992))。cnp更广泛表达包含于中枢神经系统、生殖道、骨和血管内皮中(《高血压》,49:419-426(2007))。
[0108]
先前已描述天然cnp基因和多肽。美国专利第5,352,770号公开从猪脑分离和纯化的序列与人类cnp相同的cnp-22以及其治疗心脏血管适应症的用途。美国专利第6,034,231号公开前-原cnp(126个氨基酸)的人类基因和多肽以及人类cnp-53基因和多肽。成熟cnp为22个氨基酸的肽(cnp-22)。某些cnp变体公开于美国专利8,198,242中,其以引用的方式并入本文中。
[0109]
在各种实施例中,本公开的cnp包含范围介于人类cnp-17(hcnp-17)至人类cnp-53(hcnp-53)且具有源自hcnp-53的野生型氨基酸序列的截短cnp。此类截短cnp肽包含:
[0110]
dlrvdtksraawarllqehpnarkykgankkglskgcfglkldrigsmsglgc(cnp-53)(seq id no:56);
[0111]
lrvdtksraawarllqehpnarkykgankkglskgcfglkldrigsmsglgc(cnp-52)(seq id no:15);
[0112]
rvdtksraawarllqehpnarkykgankkglskgcfglkldrigsmsglgc(cnp-51)(seq id no:16);
[0113]
vdtksraawarllqehpnarkykgankkglskgcfglkldrigsmsglgc(cnp-50)(seq id no:17);
[0114]
dtksraawarllqehpnarkykgankkglskgcfglkldrigsmsglgc(cnp-49)(seq id no:18)
[0115]
tksraawarllqehpnarkykgankkglskgcfglkldrigsmsglgc(cnp-48)(seq id no:19);
[0116]
ksraawarllqehpnarkykgankkglskgcfglkldrigsmsglgc(cnp-47)(seq id no:
20);
[0117]
sraawarllqehpnarkykgankkglskgcfglkldrigsmsglgc(cnp-46)(seq id no:21);
[0118]
raawarllqehpnarkykgankkglskgcfglkldrigsmsglgc(cnp-45)(seq id no:22);
[0119]
aawarllqehpnarkykgankkglskgcfglkldrigsmsglgc(cnp-44)(seq id no:23);
[0120]
awarllqehpnarkykgankkglskgcfglkldrigsmsglgc(cnp-43)(seq id no:24);
[0121]
warllqehpnarkykgankkglskgcfglkldrigsmsglgc(cnp-42)(seq id no:25);
[0122]
arllqehpnarkykgankkglskgcfglkldrigsmsglgc(cnp-41)(seq id no:26);
[0123]
rllqehpnarkykgankkglskgcfglkldrigsmsglgc(cnp-40)(seq id no:27);
[0124]
llqehpnarkykgankkglskgcfglkldrigsmsglgc(cnp-39)(seq id no:28);
[0125]
lqehpnarkykgankkglskgcfglkldrigsmsglgc(cnp-38)(seq id no:2);
[0126]
qehpnarkykgankkglskgcfglkldrigsmsglgc(cnp-37)(seq id no:3);
[0127]
ehpnarkykgankkglskgcfglkldrigsmsglgc(cnp-36)(seq id no:29);
[0128]
hpnarkykgankkglskgcfglkldrigsmsglgc(cnp-35)(seq id no:30);
[0129]
pnarkykgankkglskgcfglkldrigsmsglgc(cnp-34)(seq id no:4);
[0130]
narkykgankkglskgcfglkldrigsmsglgc(cnp-33)(seq id no:31);
[0131]
arkykgankkglskgcfglkldrigsmsglgc(cnp-32)(seq id no:32);
[0132]
rkykgankkglskgcfglkldrigsmsglgc(cnp-31)(seq id no:33);
[0133]
kykgankkglskgcfglkldrigsmsglgc(cnp-30)(seq id no:34);
[0134]
ykgankkglskgcfglkldrigsmsglgc(cnp-29)(seq id no:35);
[0135]
kgankkglskgcfglkldrigsmsglgc(cnp-28)(seq id no:36);
[0136]
gankkglskgcfglkldrigsmsglgc(cnp-27)(seq id no:37);
[0137]
ankkglskgcfglkldrigsmsglgc(cnp-26)(seq id no:38);
[0138]
nkkglskgcfglkldrigsmsglgc(cnp-25)(seq id no:39);
[0139]
kkglskgcfglkldrigsmsglgc(cnp-24)(seq id no:40);
[0140]
kglskgcfglkldrigsmsglgc(cnp-23)(seq id no:41);
[0141]
glskgcfglkldrigsmsglgc(cnp-22)(seq id no:68);
[0142]
lskgcfglkldrigsmsglgc(cnp-21)(seq id no:42);
[0143]
skgcfglkldrigsmsglgc(cnp-20)(seq id no:43);
[0144]
kgcfglkldrigsmsglgc(cnp-19)(seq id no:44);
[0145]
gcfglkldrigsmsglgc(cnp-18)(seq id no:45);和
[0146]
cfglkldrigsmsglgc(cnp-17)(seq id no:67)。
[0147]
在各种实施例中,cnp变异肽为经修饰的cnp-37或cnp-38肽,任选地具有弗林蛋白酶裂解位点(加下划线)处的一个或多个突变/一个或多个取代和/或含有n端处的甘氨酸或脯氨酸-甘氨酸。示例性cnp-37变体包含(但不限于):
[0148]
qehpnarkykgankkglskgcfglkldrigsnsglgc[cnp-37(m32n);seq id no:46];
[0149]
mqehpnarkykgankkglskgcfglkldrigsmsglgc(met-cnp-37;seq id no:47);
[0150]
pqehpnarkykgankkglskgcfglkldrigsmsglgc(pro-cnp-37;seq id no:48);
[0151]
gqehpnarkykgankkglskgcfglkldrigsnsglgc[gly-cnp-37(m32n);seq id no:49];
[0152]
pgqehpnarkykgankkglskgcfglkldrigsmsglgc(pro-gly-cnp-37;seq id no:1);
[0153]
mgqehpnarkykgankkglskgcfglkldrigsmsglgc(met-gly-cnp-37;seq id no:50);
[0154]
gqehpnarkykgankkglskgcfglkldrigsmsglgc(gly-cnp-37:seq id no:51)
[0155]
gqehpnarkykganpkglskgcfglkldrigsmsglgc(seq id no:52);
[0156]
gqehpnarkykganqkglskgcfglkldrigsmsglgc(seq id no:53);
[0157]
gqehpnarkykganqqglskgcfglkldrigsmsglgc(seq id no:54);和
[0158]
gqehpnarkykgankpglskgcfglkldrigsmsglgc(seq id no:55);
[0159]
在各种实施例中,本公开的cnp变体包含
[0160]
pgqehpqarryrgaqrrglsrgcfglkldrigsmsglgc(seq id no:5);
[0161]
pgqehpnarkykgankkglskgcfglkldrigsmsglgc(seq id no:1);
[0162]
pgqehpnarryrganrrglsrgcfglkldrigsmsglgc(seq id no:6);
[0163]
pgqehpqarryrgaqrrglsrgcfglkldrigsmsglgc(seq id no:5);
[0164]
pgqehpqarkykgaqkkglskgcfglkldrigsmsglgc(seq id no:7);
[0165]
pgqehpqarryrgaqrrglsrgcfglk(aeea-aeea-γglu-c18da)ldrigsmsglgc(seq id no:5);和
[0166]
pgqehpnarkykgankkglskgcfglk(aeea-aeea-γglu-c18da)ldrigsmsglgc(seq id no:1)。
[0167]
经进一步考虑本文所描述的具有少于53个氨基酸的任何变体可通过向肽的n-末端添加氨基酸来延伸。举例来说,如果与wt cnp相比,cnp变体为具有经改变的氨基酸的34-聚体、35-聚体、36-聚体、37-聚体、38-聚体或39-聚体,则此类变体可在具有野生型或来自cnp53或来自其它肽的经修饰残基的n-末端上延伸。
[0168]
在各种实施例中,cnp变体进一步包括乙酰基。在各种实施例中,乙酰基位于n端、c端上或连接至内部氨基酸侧基。在各种实施例中,乙酰基位于肽的n端上。
[0169]
在各种实施例中,肽变体于c端进一步包括oh或nh2基团。
[0170]
在各种实施例中,cnp变体选自由以下组成的群组:
[0171]
ac-pgqehpqarryrgaqrrglsrgcfglkldrigsmsglgc-oh(seq id no:8),
[0172]
ac-pgqehpnarkykgankkglskgcfglkldrigsmsglgc-nh2(seq id no:9)、
[0173]
ac-pgqehpnarryrganrrglsrgcfglkldrigsmsglgc-oh(seq id no:10),
[0174]
ac-pgqehpnarryrganrrglsrgcfglkldrigsmsglgc-nh2(seq id no:11)和
[0175]
ac-pgqehpqarryrgaqrrglsrgcfglkldrigsmsglgc-nh2(seq id no:12)。
[0176]
在各种实施例中,cnp变体选自由以下组成的群组:
[0177]
pgqehpqarryrgaqrrglsrgcfglkldrigsmsglgc-oh(seq id no:8),
[0178]
pgqehpnarkykgankkglskgcfglkldrigsmsglgc-nh2(seq id no:9),
[0179]
pgqehpnarryrganrrglsrgcfglkldrigsmsglgc-oh(seq id no:10),
[0180]
pgqehpnarryrganrrglsrgcfglkldrigsmsglgc-nh2(seq id no:11)和
[0181]
pgqehpqarryrgaqrrglsrgcfglkldrigsmsglgc-nh2(seq id no:12)
[0182]
pgqehpqarkykgaqkkglskgcfglkldrigsmsglgc-oh(seq id no:7)。
[0183]
在各种实施例中,cnp变体选自由以下组成的群组:
[0184]
ac-pgqehpqarryrgaqrrglsrgcfglkldrigsmsglgc-oh(seq id no:8),
[0185]
ac-pgqehpnarkykgankkglskgcfglkldrigsmsglgc-nh2(seq id no:9),
[0186]
ac-pgqehpnarryrganrrglsrgcfglkldrigsmsglgc-oh(seq id no:10),
[0187]
ac-pgqehpnarryrganrrglsrgcfglkldrigsmsglgc-nh2(seq id no:11),
[0188]
ac-pgqehpqarryrgaqrrglsrgcfglkldrigsmsglgc-nh2(seq id no:12);
[0189]
ac-pgqehpqarkykgaqkkglskgcfglkldrigsmsglgc-nh2(seq id no:13);以及
[0190]
ac-pgqehpqarkykgaqkkglskgcfglkldrigsmsglgc-oh(seq id no:14)。
[0191]
在各种实施例中,cnp变体选自由ac-pgqehpqarryrgaqrrglsrgcfglk(aeea-aeea-γglu-c18da)ldrigsmsglgc-oh(seq id no:8)组成的群组。在各种实施例中,cnp变体为ac-pgqehpnarkykgankkglskgcfglk(aeea-aeea-γglu-c18da)ldrigsmsglgc-oh(seq id no:1)。在各种实施例中,cnp变体为pgqehpnarkykgankkglskgcfglk(aeea-aeea-γglu-c18da)ldrigsmsglgc-oh(seq id no:1)。
[0192]
在额外实施例中,对于具有一个或多个天冬酰胺(asn/n)残基和/或一个或多个谷氨酰胺(gln/q)残基的本文所描述的cnp变体中的任一者,不论其是否具有野生型序列或非天然氨基酸序列,任何一个或多个asn残基和/或任何一个或多个gln残基可独立地经任何其它天然或非天然氨基酸取代,包含保守取代,如asn至gln。一个或多个此类取代部分地经设计以最小化或避免天冬酰胺和/或谷氨酰胺的任何潜在脱酰胺作用。
[0193]
在额外实施例中,对于具有一个或多个赖氨酸(lys/k)残基的本文所描述的cnp变体中的任一者,无论其是否具有野生型序列或非天然氨基酸序列,任何一个或多个lys残基可独立地经任何其它天然或非天然氨基酸取代,包含如lys至arg的取代。在各种实施例中,除了cnp变体环状域中的lys残基未经任何其它天然或非天然氨基酸取代以外,所有赖氨酸残基独立地经任何其它天然或非天然氨基酸取代,包含如lys至arg的取代。
[0194]
在一个实施例中,cnp变体经由在cys6与cys
22
之间形成双硫键而环化,如wtcnp22肽中所指示。cys6可为半胱氨酸类似物,如高半胱氨酸或青霉胺。在另一实施例中,cnp变体可通过形成头对尾、侧链对侧链、侧链对头或侧链对尾的共价键而环化。在一实施例中,共价键形成于在n端处或朝向n端的氨基酸与在肽的c端处或朝向肽的c端的氨基酸(在此情形下称为“末端”氨基酸)之间。在另一实施例中,共价键形成于两个末端氨基酸的侧链之间。在另一实施例中,共价键形成于一个末端氨基酸的侧链与另一末端氨基酸的端基之间,或两个末端氨基酸的端基之间。
[0195]
末端胺与末端羧基的头对尾环化可使用多种方法进行,例如使用对硝苯基酯、2,4,5-三氯苯基酯、五氟苯基酯、叠氮方法、混合酸酐方法、hatu、碳化二亚胺(例如dic、edc或dcc)与如hobt、honsu或hoat的催化剂或树脂上环化。
[0196]
另外,环状结构可经由涉及cnp变体的氨基酸残基和/或末端氨基酸残基的侧链的桥基形成。桥基为使得肽的两个部分环化的化学部分。桥基的非限制性实例包含酰胺、硫醚、硫酯、二硫化物、脲、氨基甲酸酯、磺酰胺和其类似者。本领域中已知多种用于并入具有此类桥基的单元的方法。举例来说,内酰胺桥(即,环酰胺)可形成于n端氨基或侧链上的氨基与c端羧酸或侧链上的羧基之间,例如赖氨酸或鸟胺酸的侧链和谷氨酸或天冬氨酸的侧链。硫酯可形成于c端羧基或侧链上的羧基与半胱氨酸或半胱氨酸类似物的侧链上的硫醇基之间。
[0197]
可替代地,可通过并入羊毛硫胺酸(硫-二丙氨酸)残基以连接通过硫醚键共价键
结在一起的丙氨酸残基来形成交联。在另一方法中,交联剂,如二羧酸(例如,辛二酸(suberic acid/octanedioic acid))可连接氨基酸侧链的官能团,如游离氨基、羟基和硫醇基。
[0198]
还可使用酶催化的环化。举例来说,已报告泰罗雪定(tyrocidine)合成酶的硫酯酶域可用于环化硫酯前体,枯草杆菌蛋白酶(subtilisin)突变可用于环化乙醇酸肽苯丙氨酰胺酯,且抗体接合酶16g3可用于环化对硝苯基酯。对于肽环化的综述,参见davies,j.《肽科学(peptide sci.》,9:471-501(2003),其以全文引用的方式并入本文中。
[0199]
在某些实施例中,最终产物具有至少约70%、75%、80%、85%、90%、95%、96%、97%、98%或至少约99%的纯度。
[0200]
肽共轭物
[0201]
肽治疗剂为有吸引力的生物治疗剂,但通常由于在溶液中的低稳定性和短半衰期而为不利的(tang等人,《欧洲医药科学杂志(eur j pharm sci.)》102:63-70,2017)。通过增强稳定性和/或延长半衰期来尝试改良肽治疗剂的功效,包含尝试将亲水性肽囊封至如脂质体或聚合物粒子的可生物降解粒子中。然而,由于这些肽的阳离子性质和其与带负电聚合物的脂质体静电相互作用的能力,此一直为困难的(griesser等人,《国际医药学杂志(int j pharmaceutics)》520:267-274,2017)。肽共轭物的产生已成为用于能够更好地将亲水性聚合物囊封至微粒或脂质体中的一种方式(lu等人,《分子医药学(mol.pharmaceutics)》15:216-225,2018)。
[0202]
肽可为5至100个氨基酸的一串氨基酸。肽可具有带正电氨基酸、带负电氨基酸或两者的混合物,使得肽能够与带电部分,例如具有与肽中的带电物质相反的带电物质的阳离子、阴离子或其组合相互作用。
[0203]
经考虑肽与赋予增加的稳定性或半衰期的部分(例如共轭部分)错合。在各种实施例中,共轭部分经由非共价键错合或通过共价键连接。所述部分可经由静电相互作用与肽非共价连接。可替代地,所述部分可经由一个或多个连接子部分与肽共价结合。连接子可为可裂解和不可裂解连接子。可裂解连接子可经由酶、亲核/碱性试剂、还原剂、光照射、亲电/酸性试剂、有机金属和金属试剂或氧化试剂裂解。连接子还可以是自分解型连接子。示例性连接子包含(但不限于):n-丁二酰亚氨基-3-(2-吡啶基二硫醇)丙酸酯(spdp)、亚氨基硫杂环戊烷(it)、酰亚胺酯的双官能衍生物(如盐酸二亚胺代己二酸二甲酯)、活性酯(如辛二酸二丁二酰亚胺酯)、醛(如戊二醛)、双叠氮基化合物(如双(对叠氮基苯甲酰基)己二胺)、双重氮衍生物(如双(对重氮苯甲酰基)-乙二胺)、二异氰酸酯(如甲苯2,6-二异氰酸酯)和双活性氟化合物(如1,5-二氟-2,4-二硝基苯)、β丙氨酸、4-氨基丁酸(gaba)、2-氨基乙氧基酸(aea)、氨基乙氧基-2-乙氧基乙酸(aeea)、5氨基戊酸(ava)、6-氨基己酸(abx)、邻二醇可裂解连接子、三甲基锁内酯化、对烷氧基苯基氨基甲酸酯、bicin、类肽或bicin型连接子以及如本文所描述的电子连接子。
[0204]
在各种实施例中,连接子连接至cnp环状域内的cnp变体的残基上或位于除所述cnp环状域之外的位点处。在各种实施例中,连接子连接至赖氨酸残基。在各种实施例中,连接子连接至cnp环状域中的赖氨酸残基。
[0205]
在各种实施例中,cnp变体经由连接子连接至共轭部分。在各种实施例中,连接子经由共轭部分的亲水性间隔基连接至共轭部分。
3,6-二氧杂辛酸)基团。在各种实施例中,亲水性间隔基为oeg(8-氨基-3,6-二氧杂辛酸)。在各种实施例中,间隔基为oeg(8-氨基-3,6-二氧杂辛酸)或γglu。在各种实施例中,亲水性间隔基为与一个或多个oeg(8-氨基-3,6-二氧杂辛酸)基团连接的γ谷氨酸(γglu)。在各种实施例中,亲水性间隔基为与一或两个oeg(8-氨基-3,6-二氧杂辛酸)基团(dieg)连接的γ谷氨酸(γglu)。在各种实施例中,酸部分和亲水性间隔基具有结构aeea-aeea-γglu-c18da。
[0213]
在各种实施例中,cnp变体具有以下结构:
[0214]
pgqehpqarryrgaqrrglsrgcfglk(aeea-aeea-γglu-c18da)ldrigsmsglgc(seq id no:5),或
[0215]
ac-pgqehpqarryrgaqrrglsrgcfglk(aeea-aeea-γglu-c18da)ldrigsmsglgc-oh(seq id no:8)。在各种实施例中,cnp变体具有结构pgqehpnarkykgankkglskgcfglk(aeea-aeea-γglu-c18da)ldrigsmsglgc、ac-pgqehpnarkykgankkglskgcfglk(aeea-aeea-γglu-c18da)ldrigsmsglgc-oh(seq id no:1),或pgqehpnarkykgankkglskgcfglk(aeea-aeea-γglu-c18da)ldrigsmsglgc-oh(seq id no:1)。在各种实施例中,cnp变体包括上述肽的asn至glu变体。
[0216]
在各种实施例中,本公开涵盖亲水性或水溶性聚合物(例如氧化烷基链,其中碳原子可经一个或多个氧原子置换,如聚乙二醇(peg)或聚氧化乙烯(peo)等)的用途。在各种实施例中,水溶性聚合物的类型(例如均聚物或共聚物;无规、交替或嵌段共聚物;直链或分支链;单分散或多分散)、键(例如可水解或稳定键,如酰胺、亚胺、缩醛胺、伸烷基或酯键)、共轭位点(例如在n端、内部和/或c端)和长度(例如约0.2、0.4或0.6kda至约2、5、10、25、50或100kda)可变化。如本领域中已知,亲水性或水溶性聚合物可通过基于n-羟基丁二酰亚胺(nhs)或醛的化学物质或其它化学物质与cnp变体共轭。在各种实施例中,带负电peg-cnp变体可经设计用于降低肾清除率,包含(但不限于)使用羧化、硫酸化和磷酸化的化合物(caliceti,《先进药物递送评论(adv.drug deliv.rev.)》,55:1261-77(2003);perlman,《临床内分泌与代谢杂志》,88:3227-35(2003);pitkin,《抗菌剂与化疗(antimicrob.ag.chemo.)》,29:440-444(1986);vehaskari,《国际肾脏杂志(kidney int'l)》,22:127-135(1982))。在一个实施例中,peg(或peo)部分含有一个或多个羧基、一个或多个硫酸基和/或一个或多个磷酸基。
[0217]
在另一实施例中,与本文所描述的cnp变体的n端、c端和/或一个或多个内部位点共轭的亲水性聚合物(例如,peg或peo)含有一个或多个在生理条件下带正电的官能团。此类部分尤其经设计以改良此类共轭的cnp变体向软骨组织中的分布。在一个实施例中,peg部分含有一个或多个伯、仲或叔氨基、季铵基和/或其它含胺(例如脲)基。
[0218]
制备方法
[0219]
本文还涵盖制备包括cnp变体且任选地包括如本文所描述的共轭部分的组合物的方法。
[0220]
在各种实施例中,cnp变体使用标准蛋白质合成化学方法以合成方式制得。举例来说,使用固相树脂和标准fmoc化学方法逐步合成肽。肽使用三氟乙酸(tfa)从树脂裂解且通过逆相高效液相色谱(rp-hplc)纯化。
[0221]
在各种实施例中,所述方法进一步包括通过使树脂与nmp/ac2o/diea任选地以10:
1:0.1,v/v/v反应而将肽乙酰化。
[0222]
进一步提供一种方法,其中肽与任选地存在于赖氨酸残基上的共轭部分共轭。步骤包括使赖氨酸上的保护性氨基裂解、使肽与2
×
fmoc-氨基peg(2)反应接着与氨基酸反应,接着使脂质或脂肪酸部分共轭。在各种实施例中,共轭部分包括一种或多种脂质或脂肪酸和疏水性间隔基。
[0223]
所述方法进一步提供通过与三氟乙酸接触从树脂裂解肽的步骤,和通过逆相hplc纯化肽的步骤。
[0224]
在某些实施例中,本文所描述的cnp变体通过重组方法产生,所述重组方法包括在引起由多核苷酸编码的融合多肽的表达的条件下在培养基中培养宿主细胞,所述宿主细胞包括编码cnp变体多肽的第一多核苷酸,任选地与编码可裂解肽或蛋白质的第二多核苷酸连接。在一些实施例中,宿主细胞用包括编码cnp变体多肽的多核苷酸的表达载体转型,所述多核苷酸任选地与编码可裂解肽或蛋白质的多核苷酸连接。在某些实施例中,融合多肽表达为可溶性蛋白质或包涵体。经表达的融合多肽可从宿主细胞或培养物分离,且经分离的融合多肽可与裂解剂接触以释放cnp变体。
[0225]
制备cnp变异肽的方法,包含使用宿主细胞、表达载体、可裂解肽以及培养物参数,公开于美国专利8,198,242中,其特此以引用的方式并入。
[0226]
使用方法
[0227]
软骨发育不全为成纤维细胞生长因子受体3(fgfr-3)的基因中常染色体显性突变的结果,此导致软骨形成异常。fgfr-3对软骨细胞生长通常具有负调节作用,且因此对骨生长具有负调节作用。在软骨发育不全中,fgfr-3的突变形式为组成性活性的,其导致骨严重缩短。在人类中,fgfr-3的活化突变为遗传性侏儒症的主要原因。具有活化fgfr-3的小鼠充当软骨发育不全(骨骼发育不良的最常见形式)的模型,且cnp的过度表达拯救这些动物免遭侏儒症。因此,cnp的功能变体为治疗多种骨胳发育不良的潜在治疗剂。
[0228]
通过刺激软骨细胞的基质产生、增殖和分化以及增加长骨生长,本公开的cnp变体适用于治疗罹患骨相关病症(如骨胳发育不良)的哺乳动物,包含人类。cnp反应性骨相关病症和骨胳发育不良的非限制性实例包含软骨发育不全、软骨生成减退、身材矮小、侏儒症、骨软骨发育不良、致死性骨发育不良、成骨不全、软骨成长不全、先天性成骨不全、纯合性软骨发育不全、先天性成骨不全、屈肢骨发育不良、先天性致死型低磷酸酯酶症、围产期致死型成骨不全、短肋多指综合征、软骨生成减退、肢根型点状软骨发育不良、扬森型干骺端发育不良、先天性脊椎骨骺发育不良、骨发育不全、扭曲性骨发育不良、先天性股骨短、兰格型肢中骨发育不良、尼维格型肢中骨发育不良、罗氏综合征、莱因哈特综合征、肢端发育不全、周围骨发育障碍、克尼斯特发育不良、纤维软骨生成、罗伯茨综合征、肢端肢中发育不良、小肢、莫奎氏综合征、克尼斯特综合征、后生营养发育不良和脊椎骨骺干骺端发育不良。本文涵盖的身材矮小、生长板病症、骨相关病症或骨胳发育不良包含与npr2突变、shox突变(特纳氏综合征/莱里维尔)和ptpn11突变(努南氏综合征)相关的病症。
[0229]
通过刺激软骨细胞的基质产生、增殖和分化以及增加长骨生长,本公开的cnp变体适用于治疗罹患骨相关病症(如骨胳发育不良)的哺乳动物,包含人类。cnp反应性骨相关病症和骨胳发育不良的非限制性实例包含软骨发育不全、软骨生成减退、身材矮小、侏儒症、骨软骨发育不良、致死性骨发育不良、成骨不全、软骨成长不全、先天性成骨不全、纯合性软
骨发育不全、先天性成骨不全、屈肢骨发育不良、先天性致死型低磷酸酯酶症、围产期致死型成骨不全、短肋多指综合征、软骨生成减退、肢根型点状软骨发育不良、扬森型干骺端发育不良、先天性脊椎骨骺发育不良、骨发育不全、扭曲性骨发育不良、先天性股骨短、兰格型肢中骨发育不良、尼维格型肢中骨发育不良、罗氏综合征、莱因哈特综合征、肢端发育不全、周围骨发育障碍、克尼斯特发育不良、纤维软骨生成、罗伯茨综合征、肢端肢中发育不良、小肢、莫奎氏综合征、克尼斯特综合征、后生营养发育不良和脊椎骨骺干骺端发育不良。本文涵盖的身材矮小、生长板病症、骨相关病症或骨胳发育不良包含与npr2突变、shox突变(特纳氏综合征/莱里维尔)、ptpn11突变(努南氏综合征)以及igf1r突变相关的病症。
[0230]
方法涵盖的额外身材矮小和生长板病症包含与胶原蛋白(col2a1、col11a1、col9a2、col10)、聚集蛋白聚糖(acan)、印度刺猬因子(ihh)、ptpn11、npr2、nppc或fgfr3的突变相关的病症。
[0231]
方法涵盖的额外身材矮小和生长板病症包含与胶原蛋白(col2a1、col11a1、col9a2、col10)、聚集蛋白聚糖(acan)、印度刺猬因子(ihh)、ptpn11、npr2、nppc、fgfr3或igf1r的突变相关的病症。
[0232]
此外,cnp变体适用作用于治疗特发性身材矮小和其它骨骼发育不良的生长激素的佐剂或替代物。
[0233]
生长板病症包含导致身材矮小或骨生长异常和可为涉及骨生长的基因中的基因突变的结果的病症,所述基因包含胶原蛋白(col2a1、col11a1、col9a2、col10)、聚集蛋白聚糖(acan)、印度刺猬因子(ihh)、ptpn11、npr2、nppc或fgfr3。在各种实施例中,生长板病症包含导致身材矮小或骨生长异常和可为涉及骨生长的基因中的基因突变的结果的病症,所述基因包含胶原蛋白(col2a1、col11a1、col9a2、col10)、聚集蛋白聚糖(acan)、印度刺猬因子(ihh)、ptpn11、npr2、nppc、fgfr3或igf1r。在各种实施例中,生长板病症或身材矮小与相关于拉索病的基因中的一个或多个突变相关。在各种实施例中,患有生长板病症的个体对于生长板基因中的突变为异型接合的。在各种实施例中,突变为功能损失型突变。在各种实施例中,突变为功能获得型突变。生长板病症包含但不限于家族性身材矮小、显性家族性身材矮小(其也称为显性遗传性身材矮小)或特发性身材矮小。参见例如plachy等人,《临床内分泌代谢杂志(j clin endocrinol metab)》104:4273-4281,2019。
[0234]
acan的突变可引起家族性剥脱性骨软骨炎和身材矮小且最终引起骨关节炎,其特征在于由软骨和有时骨头在关节处从骨末端脱离引起的骨损伤(或病变)区域。已提出骨生长中的软骨网状结构错乱会损害其生长,导致身材矮小。与acan和身材矮小相关的突变包含val2303met。参见stattin等人《美国人类遗传学杂志(am j hum genet)》86(2):126-37,2010。经考虑具有导致身材矮小的acan突变的患者将受益于cnp治疗,因为施用可能够通过cnp与fgfr3的已知相互作用增加这些患者的身高。
[0235]
已展示利尿钠肽系统(包含受体npr2)参与软骨内化骨生长的调节(vasques等人,《儿科激素研究(horm res pediat)》82:222-229,2014)。研究已展示npr2中的同型接合或复合异型接合功能损失型突变引起肢端肢中发育不良型maroteaux(amdm),其为骨胳具有极其身材矮小的发育不良(vasquez等人,2014,见上文)。有报告暗示异型接合功能损失型(如显性负性)npr2突变是身材矮小的原因,而功能获得型npr2异型接合突变已被认为是身材高大的原因(vasquez等人,2014,见上文)。鉴于cnp与npr2相互作用以刺激cgmp生成,增
加cgmp含量在这些情况下为期望的,且将在管理来自这些疾病和病状的并发症中具有治疗益处。
[0236]
相信npr2的异型接合突变导致特发性身材矮小和其它形式的身材矮小。npr2基因的突变阐述于下文且描述于以下各者中:amano等人,《临床内分泌代谢杂志》99:e713-718,2014;hisado-oliva等人,《临床内分泌代谢杂志》100:e1133-1142,2015和vasques等人,《临床内分泌代谢杂志》98:e1636-1644,2013,特此以引用的方式并入。经考虑患有待用如本文所描述的cnp变体治疗的身材矮小的个体具有小于-1.0、-1.5、-2.0、-2.5或-3.0的身高sds,且具有至少一个具有小于-1.0、-1.5、-2.0或-2.5的身高sds的亲代,任选地其中第二亲代的身高在正常范围内。在各种实施例中,cnp变体适用于治疗具有身高sds为-2.0至-3.0的身材矮小的个体。在各种实施例中,cnp变体适用于治疗具有身高sds为-2.0至-2.5的身材矮小的个体。然而,由于npr2中的新生突变可导致如由小于-1.5、-2.0、-2.5或-3.0的身高sds所定义的身材矮小,因此还涵盖治疗任一亲代均不患有身材矮小的作为npr2中的有害突变的异型接合携带者的个体。经进一步考虑用cnp治疗对于其它生长板基因中的有害突变为异型接合的个体,以改善身材和/或增强骨生长。
[0237]
可用cnp变体治疗的患者的示例性npr2突变包含:
[0238]
[0239][0240]
nppc在骨胳生长中的作用已得到充分证明(hisado-oliva等人,《遗传学药物(genetics medicine)》20:91-97,2018)。nppc基因敲除小鼠展示严重不成比例形式的侏儒症,包含四肢缩短和软骨内骨化(hisado-oliva等人,2018,见上文)。人类全基因组研究已展示nppc与身高之间的关联(hisado-oliva等人,2018,见上文)。尽管相信cnp单倍剂量不足为人类身材矮小的原因,但近来的研究鉴别了身材矮小和双手短小的家族中的异型接合突变(hisado-oliva等人,2018,见上文)。这些研究观测到以异型接合状态测量的cgmp产量显著降低(hisado-oliva等人,2018,见上文)。nppc的突变包含引起gly119cys改变的355g》t误义突变和引起arg117gly改变的349c》g误义突变。拯救cgmp产生的cnp变体可在具有异型接合功能损失型nppc突变的患者的病症管理中提供治疗益处。
[0241]
莱里-维尔软骨骨生成障碍(leri-weill dyschondrosteosis;lwd)为稀有遗传病症,其特征在于前臂和小腿缩短、手腕异常错位(手腕马得隆变形(madelung deformity))和相关的身材矮小。lwd是由位于性染色体的假常染色体区域1(pseudoautosomal region 1;par1)上的含身材矮小同源盒(shox)基因或其调节元件中的异型接合突变引起。(参见稀有疾病数据库和carmona等人,《人类分子遗传学(hum mol genet)》20:1547-1559,2011)。病症兰格肢中骨发育不良在存在两个shox突变时产生,且可由各染色体上的突变(同型接合或复合异型接合突变)产生。shox突变的子集引起特发性身材矮小。特纳氏综合征由于可包含shox基因的x染色体上的缺失而产生。shox已鉴别为参与fgfr3转录调节且有助于骨生长控制(marchini等人,《内分泌综述(endocr rev.)》37:417-448,2016)。shox缺乏导致fgfr3信号传导增加,且一些证据支持shox还与cnp/npr2直接相互作用(marchini,见上文)。鉴于shox与fgfr3和骨生长的关联,经考虑具有同型接合或异型接合shox突变的个体将受益于用如本文所描述的cnp变体治疗。
[0242]
拉索病为由ras/促分裂原活化蛋白激酶(mitogen-activated protein kinase;mapk)路径基因中的突变引起的一组罕见遗传病状。拉索病为特征在于经由ras/mapk路径的信号传导增加的一组病症。此路径导致raf/mek/erk路径的下游活化。身材矮小为某些拉索病的典型特征。举例来说,cnp信号传导抑制raf且使得mek和erk活化降低。
[0243]
本文涵盖拉索病的治疗。与身材矮小相关的拉索病包含努南氏综合征、科斯特洛综合征、心脸皮肤综合征、1型神经纤维瘤和leopard综合征。遗传性1型齿龈纤维瘤病也是本文所涵盖的拉索病。拉索病患者(包含努南氏综合征、科斯特洛综合征、心脸皮肤综合征、
1型神经纤维瘤、leopard综合征、遗传性1型齿龈纤维瘤病)包含具有以下基因中的一或多者中的异型接合变体的患者:braf、cbl、hras、kras、lztr1、map2k1、map2k2、mras、nf1、nras、ppp1cb、ptpn11、raf1、rras、rit1、shoc2、sos1或sos2(tajan等人《内分泌综述》2018;39(5):676-700)。
[0244]
cfc是由ras/mapk信号传导路径中的若干基因的突变引起,包含k-ras、b-raf、mek1和mek2。科斯特洛综合征(也称为颜面皮肤骨胳(fcs)综合征)是由h-ras基因中的活化突变引起。遗传性i型齿龈纤维瘤病(hgf)是由sevenless同源物1的子代(son of sevenless homolog 1;sos1)基因中的显性突变引起,所述基因编码作用于小gtp酶的ras子族的鸟嘌呤核苷酸交换因子(sos)。i型神经纤维瘤(nf1)是由神经纤维瘤蛋白1基因中的突变引起,所述基因编码ras/mapk信号传导路径的负调节因子。努南氏综合征(ns)是由若干基因中的一者的突变引起,所述基因包含ptpn11(其编码shp2)和sos1,以及k-ras和raf-1。
[0245]
cnp已证明为拉索病模型中的有效疗法。ono等人产生在ii型胶原蛋白生产细胞中缺乏nf1的小鼠(ono等人,《人类分子遗传学(hum.mol.genet.)》2013;22(15):3048-62)。这些小鼠展现组成性erk1/2活化,和软骨细胞增殖减少,和成熟。向这些小鼠每日注射cnp使得erk磷酸化降低且校正了身材矮小。使用braf突变(p.q241r)的心脸皮肤综合征的小鼠模型(inoue等人《人类分子遗传学》2019;28(1):74-83)展现相比于野生型减小的体长和减小的生长板宽度与较小的增殖和肥大区域,且施用cnp使得这些动物的体长增加。
[0246]
多个基因的突变可引起努南氏综合征,其特征在于身材矮小、心脏缺陷、出血问题和骨胳畸形。ptpn11基因的突变引起努南氏综合征的所有病例的约一半。sos1基因突变引起额外10%至15%病例,且raf1和rit1基因各自占病例的约5%。其它基因的突变各自占少数病例。15%至20%患有此病症的人群的病因为未知的。
[0247]
ptpn11、sos1、raf1和rit1基因均编码在ras/mapk细胞信号传导路径中重要的蛋白质,所述路径对于细胞分裂和生长(增殖)、分化和细胞迁移是必需的。与努南氏综合征相关的基因中的许多突变使所得蛋白质被打开(活化),且此长时间活化改变正常ras/mapk信号传导,其破坏细胞生长和分裂调节,从而导致努南氏综合征的典型特征。参见例如chen等人,《美国国家科学院院刊(proc natl acad sci u s a.)》111(31):11473-8,2014,romano等人,《婴儿病学(pediatrics.)》126(4):746-59,2010,和等人,《美国医学遗传学杂志(am j med genet)》170(7):1874-80,2016。经考虑具有活化mapk路径的突变的个体将受益于用如本文所描述的cnp变体治疗,以改善骨生长和身材矮小。还考虑具有活化mapk路径的突变的个体将受益于用如本文所描述的cnp变体治疗,以改善与整个身体的其它细胞(其中npr2受体表达于其表面上)中的过度活化mapk路径相关的其它共患病。
[0248]
ptpn11基因(其编码非受体蛋白酪胺酸磷酸酶shp-2)的突变导致特征在于身材矮小的病症,如努南氏综合征(musente等人,《欧洲人类遗传学杂志(eur j hum genet)》11:201-206(2003)。musente(见上文)鉴别ptpn11基因中导致身材矮小的许多突变。功能获得型突变经由shp2的过度活化信号传导且抑制生长激素诱导的igf-1释放,从而使得骨生长降低(rocca serra-n
édé
lec,《美国国家科学院院刊(pnas)》109:4257-4262,2012)。经考虑具有同型接合或异型接合ptpn11突变的个体将受益于用如本文所描述的cnp变体治疗,以改善骨生长和身材矮小。
[0249]
印度刺猬因子(ihh)基因(其与软骨内骨化的调节有关)的突变还与身材矮小综合征相关(vasques等人,《临床内分泌代谢杂志》103:604-614,2018)。许多经鉴别的ihh突变以显性遗传模式与身材矮小分隔。鉴于ihh与骨生长和骨化的关联,经考虑具有同型接合或异型接合ihh突变的个体将受益于用如本文所描述的cnp变体治疗。
[0250]
fgfr3的突变,包含n540k和k650n导致身材矮小和软骨生成减退。
[0251]
胰岛素样生长因子1受体(igf1r)为具有内在激酶活性的杂四聚体(α2β2)跨膜糖蛋白。已展示igf1r在产前和产后生长中起作用。已在小于胎龄儿(gestational age children;sga)和患有家族性身材矮小的个体中鉴别igf1r的异型接合突变(kawashima等人,《内分泌杂志(endocrine j.)》59:179-185,2012)。与身材矮小相关的igf1r突变包含r108q/k115n、r59t、r709q、g1050k、r481q、v599e和g1125a(kawashima,见上文)。
[0252]
身高为可受数百个或数千个基因的组合效应影响的高度遗传性性状(wood等人,2014,《自然遗传学》,46:1173-1189)。个体的身材矮小可为这些基因的组合效应的结果,单一基因并非主要贡献者。鉴于cnp增加正常动物的长度,例如增强骨生长和骨长度的能力,经考虑患有由小于-1.0、-1.5、-2.0、-2.5或-3.0的身高sds定义的身材矮小的此类个体可有益地用cnp变体治疗。
[0253]
在各种实施例中,cnp变体适用于治疗具有如下的身材矮小的个体:身高sds为小于-1.0、-1.5、-2.0、-2.5或-3.0,且至少一个亲代的身高sds为小于-1.0、-1.5、-2.0或-2.5,任选地其中第二亲代的身高在正常范围内。在各种实施例中,cnp变体适用于治疗具有身高sds为-2.0至-3.0的身材矮小的个体。在各种实施例中,cnp变体适用于治疗具有身高sds为-2.0至-2.5的身材矮小的个体。在各种实施例中,身材矮小与相关于身材矮小的基因中的一个或多个突变相关,如胶原蛋白(col2a1、col11a1、col9a2、col10)、聚集蛋白聚糖(acan)、印度刺猬因子(ihh)、ptpn11、npr2、nppc、fgfr3或胰岛素生长因子1受体(igf1r)或其组合。
[0254]
在各种实施例中,生长板病症或身材矮小与相关于拉索病的基因中的一个或多个突变相关。
[0255]
在各种实施例中,身材矮小为如通过多基因风险评分(prs)所确定的多个基因的突变的结果。使用针对身高的公布的最大gwas综合分析计算身高的多基因风险评分(prs),所述综合分析不包含来自如实例4中所描述的uk生物库项目的任何样品。将群组分为五个prs五分位数(prs 1为最矮身高,prs 5为最高身高)。在各种实施例中,个体具有npr2的突变和低prs。在各种实施例中,个体具有fgfr3的突变和低prs。在各种实施例中,个体具有npr2的突变和低prs。在各种实施例中,个体具有igf1r的突变和低prs。在各种实施例中,个体具有nppc的突变和低prs。在各种实施例中,个体具有shox的突变和低prs。在各种实施例中,个体具有fgfr3、igf1r、nppc、npr2和shox中的一或多者的一个或多个突变和低prs。在各种实施例中,prs为1或2。在各种实施例中,prs为1。在各种实施例中,prs为2。
[0256]
另外,cnp变体适用于治疗其它骨相关病状和病症,如佝偻病、低磷酸盐血性佝偻病[包含x连锁低磷酸盐血性佝偻病(也称为维生素d耐药性佝偻病)和常染色体显性低磷酸盐血性佝偻病],和骨质软化[包含肿瘤诱导的骨质软化(也称为致癌骨质软化或致癌低磷酸盐血性骨质软化)]。
[0257]
本公开的cnp变体还可用于治疗骨关节炎。骨关节炎为关节软骨的退化疾病且在
questionnaire user's manual.)lengerich:pabst科学出版社(pabst science publishers);2013)。
[0267]
药物组合物
[0268]
本公开提供药物组合物,包含缓释组合物,其包括本文所描述的cnp变体,和一种或多种药学上可接受的赋形剂、载剂和/或稀释剂。在某些实施例中,组合物进一步包括一种或多种其它生物活性剂(例如蛋白酶、受体酪胺酸激酶和/或清除受体npr-c的抑制剂)。
[0269]
本公开提供包括如本文所描述的共轭部分的缓释组合物。缓释组合物包含在施用后延迟递送药物(延迟释放剂量)或持续延长时间段递送药物(延释剂量)的那些组合物。本文所提供的cnp肽共轭物的各种实施例包含缓释组合物,如延释、持续或受控释放,和延迟释放。术语“延释组合物”是指以便于制备在施用后的延长时间段内可用的活性成分/药物的方式配制的组合物(美国药典(us pharmacopeia))。延释剂量包含持续释放(sr)或受控释放(cr)形式。持续释放经持续时间段维持药物释放,但未必以恒定速率,而cr经持续时间段以几乎恒定速率维持药物释放(《制药学:药物递送和靶向(pharmaceutics:drug delivery and targeting)》,yvonne perrie,thomas rades,医药出版社(pharmaceutical press),2009)。延迟释放组合物或产物经修改以在初次施用之后的一定时间段内延迟药物物质的释放。
[0270]
在各种实施例中,缓释组合物为延释组合物。
[0271]
在各种实施例中,对于延释组合物,在ph 7至7.6下,(i)第1天释放小于约20%的肽;和(ii)每周释放约90%的肽,或每两周释放约90%的肽,或每月释放约90%的肽。
[0272]
在各种实施例中,在ph 7至7.6下,第1天释放小于约20%的肽。在各种实施例中,在ph 7至7.6下,第1天释放小于约10%的肽。经进一步考虑(i)在ph 7.0至7.6下,第1天释放小于约30%、或约40%、或约50%的肽;和(ii)在ph 7至7.6下,每周释放约90%的肽,或每两周释放约90%的肽,或每月释放约90%的肽。经进一步考虑(i)在ph 7.0至7.6下,第1天释放小于约30%、或约40%、或约50%、或约60%的肽;和(ii)在ph 7至7.6下,每周释放约70%、约80%或约90%的肽;或每两周释放约70%、约80%或约90%的肽;或每三周释放约70%、约80%或约90%的肽;或每月释放约70%、约80%或约90%的肽。在各种实施例中,在ph 7至7.6下,每周释放约90%的肽。在各种实施例中,在ph 7至7.6下,每两周释放约90%的肽。在各种实施例中,在ph 7至7.6下,每月释放约90%的肽。经进一步考虑所述释放可在ph 7.0至7.6、ph 7.1至7.5、ph 7.2至7.4、ph 7.2至7.6或ph 7.0至7.4的ph下。
[0273]
在各种实施例中,(i)在ph 7.0至7.6下,第1天释放小于约25%、约30%、约35%、约40%、约45%、约50%、约55%、约60%、约65%、约70%或约75%的肽;和(ii)在ph 7至7.6下,每周释放约90%的肽、或每两周释放约90%的肽、或每月释放约90%的肽。经进一步考虑(i)在ph 7.0至7.6下,第1天释放小于约25%、约30%、约35%、约40%、约45%、约50%、约55%、约60%、约65%、约70%或约75%的肽;和(ii)在ph 7至7.6下,每周释放约70%、约80%或约90%的肽;或每两周释放约70%、约80%或约90%的肽;或每三周释放约70%、约80%或约90%的肽;或每月释放约70%、约80%或约90%的肽;或可替代地ii)在ph 7至7.6下,每周释放约70%、约75%、约80%、约85%或约90%的肽;或每两周释放约70%、约75%、约80%、约85%或约90%的肽;或每三周释放约70%、约75%、约80%、约85%或约90%的肽;或每月释放约70%、约75%、约80%、约85%或约90%的肽。
[0274]
在各种实施例中,组合物包括赋形剂、稀释剂或载剂。在各种实施例中,延释组合物包括赋形剂、稀释剂或载剂。在各种实施例中,赋形剂、稀释剂或载剂为药学上可接受的赋形剂、稀释剂或载剂。
[0275]
赋形剂、载剂和稀释剂的非限制性实例包含媒剂、液体、缓冲剂、等张剂、添加剂、稳定剂、防腐剂、增溶剂、表面活性剂、乳化剂、润湿剂、佐剂等。组合物可含有液体(例如水、乙醇);多种缓冲液内容物(例如tris-hcl、磷酸盐、乙酸盐缓冲液、柠檬酸盐缓冲液)的稀释剂、ph和离子强度;清洁剂和增溶剂(例如聚山梨醇酯20、聚山梨醇酯80);抗氧化剂(例如甲硫氨酸、抗坏血酸、偏亚硫酸氢钠);防腐剂(例如硫柳汞(thimerosol)、苯甲醇、间甲酚);以及膨化物质(例如乳糖、甘露糖醇、蔗糖)。在药物组合物的配制中使用的赋形剂、稀释剂和载剂为本领域中已知的;参见例如《雷明顿氏药物科学(remington's pharmaceutical sciences)》,第18版,第1435-1712页,马克出版公司(mack publishing co.)(easton,pennsylvania(1990)),其以全文引用的方式并入本文中。
[0276]
举例来说,载剂包含(但不限于)稀释剂、媒剂和佐剂,以及植入物载剂,和惰性、无毒固体或液体填充剂和囊封材料,其不与一种或多种活性成分反应。载剂的非限制性实例包含磷酸盐缓冲盐水、生理盐水、水以及乳液(例如油/水乳液)。载剂可为含有例如乙醇、多元醇(例如甘油、丙二醇、液体聚乙二醇和其类似者)、植物油和其混合物的溶剂或分散介质。
[0277]
在一些实施例中,组合物为液体配制物。在某些实施例中,配制物包括浓度在约0.1mg/ml至约20mg/ml、或约0.5mg/ml至约20mg/ml、或约1mg/ml至约20mg/ml、或约0.1mg/ml至约10mg/ml、或约0.5mg/ml至约10mg/ml、或约0.5至5mg/ml、或约0.5至3mg/ml、或约1mg/ml至约10mg/ml范围内的cnp变体。在各种实施例中,cnp变体的浓度为0.8mg/ml至2mg/ml。在各种实施例中,cnp变体的浓度为0.8mg/ml。在各种实施例中,cnp变体的浓度为2.0mg/ml。在各种实施例中,cnp变体由冻干粉复原。
[0278]
在其它实施例中,组合物包括缓冲溶液或缓冲剂以将含有cnp的溶液或悬浮液的ph维持在所要范围内。缓冲溶液的非限制性实例包含磷酸盐缓冲盐水、tris缓冲盐水和汉克氏缓冲盐水(hank's buffered saline)。缓冲剂包含(但不限于)乙酸钠、磷酸钠和柠檬酸钠。还可使用缓冲剂的混合物。在某些实施例中,缓冲剂为乙酸/乙酸盐或柠檬酸/柠檬酸盐。组合物中适合的缓冲剂的量部分取决于所使用的特定缓冲剂以及溶液或悬浮液的所要ph。在一些实施例中,缓冲剂的浓度为约10mm
±
5mm。在某些实施例中,组合物的ph为约ph 3至约ph 9、或约ph 3至约ph 7.5、或约ph 3.5至约ph 7、或约ph 3.5至约ph 6.5、或约ph 4至约ph 6、或约ph 4至约ph 5,或为约ph 5.0
±
1.0。在各种实施例中,ph为约5.0、5.1、5.2、5.3、5.4、5.5、5.6、5.7、5.8、5.9或6.0。在各种实施例中,ph为5.5。
[0279]
在其它实施例中,组合物含有等张调节剂以使溶液或悬浮液等张且与施用更相容。等张剂的非限制性实例包含nacl、右旋糖、葡萄糖、甘油、山梨糖醇、木糖醇和乙醇。在某些实施例中,等张剂为nacl。在某些实施例中,nacl的浓度为约160
±
20mm、或约140mm
±
20mm、或约120
±
20mm、或约100mm
±
20mm、或约80mm
±
20mm、或约60mm
±
20mm。
[0280]
在又其它实施例中,组合物包括防腐剂。防腐剂包含(但不限于)间甲酚和苯甲醇。在某些实施例中,防腐剂的浓度为约0.4%
±
0.2%、或约1%
±
0.5%、或约1.5%
±
0.5%、或约2.0%
±
0.5%。
[0281]
在再其它实施例中,组合物含有抗吸附剂(例如,用以减少cnp变体吸附至玻璃或塑料)。抗吸附剂包含(但不限于)苯甲醇、聚山梨醇酯20和聚山梨醇酯80。在某些实施例中,抗吸附剂的浓度为约0.001%至约0.5%、或约0.01%至约0.5%、或约0.1%至约1%、或约0.5%至约1%、或约0.5%至约1.5%、或约0.5%至约2%、或约1%至约2%。
[0282]
在其它实施例中,组合物包括稳定剂。稳定剂的非限制性实例包含甘油、丙三醇、硫甘油、甲硫氨酸以及抗坏血酸和其盐。在一些实施例中,当稳定剂为硫甘油或抗坏血酸或其盐时,稳定剂浓度为约0.1%至约1%。在其它实施例中,当稳定剂为甲硫氨酸时,稳定剂的浓度为约0.01%至约0.5%、或约0.01%至约0.2%。在再其它实施例中,当稳定剂为甘油时,稳定剂的浓度为约5%至约100%(纯)。
[0283]
在其它实施例中,组合物含有抗氧化剂。示例性抗氧化剂包含(但不限于)甲硫氨酸和抗坏血酸。在某些实施例中,抗氧化剂与cnp的摩尔比为约0.1:1至约15:1、或约1:1至约15:1、或约0.5:1至约10:1、或约1:1至约10:1或约3:1至约10:1。
[0284]
药学上可接受的盐可用于组合物中,包含(但不限于)无机酸盐(例如盐酸盐、氢溴酸盐、磷酸盐、硫酸盐)、有机酸盐(例如乙酸盐、丙酸盐、丙二酸盐、苯甲酸盐、甲磺酸盐、甲苯磺酸盐)和胺(例如异丙胺、三甲胺、二环己胺、二乙醇胺)盐。药学上可接受的盐的充分论述见于《雷明顿氏医药科学》,第18版,马克出版公司,(easton,pennsylvania(1990))中。
[0285]
药物组合物可以各种形式施用,如片剂、胶囊、颗粒、散剂、溶液、悬浮液、乳液、软膏和经皮贴片。组合物的剂型可调适为组合物的所要施用模式。对于经口施用,组合物可采取例如片剂或胶囊(包含软凝胶胶囊)的形式,或可为例如水性或非水性溶液、悬浮液或糖浆。用于经口施用的片剂和胶囊可包含一种或多种常用赋形剂、稀释剂和载剂,如甘露糖醇、乳糖、葡萄糖、蔗糖、淀粉、玉米淀粉、糖精钠、滑石、纤维素、碳酸镁和润滑剂(例如硬脂酸镁、硬脂酰反丁烯二酸钠)。必要时,可将调味剂、着色剂和/或甜味剂添加至固体和液体配制物。用于口服配制物的其它任选的成分包含(但不限于)防腐剂、悬浮剂和增稠剂。口服配制物还可具有肠溶衣以保护cnp变体免受胃的酸性环境侵害。制备固体和液体剂型的方法为已知的,或将为本领域技术人员显而易见的(参见例如上文引用的《雷明顿氏医药科学》)。
[0286]
用于非经肠施用的配制物可制备为例如液体溶液或悬浮液形式、适于在注射之前溶解或悬浮于液体介质中的固体形式或乳液形式。举例来说,无菌可注射溶液和悬浮液可根据本领域中已知的技术使用适合的稀释剂、载剂、溶剂(例如缓冲水溶液、林格氏溶液(ringer's solution)、等张氯化钠溶液)、分散剂、润湿剂、乳化剂、悬浮剂和其类似者配制。另外,可使用无菌不挥发性油、脂肪酯、多元醇和/或其它非活性成分。作为其它实例,用于非经肠施用的配制物包含可含有抗氧化剂、缓冲剂、抑菌剂和使配制物与预期接受者血液等张的溶质的水性无菌注射溶液;以及可含有悬浮剂和增稠剂的水性和非水性无菌悬浮液。
[0287]
包括cnp变体的组合物还可为冻干配制物。在某些实施例中,冻干配制物包括缓冲剂和膨化剂,以及任选的抗氧化剂。示例性缓冲液包含(但不限于)乙酸盐缓冲液和柠檬酸盐缓冲液。示例性膨化剂包含(但不限于)甘露糖醇、蔗糖、聚葡萄糖、乳糖、海藻糖和聚维酮(pvp k24)。在某些实施例中,甘露糖醇的量为约3%至约10%、或约4%至约8%、或约4%至约6%。在某些实施例中,蔗糖的量为约6%至约20%、或约6%至约15%、或约8%至约12%。
示例性抗氧化剂包含(但不限于)甲硫氨酸和抗坏血酸。
[0288]
在各种实施例中,配制物包括柠檬酸、柠檬酸钠、海藻糖、甘露糖醇、甲硫氨酸、聚山梨醇酯80和任选的注射用无菌水(wfi)。
[0289]
本公开还提供试剂盒,其含有例如瓶子、小瓶、安瓿、试管、套筒和/或注射器,其包括液体(例如无菌可注射)配制物或固体(例如冻干)配制物。试剂盒还可含有药学上可接受的媒剂或载剂(例如溶剂、溶液和/或缓冲液),其用于将固体(例如冻干)配制物复原为溶液或悬浮液以用于施用(例如通过注射),包含(但不限于)复原注射器中的冻干配制物以用于注射或将浓缩物稀释至较低浓度。此外,即用型注射溶液和悬浮液可从例如包括含有cnp的组合物的无菌粉末、颗粒或片剂制备。试剂盒还可包含施配装置(如喷雾或注射施配装置)、笔式喷射器、自喷射器、无针喷射器、注射器和/或针。
[0290]
作为非限制性实例,试剂盒可包含具有单腔室或双腔室的注射器。对于单腔室注射器,所述单腔室可含有准备好进行注射的液体cnp配制物,或固体(例如冻干)cnp配制物或cnp变体于相对较小量的适合的溶剂系统(例如甘油)中的液体配制物,其可复原为注射用溶液或悬浮液。对于双腔室注射器,一个腔室可含有药学上可接受的媒剂或载剂(例如溶剂系统、溶液或缓冲液),且另一腔室可含有固体(例如冻干)cnp配制物或cnp变体于相对较小量的适合的溶剂系统(例如甘油)中的液体配制物,其可使用来自第一腔室的媒剂或载剂复原为注射用溶液或悬浮液。
[0291]
作为另一实例,试剂盒可包含一个或多个笔式喷射器或自动喷射器装置,和双腔室药筒。药筒的一个腔室可含有药学上可接受的媒剂或载剂(例如溶剂系统、溶液或缓冲液),且另一腔室可含有固体(例如冻干)cnp配制物或cnp变体于相对较小量的适合的溶剂系统(例如甘油)中的液体配制物,其可使用来自第一腔室的媒剂或载剂复原为注射用溶液或悬浮液。药筒可包括足以在所要时间段(例如2天、3天、1周、2周、3周、4周等)内给药的量的cnp变体。笔式喷射器或自动喷射器可经调节以施用所要量的来自药筒的cnp配制物。
[0292]
施用和给药
[0293]
cnp变体或包括其的药物组合物或配制物可以不同方式向个体施用,如皮下、关节内、腹膜内、肌肉内、皮内或经口。在一个实施例中,每日一次、每周一次、每两周一次、每三周一次、每4周一次、每6周一次、每两个月一次、每三个月一次或每六个月一次地施用cnp变体组合物。
[0294]
cnp变体或其组合物还可通过在目标作用部位(例如异常或退化的关节或软骨区域)植入药物储槽来施用。可替代地,cnp变体可通过经皮递送(例如通过皮肤上的贴片)在舌下(例如舌下片剂)以舌下方式施用,或以微球、微胶囊、脂质体(不带电或带电(例如阳离子))、聚合微粒(例如聚酰胺、聚丙交酯、聚乙交酯、聚(丙交酯-乙交酯)、微乳液和其类似形式经口施用。
[0295]
本文所描述的cnp变体组合物可以治疗有效剂量向有需要的患者施用,以治疗、改善或预防骨相关病症(例如骨胳发育不良,包含软骨发育不全)。cnp变体的安全性和治疗功效可通过细胞培养物或实验动物中的标准药理学程序测定,如通过测定ld
50
(对于50%的群体致死性的剂量)和ed
50
(在50%的群体中治疗有效的剂量)。毒性作用与治疗作用之间的剂量比为治疗指数且其可以比率ld
50
/ed
50
表示。展现较大治疗指数的活性剂通常是优选的。
[0296]
在某些实施例中,本文所描述的cnp变体组合物以在约3、4、5、6、7、8、9或10nmol/
kg至约300nmol/kg,或约20nmol/kg至约200nmol/kg范围内的剂量施用。在一些实施例中,cnp组合物以约3、4、5、6、7、8、9、10、15、20、25、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100、110、120、125、130、140、150、160、170、175、180、190、200、210、220、230、240、250、260、270、280、290、300、350、400、450、500、750、1000、1250、1500、1750或2000nmol/kg或由治疗医师认为适当的其它剂量施用。在其它实施例中,cnp变体组合物以约3、4、5、6、7、8、9、10、15、20、25、30、40、50、60、70、80、90、100、110、120、130、140、150、160、170、180、190、200、250、300、350、400、450、500、550、600、650、700、750、800、850、900、950或1000μg/kg,或约0.5、0.8、1.0、1.25、1.5、2、2.5、3、3.5、4、4.5、5、5.5、6、6.5、7、7.5、8、8.5、9、9.5或10mg/kg,或由治疗医师认为适当的其它剂量施用。本文所描述的cnp或cnp变体的剂量可根据本文所描述的给药频率/施用频率施用,包含(但不限于)每日一次、每周2次或3次、每周一次、每2周一次、每3周一次、每月一次等。在各种实施例中,cnp或cnp变体每日皮下施用。在各种实施例中,cnp或cnp变体每周皮下施用。在各种实施例中,cnp变体以2.5μg/kg/天至60μg/kg/天、10μg/kg/天至45μg/kg/天或15μg/kg/天至30μg/kg/day的剂量施用。在各种实施例中,cnp变体以15μg/kg/天的剂量施用。在各种实施例中,cnp变体以30μg/kg/天的剂量施用。
[0297]
针对特定个体的cnp变体的给药/施用频率可视多种因素而变化,包含所治疗病症和病状和个体对疗法的反应。cnp变体可以每次给药单次剂量或多次剂量施用。在某些实施例中,如下地施用cnp变体组合物:以单次剂量或多次剂量,每日一次、每周一次、每两周一次、每三周一次、每4周一次、每6周一次、每两个月一次、每三个月一次或每六个月一次,或以由治疗医师认为适当的频率。在各种实施例中,持续3个月、6个月、12个月或更久施用cnp变体。
[0298]
在一些实施例中,施用cnp变体组合物以允许生长期(例如软骨生成),接着为恢复期(例如成骨)。举例来说,cnp组合物可皮下或通过另一模式每日或每周多次地施用一段时间,接着为无治疗期,随后重复所述周期。在一些实施例中,初始治疗期(例如每日施用或每周多次施用cnp变体组合物)持续3天、1周、2周、3周、4周、5周、6周、7周、8周、9周、10周、11周或12周。在一相关实施例中,无治疗期持续3天、1周、2周、3周或4周。在某些实施例中,cnp变体组合物的给药方案为每日一次持续3日,接着停药3日;或每日一次或每周多次持续1周,接着停药3天或1周;或每日一次或每周多次持续2周,接着停药1或2周;或每日一次或每周多次持续3周,接着停药1、2或3周;或每日一次或每周多次持续4、5、6、7、8、9、10、11或12周,接着停药1、2、3或4周。
[0299]
生物标记
[0300]
为了治疗骨相关病症,可测量生长指标,如子宫内和新生儿的长骨生长测量,和测量骨生长生物标记,如cnp、cgmp、胶原蛋白ii、胶原蛋白x、骨钙化素和增殖细胞核抗原(pcna)。
[0301]
一种cnp信号传导标记为cgmp(3',5'环状单磷酸鸟苷)。此胞内信号传导分子的含量在与cnp结合和活化其同源受体npr-b之后增加。升高的cgmp含量可在cnp暴露之后从细胞培养提取物(体外)、来自cnp暴露之后的骨外植研究的经调节的培养基(离体)和在皮下、静脉内或经由本领域中已知的其它施用途径施用cnp几分钟内的血浆内(体内)测量。
[0302]
还可测量软骨和骨特异性分析物(或软骨和骨相关标记)以评估cnp功效。举例来
说,裂解的ii型胶原蛋白的片段为软骨更新的软骨特异性标记。ii型胶原蛋白为软骨的主要有机成分且ii型胶原蛋白的片段(裂解的胶原蛋白)释放至循环中,且随后在软骨更新后分泌至尿液中。软骨更新先于新骨形成。
[0303]
可测量的骨形成的骨特异性生物标记为i型原胶原(pinp)的n端前肽。i型胶原蛋白的合成为骨形成中的重要步骤,因为i型胶原蛋白是骨基质中的主要有机组分。在胶原蛋白合成期间,前肽从原胶原分子释放且可在血清中检测到。另外,i型胶原蛋白的片段可测量为骨再吸收的标记。
[0304]
软骨和骨形成和生长的其它潜在生物标记包含聚集蛋白聚糖硫酸软骨素(软骨更新的软骨特异性标记)、ii型胶原蛋白的前肽(软骨形成的软骨特异性标记)、i型胶原蛋白c端肽(ctx)、碱性磷酸酶(骨特异性)和骨钙化素(骨形成的骨特异性标记)。软骨和骨相关生物标记可使用市售试剂盒例如在来自功效/药效学体内研究,和来自离体研究的经调节的培养基的血清中测量。
[0305]
在一个实施例中,在已施用本文所描述的cnp变体或组合物的个体中分析或测量至少一种骨相关或软骨相关的生物标记的含量,以便监测cnp组合物对体内骨和软骨形成和生长的作用。举例来说,至少一种骨相关或软骨相关的生物标记的含量增加可指示施用cnp变体或组合物对骨生长具有积极作用,且适用于治疗骨胳发育不良和与cnp活性降低相关的其它骨相关或软骨相关的疾病或病症。示例性骨相关或软骨相关的生物标记包含(但不限于)cnp(例如cnp的内源性含量)、cgmp、ii型胶原蛋白和其片段的前肽、ii型胶原蛋白和其片段、i型胶原蛋白c端肽(ctx)、骨钙化素、增殖细胞核抗原(pcna)、i型原胶原的前肽(pinp)和其片段的前肽、i型胶原蛋白和其片段、聚集蛋白聚糖硫酸软骨素和碱性磷酸酶。
[0306]
在各种实施例中,通过从将施用、正施用或已施用cnp变体的个体获得生物样品来测量生物标记。可使用本领域中已知的技术测量生物标记,包含(但不限于)蛋白质印迹(western blot)、酶联免疫吸附分析(enzyme linked immunosorbant assay;elisa)和酶活性分析。生物样品可为血液、血清、尿液或其它生物流体。
[0307]
本公开的额外方面和细节将从以下实例显而易知,所述实例旨在说明性而非限制性的。
[0308]
实例
[0309]
实例1:cnp变体的合成
[0310]
cnp变异肽使用将在symphony/prelude(protein technologies inc.,美国)、voyager(cem gmbh,德国)或syroii(multisyntech,德国)合成器上留下c端cooh的树脂在固相上合成。
[0311]
侧链官能团经n-t-boc(kw)、n-trt(hnq)、s-trt(c)或n-pbf(r)基团保护的所有fmoc-氨基酸均购自biosolve(荷兰)或bachem gmbh(德国)。对于每个氨基酸偶合步骤,在nmp中使用5倍过量的hbtu/hobt/氨基酸/dipea(1:1:1:2),其中采用使用双偶合的20分钟活化时间。
[0312]
肽的乙酰化(ac)通过使树脂与nmp/ac2o/diea(10:1:0.1,v/v/v)在室温下反应30分钟来进行。
[0313]
对于部分的共轭,赖氨酸上的保护性氨基经裂解以产生反应性基团。标准fmoc合成用于使2
×
fmoc-氨基peg(2)反应,接着与谷氨酸反应,接着与c18-二酸反应。
[0314]
在室温下,通过与tfa(40ml/mmol树脂)反应2小时使完整肽从树脂裂解。过滤粗肽,用冰冷的et2o沈淀,接着冻干且最终通过制备型逆相高效液相色谱(rp-hplc)纯化。最终产物和纯度通过质谱分析确认。
[0315]
cnp变体是基于pro-gly cnp-37
[0316]
(pgqehpnarkykgankkglskgcfglkldrigsmsglgc(seq id no:1))的序列产生,任选地具有不同氨基酸残基的变化和/或n端的乙酰化,和/或其它修饰,且包含(以下加下划线的氨基酸变化):
[0317]
cnp-8:ac-pgqehpqarryrgaqrrglsrgcfglkldrigsmsglgc-oh(seq id no:8),
[0318]
cnp-5:ac-pgqehpnarkykgankkglskgcfglkldrigsmsglgc-nh2(seq id no:9),
[0319]
cnp-6:ac-pgqehpnarryrganrrglsrgcfglkldrigsmsglgc-oh(seq id no:10),
[0320]
cnp-7:ac-pgqehpnarryrganrrglsrgcfglkldrigsmsglgc-nh2(seq id no:11)、cnp-9:ac-pgqehpqarryrgaqrrglsrgcfglkldrigsmsglgc-nh2(seq id no:12),
[0321]
ac-pgqehpqarryrgaqrrglsrgcfglk(aeea-aeea-γglu-c18da)ldrigsmsglgc-oh(seq id no:8)以及
[0322]
pgqehpqarkykgaqkkglskgcfglkldrigsmsglgc-oh(seq id no:7)。
[0323]
将完全还原的肽溶解于具有或不具有盐酸胍的0.1m tris-缓冲液(ph 8.0)中且在室温下搅拌,所述缓冲液以0.1mg/ml的最终浓度含有1mm半胱氨酸(ss-形式)和8mm半胱氨酸(sh-形式)。通过hplc-分析监测二硫化物形成,直至不再观测到进一步的峰值变化。将混合物装载于制备型rp-hplc上以进行纯化。
[0324]
实例2:合成的cnp变体的表征
[0325]
通过质谱分析和uv光谱法来分析如实例1中所合成的cnp变体,以确定10天后的纯度和稳定性。
[0326]
稳定性使用历经时间t0至t10的rp-hplc纯度分析来测量。简而言之,将cnp变体在以下缓冲液中以1:5稀释:5mm柠檬酸盐、6%蔗糖、1.5%甘露糖醇、0.7mg/ml甲硫氨酸和0.005%tween80,ph 5.6,将10μl的注射体积注入phenomenex aeris xb-c18 rp柱(2μm,100a,2.1
×
250mm;p/n 00g-4505-an)hplc条件为:流动相a:h2o/0.05%tfa,ph 3w/nh4oh(最终约3mm),流动相b:70%ch3cn于h2o/0.05%tfa中,ph 3w/nh4oh(最终约3mm)和0.25ml/分钟的流动速率。测量是用55℃的柱温度和uv:214nm(bw 4nm);ref 360nm(bw 20nm),uv:280nm(bw 4nm);ref 360nm(bw 20nm)进行。cnp变体在pbs(ph 7.4)中在37℃下保持10天且获得稳定性测量结果。稳定性测量的结果在以下表1中展示为在t0(0天)或t10(10天)所检测的变体%。
[0327]
表1
[0328]
肽t0,%t10,%ec50,t0,nmpro-gly cnp3776.739.51.7cnp-583473cnp-690580.4cnp-777532.1cnp-891880.2cnp-992770.9
[0329]
cnp变体通过cgmp刺激分析使用catchpoint cyclic-gmp荧光分析主体试剂盒(fluorescent assay bulk kit)(molecular devices,r8075)来测试活性。简而言之,将nih3t3细胞(atcc,crl-1658)和hek293细胞以每孔60,000个细胞接种于96孔板(96孔黑色成像板,grenier,#655090)中。培养基为如下:nih3t3培养基:dmem高葡萄糖,丙酮酸盐(thermo,11995-073) 10%fbs 1
×
pen strep(缩写为p/s,thermo,目录号15140122)。nih3t3为cgmp分析hek293培养基的对照系统:emem 10%fbs 1
×
p/s 1
×
gmax。无血清nih3t3培养基:dmem 1
×
p/s,用于以ibmx(cas 28822-58-4)处理细胞;含bsa的无血清nih3t3培养基:dmem 1
×
p/s 0.5mg/ml bsa(thermo,a9418-100g),用于以cnp处理细胞。
[0330]
细胞在37℃、5%co2下培育24小时。对于用cnp变体处理的细胞,板在使用之前15分钟用ibmx(enzo life sciences,89161-340,1g)预处理。ibmx为磷酸二酯酶的强效、非特异性抑制剂。ibmx的800mm储备溶液在ibmx稀释培养基(无血清培养基(dmem 1
×
pbs与1
×
pbs 1:1混合)中稀释为0.75mm工作储备液。
[0331]
cnp变体如下制备:在cnp稀释培养基(dmem 1
×
p/s 0.5mg/ml bsa)中以1:1000稀释10mg/ml cnp溶液。进一步稀释此溶液以获得cnp起始溶液,其以100nm cnp/孔涂铺。此100nm cnp溶液进一步以1:5连续稀释六份稀释液,以获得0.0064nm cnp/孔的下端浓度。此提供用于分析的7点剂量曲线。
[0332]
对于细胞处理,从培育箱移除细胞,从细胞和用ibmx处理的细胞移除生长培养基。将80μl 0.75mm ibmx添加至各孔中且将细胞返回至37℃培育箱中15分钟。在15分钟之后,将cnp(40μl/孔)添加至各测试孔且将细胞返回至37℃培育箱中15分钟。通过轻敲混合所述板。使板在solentim细胞度量上成像以使细胞可视化,并且确定是否有任何细胞上浮且随后将其放回37℃培育箱中。
[0333]
终止反应且通过添加40μl溶解缓冲液(来自cgmp试剂盒)使细胞溶解。将板置于振荡器上5分钟以完全溶解。细胞溶解物用于cgmp分析。
[0334]
使用根据制造商方案制备的cgmp校准剂、兔抗cgmp抗体和hrp-cgmp进行cgmp分析。将40μl校准剂添加至涂有抗cgmp抗体的板的孔中,且将40μl待分析的溶解物添加至适当孔中。将40μl经复原的兔抗cgmp抗体添加至所有孔中,且将板置放于振荡器上五分钟以进行混合。将40μl经复原的hrp-cgmp添加至各孔中且在室温下培育2小时。将板手动抽吸且用300μl洗涤缓冲液洗涤4次。将100μl信号灯红色底物添加至各孔中,所述板被覆盖且在室温下避光保持至少10分钟。在spectramax m或类似仪器上,在530nm激发和590nm发射下读取板的荧光强度。
[0335]
表1展示cnp变体刺激cgmp产生,表明本文所描述的稳定变体适用作治疗骨相关病症的治疗剂。
[0336]
实例2a:cnp变体或共轭物于血浆中的稳定性
[0337]
历经24小时时间段测试不同cnp变体或cnp共轭物在人类血浆中的稳定性。简而言之,c18脂肪酸使用2个oeg间隔子与γ谷氨酸稠合(参见例如lau等人,《药物化学杂志(j.med.chem)》58:7370-7380,2015)。对于色谱,waters uplc h-class与beh c18 1.7μm,2.1
×
150mm连接;移动相a:1%dmso 0.1%甲酸/水;移动相b:1%dmso 0.1%甲酸/can。使用ab sciex qtrap进行质谱。
[0338]
在人类血浆li肝素中以200nm制备各cnp变体且在37℃5%co2下培育样品。反应物
在0、1、2、4、8、24小时用0.5m柠檬酸钠ph 4淬灭。血浆蛋白质用含0.2%甲酸的meoh沉淀,且样品使用wcx 96孔uelution板制备且通过lc-ms/ms 6500进行分析。
[0339]
变体cnp-r是指cnp37变体,其中环部分中不存在的k残基改变为r残基,且cnp q/r是指cnp37变体,其中n残基改变为q且环部分中不存在的k残基改变为r。
[0340]
图1说明具有不同连接子结构的cnp共轭物。
[0341]
图2展示与血浆中的聚乙二醇化或非共轭肽相比,脂化共轭物在血浆中的稳定性经改良。
[0342]
还在不同条件下分析不同共轭物的稳定性。简而言之,在37℃(对照)、37℃ 0.5m nacl、37℃ 蛋白酶抑制剂或4℃下使用与上文相同的方案。图3展示pg-cnp37和变体易于在人类血浆中蛋白水解,且pg-cnp37展示与其它变体相比更大的稳定性。
[0343]
实例3:异型接合npr2突变对cnp处理有反应
[0344]
为了确定cnp对患有由npr2突变引起的身材矮小的个体的效应,开发npr2突变的细胞模型。所分析的示例性npr2突变阐述于图6中。具有npr2基因敲除或所述基因中的异型接合功能丧失突变的大鼠软骨肉瘤(rat chondrosarcoma;rcs)细胞通过使用125ng npr2变体将rnp转染至rcs细胞中或转染至rcs或hek293细胞中的野生型npr2质体dna制得。单细胞克隆经接种且通过桑格测序(sanger sequencing)进行基因分型。细胞模型能够再现公布的不同突变的cgmp表型。
[0345]
通过在rcs细胞中的npr2的第一外显子中产生插入和缺失而产生npr2克隆。npr2中第一外显子的序列通过下一代测序确认,且阐述于图5中。通过在用6nm pro-gly cnp37处理后,使用catchpoint cyclic-gmp荧光分析进行cgmp刺激分析来测试npr2突变细胞回应于cnp施用的活性。将大鼠软骨肉瘤(rcs)细胞以每孔40,000个细胞接种于rcs培养基中:dmem 10%fbs 1
×
pen strep。图4展示添加外源性pro-gly-cnp37变体拯救npr2 /-大鼠软骨肉瘤细胞模型的cgmp读数。
[0346]
前述活化数据报告cgmp ec50在40至360nm范围内,用于活化prkg2(campbell等人,《acs化学生物学(acs chem biol)》12,2388-2398,2017);vaandrager等人,《生物化学杂志(j biol chem)》272,11816-23,1997);pohler等人,《欧洲生物化学协会联合会快报(febs lett)》374,419-25,1995)。在异型接合npr2基因敲除细胞中,》0.163nm的cnp剂量能够达成超出prkg2活化cgmp的ec50范围的细胞内浓度(图4)。而在野生型细胞中,0.040nm的cnp剂量能够达成相同的cgmp浓度。这些结果表明cnp补充可达成prkg2活化和在具有npr2功能损失型突变的细胞生长所需的cgmp含量。
[0347]
这些结果还表明施用cnp变体适用于使患有npr2活性降低的身材矮小的个体恢复骨生长。经进一步考虑用cnp变体治疗将对在cgmp信号传导可受损的其它生长板基因中具有突变的个体有益。
[0348]
实例4:与身材矮小相关的突变的鉴别
[0349]
假设展示基因驱动的双向效应的明确证据的基因更可能代表可在广泛患者群体中有效调节的治疗目标。为了鉴别为生长的核心调节因子的基因,分析了五个基因列表的交集,包含来自全基因组关联研究(genome-wide association study;gwas)的基因列表。核心生长调节因子将最可能含有具有双向效应(即,身材矮小或骨胳发育不良和身材高大或过生长)的稀有编码突变。
[0350]
查询的数据库包含:gwas,提取了由使用约700,000个个体的大型gwas身高综合分析报告的3,290个独立遗传变体中的每一者的2,067个非重复最近基因;hgmd,查询来自hgmd版本v2019_2的“allmut”表以寻找标记为“dm”的在相同基因中具有“身材矮小”和“身材高大或过生长”的所有致病变体;omim,先前描述了与生长病症相关的omim基因的列表且使用以下关键词创建:身材矮小、过生长、骨胳发育不良、短指症。
[0351]
首先,关于与身材矮小或身材高大相关的基因查询人类基因突变数据库(hgmd版本v2019_2)(stenson等人,《人类遗传学(hum genet)》136:665-677,2017)。文献中报告了47种标注有至少一种致病变体的基因,其引起“身材矮小”。仅20种基因被标注为身材高大或过生长基因。第二,使用258个omim基因(248个矮小、20个高大)的手动策划列表,其使用以下关键词创建:身材矮小、过生长、骨胳发育不良、短指症(wood等人,《自然遗传学(nat genet)》46:1173-86,2014)。第三,将这些列表的交集与来自gwas的基因列表进行比较。在这些列表的交集处,存在三种已知与身高相关的基因(igf1r、nppc、npr2),且鉴别出两种额外基因(fgfr3、shox)。
[0352]
额外分析使得产生一组新的五个核心基因,其展示显著降低的身高(β=-0.20,95%ci[-0.26至-0.14],p=4.04
×
10-11)和显著提高的特发性身材矮小(iss)风险(or=2.75,95%ci[1.92-3.96]。五个核心基因(fgfr3、igf1r、nppc、npr2和shox)中的每一个在单独考虑时与身高相关,且在与其它突变组合使用时还与身材矮小相关。fgfr3、igf1r、nppc、npr2和shox的示例性突变阐述于图7中。
[0353]
npr2和igf1r中的组合功能丧失(loss of function;lof)和误义变体还与iss风险增加相关(分别为or=3.31,p=0.001,or=2.85,p=0.002)。已在具有不同严重程度的家族性身材矮小中报告shox、igf1r、nppc、npr2中引起蛋白质功能丧失的整体基因缺失和/或突变。
[0354]
分析展示五个核心基因中的任一者的变体携带者的iss风险增加大致3倍,且占总iss群体的6.7%。此外,表明添加外源性cnp之后,npr2单倍剂量不足的细胞模型中npr2信号传导的剂量依赖性拯救。
[0355]
根据全基因模型(liu等人,《细胞(cell)》177:1022-1034e6(2019);boyle等人,《细胞》169:1177-1186(2017)),如果这些基因为核心人类生长基因,则其效应应通过驱动调节网路的多个较弱的常见遗传变体调节。为了间接测试此假设,使用针对身高的公布的最大gwas综合分析计算身高的多基因风险评分(prs),所述综合分析不包含来自uk生物库项目的任何样品。将群组分为五个相等大小的(n=6,824)prs五分位数(prs 1为最矮身高,prs 5为最高身高)。prs评分增加与平均身高之间存在剂量依赖性关系(各prs五分位数增加的β=0.30)(图8a)。跨越五个不同prs背景,五个核心基因中lof变体的携带者始终比非携带者矮。参见图8。数据表明prs和稀有蛋白质变体的组合效应与加法模型一致:多基因效应调节携带者和非携带者的身高。
[0356]
使用prs=3作为参考来计算跨越prs组的iss风险。最低prs组与iss风险提高相关,且最高prs组与风险降低相关(对于prs 1和prs 5分别为or=5.43,p=8.58
×
10-34;or=0.22,p=4.49
×
10-7)。评估五个核心基因的稀有编码变体对由prs组分层的iss的效应。在前三个五分位数中,五个核心基因中的任一者的携带者患iss的风险增加(or=2.64,p=3.09
×
10-5;or=2.17,p=0.04;or=5.29,p=1.58
×
10-5;or=2.72,p=0.09,图8c-f)。
对于各个别核心基因的携带者,观测到由prs分层的iss风险的一致效应方向(图8c-f)。
[0357]
此外,主要来自多个具有个别小效应的常见遗传变异的prs的累加效应预测数据集中20.1%的身高差异。prs的这些累加效应似乎对核心基因的稀有编码变化形式的携带者以及非携带者具有类似的量值。此观测结果指示prs可为稀有致病变体的外显率差异的重要贡献者(尤其在单倍剂量不足的模型,如本文所描述的模型中)。支持此想法,观测到八个具有低npr2活性的npr2变体携带者中的两个具有低-正常身高。此数据表明大部分具有npr2突变的iss个体还可具有多基因背景,使其更易受丧失npr2活性的致病效应。
[0358]
这些结果支持基于cnp的治疗可在npr2单倍剂量不足患者群体中有效的观点。此外,展示普通人群的npr2携带者中cgmp含量与身高的显著双向(lof和gof)相关性的结果表明用cnp类似物靶向此受体可为用于所有iss个体的有效疗法。
[0359]
应理解,本文所描述的本公开的每一实施例可任选地与本文所描述的其它实施例中的任何一或多者组合。本文所引用的每一专利文献和每一非专利文献以全文引用的方式并入本文中。
[0360]
因此,应理解,本发明不限于所公开的特定实施例,而意欲涵盖所有修改,所述修改在如由所附权利要求书、以上说明书中所定义和/或随附图式中所示的本发明的精神和范围内。因此,仅在随附权利要求书中呈现的此类限制应列入本公开中。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。