1.本发明涉及补骨脂素的新用途,尤其涉及补骨脂素联合骨骼干细胞在制备治疗放射性骨创伤的产品中的应用。
背景技术:
2.骨软骨组织的恶性肿瘤常常需要手术切除,并且联合放射治疗以清除手术后可能残留的肿瘤组织,降低恶性肿瘤复发风险。虽然该策略可以有效治疗恶性骨软骨肿瘤,但是常常产生因为手术形成巨大骨缺损,并且由于放疗导致局部的骨组织难以再生,严重影响患者生活质量甚至危及生命。现有的救治策略包括自体骨移植,骨组织局部修补成形术等,但是这些方案或者涉及从自身健康部位取骨,形成新的创伤,要么涉及二次甚至多次手术,反复麻醉和多次外科操作给患者带来痛苦和风险。因此,寻找新的治疗放射性骨创伤的方法已经成为相关领域学者和医生关注的重点。
3.组织工程技术是指通过给予组织受损部位填充模拟细胞外基质的生物材料,植入具有分化为新生组织能力的种子细胞,并联合应用调节因子,来实现受损伤组织的修复,已经被基础研究和临床应用证明为一项较为有效的治疗策略。骨骼干细胞是一类最新从骨组织中发现的骨骼系统内源性多潜能干细胞,在适宜的环境中具有重建骨,软骨和骨髓基质的能力,在骨骼系统发育和再生中发挥重要作用。
4.补骨脂素是豆科植物补骨脂(psoraleacorylifolia l.)干燥成熟果实的活性成分之一,现在已经可以化学合成。补骨脂素以往被报道可调节成骨细胞分化,促进骨折愈合,但是目前未见补骨脂素对于骨骼干细胞的调控作用的报道,更未见到采用补骨脂素联合骨骼干细胞治疗放射性骨创伤的策略及其应用。
技术实现要素:
5.本发明的目的是提供补骨脂素联合骨骼干细胞在制备治疗放射性骨创伤的产品中的应用,为开展补骨脂素联合骨骼干细胞制备抗放射性骨损伤产品相关的研究和应用奠定了基础。
6.本发明中,所述补骨脂素的cas号为66-97-7,结构式如式ⅰ所示:
[0007][0008]
在本发明的具体实施例中,所述放射性骨创伤为钴源照射引起的放射性骨创伤。
[0009]
第一方面,本发明保护补骨脂素联合骨骼干细胞在制备修复放射性骨创伤的产品中的应用。
[0010]
上述的应用中,所述修复放射性骨创伤体现在下述至少一方面:
[0011]
a1)修复放射性骨创伤的骨影像学结构;
[0012]
a2)改善放射性骨创伤的骨组织学形态;
[0013]
a3)提升具有修复骨组织作用的骨钙素的表达;
[0014]
a4)提升具有修复骨组织作用的i型胶原的表达。
[0015]
第二方面,本发明保护一种修复放射性骨创伤的产品,包括补骨脂素和骨骼干细胞。
[0016]
优选地,所述产品为植入体,由补骨脂素、骨骼干细胞和微凝胶制成。
[0017]
第三方面,本发明保护补骨脂素的应用,为如下b1)-b3)中的至少一种:
[0018]
b1)提升具有对抗放射性骨创伤作用的碱性磷酸酶的表达;
[0019]
b2)促进骨骼干细胞分化为成熟骨细胞;
[0020]
b3)减轻电离辐射带来的骨骼干细胞的干性损伤。
[0021]
第四方面,本发明保护补骨脂素在制备产品中的应用,所述产品的功能为如下b1)-b3)中的至少一种:
[0022]
b1)提升具有对抗放射性骨创伤作用的碱性磷酸酶的表达;
[0023]
b2)促进骨骼干细胞分化为成熟骨细胞;
[0024]
b3)减轻电离辐射带来的骨骼干细胞的干性损伤。
[0025]
第五方面,本发明保护一种产品,其含有补骨脂素;所述产品的功能为如下b1)-b3)中的至少一种:
[0026]
b1)提升具有对抗放射性骨创伤作用的碱性磷酸酶的表达;
[0027]
b2)促进骨骼干细胞分化为成熟骨细胞;
[0028]
b3)减轻电离辐射带来的骨骼干细胞的干性损伤。
[0029]
本发明应用中,补骨脂素或补骨脂素联合骨骼干细胞作用于人或哺乳动物。
[0030]
第六方面,本发明保护一种促进骨骼干细胞分化为成熟骨细胞的方法,包括如下步骤:使用含有补骨脂素的成骨分化培养基诱导骨骼干细胞体外成骨。
[0031]
所述补骨脂素在所述成骨分化培养基中的浓度具体可为10μm。
[0032]
我们最新的研究工作发现:补骨脂素可以有效促进骨骼干细胞分化为成熟的成骨细胞,并且可以减轻电离辐射带来的骨骼干细胞的干性损伤。以补骨脂素预处理骨骼干细胞再结合生物材料支架进行移植,可以有效修复放射性骨创伤。具体包括:我们在骨骼干细胞的培养体系中添加补骨脂素,然后评价其分化和自我更新能力。我们以钴源照射(2gy)实验小鼠股骨,并联合手术建立放射性骨创伤动物模型,以补骨脂素处理骨骼干细胞并制备生物材料凝胶,移植给予动物模型,采用microct检测评价骨组织结构,以苏木素伊红染色,抗骨钙素染色,抗i型胶原染色来评价补骨脂素联合骨骼干细胞对于放射性骨创伤的修复作用。microct结果表明:补骨脂素联合骨骼干细胞可以有效修复放射性骨创伤的骨影像学结构,苏木素伊红染色,抗骨钙素染色,抗i型胶原染色结果表明:补骨脂素联合骨骼干细胞可以改善放射性骨创伤的骨组织学形态,提升骨钙素和i型胶原的表达。综上所述,我们的工作首次证实补骨脂素联合骨骼干细胞对于放射性骨创伤具有显著的修复作用。我们的发明基于扎实的研究基础之上,是该领域的原始性创新。
[0033]
本发明方法操作简单、作用明确、方便实用,能够显著修复放射性骨创伤,对于减
轻电离辐射带来的骨组织损伤具有积极意义。因此,本发明报道了补骨脂素联合骨骼干细胞对于放射性骨创伤的保护作用,建立了稳定的复合制剂配制,储存和应用技术体系,为开展以补骨脂素和骨骼干细胞为基础的抗放射性骨创伤药物相关的研究和应用奠定了基础。
附图说明
[0034]
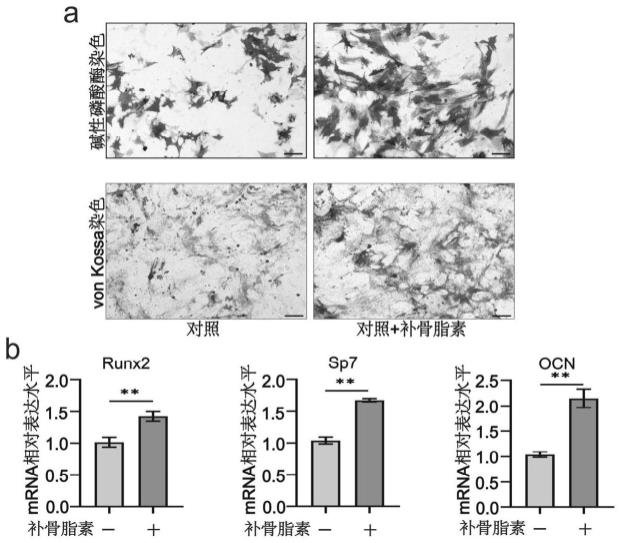
图1为补骨脂素制剂促进骨骼干细胞的早期成骨(碱性磷酸酶染色)和晚期成骨(von kossa染色)能力(图1a),同时促进其向成熟骨细胞分化时runx2、sp7和ocn(图1b)的表达(*,p<0.05,**,p<0.01)。图中标尺均代表100微米。
[0035]
图2为补骨脂素制剂能够减轻电离辐射(2gy)带来的骨骼干细胞的干性损伤(图2a,b),同时发现补骨脂素能促进自我分化相关的sox2和oct-4(图2c)的表达(*,p<0.05,**,p<0.01)。图中标尺均代表1毫米。
[0036]
图3为给予补骨脂素预处理的骨骼干细胞可以改善放射性骨创伤动物模型的骨影像学结构(micro-ct)。图中标尺均代表2毫米。
[0037]
图4为给予补骨脂素预处理的骨骼干细胞可以改善放射性骨创伤的骨组织形态(he,masson),提升骨钙素和i型胶原的表达。图中标尺均代表200微米。
具体实施方式
[0038]
下面结合具体实施方式对本发明进行进一步的详细描述,给出的实施例仅为了阐明本发明,而不是为了限制本发明的范围。以下提供的实施例可作为本技术领域普通技术人员进行进一步改进的指南,并不以任何方式构成对本发明的限制。
[0039]
下述实施例中所使用的实验方法如无特殊说明,均为常规方法;所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
[0040]
实施例1、补骨脂素联合骨骼干细胞在制备治疗放射性骨创伤的产品中的应用
[0041]
1、补骨脂素制剂的配置和储存
[0042]
补骨脂素(98%纯度,cas66-97-7)购自efebio(上海,中国),在dmso中溶解,制备20mm的原液,然后在细胞培养基(添加有牛血清蛋白的α-mem培养基,胎牛血清的终浓度为10%(体积百分含量);α-mem培养基的组成:1lα-mem培养基含12.1gα-mem粉末、终浓度为2mmol/l的l-谷氨酰胺(l-glutamine)和终浓度为25mmol/l的hepes buffer和2.4g nahco3)中稀释,使dmso占总体积的《0.1%,补骨脂素的浓度为10μm。
[0043]
2、补骨脂素制剂促进骨骼干细胞分化为成熟骨细胞
[0044]
设置如下两个实验组:
[0045]
对照组:诱导体外成骨过程中不添加补骨脂素;
[0046]
实验组:诱导体外成骨过程中添加10μm补骨脂素;
[0047]
具体步骤如下:
[0048]
1周龄c57bl/6n小鼠的股骨和胫骨,将骨髓细胞冲洗出来,然后剪碎,用胶原酶ii在37℃下消化1小时,将细胞(5
×
103/孔)接种到48孔板(每组5孔)中,并使用含有100nm地塞米松,10mmβ甘油磷酸盐和50μg/ml抗坏血酸(全部来自sigma)的成骨分化培养基诱导体外成骨,补充或不补充10μm补骨脂素。其中,骨骼干细胞培养基组成:添加有牛血清蛋白的α-mem培养基,胎牛血清的终浓度为10%(体积百分含量);α-mem培养基的组成:1lα-mem培
养基含12.1gα-mem粉末、终浓度为2mmol/l的l-谷氨酰胺(l-glutamine)和终浓度为25mmol/l的hepes buffer和2.4g nahco3。
[0049]
当14天进行碱性磷酸酶染色,观察对照组和实验组的细胞的碱性磷酸酶染色情况;当28天进行von kossa染色,观察对照组和实验组的细胞von kossa染色情况;对对照组和实验组中标志性基因runx2、sp7和ocn的表达情况进行检测。对于alp染色,细胞在分化14天后按照制造商的说明使用碱性磷酸酶试剂盒进行检测。对于vonkossa染色,细胞在分化28天后进行检测,具体步骤如下:细胞用4%多聚甲醛固定30分钟。用蒸馏水洗涤细胞三次后,用5%硝酸银水溶液染色,在明亮的阳光下孵育30分钟。再次清洗细胞,除去水,加入5%硫代硫酸钠水溶液5分钟。
[0050]
基因表达:总rna用trizol试剂提取,并按照制造商的说明使用mrna选择性pcr试剂盒(takara)进行逆转录。实时荧光定量pcr采用sybrpcr混合试剂盒(sigma-aldrich)和7500实时荧光定量pcr检测系统(应用生物系统公司,abi)进行。所有数据均归一化为对照,使用gapdh作为内部对照。
[0051]
各实验组的结果如图1所示,结果表明:补骨脂素可以有效促进骨骼干细胞分化为成熟的成骨细胞。
[0052]
3、补骨脂素制剂减轻电离辐射带来的骨骼干细胞的干性损伤
[0053]
设置如下四个实验组:
[0054]
对照:正常细胞不做处理;
[0055]
辐射:细胞接受co-60电离辐射2gy;
[0056]
对照 补骨脂素:细胞用10μm补骨脂素处理48h(正常小鼠骨骼干细胞在培养至3-6代后用含10μm浓度补骨脂素的细胞培养基培养48h);
[0057]
辐射 补骨脂素:细胞接受co-60电离辐射2gy后用10μm补骨脂素处理48h(正常小鼠骨骼干细胞在培养至3-6代后接受co-60电离辐射2gy并用含10μm浓度补骨脂素的细胞培养基培养48h);
[0058]
具体步骤如下:
[0059]
贴壁细胞以0.98gy/min的速率暴露于2gy剂量的γ辐射(co-60),然后将细胞接种到六孔板(5
×
102个细胞/孔)中,并培养长达14天,直到集落清晰可见。用4%多聚甲醛固定菌落并用0.5%结晶紫染色,并计数具有50个以上细胞的集落。
[0060]
对于alp染色,在诱导14天后,按照制造商的说明使用碱性磷酸酶试剂盒测定细胞。对于von kossa染色,在诱导28天后先用4%多聚甲醛固定细胞30分钟,用蒸馏水洗涤细胞三次后,用5%硝酸银水溶液染色细胞,并在紫外光下孵育30分钟。再次洗涤细胞,除去水,加入5%硫代硫酸钠水溶液5分钟。总rna用trizol试剂提取,并按照制造商的说明使用mrna选择性pcr试剂盒(takara)进行逆转录。实时荧光定量pcr采用sybrpcr混合试剂盒(sigma-aldrich)和7500实时荧光定量pcr检测系统(应用生物系统公司,abi)进行。所有数据均归一化为对照,使用gapdh作为内部对照。
[0061]
各实验组的结果如图2所示,结果表明:补骨脂素能够减轻电离辐射带来的骨骼干细胞的干性损伤。
[0062]
4、放射性骨创伤小鼠模型的建立
[0063]
在麻醉下仅将小鼠股骨(用铅板覆盖其他部分)以0.98gy/min的速率暴露于2gy剂
量的γ辐射(co-60)。骨缺损手术在照射后立即进行。在靠近干骺端的右侧股骨远端产生1.0mm圆形缺损。在术后1周,2周和3周处死小鼠。标本采集后,将股骨样品在4℃下固定在4%多聚甲醛中48小时,转移到70%乙醇中并储存在4℃下以进一步实验。
[0064]
5、补骨脂素预处理的骨骼干细胞联合生物材料凝胶修复放射性骨创伤小鼠模型设置如下六个实验组:
[0065]
对照:不做任何处理的放射性骨创伤动物模型;
[0066]
载体:仅植入微凝胶的放射性骨创伤动物模型;
[0067]
载体 细胞:植入含有ssc的微凝胶的放射性骨创伤动物模型;
[0068]
载体 细胞 补骨脂素:植入含有经过补骨脂素处理(在培养至3-6代后用含10μm浓度补骨脂素的细胞培养基培养48h)的ssc的微凝胶的放射性骨创伤动物模型;
[0069]
载体 辐射细胞:植入含有经辐射处理(co-60电离辐射2gy)的ssc的微凝胶的放射性骨创伤动物模型;
[0070]
载体 辐射细胞 补骨脂素:植入含有经过补骨脂素处理(在培养至3-6代后用含10μm浓度补骨脂素的细胞培养基培养48h)的经辐射处理(co-60电离辐射2gy)的ssc的微凝胶的放射性骨创伤动物模型;
[0071]
具体步骤如下:
[0072]
为了促进ssc移植,将正常/辐照的细胞或补骨脂素预处理的正常/辐照的细胞(术前48小时)收获并以1
×
107个细胞/ml的浓度重悬在200μl pbs(5%胎牛血清)中。将200μl细胞悬液滴到可分散和可溶解的多孔微载体片上,然后将ssc微凝胶(北京华龛生物科技有限公司(cytoniche),catno:f01-50lot no:01hk02cn06,20mg/片,1片微凝胶载体负载2
×
106个细胞的浓度重悬在200μl pbs中)在37℃的co2培养箱中保持1小时,以允许进一步的细胞附着。然后,用ssc微凝胶填充圆形骨缺陷。使用相同浓度的不含ssc的微凝胶作为对照。
[0073]
6、以microct检测放射性骨创伤小鼠和接受了补骨脂素预处理骨骼干细胞移植的放射性骨创伤小鼠的骨影像学结构
[0074]
将股骨固定在4%聚甲醛中2天,然后在4℃下储存在70%乙醇中,然后进行处理。使用scancoμct-40(scanco medical)进行μct扫描和分析,以评估小梁骨和骨再生。以8μm的分辨率(55kv,114ma,500ms积分时间)扫描股骨,并进行三维(3d)图像的重建。
[0075]
各实验组的结果如图3所示,结果表明:补骨脂素联合骨骼干细胞可以有效修复放射性骨创伤的骨影像学结构。
[0076]
7、以组织病理技术检测检测放射性骨创伤小鼠和接受了补骨脂素预处理骨骼干细胞移植的放射性骨创伤小鼠的骨组织学形态
[0077]
取股骨下端,用10%edta脱钙,然后包埋在石蜡中。制备了骨缺损区域的5微米矢状切片,用he和masson染色,并通过光学显微镜观察。对于col i和ocn免疫组织化学染色,在用内源性过氧化物酶淬灭(抑制剂为3%双氧水溶液),抗原检索和阻断非特异性结合位点后(一抗4℃孵育过夜,二抗室温一小时,dab显色后复染细胞核,脱水封片),将股骨切片与anti-col i孵育(1:100;servicebio,中国)和anti-ocn(1:100;servicebio,中国)孵育。
[0078]
各实验组染色的切片的光学显微照片如图4所示,苏木素伊红染色,抗骨钙素染色,抗i型胶原染色结果表明:补骨脂素联合骨骼干细胞可以改善放射性骨创伤的骨组织学形态,提升骨钙素和i型胶原的表达。
[0079]
以上对本发明进行了详述。对于本领域技术人员来说,在不脱离本发明的宗旨和范围,以及无需进行不必要的实验情况下,可在等同参数、浓度和条件下,在较宽范围内实施本发明。虽然本发明给出了特殊的实施例,应该理解为,可以对本发明作进一步的改进。总之,按本发明的原理,本技术欲包括任何变更、用途或对本发明的改进,包括脱离了本技术中已公开范围,而用本领域已知的常规技术进行的改变。按附带的权利要求的范围,可以进行一些基本特征的应用。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。