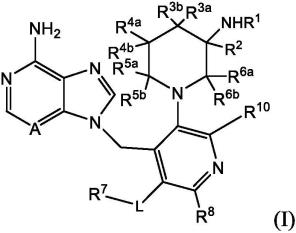
1.本发明涉及雄激素受体剪接变体和雄激素受体相关障碍的治疗(treatment)。
背景技术:
2.雄激素受体(androgen receptor,ar)是i型核受体超家族的成员,这是一类由类固醇激素激活的转录因子。位于x染色体上的ar,在多种组织中表达,特别是在男性的性器官以及运动神经元和肌细胞中表达。ar信号传导通路在男性生殖器官(如前列腺和附睾)以及肌肉骨骼系统、心血管系统、免疫系统、神经系统与造血系统的正常发育和功能中发挥关键作用。
3.鉴于ar的广泛多样的和重要的生理功能,已经在各种疾病中鉴定出其异常。例如,不存在雄激素或功能性ar的情况下,男性性别分化未发生。男性的ar功能的完全丧失导致完全性雄激素不敏感综合征。ar活性也与前列腺癌密切相关,前列腺癌是美国最普遍存在的非皮肤性癌症,每6名男性中就有1名患前列腺癌,并且它是男性中癌症相关的死亡的第二大原因。导致毒性功能获得性(toxic gain-of-function)ar变体的ar的n端结构域(ntd)中的多态性多聚谷氨酰胺重复片段与脊髓延髓肌肉萎缩症(spinal and bulbar muscular atrophy,sbma)相关,sbma也称为肯尼迪病(kennedy's disease),是一种进行性神经退行性病症。还有越来越多的研究将ar的作用与乳腺癌、喉癌、肝癌和睾丸癌相关联。
4.目前没有可用于ar相关障碍的改善疾病的治疗方法。迄今为止,治疗ar相关障碍的策略一直无效,主要是由于严重的副作用和耐药性。这些策略包括雄激素剥夺(例如化学去势)、基因沉默(例如通过反义寡核苷酸或aav递送的mirna)或ar功能的调控(例如通过靶向疾病特异性的翻译后修饰或与辅助因子的相互作用)。例如,由于高免疫原性和未能改善肌肉力量或功能,旨在增加sbma患者的ar的磷酸化作用和随后降解作用的使用igf-1模拟物的临床试验尚未成功(1)。
5.因此,本发明的目的为发现治疗ar相关障碍的其它与改进的方法。
技术实现要素:
6.发明人发现,天然存在于正常组织中的ar的剪接变体ar2,能够抑制ar的活性。发明人还确认,ar2的某些性质,包括与ar形成异源二聚体的能力以及自身不能反式激活的能力,对于抑制ar活性特别有用。发明人在代表ar相关疾病sbma的小鼠模型中测试了ar2过表达。sbma小鼠表达具有扩展的cag延伸的人类ar转基因,其编码100个谷氨酰胺(ar100q)。在用ar2处理了这些小鼠的情况下,它们表现出提高的存活率、增加的体重与运动功能。有趣的是,发明人发现,用靶向ar2的sirna处理的携带完整ar基因并因此内源性表达ar2的雄性小鼠导致神经肌肉表型的恶化。因此,能够与ar形成异源二聚体并且自身不能反式激活的ar变体(如ar2)是ar相关障碍的有用的治疗物。
7.尽管不希望受理论约束,发明人推测,在正常细胞中,ar2可以通过与ar形成异源复合物以作为诱饵,从而可能在靶基因的雄激素应答元件(are)的水平作为抑制ar的活性
的转录抑制因子。因此,ar2可以用于微调ar活性,从而恢复正常细胞中ar活性的稳态(homeostatic state)。
8.对于与增加的ar活性相关的障碍,如由毒性功能获得性ar变体引起的那些,ar2可以用于抑制与障碍相关的ar变体的活性。因此,在这些障碍中,ar2的增强的活性(例如通过基因递送技术)可以是有益的。
9.对于与减少的ar活性相关的障碍,抑制内源性表达的ar2的表达(例如通过基因沉默技术)可以是有益的。
10.基于ar2的治疗策略优于用于治疗ar相关障碍的当前策略,因为当前策略通常涉及改变ar蛋白质水平(例如靶向ar的反义寡核苷酸)或激素水平(例如化学去势),或者靶向翻译后修饰机制或辅助因子,所有这些要么破坏ar的基因组和非基因组活性,要么对ar是非特异性的,并且因此通常与不希望出现的副作用相关联。此外,这些策略通常受到与雄激素功能丧失相关的体征和症状的加剧的可能性的阻碍,特别是因为大多数受影响的患者为男性,他们只有一个ar基因副本。与此相反,本发明涉及基于天然存在的ar2的治疗方法,所以这些ar变体在一定程度上模拟了ar的天然活性,例如,它们将以相似的方式被调控并具有相似的靶基因。因此,根据本发明的基于ar2的治疗物能够调控ar的活性,并且对调节ar、其转录输出和信号传导通路的复杂网络的干扰最小。
11.因此,本发明的一方面提供了一种编码ar变体的表达构建体,其在用于通过疗法治疗人体或动物体的方法中使用,所述ar变体包含与雄激素受体剪接变体2(ar2)具有≥70%(即70%或更多)、≥80%、≥90%、≥95%、≥99%或具有100%的同一性(identity)的多肽序列。
12.本发明还提供了一种宿主细胞,包含或产生一种在用于通过疗法治疗人体或动物体的方法中使用的表达构建体,其中,所述表达构建体编码ar变体,其中,所述ar变体包含与ar2具有≥70%、≥80%、≥90%、≥95%、≥99%或具有100%的同一性的多肽序列。
13.本发明还提供了一种药物组合物,其在用于通过疗法治疗人体或动物体的方法中使用,其中,所述药物组合物包含药学上可接受的载体和:(a)编码ar变体的表达构建体,其在用于通过疗法治疗人体或动物体的方法中使用,其中,所述ar变体包含与ar2具有≥70%、≥80%、≥90%、≥95%、≥99%或具有100%的同一性的多肽序列,或(b)包含或产生所述表达构建体的宿主细胞。
14.本发明还提供了一种在有需要的患者中治疗ar相关障碍的方法,包括施用治疗有效量的:(a)编码ar变体的表达构建体,其在用于通过疗法治疗人体或动物体的方法中使用,其中,所述ar变体包含与ar2具有≥70%、≥80%、≥90%、≥95%、≥99%或具有100%的同一性的多肽序列,(b)包含或产生所述表达构建体的宿主细胞,和/或(c)包含(a)或(b)以及药学上可接受的载体的药物组合物。
15.在另一方面,本发明提供了一种能够调控(例如抑制)ar2的表达和/或活性的试剂。本发明还提供了一种包含所述试剂的药物组合物。本发明还提供了所述试剂或所述药物组合物在用于治疗ar相关障碍的方法中的用途。本发明还提供了一种在有需要的患者中治疗ar相关障碍的方法,包括对所述患者施用有效量的所述试剂或所述药物组合物。
16.在另一方面,本发明提供了一种ar变体,包含与seq id no:1具有≥70%、≥80%、≥90%、≥95%、≥99%或具有100%的同一性的多肽序列;其中,所述ar变体能够与ar形成
异源二聚体,单独的所述ar变体不能反式激活,并且所述ar变体不是seq id no:3。本发明还提供了一种编码所述ar变体的表达构建体,以及一种包含或产生所述表达构建体的宿主细胞。本发明还提供了一种包含所述表达构建体或所述宿主细胞的药物组合物。本发明还提供了所述ar变体、表达构建体、所述宿主细胞或所述药物组合物在用于治疗ar相关障碍的方法中的用途。本发明还提供了一种在有需要的患者中治疗ar相关障碍的方法,包括对所述患者施用治疗有效量的所述ar变体、表达构建体、所述宿主细胞或所述药物组合物。本发明还提供了所述ar变体、表达构建体、所述宿主细胞或所述药物组合物在制备治疗ar相关障碍的方法中的药剂中的用途。
附图说明
17.图1显示ar2在人体组织中高度表达。a)使用illumina hiseq 4000平台对人脑组织进行rna测序(rna-seq)。显示了来自所示的人脑组织的ar剪接变体表达水平。表达值表示为对数标准化计数。数据为平均值
±
s.e.m。每个点表示一次重复试验(n=7),*p《0.05;**p《0.01。b)显示38种不同人体组织中的相对ar2水平的热图。c)与人类成肌细胞中的ar1相比,ar2的相对mrna表达水平。数据为平均值
±
s.e.m。每个点表示一次重复试验(n=6)。d)显示了不同人类mrna ar剪接变体的示意图。空方块和实方块分别表示utr和外显子。e)与内含子1上的下游序列相比,ar基因的外显子1b上的chip-qpcr显示增加的rna pol ii占据率。数据为平均值
±
s.e.m。每个点表示一次重复试验(n=3)。f)与ar1相比,包含替代性外显子1b导致ar2(milwlhs;seq id no:35)中的n端氨基酸序列(ntd)不同。ar1和ar2共用相同的剩余序列(左)。ar1和ar2剪接变体在hek293t细胞中表达。全细胞提取物通过sds page分离,然后使用c端ar抗体实施免疫印迹法。显示了分子大小(右)。
18.图2显示ar2调控全长ar转录活性。a)用所示的载体与荧光素酶pare-e1b-luc和β-半乳糖苷酶pcmvβ报告构建体一起转染hek293t细胞。通过荧光素酶测定在存在和不存在dht的情况下测量ar反式激活。数据为平均值
±
s.e.m。每个点表示一次重复试验(n=5),**p《0.01。b)荧光素酶测定是在ar2构建体的浓度增加的情况下进行的,以μg表示。c)将所示的融合构建体共转染到hek293t细胞中,并且在添加nanobret(纳米bret)halotag 618配体后测量bret信号。校正的nanobret比率表示为millibret单位(mbu)。数据为平均值
±
s.e.m。每个点表示一次重复试验(n=3),**p《0.01。d)用多个靶向ar2的独有的n端序列的sirna处理48小时后,ar1和ar2转录物的mrna相对表达。相对于具有相同化学骨架的非靶向序列(nts)sirna对数据进行标准化。对于所有测试的sirna,ar2表达水平显著降低(p《0.01)。还显示了未转染的(ut)成肌细胞的表达值。数据为平均值
±
s.e.m。每个点表示一次重复试验(n=3)。e)人类成肌细胞中ar2过表达或被敲低的差异表达转录物中含有are的基因的饼状图分解。上调和下调的基因分别以红色/蓝色和粉红色/浅蓝色表示。f)和g)描绘样本间(sample to sample)距离的层次聚类(hierarchical clustering)的热图。使用含有are的转录物的方差稳定转换的rna测序读取计数,以计算用于层次聚类的样本间的欧几里德(euclidean)距离(灰度等级)。oe:过表达;ev:空白载体;sirna:sirna处理的;ntc:非靶向对照。过表达组中的转录物分为3个主要组:非常下调(1)、轻度下调(2)和上调(3)。h)将来自瞬时表达ar2-flag的用etoh或dht处理24小时的mcf7细胞的交联染色质,用抗flag抗体或igg同种型对照进行免疫沉淀。greb1、znf485和ehf是已知的ar靶基因。数据为平均
值
±
s.e.m。每个点表示一次重复试验(n=3),**p《0.01。i)工作模型的示意图:包括形成ar:ar同源二聚体在内,ar还与ar2形成异源二聚体,从而导致效率较低的反式激活复合物。
19.图3显示,在sbma小鼠的临床前试验中,ar2的过表达改善了表型结果与病理退化。a)动物实验的设计的示意图。整个图中的配色方案保持不变(aav9-ar2:n=8;aav9-模拟物:n=6;盐水:n=4)。b)ar100q小鼠的kaplan-meier生存估计(对数秩检验(log-rank test))。c)在ar2处理的小鼠中,中值疾病发作延迟。d)从5周龄到终末期的ar100q小鼠平均体重。e)ar100q小鼠的转棒性能(rotarod performance)的kaplan-meier估计。失败设置为骑行跌落时间(drop of riding time)≥30秒。f)来自11周龄野生型以及用表达ar2或模拟物序列的ravv9处理的ar100q小鼠的代表性骨骼肌切片(腓肠肌)。切片用h&e或nadh染色用于肌肉形态学。箭号(arrow)表示萎缩的肌纤维。箭头(arrowhead)表示含有集中核的肌纤维。比例尺表示20μm(顶部)。按转基因基因型和ar2处理的与模拟物分类的肌纤维横截面直径大小的相对频率分布(底部)。g)在用表达ar2或模拟物序列的raav9处理的ar100q小鼠中,用针对ncam和psa-ncam的抗体染色的骨骼肌的代表性图像。比例尺表示50μm(顶部)。psa-ncam/ncam共定位区域的量化。对于所有组,n=6个区域,每组3只小鼠(底部)。h)模拟物和ar2处理的ar100q小鼠的脊髓和肌肉切片(cross sections)的泛素染色。显示了来自3个独立实验的代表性图像。对于脊髓切片,比例尺表示20μm,而对于肌肉切片,比例尺表示10μm。i)来自3个独立实验的模拟物和ar2处理的ar100q小鼠的代表性脊髓和骨骼肌切片。用1c2抗体染色切片。比例尺表示100μm。j)相对于来自模拟物或ar2处理的ar100q小鼠的脊髓(megf10和nqo1)和肌肉(cacng1、chrna1、mybpc2、mybph、tnnt3和unc45b)裂解物中的hprt管家基因对mrna表达水平标准化。数值表示为对野生型动物的倍数变化,设置为1。
20.图4a)显示动物实验的设计的示意图。整个图中的配色方案保持不变(sirna ar-2:n=6;模拟物:n=5)。b)来自sirna处理的与模拟物处理的ar121q小鼠的股四头肌中内源性ar2的mrna水平相对于hprt管家基因进行标准化。数据为平均值
±
s.e.m。每个点表示一次重复试验(n=3)。单尾t检验。c)在用靶向ar2的sirna或模拟物序列处理的ar121q小鼠的研究的最后3周中,以力的单位(n:牛顿)表示的平均值
±
s.e.m握力。d)在研究的最后一周,用靶向ar-2的sirna或模拟物序列处理的ar121q小鼠的转棒性能。数据为平均值
±
s.e.m。每个点表示一次重复试验(在模拟物处理的组中n=4,而在sirna处理的组中n=6。)。
21.图5显示aav9-ar2处理改善了sbma小鼠的表型结果。a)sbma小鼠的生存-kaplan-meier生存估计(对数秩检验)。b)疾病发作——左图:疾病发作的kaplan-meier估计。疾病发作被定义为小鼠开始表现出连续两周持续体重减轻的那天中的时间。右图:发作的平均天数。c)体重——左图:从8周龄到终末期的体重百分比,第8周的平均体重设置为100%。右图:来自两个处理组的sbma小鼠在13周龄的平均体重。d)握力——从8周龄到终末期的平均握力的百分比,第8周的平均握力设置为100%。e)平均转棒活性(rotarod activity)。aav9-ar2在图中被称为aav9-ar45。
22.序列的简要说明
23.seq id no:1显示ar变体的多肽序列。
24.seq id no:2显示编码seq id no:1的ar变体的多核苷酸序列。
25.seq id no:3显示人类ar2的多肽序列。
26.seq id no:4显示人类ar2的cdna序列。
27.seq id no:5显示人类ar的ntd的多肽序列。
28.seq id no:6显示人类ar的多肽序列。
29.seq id no:7显示ar变体的多肽序列。
30.seq id no:8显示ar变体的多肽序列。
31.seq id no:9-34显示实施例中使用的sirna序列(正义链和反义链)。
32.seq id no:35显示在来源于替代性外显子1b的ar2的n端的多肽序列。
具体实施方式
33.ar变体
34.本发明涉及ar变体,特别是ar的剪接变体2(ar2)。来自任何动物的ar2,特别是人类ar2(enst00000396043、ensp00000379358),都可以用于本发明。人类ar2的多肽序列在seq id no:3中提供,并且对应的cdna在seq id no:4中提供。
35.ar2是正常组织中九种天然存在的剪接变体之一。ar2最初是通过用从人类胎盘组织中分离的rna快速扩增cdna端(race)来鉴定的(17)。发现ar2 mrna来源于包含位于外显子1的下游22.1kb的替代性外显子1(外显子1b)(图1d)。编码的蛋白质含有代替典型ntd的独有的n端序列且具有45kda的分子质量,因此,ar2在文献中也称为ar45(图1f)。然而,迄今为止,对其功能知之甚少。发明人现已将ar2鉴定为健康人脑组织、运动神经元和骨骼肌中最高表达的剪接变体。发明人还示出了用ar2过表达处理的sbma小鼠的有益效果,以及用ar2敲低处理的sbma小鼠的恶化效果。
36.本发明还涉及序列变体。这些变体包含与ar2(例如人类ar2(seq id no:3))具有≥70%(即70%或更多)、≥75%、≥80%、≥85%、≥90%、≥95%或具有99%的序列同一性的多肽。
37.可以用于本发明的其它ar变体可以包含与seq id no:1具有≥70%(即70%或更多)的同一性的多肽序列。例如,ar变体可以包含与seq id no:1具有≥80%、≥90%、≥95%、≥99%或具有100%的同一性的多肽序列,或由与seq id no:1具有≥80%、≥90%、≥95%、≥99%或具有100%的同一性的多肽序列组成。在本发明的一些实施方式中,ar变体不是ar2,例如ar变体不是seq id no:3。
38.对应于seq id no:1的cdna在seq id no:2中提供。ar变体可以包含与seq id no:2具有≥80%、≥90%、≥95%或≥99%的同一性的多核苷酸序列,或由与seq id no:2具有≥80%、≥90%、≥95%或≥99%的同一性的多核苷酸序列组成。
39.seq id no:1对应于seq id no:6的氨基酸556-920。seq id no:6是人类雄激素受体(ar;enst00000374690)的多肽序列,在此也称为ar1。人类ar由三个主要结构域组成:(i)外显子1编码高度可变的氨基端结构域(ntd)(氨基酸1-555;提供为seq id no:5),具有强效的转录激活因子能力,(ii)外显子2和3编码中心的两个锌指基序dna结合结构域(dbd)与铰链区(氨基酸556-670),以及(iii)外显子4-8编码非常保守的羧基端配体结合结构域(lbd;氨基酸671-920),负责与转录机制相互作用。
40.根据本发明的ar变体能够与ar形成异源二聚体。尽管不希望受理论约束,但根据本发明的该ar变体可以通过与疾病相关的ar突变体形成异源复合物以作为诱饵,从而可能在靶基因的雄激素应答元件(are)的水平上调控与疾病相关的ar突变体的活性。在ar中,二
聚化主要经由fxxlf基序通过n/c端相互作用和经由二聚化盒(d-box)通过dbd/dbd相互作用介导。因此,根据本发明的ar变体可以包含ar的dbd和lbd结构域,即seq id no:1,其对应于seq id no:6的氨基酸556-920。
41.确定是否ar二聚化的方法是本领域已知的并在本文的实施例中描述,例如,生物发光共振能量转移(bret)测定,其允许实时检测复合物的形成,或免疫共沉淀测定。
42.即使在配体存在的情况下,根据本发明的ar变体也不能单独进行反式激活。具有反式激活功能的区域是ar的ntd中的激活功能1(af-1)子结构域,其跨越氨基酸51-211。因此,根据本发明的ar变体可能部分缺少ntd,如缺少af-1子结构域。例如,根据本发明的ar变体可以是seq id no:7,其缺少seq id no:6的氨基酸51-211。根据本发明的ar变体可以是seq id no:8,其缺少seq id no:6的氨基酸1-211。在其它实施方式中,ar变体可以缺少整个ntd,例如ar变体不包含seq id no:5。
43.ar变体可以由部分缺少经典(canonical)外显子1的mrna编码。该ar变体可以由缺少ar的整个经典外显子1的mrna编码。
44.确定ar变体是否能够单独激活转录的方法是本领域已知的并在本文的实施例中描述,例如,体外报告基因表达测定,如荧光素酶测定。
45.此外,ntd包含多聚谷氨酰胺片段(tract)(5-36个残基)(seq id no:6的氨基酸59-89),并且该多聚谷氨酰胺片段的大小影响ar功能,较长的片段与较低的ar活性相关。例如,这种多聚谷氨酰胺片段的扩展(例如38-68个残基)导致sbma。因此,根据本发明的ar变体可以缺少对应于多聚谷氨酰胺片段的区域。
46.根据本发明的ar变体可以包含相对于seq id no:1、3、7和8中的任何一个的修饰,如氨基酸替换、添加或缺失。例如,该ar变体可以包含1、2、3、4、5、6、7、8、9、10个或更多个以任意组合被替换、缺失或添加的氨基酸残基。
47.例如,该变体可以具有不显著改变ar2的生物活性的氨基酸残基的添加、缺失或替换。例如,可以通过检查ar2结构域的结构来确定可以在不影响生物活性的情况下改变的ar2的那些单个位点或区域。可替代地,可以通过丙氨酸扫描突变来确定会容许氨基酸替换的区域(2)。在此方法中,选择的氨基酸残基分别用中性氨基酸(例如丙氨酸)替换,以确定对生物活性的影响。
48.ar变体可以包含最不可能扰乱多肽的结构和/或功能的保守氨基酸改变。例如,该变体可以包含在seq id no:1、3、7和8中的任何一个内的一个或多个保守氨基酸改变。保守氨基酸改变通常涉及用结构和/或功能相似的另一种氨基酸替换一种氨基酸(例如,侧链大小、电荷和形状相似的氨基酸)。具有相似侧链的氨基酸残基是本领域已知的。这些包括具有碱性侧链(例如赖氨酸、精氨酸、组氨酸)、酸性侧链(例如天冬氨酸、谷氨酸)、不带电荷的极性侧链(例如甘氨酸、天冬酰胺、谷氨酰胺、丝氨酸、苏氨酸、酪氨酸、半胱氨酸、色氨酸)、非极性侧链(例如丙氨酸、缬氨酸、亮氨酸、异亮氨酸、脯氨酸、苯丙氨酸、甲硫氨酸)、β-支链侧链(例如苏氨酸、缬氨酸、异亮氨酸)和芳香侧链(例如酪氨酸、苯丙氨酸、色氨酸、组氨酸)的氨基酸。因此,ar2中的一个或多个氨基酸残基可以被具有相似侧链的其它氨基酸残基替换,并且可以使用本文所描述的功能测定来测试改变的蛋白质的所保留的功能。可以通过本领域已知的标准技术引入修饰,如位点特异性诱变(3)和pcr介导的诱变,条件是保留活性,例如用ar形成异源二聚体化的能力。
49.与未改变的序列相比,ar变体可以进行密码子优化以增加宿主细胞中相应蛋白质的表达水平。用于密码子优化的方法是本领域已知的,例如,可以使用genscript optimum genetm算法。
50.本发明涉及编码ar2的多核苷酸,例如人类ar2(seq id no:4)。本发明还涉及编码ar变体的多核苷酸。由于遗传密码的简并性,该多核苷酸可以与seq id no:4中所示的多核苷酸序列不同,而因此编码与seq id no:4中所示的多核苷酸序列所编码的蛋白质相同的蛋白质。
51.例如,该多核苷酸可以与seq id no:4具有≥70%(即70%或更多)、≥75%、≥80%、≥85%、≥90%、≥95%或具有100%的序列同一性。
52.该多核苷酸可以编码本文所描述的任何ar变体蛋白。
53.表达构建体
54.本发明还提供了用于治疗的编码根据本发明的ar变体的表达构建体。适于在人类和动物中表达的任何表达构建体都可以用于本发明。例如,该表达构建体可以是基于非病毒质粒的载体或病毒载体。
55.病毒载体可以是来源于腺病毒、腺相关病毒(aav)或逆转录病毒的载体,包括慢病毒,如人类免疫缺陷病毒(hiv)。可以通过本领域已知的标准方法制备该表达构建体,以提供用于基因治疗的表达构建体。因此,良好建立的公共结构域转染和/或转导、包装与纯化方法可以用于制备合适的载体制剂以及合适的病毒颗粒。
56.该表达构建体还可以包含允许编码的蛋白质的表达和优选分泌的调控序列,例如,启动子、增强子、多聚腺苷酸化信号、内部核糖体进入位点(ires)、编码蛋白质转导结构域(ptd)的序列。
57.该表达构建体可以包括包含可操作地连接至ar2的启动子区域的多核苷酸,以引起或改善治疗性蛋白质在感染的宿主细胞中的表达。启动子可以是普遍存在的、组织特异性的、强的、弱的、调节的或嵌合的。通常选择启动子以允许在感染的组织中有效且合适地产生蛋白质。启动子可以是哺乳动物(例如人类或鼠类)来源的,或其它来源的,包括细胞的、病毒的、真菌的、植物的或合成的启动子。启动子可以在神经细胞中起作用,例如运动细胞和肌肉细胞,特别是在人体细胞中。
58.可以用于本发明的调控的启动子的实施例包括含有tet开/关元件的启动子、雷帕霉素可诱导的启动子和金属硫蛋白启动子。
59.启动子可以是组织特异性的,如肌肉特异性启动子。可以用于本发明的肌肉特异性启动子可以是哺乳动物肌肉肌酸激酶(mck)启动子、哺乳动物结蛋白(des)或基于mck(例如enh358mck,参见参考文献4)或des的人工启动子。
60.可以用于本发明的另一种组织特异性启动子可以是运动神经元特异性启动子。运动神经元特异性启动子的实施例包括胆碱乙酰转移酶(choline acetyl transferase,chat)的启动子。在运动神经元中起作用的其它启动子包括降钙素基因相关肽(calcitonin gene-related peptide,cgrp)的启动子(已知的运动神经元衍生的因子)、神经元特异性烯醇化酶(neuron specific enolase,nse)的启动子、突触蛋白(synapsin)的启动子或普遍存在的启动子,包括神经元特异性沉默元件(neuron specific silencer elements,nrse)。
61.可替代地,该启动子可以是组成型活性启动子,选自由以下组成的组:巨细胞病毒(cmv)启动子、磷酸甘油酸激酶(pgk)启动子、猿猴病毒40(sv40)启动子、泛素c(ubiquitin c,ubc)启动子、cag启动子、普遍存在的染色质开放元件(ucoe)启动子、cd11b启动子、wiskott-aldrich综合征(was)启动子和甘油醛3-磷酸脱氢酶(gapdh)启动子。
62.可以用于本发明的表达构建体包含enh358mck启动子。enh358mck启动子是本领域已知的,是通过将约200bp增强子与鼠科mck基因的358bp近端启动子连接而构建的。因此,根据本发明的该ar变体从enh358mck启动子开始表达。
63.可以用于本发明的表达构建体包含胆碱乙酰转移酶(choline acetyl transferase,chat)。因此,根据本发明的ar变体从chat启动子开始表达。
64.基因递送
65.本文所描述的ar变体、多核苷酸和表达构建体可以通过基因疗法施用以治疗ar2相关障碍,使得表达构建体产生其编码的蛋白质以在宿主中介导治疗效果。
66.可以使用本领域可用的任何基因治疗方法,例如,参考文献5、6、7、8、9和10中综述的那些。涉及重组dna技术的方法是本领域已知的(11,12)。
67.体内(in vivo)基因治疗方法可以用于本发明。因此,根据本发明的治疗方法可以包括将表达构建体直接递送到患者或细胞中的步骤。因此,该表达构建体可以直接在体内施用,在那里它被表达以产生编码产物。这可以通过本领域已知的许多方法中的任何一种来完成,例如,通过使用有缺陷的或减毒的逆转录病毒或其它病毒载体进行感染,或通过直接注射裸dna,或通过使用微粒轰击(例如基因枪;biolistic,dupont),或用脂质或细胞表面受体或转染剂包被,包封在脂质体、微粒、微胶囊、纳米颗粒或纳米胶囊中,或通过将它们与已知进入细胞核的肽结合(linkage)施用,通过将其与受到受体介导的内吞作用的配体结合施用,例如参见参考文献13,其可以用于靶向特异性表达受体的细胞类型。此外,通过靶向特异性受体,该表达构建体可以在体内靶向细胞特异性摄取与表达,例如参见参考文献14。在某些实施方式中,可以通过同源重组将该表达构建体引入细胞内并掺入宿主细胞dna中用于表达,例如参见参考文献15和16。
68.离体(ex vivo)基因治疗方法可以用于本发明。因此,根据本发明的治疗方法可以包括在体外(in vitro)用表达构建体转化宿主细胞,然后将宿主细胞移植到患者中。将表达构建体引入组织培养物中的细胞的方法是本领域众所周知的,包括转染、电穿孔、显微注射、用含有核酸序列的病毒或噬菌体载体感染、细胞融合、染色体介导的基因转移、微细胞介导的基因转移、原生质球融合。该技术通常提供表达构建体向宿主细胞的稳定转移,使得该表达构建体可以由宿主细胞表达并且可以由其细胞后代遗传和表达。引入表达构建体的方法可以进一步包括将选择性标记引入宿主细胞,并将宿主细胞置于选择下,并分离已经摄取且正在表达转移的基因的宿主细胞。可以通过本领域已知的各种方法将得到的重组细胞递送给患者。
69.本发明还提供了包含或产生根据本发明的表达构建体的宿主细胞。出于基因治疗目的可以引入表达构建体的宿主细胞包括任何所需的、可用的细胞类型。例如,可以使用干细胞或祖细胞。可以潜在地使用可以在体外分离并维持的任何干细胞和/或祖细胞,例如,参考文献17、18、19和20中描述的那些。例如,在宿主细胞为血细胞的情况下,重组血细胞(例如造血干细胞或祖细胞)可以静脉内施用。使用的宿主细胞的量取决于各种因素,如所
需的效果和患者状态,并且可以由本领域技术人员常规确定。
70.ar2活性的调控
71.本发明涉及使用能够调控ar2的活性的试剂(agent)。该试剂可以是下调ar2的转录水平和/或蛋白质水平的试剂,调控ar2与其辅助因子(如共激活蛋白或dna应答元件)之间的相互作用的试剂,以及调控ar2的翻译后修饰的试剂。
72.该试剂可能够特异性调控ar2活性,而不影响ar和ar的其它内源性表达的剪接变体的活性。与ar或ar的任何其它内源性表达的剪接变体(即ar1、ar3、ar4、ar5、ar6、ar7、ar8或ar9)相比,该试剂可以具有≥50%(即50%或更多)、≥60%、≥70%、≥80%、≥90%或具有100%的对ar2的选择性。
73.该试剂可以是ar2转录抑制剂、ar2翻译抑制剂或ar2的拮抗剂。该试剂可以抑制ar2mrna的表达。例如,它可以是反义寡核苷酸、rna干扰寡核苷酸(rnai)、核酶、降解ar2转录所需的转录因子的试剂或与ar2结合的抗体。例如,与没有施用该试剂时相比,该试剂可以使ar2的mrna表达的水平降低≥50%(即50%或更多)、≥60%、≥70%、≥80%、≥90%或100%。
74.该试剂可以抑制ar2的功能。例如,与没有施用该试剂时相比,ar2的活性可以被降低≥50%(即50%或更多)、≥60%、≥70%、≥80%、≥90%或100%。
75.rnai技术可以用于敲低细胞中的ar2。例如,该试剂可以以dsrna(双链rna)或shrna(短发夹rna)分子的形式存在,它们在体内被消化成介导rnai效应的21-23nt片段小干扰rna(sirna)。sirna可以由ar2的多核苷酸序列(例如seq id no:4)内的核苷酸序列编码。sirna的长度可以是约20-50个核苷酸,例如长度约为21-23个核苷酸。该sirna可以与ar2(例如seq id no:4)具有≥70%(即70%或更多)、≥80%、≥90%、≥95%、≥99%或具有100%的序列同一性。例如,该sirna可以包含seq id no:9-32中任一个列出的序列。该sirna可以包含seq id no:31和32中列出的序列。
76.sirna可以由常规的核苷酸a、g、t、c或u或不常见的或修饰的核苷酸(如肌苷酸、1-甲基肌苷酸、1-甲基鸟苷酸、nn-二甲基鸟苷酸、假尿苷酸、核糖苷酸、5-羟甲基胞嘧啶和5-羟甲基尿苷)组成。
77.sirna或编码其的载体可以通过本领域已知的技术递送至细胞,诸如如上所描述的体内或离体基因治疗方法。sirna可以通过本领域已知的任何方法制备,包括但不限于寡核苷酸合成、体外转录、核糖核酸酶消化或体内sirna的生成。
78.根据本发明也可以使用反义技术。根据本发明有用的反义寡核苷酸可以是与ar2(例如seq id no:4)互补并且能够与ar2杂交并抑制ar2表达的rna或dna。该反义寡核苷酸可以与ar2具有≥70%(即70%或更多)、≥80%、≥90%、≥95%、≥99%或具有100%的互补性。该反义寡核苷酸的长度可以是15bp至30bp。本领域已知的其它标准可以用于选择反义寡核苷酸,变化靶序列中的长度或退火位置。该反义寡核苷酸可以包括衍生物,如s寡核苷酸(硫代磷酸酯衍生物或s-寡核苷酸(oligos))。该反义寡核苷酸与增强细胞摄取反义分子的试剂共同施用,例如可以是以脂质体形式存在的亲脂性阳离子化合物。该反义寡核苷酸可以与亲脂性载体(如甾醇,例如胆固醇、胆酸盐和脱氧胆酸)结合。该反义寡核苷酸可以与被细胞摄取的肽(例如肽激素、抗原或抗体或肽类毒素)缀合。
79.核酶也可以用于本发明。例如,可以使用包含靶向ar2的反义rna和切割rna的核酶
的反义rna/核酶融合物。核酶分子可以基于氯霉素乙酰转移酶核酶或发夹核酶。
80.治疗和医学用途
81.本发明还涉及本文所描述的ar变体、表达构建体、宿主细胞、ar2调控试剂或药物组合物在用于通过疗法治疗人体或动物体的方法中使用。本发明还涉及本文所描述的ar变体、表达构建体、宿主细胞、ar2调控试剂或药物组合物在用于通过疗法治疗人体或动物体的方法中的用途。本发明还涉及本文所描述的ar变体、表达构建体、宿主细胞、ar2调控试剂或药物组合物在制备用于通过疗法治疗人体或动物体的方法的药剂中的用途。本发明还涉及治疗方法,其使用本文所描述的ar变体、表达构建体、宿主细胞、ar2调控试剂或药物组合物。
82.特别地,本发明涉及治疗ar相关障碍的方法。例如,本发明的方法和用途可以包括:抑制疾病状态,例如抑制其发展;和/或缓解疾病状态,例如导致疾病状态的消退,直到达到所需的终点。本发明的方法和用途可以包括ar相关障碍的症状的改善(例如减轻疼痛或不适),这种改善可以直接影响疾病或可以不直接影响疾病。本发明的方法和用途可以包括防止哺乳动物(例如人类)中发生ar障碍,特别是当这种哺乳动物易患ar障碍但尚未被诊断为患有ar障碍时。本发明的方法和用途可以包括将患者的ar活性和/或ar信号传导恢复到健康受试者的正常水平。
83.ar障碍是与异常ar活性相关的障碍。该障碍可以由增加的ar活性部分引起或加剧,例如由于毒性功能获得性ar突变体引起(例如在smba中)。例如,与健康受试者中的ar活性相比,这些障碍中的ar活性可以被增加≥50%(即50%或更多)、≥60%、≥70%、≥80%、≥90%、≥100%或≥200%。在这种情况下,通过本文所描述的ar变体抑制ar活性可以是有益的。
84.该障碍可以由减少的ar活性部分引起或加剧,例如由于功能丧失性ar变体引起(例如在雄激素不敏感综合征中)。例如,与健康受试者中的ar活性相比,这些障碍中的ar活性可以被减少≥50%(即50%或更多)、≥60%、≥70%、≥80%、≥90%或≥100%。在这种情况下,通过减轻其抑制,例如通过使用本文所描述的ar2调控试剂抑制ar2表达增加ar活性可以是有益的。
85.本发明的方法和用途可以包括确定来自患者的样本中ar和与障碍相关的ar突变体的表达和/或活性水平的步骤。确定ar和与障碍相关的ar突变体的表达和/或活性水平的方法是本领域已知的并且在本文所描述的实施例中举例说明(例如,参见图2a和2b)。例如,ar表达的水平可以通过检测和测量ar转录来测定。ar反式激活活性可以通过报告基因测定来测量,如荧光素酶测定,其包括:将在报告基因上游插入雄激素应答元件(are)的报告载体转染到细胞中,然后测量表达水平或报告基因。通过本领域已知的杂交或pcr技术可以分离并测试来自样本的rna。可替代地,ar2表达测定可以原位实施,即直接在从活检或切除物获得的患者组织的组织切片(固定和/或冷冻的)上实施,使得无需核酸纯化。也可以使用免疫测定。
86.本发明的方法和用途可以包括鉴定患有ar相关障碍的患者的步骤。鉴定患有ar相关障碍的患者的方法是本领域已知的。例如,可以对ar基因中的重复次数(例如,cag多聚谷氨酰胺和/或ggn多聚甘氨酸重复(repeat))或突变进行临床测试。结果表明,短的cag重复引起ar反式激活增加(例如在良性前列腺增生中),而较长的cag延伸导致活性降低(例如在
sbma中)。此外,它们在改变ar转录活性方面的作用已被认为累积地促成癌症风险与诊断年龄(age of diagnosis),例如在前列腺癌中。
87.患者可以是男性或女性。患者通常是男性。
88.患者可以患有ar相关障碍或可以有患ar相关障碍的风险。患者可以被鉴定为有患ar相关障碍的风险或患有ar相关障碍。患者可以是无症状的。患者可以易患ar相关障碍。该方法或用途可以包括鉴定患者是否有发展ar相关障碍的风险或患有ar相关障碍的步骤。
89.ar相关障碍的实例包括sbma、雄激素不敏感综合征、骨骼和/或代谢病症、前列腺癌、雄激素缺乏症、性腺机能减退、良性前列腺增生(bph)。ar相关障碍在本领域中是已知的,例如,在davey和grossmann(21)以及shukla等人(22)中综述。
90.脊髓延髓肌肉萎缩症(spinal bulbar muscular atrophy)
91.本发明涉及治疗脊髓延髓肌肉萎缩症(sbma)。
92.脊髓延髓肌肉萎缩症,也称为肯尼迪病,是一种x相关的疾病,其由ar基因中cag重复扩增引起,以运动神经元退化与原发性肌肉萎缩为特征。退化的运动神经元主要位于脊髓前角和延髓区域。多态性cag重复通常由9-36个重复组成;超过40个重复的扩增会导致神经毒性。sbma仅影响男性,其患病率为1/50:000。
93.在sbma患者中,神经肌肉症状通常首先表现为四肢、嘴和喉咙的肌肉痉挛与无力,由于运动神经元的丧失而向肌肉萎缩发展。目前尚无已知的sbma治愈方法,并且治疗方法是对症的,通常需要物理疗法与康复。患有sbma的患者在以后的生活中经常被限制在轮椅上,并且需要帮助完成日常任务,如进食。ar沉默长期以来一直作为一种有吸引力的治疗策略受到追寻,尽管它受到与ar功能丧失相关的直接和间接影响的阻碍。
94.本发明的方法和用途可以包括减轻与sbma相关的一种或多种症状,包括预防、延迟或减少:肌肉量(muscle mass)的丧失、活动能力的丧失和体力的丧失。本发明还可以涉及逆转受试者中雄激素不敏感的体征(sign)。
95.对于sbma,由本文所描述的ar变体抑制ar活性可以是有益的。因此,本发明提供了在用于治疗sbma的方法中使用的本文所描述的ar变体、表达构建体、宿主细胞和药物组合物。本发明还提供了本文所描述的ar变体、表达构建体、宿主细胞和药物组合物在治疗sbma的方法中的用途。本发明还提供了本文所描述的ar变体、表达构建体、宿主细胞和药物组合物在制备用于治疗sbma的方法的药剂中的用途。本发明还提供了一种使用本文所描述的ar变体、表达构建体、宿主细胞和药物组合物治疗sbma的方法。
96.雄激素不敏感综合征(androgen insensitivity syndrome)
97.本发明涉及治疗雄激素不敏感综合征,如完全雄激素不敏感(complete androgen insensitivity,cais)或部分雄激素不敏感(partial androgen insensitivity,pais)。
98.导致功能丧失性ar突变的ar基因中的错义和无义突变引起广谱的男性发育异常。这种异常的范围从轻微的男性化缺陷到完全的男性到女性的表型性别反转;这些突变导致完全雄激素不敏感(cais)或部分雄激素不敏感(pais)。
99.对于ais,通过减轻其抑制,例如,通过使用如本文所描述的ar2调控试剂或包含ar2调控试剂的药物组合物抑制ar2表达来增加ar活性可以是有益的。因此,本发明提供了如本文所描述的ar2调控试剂和包含ar2调控试剂的药物组合物,用于治疗ais的方法中使用。本发明还提供了如本文所描述的ar2调控试剂和包含ar2调控试剂的药物组合物在治疗
ais的方法中的用途。本发明还提供了如本文所描述的ar2调控试剂和包含ar2调控试剂的药物组合物在制备用于治疗ais的方法的药剂中的用途。本发明还提供了一种使用本文所描述的ar2调控试剂和包含ar2调控试剂的药物组合物治疗ais的方法。
100.骨骼/代谢病症
101.本发明涉及治疗骨骼或代谢病症,并且通常这些病症由减少的ar活性部分引起或加剧,例如由功能丧失性ar突变体引起。
102.可以用于本发明的骨骼或代谢病症包括骨质疏松症(如与年龄有关的骨质疏松症)、骨质减少症、糖皮质激素诱导的骨质疏松症、牙周病、hin消瘦、癌性恶病质、骨折、骨重建手术后的骨损伤、肌肉营养不良、肌肉减少症、虚弱(例如,减少的骨量、减少的肌肉量和较低的力量)、皮肤老化、男性性腺机能减退、女性绝经后症状、女性性功能障碍、卵巢功能早衰、自身免疫病、动脉粥样硬化、高胆固醇血症、高脂血症、再生障碍性贫血以及其它造血障碍、关节炎和关节修复。
103.对于这些骨骼或代谢病症,通过减轻其抑制,例如,通过使用如本文所描述的ar2调控试剂或包含ar2调控试剂的药物组合物抑制ar2表达来增加ar活性可以是有益的。因此,本发明提供了如本文所描述的ar2调控试剂和包含ar2调控试剂的药物组合物,用于治疗骨骼或代谢病症的方法中使用。本发明还提供了如本文所描述的ar2调控试剂和包含ar2调控试剂的药物组合物在治疗骨骼或代谢病症的方法中的用途。本发明还提供了如本文所描述的ar2调控试剂和包含ar2调控试剂的药物组合物在制备用于治疗骨骼或代谢病症的方法的药剂中的用途。本发明还提供了一种使用本文所描述的ar2调控试剂和包含ar2调控试剂的药物组合物治疗骨骼或代谢病症的方法。
104.前列腺癌
105.本发明涉及治疗前列腺癌。
106.前列腺发育和前列腺癌严重依赖于雄激素信号传导。事实上,雄激素剥夺疗法仍然是晚期前列腺癌患者最广泛使用的治疗方法。然而,虽然雄激素剥夺最初导致前列腺肿瘤消退,但肿瘤最终会重新出现,并且产生的激素难治(雄激素非依赖性)状态总是致命的。即使在获得去势抵抗后,前列腺肿瘤也依赖于ar信号传导。
107.评估肿瘤消退的方法是本领域已知的。例如,前列腺特异性抗原(psa)的水平随着前列腺癌的进展而增加。因此,本发明可以包括确定患者的psa水平以评估患者的前列腺癌的消退的步骤。
108.本发明提供了本文所描述的ar变体、表达构建体、宿主细胞、ar2调控试剂和药物组合物,用于治疗前列腺癌的方法中使用。本发明还提供了本文所描述的ar变体、表达构建体、宿主细胞、ar2调控试剂和药物组合物在治疗前列腺癌的方法中的用途。本发明还提供了本文所描述的ar变体、表达构建体、宿主细胞、ar2调控试剂和药物组合物在制备用于治疗前列腺癌的方法的药物中的用途。本发明还提供了一种使用本文所描述的ar变体、表达构建体、宿主细胞、ar2调控试剂和药物组合物治疗前列腺癌的方法。
109.药物组合物与剂量
110.本发明还提供了一种药物组合物,其包含本文所描述的ar变体、多核苷酸、表达构建体、宿主细胞或ar2调控试剂。本发明的药物组合物可以包含药学上可接受的赋形剂、载体、缓冲剂、稳定剂或本领域技术人员熟知的其它材料。这种材料通常是无毒的并且不会干
扰活性成分的功效。载体或其它材料的确切性质可以由技术人员根据施用途径确定。
111.该药物组合物通常以液体形式存在。液体药物组合物通常包含液体载体,如水、石油、动物油或植物油、矿物油或合成油。可以包含生理盐水溶液、氯化镁、葡萄糖或其它糖类溶液,或二醇类,如乙二醇、丙二醇或聚乙二醇。在某些情况下,可以使用表面活性剂,如0.001%的普朗尼克酸(pluronic acid)(pf68)。
112.对于在痛苦部位注射,活性成分将以无热原的并具有合适的ph、等渗性和稳定性的水溶液形式的形式存在。本领域相关技术人员能够很好地使用例如等渗媒介(如氯化钠注射液(sodium chloride injection)、林格注射液(ringer's injection)、乳酸钠林格注射液(lactated ringer's injection)、哈特曼氏溶液(hartmann's solution))制备合适的溶液。根据需要,可以包含防腐剂、稳定剂、缓冲剂、抗氧化剂和/或其它添加剂。
113.为了延缓释放,载体可以包含在配制用于缓慢释放的药物组合物中,如根据本领域已知的方法在由生物相容性聚合物形成的微胶囊中或在脂质体载体系统中。
114.剂量和剂量方案可以在负责组合物的施用的医师的正常技能范围内确定。例如,出于治疗目的,会对此类受试者施用治疗有效量的根据本发明的表达构建体、宿主细胞、ar2调控试剂或药物组合物。治疗有效量是有效改善障碍的一种或多种症状的量。
115.剂量可以根据各种参数确定,特别是根据待治疗的患者的年龄、体重和状况,施用的途径,以及所需的治疗方案确定。医师将能够确定任何特定患者所需的施用的途径与剂量。剂量可以提供为单次剂量,但可以重复或在载体可能未靶向正确区域和/或组织的情况下(如手术并发症)。治疗方法优选为单次永久性治疗,但例如在未来几年重复注射。
116.一旦受试者中已出现了ar相关障碍的症状,就可以进行施用,例如以治疗疾病的现有症状。
117.联合疗法
118.根据本发明的ar变体、多核苷酸、表达构建体、宿主细胞、ar2调控试剂和/或药物组合物可以组合使用,和/或与用于治疗ar相关障碍的任何其它疗法组合使用。
119.其它
120.应当理解,本文使用的术语仅仅是出于描述本发明的特定实施方式的目的,而并非旨在限制。
121.此外,如在本说明书和所附权利要求书中使用的,单数形式的“一个(a)”、“一种(an)”和“所述(the)”包括复数形式提及,除非内容另有明确规定。因此,例如,提及“一种表达构建体”包括“多种表达构建体”,即包括两种或更多种表达构建体。
122.术语“约(about)”或“大约(approximately)”是指在由本领域普通技术人员确定的特定值的可接受的误差范围内,这将部分取决于如何测量或确定该值,即测量系统的限度。例如,根据本领域的实践,“约”可以表示在1个或超过1个标准偏差内。可替代地,“约”可以表示给定值的高达20%的范围,优选高达10%、更优选高达5%、并且仍然更优选高达1%的范围。可替代地,特别是关于生物系统或过程,该术语可以表示在一个值的数量级以内,优选在5倍以内,并且更优选在2倍以内。在本技术和权利要求书中描述了特定值的情况下,除非另有说明,否则术语“约”的含义应假设在该特定值的可接受误差范围内。
123.如本文所使用的“ar变体”是一个统称,是指不同于人类ar(ensp00000363822)(seq id no:6)的任何多肽,在本文中也称为ar1,并且保留了ar的至少一些生物活性(例
如,能够二聚化、能够结合雄激素、能够结合雄激素应答元件(are)和/或能够反式激活)。因此,术语“ar变体”包括如本文所描述的ar2及其变体。
124.此外,当在本文中提及“≥x”时,这意味着等于或大于x。
125.可以使用任何合适的算法计算序列同一性。例如,pileup和blast算法可以用于计算同一性或排列序列(如鉴定等同的或对应的序列(通常在其默认设置上)),例如,如altschul(23;24)中所述。用于实施blast分析的软件通过国家生物技术信息中心(national center for biotechnology information)可公开获得(http://www.ncbi.nlm.nih.gov/)。这种算法首先通过鉴定当与数据库序列中相同长度的词对齐时查询序列中长度为w的匹配或满足某个正值阈值得分t的短词来鉴定高得分序列对(hsp)。t被称为邻域词得分阈值(上文的altschul等人)。这些初始邻域词命中(word hit)作为启动搜索的种子,以查找包含它们的hsp。词命中沿着每个序列在两个方向上扩展,只要可以增加累积比对得分。在以下情况下,在每个方向上的词命中扩展都停止:累积比对得分从其最大达到值下降了数量x;由于一个或多个负得分残基比对的累积,累积得分变为零或更低;或到达任一序列的末端。blast算法参数w、t和x确定比对的灵敏度和速度。blast程序默认使用11的词长(w),50的blosum62评分矩阵(25)比对(b),10的期望(e),m=5,n=4,以及两条链的比较。
126.blast算法对两个序列之间的相似性实施统计分析;例如,参见参考文献26。由blast算法提供的一种相似性度量是最小和概率(p(n)),其提供了两个多核苷酸或氨基酸序列之间偶然发生匹配的概率的指示。例如,如果第一个序列与第二个序列比较的最小和概率小于约1,优选小于约0.1,更优选小于约0.01,并且最优选小于约0.001,则认为一个序列与另一个序列相似。可替代地,uwgcg包提供了可用于计算同一性的bestfit程序(例如在其默认设置上使用)(27)。
127.本文引用的所有出版物、专利和专利申请,无论是上文还是下文,均通过引用以其整体并入本文。
128.本发明将在以下实施例中进一步描述,这些实施例并不限制权利要求中描述的本发明的范围。
129.实施例
130.实施例1
131.材料和方法
132.小鼠
133.分析中仅使用雄性小鼠。
134.使用了ar100q26和bac ar121q131转基因动物。
135.为了在小鼠中表达ar2,使用了双启动子aav载体质粒(由signagen实验室提供(rockville,md))。这些质粒含有表达盒,该表达盒由人类延伸因子-1α(eif1α)启动子,随后是ar2 cdna或模拟物序列和人类巨细胞病毒(cmv)启动子,随后是编码gfp的cdna组成。将10
11
个载体基因组(vg)的病毒载量注射到sbma ar100q小鼠的尾静脉中。
136.对于敲低实验,对bac ar121q小鼠皮下注射悬浮于pbs(100μl)中的20mg/kg sirna。每周使用吊线和力量计(bioseb)记录体重、转棒和握力。
137.细胞系与试剂
138.使用了hek293t细胞(atcc)、mcf7细胞(atcc)、永生化的人类成肌细胞(mrc cnmd生物银行伦敦l954/1284m-i)。
139.根据公布的方案(grunseich c,2014),培养诱导的多能性干细胞并使其分化为运动神经元样细胞。
140.通过在各自的细胞培养基中添加二氢睾酮(dht,sigma-aldrich)至终浓度为10nm以实施ar诱导。对未诱导的对照添加等体积的乙醇。
141.分析了来自对照和sbma患者来源的原代成肌细胞的细胞裂解物。
142.人类样本
143.使用了匿名的脑组织:cgnd_hra_00063、cgnd_hra_00218、cgnd_hra_00224、cgnd_hra_00035、cgnd_hra_00236、cgnd_hra_00399、cgnd_hra_00400、cgnd_hra_00402、cgnd_hra_00411、cgnd_hra_00412、cgnd_hra_00654、cgnd_hra_00655、cgnd_hra_00657、cgnd_hra_00091。
144.质粒构建
145.为了生成不同的ar fl(12q)、ar fl(55q)和ar2构建体,分别扩增ar fl(12q)、ar fl(55q)和ar2 cdna并将其克隆到在巨细胞病毒启动子下的哺乳动物表达载体中,具有或不具有n端flag表位标签。
146.为了生成nanobret融合构建体,pcr扩增子被分别克隆到pfn21a halotag cmv flexi、pfc14k halotag cmv flexi、pfn31k nluc cmv-neo flexi和pfc32k nluc cmv-neo flexi载体中(promega)。通过定点诱变(site-directed mutagenesis)生成在ar的fxxlf基序(f23,27a/l26a)或(g21e)、d盒(a596t/s597t)或dna结合结构域(a574d)处具有突变的突变构建体。
147.荧光素酶报告分析
148.为了确定ar2对ar依赖性转录活性的影响,用0.5μg pare-e1b-luc(在luc2基因上游插入雄激素应答元件(are)的荧光素酶报告载体)、0.5μg prl-tk(海肾荧光素酶(renilla luciferae)对照)(promega)和0.5μg ar fl和/或ar2载体质粒瞬时转染hek293t细胞。转染24小时后,洗涤细胞并用dht处理或等体积乙醇处理作为阴性对照。24小时后收获细胞,加入萤火虫(firefly)和海肾荧光素酶底物(双荧光素酶报告基因测定,promega),并且根据制造商的方案,使用微孔板分光光度计测量荧光素酶活性。海肾荧光素酶活性用作内部标准化对照。
149.nanobret测定
150.为了研究ar fl蛋白和ar2蛋白之间的相互作用,实施了nanobret测定(promega nanobrettm蛋白质:蛋白质相互作用系统)。简而言之,hek293t细胞用nanoluc荧光素酶(nluc)融合质粒和具有阳离子脂质体(lipofectamine)2000试剂的halotag融合质粒共转染。nluc-mdm2和p53-halotag对被包括作为阳性对照,而nluc-mdm2和halotag-smad4对作为阴性对照。在转染后24小时,使用或不使用10nm dht处理细胞。添加了halotag nanobret 618配体或dmso(无配体对照)。在24小时,添加nanobret nano-glo底物,并且在460nm和618nm得到nanobret读数。使用下式计算以millibret为单位的平均校正的nanobret比率:平均校正的nanobret比率(millibret)=[(618nmem/460nmem)实验值-(618nmem/460nmem)无配体对照]
×
1000
[0151]
染色质免疫沉淀(chip)
[0152]
在用flag-ar2质粒瞬时转染的mcf7细胞上实施ar2 chip。未转染的mcf7细胞被包括作为阴性对照。转染后24小时用10nm dht处理细胞。在48小时,细胞用1%甲醛交联并收获和裂解。使用300μg染色质和14μg抗flag抗体(sigma aldrich f1804)或抗兔igg抗体(cell signaling technology,2729)如(28)中所述进行实验。
[0153]
如(29)中所述,使用pol ii抗体(santa cruz biotechnology,sc-9001)对dht处理的人类成肌细胞实施rna pol ii chip。纯化的dna样本用于半定量实时pcr。
[0154]
rna和cdna制备与实时定量pcr(rt-qpcr)
[0155]
将10mg肌肉或脊髓组织均质化。分离总rna。1μg rna用于用高容量cdna逆转录试剂盒(applied biosystems)的cdna合成。使用20-50ng dna模板,采用快速sybr green master mix或taqman基因表达master mix(applied biosystems)建立rt-qpcr反应。
[0156]
人类成肌细胞中的ar2过表达与敲低
[0157]
对于ar2过表达实验,用1μg flag-ar2或空载体瞬时转染人类成肌细胞,并在转染后24小时用或不用dht处理。
[0158]
对于ar2敲低实验,将人类成肌细胞用1μm ar2靶向sirna(sbma-1)或非靶向sirna对照(ntt)处理48小时。转染后24小时向细胞中加入10nm dht。如参考文献30所述,使用修饰的(2'-f,2'-ome)亚磷酰胺与标准保护基团和胆固醇缀合物合成sirna。
[0159]
rna测序文库的生成
[0160]
对于人类组织,使用illumina truseq stranded total rna试剂盒从500ng总rna中制备rna测序文库。使用illumina hiseq 4000平台,对每个样本40m读数对的目标深度进行配对末端(2
×
150bp)测序。
[0161]
对于ipsc衍生的运动神经元,使用rna测序stranded ribozero gold从500ng总rna中制备rna测序文库。使用illumina hiseq 4000平台,对每个样本100m读数对的目标深度进行配对末端(2
×
75bp)测序。
[0162]
对于ar2过表达或敲低的人类成肌细胞,使用1.5μg总rna和ultra
tm iidirectional rna library prep kit for illumina生成mrna文库。
[0163]
在illumina hiseq 4000平台上对文库进行多路复用(multiplexed)、qc和双末端(pair-end)测序。
[0164]
rna测序分析流程
[0165]
对于大脑和ipsc数据集,使用fastqc工具(https://www.bioinformatics.babraham.ac.uk/projects/fastqc/)对每个样本的配对末端序列文件(.fastq)进行质量检验,然后使用trimmoma tic工具(http://www.usadellab.org/cms/?page=trimmomatic)剪辑(truseq3-pe-2.fa:2:30:10)并修剪连接物(adaptor)以去除5'核苷酸偏差(headcrop:12)与低质量调用(trailing:20slidingwindow:4:20minlen:15)。每个样本的完整保存的读数对被参考映射到人类基因组(grch38.82)的目前实例。以每千碱基百万转录本(transcripts per kilobase million,tpm)单位的每个已知的注释基因(homo_sapiens.grch38.82.chr.gtf)的表达被2固定(ped estalled),然后进行log2转换。至少一个样本的转换后表达值不大于1的基因作为未检测到而被丢弃,而未丢弃的基因跨样本的表达被分位数标准化。为了确保标准化后数据的质量,使用tukey箱线图、基于协方差的pca
散点图和基于相关性的热图实施探索性检查。为了去除噪声偏差的表达值,局部加权散点图平滑(lowess)被按样本类别应用于所有基因的标准化表达(变异系数~平均表达)。然后对lowess拟合进行过度绘制(over-plotted)并检查,以鉴定平均表达(即“信号”)和变异系数(即“噪声”)之间的关系严重偏离线性的常见低端表达值。如果小于该值,则将表达值降低以等于该值,而对于至少一个样本而言,未观察到大于该值的基因的表达被作为噪声偏差丢弃。对于未被丢弃的基因,在benjamini-hochberg(bh)错误发现率(false discovery rate,fdr)多重比较校正(multiple comparis on correction,mcc)条件下,使用样本类别作为因子,使用单因素方差分析(one-factor analysis of variance,anova)检验对样本类别之间的表达差异进行了测试。然后通过该测试将具有iii型校正p《0.05的基因作为子集,并且使用tukeyhsd事后测试为每个可能的类别成对比较生成平均差值和p值。对于特定比较具有事后p《0.05和对于相同比较具有均值线性差值≥1.5x的基因被认为在所比较的类别之间分别具有显著不同的表达。测试后,通过基于协方差的pca散点图和基于pearson相关性的聚类热图,使用被认为在至少两个类别之间具有显著表达差异的基因的独有联合来研究样本-样本的关系。
[0166]
对于人类成肌细胞数据集,序列读数为连接物和用trim galore!(v 0.4.1,https://github.com/felixkrueger/trimgalore)修剪的质量。用fastqc(v 0.11.7,https://www.bioinformatics.babraham.ac.uk/projects/fastqc/)和multiqc(v 0.9)对原始读数和修剪的读数完成质量控制(31)。然后用salmon(v 0.12)将修剪的读数与人类参考转录组(gencode v29,https://www.gencodegenes.org/human/release_29.html)对齐(32)。使用tximport包(v 1.12.3)将得到的量化文件组合并读入r(33),并且用deseq2(v 1.24)实施差异表达分析38。使用fgsea包(v 1.10.0)对差异表达的基因实施通路分析(34)。
[0167]
为了从具有ar2过表达的人类成肌细胞中的711个差异调控的基因缩小到与sbma相关的基因列表,这些基因与两个可公开获得的鼠科sbma肌肉转录组数据集重叠29,30。只有来自这两个列表的倍数变化超过1.5的基因被包括在分析中。得到的57个基因用于评估ar100q转基因小鼠在aav9-ar2处理后的转录变化。
[0168]
环己酰亚胺追踪测定
[0169]
用1μg flag-ar2质粒转染mcf7细胞。转染后8小时,用10nm dht或等体积乙醇处理细胞。12小时后,将100μg环己酰亚胺的dmso溶液(sigma-aldrich)添加到细胞中(t=0),并在0和24小时收获细胞用于蛋白质表达分析。包括用环己酰亚胺处理的未转染的mcf7细胞进行比较。
[0170]
免疫印迹法,elisa
[0171]
对于免疫印迹分析,蛋白质在nupage 10%bis-tris凝胶(invitrogen)上分离,并且使用invitrogen novex xcell surelock迷你细胞和xcell ii印迹模块转移到pvdf膜上。将膜与1:1000稀释度的一抗、抗ar抗体(santa cruz,h-280或abcam,ab52615)、抗微管蛋白(abcam,ab6160)或抗黏着斑蛋白(sigma-aldrich,hvin-1)孵育过夜,然后与1:10000稀释度的二抗、抗小鼠hrp缀合的抗体(invitrogen,62-6520)或抗兔hrp缀合的抗体(invitrogen,31460)孵育1小时。
[0172]
对于co-ip实验,细胞被裂解并离心。将上清液于4℃与抗flag m2缀合的磁珠
(sigma-aldrich,m8823)或未标记的磁珠(chromotek bab-20)作为对照一起孵育过夜。磁珠用清洗缓冲液[tris-hcl 0.1m,nacl 0.3m,triton x-100 1%(v/v),ph 7.5]清洗3次,然后用1
×
样本缓冲液洗脱,在sds-page凝胶上分离,并按照标准方案通过免疫印迹进行分析。
[0173]
根据制造商的方案,使用睾酮参数测定试剂盒(testosterone parameter assay kit)(r&dsystems kge010)测量11周龄的ar2处理的ar100q小鼠与模拟物处理的ar100q小鼠的血清睾酮水平。
[0174]
免疫荧光与免疫组织化学
[0175]
对于免疫荧光实验,脊髓和股四头肌的切片在0.1%triton-x 100中透化,并在具有4%bsa和2%ngs的pbs中封闭。将切片以1:100稀释度与抗ncam(proteintech,14255-1-ap)抗体、抗psa-ncam(emd millipore,5324)抗体或抗泛素(abcam,ab7780)抗体于4℃孵育过夜,然后用合适的alexa fluor缀合的二抗(thermofisher scientific,1:1000)孵育1小时(20-25℃)。为了确定内含物的数量,组织切片使用mouse on mouse basic试剂盒(vector laboratories bmk-2202)用1c2抗体(emd millipore,5tf1-1c2,1:5000)染色。
[0176]
为了量化,使用caseviewer软件取得了至少4个连续切片的图像,并由盲测调查员使用fiji软件对处理进行分析40。
[0177]
ar2 sirna筛选
[0178]
如(35)所述设计并合成一组靶向对ar2转录物特异性的所有可能区域的11种sirna和一种非靶向对照sirna(ntt)。这些sirna在表1中提供。这些sirna中的每一个的正义链和反义链分别对应于seq id no:9-30中的序列。将1μm sirna-ar2或sirna-ntt添加到mcf7细胞中。从细胞中提取总rna。如前一部分中所述制备cdna并且实施rt-qpcr,使用对ar1特异性的fam标记的taqman芯片(array)hs04272731_s1、对ar2特异性的hs04275959_m1以及对gapdh特异性的hs99999905_m1用于标准化。
[0179]
表1:靶向ar2的sirna。as=反义;s=正义;m=2’ome;f=2’f;p=磷酸盐;#=硫代磷酸酯键(linkage)
[0180]
[0181]
[0182][0183]
统计分析
[0184]
通过kaplan-meier估计确定sbma小鼠的存活率、发病时间和跌落潜伏期(latency to fall),并且与对数秩检验进行比较。进行单向方差分析(anova)以比较处理对动物体重的影响,使用处理作为受试者间因素并使用时间作为受试者内因素。所有其它数据在所表示处通过双尾或单尾t检验分析。
[0185]
ar变体在人脑中的表达
[0186]
确定了人脑中ar变体表达的生理水平。通过使用来自人类内侧和外侧运动皮层、颈椎和腰椎脊髓以及ips衍生的运动神经元的rna,以高测序深度(>1亿每读数)采用rna测序,发明人发现,与经典的剪接变体1(enst00000374690;ar1)相比,ar剪接变体2(enst00000396043;ar2)是最高表达的ar变体(图1a)。与对照组相比,来自sbma患者的运动神经元没有观察到差异。有趣的是,发现ar2在雄激素应答组织中特别丰富,如前列腺和肌肉,表明在ar调控中的作用(图1b)。
[0187]
发明人证实,与来自对照和sbma受试者的人类成肌细胞中的ar1相比,它的表达水平更高(图1c)。ar2是一种天然存在的变体,最初是通过人类胎盘组织中的cdna末端的快速扩增(race)鉴定的(17)。发现ar2 mrna来源于包含位于外显子1的下游22.1kb的替代性外显子1(外显子1b)(图1d)。如dnase i超敏性与chip-seq追踪以及通过染色质免疫沉淀测定定量pol ii在外显子1b上的占据率所示(图1e),该染色质基因座在功能上是可使用的并且被主动转录。外显子1b和侧翼区的多序列分析表明与恒河猴(rhesus macaque)具有接近100%的同源性,并且在小鼠和大鼠中保守性较差,其中起始密码子下游的终止密码子推断出这些物种中不存在ar2剪接变体(18)。本发明人证实在野生型动物中不表达ar2。含有代替经典ntd的独有的n端序列的编码的蛋白质具有45kda的分子质量,因此ar2也称为ar45(17)(图1f)。
[0188]
ar2在ar生物学中的作用
[0189]
发明人接下来继续表征了ar2在ar生物学中的作用。ar2导致响应于dht的全长ar转录活性的剂量依赖性抑制,并且通过在转基因中引入dbd失活替换a574d消除了这种效应(图2a;图2b)。总的来说,这些发现表明ar2对ar反式激活的影响是选择性的,并且需要与dna结合(图2a)。值得注意的是,单独的ar2不能激活转录(图2a)。转录的激活需要ar二聚化,其主要经由fxxlf基序通过n/c端相互作用和经由二聚化盒(d-box)通过dbd/dbd相互作用介导(19)。
[0190]
因为dbd和lbd是保守的,所以发明人假设ar也可以与ar2形成异源二聚体。发明人通过使用允许实时检测复合物形成的生物发光共振能量转移(bret)测定来测试此假设
(20)。n端与c端融合构建体的所有组合都被转染到无ar(ar-null)细胞中,并选择表现出最高bret信号的组合之一用于进一步分析。bret饱和曲线表明特异性蛋白质-蛋白质相互作用。fxxlf基序(f23,27a/l26a;f-mut)或该基序的n端(g21e)而非d-盒基序(a596t/s597t;d-mut)的突变抑制了ar/ar2二聚化(图2c)。有趣的是,发明人还发现ar2形成同源二聚体。通过免疫共沉淀测定进一步证明了ar/ar2相互作用。
[0191]
ar蛋白质水平不受环己酰亚胺追踪实验中ar2存在的影响,这表明ar2不会改变ar蛋白质的稳态(steady state)。
[0192]
ar2功能
[0193]
为了更好地描述ar2功能,发明人接下来概述了ar2过表达(oe)或敲低(kd)的人类成肌细胞中的基因表达。首先,发明人设计了小干扰rna(sirna)、跨越外显子1b序列的11种组合。为了改进它们的药代动力学性质,这些sirna进行了化学修饰和脂质缀合(21)。这些sirna导致内源性ar2的选择性沉默(范围从45%到90%)(图2d)。qrt-pcr证实了使用最佳表现的sirna的ar2过表达和敲低。对表达数据的主成分分析(pca)显示了根据处理的样本的聚类。使用差异表达分析(deseq;p《0.05,倍数变化》1.5),发明人观察到在ar2过表达(63%)和敲低(59%)时上调的转录物数量略多。用于鉴定与ar2调控基因相关的生物过程的基因集富集分析表明,在ar2 oe样本中与ar应答相关的基因下调,而在ar2 kd中观察到相反趋势。在差异表达的基因列表中,发现oe和kd数据集中的31%和32%分别在启动子区域中包含are序列(图2e)。此外,ar2 oe成肌细胞中的若干个ar靶基因,例如mybph(集群1)、c3(集群2)、myl4、casq2、igf2(集群3),与基因组ar敲除小鼠的肌肉相比,显示出相同的失调模式(22)(图2f)。值得注意的是,内源性ar2的敲除导致hspa8的下调与nfe2l1的上调,hspa8是伴侣辅助选择性自噬复合物的成员,nfe2l1是蛋白酶体亚基的主要调节物,有趣的是,这表明ar2可能有助于阻碍雄激素诱导的细胞应激信号(23,24)(图2g)。
[0194]
为了研究ar和ar2是否共同占据相同的基因组位点,发明人对已知的ar靶基因(greb1、znf485和ehf)进行了chip实验(25)。发明人检测到阳性信号富集(图2h),表明在are基因座处的剪接变体的功能相互作用。发明人证实ar2的过表达导致这些靶标的反式激活减少。总之,这些结果表明ar2与ar形成异源二聚体并抑制ar应答基因的转录(图2i)。
[0195]
ar2过表达改善sbma小鼠中的疾病表型
[0196]
鉴于其作为ar活性的转录抑制因子的作用,发明人假设ar2的过表达能够改善sbma小鼠的疾病表型。对5周龄的雄性转基因小鼠外周注射编码ar2 cdna的aav9、绿色荧光蛋白(gfp)或盐水(图3a)。该模型表达聚q ar转基因(ar100q)并表现出疾病相关的表型(26)。从大约7周龄开始,与非转基因同窝小鼠相比,这些小鼠在存活率、体重和转棒活性方面表现出快速的雄激素依赖性下降(26)。处理导致广泛的转导,特别是在肌肉中,这是该疾病的主要病理部位(27,28),如注射后6周的高ar2表达所示。
[0197]
ar2过表达显著延长存活率(图3b),延迟疾病发作(图3c),改善的体重减轻(图3d)和转棒活性(图3e)。此外,发明人观察到骨骼肌的病理外观的显著改善(图3f),ncam/psa-ncam染色的共定位减少,ncam/psa-ncam染色是去神经/再神经支配活性的标记,这与神经肌肉表型的改善一致(图3g)。ar2处理的小鼠具有正常水平的血清睾酮。
[0198]
正如预期的那样,在脊髓和骨骼肌中,未观察到ar蛋白质水平以及泛素阳性(图3h)和polyq阳性(图3i)内含物的数量改变,这支持一种模型,其中疗效可以独立于polyq介
导的蛋白质毒性(proteotoxicity)来实现。
[0199]
为了证实剪接变体过表达的分子活性,发明人在sbma小鼠的已知失调转录物中选择了脊髓中的两个基因(megf10,nqo1)与肌肉中的五个基因(cacng1,chrna1,mybpc2,mybph,tnnt3,unc45b)(29,30),这些基因在人类成肌细胞的oe数据集中被上调,并且证实了体内ar2处理后的表达的统计学显著增加(图3j)。
[0200]
sirna ar2处理加剧了运动功能
[0201]
发明人用靶向ar2的脂质缀合的sirna处理了一组携带完整ar基因(27)并因此内源表达此剪接变体的雄性转基因小鼠。
[0202]
表2显示了本研究的正义和反义ar2靶向与模拟物序列。靶向ar2的sirna的正义链(s)的序列也在seq id no:31中提供。靶向ar2的sirna的反义链(as)的序列也在seq id no:32中提供。模拟物sirna的正义链(s)的序列也在seq id no:32中提供。模拟物sirna的反义链(as)的序列也在seq id no:34中提供。磷酸胆碱二十二烷酸(pc-dca)缀合物共价连接到sirna正义链的3'端。
[0203]
表2:本研究中使用的sirna。as=反义;s=正义;m=2’ome;f=2’f;p=磷酸盐;#=硫代磷酸酯键;pc-dca=磷酸胆碱二十二烷酸;vp=乙烯基膦酸酯
[0204][0205]
以20mg/kg重复皮下注射导致肌肉中ar2水平在最后一次注射后6周仍然持续减少(图4a),并确定神经肌肉表型恶化(图4b-d),进一步证实ar2过表达有益于sbma。
[0206]
总之,发明人证明,ar剪接变体2通过与全长ar异源二聚体化并结合至其特异性基因组靶标,作为转录因子诱饵,调控ar活性。此外,发明人将这种变体的治疗调控确立为治疗sbma和其它具有高转化潜力的ar相关障碍的新范例。
[0207]
实施例2
[0208]
为了进一步评估ar剪接变体2(ar2;也称为ar45)的治疗能力,实施例1中涉及sbma小鼠(n=8)的aav9-ar2处理的实验被扩展以将小鼠数量增加到每个处理组15只小鼠,该组数量与全面的临床前试验的数量相当。
[0209]
如实施例1中所述,对sbma小鼠注射编码ar2 cdna的aav9或绿色荧光蛋白(gfp),或生理盐水。如实施例1中所述,观察这些小鼠的存活率、体重、握力和转棒活性。
[0210]
结果表明,sbma小鼠的aav9-ar2(图中称为aav9-ar45)处理显著延长了寿命(图
5a),延迟了疾病发作(图5b),改善了体重减轻(图5c)、握力(图5d)和转棒活性(图5e)。
[0211]
这些结果与实施例1中的观察结果一致,表明ar2处理能够改善sbma和其它ar相关障碍的疾病表型。
[0212]
参考文献
[0213]
1 grunseich等,lancet neurol.2018dec;17:1043-1052
[0214]
2 cunningham等science 244,1081-1085(1989)
[0215]
3 sambrook等,molecular cloning:a laboratory manual,csh press 1989,pp.15.3
–
15.108
[0216]
4 wang等,gene therapy 15,1489-1499(2008)
[0217]
5 goldspiel等,clinical pharmacy 12:488-505(1993)
[0218]
6 wu and wu,biotherapy 3:87-95(1991)
[0219]
7 tolstoshev,ann.rev.pharmacol.toxicol.32:573-596(1993)
[0220]
8 mulligan,science 260:926-932(1993)
[0221]
9 morgan and anderson,ann.rev.biochem.62:191-217(1993)
[0222]
10 may,tibtech 1 1(5):155-215(1993)
[0223]
11 ausubel等(eds.),current protocols in molecular biology,john wiley&sons,ny(1993)
[0224]
12 kriegler,gene transfer and expression,a laboratory manual,stockton press,ny(1990)
[0225]
13 wu and wu,j biol.chem.262:4429-4432(1987)
[0226]
14 wo 92/06180
[0227]
15 koller and smithies,proc.natl.acad.sci.usa 86:8932-8935(1989)
[0228]
16 zijlstra等,nature 342:435-438(1989)
[0229]
17 wo 94/08598
[0230]
18 stemple and anderson,cell 71:973-985(1992)
[0231]
19 rheinwald,meth.cell bio.21a:229(1980)
[0232]
20 pittelkow and scott,mayo clinic proc.61:771(1986)
[0233]
21 davey and grossmann,clin.biochem.rev.37(1)(2016)
[0234]
22 shukla等,andrology,4,366-381(2016)
[0235]
23 altschul,j mol evol.1993mar;36(3):290-300
[0236]
24 altschul,j mol biol.1990oct 5;215(3):403-10
[0237]
25 henikoff and henikoff(1992)pnas 15:10915-9
[0238]
26 karlin and altschul(1993)pnas 15:5873-7
[0239]
27 devereux等(1984)nucleic acids res.12:387-395
[0240]
28 schmidt,等,methods 48,240
–
248(2009)
[0241]
29 burger等nucleic acids res.47,3467
–
3484(2019)
[0242]
30 haraszti等.nucleic acids res.45,7581
–
7592(2017)
[0243]
31 haraszti等.nucleic acids res.45,7581
–
7592(2017)
[0244]
32 patro等,nat.methods 14,417
–
419(2017)
[0245]
33 soneson等,f1000research 4,1521(2016)
[0246]
34 sergushichev等,biorxiv 060012(2016)
[0247]
35 turanov等.nat.biotechnol.36,1164
–
1173(2018)
[0248]
序列信息
[0249]
seq id no:1-ar变体的多肽序列
[0250]
pqktclicgdeasgchygaltcgsckvffkraaegkqkylcasrndctidkfrrkncpscrlrkcyeagmtlgarklkklgnlklqeegeassttspteettqkltvshiegyecqpiflnvleaiepgvvcaghdnnqpdsfaallsslnelgerqlvhvvkwakalpgfrnlhvddqmaviqyswmglmvfamgwrsftnvnsrmlyfapdlvfneyrmhksrmysqcvrmrhlsqefgwlqitpqeflcmkalllfsiipvdglknqkffdelrmnyikeldriiackrknptscsrrfyqltklldsvqpiarelhqftfdllikshmvsvdfpemmaeiisvqvpkilsgkvkpiyfhtq
[0251]
seq id no:2-编码seq id no:1的ar变体的cdna
[0252]
ccccagaagacctgcctgatctgtggagatgaagcttctgggtgtcactatggagctctcacatgtggaagctgcaaggtcttcttcaaaagagccgctgaagggaaacagaagtacctgtgcgccagcagaaatgattgcactattgataaattccgaaggaaaaattgtccatcttgtcgtcttcggaaatgttatgaagcagggatgactctgggagcccggaagctgaagaaacttggtaatctgaaactacaggaggaaggagaggcttccagcaccaccagccccactgaggagacaacccagaagctgacagtgtcacacattgaaggctatgaatgtcagcccatctttctgaatgtcctggaagccattgagccaggtgtagtgtgtgctggacacgacaacaaccagcccgactcctttgcagccttgctctctagcctcaatgaactgggagagagacagcttgtacacgtggtcaagtgggccaaggccttgcctggcttccgcaacttacacgtggacgaccagatggctgtcattcagtactcctggatggggctcatggtgtttgccatgggctggcgatccttcaccaatgtcaactccaggatgctctacttcgcccctgatctggttttcaatgagtaccgcatgcacaagtcccggatgtacagccagtgtgtccgaatgaggcacctctctcaagagtttggatggctccaaatcaccccccaggaattcctgtgcatgaaagcactgctactcttcagcattattccagtggatgggctgaaaaatcaaaaattctttgatgaacttcgaatgaactacatcaaggaactcgatcgtatcattgcatgcaaaagaaaaaatcccacatcctgctcaagacgcttctaccagctcaccaagctcctggactccgtgcagcctattgcgagagagctgcatcagttcacttttgacctgctaatcaagtcacacatggtgagcgtggactttccggaaatgatggcagagatcatctctgtgcaagtgcccaagatcctttctgggaaagtcaagcccatctatttccacacccagtga
[0253]
seq id no:3-人类ar2的多肽序列(ensp00000379358)
[0254]
milwlhsletardhvlpidyyfppqktclicgdeasgchygaltcgsckvffkraaegkqkylcasrndctidkfrrkncpscrlrkcyeagmtlgarklkklgnlklqeegeassttspteettqkltvshiegyecqpiflnvleaiepgvvcaghdnnqpdsfaallsslnelgerqlvhvvkwakalpgfrnlhvddqmaviqyswmglmvfamgwrsftnvnsrmlyfapdlvfneyrmhksrmysqcvrmrhlsqefgwlqitpqeflcmkalllfsiipvdglknqkffdelrmnyikeldriiackrknptscsrrfyqltklldsvqpiarelhqftfdllikshmvsvdfpemmaeiisvqvpkilsgkvkpiyfhtq
[0255]
seq id no:4-人类ar2的cdna序列
[0256]
atgatactctggcttcacagtttggagactgccagggaccatgttttgcccattgactattactttccaccccagaagacctgcctgatctgtggagatgaagcttctgggtgtcactatggagctctcacatgtggaagctgcaaggtcttcttcaaaagagccgctgaagggaaacagaagtacctgtgcgccagcagaaatgattgcactattgataaattccgaaggaaaaattgtccatcttgtcgtcttcggaaatgttatgaagcagggatgactctgggagcccggaagctgaagaaacttggtaatctgaaactacaggaggaaggagaggcttccagcaccaccagccccactgaggagacaaccca
gaagctgacagtgtcacacattgaaggctatgaatgtcagcccatctttctgaatgtcctggaagccattgagccaggtgtagtgtgtgctggacacgacaacaaccagcccgactcctttgcagccttgctctctagcctcaatgaactgggagagagacagcttgtacacgtggtcaagtgggccaaggccttgcctggcttccgcaacttacacgtggacgaccagatggctgtcattcagtactcctggatggggctcatggtgtttgccatgggctggcgatccttcaccaatgtcaactccaggatgctctacttcgcccctgatctggttttcaatgagtaccgcatgcacaagtcccggatgtacagccagtgtgtccgaatgaggcacctctctcaagagtttggatggctccaaatcaccccccaggaattcctgtgcatgaaagcactgctactcttcagcattattccagtggatgggctgaaaaatcaaaaattctttgatgaacttcgaatgaactacatcaaggaactcgatcgtatcattgcatgcaaaagaaaaaatcccacatcctgctcaagacgcttctaccagctcaccaagctcctggactccgtgcagcctattgcgagagagctgcatcagttcacttttgacctgctaatcaagtcacacatggtgagcgtggactttccggaaatgatggcagagatcatctctgtgcaagtgcccaagatcctttctgggaaagtcaagcccatctatttccacacccagtga
[0257]
seq id no:5-人类ar的ntd的多肽序列
[0258]
mevqlglgrvyprppsktyrgafqnlfqsvreviqnpgprhpeaasaappgasllllqqqqqqqqqqqqqqqqqqqqqqqetsprqqqqqqgedgspqahrrgptgylvldeeqqpsqpqsalechpergcvpepgaavaaskglpqqlpappdeddsaapstlsllgptfpglsscsadlkdilseastmqllqqqqqeavsegsssgrareasgaptsskdnylggtstisdnakelckavsvsmglgvealehlspgeqlrgdcmyapllgvppavrptpcaplaeckgsllddsagkstedtaeyspfkggytkglegeslgcsgsaaagssgtlelpstlslyksgaldeaaayqsrdyynfplalagpppppppphphariklenpldygsawaaaaaqcrygdlaslhgagaagpgsgspsaaassswhtlftaeegqlygpcgggggggggggggggggggggggeagavapygytrppqglagqesdftapdvwypggmvsrvpypsptcvksemgpwmdsysgpygdmrletardhvlpidyyfp
[0259]
seq id no:6-人类ar的多肽序列(ensp00000363822)
[0260]
mevqlglgrvyprppsktyrgafqnlfqsvreviqnpgprhpeaasaappgasllllqqqqqqqqqqqqqqqqqqqqqqqetsprqqqqqqgedgspqahrrgptgylvldeeqqpsqpqsalechpergcvpepgaavaaskglpqqlpappdeddsaapstlsllgptfpglsscsadlkdilseastmqllqqqqqeavsegsssgrareasgaptsskdnylggtstisdnakelckavsvsmglgvealehlspgeqlrgdcmyapllgvppavrptpcaplaeckgsllddsagkstedtaeyspfkggytkglegeslgcsgsaaagssgtlelpstlslyksgaldeaaayqsrdyynfplalagpppppppphphariklenpldygsawaaaaaqcrygdlaslhgagaagpgsgspsaaassswhtlftaeegqlygpcgggggggggggggggggggggggeagavapygytrppqglagqesdftapdvwypggmvsrvpypsptcvksemgpwmdsysgpygdmrletardhvlpidyyfppqktclicgdeasgchygaltcgsckvffkraaegkqkylcasrndctidkfrrkncpscrlrkcyeagmtlgarklkklgnlklqeegeassttspteettqkltvshiegyecqpiflnvleaiepgvvcaghdnnqpdsfaallsslnelgerqlvhvvkwakalpgfrnlhvddqmaviqyswmglmvfamgwrsftnvnsrmlyfapdlvfneyrmhksrmysqcvrmrhlsqefgwlqitpqeflcmkalllfsiipvdglknqkffdelrmnyikeldriiackrknptscsrrfyqltklldsvqpiarelhqftfdllikshmvsvdfpemmaeiisvqvpkilsgkvkpiyfhtq
[0261]
seq id no:7-ar变体的多肽序列
[0262]
mevqlglgrvyprppsktyrgafqnlfqsvreviqnpgprhpeaasaappreasgaptsskdnylggtstisdnakelckavsvsmglgvealehlspgeqlrgdcmyapllgvppavrptpcaplaeckgsllddsagkstedtaeyspfkggytkglegeslgcsgsaaagssgtlelpstlslyksgaldeaaayqsrdyynfplalagpppppppphphariklenpldygsawaaaaaqcrygdlaslhgagaagpgsgspsaaassswhtlftaeegqlygpcggggggggggg
ggggggggggggeagavapygytrppqglagqesdftapdvwypggmvsrvpypsptcvksemgpwmdsysgpygdmrletardhvlpidyyfppqktclicgdeasgchygaltcgsckvffkraaegkqkylcasrndctidkfrrkncpscrlrkcyeagmtlgarklkklgnlklqeegeassttspteettqkltvshiegyecqpiflnvleaiepgvvcaghdnnqpdsfaallsslnelgerqlvhvvkwakalpgfrnlhvddqmaviqyswmglmvfamgwrsftnvnsrmlyfapdlvfneyrmhksrmysqcvrmrhlsqefgwlqitpqeflcmkalllfsiipvdglknqkffdelrmnyikeldriiackrknptscsrrfyqltklldsvqpiarelhqftfdllikshmvsvdfpemmaeiisvqvpkilsgkvkpiyfhtq
[0263]
seq id no:8-ar变体的多肽序列
[0264]
reasgaptsskdnylggtstisdnakelckavsvsmglgvealehlspgeqlrgdcmyapllgvppavrptpcaplaeckgsllddsagkstedtaeyspfkggytkglegeslgcsgsaaagssgtlelpstlslyksgaldeaaayqsrdyynfplalagpppppppphphariklenpldygsawaaaaaqcrygdlaslhgagaagpgsgspsaaassswhtlftaeegqlygpcgggggggggggggggggggggggeagavapygytrppqglagqesdftapdvwypggmvsrvpypsptcvksemgpwmdsysgpygdmrletardhvlpidyyfppqktclicgdeasgchygaltcgsckvffkraaegkqkylcasrndctidkfrrkncpscrlrkcyeagmtlgarklkklgnlklqeegeassttspteettqkltvshiegyecqpiflnvleaiepgvvcaghdnnqpdsfaallsslnelgerqlvhvvkwakalpgfrnlhvddqmaviqyswmglmvfamgwrsftnvnsrmlyfapdlvfneyrmhksrmysqcvrmrhlsqefgwlqitpqeflcmkalllfsiipvdglknqkffdelrmnyikeldriiackrknptscsrrfyqltklldsvqpiarelhqftfdllikshmvsvdfpemmaeiisvqvpkilsgkvkpiyfhtq
[0265]
seq id no:9-34-参见sirna序列(正义和反义)的实例
[0266]
seq id no:35-在来源于替代性外显子1b的ar2的n端的多肽序列
[0267]
milwlhs
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。