1.本发明涉及奶粉检测技术领域,具体涉及一种针对特殊医学用途配方奶粉中牛磺酸含量的检测方法。
背景技术:
2.牛磺酸(taurine,c2h7no3s,ho3s-ch
2-ch
2-nh2)化学名为β-氨基乙磺酸,是一种特殊的含硫非蛋白氨基酸,以游离状态分布于组织间液和细胞内液中。牛磺酸具有突出的生理药理作用,能调节机体内糖类和脂类的代谢,提高机体免疫力,维持渗透压平衡,增强细胞膜抗氧化能力等,对婴幼儿智力开发的促进和神经系统的发育也有重要作用。目前,牛磺酸已作为一种必备的营养强化剂添加在食品中,欧美等发达国家规定在婴幼儿食品中必须添加一定量的牛磺酸.我国食品安全国家标准也规定,为了改善婴儿配方食品的蛋白质质量,提高其营养价值,推荐婴幼儿配方乳制品中添加适当牛磺酸。
3.特殊医学用途配方奶粉(特医奶粉)主要包括:部分水解,深度水解和全氨基酸水解配方奶粉,是针对过敏体质婴儿专门设计的。婴幼儿免疫系统未完全发育以及胃肠道屏障发育不成熟,牛奶蛋白对婴幼儿来说是一种异种蛋白,牛奶中的β-乳球蛋白有很强的致敏性,极易出现婴幼儿牛奶蛋白过敏,造成便血,腹胀,甚至会导致患儿出现死亡以及过敏性休克。牛奶蛋白过敏的发病率为6%,已成为对婴幼儿健康成长发育产生影响的首要因素。水解配方奶粉在加工时将牛奶中的蛋白质部分水解或者完全水解,以降低过敏概率,但不会影响蛋白质的营养,已成为大多婴幼儿食用的首选。
4.特医奶粉的基质体系相对于普通婴儿配方奶粉复杂很多,蛋白质被水解后形成大量的氨基酸于基质中,对于牛磺酸的定量分析会造成严重的干扰。其中,薄层扫描法就很容易受到其余氨基酸的干扰,准确性较低;高效液相色谱——串联质谱法应用广泛,但对于奶粉本身的基质效应显著,重复性不理想;高效液相色谱——紫外检测,受到牛磺酸自身紫外吸收较弱的影响,灵敏度较低。
5.丹磺酰氯(二甲氨基—萘磺酰氯dns-cl)是一种强荧光剂,能专一地与肽链n-端的α-氨基反应生成丹磺酰-肽,后者水解生成的丹磺酰-氨基酸具有很强的荧光信号。国标gb 5009.169-2016中,传统婴儿配方奶粉在沉淀蛋白后,利用1.5mg/ml的dns-cl衍生液在碱性条件下衍生,得到荧光产物,虽然采用上述方法检测普通的婴幼儿奶粉中给的牛磺酸,其回收率均能达到90%以上;但是由于在全氨基酸水解配方奶粉中,其余氨基酸同样可以与dns-cl反应,导致牛磺酸的衍生反应不完全,其回收率都低于30%,相对标准偏差也较大,从而导致该法也无法对全氨基酸水解配方等特医奶粉中的牛磺酸含量进行准确定量。
6.因此,亟需设计一种针对特殊医学用途配方奶粉中牛磺酸含量的检测方法,以实现对特医奶粉,尤其是对全氨基酸水解配方奶粉中的牛磺酸含量进行高效、精准的检测。
技术实现要素:
7.鉴于上述问题,本发明提供一种针对特殊医学用途配方奶粉中牛磺酸含量的检测
方法,以用于准确定量全氨基酸水解配方奶粉中牛磺酸的含量。
8.本发明的技术方案如下:一种针对特殊医学用途配方奶粉中牛磺酸含量的检测方法,包括如下步骤:
9.(1)配制标准品工作液:精确称取牛磺酸标准品,以水为溶剂配制牛磺酸的标准品工作液;
10.(2)提取奶粉待测样品中的牛磺酸:精确称取待测奶粉样品溶解于水中,超声后,加入沉淀剂,经涡旋混合均匀后,离心,提取上清液,并用纯水进行定容得到待测样品溶液;
11.(3)衍生处理:将步骤(1)和(2)中配制的标准品工作液和待测样品溶液中分别加入衍生化试剂,在碱性环境下进行衍生反应,反应结束后经膜过滤,得到标准品衍生产物和样品衍生产物;
12.(4)检测分析:采用二维液相系统对步骤(3)制备的标准品衍生产物和样品衍生产物进行检测,以研究并分析特医奶粉样品中牛磺酸的含量;所述二维液相系统包括一维液相体系和二维液相体系,以及用于连接所述一维液相体系和二维液相体系的六通阀;
13.其中:所述沉淀剂为亚铁氰化钾和乙酸锌,所述衍生化试剂为丹磺酰氯。
14.优选地,步骤(4)中,所述一维液相体系包括第一高效液相色谱体系和紫外检测器,所述二维液相体系包括第二高效液相色谱体系和荧光检测器;通过比较标准品衍生产物和样品衍生产物在一维液相体系中的保留时间,确定由一维液相体系切换至二维液相体系的时间,由二维液相体系精确测定特医奶粉中牛磺酸的含量。
15.二维液相系统是将分离机理不同而又相互独立的两支色谱柱串联起来构成的分离系统,通过柱切换技术完成牛磺酸在二维色谱柱之间的流动。样品经过所述一维液相体系的色谱柱洗脱分离后,锁定目标物的出峰时间,进入六通阀的接口中,经捕集和中心切割后,被切换进入所述二维液相体系的色谱柱及检测器,由此得到的牛磺酸具有更高的峰容量和分辨力。
16.优选地,步骤(1)中,精确称取牛磺酸标准品100.0mg于100ml容量瓶,配制成浓度为1.0mg/ml的标准品储备液,将所述标准品储备液用水稀释成浓度为1.0、5.0、10.0、15.0、20.0μg/ml的标准品工作液备用。
17.优选地,步骤(2)中,精确称取1.00
±
0.05g特医奶粉样品于50ml聚四氟乙烯塑料离心管中,加入35ml超纯水,超声10~20min,加入1ml 150g/l亚铁氰化钾溶液和1ml 300g/l乙酸锌溶液,涡旋5~10min进行均匀混合,去除基质中的蛋白质,以9000~10000r/min转速离心2~5min,将离心后的上清液转移至50ml容量瓶中,用超纯水定容至刻度,制得待测样品溶液。
18.优选地,步骤(3)中,所述衍生化试剂为以乙腈为溶剂、浓度为15~45mg/ml的丹磺酰氯衍生液;并使用三乙胺作为缓冲溶液调整衍生反应的环境ph至9~11。
19.优选地,步骤(3)中,标准品工作液和待测样品溶液的衍生处理具体步骤为:分别取1ml需要衍生处理的溶液于10ml聚四氟乙烯塑料离心管中,加入1ml 30mg/ml丹磺酰氯衍生液,10μl三乙胺,60℃避光加热1.0
±
0.1h,加入0.1ml质量浓度为20mg/l的盐酸甲胺溶液终止反应,过0.22μm ptfe滤膜,制得标准品衍生产物和样品衍生产物待检测。
20.优选地,在进行避光加热处理时,需每隔15min取出进行涡旋30sec,以使反应更加充分均匀。
21.优选地,一维液相体系条件:一维色谱柱:agilent xdb-c18(3.0mm
×
150mm,3.5μm);柱温:35
±
1℃;进样量:20μl;流动相a1:0.1%三氟乙酸水;流动相b1:甲醇;流速:0.4ml/min;梯度洗脱程序见下表;紫外检测器:254nm。
[0022][0023]
流动相中的三氟乙酸通过与疏水键合相和残留的极性表面以多种模式相互作用,来抑制待测物和反相色谱柱填料表面残留的硅羟基的作用,保证牛磺酸衍生物良好的峰形。并且,三氟乙酸的紫外最大吸收峰低于200nm,对多肽在低波长处的检测干扰很小。牛磺酸衍生物在最大紫外波长(254nm)吸收下的响应和峰面积虽然很低,但这并不影响六通阀切换的时间。
[0024]
优选地,所述一维液相体系切换至二维液相体系的时间为4.2min~5.2min。在该时间段,目标物牛磺酸衍生物被顺利切入二维液相体系中进行检测,而其余氨基酸被保留在一维液相体系中。
[0025]
优选地,二维液相体系条件:二维色谱柱:thermal accucore
tm pfp(3.0mm
×
150mm,2.6μm);柱温:35
±
1℃;进样量:20μl;流动相a2:0.1%甲酸水;流动相b2:乙腈;流速:0.6ml/min;梯度洗脱程序见下表;荧光检测器:激发波长为330nm,发射波长为530nm。
[0026][0027]
五氟苯基(pfp)固定相中的氟化基团可为卤代化合物中含极性官能团的化合物提供独特的选择性,对含有双苯环的丹磺酰—氨基乙磺酸具有很好的保留,同时,其高硅胶表面覆盖率最大程度减少了次级相互作用和峰拖尾的情况,可以获得很好的峰形。
[0028]
优选地,所述特殊医学用途配方奶粉包括全氨基酸水解配方奶粉、深度水解婴幼儿配方奶粉和部分水解婴幼儿配方奶粉。
[0029]
本发明的有益效果:
[0030]
(1)本发明通过改进了特医奶粉样品的前处理方法,并构建二维液相系统,利用荧
光检测器精确测定奶粉中牛磺酸的含量,该方法准确性高,抗干扰能力强。
[0031]
(2)采用本发明的方法处理的待测奶粉样品,其牛磺酸衍生物在二维液相色谱中具有足够强的荧光响应信号和良好的色谱峰形,分离度和灵敏度均满足了奶粉中牛磺酸检测的要求。
[0032]
(3)本发明的方法不仅可以用于普通婴幼儿奶粉中牛磺酸含量的检测,还可以用于特医奶粉的检测,尤其是对于基质最为复杂的全氨基酸水解配方奶粉中的牛磺酸含量仍能精确检测。
[0033]
(4)本发明的方法在处理待测奶粉样品时,相比较现有技术,缩短了丹磺酰氯的柱前衍生时间,具有更快的衍生速度和效率,从而提高检测效率。
附图说明
[0034]
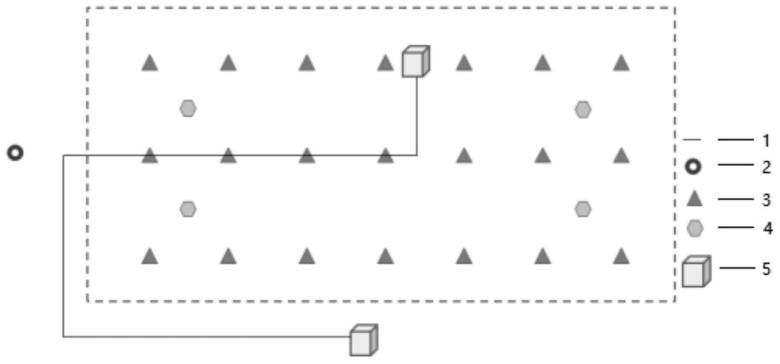
图1二维液相系统连接示意图。
[0035]
图2为实施例1中牛磺酸衍生物一维紫外色谱图。
[0036]
图3为实施例1中牛磺酸衍生物在不同二维流动相体系中的峰面积。
[0037]
图4为实施例1中牛磺酸衍生物二维荧光色谱图。
[0038]
图5为实施例4中衍生时间对牛磺酸含量和回收率的影响。
具体实施方式
[0039]
本发明提供一种针对特殊医学用途配方奶粉中牛磺酸含量的检测方法,以解决现有技术中对特殊医学用途配方奶粉,尤其是特医奶粉中的全氨基酸水解配方奶粉中的牛磺酸含量无法准确定量的问题。
[0040]
下面结合具体实施例,进一步阐述本发明。应理解,本实施例仅用于说明本发明而不用于限制本发明的范围。此外应理解,在阅读了本发明讲授的内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本技术所附权利要求书所限定的范围。
[0041]
本发明实施例中采用的仪器包括:dionexultimate 3000系统(双三元梯度泵,美国thermal scientific),配有紫外检测器(dad)、荧光检测器(fld)和一个六通阀;mszo 204s型电子天平(瑞士mettler toledo);centrifuge 5804高速离心机(德国eppendorf);d-91126多管涡旋振荡器(德国heidolph);c9nk-sk1200btu超声波清洗机(中国kudos);milli-q超纯水系统(美国millipore)。
[0042]
所使用的试剂包括:牛磺酸标准品;婴幼儿配方奶粉、特殊医学用途水解配方奶粉(国内某知名乳业有限公司);丹磺酰氯(日本,东京化成工业株式公社);甲醇,乙腈(色谱纯,美国thermal fisher chemical);甲酸(色谱纯,美国acs色谱试剂);三乙胺(色谱纯,美国tedia);三氟乙酸,亚铁氰化钾,乙酸锌(分析纯,国药集团化学试剂有限公司)。
[0043]
实施例1检测方法的选择与优化
[0044]
1、标准工作液的配制
[0045]
精确称取牛磺酸标准品100.0mg于100ml容量瓶,以水为溶剂配制成浓度为1.0mg/ml的标准品储备液。实验前,将标准品储备液用水稀释成浓度为1.0、5.0、10.0、15.0、20.0μg/ml的标准品工作液备用。
[0046]
2、提取待测奶粉样品的牛磺酸:精确称取1.00
±
0.05g奶粉样品于50ml聚四氟乙烯塑料离心管中,加入约35ml超纯水,超声15min,加入1ml 150g/l亚铁氰化钾溶液和1ml 300g/l乙酸锌溶液,涡旋5min进行均匀混合,去除基质中的蛋白质,以9000r/min转速离心2min,将上清液转移至50ml容量瓶中,用超纯水定容至刻度,得到待测样品溶液。
[0047]
3、衍生处理:将标准品工作液和样品溶液进行衍生,具体步骤为:取1ml需要衍生的溶液于10ml聚四氟乙烯塑料离心管中,加入1ml30 mg/ml高浓度丹磺酰氯衍生液(dns-cl)作为衍生化试剂,所述丹磺酰氯衍生液的溶剂为乙腈,添加10μl三乙胺为缓冲溶液调节溶液为碱性,60℃避光水浴加热1.0
±
0.1h,每15min取出涡旋30sec,加入0.1ml质量浓度为20mg/l的盐酸甲胺终止反应,过0.22μm ptfe滤膜,得到待测的标准品衍生产物和样品衍生产物供二维液相系统(2d-lc)检测,检测标准品衍生产物,以保留时间定性,外标法定量。
[0048]
4、色谱条件
[0049]
所述二维液相系统的连接流程如图1所示,所述二维液相系统包括一维液相体系和二维液相体系,以及用于连接一维液相体系和二维液相体系的六通阀1-1;所述一维液相体系包括依次连接的第一泵、第一高效液相色谱体系和dad检测器,二维液相体系包括依次连接的第二高效液相色谱体系和fld检测器;待测样经自动进样器进入第一高效液相色谱体系,经第一高效液相色谱体系的色谱柱洗脱分离后,由dad检测器进行检测,锁定目标物的出峰时间,进入六通阀1-1的接口中;切换六通阀从1-2连通状态转变为1-6连通,目标物被中心切入至二维液相体系,经第二高效液相色谱体系的色谱柱洗脱分离后,经fld检测器进行检测分析。
[0050]
4.1一维色谱条件
[0051]
色谱柱:agilent xdb-c18(3.0mm
×
150mm,3.5μm);柱温:35℃;进样量:20μl;流动相a1:0.1%三氟乙酸水;流动相b1:甲醇;流速:0.4ml/min;一维梯度洗脱程序见表1;紫外检测器:254nm。
[0052]
表1一维液相色谱条件
[0053][0054]
本实施例中,采用上述样品处理方法和一维色谱条件分别对牛磺酸标准品a、普通婴幼儿奶粉b和全氨基酸水解配方奶粉c的样品溶液衍生液进行高效液相色谱-紫外检测器检测,检测结果如图2所示。比较图2-b和图2-c可知,全氨基酸水解配方奶粉中含有大量普通婴幼儿奶粉中没有的氨基酸,并且因为牛磺酸本身紫外吸收很弱,与其余氨基酸衍生物相比,牛磺酸衍生物的响应小了很多数量级,无法精确积分定量,因此应将其分离出来。由
图2-a显示,牛磺酸衍生物在一维色谱体系中的保留时间为4.67min,根据图2-a的牛磺酸衍生物的出峰位置,确定一维色谱体系切换至二维色谱体系,也即六通阀由1-2连通状态转变为1-6连通的切换时间为4.2min~5.2min,此时,目标物牛磺酸衍生物被顺利切入二维液相色谱中,而其余氨基酸都被保留在一维色谱体系中。
[0055]
4.2二维色谱条件
[0056]
色谱柱:thermal accucore
tm
pfp(3.0mm
×
150mm,2.6μm);柱温:35℃;进样量:20μl;流动相a2:0.1%甲酸水;流动相b2:乙腈;流速:0.6ml/min;二维梯度洗脱程序见表2;荧光检测器:激发波长为330nm,发射波长为530nm。
[0057]
表2二维液相色谱条件
[0058][0059]
二维液相色谱既要考虑两个维度的兼容性,又要考虑不同液相体系存在的差异。本实施例中考察了牛磺酸标准品衍生产物在不同流动相体系中的峰面积和稳定性,不同流动相体系分别为0.1%甲酸水 乙腈、0.1%甲酸水 甲醇、0.1%三氟乙酸 乙腈、0.1%三氟乙酸 甲醇,实验结果如图3所示。由图3牛磺酸衍生物在不同流动相体系中的检测结果可知,0.1%甲酸水 乙腈体系在峰面积的大小和稳定性上具有突出的优异性,因此确定选择离解常数更温和的0.1%甲酸水作为二维水相;化合物的保留时间更稳定,柱压更小的乙腈作为二维有机相。
[0060]
在上述确定二维液相系统的色谱条件后,分别对牛磺酸标准品a、普通婴幼儿奶粉b和全氨基酸水解配方奶粉c样品的衍生产物检测,通过对牛磺酸衍生物含量的检测,实现对奶粉中牛磺酸定量分析。各样品中牛磺酸衍生物二维荧光色谱图分别如图4所示,图4的结果说明牛磺酸衍生物在二维液相色谱中具有足够强的荧光响应信号和良好的色谱峰形,分离度和灵敏度均满足了奶粉中牛磺酸检测的要求。
[0061]
实施例2不同dns-cl衍生液浓度的影响
[0062]
本实施例以全氨基酸水解配方奶粉为待测样品,样品中牛磺酸的企业理论添加量为40.0mg/100g。采用实施例1中的方法对样品进行提取和衍生化处理,并将制备的样品衍生产物通过二维液相系统进行检测。本实施例中,通过改变衍生化试剂dns-cl衍生液的浓度,考察衍生化试剂浓度对于检测特医奶粉样品中牛磺酸含量的影响。样品处理和检测方法均和实施例1相同,区别在于:设置不同组的dns-cl衍生液的浓度,考虑到dns-cl在乙腈中的溶解度为50mg/ml,dns-cl衍生液的浓度分别设置为15mg/ml、30mg/ml、45mg/ml,并设置衍生反应避光加热时间为2h,每组试验取12个样品,结果取12个样品的平均值,实验结果如表3所示。
[0063]
表3不同dns-cl浓度下检测全氨基酸水解配方奶粉中牛磺酸的含量
[0064][0065]
通过表3的结果显示,随着dns-cl浓度的增大,全氨基酸水解配方奶粉样品中牛磺酸的回收率有大幅度的提升。当使用15.0mg/ml浓度的dns-cl衍生液,牛磺酸的回收率仍然低于50%,这说明该组实验中衍生反应依旧不完全;而30.0和45.0mg/ml浓度的dns-cl衍生液均能确保牛磺酸得到较为完整的衍生过程,其牛磺酸的回收率都在90%以上,衍生产物丹磺酰-氨基乙磺酸dns-nh-(ch2)2–
so3h的色谱峰形更为尖锐,峰面积,峰高均大幅度增加。在试验过程中,45.0mg/ml的dns-cl在与牛磺酸反应的同时,因为自身溶解度的问题,衍生一段时间后,会有反应物沉淀析出的现象,造成衍生过程的不均匀,重现性不理想,这可能是其结果的相对标准偏差更大的主要原因。另外,高浓度的dns-cl衍生得到的丹磺酰-氨基乙磺酸中会伴有其他杂质,经过波长鉴定,与丹磺酰基团有关,其对色谱柱的分离和柱效都会有影响,目标峰的相对百分比也会下降,应尽量避免。因此,在30.0和45.0mg/ml的dns-cl对于牛磺酸检测结果没有显著性差异的情况下,确定30.0mg/ml的dns-cl衍生液作为后续试验中优选的衍生液浓度。
[0066]
实施例3衍生环境ph值的影响
[0067]
牛磺酸与dns-cl的反应过程中,随着荧光产物丹磺酰-氨基乙磺酸dns-nh-(ch2)2–
so3h的生成,dns-cl上的cl-与h
结合为hcl,降低了溶液的ph值,会抑制反应向正方向进行,因此在衍生过程中,需要保持溶液体系在碱性环境中进行。本实验中,同样地以全氨基酸水解配方奶粉为待测样品,奶粉样品中牛磺酸的企业理论添加量40.0mg/100g。采用实施例1中的方法进行样品的提取和衍生化处理,制备样品衍生产物后通过二维液相系统进行检测。样品处理和检测方法均和实施例1相同,区别在于:通过改变三乙胺的添加量改变衍生环境的ph,并设置衍生反应避光加热时间为2h,每组试验取12个样品,结果取12个样品的平均值,实验结果如表4所示。
[0068]
表4在不同三乙胺添加量下检测全氨基酸水解配方奶粉中牛磺酸的含量
[0069][0070]
由表4的结果显示,在没有三乙胺添加的情况下,牛磺酸的回收率仅为4.1%。而加
入三乙胺能迅速提升溶液的ph值。三乙胺(c2h5)3n中的n孤电子对为sp3杂化,很容易给出电子;同时,三乙胺结合氢质子后,其三个乙基可以通过超共轭效应来稳定电荷,保证衍生溶液的稳定性。牛磺酸的最佳起始衍生环境通常控制在ph=9.5左右,10μl三乙胺可以将溶液的ph值调节至10.1,已经可以充分满足衍生条件,其回收率达到了90%以上。且实验结果显示随着三乙胺的增加,目标物的色谱峰面积和回收率并没有显著性增加,考虑到三乙胺具有一定的刺激性,在保证衍生充分性的前提下,尽量控制其添加量。因此确定10μl三乙胺的添加量为优选项用以调节衍生液的ph值。
[0071]
实施例4衍生反应时间的影响
[0072]
本实施例的奶粉样品处理和检测方法均和实施例1相同,区别在于:设置不同组的衍生反应时间,分别为0.5h、1.0h、1.5h、2.0h,同样地,每组试验取12个样品,结果取12个样品的平均值。
[0073]
另外本实验中,还分别比较了以本实验的衍生方法分别检测全氨基酸特医配方奶粉(a)和普通婴幼儿奶粉(b),以及考察了以国标gb 5009.169-2016的方法进行衍生处理,并检测处理后的普通婴幼儿奶粉(c)和全氨基酸特医配方奶粉(d),实验结果如图5所示。
[0074]
由图5-a可知,在反应后的0.5h,利用本试验方法得到的牛磺酸含量大约达到25.6mg/100g(回收率为64%),1h后,牛磺酸含量已经接近企业理论添加量40mg/100g,而1.5h后,其含量没有显著性增加。另外,本试验方法同样可以用于检测普通婴幼儿配方奶粉中的牛磺酸,结果如图5-b所示,虽然奶粉基质体系不同,但在牛磺酸添加量相同的情况下,其检测结果随反应时间增加的变化趋势相同,经过1h的衍生,回收率均已达到90%以上。并且,通过比较图5-b和图5-c的结果可知,本发明的方法与国标gb 5009.169-2016相比,当检测同一种普通婴幼儿配方奶粉时,可以将衍生时间缩短一半,衍生过程可以在1h左右完成,这加快了衍生反应的效率,从而减少了反应时间和能耗;而图5-d也说明现有的国标方法无法完全衍生全氨基酸水解配方奶粉。
[0075]
综上所述,本发明利用高浓度的dns-cl在60℃的水浴中避光加热反应物,旨在使其充分反应,并提高衍生速度和效率。对于全氨基酸水解配方奶粉基质,加热能提升高浓度dns-cl的溶解度,降低dns-cl的析出,促使整个衍生反应更加均匀和彻底。因此,全氨基酸水解配方特医奶粉在30.0mg/ml的dns-cl,10μl三乙胺的衍生条件下,60℃加热1h,可以衍生得到最理想量的衍生产物丹磺酰—氨基乙磺酸,供荧光检测器检测。
[0076]
实施例5结果评价
[0077]
1、线性关系
[0078]
牛磺酸标准品浓度在1.0-20.0mg/l范围内,标准曲线有良好的线性,相关系数(r2)达到了0.9996。其浓度与峰面积的线性方程:y=10433.78x 1769.98。
[0079]
2、回收率和精密度
[0080]
采用实施例1的样品处理和检测方法对4种不同基质奶粉中的牛磺酸含量进行测定,同样地,样品中牛磺酸的理论添加量为40mg/100g,每组各取12个样品,结果取12个样品的平均值,通过检测出的牛磺酸衍生物的浓度,得到奶粉中牛磺酸的实际含量。检测结果如表5所示,每组回收率均在90%以上,相对标准偏差均在5%以内。表明该试验方法在检测特医配方奶粉和普通婴幼儿配方的奶粉上均具有良好的精密度、稳定性和一致性。
[0081]
表5四种不同基质奶粉中牛磺酸含量的测定
[0082][0083]
综上所述,本发明建立了一套样品前处理方法和二维液相色谱体系,用于研究特殊医学用途全氨基酸水解配方奶粉中牛磺酸的含量。该方法在牛磺酸浓度1.0-20.0mg/l内线性良好,线性相关系数达到0.9996,并且12个实际样品的平均回收率为95.2%,相对标准偏差为1.86%。该方法准确性高,抗干扰能力强,并且缩短了丹磺酰氯的柱前衍生时间,具有较好的实际运用价值,解决了国家食品安全标准和iso标准目前无法准确分析全氨基酸水解配方奶粉中牛磺酸含量的问题,为特殊医学用途乳制品的检测提供了新的技术支持,有助于质检部门加强对乳制品市场的监管。另外,此方法同样适合于其他奶粉基质,可以为深度水解配方奶粉,部分水解配方奶粉,和普通婴幼儿配方奶粉中其他营养物质检测技术的优化提供新的思路。
[0084]
以上所述仅为本发明的优选实施例,并非因此限制本发明的专利范围,凡是利用本发明说明书及附图内容所作等效结构或等效流程变换,均同理包括在本发明的专利保护范围内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。