具有中和活性的抗h1n1流感病毒血凝素蛋白单克隆抗体zcmu-h1n1及其应用
技术领域
1.本发明属于生物技术领域,涉及抗h1n1流感病毒血凝素蛋白中和性单克隆抗体的制备及应用,是利用细胞工程、抗体工程技术,获得分泌抗血凝素蛋白的单克隆抗体的杂交瘤细胞系,通过同品系的小鼠诱导腹水,制备抗血凝素蛋白的单克隆抗体zcmu-h1n1,鉴定为igg1、κ型,再通过亲和纯化等技术实现对该抗体的应用。
背景技术:
2.季节性流感病毒仍然是全球公共卫生威胁,其流行给公众健康和社会经济带来严重的影响。据估计,每年由流感病毒引起的死亡人数超过30万人,而引起人类流感感染最常见的病因是甲型流感病毒(包括h1n1和h3n2亚型)。2009-2010年,甲型流感病毒(h1n1 pdm09)率先在墨西哥、加拿大和美国出现并迅速在全球蔓延,在流行期间第一年导致全球有至少15万人死亡。随后,甲型流感(h1n1 pdm09)取代了先前流行的季节性h1n1病毒,并一直保持季节性流行。另外,流行病学分析表明,在早期甲型h1n1流感大流行期间80%的死亡病例发生在年轻人(≤65岁)中,31%的甲型h1n1感染患者出现了继发性细菌性肺炎,这显著增加了住院率和死亡率。
3.当前接种流感疫苗仍然是控制流感的最经济有效的方法,但季节性流感病毒流行每年仍然会造成数以百万的感染以及数十万的住院病例发生。流感的早期临床症状与普通感冒相似,易被轻视,但流感患者病情可迅速进展,突然高热、肺炎,重者可以出现呼吸衰竭、多器官损伤,甚至死亡,病死率达6%。
4.当前临床治疗流感感染的治疗原则主要为抗病毒药物治疗(如奥司他韦)和支持治疗。其中抗病毒药物治疗需在症状出现后48小时内用药,否则抗病毒治疗的疗效将明显下降。另外,在临床研究中发现流感病毒在药物暴露期间会出现耐药突变,导致出现对奥司他韦耐药。由于耐药率增加、治疗时间窗等受限,寻求新型治疗流感感染的药物迫在眉睫。单克隆抗体因其具有高度的特异性和良好的安全性而得到广泛的应用,除了用于治疗癌症和自身免疫疾病外,一些单克隆抗体药物已被批准用于预防和治疗各种传染病的临床试验,例如帕利珠单克隆抗体预防呼吸道合胞病毒感染。
5.基于以上背景,本发明选定h1n1流感病毒血凝素蛋白为靶抗原,采用融合杂交瘤技术建立稳定分泌抗h1n1流感病毒血凝素蛋白单克隆抗体的杂交瘤细胞系,并大量制备、纯化和鉴定这些单克隆抗体。该中和性单克隆抗体的成功获得,为治疗h1n1流感病毒感染提供新思路。
6.本发明用到杂交瘤细胞技术。该技术将免疫小鼠的b淋巴细胞与骨髓瘤细胞融合,以建立分泌均质抗体的杂交瘤细胞系,也称为单克隆抗体技术。该技术涉及到动物免疫、细胞培养、细胞融合、细胞克隆培养和免疫测定等一系列方法。
技术实现要素:
7.本发明的目的是提供一种抗h1n1流感病毒血凝素蛋白单克隆抗体,能识别h1n1季节性流感病毒。该单克隆抗体亚型为igg1、κ型,命名为zcmu-h1n1,能特异性识别流感病毒的血凝素蛋白。
8.seq id no.1
9.heavy chain:dna sequence(360bp)
10.signal sequence-fr1-cdr1-fr2-cdr2-fr3-cdr3-fr4
11.cagatccagttggtgcagtctggacctgagctgaagaagcctggagagacagtcaagatctcctgcaaggcttctggatacaccttcacaaattatggaatgaactgggtgaagcaggctccaggaaagggtttaaggtggatgggctggataaacacctacactggagagccaacatatgatgatcattttaagggacgatttgccttctctttggaaacctctgccagcactgcctatttgcagatcaacaacctcaaaaatgaggacatggctacatatttctgtgcaagggaggataattacgccccttcctggtttactcactggggccaagggactctggtcactgtctctgca
12.seq id no.2
13.heavy chain:amino acid sequence(120aa)
14.signal peptide-fr1-cdr1-fr2-cdr2-fr3-cdr3-fr4qiqlvqsgpelkkpgetvkisckasgytftnygmnwvkqapgkglrwmgwintytgeptyddhfkgrfafsletsastaylqinnlknedmatyfcarednyapswfthwgqgtlvtvsa
15.seq id no.3
16.light chain:dna sequence(324bp)
17.signal sequence-fr1-cdr1-fr2-cdr2-fr3-cdr3-fr4
18.caaattgttctctcccagtctccaaccaccatggctgcatctcccggggagaagatcactatcacctgcagtgccagctcaagtataagttccaattacttgcattggtatcagcagaggccaggattctcccctaaactcttgatttataggacatccaatctggcttctggagtcccagctcgcttcagtggcagtgggtctgggacctcttactctctcacaattggcaccatggaggctgaagatgttgccacttactactgccagcagggtcatagtataccatacacgttcggaggggggaccaagctggaaataaaa
19.seq id no.4
20.light chain:amino acid sequence(108aa)
21.signal peptide-fr1-cdr1-fr2-cdr2-fr3-cdr3-fr4
22.qivlsqspttmaaspgekititcsasssissnylhwyqqrpgfspklliyrtsnlasgvparfsgsgsgtsysltigtmeaedvatyycqqghsipytfgggtkleik
23.本发明的第二个目的提供抗h1n1流感病毒血凝素蛋白单克隆抗体的制备方法,通过以下步骤和技术方案实现:
24.(1)动物的免疫:选择6周龄的balb/c小鼠,以纯化的h1n1流感病毒血凝素蛋白对小鼠进行免疫。血凝素蛋白由h1n1流感病毒疫苗株(a/michigan/45/2015)接种鸡胚,培养并收获病毒液,经甲醛灭活、纯化、裂解及再纯化等方法,以磷酸缓冲液稀释制备获得。
25.(2)小鼠骨髓瘤细胞的培养:培养小鼠骨髓瘤细胞sp2/0并使之保持良好的生长状态用于细胞融合。
26.(3)细胞融合:采用聚乙二醇融合法。以balb/c小鼠腹腔巨噬细胞作为饲养细胞,在融合前一天,接种balb/c小鼠腹腔巨噬细胞于96孔培养板,含20%牛血清的次黄嘌呤-鸟
嘌呤-磷酸核糖转移酶培养基培养一天。将(1)中备好的小鼠处死,获取脾脏淋巴细胞。收集(2)中的小鼠骨髓瘤细胞。将上述两种细胞混合离心,然后以聚乙二醇介导细胞融合。融合后的细胞适当稀释,接种至饲养细胞培养板,适当条件培养。
27.(4)杂交瘤细胞的筛选:将上述培养物在次黄嘌呤-磷酸核糖转移酶选择性培养基中培养。在细胞集落长到大小合适时,吸取细胞培养上清液做抗体鉴定,筛选阳性克隆。
28.(5)杂交瘤细胞的克隆化:以有限稀释法克隆杂交瘤细胞,将稀释到一定密度的细胞接种至96孔板,使每孔只有一个细胞生长。形成细胞集落的孔取培养上清液做酶联免疫吸附实验,鉴定阳性克隆。重复有限稀释克隆若干次,直到杂交瘤细胞的阳性孔率达到100%。将克隆化后的杂交瘤细胞扩大培养做抗体鉴定及理化性状分析。
29.(6)单克隆抗体腹水的诱导:在接种杂交瘤细胞前一周,给balb/c小鼠腹腔注射石蜡油每只0.5毫升,然后每只接种5
×
106个阳性杂交瘤细胞,10天后收集腹水离心,测定抗体效价,并纯化单克隆抗体。
30.(7)单克隆抗体的纯化:利用protein g亲和纯化法纯化腹水中的单克隆抗体。
31.(8)本发明得到一株产生抗h1n1流感病毒血凝素蛋白单克隆抗体杂交瘤系,即zcmu-h1n1,zcmu-h1n1杂交瘤细胞系经4次克隆化,持续培养六月余,分泌抗体稳定。该细胞株经液氮冻存,复苏后生长良好,抗体分泌未见衰退。酶联免疫吸附间接法实验测得zcmu-h1n1培养上清效价为1:64,腹水效价为1:2048。经单克隆抗体免疫球蛋白亚型分析显示该杂交瘤细胞产生的抗体类型为igg1。
32.本发明提供产生单克隆抗体的杂交瘤细胞,它是由免疫的balb/c小鼠脾细胞和小鼠骨髓瘤细胞sp2/0经融合、筛选、克隆、传代和反复冻存、复苏后获得的小鼠杂交瘤细胞系zcmu-h1n1,能稳定分泌抗h1n1流感病毒血凝素蛋白的单克隆抗体zcmu-h1n1。
33.本发明的另一个目的是提供该单克隆抗体zcmu-h1n1能有效结合、中和h1n1流感病毒的应用及其使用方法。
34.本发明还提供了一种h1n1季节性流感预防和/或治疗药物,包含单克隆抗体zcmu-h1n1。
35.本发明的优点在于提供了一种抗h1n1流感病毒血凝素蛋白的单克隆抗体,并在细胞及动物体内验证了该抗体的抗病毒效应,将为抗h1n1流感病毒的预防与治疗提供新的参考方案。
36.说明书附图
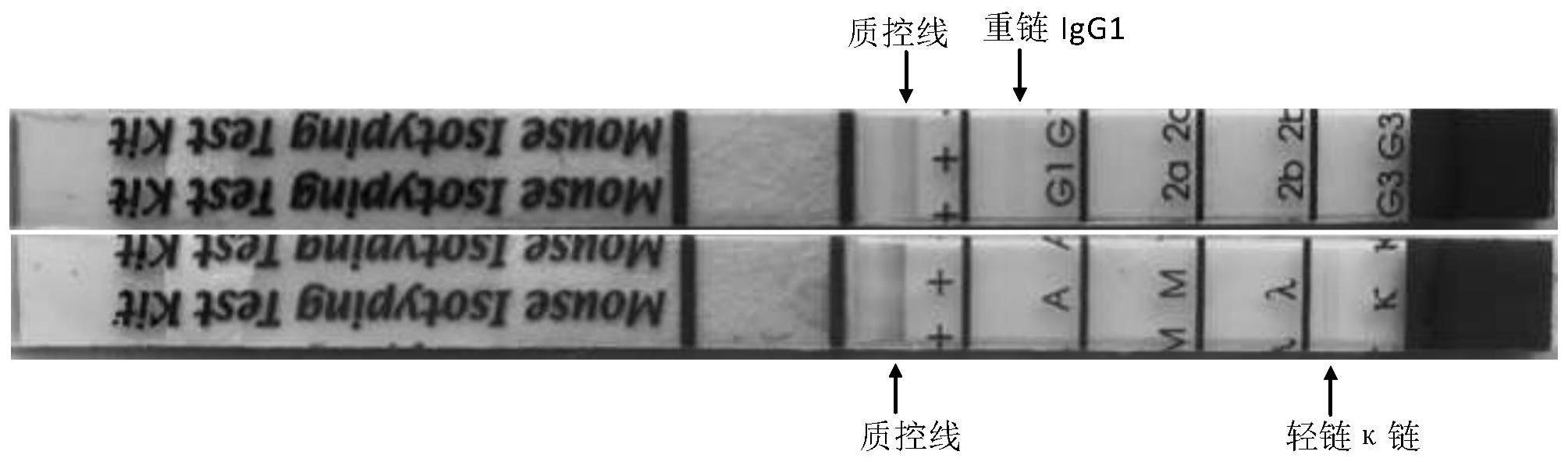
37.图1为单克隆抗体zcmu-h1n1的免疫球蛋白亚型分析。
38.图2为单克隆抗体zcmu-h1n1的效价检测。
39.图3为单克隆抗体zcmu-h1n1体外中和效应检测。
40.图4为单克隆抗体zcmu-h1n1在小鼠体内的预防效果。
41.图5为单克隆抗体zcmu-h1n1在小鼠体内的治疗效果。
具体实施方式
42.下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。
43.实施例1.抗h1n1流感病毒血凝素蛋白的单克隆抗体的制备方法
44.(1)小鼠的免疫:首次免疫,将h1n1流感病毒血凝素全蛋白与佐剂按等体积混合均匀,总体积600微升。每只balb/c小鼠0.1毫升(含h1n1流感病毒血凝素全蛋白抗原30微克),大腿内侧肌肉注射。第21天按同样方式加强免疫一针。第35天采微量尾血进行酶联免疫吸附实验测定,抗体滴度达到1:100000,随即尾静脉注射加强免疫一次,于3天后进行细胞融合。
45.(2)小鼠骨髓瘤细胞sp2/0的培养:把来自balb/c小鼠的sp2/0骨髓瘤细胞株以含10%牛血清dmem培养基培养传代,在含5%二氧化碳饱和37℃孵箱中培养。融合前一天传代以保证融合时细胞进入对数生长期。
46.(3)细胞融合:以balb/c小鼠腹腔巨噬细胞作为饲养细胞,在融合前一天,接种balb/c小鼠腹腔巨噬细胞于96孔培养板,含20%牛血清的次黄嘌呤-鸟嘌呤-磷酸核糖转移酶培养基培养一天。次日取(1)中小鼠脾脏,采用压力注水法分离脾细胞,离心洗涤细胞2次后用培养液重悬。收集(2)中sp2/0细胞,离心,洗涤2次后用培养液重悬,作为待融合的sp2/0细胞。以1
×
108个免疫小鼠脾淋巴细胞与2
×
107个小鼠骨髓瘤细胞sp2/0混合,在聚乙二醇作用下融合。两种细胞混合后洗涤一次,离心弃上清,轻弹管壁悬开细胞,用37℃预温的聚乙二醇0.9毫升于90秒内逐滴加入细胞沉淀中,其间轻轻振摇离心管,静置1分钟,然后按先慢后快的原则,于第1分钟内加完1毫升无血清dmem,于第2分钟内加完2毫升无血清dmem,于第3分钟内加完7毫升无血清dmem,以后1分钟内逐渐加入37℃预温的无血清dmem培养基40毫升。1000转每分钟低速离心10分钟。然后加入培养基,分别接种到加有饲养细胞的96孔培养板,置细胞孵箱中培养。
47.(4)杂交瘤细胞的筛选:每隔4天换一半培养液(含次黄嘌呤-鸟嘌呤-磷酸核糖转移酶)一次,10天后改用含次黄嘌呤-磷酸核糖转移酶培养液。融合后的杂交瘤细胞在含次黄嘌呤-磷酸核糖转移酶的选择性培养液中大约持续培养两周。吸取培养上清做酶联免疫吸附实验,筛选阳性克隆。采用酶联免疫吸附实验间接法筛选阳性杂交瘤克隆。主要步骤:
①
0.01摩尔每升ph9.6碳酸盐缓冲液稀释h1n1血凝素蛋白,分别于96孔酶标板加入0.1毫升每孔,蛋白浓度20纳克/孔,4℃过夜;
②
0.01摩尔每升ph 7.4磷酸盐缓冲液(含吐温20)洗板三次;
③
用5%牛血清白蛋白0.01摩尔每升ph 7.4的磷酸盐缓冲液封闭2小时;
④
同上洗板;
⑤
加入杂交瘤培养上清,0.1毫升每孔,同时设阳性对照(免疫小鼠血清)、阴性对照(sp2/0培养上清液)和空白对照,室温反应2小时;
⑥
洗板;
⑦
加1:6000稀释的辣根过氧化物酶标记的羊抗小鼠igg,0.1毫升每孔,室温反应1小时;
⑧
洗板;
⑨
加入底物室温避光反应5分钟;
⑩
2摩尔每升硫酸终止反应;450纳米测定其光密度值,以测定值除以阴性≥2.1为阳性。
48.(5)杂交瘤细胞的克隆化:杂交瘤细胞的克隆化培养按有限稀释法进行,选择抗体检测阳性的杂交瘤孔细胞作适当增殖后,准确计数细胞。用完全dmem培养基稀释成10个每毫升的细胞悬液接种到已有饲养细胞的96孔培养板中,每孔0.1毫升,10天后观察细胞生长情况,并检测上清液中抗体水平,选择5个抗体滴度最高的,呈单个克隆细胞生长的培养孔,作再次有限稀释。此方法可重复多次,直至单克隆孔抗体检测阳性率为100%。
49.(6)诱生腹水:在接种杂交瘤细胞前一周,给balb/c小鼠腹腔注射石蜡油每只0.5毫升,然后每只接种5
×
106个阳性杂交瘤细胞,10天后收集腹水测定抗体效价。
50.(7)单克隆抗体的纯化:采用亲和纯化法(protein g交联的sepharose)纯化腹水中单克隆抗体。
①
腹水用冷结合缓冲液稀释3倍后,于4℃10000转每分钟离心15分钟去除沉
淀物。
②
将预装有sepharose-protein g的亲和纯化柱用10倍柱床体积的结合缓冲液充分流洗。
③
将稀释的腹水上柱,控制流速10滴每分钟。
④
将流穿的腹水重复上柱一次。
⑤
用20倍柱床体积的结合缓冲液充分洗涤,直至流穿液280纳米吸光值小于0.01。
⑥
用洗脱缓冲液洗脱结合的单克隆抗体,控制流速10滴每分钟,收集洗脱液于预加有0.1毫升的磷酸钾缓冲液(ph7.9)的收集管中,每管收集0.5毫升含抗体的洗脱液,共收集20管以上。
⑦
于280纳米检测每管洗脱液的吸光度,并收集吸光值大于0.2的洗脱液。
⑧
将收集的洗脱液置于透析卡中,并于0.1摩尔每升ph7.4的磷酸盐缓冲液中透析。每隔6小时换液一次,共透析24小时。
⑨
将透析后的抗体溶液稀释后,于280纳米测蛋白含量。
⑩
将纯化的抗体分装于小管中,置于低温冰箱备用。
51.(8)单克隆抗体的亚型鉴定:采用bio-rad公司的小鼠单克隆抗体免疫球蛋白分型试剂盒分析。将纯化的单克隆抗体作适当稀释后进行检测,操作严格按试剂盒说明书进行。试验结果为zcmu-h1n1杂交瘤细胞分泌的单克隆抗体为igg1、κ型。
52.结果见附图1。
53.(9)单克隆抗体的效价检测:采用elisa方法检测单克隆抗体zcmu-h1n1对h1n1血凝素蛋白的效价:
①
0.01摩尔每升ph9.6碳酸盐缓冲液稀释h1n1血凝素蛋白,分别于96孔酶标板加入0.1毫升每孔,蛋白浓度20纳克/孔,4℃过夜;
②
0.01摩尔每升ph7.4磷酸盐缓冲液(含吐温20)洗板三次;
③
用5%牛血清白蛋白0.01摩尔每升ph7.4的磷酸盐缓冲液封闭2小时;
④
同上洗板;
⑤
用碳酸盐缓冲液稀释单克隆抗体zcmu-h1n1至起始浓度,10微克每毫升。将碳酸盐缓冲液和免疫小鼠血清用作阴性对照和阳性对照。将所有的待测样本做两个复孔,并用碳酸盐缓冲液进行2倍倍比稀释(1:1、1:2、1:4、1:8、1:16、1:32、1:64、1:128、1:256、1:512、1:1024、1:2048)。加入稀释好的样本,0.1毫升每孔,室温反应2小时;
⑥
洗板;
⑦
加1:6000稀释的辣根过氧化物酶标记的羊抗小鼠igg,0.1毫升每孔,室温反应1小时;
⑧
洗板;
⑨
加入底物室温避光反应5分钟;
⑩
2摩尔每升硫酸溶液终止反应;450纳米测定其光密度值,以测定值除以阴性≥2.1为阳性。
54.结果见附图2。
55.实施例2.抗h1n1流感病毒ha蛋白的单克隆抗体zcmu-h1n1抗病毒效应
56.(1)微量中和实验:
①
h1n1流感病毒(a/michigan/45/2015)进行半数组织细胞感染剂量滴定;
②
mdck细胞接种于96孔培养板,每孔2
×
104个细胞,于含5%二氧化碳饱和37℃孵箱中培养24小时;
③
用含0.2%胰酶的病毒培养液稀释病毒至100倍半数组织细胞感染剂量每50微升;
④
在96孔培养板中将10微克每毫升的单克隆抗体zcmu-h1n1用病毒培养液倍比稀释至不同浓度(1:1、1:2、1:4、1:8、1:16、1:32、1:64、1:128、1:256、1:521),每孔50微升;
⑤
在加有抗体的孔中加入50微升的100倍半数组织细胞感染剂量每50微升的病毒液,混匀,每一稀释度做4个复孔;倒数第二列做病毒回滴,病毒从100倍半数组织细胞感染剂量每100微升倍比稀释(1:1、1:2、1:4、1:8、1:16、1:32、1:64、1:128),每孔100微升;最后一列作对照,4孔作为阴性细胞对照(每孔加入100微升的病毒培养液)和4孔作为阳性细胞对照(每孔加入100微升的100倍半数组织细胞感染剂量每100微升的病毒液),于含5%二氧化碳饱和37℃孵箱中孵育2小时;
⑥
取出准备好的96孔mdck细胞培养板,磷酸盐缓冲液洗细胞1遍,将
⑤
中96孔板中的准备好的液体转入细胞培养板中,于含5%二氧化碳饱和37℃孵箱中孵育2小时;
⑦
取出上述96孔细胞板,用磷酸盐缓冲液洗细胞2遍;每孔加入200微升病毒培养
液,于含5%二氧化碳饱和37℃孵箱中孵育72小时;
⑧
取培养72小时后的96孔细胞板,每孔取培养上清液50微升,转至血凝板,再在血凝板中每孔加入50微升的1%鸡红细胞;
⑨
30分钟后观察结果,zcmu-h1n1对h1n1流感病毒具有较好的体外中和效应。
57.结果见附图3。
58.(2)小鼠预防实验:
①
h1n1流感病毒(a/michigan/45/2015)小鼠半数致死量滴定;
②
小鼠分组:7周龄雌性balb/c小鼠,每组5只,共五组,分别编号为第一组至第五组;
③
每只小鼠称重并记录;
④
第一组和第三组小鼠通过腹腔注射3毫克每千克体重的单克隆抗体zcmu-h1n1,第二组和第四组小鼠通过腹腔注射30毫克每千克体重的单克隆抗体zcmu-h1n1,第五组注射30毫克每千克体重的鼠igg1型无关抗体;
⑤
将h1n1流感病毒稀释至10倍半数致死量每50微升,第一、二、五组在注射单克隆抗体zcmu-h1n1或无关抗体6小时后,通过鼻内接种h1n1流感病毒,50微升每只;
⑥
第三、四组在注射单克隆抗体48小时后,通过鼻内接种h1n1流感病毒,50微升每只;
⑥
每天观察并记录体重,单克隆抗体zcmu-h1n1在小鼠体内可以有效预防h1n1流感病毒的感染,在30毫克每千克体重的浓度下可达到100%的保护效率。
59.结果见附图4。
60.(3)小鼠治疗实验:
①
小鼠分组:7周龄雌性balb/c小鼠,每组5只,共七组,分别编号为第一组至第七组;
②
每只小鼠称重并记录;
②
将h1n1流感病毒稀释至10倍半数致死量每50微升,第一组至第七组中所有小鼠通过鼻内接种h1n1流感病毒,50微升每只;
③
感染6小时后,第一、二、三组小鼠分别通过腹腔注射3、10、30毫克每千克体重的单克隆抗体zcmu-h1n1,第七组腹腔注射30毫克每千克体重的鼠igg1型无关抗体;
④
感染48小时后,第四、五、六组小鼠分别通过腹腔注射3、10、30毫克每千克体重的单克隆抗体zcmu-h1n1;
⑤
每天观察并记录体重,单克隆抗体zcmu-h1n1在小鼠体内可以有效治疗h1n1流感病毒的感染,并且治疗效果与治疗时间密切相关,在30毫克每千克体重的浓度下,在感染48小时后仍能达到80%的保护效率。
61.结果见附图5。
62.应理解,本发明是结合最佳实施例进行描述的,然而在阅读了本发明的上述内容后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本技术所附权利要求书所限定的范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。