1.本发明涉及脑电极技术领域,特别涉及一种一体化脑电极结构及其制备方法。
背景技术:
2.脑电监测对于脑类疾病的诊断和手术定位一直以来都具有不可替代的作用,近年来,随着全世界范围“脑计划”的推出,有效高质量的脑电信号采集显得愈发重要,将直接有助于脑功能解码,促进一系列以此为基础的高新技术发展,比如:脑机接口、神经调控等。针对脑电信号采集的方法主要依靠脑部电极,目前应用比较广泛的脑部电极包括4种:1)头皮脑电(eeg);2)皮层脑电(ecog);3)皮层微电极;4)深度脑电极(seeg)。其中,介于颅内刺入式微电极和头皮外脑电极之间的脑部皮层平面电极(ecog),放置电极于硬脑膜下皮层表面,由于其侵入损伤小,采集的脑部皮层表面电信号,比头皮脑电信噪比高、分辨率高(达亚微米级)、信号采集频率范围更大,包含皮层神经元群体活动信息,在脑疾病的诊断与监测、脑机接口系统的性能改善等方面具有广泛的应用前景。皮层脑电采集可认为在信号保真度和临床实用性之间达到了理想的平衡,因此皮层脑电极已在临床上得到了广泛的应用。
3.目前而言,柔性皮层脑电电极系统分为四大部分,分别为前端柔性器件1、柔性电路板(flexible printed circuit,fpc)2、导联线3、信号采集设备(如图1所示)。其中,前端柔性器件1部分仅满足覆盖待测目标区域大脑皮层的面积,作为后端信号连接的柔性电路板2则应试验手术需求设计长度为20厘米~50厘米。柔性电路板2本身仅用作于器件与导联线3的转接,采用工业化的印刷电路板制造工艺,批量加工精度极限约为2密耳(0.508毫米),大面积板材加工难度高,因此,对各类型电路板的设计有较大的局限性。在最终脑电信号采集系统中,柔性电路板2会利用异方导电薄膜(acf)与柔性电极器件热压连接以完成导通组装。由于器件与fpc分体式组装设计以及fpc本身加工等的限制,目前广泛使用的分体式脑电极仍存在许多不足之处,由于fpc本身厚度可达百微米,相较前端器件(厚度小于二十微米)厚度、刚度过大,柔性及贴服性远不及前端器件。因两者连接处靠近大脑组织,fpc的存在可能导致以下问题:
4.1)前端柔性器件无法良好贴服大脑皮层采集位点(如图2所示);
5.2)因其刚性有损伤脑组织的风险;
6.3)两者连接处存在长时间接触体液而失效的风险。
7.4)fpc因其加工工艺极限的限制,导致一定通道数的电路板面积巨大,多层电路板的设计则会成倍的增加其厚度,难以兼具小尺寸和柔性,也难以满足高通量器件的需求;
8.5)面积巨大的电极后端连接板,增加了试验手术上使用操作的难度。
技术实现要素:
9.本发明要解决的是解决现有技术中这种分体式脑电极,使得柔性皮层电极后端需要通过fpc转接件与导联线连接,该fpc转接件过于靠近脑组织,面积较大,难以兼顾小尺寸、高柔性,对实验手术操作不友好等问题。
10.为解决上述技术问题,本技术于一方面公开了一种一体化脑电极结构,其包括依次层叠的柔性衬底层、导线层和绝缘层;
11.导线层包括依次连接的信号采集电极、连接线和焊盘;
12.该绝缘层包括依次连接的第一通孔区、连接区和第二通孔区;
13.该第一通孔区设有第一通孔,该第一通孔能够暴露该信号采集电极,以使该信号采集电极能够接触头皮层,采集脑电信号;
14.该第二通孔区设有第二通孔,该第二通孔能够暴露该焊盘;该焊盘与信号采集设备连接;
15.其中,该连接线、该连接区与柔性衬底层对应的区域形成连接结构,该连接结构为弯折结构,该弯折结构能够拉伸形成长度大于等于预设长度的结构。
16.可选的,该连接结构为螺旋结构;
17.该螺旋结构中相邻的螺旋线之间存在预设距离;
18.该预设距离大于0,且小于等于1厘米。
19.可选的,该第二通孔区的横截面积小于该第一通孔区的横截面积;
20.该连接线结构为环绕该第一通孔区形成的螺旋结构;
21.该第二通孔区位于该螺旋结构的外侧。
22.可选的,该第二通孔区的横截面积小于该第一通孔区的横截面积;
23.该连接线结构为环绕该第二通孔区形成的螺旋结构;
24.该第一通孔区位于该螺旋结构的外侧。
25.可选的,该螺旋结构的螺旋线极坐标路径满足r=a bθ;
26.其中,r表示螺旋线上的点距离中心点的距离;θ为螺旋线上的点相对于与标准线的夹角;a和b表示与螺旋线宽度相关的特征参数。
27.可选的,该连接结构为弧形结构或者波纹结构。
28.可选的,该信号采集电极包括采集电极阵列;
29.该采集电极阵列包括64通道电极阵列、256通道电极阵列或者529通道电极阵列。
30.可选的,该柔性衬底层的材料包括柔性高分子材料;
31.该绝缘层的材料包括柔性高分子材料。
32.可选的,还包括支撑衬底;
33.该支撑衬底设于该柔性衬底的支撑区域的底部;
34.该支撑区域与该焊盘对应。
35.本技术于另一方面还公开了一种一体化脑电极结构的制备方法,其包括:
36.提供一硅衬底;
37.在该硅衬底上制备牺牲层;
38.在该牺牲层上制备柔性衬底层;
39.在该柔性衬底层上形成导线层;该导线层包括依次连接的信号采集电极、连接线和焊盘;
40.在该导线层上形成绝缘层;
41.图形化、并刻蚀该绝缘层形成第一通孔和第二通孔;该绝缘层包括依次连接的第一通孔区、连接区和第二通孔区;该第一通孔位于该第一通孔区,该第一通孔能够暴露该信
号采集电极,以使该信号采集电极能够接触头皮层,采集脑电信号;该第二通孔位于该第二通孔区,该第二通孔区设有第二通孔,该第二通孔能够暴露该焊盘;该焊盘与信号采集设备连接;
42.释放该牺牲层和该牺牲层对应的硅衬底区域,得到该一体化脑电结构,该连接线、该连接区与对应的柔性衬底层的区域形成连接结构,该连接结构为弯折结构,该弯折结构能够拉伸形成长度大于等于预设长度的结构;该硅衬底位于该柔性衬底的支撑区域的底部,该支撑区域与该焊盘对应。
43.采用上述技术方案,本技术提供的一体化脑电极结构具有如下有益效果:
44.该一体化脑电极结构包括依次层叠的柔性衬底层、导线层和绝缘层,导线层包括依次连接的信号采集电极、连接线和焊盘,该绝缘层包括依次连接的第一通孔区、连接区和第二通孔区,该第一通孔区设有第一通孔,该第一通孔能够暴露该信号采集电极,以使该信号采集电极能够接触头皮层,采集脑电信号,该第二通孔区设有第二通孔,该第二通孔能够暴露该焊盘;该焊盘与信号采集设备连接,其中,该连接线、该连接区与对应的柔性衬底层的区域形成连接结构,该连接结构为弯折结构,该弯折结构能够拉伸形成长度大于等于预设长度的结构;而现有技术中受限于基板尺寸(宽度为10厘米),只能通过后续使用fpc板来实现将电极与信号采集设备连接,存在fpc转接件过于靠近脑组织,面积较大,难以兼顾小尺寸、高柔性,对实验手术操作不友好等问题;基于本技术公开的该一体化脑电极结构,后续在使用过程中,可以利用生物硅胶对连接结构进行形状固定,从而可以得到所需的连接结构长度,该连接结构不受限于制备过程中基板尺寸的限制,具有避免fpc板与电极结构后端连接易造成电极结构贴附性差;且该种一体式结构与分体式相比,具有通量大的优点。
附图说明
45.为了更清楚地说明本技术实施例中的技术方案,下面将对实施例描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本技术的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
46.图1为现有技术中柔性皮层脑电电极系统的结构示意图;
47.图2为现有技术中前端柔性器件与柔性电路板的连接示意图;
48.图3为本技术一种可选的一体化脑电极结构的结构示意图;
49.图4为本技术另一种可选的一体化脑电极结构的结构示意图;
50.图5为本技术一种可选的脑电极结构的制备流程图;
51.图6为本技术扭转固定后的脑电极结构的示意图;
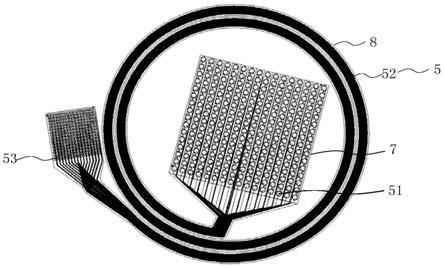
52.图7为本技术提供的一种可选的脑电极结构应用场景图;
53.图8为本技术提供的另一种可选的脑电极结构应用场景图。
54.以下对附图作补充说明:
55.1-前端柔性器件;2-柔性电路板;3-导联线;4-信号采集设备;5-导线层;51-信号采集电极;52-连接线;53-焊盘;6-柔性衬底;7-绝缘层;71-第一通孔;72-第二通孔;8-连接结构;9-采集电极结构;10-焊盘结构;11-硅衬底;12-牺牲层;13-支撑衬底。
具体实施方式
56.下面将结合本技术实施例中的附图,对本技术实施例中的技术方案进行清楚、完整地描述。显然,所描述的实施例仅仅是本技术一部分实施例,而不是全部的实施例。基于本技术中的实施例,本领域普通技术人员在没有作出创造性劳动的前提下所获得的所有其他实施例,都属于本技术保护的范围。
57.此处所称的“一个实施例”或“实施例”是指可包含于本技术至少一个实现方式中的特定特征、结构或特性。在本技术的描述中,需要理解的是,术语“上”、“下”、“顶”、“底”等指示的方位或位置关系为基于附图所示的方位或位置关系,仅是为了便于描述本技术和简化描述,而不是指示或暗示所指的装置或元件必须具有特定的方位、以特定的方位构造和操作,因此不能理解为对本技术的限制。此外,术语“第一”、“第二”仅用于描述目的,而不能理解为指示或暗示相对重要性或者隐含指明所指示的技术特征的数量。由此,限定有“第一”、“第二”的特征可以明示或者隐含的包括一个或者更多个该特征。而且,术语“第一”、“第二”等是用于区别类似的对象,而不必用于描述特定的顺序或先后次序。应该理解这样使用的数据在适当情况下可以互换,以便这里描述的本技术的实施例能够以除了在这里图示或描述的那些以外的顺序实施。
58.尽管阐述本发明的广泛范围的数值范围和参数是近似值,但是具体实例中列出的数值尽可能精确地报告。然而,任何数值固有地包含由其各自测试测量中发现的标准偏差必然产生的某些误差。
59.当本文中公开一个数值范围时,上述范围视为连续,且包括该范围的最小值及最大值,以及这种最小值与最大值之间的每一个值。进一步地,当范围是指整数时,包括该范围的最小值与最大值之间的每一个整数。此外,当提供多个范围描述特征或特性时,可以合并该范围。换言之,除非另有指明,否则本文中所公开之所有范围应理解为包括其中所归入的任何及所有的子范围。例如,从“1至10”的指定范围应视为包括最小值1与最大值10之间的任何及所有的子范围。范围1至10的示例性子范围包括但不限于1至6.1、3.5至7.8、5.5至10等。
60.参阅图3,图3为本技术一种可选的一体化脑电极结构的结构示意图。该一体化脑电极结构包括依次层叠的柔性衬底层、导线层和绝缘层,导线层包括依次连接的信号采集电极、连接线和焊盘,该绝缘层包括依次连接的第一通孔区、连接区和第二通孔区,该第一通孔区设有第一通孔,该第一通孔能够暴露该信号采集电极,以使该信号采集电极能够接触头皮层,采集脑电信号,该第二通孔区设有第二通孔,该第二通孔能够暴露该焊盘;该焊盘与信号采集设备连接,其中,该连接线、该连接区与柔性衬底层对应的区域形成连接结构,该连接结构为弯折结构,该弯折结构能够拉伸形成长度大于等于预设长度的结构。
61.参阅图1-2,现有技术中受限于基板尺寸(宽度为10厘米),只能通过后续使用fpc板来实现将电极与信号采集设备4连接,存在fpc转接件过于靠近脑组织,面积较大,难以兼顾小尺寸、高柔性,对实验手术操作不友好等问题;基于本技术公开的一体化脑电极结构,后续在使用过程中,可以利用生物硅胶对连接结构8进行形状固定,从而可以得到所需的连接结构8长度,该连接结构8不受限于制备过程中基板尺寸的限制,具有避免fpc板与电极结构后端连接易造成电极结构贴附性差;且该种一体式结构与分体式相比,具有通量大的优点。
62.需要说明的是,上述仅对导线层5和绝缘层7进行了相应的划分,实际上,柔性衬底6为了适配导线层5的信号采集电极51、连接线52和焊盘53,也可划分为对应的三个区域。第一通孔区、信号采集电极51以及对应的柔性衬底层6形成采集电极结构;第二通孔区、焊盘53和对应的柔性衬底层6形成焊盘结构。
63.可选的,考虑到实验操作中的无菌要求,减小手术的感染风险,连接结构8部分最终使用时应满足一定长度需求,可以是10~30厘米。
64.于一种可行的实施例中,为了适配mems加工工艺的标准硅基底4寸或6寸晶圆,将电极的连接线52部分设计为螺旋结构,该螺旋结构中相邻的螺旋线之间存在预设距离,该预设距离大于0,且小于等于1厘米,可选的,该预设距离大于50微米,小于500微米。从而实现一定长度连接线52的器件总体加工面积小且集中,改设计可应用于各通道数型号的柔性皮层电极上。
65.于一种可行的实施例中,参阅图3,该第二通孔区的横截面积小于该第一通孔区的横截面积,该连接线52结构为环绕该第一通孔区形成的螺旋结构,该第二通孔区位于该螺旋结构的外侧。于另一种可行的实施例中,参阅图4,图4为本技术另一种可选的一体化脑电极结构的结构示意图。该第二通孔区的横截面积小于该第一通孔区的横截面积,该连接线52结构为环绕该第二通孔区形成的螺旋结构,该第一通孔区位于该螺旋结构的外侧。上述两种结构布局可以根据通道数以及螺旋线的宽度设计,只要保证整体结构占用面积较小即可。
66.于一种可行的实施例中,为了使得该脑电极结构的整体结构在基板上的尺寸占用较小,该螺旋结构的螺旋线极坐标路径满足r=a bθ,其中,r表示螺旋线上的点距离中心点的距离;θ为螺旋线上的点相对于与标准线的夹角;a和b表示与螺旋线宽度相关的特征参数。
67.于另一种可行的实施例中,该连接结构8为弧形结构或者波纹结构。
68.于一种可行的实施例中,根据不同型号电极的通道数多少,设计选择连接结构8的围绕中心为采集电极结构9或者焊盘结构10。该信号采集电极51包括采集电极阵列,该采集电极阵列包括64通道电极阵列、256通道电极阵列或者529通道电极阵列。
69.于一种可行的实施例中,该柔性衬底层6的材料包括柔性高分子材料,该绝缘层7的材料包括柔性高分子材料,该柔性高分子材料包括聚酰亚胺或者su8。
70.于一种可行的实施例中,该一体化脑电极结构还包括支撑衬底13,该支撑衬底13设于该柔性衬底6的支撑区域的底部,该支撑区域与该焊盘53对应,便于将该焊盘结构10与信号采集设备4连接。
71.参阅图5,图5为本技术一种可选的脑电极结构的制备流程图。本技术于另一方面还公开了一种一体化脑电极结构的制备方法,其包括:
72.1)提供一硅衬底11,参阅图5中的图(a)。
73.2)在该硅衬底11上制备牺牲层12。
74.可选的,该牺牲层12的材料可以是铝,厚度为0.5-2微米。
75.可选的,在步骤2)中,可以先溅射牺牲层12(如图5中的图(b)所示),再对该牺牲进行图形化,从而得到如图5中的图(c)所示的结构。
76.3)在该牺牲层12上制备柔性衬底层6,参阅图5中的图(d)。
77.可选的,该柔性衬底层6的材料可以为生物相容性良好的聚酰亚胺。
78.4)在该柔性衬底层6上形成导线层5;该导线层5包括依次连接的信号采集电极51、连接线52和焊盘53,参阅图5中的图(e)和图(f)。
79.可选的,信号采集电极51和连接线52的材料可以为铬/金、铬/银或者铬/铂中的任一种。
80.可选的,焊盘53的材料可以为铬/镍/金、铬/镍/银或者铬/镍/铂中的任一种,增加了焊盘53的厚度,提高了焊盘53与外部设备连接的强度。
81.可选的,步骤4)具体可以阐述为:在该柔性衬底6上沉积金属材料层,图形化该金属材料层,并对其进行刻蚀,形成上述导线层5。
82.5)在该导线层5上形成绝缘层7,参阅图5中的图(g)。
83.6)图形化、并刻蚀该绝缘层7形成第一通孔71和第二通孔72,参阅图5中的图(h)。
84.该绝缘层7包括依次连接的第一通孔区、连接区和第二通孔区,该第一通孔71位于该第一通孔区,该第一通孔71能够暴露该信号采集电极51,以使该信号采集电极51能够接触头皮层,采集脑电信号;该第二通孔72位于该第二通孔区,该第二通孔区设有第二通孔72,该第二通孔72能够暴露该焊盘53,该焊盘53与信号采集设备4连接。
85.7)释放该牺牲层12和该牺牲层12对应的硅衬底11区域,得到该一体化脑电结构,该连接线52、该连接区与对应的柔性衬底层6的区域形成连接结构8,该连接结构8为弯折结构,该弯折结构能够拉伸形成长度大于等于预设长度的结构;该硅衬底11位于该柔性衬底6的支撑区域的底部,该支撑区域与该焊盘53对应,参阅图5中的图(i)。
86.制备完成后,连接结构8无法仅靠其平面的结构布局而拉伸呈直线,故后续需要将器件的连接结构8进行扭转卷曲,使其整体形成一条细线;之后利用生物硅胶将扭转后的器件进行定形。
87.连接线52可根据扭转卷曲的疏密控制最终形成的连接线52的线径粗细(线径最细约为1毫米),而与版图设计的平面宽度无关;扭转组装后的连接线52长度也因此可调。例如平面设计长度为45厘米的连接线52扭转组装后长度范围为20~35厘米。
88.对上述连接线52进行扭转卷曲后,使用生物硅胶对连接线52进行形状固定。生物硅胶a型、b型以1:1的比例充分混合,将混合液涂覆于扭转后的连接线52上,使其完全包裹连接。之后将器件置于烘箱中,在50℃下烘烤2h使其充分固化。因生物硅胶的的弹性,固化后的连接线52部分仍具备一定的可拉伸性,长度伸长范围控制在0~5厘米,参阅图6,图6为本技术扭转固定后的脑电极结构的示意图。
89.需要说明的是,除了上述先扭转再固定的方法外,实际上也可直接将上述弯折结构拉伸后的结构使用生物硅胶进行固定,从而形成所需的连接线52。
90.本技术提供的一体化柔性皮层脑电极结构,可应用在神经科学研究中大范围脑电信号的探测以及前沿科技与人工智能相关的信号采集等领域。针对目前分体式电极庞大冗余的后端连接设计,集成柔性脑电极前端信号采集部分与后端fpc连接板,设计了一体化的柔性皮层脑电极器件,器件设计有细长的柔性连接线52部分,并使用二维螺旋结构提高可加工性。利用mems加工工艺可设计器件在电极进行高通量设计时,仍具备轻便、细长的后端连接;连接线52可根据应用需求进行扭转组装,并使用生物硅胶固定形状。其组装长度、粗细可调,定型后仍具备一定拉伸性能,可能增强其操作便捷性,大大降低器件可能引起的生
物学风险,并为脑电信号微创长期采集提供可能性。
91.实施案例1
92.采用上述制备方法制备得到脑电极结构可以进行急性脑电信号采集,如图7所示,图7为本技术提供的一种可选的脑电极结构应用场景图。该脑电极结构放置在脑皮层上,其中细长的连接线52可埋于皮下,直至挂于耳后或至锁骨处,焊盘结构10与导联线3连接,该导联线3与信号采集设备4连接。
93.实施案例2
94.按照前述制造流程制得的一体化脑电极结构可以在体长期植入,以采集对应区域信号,参阅图8,图8为本技术提供的另一种可选的脑电极结构应用场景图。该脑电极结构放置在脑部待采集区域上,连接结构8埋于颅骨下,后经颅骨连接至焊盘结构10,该焊盘结构10可固定于颅顶基座内,体积小且轻,焊盘结构10与导联线3连接,该导联线3与信号采集设备4连接。
95.以上所述仅为本技术可选实施例,并不用以限制本技术,凡在本技术的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本技术的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
