1.本发明属于生物医用材料及其制备领域,特别涉及一种骨-韧带-骨一体化支架及其制备方法。
背景技术:
2.人体韧带白色带状的结缔组织,质坚韧,有弹性,能把骨骼连接在一起,加强骨头的稳定性。当遭受暴力,产生非生理性活动,韧带被牵拉而超过其耐受力时,即会发生损伤。韧带损伤主要是由剧烈运动和外力因素,包括断裂、撕裂、退行性变或炎症,已成为人体最常见的损伤之一。另外,膝关节是人体最容易受伤的关节之一,膝关节的稳定性主要靠膝关节内外一系列结构来维系,包括骨性结构、关节外结构以及关节内结构;骨性结构主要包括髌骨、股骨髁远端和胫骨髁。
3.当前,临床治疗上主要手段为直接缝合、自体移植、同种异体移植、异种移植和人工假体材料修复术来修复韧带损伤。自体移植和异体移植物具有良好生物相容性,为临床首选,但存在供体来源少、对供体有损伤、免疫排斥等固有缺陷,而人工韧带由于其不存在来源不足的缺点、力学强度高、无疾病传播风险、早期重建效果较好等明显优势,引起人们的重视。然而,这些手术或修复技术都有其固有的缺陷,例如供体缺乏、供体部位并发症、机械强度不足、复发性撕裂、免疫排斥和较差的支架整合性等。
4.人工韧带植入骨道后与宿主骨之间在组织学特征上有一定差异,韧带假体缺乏骨传导性,无法刺激骨道愈合,导致移植物-骨愈合障碍,骨道扩大严重,造成其在骨道内难以自体化。因此当前临床的突出问题是骨道的扩大。目前许多基础研究偏向于骨道段/关节腔段支架的单一改进,未对骨道段和关节腔段做整体性的研究。现有的人工韧带无法实现韧带段与骨段支架的整合,很难达到韧带和骨同时修复的理想效果,影响韧带功能。目前,尚缺乏一种理想的韧带修复支架,为韧带和骨到再生提供适宜的理化和生物学微环境,确保手术方式操作简单便捷。因此,寻找新型的骨-韧带-骨一体化支架具有极其重要的临床意义。针对上述问题,有必要对现有的人工韧带的结构进行改进,对其结构进行精密设计和整合,制备出一种骨-韧带-骨一体化支架,实现韧带和骨修复的协同、快速和预后良好的多重目的。
5.中国专利cn110037830a公开了一种仿生全成型三相结构人工韧带及其制备方法,该韧带包括由位于中部的关节腔纤维束段及位于两端的骨隧道编织段组成的三相结构,但其骨隧道编织段无法紧密充实骨道,并且支撑骨道的力学强度。
技术实现要素:
6.本发明所要解决的技术问题是提供一种骨-韧带-骨一体化支架及其制备方法,以克服现有技术中人工韧带支架无法实现关节腔段韧带和骨同时修复的缺陷。
7.本发明提供一种骨-韧带-骨一体化支架,所述一体化支架为三段式结构,包括两端骨支架部分和中间段韧带支架部分,所述中间段韧带支架部分为关节腔纳米纤维纱线编
织段,所述骨支架部分为相分离支架段。
8.优选地,所述关节腔纳米纤维纱线编织段是由纳米纤维纱线编织而成,所述纳米纤维纱线包括芯层聚合物线和外层电纺纳米纤维。
9.优选地,所述聚合物线包括pla线、plcl线、plga线、sf线中的一种或几种。
10.优选地,所述电纺纳米纤维材料包括聚己内酯、乳酸-己内酯共聚物、乳酸-羟基乙酸共聚物、丝素蛋白、明胶、海藻酸钠、羧甲基纤维素、壳聚糖、透明质酸钠中的一种或几种。
11.优选地,所述电纺纳米纤维材料还包括可负载生长因子、抗炎药物中的一种或几种。
12.优选地,所述相分离支架段是由相分离溶液相分离而成,所述相分离溶液为可降解合成聚合物溶液或天然高分子物质溶液。
13.优选地,所述可降解合成聚合物包括pla、pcl、plga、聚羟基脂肪酸酯中的一种或几种。
14.优选地,所述天然高分子物质包括明胶、壳聚糖、胶原蛋白、丝素蛋白中的一种或几种。
15.优选地,所述相分离溶液含有小分子化合物、无机矿物质、多肽类物质中的一种或几种。
16.优选地,所述小分子化合物包括去铁胺、双膦酸盐、地塞米松中的一种或几种。
17.优选地,所述无机矿物质包括羟基磷灰石、介孔硅、生物活性玻璃、乳酸钙、生物陶瓷中的一种或几种。
18.优选地,所述多肽类物质包括骨形态发生蛋白、血小板衍生生长因子、转化生长因子中的一种或几种。
19.优选地,所述一体化支架长度为25~120mm,韧带支架部分长度为10~50mm,直径为2~10mm,两端骨支架部分中单边骨段支架长度为10~30mm,直径为2~15mm。
20.本发明还提供一种骨-韧带-骨一体化支架的制备方法,包括以下步骤:
21.(1)将可降解合成聚合物或天然高分子物质溶于溶剂中,得到纺丝液,将芯层聚合物线穿过中间旋转漏斗,将纺丝液转移至两个对喷注射器中,对两个对喷注射器纺丝头分别施加正负电场,向中间旋转漏斗和聚合物线喷出纳米纤维,利用旋转漏斗将纳米纤维加捻到聚合物线,得到纳米纤维纱线,编织,得到编织支架;
22.(2)将可降解合成聚合物或天然高分子物质溶于有机溶剂中,得到相分离溶液,将步骤(1)中编织支架两端分别置于模具内部,然后向模具中加入相分离溶液,冷冻,冷冻干燥,得到骨-韧带-骨一体化支架。
23.优选地,所述步骤(1)中可降解合成聚合物包括聚己内酯、乳酸-己内酯共聚物、乳酸-羟基乙酸共聚物中的一种或几种。
24.优选地,所述步骤(1)中天然高分子物质包括丝素蛋白、明胶、海藻酸钠、羧甲基纤维素、壳聚糖、透明质酸钠中的一种或几种。
25.优选地,所述步骤(1)中溶剂包括六氟异丙醇、三氟乙醇、二氯甲烷、三氟乙酸中的一种或几种。
26.优选地,所述步骤(1)中纺丝液质量分数浓度为5%~20%。进一步优选8%、10%、12.3%、15.5%、19%,更优选10%。
27.优选地,所述步骤(1)中纺丝液中加入药物;所述药物包括生长因子以及抗炎药物中的一种或几种。
28.优选地,所述步骤(1)中注射器的供液速度为0.8ml/h~2.5ml/h,两个对喷注射器纺丝头与旋转漏斗之间的距离为8cm~20cm,正电场的电压为6kv~18kv,负电场的电压为6kv~18kv,旋转漏斗的转速为100转/分钟~800转/分钟。
29.优选地,所述步骤(1)中聚合物线是由直径在20~50微米的聚合物单纤维经并合、牵伸形成的直径为0.03~0.1mm的单根线。
30.优选地,所述步骤(1)中编织根数为6~20根;编织方式为手工编织、针织以及机器编织、针织中的一种或几种。
31.优选地,所述步骤(2)中有机溶剂包括二氧六环、二甲基亚砜、四氢呋喃中的一种或几种。
32.优选地,所述步骤(2)中相分离溶液浓度为0.05~0.15g/ml。
33.优选地,所述步骤(2)中相分离溶液中加入小分子化合物、无机矿物质、多肽类物质中一种或几种。
34.优选地,所述步骤(2)中模具为圆柱形,直径为2~8mm,长度为1~12cm。
35.优选地,所述步骤(2)中冷冻温度为-80℃~-200℃,冷冻时间为12~72h。
36.本发明还提供一种上述制备方法制备得到的骨-韧带-骨一体化支架。
37.本发明还提供一种一体化支架在制备韧带修复材料中的应用。
38.本发明包括由位于中部的关节腔纳米纤维纱线编织段和位于两端的骨道相分离支架段组成的一体化支架,填补了人工韧带支架无法实现关节腔段韧带和骨同时修复的空白。
39.本发明涉及的编织支架类似于“麻花辫”结构。
40.有益效果
41.(1)本发明骨-韧带-骨一体化支架由两个部分组成,支架两端为骨支架,中间段为韧带支架,该支架对骨道段和关节腔段整体性的研究。
42.(2)本发明骨-韧带-骨一体化支架,植入后在关节腔内实现引导韧带组织再生,在骨道中促进骨道愈合,解决骨道扩大问题。
43.(3)本发明骨-韧带-骨一体化支架,骨段支架不仅能够有效刺激骨组织生长,而且为骨道修复提供力学支撑。
44.(4)本发明骨-韧带-骨一体化支架,韧带段支架具有较强的力学性能,满足患者日常生活、运动等力学要求,并且孔径大小适宜,有利于细胞长入,引导韧带组织再生。
45.(5)本发明中所用地聚合物和天然高分子均为生物可降解材质,在一定时期内可以逐渐降解掉,降解产物可以随人体正常新陈代谢排出,对人体没有任何副作用,支架起到暂时性替代作用,完全修复后不影响人体正常组织功能。
46.(6)本发明骨-韧带-骨一体化支架,可根据临床需求,可在制备过程中在纳米纤维纱线中加入抗炎、防组织粘连药物或生长因子,减轻炎症反应、避免组织粘连和促进韧带修复及正常功能恢复;在骨段支架中加入小分子化合物、无机矿物质、多肽类物质等,刺激骨生长和增强支架力学性能。
附图说明
47.图1为本发明骨-韧带-骨一体化支架三段式结构示意图,其中b1、b2为骨支架,t为韧带支架;
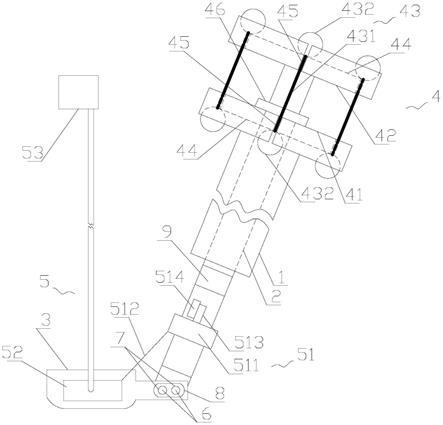
48.图2为本发明静电纺纳米纤维纱线制备过程示意图;
49.图3为本发明骨-韧带-骨一体化支架制备流程示意图;
50.图4为本发明实施例1中乳液静电纺ctgf@plcl皮芯结构纳米纤维扫描电镜图;
51.图5为本发明实施例1中介孔羟基磷灰石透射电镜图;
52.图6为本发明实施例1中一体化支架的韧带段支架扫描电镜(插图为放大图)和水接触角图片;
53.图7为本发明实施例1中一体化支架的骨段支架扫描电镜(插图为放大图)和水接触角图片;
54.图8为本发明骨-韧带-骨一体化支架实物照片;
55.图9为本发明实施例1中骨-韧带-骨一体化支架的拉伸过程(a)和承重(b)照片;pla、pla/mha和pla/dfo@mha支架的压缩应力-应变曲线(c)、弹性模量(d)和压缩强度(e);sf、sf/plcl和sf/ctgf@plcl支架的拉伸应力-应变曲线(f)、杨氏模量(g)、拉伸强度(h)和断裂伸长率(i);
56.图10为本发明骨-韧带-骨一体化支架(sf/ctgf@plcl韧带段支架与pla/dfo@mha相分离溶液对应制备的骨-韧带-骨一体化支架)用于新西兰白兔膝关节交叉韧带修复的手术过程图片(
ⅰ‑ⅵ
);
57.图11为本发明实施例1骨-韧带-骨一体化支架用于新西兰白兔膝关节交叉韧带修复24周后观察图片,其中(
ⅰ‑ⅲ
)分别为sf、sf/plcl和sf/ctgf@plcl组支架用于兔子前交叉韧带重建术后6个月大体观察。
具体实施方式
58.下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。此外应理解,在阅读了本发明讲授的内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本技术所附权利要求书所限定的范围。
59.实施例1
60.本实施例以丝素蛋白线(直径100-200μm;上海同杰良生物材料有限公司)作为纳米纤维纱线的芯层,以高分子聚合物plcl和结缔组织生长因子ctgf共混制备纺丝液,以介孔羟基磷灰石(mha)负载去铁胺(dfo)与高分子聚合物pla配成相分离溶液。具体制备过程如下:
61.s1:配制纺丝液:用磷酸盐缓冲液配置浓度为2μg/ml的ctgf(美国peprotech公司)溶液,准确量取10ml二氯甲烷(购于国药集团化学试剂有限公司)置于玻璃瓶中,同时向二氯甲烷溶液中滴加0.1ml的司盘80(购于阿拉丁生化科技股份有限公司)和0.5ml的ctgf溶液,然后高速搅拌12h,最后加入1.0g的plcl(mw=80000,济南岱罡生物科技有限公司),继续搅拌过夜,配成质量体积浓度为0.1g/ml的ctgf@plcl纺丝液。
62.s2:纳米纤维纱线的制备:如图2所示,丝素蛋白线2穿过多功能静电纺纱机的中间
旋转漏斗1中,作为芯层,将s1中10ml纺丝液(转移至多功能静电纺纱机的两个对喷注射器4中,注射器4置于推进泵5上,两个对喷注射器纺丝头3分别施加正负高压电源8,启动多功能静电纺纱机,两个对喷注射器喷头3喷出纳米纤维6,利用旋转漏斗1将纳米纤维6加捻到丝素蛋白线中,接收辊9收集,得到纳米纤维纱线7。纺丝液分别为plcl溶液(s1中不添加ctgf溶液,其余均与上述s1相同)和ctgf@plcl溶液时,制备得到sf/plcl和sf/ctgf@plcl纱线。纺丝参数如下:直流高压8kv,推进速度1.2ml/h,接收距离12cm,旋转漏斗转速400转/分钟,接收辊8转/分钟。
63.s3:韧带段支架的制备:将8根s2中得到的纳米纤维纱线通过手工编织的方式(类似于“麻花辫”结构)制成韧带段支架。
64.s4:介孔羟基磷灰石的制备:称量5.55g cacl2(购于国药集团化学试剂有限公司)溶于100ml去离子水中,称量7.10g na2hpo4溶于100ml去离子水中;称量0.005mol十六烷基三甲基溴化铵(ctab,购于阿拉丁生化科技股份有限公司)加入na2hpo4溶液中搅拌1h;将na2hpo4和ctab混合溶液滴加到16.7ml剧烈搅拌的cacl2溶液中;用浓度为1m的naoh溶液调节反应体系ph值再11~12;将混合溶液倒入反应釜,置于油浴锅中150℃反应15h,冷却后分别用水和酒精对所得沉淀物离心洗涤多次,于烘箱中80℃干燥12h;最后,将粉体在马弗炉中600℃煅烧去除模板剂ctab,得到介孔羟基磷灰石。
65.s5:介孔羟基磷灰石载dfo:准确称量3mg dfo(美国sigma-aldrich公司)溶于10ml pbs溶液,配成0.3mg/mldfo溶液;称量100mg mha加入dfo溶液中,连续搅拌24h,然后离心收集沉淀物,冷冻干燥得到载dfo的介孔羟基磷灰石(dfo@mha)。
66.s6:称量0.8g聚乳酸(购于济南岱罡生物科技有限公司)溶于10ml二氧六环溶剂(购于国药集团化学试剂有限公司)中,配制0.08g/ml的pla相分离溶液;称量0.08g s5中得到的dfo@mha加入pla相分离溶液中,充分搅拌、超声混匀。相分离溶液分别为pla溶液(在步骤s6不添加dfo@mha,其余与pla/dfo@mha相同),pla/mha溶液(不进行步骤s5,直接进行步骤s4和s6),pla/dfo@mha溶液。
67.s7:将s3中所述的编织支架两端分别置于模具(圆柱形,直径为3mm,高为12mm)内部,然后向模具中加入s6中的0.5ml相分离溶液,迅速置于-80℃条件下冻存48小时,然后置于冷冻干燥机中冻干得到骨-韧带-骨一体化支架(单纯的丝素蛋白线编织支架与pla相分离溶液对应制备骨-韧带-骨一体化支架,sf/plcl韧带段支架与pla/mha相分离溶液对应制备骨-韧带-骨一体化支架,sf/ctgf@plcl韧带段支架与pla/dfo@mha相分离溶液对应制备骨-韧带-骨一体化支架)。
68.图9对应的pla、pla/mha和pla/dfo@mha支架是分别将pla相分离溶液、pla/mha相分离溶液、pla/dfo@mha相分离溶液加入模具冻存、冻干得到,其中不需要将编织支架两端分别置于模具,模具、冻存条件与上述s7相同。
69.图9对应的sf、sf/plcl和sf/ctgf@plcl支架是分别将单纯的丝素蛋白线、sf/plcl纱线和sf/ctgf@plcl纱线进行上述s3得到。
70.图4表明:本实施例制备的包芯纱其外层纳米纤维为皮芯结构,纳米纤维的核层为ctgf溶液,壳层为plcl,纳米纤维直径约500nm。乳液静电纺纳米纤维的过程中,水相以小液滴的形式分散于油相中,乳化剂在界面吸附形成界面膜,从而在一定程度上保证了乳化液的稳定性。静电纺丝过程中包覆在油相溶液中的水相小液滴,由于静电拉伸力影响两种溶
液之间摩擦力而形成“皮芯”结构。
71.图5表明:本实施例制备的介孔羟基磷灰石为棒状结构,直径约100nm,羟基磷灰石上含有大量直径为4~5nm的介孔结构,这种介孔结构有利于吸附小分子化合物、多肽等活性物质。
72.图6表明:本实施例制备的韧带段支架显微结构,单纯的丝素蛋白线编织支架内部为微米纤维结构,表面光滑,不利于细胞黏附、生长;丝素蛋白外层包裹纳米纤维后得到的sf/plcl以及sf/ctgf@plcl纱线编织支架内部为纳米纤维结构,并且表面较为粗糙,有利于细胞黏附、生长。水接触角小于90度表明支架具有良好的亲水性,也更有益于细胞黏附。
73.图7表明:本实施例制备的骨段支架具有相互连通的大孔结构,孔径为5~20μm;单纯的pla支架水接触角为126
°
,加入介孔羟基磷灰石后显著改善了pla的亲水性(水接触角为83
°
和84
°
)。大孔结构有利于细胞生长、渗透,亲水性提高有利于增加细胞黏附性能。
74.图8表明:本实施例制备的骨-韧带-骨一体化支架外观为三段式结构,中间段为纳米纤维纱线编织结构,具有大孔结构,用于修复韧带;两端为相分离支架,支架外观致密,为骨道提供力学支撑,用于修复骨段。临床上用于韧带修复时,可根据实际损伤部位、损伤韧带位置以及韧带尺寸等信息,对该骨-韧带-骨一体化支架进行相应的设计、制备、生产等,制备适于损伤韧带的形状以及尺寸。
75.图9表明:本实施例制备的骨-韧带-骨一体化支架具有良好的力学性能,受一定力作用后,相分离支架和编织支架均不会断裂,并且相分离支架与编织支架不会发生脱离,说明两者之间紧密结合在一起,能够满足手术过程中对支架的牵拉力,植入后不会轻易脱离。
76.图9(a)为骨-韧带-骨一体化支架拉伸过程照片,施加一定拉力后一体化支架两端的热致相分离支架最先出现裂纹,随着拉力的持续增加,编织支架也开始破裂直至完全断裂。在整个拉伸过程中,热致相分离支架和编织支架之间始终保持紧密结合,没有发生相互脱落。图9(b)展示了骨-韧带-骨一体化支架拉伸承重能力,单个一体化支架至少可以承受约1.5kg的重量,大约是其自身重量的30000倍,说明支架具有良好的力学性能,能够满足手术过程中对其牵拉的力学要求。为了研究mha对pla支架的力学增强效果,测试了pla、pla/mha和pla/dfo@mha支架的压缩应力-应变曲线(图9c)、压缩模量(图9d)以及抗压强度(图9e)。由结果可知,三组支架的抗压强度随着压缩应变的增加而增大,并且表现出相似的应力-应变曲线。pla/mha(7.05
±
1.20mpa)和pla/dfo@mha(6.98
±
0.21mpa)支架的压缩模量均显著高于pla支架(4.95
±
0.59mpa)(p《0.05),分别提高了42.4%和41.0%。此外,pla/mha(4.05
±
0.40mpa)和pla/dfo@mha(3.83
±
0.31mpa)支架的抗压强度略高于pla支架(3.71
±
0.57mpa)。由此可见,mha的加入提高了pla支架的力学性能。其中,压缩力学测试条件:样品置于两个压板正中间位置,以2mm/min的速率缓慢、均匀地进行压缩,当压缩至80%后停止加载,得到相应的应力-应变曲线。通过应力-应变曲线起始段的斜率计算压缩模量。拉伸力学测试条件:样品两端分别固定在拉力试验机的夹具上,原始标距为20mm,以拉伸速率10mm/min进行单轴拉伸直至样品断裂,得到相应的应力-应变曲线。
77.sf、sf/plcl和sf/ctgf@plcl三种编织支架的拉伸应力-应变曲线、相关机械性能如图9(f-i)所示。sf/plcl支架的杨氏模量(图9g)和拉伸强度(图9h)分别为132.50
±
12.29mpa和40.23
±
1.53mpa,均显著高于sf支架(杨氏模量和拉伸强度分别为98.29
±
11.85mpa和32.17
±
1.67mpa)。同样,sf/ctgf@plcl支架的杨氏模量(127.85
±
12.61mpa)和
拉伸强度(36.38
±
1.15mpa)也显著高于sf支架(p《0.05),说明皮层纳米纤维能够提高支架的机械强度。三组支架的断裂伸长率在31.8%-35.1%之间,无显著性差异(p》0.05)(图9i)。根据文献报道,人体正常前交叉韧带的抗拉强度约为35mpa,因此,该支架的抗拉强度与人体前交叉韧带相匹配。
78.验证实施:
79.如图10所示,本实施例制备的骨-韧带-骨一体化支架用于新西兰白兔膝关节交叉韧带修复的手术过程图片。采用兔膝关节交叉韧带损伤模型,实验兔麻醉后固定在实验台上,膝关节皮肤酒精消毒,用手术刀切开皮肤暴露膝关节交叉韧带;将膝关节交叉韧带切掉,用无菌电钻分别在股骨和胫骨上钻两个直径为3mm的骨道;然后将本实施例制备的骨-韧带-骨一体化支架沿股骨的骨道牵拉植入对应部位,两端骨段支架分别植入股骨和胫骨骨道,韧带段支架植入关节腔;最后缝合皮肤,置于无菌动物房饲养。
80.如图11所示,本实施例制备的骨-韧带-骨一体化支架用于新西兰白兔膝关节交叉韧带修复24周,可以看到经过修复后成功再生出膝关节交叉韧带,并且骨道愈合,说明本发明提供的骨-韧带-骨一体化支架具有良好的韧带再生以及促进骨愈合效果。
81.实施例2
82.本实施例以pla线作为纳米纤维纱线的芯层,以高分子聚合物pcl制备纺丝液,以二氧化硅与聚乳酸-羟基乙酸共聚物(plga)配成相分离溶液。具体制备过程如下:
83.s1:配制纺丝液:准确称量1.0g pcl(mw=100000,深圳光华伟业股份有限公司)溶于10ml六氟异丙醇(购于上海达瑞精细化学品有限公司)中,搅拌过夜,配成质量体积浓度为0.1g/ml的pcl纺丝液。
84.s2:纳米纤维纱线的制备:如图1所示,将pla线2(直径50-100μm;上海同杰良生物材料有限公司)穿过多功能静电纺纱机的中间旋转漏斗1中,作为芯层,将s1中10ml纺丝液转移至多功能静电纺纱机的两个对喷注射器4中,注射器4置于推进泵5上,两个对喷注射器纺丝头3分别施加正负高压电源8,启动多功能静电纺纱机,两个对喷注射器喷头3喷出纳米纤维6,利用旋转漏斗1将纳米纤维6加捻到丝素蛋白线中,接收辊9收集,得到纳米纤维纱线7。纺丝参数如下:直流高压8kv,推进速度1.2ml/h,接收距离12cm,旋转漏斗转速400转/分钟,接收辊8转/分钟。
85.s3:韧带段支架的制备:将8根s2中得到的纳米纤维纱线通过手工编织(经线和纬线交织形成平纹结构)的方式制成韧带段支架。
86.s4:称量1.0g plga(购于济南岱罡生物科技有限公司)溶于10ml四氢呋喃溶剂(购于国药集团化学试剂有限公司)中,配制0.1g/ml的plga相分离溶液;称量0.1g二氧化硅加入plga相分离溶液中,充分搅拌、超声混匀。
87.s5:将s3中所述的编织支架两端分别置于模具(圆柱形,直径为5mm,高为20mm)内部,然后向模具中加入s6中的0.5ml相分离溶液,迅速置于-80℃条件下冻存48小时,后置于冷冻干燥机中冻干得到骨-韧带-骨一体化支架。
88.中国专利cn110037830b公开了一种仿生全成型三相结构人工韧带及其制备方法,三相结构即两段端部骨隧道编织段和关节腔纤维束段。本发明与该专利区别在于:(1)该专利支架的两端骨隧道段为编织方式制备,中间关节腔段为纤维束。而本发明的人工支架的两端骨隧道段的制备方法为相分离技术,中间关节腔段制备方法为静电纺丝技术结合编织
工艺。两者的制备方法完全不同。
89.(2)该专利支架的两端骨隧道段为管状编织物结构,中间关节腔段为不编织的平行纤维束结构。而本发明的人工支架的两端骨隧道段为圆柱形三维多孔结构,中间关节腔段为纳米纤维纱线编织结构。两者的结构完全不同。
90.虽然本发明公开披露如上,但本发明公开的保护范围并非仅限于此。本领域技术人员,在不脱离本公开的精神和范围的前提下,可进行各种变更与修改,这些变更与修改均将落入本发明的保护范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。