一种基于vhl配体的微管蛋白降解剂及其应用
技术领域
1.本发明涉及一种微管蛋白降解剂,尤其涉及一种基于偶氮类化合物光致异构性能的微管蛋白降解剂,及其药学上可用的盐、其合成方法及其在选择性降解微管蛋白的药物中的应用。
背景技术:
2.微管(microtubule)是由α、β两种类型的微管蛋白形成的二聚体,在细胞内呈网状或束状分布,参与细胞骨架的构成、细胞形态的维持、细胞收缩、细胞内物质运输以及细胞分裂等。因此,通过抑制细胞分裂过程中微管蛋白聚合成微管,或者抑制微管解聚为微管蛋白,必将造成有丝分裂无法进行或停滞,细胞有丝分裂过程的中断必将对细胞产生更大的影响,使其生长受到抑制,最终诱导细胞调亡的发生,从而达到抑制细胞增值生长的目的。鉴于癌细胞与正常细胞最大的区别在于癌细胞的有丝分裂异常频繁而且不受控制,因此,阻断微管蛋白的合成对恶性肿瘤的治疗尤其具有重要意义,也广泛用于抗真菌、驱虫等。
3.康普瑞汀(风车子抑素,combretastatin a4,ca4)取自南非灌木非洲风车子(combretum caffrum)。ca4具有的顺式二苯乙烯结构可以在体内靶向微管蛋白,抑制其聚合,并进一步破坏肿瘤血管,从而起到抗肿瘤作用。ca4在多种肿瘤模型上都有效,是个很有前景的抗肿瘤药物,然而ca4的水溶性极差,只有11.8μg/ml,使其口服生物利用度较低;同时,其二苯乙烯母核易变构为反式而导致活性消失的特点亦限制了其临床应用价值。为了克服ca4的缺陷,科研人员对其进行了广泛的构效关系研究,开发了其水溶性磷酸盐前药ca4p,目前已在ⅲ期临床试验。
4.然而,目前包括ca4在内的微管蛋白抑制剂都是非特异性的,其生物活性不能在限定在特定肿瘤部位,对正常细胞和健康细胞也有毒性。这种非特异性会在癌症的治疗中引起严重的全身性副作用,例如心脏毒性和神经毒性,这大大限制了此类抑制剂的用药剂量和用药途径;同时,获得性耐药的产生,也极大地削弱了它们的临床治疗价值。
5.为了增强其靶向性,鉴于ca4的二苯乙烯核心结构以及其顺反异构体的活性变化,偶氮苯光开关是一个很好的修饰途径。偶氮苯类化合物含有特殊共轭π化学结构,因而具有光致异构性能,即:可在特殊波段的光照射后,反式异构体与顺式异构体可以相互转化。2015年国际顶尖杂志《cell》报道borowjak等用偶氮苯代替ca4中的二苯乙烯片段(即将c=c替换为n=n键),合成了几个ca4的偶氮化衍生物psts(borowjak et al 2015.cell 162,403-411)。研究发现:由于偶氮类化合物具有独特的光致异构性能,黑暗下或正常日常照射情况下,psts以无活性的反式异构体(trans-)状态存在;而在一定波长的光照射下,无活性的反式异构体可以很快地转化为具有生物活性的顺式异构体(cis-),靶向微管蛋白,抑制其聚合,能够实现有针对性的单细胞死亡。
6.这种ca4的偶氮化衍生物,可以在体内无毒运输,并在靶部位激活,从而在一定程度上解决了微管蛋白抑制剂存在的靶向性问题。但由于其仍然是对微管蛋白的抑制而发挥药理作用,需要一定的剂量结合并长期占据在微管蛋白的活性位点以抑制其活性,故而仍
不能解决微管蛋白抑制剂所固有的获得性耐药性缺陷。
技术实现要素:
7.本发明的目的是针对现有技术的不足,提供一种基于vhl配体的微管蛋白降解剂,及其药学上可用的盐及其在选择性降解微管蛋白的药物中的应用。
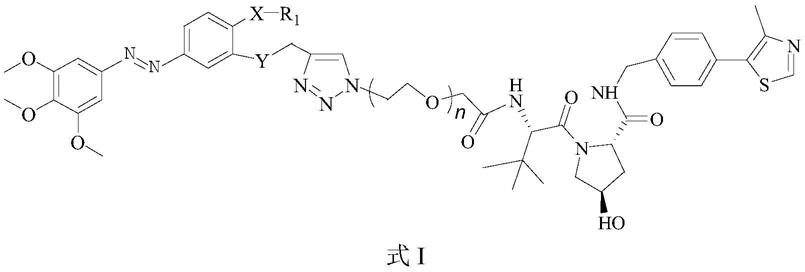
8.本发明的目的是通过以下技术方案来实现的:一种降解微管蛋白的偶氮类化合物,具有如下结构:
9.liganda-linker-ligandb
10.其中:liganda为偶氮苯类小分子,其具有如下结构:
[0011][0012]
其中,r1、r2独立地选自氢、c1-c12烷基、c1-c12羰基、c1-c12烯基、c1-c12卤代烷基、c1-c12氧杂烷基、c1-c12氮杂烷基、芳基、取代芳基;
[0013]
r3、r4、r5、r6、r7、r8、r9、r
10
独立地选自氢、羟基、胺基、卤素、c1-c12烯基、c1-c12烷基、c1-c12卤代烷基、c1-c12氧杂烷基、c1-c12氮杂烷基、酮(酰)基、芳基、取代芳基;
[0014]
x、y独立地为氢、氧、硫或氮;
[0015]
r1或r2位置可以独立连接linker。
[0016]
linker是连接链,包含非线性链、脂肪族链、芳香链、杂芳环结构链,通过共价键与liganda和ligandb相连,部分连接链结构如下通式所示:
[0017][0018]
其中:
[0019]
n选自0-30之间的整数。
[0020]
ligandb是可以招募泛素e3连接酶的配体,包括但不限于von hippel-lindau(vhl),cereblon(crbn),murine double mimute 2(mdm2)和cellular inhibitors of apoptosis proteins 1(ciap1)的配体,其相应的配体结构举例如下:
[0021][0022]
其中x为ch2或c=o,y独立地为氧或氮,式中r为连接linker位置。
[0023]
进一步地,所述liganda化合物选自以下结构:
[0024]
r1、r2独立地选自氢、羰基、乙酰基、丙酰基、丁酰基、苯甲酰基、取代苯甲酰基、苄基、取代苄基、苯基、取代苯基、甲基、乙基、丙基、丁基、三氟甲基;
[0025]
r3、r4、r5、r6、r7、r8、r9、r10独立地选自氢、羟基、胺基、卤素、甲基、乙基、丙基、丁基、三氟甲基、甲氧基、乙氧基、丙氧基、芳基、取代芳基;
[0026]
x、y独立地为氧、硫或氮;
[0027]
r1或r2独立地与linker连接;
[0028]
所述ligandb选自vhl配体:
[0029][0030]
n选自1-15之间的整数。
[0031]
更进一步地,本发明所述的一种基于vhl配体的微管蛋白降解剂,选自如下结构:
[0032][0033]
其中,r1选自氢、乙酰基、丙酰基、丁酰基、苯甲酰基、取代苯甲酰基、苄基、取代苄基、苯基、取代苯基、甲基、乙基、丙基、丁基、三氟甲基;
[0034]
x、y独立地为氧、硫或氮;
[0035]
n选自0-15之间的整数。
[0036]
更进一步地,本发明所述的一种基于vhl配体的微管蛋白降解剂,选自以下结构:
[0037]
r1选自氢、甲基、乙基、丙基、丁基、三氟甲基;
[0038]
x、y独立地为氧或氮;
[0039]
n选自1-15之间的整数。
[0040]
更进一步地,本发明所述的一种基于vhl配体的微管蛋白降解剂,为以下结构的化合物:
[0041][0042]
n选自1-6之间的整数。
[0043]
本发明同时提供一种基于vhl配体的微管蛋白降解剂的制备方法,具体为:首先根据文献方法制得或购得liganda化合物及ligandb化合物,并根据r1、r2取代基的不同,用不同的化学反应与lingker连接。举例如下:
[0044][0045]
本发明所述的一种基于vhl配体的微管蛋白降解剂可以单独使用,也可以用常规的方法制备成药学上可接受的盐使用,所述药学上可接受的盐为盐酸盐、氢溴酸盐、氢碘酸盐、硫酸盐、硫酸氢盐、磷酸盐、乙酸盐、丙酸盐、丁酸盐、草酸盐、酒石酸盐、甲磺酸盐、对甲苯磺酸盐、富马酸盐、牛磺酸盐、柠檬酸盐、琥珀酸盐,或其混合盐。
[0046]
本发明还提供了一种基于vhl配体的微管蛋白降解剂及其在药学上可接受的盐在药学上的应用,该应用具体为:用于制备预防或治疗因微管蛋白表达过多所引起的疾病的药物制剂,所述的因微管蛋白表达过多所引起的疾病为肿瘤如乳腺癌、白血病、皮肤癌、子宫颈癌、食管癌、肺癌、胶质瘤等,还包括神经退行性疾病如阿尔茨海默症、肌萎缩性脊髓侧索硬化症、白内障、帕金森氏病、克-雅二氏病、亨廷顿氏病,还包括其它疾病如急性痛风、关节疼痛、家族性地中海热、肝硬化等。优选地,所述的疾病为乳腺癌、白血病、皮肤癌、子宫颈癌、食管癌、肺癌、胶质瘤等,还包括急性痛风、关节疼痛、家族性地中海热、肝硬化。
[0047]
与现有技术相比,本发明具有如下有益效果:
[0048]
基于近年来发展迅速的protac(proteolysis-targeting chimaeras,蛋白裂解靶向嵌合体)技术,本发明以蛋白降解的形式来解决获得性耐药问题:本发明提供的一种基于vhl配体的微管蛋白降解剂及其药学上可用的盐不需要像微管蛋白抑制剂那样长期占据活性位点,而只需要与微管蛋白短暂的结合即能够诱发蛋白降解效果,由于蛋白被降解后需要重新合成才能恢复功能,这就极大地推迟了抗药性的产生;对那些已经产生抗药性的蛋
白也仍然有效。因此,本发明提供的一种基于vhl配体的微管蛋白降解剂及其药学上可用的盐可能在制备预防或治疗因微管蛋白表达过多所引起的疾病的药物中有所应用。
附图说明:
[0049]
图1.buazo-peg1-vhl的质谱图;
[0050]
图2.buazo-peg2-vhl的质谱图;
[0051]
图3.buazo-peg4-vhl的质谱图;
[0052]
图4.buazo-peg1-vhl化合物的微管蛋白降解效果图。
具体实施方式
[0053]
下面结合实施例对本发明的结构、制备方法及在制备预防或治疗因微管蛋白表达过多所引起的疾病的药物制剂方面的应用作进一步阐述,但不限制本发明。
[0054]
以下实施例中,如无特别说明,出现的百分数均为质量百分数。
[0055]
样品的分析数据由以下仪器测定:
[0056]
温度计未经校正;bruker drx400核磁共振仪;安捷伦5975型质谱仪;bruker vector22红外光谱仪。
[0057]
实施例1 azo-h的合成
[0058][0059]
选取100ml三颈烧瓶,加入磁力转子,上装温度计和恒压滴液漏斗,置于磁力搅拌器上。称量3,4,5-三甲氧基苯胺1.83g(10mmol),加入95%乙醇溶液5ml,用-20℃的丙三醇冷却至-10℃,打开磁力搅拌器,搅拌溶解,反应液呈亮黄色。
[0060]
量取37%浓盐酸2ml,逐滴加入上述反应液中,滴加期间定期更换冷却液,保证反应液温度低于0℃,反应液转变为米黄色浑浊液体。
[0061]
称量亚硝酸钠1.39g(20mmol),配制成5ml水溶液,同样置于冷却液中冷却。盐酸滴加完毕后,逐滴滴加亚硝酸钠溶液,滴加期间同样注意温度,保证反应温度一直低于0℃。滴加完毕后,溶液呈现橙黄色。继续搅拌反应1h,同时维持反应液温度低于0℃。
[0062]
称取氢氧化钠8g,溶于50ml水中,配制成氢氧化钠溶液。
[0063]
称量邻炔丙氧基苯酚(9mmol),加入之前配制的氢氧化钠溶液5ml,溶解后用冷却液冷却至-10℃。
[0064]
将上述溶液逐滴滴加入重氮化反应液中,滴毕,调节ph值最终至7。移去冷却液,在室温下搅拌反应2h。分液,乙酸乙酯萃取后浓缩,产物为棕黄色固体。1h-nmr(cdcl3,ppm):7.20(s,2h,ph),6.55(d,2h,ph),3.95(s,6h,och3),3.94(s,3h,och3).
13
c-nmr(cdcl3,ppm):158.7,158.6,156.1,153.4,149.2,140.4,100.5,61.1,56.2.
[0065]
实施例2 azo-me的合成
[0066][0067]
实施例1制得的azo-h 0.55g,碳酸钾0.3g及过量的碘甲烷加至2ml dmf中,室温下搅拌反应过夜。反应毕,加水并用乙酸乙酯萃取后,得棕黄色固体。1h-nmr(cdcl3,ppm):7.66(1h,dd,ph),7.63(1h,d,ph),7.23(2h,s,ph),7.02(1h,d,ch),4.87(2h,f,ch2),3.97(9h,s,3
×
och3),3.93(3h,s,och3).
[0068]
实施例3 azo-pr的合成
[0069][0070]
按实施例2所述的方法,用溴丙烷代替碘甲烷,得azo-pr。ms(esi)m/z:[m h]
=384.
[0071]
实施例4 azo-bu的合成
[0072][0073]
如实施例2所述的方法,用溴丁烷代替碘甲烷,得棕黄色固体。1hnmr(400mhz,cdcl3)δ7.56(td,j=4.6,2.2hz,1h),7.15(s,1h),6.94(d,j=9.2hz,1h),4.78(d,j=2.4hz,1h),4.05(t,j=6.6hz,1h),3.90(s,3h),3.86(s,1h),3.50(t,j=6.7hz,1h),2.47(t,j=2.4hz,1h),1.89
–
1.73(m,2h),1.50(s,2h).ms(esi)m/z:[m h]
=398.
[0074]
实施例5 buazo-peg1-vhl的合成
[0075][0076]
在三颈烧瓶中加入实施例4获得到的azo-bu化合物119.4mg(0.3mmol),再加入市售n3-peg1-vhl化合物167.1mg(0.3mmol),加入四氢呋喃15ml溶解,加入硫酸铜4.8mg和抗坏血酸钠16mg,氮气氛围于室温搅拌反应16h。全程用tlc(ea:etoh=50:3)监测直到反应结束。反应液用ea萃取(2
×
25ml),饱和食盐水洗涤有机相,分液,收集合并乙酸乙酯层,无水硫酸钠干燥过夜。过滤,减压干燥得粗产品。柱层析(ea:etoh=50:3)分离,溶剂减压浓缩至干得到产物buazo-peg1-vhl。ms:found:[m h]
=956.4,[m na]
=979.4,cal:c48h61n9o10s=956.117。质谱图见附图1。
[0077]
实施例6 buazo-peg2-vhl的合成
[0078][0079]
按实施例5相同的方法,用市售n3-peg2-vhl化合物为原料,进行点击化学反应,得到产物buazo-peg2-vhl。ms:found:[m h]
=1000.4,[m na]
=1023.4,cal:c50h65n9o11s=1000.17。质谱图见附图2。
[0080]
实施例7 buazo-peg4-vhl的合成
[0081][0082]
按实施例5相同的方法,用市售n3-peg4-vhl化合物为原料,进行点击化学反应,得到产物buazo-peg4-vhl。ms:found:[m na]
=1110.4,cal:c54h73n9o13s=1087.5。质谱图见附图3。
[0083]
实施例8 buazo-peg2-vhl盐酸盐的制备
[0084]
如权利要求9所合成的buazo-peg2-vhl 46mg加至丙酮中溶解,搅拌下慢慢通入干燥的hcl气体至过饱和。置冰水浴中析出白色晶体,为其盐酸盐,收率70%。
[0085]
实施例9小分子化合物光致异构性能研究(以实施例4的产物为例)
[0086]
取7.96mg目标产物放置于10ml的容量瓶a中,色谱甲醇溶解,定容。另取100μl容量瓶a的溶液,放置于10ml容量瓶b中,色谱甲醇定容。配制完毕后取容量瓶b的溶解1ml分别置于6个不同的ep管中,并编号。将配制好的ep管放置于薄层色谱扫描仪中使用红光(620-630nm)照射,并于15min,30min,1h,2h,4h,8h取出其中一管放置于lc-ms中查看顺式与反式结构(顺式极性大,出峰早)比例变化。
[0087]
操作同上,改变波长,分别用黄光(580-585nm),绿光(520-530nm),蓝光(450-470nm),紫光(405nm),紫光395nm对样品进行15min,30min,1h,2h,4h,8h的光照,并记录数据。结果见表1。
[0088]
表1.不同波长光照下顺反异构体的含量(%)
[0089][0090]
可见,在红光(620-630nm)、黄光(580-585nm)、绿光(520-530nm)、蓝光(450-470nm)四种波长的照射下,无法明显引起这两种偶氮苯类化合物顺式和反式结构的互变。而395nm和405nm的紫光可会明显引起这两种偶氮苯类化合物的结构互变。
[0091]
实施例10小分子化合物的抗增殖活性:
[0092]
在标准细胞培养条件下,将hela细胞(作为人类宫颈腺癌的模型)和mcf-7细胞(乳腺癌的模型)维持在补充有10%fbs的dmem/f12培养基中。将每孔3,000个细胞接种到两组96孔板中,并将细胞与一系列单独的化合物的稀释液重复三次,孵育四天。在四天的化合物处理过程中,一组细胞在黑暗中生长,而另一组细胞在脉冲紫外线下生长(390-400nm,每0.5h照射10秒)。在化合物处理结束时,将3-(4,5-二甲基硫唑-2-基)-2,5-二苯基溴化四唑(mtt)试剂添加到每个孔中,并在37℃与细胞温育1小时。然后使用dmso溶解在每个96孔中形成的晶体。使用biotek synergy h4(biotek instruments,winooski,vt)在波长570nm和630nm处测量光密度值,并使用这两个光密度值的差异来分析每个96孔中的相对细胞存活率。ic
50
值是通过graphpad prism软件使用s型剂量响应图来计算的。
[0093]
结果如表2所示:
[0094]
表2.在黑暗/紫外线(395nm)下的ic
50
值(mtt法测定)
[0095]
fluoride,and 10mm tris-hcl;ph 7.4)冰上裂解30min,4℃12000rpm离心15分钟,取上清液蛋白定量后进行sds-page;电泳结束后样品电转至硝酸纤维素膜,然后进行免疫反应,依次进行室温封闭1小时,4℃egfr一抗孵育过夜,室温二抗孵育2小时,tbst洗膜2小时,加ecl溶液,准确温浴1分钟;将膜沥干后置暗盒中曝光数分钟,显影,定影;x光片用扫描仪扫描后metamorph软件读取条带灰度值,以gapdh为内参进行统计分析。
[0101]
结果见附图4。
[0102]
可见,本发明实施例5的产物buazo-peg1-vhl在不同浓度下能显示出对微管蛋白的降解活性,且呈现较好的剂量依赖性。鉴于该类化合物是基于protac原理设计,其它不同链长的化合物也能显示出对微管蛋白的降解活性。
[0103]
本发明提供的一种基于vhl配体的微管蛋白降解剂在黑暗环境中不显示药理活性,但因其特有的光致异构性能,在特定波长的光照下对微管蛋白显示出亲合性,并进一步促使微管蛋白降解,这可能在制备预防或治疗因微管蛋白过度增长而引起的疾病的药物中有所应用,包括肿瘤如乳腺癌、白血病、皮肤癌、子宫颈癌、食管癌、肺癌、胶质瘤等,还包括神经退行性疾病如阿尔茨海默症、肌萎缩性脊髓侧索硬化症、白内障、帕金森氏病、克-雅二氏病、亨廷顿氏病,还包括其它疾病如急性痛风、关节疼痛、家族性地中海热、肝硬化等。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。