包含阿普斯特和tyk2抑制剂的联合疗法
背景技术:
1.n-[2-[(1s)-1-(3-乙氧基-4-甲氧基苯基)-2-(甲基磺酰基)乙基]-2,3-二氢-1,3-二氧代-1h-异吲哚-4-基]乙酰胺(阿普斯特),商品名为其是一种4型磷酸二酯酶(pde4)抑制剂,目前已被批准用于治疗中度至重度斑块状银屑病和活动性银屑病关节炎。阿普斯特对pde4的抑制提高了免疫细胞中的环腺苷一磷酸(camp)水平。这反过来又通过减少促炎性介质如tnf-α、il-23、il-17和其他炎症细胞因子的表达来下调炎症应答,并增加抗炎介质的产生。研究表明,一些患者的斑块状银屑病可在短短4个月多一点的治疗中减少75%。
[0002]
酪氨酸激酶2(tyk2)是一种胞内信号转导酶,可激活信号转导和转录激活因子(stat)依赖的基因表达以及il-12、il-23和i型和iii型干扰素受体的功能性应答。除了其他病况以外,酪氨酸激酶抑制剂(tki)最近作为治疗银屑病和相关病况的有效药剂而受到关注。例如,tki抑制剂bms-986165最近在中度至重度斑块状银屑病受试者中的2期临床试验中显示出阳性结果。参见kim papp,m.d.,phase 2 trial of selective tyrosine kinase 2 inhibition in psoriasis,the new england journal of medicine,sept.12,2018。
技术实现要素:
[0003]
现在已经发现,阿普斯特与tyk2抑制剂6-(环丙烷甲酰胺)-4-((2-甲氧基-3-(1-甲基-1h-1,2,4-三唑-3-基)苯基)氨基)-n-(甲基-d3)哒嗪-3-甲酰胺(bms-986165)的组合在刺激th17细胞的条件下协同降全血测定中表达的促炎性细胞因子。例如,与单独使用每种药物相比,使用0.01μm bms-986165和1μm阿普斯特的组合对il-17f表达的抑制增加2倍以上。参见例如,在示例部分中的表5。在0.1μm浓度的bms-986165和1μm阿普斯特下观察到类似结果。参见例如,表5。bms-986165与1μm阿普斯特的组合也降低il-17a和il-22的细胞因子表达,其值是单独使用每种药物的2倍或更多。参见例如,表5。
[0004]
还发现阿普斯特与bms-986165的组合激发针对某些促炎性细胞因子的互补作用(complementary effect)。例如,bms-986165在全血测定中增加tnf-α和gm-csf细胞因子,而阿普斯特抑制这些细胞因子的产生。参见例如,表5中针对tnf-α的1μm阿普斯特占对照的百分比为10.7%,而0.01μm bms-986165占对照的百分比为143.1%。然而,当组合施用时,阿普斯特纠正了bms-986165的缺陷,从而产生了针对tnf-α的13.5%抑制的互补作用。参见例如,表5。这种趋势也在0.1μm浓度下的bms-986165和针对细胞因子cm-csf建立。参见例如,表5。这些结果说明了bms-986165和阿普斯特的协同和补充药理作用。
[0005]
除了全血测定,在lps刺激的pbmc中bms-986165和阿普斯特的组合也激发针对某些促炎性细胞因子的互补作用。bms-986165增加il-23、il-12和tnf-α,而阿普斯特抑制这些细胞因子的产生。参见例如,在示例部分中的表6。这些结果进一步支持了bms-986165与阿普斯特组合在治疗th17相关疾病中的优势。
[0006]
因此,本文提供了使用有效量的阿普斯特或其药学上可接受的盐以及有效量的
tyk2抑制剂(如bms-986165)在受试者中治疗对pde4的抑制具有应答的疾病或病症的方法。此类疾病和病症包括例如炎性疾病,如银屑病、银屑病关节炎和溃疡性结肠炎。
[0007]
本文还提供了药物组合物,其包含有效量的阿普斯特或其药学上可接受的盐和有效量的tyk2抑制剂(如bms-986165)。
附图说明
[0008]
图1显示了在抗cd3/抗cd28(th0)或抗cd3/抗cd28、il-1β、il-6和il-23(th17)刺激的全血中由阿普斯特和bms-986165产生的白介素-17a(il-17a)细胞因子(占对照的百分比)-管测定。
[0009]
图2显示了在抗cd3/抗cd28(th0)或抗cd3/抗cd28、il-1β、il-6和il-23(th17)刺激的全血中由阿普斯特和bms-986165产生的白介素-17a(il-17a)细胞因子-管测定。
[0010]
图3显示了在抗cd3/抗cd28(th0)或抗cd3/抗cd28、il-1β、il-6和il-23(th17)刺激的全血中由阿普斯特和bms-986165产生的白介素-17f(il-17f)细胞因子(占对照的百分比)-管测定。
[0011]
图4显示了在抗cd3/抗cd28(th0)或抗cd3/抗cd28、il-1β、il-6和il-23(th17)刺激的全血中由阿普斯特和bms-986165产生的白介素-17f(il-17f)细胞因子-管测定。
[0012]
图5显示了在抗cd3/抗cd28(th0)或抗cd3/抗cd28、il-1β、il-6和il-23(th17)刺激的全血中由阿普斯特和bms-986165产生的白介素-22(il-22)细胞因子(占对照的百分比)-管测定。
[0013]
图6显示了在抗cd3/抗cd28(th0)或抗cd3/抗cd28、il-1β、il-6和il-23(th17)刺激的全血中由阿普斯特和bms-986165产生的白介素-22(il-22)细胞因子-管测定。
[0014]
图7显示了在抗cd3/抗cd28(th0)或抗cd3/抗cd28、il-1β、il-6和il-23(th17)刺激的全血中由阿普斯特和bms-986165产生的肿瘤坏死因子α(tnf-α)细胞因子(占对照的百分比)-管测定。
[0015]
图8显示了在抗cd3/抗cd28(th0)或抗cd3/抗cd28、il-1β、il-6和il-23(th17)刺激的全血中由阿普斯特和bms-986165产生的肿瘤坏死因子α(tnf-α)细胞因子-管测定。
[0016]
图9显示了在抗cd3/抗cd28(th0)或抗cd3/抗cd28、il-1β、il-6和il-23(th17)刺激的全血中由阿普斯特和bms-986165产生的粒细胞-巨噬细胞集落刺激因子(gm-csf)细胞因子(占对照的百分比)-管测定。
[0017]
图10显示了在抗cd3/抗cd28(th0)或抗cd3/抗cd28、il-1β、il-6和il-23(th17)刺激的全血中由阿普斯特和bms-986165产生的粒细胞-巨噬细胞集落刺激因子(gm-csf)细胞因子-管测定。
[0018]
图11显示了在脂多糖(lps)刺激的外周血单核细胞(pbmc)中由阿普斯特产生的白
介素-23(il-23)细胞因子。
[0019]
图12显示了在lps刺激的pbmc中由阿普斯特和tyk2i(bms-986165)产生的白介素-23(il-23)细胞因子。
[0020]
图13显示了在lps刺激的pbmc中由阿普斯特和tyk2i(bms-986165)产生的白介素-12p40(il-12p40)细胞因子。
[0021]
图14显示了在lps刺激的pbmc中由阿普斯特和tyk2i(bms-986165)产生的白介素-12p70(il-12p70)细胞因子。
[0022]
图15显示了在lps刺激的pbmc中由阿普斯特和tyk2i(bms-986165)产生的肿瘤坏死因子α(tnf-α)细胞因子。
[0023]
图16显示了在lps刺激的pbmc中由阿普斯特和tyk2i(bms-986165)产生的白介素γ(ifn-γ)细胞因子。
[0024]
图17显示了在lps刺激的pbmc中由阿普斯特和tyk2i(bms-986165)产生的单核细胞趋化蛋白-1(mcp-1)细胞因子。
[0025]
发明详述
[0026]
在第一个实施方式中,本文提供了用于治疗对环核苷酸磷酸二酯酶同工酶iv(pde4)的抑制具有应答的疾病或病况的方法,所述方法包括向受试者施用有效量的n-[2-[(1s)-1-(3-乙氧基-4-甲氧基苯基)-2-(甲基磺酰基)乙基]-2,3-二氢-1,3-二氧代-1h-异吲哚-4-基]乙酰胺(阿普斯特)或其药学上可接受的盐和有效量的tyk2抑制剂。
[0027]
或者,作为第一个实施方式的一部分,提供了有效量的n-[2-[(1s)-1-(3-乙氧基-4-甲氧基苯基)-2-(甲基磺酰基)乙基]-2,3-二氢-1,3-二氧代-1h-异吲哚-4-基]乙酰胺(阿普斯特)或其药学上可接受的盐和有效量的tyk2抑制剂在制备用于治疗对环核苷酸磷酸二酯酶同工酶iv(pde4)的抑制具有应答的疾病或病况的药物中的用途。
[0028]
在另一个替代方案中,作为第一个实施方式的一部分,提供了有效量的n-[2-[(1s)-1-(3-乙氧基-4-甲氧基苯基)-2-(甲基磺酰基)乙基]-2,3-二氢-1,3-二氧代-1h-异吲哚-4-基]乙酰胺(阿普斯特)或其药学上可接受的盐和有效量的tyk2抑制剂用于治疗对环核苷酸磷酸二酯酶同工酶iv(pde4)的抑制具有应答的疾病或病况的用途。
[0029]
1.定义
[0030]
在美国专利号6,962,940中公开了n-[2-[(1s)-1-(3-乙氧基-4-甲氧基苯基)-2-(甲基磺酰基)乙基]-2,3-二氢-1,3-二氧代-1h-异吲哚-4-基]乙酰胺(阿普斯特),其内容通过引用并入本文,并且指具有以下化学结构的化合物:
[0031][0032]
阿普斯特在化学结构和名称中具有指定为(s)的手性中心。如本文所用,该名称表
示阿普司特作为(s)对映体在该位置的光学富集量相对于相应的(r)对映体至少为80%、90%、95%、98%、99%或99.9%。因此,当阿普斯特在本文中被称为以特定量的立体异构或对映异构纯时,这意味着(s)对应异构体以该量富集。例如,立体异构纯度至少为95%的n-[2-[(1s)-1-(3-乙氧基-4-甲氧基苯基)-2-(甲基磺酰基)乙基]-2,3-二氢-1,3-二氧代-1h-异吲哚-4-基]乙酰胺指所述化合物含有大于或等于95%的(s)对应异构体和5%或更少的(r)对应异构体。
[0033]
除非另有说明,否则本文所述的施用包括在施用本文所述的tyk2抑制剂之前、同时或之后施用阿普斯特。因此,出于治疗目的,不需要同时施用。在一个方面中,阿普斯特和公开的tyk2抑制剂一起施用。在另一个方面中,阿普斯特和公开的tyk2抑制剂在同一天的不同时间施用。在另一个方面中,阿普斯特和公开的tyk2抑制剂作为单独的片剂或胶囊在不同时间施用。在另一个方面中,阿普斯特和公开的tyk2抑制剂在同一片剂或胶囊中以固定剂量的组合施用。
[0034]
如本文所述,术语“治疗(treatment)”、“治疗(treat)”和“治疗(treating)”指逆转、减轻或抑制对pde4的抑制具有应答的疾病或病症的进展,或者其一种或多种症状。
[0035]
术语“受试者”指动物,如哺乳动物,和如人。术语“受试者”和“患者”可以互换使用。
[0036]
术语“有效量”或“治疗有效量”是指将引起受试者的生物学或医学应答的本文所述化合物的量,例如,0.001-100mg/kg体重/天之间的剂量。
[0037]
术语“药学上可接受的载体”指无毒载体、佐剂或载剂,其不会不利地影响与其一起配制的化合物的药理活性,并且对于人类使用也是安全的。可用于本文公开的组合物中的药学上可接受的载体、佐剂或载剂包括但不限于离子交换剂、氧化铝、硬脂酸铝、硬脂酸镁、卵磷脂、血清蛋白,如人血清白蛋白、缓冲物质,如磷酸盐、甘氨酸、山梨酸、山梨酸钾、饱和植物脂肪酸的偏甘油酯混合物、水、盐或电解质,如硫酸鱼精蛋白、磷酸氢二钠、磷酸氢钾、氯化钠、锌盐、胶体二氧化硅、三硅酸镁、聚乙烯吡咯烷酮、纤维素类物质(例如,微晶纤维素、羟丙基甲基纤维素、乳糖一水合物、月桂基硫酸钠和交联羧甲基纤维素钠)、聚乙二醇、羧甲基纤维素钠、聚丙烯酸酯、蜡、聚乙烯-聚氧丙烯-嵌段聚合物、聚乙二醇和羊毛脂。
[0038]
术语“药学上可接受的盐”指由药学上可接受的无毒酸或碱制备的盐,包括无机酸和碱以及有机酸和碱。用于本文所述的化合物的适宜的药学上可接受的碱加成盐包括但不限于包括由铝、钙、锂、镁、钾、钠和锌制成的金属盐,或者由赖氨酸、n,n'-二苄基乙二胺、氯普鲁卡因、胆碱、二乙醇胺、乙二胺、葡甲胺(n-甲基葡糖胺)和普鲁卡因制成的有机盐。适宜的无毒酸包括但不限于无机和有机酸,如乙酸、藻酸、邻氨基苯甲酸、苯磺酸、苯甲酸、樟脑磺酸、柠檬酸、乙烯磺酸、甲酸、富马酸、糠酸、半乳糖醛酸、葡糖酸、葡糖醛酸、谷氨酸、乙醇酸、氢溴酸、盐酸、羟乙磺酸、乳酸、马来酸、苹果酸、扁桃酸、甲磺酸、粘酸、硝酸、扑酸、泛酸、苯乙酸、磷酸、丙酸、水杨酸、硬脂酸、琥珀酸、对苯磺酸、硫酸、酒石酸和对甲苯磺酸。
[0039]“晶体”指化合物的固体形式,其中在原子的位置中存在长程原子序。例如,固态的结晶性质可以通过检查x-射线粉末衍射图来确认。“单晶型”指所述化合物(即,n-[2-[(1s)-1-(3-乙氧基-4-甲氧基苯基)-2-(甲基磺酰基)乙基]-2,3-二氢-1,3-二氧代-1h-异吲哚-4-基]乙酰胺)作为单晶或多个晶体存在,其中每个晶体具有相同的晶型(即,晶型b)。当晶型被定义为化合物的一种特定单晶型的特定百分比时,其余部分由非晶型和/或不同
于所指定的一种或多种特定晶型的晶型组成。在一个方面中,例如,所公开的晶型是以重量计至少80%的单晶型、至少90%的单晶型、至少95%的单晶型或至少99%的单晶型。特定晶型的重量百分比由特定晶型的重量除以特定晶体的总重量加上存在的其他晶体形式的重量加上存在的无定形形式的重量,乘以100%。
[0040]
术语“无定形”指以非结晶状态或形式存在的固体。无定形固体是分子的无序排列,因此没有可区分的晶格或晶胞,因而没有可定义的长程排序。固态的固态排序可以通过本领域公知的标准技术来确定,例如,通过x-射线粉末衍射(xrpd)或差示扫描量热法(dsc)。无定形固体也可以与结晶固体区分开来,例如,通过使用偏振光显微镜的双折射。
[0041]
本文所述的晶型的x射线粉末衍射图的2-θ值可能从一个仪器到另一个仪器会略有改变,以及由于温度变化、样品替代和内标存在与否等因素导致的样品制备和批次间的差异。因此,除非另有定义,否则本文所述的xrpd图样/归属不应被解释为绝对的并且可以变化
±
0.2度。本领域众所周知,这种可变性将解释上述因素,而不会妨碍对晶型的明确鉴定。
[0042]
2.tyk2抑制剂
[0043]
在所公开的方法和组合物中使用的tyk2抑制剂包括阻断酪氨酸激酶2作用的化合物,酪氨酸激酶2是由tyk2基因编码的非受体酪氨酸蛋白激酶。
[0044]
在第二个实施方式中,所公开的tyk2抑制剂包括但不限于在xingrui he等,expert opinion on therapeutics patents 2019,vol.29,no.2,137-149中描述的那些,其全部内容通过引用并入本文。
[0045]
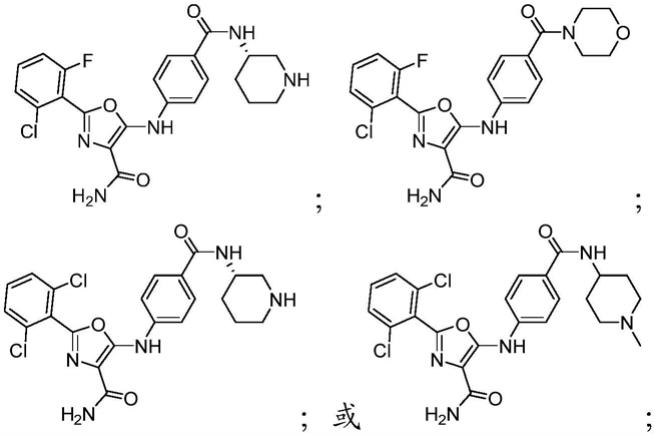
在第三个实施方式中,所公开的tyk2抑制剂可以选自具有下式的那些:
[0046][0047]
或其药学上可接受的盐,其中变量如在wo 2015/032423中所描述的,其全部内容通过引用并入本文。作为第三个实施方式的一部分的具有该式的示例性化合物包括但不限于具有下式的那些:
[0048][0049]
或其药学上可接受的盐。作为第三个实施方式的一部分的其他tyk2抑制剂包括在wo 2008/139161和wo 2010/055304中的那些,其各自的全部内容通过引用并入本文。
[0050]
在第四个实施方式中,所公开的tyk2抑制剂可以选自具有下式的那些:
[0051][0052]
或其药学上可接受的盐,其中变量如在wo 2013/174895中所描述的,其全部内容通过引用并入本文。作为第四个实施方式的一部分的具有该式的示例性化合物包括但不限于具有下式的那些:
[0053][0054]
或其药学上可接受的盐。其他tyk2抑制剂包括在wo 2012/062704中的那些,其全部内容通过引用并入本文。
[0055]
在第五个实施方式中,所公开的tyk2抑制剂可以选自具有下式的那些:
[0056][0057]
或其药学上可接受的盐,其中变量如在wo 2012/062704中所描述的,其全部内容通过引用并入本文。
[0058]
在第六个实施方式中,所公开的tyk2抑制剂可以选自具有下式的那些:
[0059][0060]
或其药学上可接受的盐,其中变量如在wo 2015/091584中所描述的,其全部内容通过引用并入本文。作为第六个实施方式的一部分的具有该式的示例性化合物包括但不限于具有下式的那些:
[0061][0062]
或其药学上可接受的盐。
[0063]
在第七个实施方式中,所公开的tyk2抑制剂可以选自具有下式的那些:
[0064][0065]
或其药学上可接受的盐,其中变量如在wo 2016/027195中所描述的,其全部内容通过引用并入本文。作为第七个实施方式的一部分的具有该式的示例性化合物包括但不限于具有下式的那些:
[0066][0067]
或其药学上可接受的盐。
[0068]
在第八个实施方式中,所公开的tyk2抑制剂可以选自具有下式的那些:
[0069][0070]
或其药学上可接受的盐,其中变量如在us 2017/0240552中所描述的,其全部内容通过引用并入本文。作为第八个实施方式的一部分的具有该式的示例性化合物包括但不限于具有下式的那些:
[0071][0072]
或其药学上可接受的盐。
[0073]
在第九个实施方式中,所公开的tyk2抑制剂可以选自具有下式的那些:
[0074][0075]
或其药学上可接受的盐,其中变量如在wo 2015/016206中所描述的,其全部内容通过引用并入本文。
[0076]
在第十个实施方式中,所公开的tyk2抑制剂可以选自具有下式的那些:
[0077][0078]
或其药学上可接受的盐,其中变量如在wo 2013/146963中所描述的,其全部内容通过引用并入本文。
[0079]
在第十一个实施方式中,所公开的tyk2抑制剂可以选自具有下式的那些:
[0080][0081]
或其药学上可接受的盐,其中变量如在wo 2016/047678中所描述的,其全部内容通过引用并入本文。
[0082]
在第十二个实施方式中,所公开的tyk2抑制剂可以选自在us 2015/0299139;wo 2015/069310;us 9,505,748;wo 2018/0162889;us 2013/0178478;或wo 2015/123453中描述的那些,其每一个的全部内容通过引用并入本文。
[0083]
在第十三个实施方式中,所公开的tyk2抑制剂可以选自具有下式的那些:
[0084][0085]
或其药学上可接受的盐,其中变量如在wo 2015/131080或wo 2016/138352中所描述的,其全部内容通过引用并入本文。
[0086]
在第十四个实施方式中,所公开的tyk2抑制剂可以选自具有下式的那些:
[0087][0088]
或其药学上可接受的盐,其中变量如在wo 2017/040757中所描述的,其全部内容通过引用并入本文。
[0089]
在第十五个实施方式中,所公开的tyk2抑制剂可以选自具有下式的那些:
[0090][0091]
或其药学上可接受的盐,其中变量如在wo 2015/131080、wo 2016/138352和wo 2017/040757中所描述的,其全部内容通过引用并入本文。
[0092]
在第十六个实施方式中,所公开的tyk2抑制剂可以选自具有下式的那些:
[0093][0094]
或其药学上可接受的盐,其中变量如在wo 2018/071794中所描述的,其全部内容通过引用并入本文。
[0095]
在第十七个实施方式中,所公开的tyk2抑制剂可以选自具有下式的那些:
[0096][0097]
或其药学上可接受的盐,其中变量如在wo 2018/075937中所描述的,其全部内容通过引用并入本文。
[0098]
在第十八个实施方式中,所公开的tyk2抑制剂可以选自具有下式的那些:
[0099][0100]
或其药学上可接受的盐,其中变量如在us 2013/0178478中所描述的,其全部内容通过引用并入本文。
[0101]
在第十九个实施方式中,所公开的tyk2抑制剂可以选自具有下式的那些:
[0102][0103]
或其药学上可接受的盐,其中变量如在wo 2015/123453中所描述的,其全部内容通过引用并入本文。
[0104]
在第二十个实施方式中,所公开的tyk2抑制剂可以选自具有下式的那些:
[0105]
[0106]
或其药学上可接受的盐,其中变量如在wo 2015/089143中所描述的,其全部内容通过引用并入本文。
[0107]
在第二十一个实施方式中,所公开的tyk2抑制剂可以选自具有下式的那些:
[0108][0109]
或其药学上可接受的盐,其中变量如在wo 2015/089143中所描述的,其全部内容通过引用并入本文。
[0110]
在第二十二个实施方式中,所公开的tyk2抑制剂可以选自具有下式的那些:
[0111][0112]
或其药学上可接受的盐,其中变量如在wo 2018/067432中所描述的,其全部内容通过引用并入本文。
[0113]
在第二十三个实施方式中,所公开的tyk2抑制剂可以选自具有下式的那些:
[0114][0115]
或其药学上可接受的盐,其中变量如在wo 2018/093968中所描述的,其全部内容通过引用并入本文。
[0116]
在第二十四个实施方式中,所公开的tyk2抑制剂可以选自具有下式的那些:
[0117][0118]
或其药学上可接受的盐,其中变量如在wo 2018/081488中所描述的,其全部内容通过引用并入本文。
[0119]
在第二十五个实施方式中,所公开的tyk2抑制剂可以选自具有下式的那些:
[0120][0121]
或其药学上可接受的盐,其中
[0122]
r1是被0-7个r
1a
任选取代的c
1-3
烷基;
[0123]r1a
在每次出现时独立地为氢、氘、f、cl、br、cf3或cn;
[0124]
r2是c
1-6
烷基或-(ch2)
r-3-14元碳环,每个基团被0-4个r
2a
取代;
[0125]r2a
在每次出现时独立地为氢、=o、卤素、ocf3、cn、no2、-(ch2)rorb、-(ch2)rsrb、-(ch2)rc(o)rb、-(ch2)rc(o)orb、-(ch2)roc(o)rb、-(ch2)rnr
11r11
、-(ch2)rc(o)nr
11r11
、-(ch2)rnrbc(o)rc、-(ch2)rnrbc(o)orc、-nrbc(o)nr
11r11
、-s(o)
p
nr
11r11
、-nrbs(o)
p
rc、-s(o)
p
r、0-3个ra取代的c
1-6
烷基、c
1-6
卤代烷基、0-3个ra取代的c
2-6
烯基、0-3个ra取代的c
2-6
炔基、0-1个ra取代的-(ch2)
r-3-14元碳环或0-2个ra取代的-(ch2)
r-5-7元杂环,所述杂环包含碳原子或1-4个杂原子,所述杂原子选自n、o和s(o)
p
;
[0126]
r3是c
3-10
环烷基、c
6-10
芳基或5-10元杂环,所述杂环含有1-4个杂原子,所述杂原子选自n、o和s,每个基团被0-4个r
3a
取代;
[0127]r3a
在每次出现时独立地为氢、=o、卤素、ocf3、cf3、chf2、cn、no2、-(ch2)rorb、-(ch2)rsrb、-(ch2)rc(o)rb、-(ch2)rc(o)orb、-(ch2)roc(o)rb、-(ch2)rnr
11r11
、-(ch2)rc(o)nr
11r11
、-(ch2)rnrbc(o)rc、-(ch2)rnrbc(o)orc、-nrbc(o)nr
11r11
、-s(o)
p
nr
11r11
、-nrbs(o)
p
rc、-s(o)
p
rc、0-3个ra取代的c
1-6
烷基、0-3个ra取代的c
2-6
烯基、0-3个ra取代的c
2-6
炔基、c
1-6
卤代烷基、0-3个ra取代的-(ch2)
r-3-14元碳环或0-3个ra取代的-(ch2)
r-5-10元杂环,所述杂环包含碳原子或1-4个杂原子,所述杂原子选自n、o和s(o)
p
;
[0128]
或两个r
3a
与其所附接的原子一起组合形成稠环,其中所述环选自苯基和5-7元杂环,所述杂环包含碳原子和1-4个杂原子,所述杂原子选自n、s或o,所述稠环进一步被r
a1
取代;
[0129]
r4和r5独立地为氢、0-1个rf取代的c
1-4
烷基、0-3个rd取代的(ch2)r-苯基或者-(ch2)-5-7元杂环,所述杂环包含碳原子或1-4个杂原子,所述杂原子选自n、o和s(o)
p
;
[0130]r11
在每次出现时独立地为氢、0-3个rf取代的c
1-4
烷基、cf3、0-1个rf取代的c
3-10
环烷基、0-3个rd取代的(ch)
r-苯基或者0-3个rd取代的-(ch2)-5-7元杂环,所述杂环包含碳原子或1-4个杂原子,所述杂原子选自n、o和s(o)
p
;
[0131]
ra和r
a1
在每次出现时独立地为氢、f、cl、br、ocf3、cf3、chf2、cn、no2、-(ch2)rorb、-(ch2)rsrb、-(ch2)rc(o)rb、-(ch2)rc(o)orb、-(ch2)roc(o)rb、-(ch2)rnr
11r11
、-(ch2)rc(o)nr
11r11
、-(ch2)rnrbc(o)rc、-(ch2)rnrbc(o)orc、-nrbc(o)nr
11r11
、-s(o)
p
nr
11r11
、-nrbs(o)
p
rc、-s(o)rc、-s(o)2rc、0-3个rf取代的c
1-6
烷基、c
1-6
卤代烷基、0-3个ra取代的c
2-6
烯基、0-3个ra取代的c
2-6
炔基、-(ch2)
r-3-14元碳环或者0-3个rf取代的-(ch2)
r-5-7元杂环,所述杂环包含碳原子或1-4个杂原子,所述杂原子选自n、o和s(o)
p
;
[0132]
rb在每次出现时独立地为氢、0-3个rd取代的c
1-6
烷基、c
1-6
卤代烷基、0-2个rd取代的c
3-6
环烷基、或者0-3个rf取代的-(ch2)
r-5-7元杂环,所述杂环包含碳原子或1-4个杂原
子,所述杂原子选自n、o和s(o)
p
或0-3个rd取代的(ch2)
r-苯基;
[0133]
rc是0-3个rf取代的c
1-6
烷基、0-3个rf取代的(ch2)
r-c
3-6
环烷基、0-3个rf取代的(ch2)
r-苯基;或者
[0134]
rd在每次出现时独立地为氢、f、cl、br、ocf3、cf3、cn、no2、-ore、-(ch2)rc(o)rc、-nrere、-nrec(o)orc、c
1-6
烷基或0-3个rf取代的(ch2)
r-苯基;
[0135]
re在每次出现时独立地选自氢、c
1-6
烷基、c
3-6
环烷基和0-3个rf取代的(ch2)
r-苯基;
[0136]
rf在每次出现时独立地为氢、卤素、cn、nh2、oh、c
3-6
环烷基、cf3、o(c
1-6
烷基)或-(ch2)
r-5-7元杂芳基,所述芳基包含碳原子或1-4个杂原子,所述杂原子选自n、o和s(o)
p
;
[0137]
p是0、1或2;和
[0138]
r是0、1、2、3或4,其中其他定义和特定化合物可以参见例如us 2015/0299139,其全部内容通过引用并入本文。
[0139]
在第二十六个实施方式中,所公开的tyk2抑制剂可以选自具有下式的那些:
[0140][0141]
或其药学上可接受的盐,其中
[0142]
r1是被0-7个r
1a
任选取代的c
1-3
烷基;
[0143]r1a
在每次出现时独立地为氢、氘、f、ci、br、cf3或cn;
[0144]
r2是0-4个r
2a
取代的c
1-6
烷基、0-4个r
2a
取代的c
3-6
环烷基、0-4个r
2a
取代的c
6-10
芳基、0-4个r
2a
取代的5-14元杂环,所述杂环包含1-4个选自n、o和s的杂原子、nr6r6或orb;
[0145]r2a
在每次出现时独立地为氢、=o、卤素、ocf3、cn、no2、-(ch2)rorb、-(ch2)rsrb、-(ch2)rc(o)rb、-(ch2)rc(o)orb、-(ch2)roc(o)rb、-(ch2)rnr
11r11
、-(ch2)rc(o)nr
11r11
、-(ch2)rnrbc(o)rc、-(ch2)rnrbc(o)orc、-nrbc(o)nr
11r11
、-s(o)
p
nr
11r11
、-nrbs(o)
p
rc、-s(o)
p
rc、0-3个r
2a
取代的c
1-6
烷基、c
1-6
卤代烷基、0-1个ra取代的-(ch2)
r-3-14元碳环或0-2个ra取代的-(ch2)
r-5-7元杂环,所述杂环包含碳原子或1-4个杂原子,所述杂原子选自n、o和s(o)
p
;
[0146]
或一个r
2a
和另一个r
2a
与其所附接的原子一起组合形成稠合的5-6元环,其中所述稠合环可以被0-2个ra取代;
[0147]
r3是0-5个r
3a
取代的-(ch2)
r-3-14元碳环;
[0148]r3a
在每次出现时独立地为氢、=o、卤素、ocf3、cn、no2、-(ch2)rorb、-(ch2)rsrb、-(ch2)rc(o)rb、-(ch2)rc(o)orb、-(ch2)roc(o)rb、(ch2)rnr
11r11
、-(ch2)rc(o)nr
11r11
、-(ch2)rnrbc(o)rc、-(ch2)rnrbc(o)orc、-nrbc(o)nr
11r11
、-s(o)
p
nr
11r11
、-nrbs(o)
p
rc、-s(o)
p
rc、0-3个ra取代的c
1-6
烷基、c
1-6
卤代烷基、0-3个ra取代的-(ch2)
r-3-14元碳环或0-3个ra取代的-(ch2)
r-5-10元杂环,所述杂环包含碳原子或1-4个杂原子,所述杂原子选自n、o和s(o)
p
;
[0149]
或两个r
3a
与其所附接的原子一起组合形成稠环,其中所述环选自苯基和5-7元杂环,所述杂环包含碳原子和1-4个杂原子,所述杂原子选自n、s或o,所述稠环可以进一步被ra取代;
[0150]
r4和r5独立地为氢、0-3个rf取代的c
1-4
烷基、0-3个rd取代的(ch2)
r-苯基或-(ch2)-5-7元杂环,所述杂环包含5个碳原子和1-4个杂原子,所述杂原子选自n、o和s(o)
p
;
[0151]
r6和r
11
在每次出现时独立地为氢、0-3个rf取代的c
1-4
烷基、cf3、0-1个rf取代的c
3-10
环烷基、0-3个rd取代的(ch)
r-苯基或0-3个rd取代的-(ch2)
r-5-7元杂环,所述杂环包含碳原子和1-4个杂原子,所述杂原子选自n、o和s(o)
p
;
[0152]
ra在每次出现时为氢、f、cl、br、ocf3、cf3、chf2、cn、no2、-(ch2)rorb、-(ch2)rsrb、-(ch2)rc(o)rb、-(ch2)rc(o)orb、-(ch2)roc(o)rb、-(ch2)rnr
11r11
、-(ch2)rc(o)nr
11r11
、-(ch2)rnrbc(o)rc、-(ch2)rnrbc(o)orc、-nrbc(o)nr
11r11
、-s(o)
p
nr
11r11
、-nrbs(o)
p
rc、-s(o)rc、-s(o)2rc、0-1个rf取代的c
1-6
烷基、c
l-6
卤代烷基、-(ch2)
r-3-14元碳环或0-3个rf取代的-(ch2)
r-5-7 15元杂环,杂环包含碳原子和1-4个杂原子,所述杂原子选自n、o和s(o)
p
;
[0153]
rb在每次出现时为氢、0-3个rd取代的c
1-6
烷基、c
1-6
卤代烷基、0-3个rd取代的c
3-6
环烷基或0-3个rf取代的-(ch2)
r-5-7元杂环,所述杂环包含碳原子和1-4个杂原子,所述杂原子选自n、o和s(o)
p
,或0-3个rd取代的(ch2)
r-苯基;
[0154]
rc是0-3个rf取代的c
1-6
烷基、0-3个rf取代的(ch2)
r-c
3-6
环烷基或0-3个rf取代的(ch2)
r-苯基;
[0155]
rd在每次出现时独立地为氢、f、cl、br、ocf3、cf3、cn、no2、ore、-(ch2)rc(o)rc、nrere、-nrec(o)orc、c
1-6
烷基或0-3个rf取代的(ch2)
r-苯基;
[0156]
re在每次出现时独立地选自氢、c
1-6
烷基、c
3-6
环烷基和0-3个rf取代的(ch2)
r-苯基;
[0157]
rf在每次出现时独立地为氢、卤素、cn、nh2、oh、c
3-6
环烷基、cf3、o(c1-6烷基)或-(ch2)
r-5-7元杂芳基,所述杂芳基包含碳原子和1-4个杂原子,所述杂原子选自n、o和s(o)
p
;
[0158]
p是0、1或2;和
[0159]
r是0、1、2、3或4。
[0160]
在第二十七个实施方式中,所公开的tyk2抑制剂可以选自具有下式的那些:
[0161][0162]
或其药学上可接受的盐,其中变量如在wo 2015/069310中所描述的,其全部内容通过引用并入本文。
[0163]
在第二十八个实施方式中,所公开的tyk2抑制剂可以选自具有下式的那些:
[0164][0165]
或其药学上可接受的盐,其中
[0166]
y是n或cr6;
nrere、-nrec(o)orc、c
1-6
烷基或0-3个rf取代的(ch2)
r-苯基;
[0181]
re在每次出现时独立地选自氢、c
1-6
烷基、c
3-6
环烷基和0-3个rf取代的(ch2)
r-苯基;
[0182]
rf在每次出现时独立地为氢、卤素、cn、nh2、oh、c
3-6
环烷基、cf3、o(c
1-6
烷基)或-(ch2)
r-5-7元杂环,所述杂环包含碳原子和1-4个杂原子,所述杂原子选自n、o和s(o)
p
;
[0183]
p是0、1或2;和
[0184]
r是0、1、2、3或4,其中其他定义和特定化合物如在us 9,505,748和wo 2018/0162889中所描述的,其每一个的全部内容通过引用并入本文。
[0185]
在第二十九个实施方式中,所公开的tyk2抑制剂可以选自具有下式的那些:
[0186][0187]
或其药学上可接受的盐,其中:
[0188]
r1是
[0189]
r2是
[0190]
在第三十个实施方式中,本文所述的tyk2抑制剂是6-(环丙烷甲酰胺)-4-((2-甲氧基-3-(1-甲基-1h-1,2,4-三唑-3-基)苯基)氨基)-n-(甲基-d3)哒嗪-3-甲酰胺(bms-986165),其具有下述化学结构:
[0191][0192]
或其药学上可接受的盐。
[0193]
与阿普斯特联合使用的所公开的tyk2抑制剂的特定剂量和治疗方案将取决于多种因素,包括年龄、体重、一般健康状况、性别、饮食、施用时间、排泄率、药物组合、治疗医师的判断以及所治疗的特定疾病的严重程度。
[0194]
在第三十一个实施方式中,与阿普斯特联合使用的所公开的tyk2抑制剂(例如,如在第二个至第三十个实施方式的任一项中)的有效量范围从0.001至50mg/kg体重/天。例如,作为第三十一个实施方式的一部分,与阿普斯特联合使用的所公开的tyk2抑制剂(例如,如在第二个至第三十个实施方式的任一项中)的有效量范围从约0.1mg/天至约250mg/天,例如,从约0.2mg/天至约100mg/天、约0.5mg/天至约50mg/天和约1.0mg至约24mg/天。
[0195]
在第三十二个实施方式中,本文所述的tyk2抑制剂是bms-986165或其药学上可接受的盐,以及bms-986165或其药学上可接受的盐的有效量范围从约0.1mg/天至约250mg/天、约0.1mg/天至约100mg/天、约0.1mg/天至约50mg/天、约0.1mg/天至约25mg/天、0.1mg/天至约15mg/天、约0.1mg/天至约10mg/天、约0.5mg/天至约15mg/天、约0.5mg/天至约10mg/天、约0.1mg/天至约5mg/天、约0.5mg/天至约5mg/天、约1mg/天至约25mg/天、约2mg/天至约14mg/天、约2mg/天至约12mg/天或约3mg/天至约12mg/天。或者,作为第三十二个实施方式的一部分,bms-986165或其药学上可接受的盐的有效量范围从约1mg/天至约15mg/天、约1mg/天至约14mg/天、约2mg/天至约14mg/天、约2mg/天至约12mg/天或约3mg/天至约12mg/天。
[0196]
在第三十三个实施方式中,本文所述的tyk2抑制剂是bms-986165或其药学上可接受的盐,以及bms-986165或其药学上可接受的盐的有效量是约0.1mg/天、约0.5mg/天、约1.0mg/天、约2mg/天、约3mg/天、约4mg/天、约5mg/天、约6mg/天、约7mg/天、约8mg/天、约9mg/天、约10mg/天、约11mg/天或约12mg/天。或者,作为第三十三个实施方式的一部分,bms-986165或其药学上可接受的盐的有效量是约2mg/天、约3mg/天、约4mg/天、约5mg/天、约6mg/天、约7mg/天、约8mg/天、约9mg/天、约10mg/天、约11mg/天或约12mg/天。在另一个替代方案中,作为第三十三个实施方式的一部分,bms-986165或其药学上可接受的盐的有效浓度是约1nm至约1μm(例如,从约0.01μm至约0.1μm)。
[0197]
3.阿普斯特
[0198]
如上所述,阿普斯特作为(s)对映异构体在光学上富集。在第三十四个实施方式中,在本文所述的方法和组合物中阿普斯特的立体异构纯度大于90%,其中tyk2抑制剂和相关特征如本文所述,例如,如第一个至第三十三个实施方式中的任一项。或者,作为第三十四个实施方式的一部分,在本文所述的方法和组合物中阿普斯特的立体异构纯度大于95%,其中tyk2抑制剂和相关特征如本文所述,例如,如第一个至第三十三个实施方式中的任一项。在另一个替代方案中,作为第三十四个实施方式的一部分,在本文所述的方法和组合物中阿普斯特的立体异构纯度大于97%,其中tyk2抑制剂和相关特征如本文所述,例如,如第一个至第三十三个实施方式中的任一项。在另一个替代方案中,作为第三十四个实施方式的一部分,在本文所述的方法和组合物中阿普斯特的立体异构纯度大于98%,其中tyk2抑制剂和相关特征如本文所述,例如,如第一个至第三十三个实施方式中的任一项。在另一个替代方案中,作为第三十四个实施方式的一部分,在本文所述的方法和组合物中阿普斯特的立体异构纯度大于99%,其中tyk2抑制剂和相关特征如本文所述,例如,如第一个至第三十三个实施方式中的任一项。在另一个替代方案中,作为第三十四个实施方式的一部分,在本文所述的方法和组合物中阿普斯特的立体异构纯度大于99.5%,其中tyk2抑制剂和相关特征如本文所述,例如,如第一个至第三十三个实施方式中的任一项。在另一个替代方案中,作为第三十四个实施方式的一部分,在本文所述的方法和组合物中阿普斯特的
立体异构纯度大于99.9%,其中tyk2抑制剂和相关特征如本文所述,例如,如第一个至第三十三个实施方式中的任一项。
[0199]
在所公开的方法和组合物中包括阿普斯特的多晶型,并且包括例如在us 9,018,243中描述的那些,其全部内容通过引用并入本文。在第三十五个实施方式中,在所公开的方法和组合物中的阿普斯特是单晶型,其中针对阿普斯特以及tyk2抑制剂的其他特征和相关特征如本文所述,例如,如第一个至第三十四个实施方式中的任一项。
[0200]
在第三十六个实施方式中,在所公开的方法和组合物中的阿普斯特是单晶型b,其特征是在选自10.1
°
、13.5
°
、20.7
°
和26.9
°
的2θ角处的x射线粉末衍射峰,其中针对阿普斯特以及tyk2抑制剂的其他特征和相关特征如本文所述,例如,如第一个至第三十四个实施方式中的任一项。或者,作为第三十六个实施方式的一部分,在所公开的方法和组合物中的阿普斯特是单晶型b,其特征是在选自10.1
°
、13.5
°
、15.7
°
、18.1
°
、20.7
°
、24.7
°
和26.9
°
的2θ角处的x射线粉末衍射峰,其中针对阿普斯特以及tyk2抑制剂的其他特征和相关特征如本文所述,例如,如第一个至第三十四个实施方式中的任一项。在另一个替代方案中,作为第三十六个实施方式的一部分,在所公开的方法和组合物中的阿普斯特是单晶型b,其特征是在选自10.1
°
、13.5
°
、15.7
°
、16.3
°
、18.1
°
、20.7
°
、22.5
°
、24.7
°
、26.2
°
、26.9
°
和29.1
°
的2θ角处的x射线粉末衍射峰,其中针对阿普斯特以及tyk2抑制剂的其他特征和相关特征如本文所述,例如,如第一个至第三十四个实施方式中的任一项。
[0201]
在第三十七个实施方式中,在所公开的方法和组合物中的阿普斯特是至少90%单晶型b,其中针对阿普斯特以及tyk2抑制剂的其他特征和相关特征如本文所述,例如,如第一个至第三十六个实施方式中的任一项。或者,在所公开的方法和组合物中的阿普斯特是至少95%单晶型b,其中针对阿普斯特以及tyk2抑制剂的其他特征和相关特征如本文所述,例如,如第一个至第三十六个实施方式中的任一项。在另一个替代方案中,在所公开的方法和组合物中的阿普斯特是至少99%单晶型b,其中针对阿普斯特以及tyk2抑制剂的其他特征和相关特征如本文所述,例如,如第一个至第三十六个实施方式中的任一项。
[0202]
与所公开的tyk2抑制剂联合使用的阿普斯特或其药学上可接受的盐的特定剂量和治疗方案将取决于多种因素,包括年龄、体重、一般健康状况、性别、饮食、施用时间、排泄率、药物组合、治疗医师的判断以及所治疗的特定疾病的严重程度。
[0203]
例如,在第三十八个实施方式中,阿普斯特或其药学上可接受的盐的有效量范围从约0.5mg至约1000mg每天、约1mg至约1000mg每天、约5mg至约500mg每天、约10mg至约200mg每天、约10mg至约100mg每天、约40mg至约100mg每天、约20mg至约40mg每天、约0.1mg至约10mg每天、约0.5mg至约5mg每天、约1mg至约20mg每天和约1mg至约10mg每天、约1mg至约100mg每天、约1mg至约80mg每天、约5mg至约70mg每天和约10mg至约60mg每天,其中针对阿普斯特以及tyk2抑制剂的其他特征和相关特征如本文所述,例如,如第一个至第三十七个实施方式中的任一项。或者,作为第三十八个实施方式的一部分,阿普斯特或其药学上可接受的盐的有效量范围从约10mg至约60mg每天,其中针对阿普斯特以及tyk2抑制剂的其他特征和相关特征如本文所述,例如,如第一个至第三十七个实施方式中的任一项。在另一个替代方案中,作为第三十八个实施方式的一部分,阿普斯特或其药学上可接受的盐的有效量范围从约40mg至约100mg每天,其中针对阿普斯特以及tyk2抑制剂的其他特征和相关特征如本文所述,例如,如第一个至第三十七个实施方式中的任一项。在另一个替代方案中,
作为第三十八个实施方式的一部分,阿普斯特或其药学上可接受的盐的有效量范围从约40mg至约100mg每天之间,其中针对阿普斯特以及tyk2抑制剂的其他特征和相关特征如本文所述,例如,如第一个至第三十七个实施方式中的任一项。在另一个替代方案中,作为第三十八个实施方式的一部分,阿普斯特或其药学上可接受的盐的有效量范围从约4mg至约10mg每天,其中针对阿普斯特以及tyk2抑制剂的其他特征和相关特征如本文所述,例如,如第一个至第三十七个实施方式中的任一项。在另一个替代方案中,作为第三十八个实施方式的一部分,阿普斯特或其药学上可接受的盐的有效量范围从约4mg至约10mg每天之间,其中针对阿普斯特以及tyk2抑制剂的其他特征和相关特征如本文所述,例如,如第一个至第三十七个实施方式中的任一项。在另一个替代方案中,作为第三十八个实施方式的一部分,阿普斯特或其药学上可接受的盐的有效量是约1mg每天、约2mg每天、约3mg每天、约4mg每天、约5mg每天、约10mg每天、约15mg每天、约20mg每天、约25mg每天、约30mg每天、约35mg每天、约40mg每天、约45mg每天、约50mg每天、约55mg每天或约60mg每天,其中针对阿普斯特以及tyk2抑制剂的其他特征和相关特征如本文所述,例如,如第一个至第三十七个实施方式中的任一项。在另一个替代方案中,作为第三十八个实施方式的一部分,阿普斯特或其药学上可接受的盐的有效量是约30mg每天或约60mg每天,其中针对阿普斯特以及tyk2抑制剂的其他特征和相关特征如本文所述,例如,如第一个至第三十七个实施方式中的任一项。在另一个替代方案中,作为第三十八个实施方式的一部分,阿普斯特以约30mg每天一次的剂量施用,其中针对阿普斯特以及tyk2抑制剂的其他特征和相关特征如本文所述,例如,如第一个至第三十七个实施方式中的任一项。在另一个替代方案中,作为第三十八个实施方式的一部分,阿普斯特以约30mg每天两次的剂量施用,其中针对阿普斯特以及tyk2抑制剂的其他特征和相关特征如本文所述,例如,如第一个至第三十七个实施方式中的任一项。在另一个替代方案中,作为第三十八个实施方式的一部分,阿普斯特的有效浓度是约100nm至约10μm(例如,从约0.1μm至约1μm),其中针对阿普斯特以及tyk2抑制剂的其他特征和相关特征如本文所述,例如,如第一个至第三十七个实施方式中的任一项。
[0204]
在第三十九个实施方式中,使用下述滴定时间表将阿普斯特滴定至约30mg每天施用两次的剂量:
[0205]
第1天:早上约10mg;
[0206]
第2天:早上约10mg和晚上约10mg;
[0207]
第3天:早上约10mg和晚上约20mg;
[0208]
第4天:早上约20mg和晚上约20mg;
[0209]
第5天:早上约20mg和晚上约30mg;和
[0210]
第6天和此后:约30mg,每天两次,其中针对阿普斯特以及tyk2抑制剂的其他特征和相关特征如本文所述,例如,如第一个至第三十七个实施方式中的任一项。或者,使用下述滴定时间表将阿普斯特滴定至约40mg/天之间至约100mg/天之间的剂量:
[0211]
第1天:早上约10mg;
[0212]
第2天:早上约10mg和晚上约10mg;
[0213]
第3天:早上约10mg和晚上约20mg;
[0214]
第4天:早上约20mg和晚上约20mg;
[0215]
第5天:早上约20mg和晚上约30mg;和
[0216]
第6天和此后:约40mg/天之间至约100mg/天之间,其中针对阿普斯特以及tyk2抑制剂的其他特征和相关特征如本文所述,例如,如第一个至第三十七个实施方式中的任一项。在另一个替代方案中,使用下述滴定时间表将阿普斯特滴定至约20mg每天施用两次的剂量:
[0217]
第1天:早上约10mg;
[0218]
第2天:早上约10mg和晚上约10mg;
[0219]
第3天:早上约10mg和晚上约20mg;
[0220]
第4天:早上约20mg和晚上约20mg;
[0221]
第5天:早上约20mg和晚上约30mg;和
[0222]
第6天和此后:约20mg,每天两次,其中针对阿普斯特以及tyk2抑制剂的其他特征和相关特征如本文所述,例如,如第一个至第三十七个实施方式中的任一项。在又一个替代方案中,使用下述滴定时间表将阿普斯特滴定至约4mg/天之间至约10mg/天之间的剂量:
[0223]
第1天:早上约1mg;
[0224]
第2天:早上约1mg和晚上约1mg;
[0225]
第3天:早上约1mg和晚上约2mg;
[0226]
第4天:早上约2mg和晚上约2mg;
[0227]
第5天:早上约2mg和晚上约3mg;和
[0228]
第6天和此后:约4mg/天之间至约10mg/天之间,其中针对阿普斯特以及tyk2抑制剂的其他特征和相关特征如本文所述,例如,如第一个至第三十七个实施方式中的任一项。在又一个替代方案中,使用下述滴定时间表将阿普斯特滴定至约3mg每天施用两次的剂量:
[0229]
第1天:早上约1mg;
[0230]
第2天:早上约1mg和晚上约1mg;
[0231]
第3天:早上约10mg和晚上约2mg;
[0232]
第4天:早上约2mg和晚上约2mg;
[0233]
第5天:早上约2mg和晚上约3mg;和
[0234]
第6天和此后:约3mg,每天两次,其中针对阿普斯特以及tyk2抑制剂的其他特征和相关特征如本文所述,例如,如第一个至第三十七个实施方式中的任一项。
[0235]
3.组合物和施用
[0236]
本文还提供了药物组合物,其包含治疗有效量的阿普斯特或其药学上可接受的盐;以及治疗有效量的tyk2抑制剂(例如,bms-986165)。所公开的药物组合物的特征包括上文所述的要素,例如,如第一个至第三十八个实施方式中的任一项。
[0237]
还提供了药物组合物用于治疗对pde4的抑制具有应答的疾病或病症的用途,所述药物组合物包含治疗有效量的阿普斯特或其药学上可接受的盐;以及治疗有效量的tyk2抑制剂(例如,bms-986165)。所公开的药物组合物的特征包括上文所述的要素,例如,如第一个至第三十八个实施方式中的任一项。
[0238]
包括药物组合物和单一单位剂型,其包含单独或以固定剂量在一起的阿普斯特和tyk2抑制剂(例如,bms-986165),用于如上文所述的施用(例如,如第一个至第三十八个实施方式中的任一项)。所公开的方法和组合物的单一单位剂型适于口服、粘膜(例如,鼻内、舌下、阴道、颊部或直肠)、胃肠外(例如,皮下、静脉内、推注、肌内或动脉内)或透皮向患者
施用。剂型的实例包括但不限于:片剂;囊片剂;胶囊剂,如软弹性明胶胶囊剂;扁囊剂;药片(troche);锭剂;分散体;栓剂;软膏;巴布剂(膏药);糊剂;粉末;敷料;霜剂;膏药;溶液;贴片;气雾剂(例如,鼻腔喷雾剂或吸入器);凝胶;适于向患者口服或粘膜施用的液体剂型,包括混悬剂(例如,水性或非水性液体混悬剂、水包油乳剂或油包水液体乳剂)、溶液和酏剂;适于向患者胃肠外施用的液体剂型;和无菌固态(例如,结晶或无定形固定),其可以重构以提供适于向患者胃肠外施用的液体剂型。
[0239]
剂型的组成、形状和类型将通常会根据其用途而改变。例如,与用于慢性治疗相同疾病的剂型相比,用于炎症或相关疾病的急性治疗的剂型可包含更大量的一种或多种活性成分。类似地,与用于治疗相同疾病或病症的口服剂型相比,胃肠外剂型可以包含更少量的一种或多种活性成分。本发明所涵盖的特定剂型彼此不同的这些和其他方式对于本领域技术人员来说将是显而易见的。参见,例如,remington's pharmaceutical sciences,18th ed.,mack publishing,easton pa.(1990)。
[0240]
在第三十九个实施方式中,在所公开的方法和组合物中的阿普斯特是胃肠外、透皮、粘膜、鼻内、颊部、舌下或口服施用的,其中针对阿普斯特以及tyk2抑制剂的其他特征和相关特征如本文所述,例如,如第一个至第三十八个实施方式中的任一项。或者,作为第三十九个实施方式的一部分,在所公开的方法和组合物中的阿普斯特是口服施用的,其中针对阿普斯特以及tyk2抑制剂的其他特征和相关特征如本文所述,例如,如第一个至第三十八个实施方式中的任一项。
[0241]
在第四十个实施方式中,在所公开的方法和组合物中的阿普斯特是以片剂或胶囊形式口服施用的,其中针对阿普斯特以及tyk2抑制剂的其他特征和相关特征如本文所述,例如,如第一个至第三十九个实施方式中的任一项。
[0242]
在第四十一个实施方式中,在所公开的方法和组合物中阿普斯特被配制成延释形式,其中针对阿普斯特以及tyk2抑制剂的其他特征和相关特征如本文所述,例如,如第一个至第三十九个实施方式中的任一项。
[0243]
在第四十二个实施方式中,在所公开的方法和组合物中阿普斯特被配制成速释形式,其中针对阿普斯特以及tyk2抑制剂的其他特征和相关特征如本文所述,例如,如第一个至第三十九个实施方式中的任一项。
[0244]
在第四十三个实施方式中,在所公开的方法和组合物中阿普斯特和tyk2抑制剂两者以固定剂量组合作为每日一次的制剂施用,其中针对阿普斯特以及tyk2抑制剂的其他特征和相关特征如本文所述,例如,如第一个至第四十二个实施方式中的任一项。
[0245]
4.由本文公开的方法和组合物治疗的病况
[0246]
使用本文公开的方法和组合物的对pde4的抑制具有应答的疾病或病症包括例如病毒性、遗传性、炎症性、过敏性和自身免疫性病况。
[0247]
在一个方面中,对pde4的抑制具有应答的疾病或病症选自慢性阻塞性肺病、哮喘、慢性肺部炎性疾病、高氧性肺泡损伤、炎症性皮肤病、银屑病、银屑病关节炎、类风湿性关节炎、类风湿性脊柱炎、骨关节炎、特应性皮炎、类风湿性脊柱炎、抑郁症、骨关节炎、接触性皮炎、强直性脊柱炎、狼疮、狼疮性肾炎、皮肤红斑狼疮、系统性红斑狼疮、麻风结节性红斑、干燥综合征、炎症性肠病、克罗恩病、白塞氏病和溃疡性结肠炎。
[0248]
在一个方面中,对pde4的抑制具有应答的疾病或病症选自银屑病、银屑病关节炎、
接触性皮炎、系统性红斑狼疮、皮肤红斑狼疮和溃疡性结肠炎。
[0249]
在一个方面中,对pde4的抑制具有应答的疾病或病症是银屑病。在另一个方面中,对pde4的抑制具有应答的疾病或病症是银屑病,并且受试者是光疗法或全身疗法的候选人。
[0250]
在一个方面中,对pde4的抑制具有应答的疾病或病症是斑块状银屑病。在另一个方面中,对pde4的抑制具有应答的疾病或病症是斑块状银屑病,并且受试者是光疗法或全身疗法的候选人。
[0251]
在一个方面中,对pde4的抑制具有应答的疾病或病症是中度至重度斑块状银屑病。在另一个方面中,对pde4的抑制具有应答的疾病或病症是重度斑块状银屑病,并且受试者是光疗法或全身疗法的候选人。
[0252]
在一个方面中,对pde4的抑制具有应答的疾病或病症是银屑病关节炎。
[0253]
在一个方面中,对pde4的抑制具有应答的疾病或病症是活动性银屑病关节炎。
[0254]
在一个方面中,对pde4的抑制具有应答的疾病或病症是心脏病,如充血性心力衰竭、心肌病、肺水肿、内毒素介导的感染性休克、急性病毒性心肌炎、心脏移植排斥和心肌梗塞。
[0255]
在一个方面中,对pde4的抑制具有应答的疾病或病症是hiv、肝炎、成人呼吸窘迫综合征、骨吸收疾病、囊性纤维化、败血性休克、败血症、内毒素休克、血流动力学休克、败血症综合征、缺血再灌注损伤、脑膜炎、纤维化疾病、恶病质、移植排斥、骨质疏松症、多发性硬化症和辐射损伤。
[0256]
在一个方面中,对pde4的抑制具有应答的疾病或病症是头部、甲状腺、颈部、眼、皮肤、口腔、咽喉、食管、胸部、骨、血液、骨髓、肺、结肠、乙状结肠、直肠、胃、前列腺、乳腺、卵巢、肾、肝、胰腺、脑、肠、心脏、肾上腺、皮下组织、淋巴结、心脏癌症及其组合。
[0257]
在一个方面中,对pde4的抑制具有应答的疾病或病症是多发性骨髓瘤、恶性黑色素瘤、恶性胶质瘤、急性淋巴细胞白血病、急性成淋巴细胞b细胞白血病、急性成淋巴细胞t细胞白血病、急性粒细胞白血病、急性早幼粒细胞白血病、急性单核细胞白血病、急性红白血病、急性巨核细胞白血病、急性粒单核细胞白血病、急性非淋巴细胞白血病、急性未分化白血病、慢性粒细胞白血病、慢性淋巴细胞白血病、毛细胞白血病、多发性骨髓瘤和急性成淋巴细胞白血病、髓性白血病、淋巴细胞性白血病和粒细胞性白血病。
[0258]
在一个方面中,对pde4的抑制具有应答的疾病或病症是实体瘤,如肉瘤、纤维肉瘤、粘液肉瘤、脂肪肉瘤、软骨肉瘤、骨肉瘤、脊索瘤、血管肉瘤、内皮肉瘤、淋巴管肉瘤、淋巴管内皮肉瘤、滑膜瘤、间皮瘤、尤文氏瘤、平滑肌肉瘤、横纹肌肉瘤、结肠癌、胰腺癌、乳腺癌、卵巢癌、前列腺癌、鳞状细胞癌、基底细胞癌、腺癌、汗腺癌、皮脂腺癌、乳头状癌、乳头状腺癌、囊腺癌、髓样癌、支气管癌、肾细胞癌、肝癌、胆管癌、绒毛膜癌、精原细胞瘤、胚胎癌、肾母细胞瘤、宫颈癌、睾丸肿瘤、肺癌、小细胞肺癌、膀胱癌、上皮癌、胶质瘤、星形细胞瘤、髓母细胞瘤、颅咽管瘤、室管膜瘤、卡波济氏肉瘤、松果体瘤、血管母细胞瘤、听神经瘤、少突胶质细胞瘤、脑血管瘤、黑色素瘤、神经母细胞瘤和视网膜母细胞瘤。
具体实施方式
[0259]
1.材料
[0260]
表1:全血测定:研究材料和试剂
[0261][0262]
表2:lps刺激的pbmc测定:研究材料和试剂
[0263][0264]
表3:用于研究的待测物
[0265][0266]
2.一般方法
[0267]
在知情同意和供体身份识别后,通过celgene供体计划接收全血。所有志愿者都是健康的,在抽血前至少72小时没有服用任何药物。在肝素钠管中收集血液。测定在抽血后2小时内开始。
[0268]
在两种不同的刺激条件下对健康供体人全血进行体外刺激。条件th0是用含抗cd3/抗cd28的管刺激。条件th17是使用含有抗cd3/抗cd28以及il-1β、il-6和il-23的管刺激。将全血分离到15毫升锥形管中,并用dmso、单独的阿普
司特、单独的bms-986165或bms-986165与阿普司特组合进行预处理。最终浓度为0.2%dmso,单独的阿普斯特为1μm,单独的bms-986165以及与1μm阿普斯特的组合为1μm、0.1μm、0.01μm和0.001μm。将血液充分混合,然后在37℃/5%co2培养箱中孵育1小时。
[0269]
将抗cd3/抗cd28(终浓度分别为200ng/ml和330ng/ml)管在工作台上解冻30分钟,然后标记。将柱塞压下然后折断。将管放置在一个直立的架子上,这样柱塞一侧在架子上朝下,管帽朝上。当与血液一起孵育时,按以下浓度将化合物人重组il-6、il-1β和il-23添加到所有th17管中:120ng il-6、120ng il-1β和150ng il-23。使用无菌无热原移液器吸头将1ml预处理全血加入每个试管中。盖上盖子,颠倒3次混合管中的内容物。将管立即置于37℃加热块中并孵育42小时(管帽端)。42小时后,将管从加热块上取下,拧开顶部,取出250μl上清液并转移到三个96孔聚丙烯板中。将样品立即在-80℃下冷冻。然后,将上清液在室温下解冻并通过luminex multi-plex magpix技术(millipore)检测细胞因子产生的洁净度或通过elisa(abcam)检测il-22。相应地遵照生产厂商的程序。
[0270]
外周血单核细胞(pbmc)的分离:在知情同意和供体身份识别后,通过celgene供体计划接收全血。所有志愿者都是健康的,在抽血前至少72小时没有服用任何药物。在肝素钠管中收集血液,并在抽血后2小时内用于pbmc分离。在分离pbmc之前,用含有2%fbs的pbs溶液(2%fbs-pbs)1:1稀释全血。将13ml ficoll-paque溶液装入管中,并将25ml稀释的血液装入ficoll-paque顶部。以1200g离心15分钟并打开制动器以分离细胞,然后将分离的pbmc转移到新管中。使用2%fbs-pbs洗涤pbmc,并以800g离心10分钟。将球团重悬在2%fbs-pbs中,并通过40μm细胞过滤器过滤以获得单细胞悬液。将3ml rbc裂解缓冲液用于消除分离的群中的红细胞。分离的pbmc用2%fbs-pbs洗涤,并重新悬浮在含有10%fbs和抗生素的rpmi生长培养基中。
[0271]
对于实施例6-11,分离来自9名健康供体的pbmc,并进行离体lps刺激,用于il-23、il-12p40、il-12p70、tnf-α、ifn-γ和mcp-1细胞因子分析。将pbmc以每孔200,000个细胞的密度接种在200μl含有10%fbs的rpmi生长培养基中,然后用dmso和化合物处理。每个孔接受相同量的dmso,最终浓度为0.3%v/v。根据下表4所示进行化合物处理的系列稀释。在化合物处理两小时后,将100ng/ml终浓度的lps作为刺激剂。然后将pbmc在37℃/5%co2培养箱中孵育16小时。
[0272]
表4:用于pbmc测定的化合物处理条件
[0273]
[0274][0275]
孵育16小时后,将上清液收集到新的96孔聚丙烯板中并以4000rpm离心10分钟以除去细胞碎片。根据生产厂商的程序,通过luminex bio-plex多路复用免疫测定(bio-rad)测量细胞因子产生情况。为确保上清液水平在该测定的标准细胞因子范围内,将样品稀释5倍用于il-12p40和27-plex测定,并针对il-23测定用于确定洁净度。
[0276]
3.数据分析
[0277]
使用milliplex analyst(millipore)进行细胞因子分析的数据处理,并将原始数据导出到excel模板以进行细胞因子分析。来自模板的数据使用graphpad prism 7.0(graphpad software,inc.,la jolla,ca)绘图,并以pg/ml或占对照%表示。还使用单因素anova和dunnett事后检验进行统计分析。
[0278]
针对pbmc测定的数据处理使用bio-plex管理器完成,并将原始数据导出到excel模板以进行细胞因子分析。数据使用graphpad prism 7.0(graphpad software,inc.,la jolla,ca)绘图,并以占dmso对照%表示。使用单因素anova和tukey多重比较检验进行统计分析。
[0279]
为评价阿普斯特和bms-986165的组合作用,通过比较两种药剂的组合应答和理论加和应答,分析来自两种独立处理的数据。使用分数乘积法计算两种药剂(a和b)的预期加和作用:(fu)a,b=(fu)a
×
(fu)b;其中fu=未受处理影响的分数。当观察到的未受组合影响的分数小于(fu)a,b时,确定组合的协同作用,而当观察到未受组合影响的分数等于(fu)a,b时,确定加和作用。当观察到的未受组合影响的分数大于(fu)a,b时,表明存在部分加和作用。
[0280]
实施例1
[0281]
在抗cd3/抗cd28(th0)或抗cd3/抗cd28、il-1β、il-6和il-23(th17)刺激的全血中由阿普斯特和bms-986165产生的白介素17a细胞因子
[0282]
在th0和th17条件下,针对il-17a、il-17f、il-22、tnf-α和gm-csf细胞因子产生情况,对来自4名健康供体的全血进行了分析。使用管系统,使用单独的阿普斯特和tyk2抑制剂bms-986165以及其组合两者预处理血液。在图1中的il-17a结果显示了il-17a占对照的%,所有数据均归一化至th17 dmso对照。阿普斯特在th0条件下抑制28%
的il-17a细胞因子表达,而在th17条件下没有影响。在这两种刺激条件下bms-986165具有类似作用,在0.001-1μm下抑制10-25%的il-17a表达。当阿普斯特与bms-986165组合时,在th0条件下观察到与1μm bms-986165的协同作用,il-17a减少65%。在th17条件下,1μm阿普斯特与0.01μm、0.1μm和1μm bms-986165的组合具有协同作用,il-17a的抑制分别为24%、44%和85%。图2显示了il-17a每毫升水平的皮克数。与th0刺激相比,th17刺激条件下的il-17a水平增加387%。在th0条件下,阿普斯特使il-17a水平从138pg/ml降至93pg/ml。1μm下的bms-986165使il-17a水平降至97pg/ml。使用th0刺激,阿普斯特与1μm bms-986165的组合使il-17a水平进一步降至24pg/ml。在th17条件下,刺激对照测得532pg/ml,并且阿普斯特不抑制il-17a水平。在0.01μm、0.1μm和1μm下,bms-986165使il-17a水平分别降至519pg/ml、428pg/ml和383pg/ml。1μm阿普斯特与0.01μm、0.1μm和1μm bms-986165的组合分别使il-17a水平降至379pg/ml、328pg/ml和68pg/ml。
[0283]
实施例2
[0284]
在抗cd3/抗cd28(th0)或抗cd3/抗cd28、il-1β、il-6和il-23(th17)刺激的全血中由阿普斯特和bms-986165产生的白介素17f细胞因子
[0285]
il-17f细胞因子表达数据见图3和图4。在th0条件下,阿普斯特将il-17f产生抑制69%,在th17条件下为49%。使用th0和th17刺激,bms-986165对il-17f具有类似作用。在最低浓度0.001μm下抑制为31%,并且具有剂量应答,在0.001μm、0.01μm、0.1μm和1μm下,il-17f表达分别抑制31%、34%、70%和95%(th17结果)。在th0条件下,1μm阿普斯特与bms-986165的组合具有部分加和作用,其范围从在0.001μm下的60%至在1μm下的95%。在th17条件下,更低浓度的bms-986165与阿普斯特的组合显示出协同作用。在th17刺激条件下,阿普斯特与bms-986165的组合在0.001μm、0.01μm、0.1μm和1μm下对il-17f产生的抑制分别为68%、70%、94%和99%。在th0刺激对照中,il-17f的水平为1085pg/ml,并且在th17刺激中增加至6524pg/ml。在th0刺激中和在th17刺激中,阿普斯特分别将il-17f减少至368pg/ml和3643pg/ml。在这两种刺激条件下,在0.1和1μm下,bms-986165显著减少il-17f。当与阿普斯特组合时并且在这两种刺激条件下,所有浓度的bms-986165均显著抑制il-17f。
[0286]
实施例3
[0287]
在抗cd3/抗cd28(th0)或抗cd3/抗cd28、il-1β、il-6和il-23(th17)刺激的全血中由阿普斯特和bms-986165产生的白介素22细胞因子
[0288]
il-22细胞因子表达数据见图5和图6。在th0条件下,阿普斯特将il-22细胞因子表达抑制85%,在th17条件下为41%。在th0刺激条件下,在0.01μm、0.1μm和1μm下,bms-986165将il-22分别抑制16%、86%和91%。在th17刺激条件下,在0.001μm下bms-986165对il-22细胞因子表达没有影响,而在0.01μm、0.1μm和1μm下分别抑制17%、60%和70%。在th0条件下,组合均与单独的阿普斯特具有类似作用,在bms-986165所有浓度下抑制~90%。在th17条件下,组合具有协同作用,在0.01μm和0.1μm下,对il-22细胞因子表达的抑制分别为60%和90%。th0刺激对照的il-22为1085pg/ml,th17对照为6524pg/ml。在th0条件下和在th17条件下,阿普斯特分别将il-22水平降低至368pg/ml和3643pg/ml。在0.1μm和1μm下,在这两种刺激条件下,bms-986165均显著降低il-22细胞因子的表达。当与阿普斯特组合时并且在这两种刺激条件下,所有浓度的bms-986165均显著抑制il-22。
[0289]
实施例4
[0290]
在抗cd3/抗cd28(th0)或抗cd3/抗cd28、il-1β、il-6和il-23(th17)刺激的全血中由阿普斯特和bms-986165产生的tnf-α细胞因子
[0291]
tnf-α细胞因子表达数据见图7和图8。在th0条件下,阿普斯特使tnf-α水平抑制90%,在th17条件下为94%。在th0刺激中,在0.001μm、0.01μm和0.1μm下,bms-986165使tnf-α表达分别增加21%、43%和61%。在最高浓度1μm下,bms-986165使tnf-α细胞因子表达抑制66%。在th17条件下,使用bms-986165可以观察到tnf-α产生的类似增加,在0.01μm和0.1μm下分别增加19%和77%。在th17刺激条件下,使用1μm bms-986165也抑制tnf-α(68%)。1μm阿普斯特与bms-986165的组合使tnf-α水平降低80-95%(th0)和93-96%(th17),其与单一药剂阿普斯特具有类似作用。这两种刺激条件对tnf-α水平具有类似作用,其中th0刺激对照为1380pg/ml和th17刺激对照为1436pg/ml。阿普斯特显著抑制tnf-α,在th0条件下和在th17条件下分别使其水平降低至148pg/ml和91pg/ml。在0.1μm下,在th17条件下,bms-986165使tnf-α水平显著增加。在这两种刺激条件下,使用1μm bms-986165显著抑制tnf-α水平。使用所有浓度并且在这两种刺激条件下,阿普斯特与bms-986165的组合显著抑制tnf-α水平。
[0292]
实施例5
[0293]
在抗cd3/抗cd28(th0)或抗cd3/抗cd28、il-1β、il-6和il-23(th17)刺激的全血中由阿普斯特和bms-986165产生的粒细胞-巨噬细胞集落刺激因子细胞因子
[0294]
粒细胞-巨噬细胞集落刺激因子(gm-csf)细胞因子表达结果见图9和图10。在th0条件下,阿普斯特使gm-csf细胞因子表达降低80%,在th17条件下降低66%。在这两种条件下,bms-986165增加gm-csf细胞因子表达。在th0条件下,在0.001μm、0.01μm、0.1μm和1μm下,bms-986165使gm-csf分别增加19%、36%、110%和31%。当将阿普斯特(0.1μm)添加至bms-986165中时,gm-csf细胞因子表达抑制60-80%。在th17刺激中,在0.01μm、0.1μm和1μm下,bms-986165使gm-csf分别增加41%、139%和104%。当添加阿普斯特时,gm-csf细胞因子表达抑制40-73%。在th0和th17刺激对照中,gm-csf的总pg/ml分别为409和637。在这两种刺激条件下,阿普斯特显著抑制gm-csf。在0.1μm(th0和th17两者)和1μm(th17)下,bms-986165显著增加gm-csf。使用所有浓度并且在这两种刺激条件下,阿普斯特与bms-986165的组合显著降低gm-csf细胞因子水平。
[0295]
实施例6
[0296]
在使用阿普斯特和tyk2i(bms-986165)处理的lps刺激的pbmc中产生的il-23
[0297]
针对在lps刺激条件下产生的细胞因子,对来自9名健康供体的pbmc进行分析(图11至图17)。图11和图12中的结果显示了il-23的水平。图11显示了在lps刺激的pbmc中阿普斯特减少il-23产生。将来自dmso处理的lps刺激的pbmc的il-23水平设定为100%(对照),细胞因子水平表示为与对照相比的归一化值(%)。与由阿普斯特导致的il-23水平降低不同的是,图12显示了在lps刺激的pbmc中bms-986165诱导il-23水平。在0.2μm-2μm范围内,与dmso组相比,bms-986165诱导il-23增加20倍。阿普斯特与bms-986165的组合能够减少bms-986165对il-23的诱导。随着阿普斯特水平的增加,il-23水平显著降低。使用anova和turkey多重比较进行统计分析,以将每种处理与单独的bms-986165进行比较。当bms-986165与低水平阿普斯特组合时,il-23显著减少,低水平阿普斯特的浓度为0.037μm(****p《0.001)。当与1μm阿普斯特组合时,il-23的诱导抑制90%,几乎达到与单独的阿普斯特相
986165对细胞因子影响的总结。协同作用以粗体表示,互补作用以下划线表示。
[0315]
在th0(抗cd3/抗cd28)或th17(抗cd3/抗cd28 il-1β、il-6和il-23)条件下,使用tyk2抑制剂bms-986165 /-阿普斯特作用48小时,在tru培养测定中检测了四名健康供体的全血。在th0和th17条件下,bms-986165抑制il-17a、il-17f和il-22细胞因子表达。当与阿普斯特组合时,进一步减少这些细胞因子,在th17条件下对il-17a、il-17f和il-22具有协同作用。bms-986165增加tnf-α和gm-csf产生,而阿普斯特抑制这些细胞因子的产生。当bms-986165与阿普斯特组合时,对tnf-α和gm-csf细胞因子表达具有互补作用,阿普斯特纠正了bms-986165的缺陷。这些组合作用提供了治疗对pde4的抑制具有应答的疾病或病症的方法,如用于治疗炎性疾病(例如,银屑病、银屑病关节炎和溃疡性结肠炎)。
[0316]
表5
[0317]
[0318][0319]
[0320]
下表6提供了在lps刺激的pbmc中阿普斯特和bms-986165对细胞因子影响的总结。向上箭头表示诱导,向下箭头表示细胞因子产生的减少。
[0321]
在lps刺激条件下,使用或不使用bms-986165或阿普斯特或这两者的组合,检测了来自9名健康供体的pbmc。单独使用bms-986165处理诱导il-23、il-12p40、il-12p70和tnf-α,而单独使用阿普斯特处理减少这些细胞因子。当bms-986165与阿普斯特组合时,与dmso对照组相比,这些细胞因子没有变化或有所减少。这些结果表明阿普斯特能够抑制由bms-986165诱导的这些细胞因子。阿普斯特和bms-986165两者减少ifn-γ和mcp-1产生,并且这两者的组合以协同作用进一步减少这两种细胞因子。bms-986165抑制th17谱系细胞因子,其提供了治疗其中th17细胞因子与发病机制有关的疾病的方法。然而,bms-986165对一些促炎性细胞因子(如il-23、il-12和tnf-α)的诱导可能在疾病治疗中是不利的。阿普斯特和bms-986165的组合作用(其中il-23、il-12和tnf-α降低)显示了将这两种化合物组合在治疗炎性疾病如银屑病、银屑病关节炎和溃疡性结肠方面的优势。
[0322]
表6
[0323][0324]
↑
诱导
[0325]
无变化
[0326]
↓
减少
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。