1.本发明属于药物应用的技术领域,具体涉及一种静灵口服液用于制备排铅以及抗衰老药物的应用。
背景技术:
2.铅是一种不可降解、具有神经毒性的重金属环境污染物,通过呼吸道或胃肠道吸收,在体内逐渐积累,对多种器官有毒性作用。铅对环境的污染日益严重,严重威胁到人类尤其是儿童的健康,暴露于胎儿和婴儿身上会不可逆转地影响神经系统的发育,导致智力下降、学习障碍。临床上,铅中毒患者常伴有神经退行性疾病、胃肠道疾病和心血管疾病等综合症状。研究证实,儿童期铅暴露可能是老年性神经退行性疾病(如阿尔茨海默病(ad)和帕金森病(pd))的一个潜在危险因素。动物实验还表明,急性和慢性铅暴露改变肾素-血管紧张素-醛固酮系统,诱发高血压和心血管疾病,还有研究报道,铅还可以改变血清、尿液和组织中其他一些具有重要生理功能的矿物质和微量元素的浓度。
3.目前排重金属药物包括传统的西药,如钙促排灵(cadtpa)、依地酸钙二钠(2naca-edta)等螯合剂,但其有肾毒性和使机体微量元素失调等作用。其作用机理主要是通过螯合体内的铅、锌、钙、锰、铁、铜等来促进他们的排泄。长期、大剂量使用一些药物容易引起体内电解质紊乱和必需微量元素失衡。研究表明,中药治疗疾病具有多成分、多靶点协同作用及副作用少等特点。因此,具有防治慢性铅等金属中毒的中药具有广阔的应用前景。
技术实现要素:
4.针对上述问题,本发明的目的在于提供一种静灵口服液的排铅以及抗氧化应用,所述静灵口服液用于铅中毒的预防和治疗以及用于制备抗衰老药物。
5.本发明的技术内容如下:
6.本发明提供了一种静灵口服液作为排铅药物的应用,用于铅中毒的预防和治疗方面,所述静灵口服液用于排铅;
7.所述静灵口服液的使用剂量为1.5~13.5μl/g;
8.优选地,所述静灵口服液的使用剂量为13.5μl/g。
9.本发明还提供了一种静灵口服液在制备抗衰老药物方面的应用,所述静灵口服液用于抗氧化;
10.所述静灵口服液的使用剂量为1.5~13.5μl/g;
11.优选地,所述静灵口服液的使用剂量为13.5μl/g。
12.本发明的有益效果如下:
13.本发明静灵口服液的排铅以及抗氧化应用,所述静灵口服液对铅、磷、钒、砷、硅、钙、钠、镁、磷、钾、铷、锶、铜等元素的体内浓度产生一定影响,其中高剂量静灵口服液具有排铅作用,可用于铅中毒的预防和治疗;此外,静灵口服液还具有抗氧化损伤作用,可用于制备抗衰老药物。
附图说明
14.图1为小鼠全血中各元素的浓度测定结果图;
15.图2为小鼠肝脏中各元素的浓度测定结果图;
16.图3为小鼠股骨中各元素的浓度测定结果图。
具体实施方式
17.以下通过具体的实施案例以及附图说明对本发明作进一步详细的描述,应理解这些实施例仅用于说明本发明而不用于限制本发明的保护范围,在阅读了本发明之后,本领域技术人员对本发明的各种等价形式的修改均落于本技术所附权利要求所限定。
18.若无特殊说明,本发明的所有原料和试剂均为常规市场的原料、试剂。
19.本发明所采用的静灵口服液来自于辽宁东方人药业有限公司,批号20190206;
20.所述静灵口服液中的成分包括熟地黄、山药、茯苓、牡丹皮、泽泻、远志、龙骨、女贞子、黄柏、知母(盐)、五味子、石菖蒲。
21.超纯水,由milli-q超纯水仪自制;
22.三水合乙酸铅(分析纯,上海阿拉丁有限公司);
23.依地酸二钠钙(2naca-edta,上海阿拉丁有限公司);
24.hno3(分析纯,国药集团化学试剂有限公司);
25.浓hno3(trace metal grade,cnw);
26.icp-ms元素分析70种元素混合标准溶液(inorganic ventures,agilent);
27.mda、sod试剂盒购自上海阿拉丁有限公司。
28.实施例1
29.1.实验分组与给药方案
30.本发明使用预防性高铅动物模型,将60只icr小鼠随机分为6组,每组10只,分别为空白对照组、模型对照组、实验组(静灵口服液)和阳性对照组(依地酸二钠钙,75mg/kg),其中实验组分为低、中、高三个剂量(1.5μl/g、4.5μl/g、13.5μl/g),分别为人体推荐量的3、9、27倍。各组给予受试样品30天。
31.实验期间,除空白对照组外,模型对照组、实验组和阳性对照组给予0.1%醋酸铅水溶液,各剂量组灌胃给予受试样品,阳性对照组腹腔注射给予依地酸二钠钙。
32.2.样品采集与保存
33.末次给予小鼠受试样品24h后取血并处死小鼠,取适量血、肝、股骨样品进行湿式消化,使用icp-ms测定铅浓度,并采用相应试剂盒对肝脏组织中mda,sod等抗氧化指标进行测定。
34.(1)全血样品采集与保存小鼠摘眼球取血,将血样收集于涂有1%肝素钠的2ml ep管中,置-80℃冰箱保存。
35.(2)组织样品采集与保存小鼠处死后,取双侧肝脏、股骨,用生理盐水清洗,将组织表面的血洗尽,于-80℃冰箱中冷冻保存。
36.3.样品处理
37.(1)全血样品处理取一定体积的血样100μl,加入1900μl 0.1%triton 1%hno3的稀释剂,充分混匀,4℃3000rpm离心15min,取上清液,用1%hno3按1:1(v/v)进一步稀释后
检测,稀释后的进样体系(样品)为1%hno3 0.05%triton x-100。
38.(2)组织样品处理称取肝组织、股骨100mg(湿重),分别加入浓hno
3 4ml,70℃水浴加热消解12h,消解至体系变清澈透明后,取0.5ml用超纯水稀释至6.8ml,稀释后的体系为5%hno3的。将稀释后的肝样品用3%hno3按1:4(v/v)稀释后进行检测;将稀释后的股骨样品用0.7%hno3按1:1(v/v)稀释后进行检测。
39.4.标准曲线制备
40.精密量取含铅的混合元素标准溶液适量,用5%hno3逐级稀释成一系列浓度的样品标准溶液。精密量取消解后的生物样品,将其与样品标准溶液等体积混合,制备质量控制(qc)样品,在选定的工作条件下,对样品进行测定。
41.表1icp-ms参数设置
[0042][0043]
5.结果统计分析
[0044]
空白对照组、模型对照组、实验组和阳性对照组间比较均采用one-way anova;
[0045]
p<0.05认为有统计学差异,所用计量数据均以mean
±
sd表示。
[0046]
表2小鼠全血样本中各元素浓度测定的方法学考察结果
[0047]
[0048][0049]
表3小鼠肝脏样本中各元素浓度测定的方法学考察结果
[0050]
[0051]
[0052][0053]
表4小鼠股骨样本中各元素浓度测定的方法学考察结果
[0054]
[0055]
[0056][0057]
由表2~表4可见,对全血、肝脏和股骨样本所建立的70种元素浓度测定的标准曲线均具有良好线性关系,线性系数r2均大于0.99;检测限和定量限结果表明,测定方法具有较好的灵敏度;qc样本中元素测定结果小于loq时,其重复性结果用n/a标示;除全血样本中pd、ad、au、hg、u,肝脏样本中i、au、ti,股骨样本中ga、zr、cs、dy、w以外,其他元素精密度良好(rsd均小于20%);这说明该构建方法精密度高,重现性好;需要说明的是,除碘和金外,其他60多种元素的回收率均高于80%;肝和骨样品中的碘元素因在4%hno3酸性基质中不稳定,导致其qc回收率低于40%,因此结果无参考意义;肝和骨样品中金元素加样回收率低于70%,其结果不具参考价值。
[0058]
6.小鼠组织中各元素的浓度测定
[0059]
如图1、图2、图3分别为小鼠全血、肝脏以及股骨中各元素的浓度测定结果图。
[0060]
图中,control为空白对照组(未给药小鼠);model为模型组;positive为阳性对照组(给予鱼油软胶囊);low,mid,high分别为低、中、高实验组(分别给予静灵口服液1.5μl/g,4.5μl/g,13.5μl/g);
[0061]
其中,
#
p<0.05,
##
p<0.01,
###
p<0.001,
####
p<0.0001vs control group;
[0062]
*p<0.05,**p<0.01,***p<0.001,****p<0.0001vs model group。
[0063]
小鼠全血样本中共检测出26种无机元素(铅、锂、钠、镁、磷、硫、氯、钾、钙、钒、锰、铁、钴、铜、锌、砷、硒、溴、铷、锶、碘、钼、锡、铯、铊、钨);
[0064]
如图1所示,其为小鼠全血中各元素浓度,与对照组(正常小鼠)相比,模型组中铅浓度呈显著上升(p<0.0001),而锂、镁、钒、锰、砷、锶6种元素的浓度均显著下降(钒下降幅度最大,约40%),其余19种元素无显著性变化(p>0.05);
[0065]
血铅浓度测定结果表明,给予0.1%醋酸铅饮用水造模后,与模型组相比,静灵口服液高剂量给药组和阳性对照组(依地酸钠钙)的血铅浓度均呈下降趋势(p>0.05,无统计学差异),低、中剂量给药组的血铅浓度无明显变化(p>0.05),而阳性对照组血铅浓度显著下降(p<0.01);
[0066]
与模型组相比,给予不同剂量的静灵口服液,低剂量组的血磷显著升高(p<0.05)且接近正常水平,低(p<0.0001)、中(p<0.05)、高(p<0.05)剂量组的血钒显著升高,高剂量组的血砷则显著下降(p<0.001),其余无显著性变化;
[0067]
与模型组相比,给予阳性对照药的小鼠血砷(p<0.001)、硒(p<0.05)浓度显著下降,锶(p<0.0001)、钙(p<0.01)浓度显著升高,钒浓度则无显著变化;
[0068]
与对照组相比,给予静灵口服液或阳性对照药后,低剂量组中钠(p<0.01)、铁(p<0.05)浓度显著下降,低(p<0.01)、中(p<0.05)剂量组氯浓度显著下降,中、高剂量组中锡浓度显著降低(p<0.01),低、中、高剂量组中钙和钨浓度显著性下降;阳性对照组中钾、铁、锡浓度显著下降(p<0.001),而铜浓度则显著升高(p<0.0001)。
[0069]
如图2所示,其为小鼠肝脏中各元素浓度,肝脏样本中共检测出21种无机元素。与
对照组相比,模型组中铅浓度显著上升(p<0.0001),而溴浓度显著下降(p<0.05);与模型组相比,静灵口服液中、高剂量给药组和阳性对照组的肝铅浓度均呈下降趋势(p>0.05,无显著性差异),低剂量给药组的肝铅浓度则呈上升趋势;
[0070]
与对照组相比,模型组中大部分元素浓度呈下降趋势,但无显著性差异(p>0.05);与模型组比较,给予静灵口服液和阳性药物后,低剂量组中硅浓度和钒浓度显著上升(p<0.05),阳性对照组中钠和锌浓度显著上升(p<0.05),其余则无显著性差异(p>0.05);与对照组比较,低剂量组中铁浓度显著上升(p<0.05),高剂量组中的砷浓度显著下降(p<0.05)。
[0071]
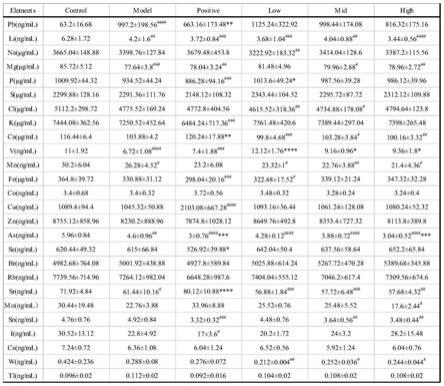
如图3所示,其为小鼠股骨中各元素浓度,股骨样本中共检测出17种无机元素。与对照组相比,模型组中骨铅(p<0.0001)、骨铜浓度显著上升(p<0.05);
[0072]
与模型组相比,静灵口服液中剂量给药组(p<0.05)、高剂量给药组(p<0.001)和阳性对照组(p<0.0001)的骨铅浓度均呈下降趋势,且随着给药剂量增加而降低;
[0073]
与模型组比较,给予静灵口服液后,高剂量组中钙浓度显著下降(p<0.05),中、高剂量组的钠、镁、磷、钾、铷、锶浓度均显著下降,低(p<0.05)、中(p<0.001)、高(p<0.001)剂量组的铜浓度显著下降。与模型组比较,阳性对照组中铁(p<0.01)、锌(p<0.05)、铜(p<0.01)浓度显著下降。
[0074]
结合图1~图3中铅浓度数据可见,模型组的血铅、骨铅、肝铅浓度均较空白组显著升高,说明小鼠铅中毒模型造模成功。给予高剂量静灵口服液,可使铅中毒小鼠的骨铅浓度显著降低,其排铅效果接近于阳性对照药,但对血铅和肝铅浓度的影响不显著。此外,静灵口服液对血中磷、钒、砷、钨,肝中硅、骨中钙、钠、镁、磷、钾、铷、锶、铜等元素的浓度具有显著影响(表3~4可见)。
[0075]
与模型组相比,给予低、中、高剂量的静灵口服液后,小鼠血、肝脏、骨骼中主要元素的浓度变化见表5。
[0076]
表5静灵口服液对铅中毒小鼠体内元素的影响
[0077]
[0078][0079]
实施例2
[0080]
采用实施例1所示的小鼠组别,观察静灵口服液对小鼠sod/mda的影响,结果如下表所示:
[0081]
表6静灵口服液对铅中毒小鼠体内元素的影响
[0082][0083]
如表6所示,与对照组相比,实验组(给予低、中、高剂量静灵口服液)小鼠肝脏sod活性呈升高趋势,肝脏mda活性呈降低趋势,其中高剂量组sod和mda的活性变化均有显著性差异(p<0.05),表明静灵口服液具有一定的抗氧化损伤作用,可用于制备抗衰老药物。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
