1.本发明属于核医学技术、药学领域,具体地,涉及核素标记的病毒受体结合域(rbd)放射性药物及其制备方法,与血管紧张素2转换酶2(ace2)的作用关系与初步应用。
背景技术:
2.最新研究表明ace2是新冠肺炎(covid-19)的重要感染靶标,受体结合域(receptor binding domain,rbd)是从sars-cov-2病毒中提取的,能与人体中的血管紧张素转化酶2(ace2)结合的一种重组刺突蛋白。
3.sars-ncov-2病毒感染的过程是复杂的,但具有精确的步骤,包括病毒和宿主细胞之间不同分子途径的许多相互作用。血管紧张素转换酶2(ace2)是羧肽酶ace的同系物,是肾素-血管紧张素系统(ras)的主要活性肽。赵等发现,通过s蛋白与人ace2的相互作用感染人呼吸道上皮细胞。后来,德国莱布尼茨灵长类研究所的markus hoffmann等人发表了一篇关于biorxiv的相关研究,表明新型冠状病毒是由与sars冠状病毒相同的受体,即ace2诱导的;和用于新型冠状病毒的细胞蛋白酶tmprss2。随着对ace2(新型冠状病毒侵入细胞的唯一入口)的了解,尽早开发靶向和抑制病毒进入的临床药物尤为重要。
4.刺突蛋白是冠状病毒最重要的包膜蛋白,包括s1和s2两个亚基。s1主要包含受体结合域(rbd),负责识别细胞受体。新型冠状病毒通过与ace2结合的刺突蛋白感染人类呼吸上皮细胞,并进一步感染人类肺组织和其他器官。ace2与从新型冠状病毒中提取的重组刺突蛋白rbd的特异性结合不仅是建立新型冠状病毒入侵细胞途径的关键,也是抑制ace2表达并引起其他疾病的过程。
5.rbd只与体内的ace2受体相结合,利用这一特性可将其作为探针,从分子、细胞和器官的不同水平上,检测ace2、分析ace2的结构与功能的关系,阐明其作用机理。利用核素标记单克隆抗体作为探针,能方便地确定与其结合的相应生物大分子(蛋白质、核酸、酶等)体内的位置和分布。
6.理论上rbd探针能够竞争性结合sars-ncov-2病毒在人体的代谢,作为一种竞争性代谢制剂。核素标记的rbd,特别是[
124
i]i及其同位素-rbd,有望实现病毒诊疗一体的特效。
技术实现要素:
[0007]
为解决现有技术中存在的技术问题,本发明的目的在于提供放射性核素标记的病毒受体结合域及其制备方法与应用。
[0008]
第一方面,本发明提供放射性核素标记的病毒受体结合域,所述放射性核素标记的病毒受体结合域由所述病毒受体结合域以n-溴代琥珀酰亚胺介导、或者与双功能螯合剂偶联后,进行放射性核素标记得到;每1mg病毒受体结合域上标记的放射性核素为140-220mbq。
[0009]
本发明中,所述放射性核素优选为碘的放射性同位素、
64
cu或
89
zr,所述碘的放射性同位素优选为
124
i、
123
i、
125
i或
131
i。
[0010]
124
i(t1/2=4.2d)、
64
cu(t1/2=12.7h)、
89
zr(t1/2=78.4h)是新型固体靶pet核素。与目前临床常用的pet正电子核素
18
f(t1/2=110min)和
11
c(t1/2=20.4min)等相比,
124
i、
64
cu、
89
zr具有相对较长的半衰期,可进行长时间的显像研究,并且更加方便核素的运输,且肝脏摄取较低,有利于肝脏病灶的检出,具有广阔的临床应用前景。
[0011]
本发明中,所述双功能螯合剂包括但不限于dota、nota或dfo(deferoxamine,去铁胺)。
[0012]
本发明所述病毒受体结合域特别指ace2靶向分子sars-cov-2rbd。本文中术语“rbd”即指sars-cov-2rbd。
[0013]
sars-cov-2rbd是从sars-cov-2的s蛋白上提取出来的受体结合域,能与宿主细胞上的ace2受体结合。本发明以sars-cov-2rbd为例,使用下一代核素
124
i、
64
cu或
89
zr标记sars-cov-2rbd。本发明发现,采用n-溴代琥珀酰亚胺(nbs)介导、或者与双功能螯合剂nota或dfo偶联后,进行rbd的
124
i、
64
cu或
89
zr核素标记,能够显著提高标记率且同时降低核素标记对前体活性的影响,能够同时保证较高的标记率、放化学纯度、功能活性以及稳定性。动物实验结果显示其在ace2高表达肿瘤中有明显摄取,表明核素标记的pd-1靶向单抗可作为一种特异性靶向ace2的探针,用于检测体内ace2的分布显像剂。
[0014]
第二方面,本发明提供所述放射性核素标记的病毒受体结合域在制备靶向ace2的pet/ct分子诊断显像剂中的应用。
[0015]
第三方面,本发明提供一种靶向ace2的病毒感染部位的诊断或治疗放射性药物,包含所述放射性核素标记的病毒受体结合域。所述药物可以靶向ace2且无创评价其在体内的分布,可作为pet/ct分子诊断显像剂或ace2靶向药物。
[0016]
第四方面,本发明提供所述放射性核素标记的病毒受体结合域的制备方法,所述制备方法可根据采用的核素不同分为两个并列技术方案。
[0017]
当采用碘的放射性同位素(如
124
i)标记时,可利用nbs方法实现
124
i对病毒受体结合域分子结构中苯环羟基的邻对位进行标记。具体地,所述制备方法包括:将病毒受体结合域与碘的放射性同位素的盐(如
124
i盐)、n-溴代琥珀酰亚胺和反应缓冲液混合进行标记反应;所述病毒受体结合域、碘的放射性同位素的盐和n-溴代琥珀酰亚胺的用量比为(0.1-0.5mg):(3
×
10
7-1.5
×
108bq):(20-100μg)。
[0018]
对于其他碘的放射性同位素,如
123
i、
125
i、或
131
i,所用的盐相应为
123
i盐、
125
i盐、或
131
i盐。
[0019]
根据本发明,优选地,所述反应缓冲液为0.05-0.2m、ph7-7.5的pb缓冲液。
[0020]
根据本发明,优选地,所述反应缓冲液占反应体系总体积的30%-75%。
[0021]
根据本发明一种优选实施方式,所述标记反应为在常温反应0.8-1.2min,以8-12%的人血清白蛋白终止反应。例如,在常温反应1min,以10%的人血清白蛋白终止反应。
[0022]
作为本发明的优选方案,所述制备方法包括:每0.5-1.0ml的60-90kbq/μl的na
124
i溶液中加入0.5-1.0ml、0.1m ph 7.2的pb缓冲液、0.1-0.5mg病毒受体结合域和20-100μg n-溴代琥珀酰亚胺,于常温反应1min,向反应体系中加入0.05-0.2ml、10%人血清白蛋白终止反应;所得反应液用pd-10柱纯化后,得到
124
i标记的病毒受体结合域。
[0023]
作为并列技术方案,当以
64
cu或
89
zr标记病毒受体结合域时,通过双功能螯合剂(如nota或dfo)分别实现
64
cu或
89
zr标记病毒受体结合域。
[0024]
具体地,所述制备方法包括:
[0025]
(1)将病毒受体结合域与双功能螯合剂混合反应得到标记前体,所述病毒受体结合域与双功能螯合剂的用量摩尔比为1:(5-10);
[0026]
(2)采用
64
cu或
89
zr对所述标记前体进行标记反应,所述标记前体与
64
cu或
89
zr的用量比为(0.1-0.5mg):(6
×
10
7-3
×
108bq)。
[0027]
优选地,步骤(1)中,以去离子化处理的0.05-0.1m碳酸氢钠溶液调节反应体系的ph值至8.0-8.5,于37℃条件下反应0.5-2h。
[0028]
步骤(2)中,将所述标记前体加入至0.05-0.15m、ph 5.0-5.5的醋酸钠溶液中,再加入
64
cu或
89
zr溶液,调整ph值至7.0-7.2,于37℃孵育30-60min。
[0029]
作为本发明的优选方案,所述制备方法包括:
[0030]
(1)向浓度为2-5mg/ml的病毒受体结合域溶液中加入相当于病毒受体结合域6倍摩尔当量的dfo,以去离子化处理的0.1m碳酸氢钠溶液调节反应体系的ph值为8.5;37℃条件下反应0.5-2h,得到标记前体dfo-病毒受体结合域;
[0031]
(2)取0.1-0.5mg标记前体,加入0.1-1.0ml、0.1m ph 5.5的醋酸钠溶液中,然后加入60-300mbq新鲜配制的
64
cu或
89
zr溶液,调整ph值到7.0,然后控制温度为37℃,孵育1h;所得反应液经pd-10柱分离纯化,得到
64
cu或
89
zr标记的病毒受体结合域。
[0032]
本发明所述的制备方法中,当标记率大于90%,使用pd-10柱纯化后,目标产物的放射性化学纯度大于99%。
[0033]
在进行pd-10柱分离纯化时,pd-10柱先用0.01m ph 7.4的pbs缓冲液平衡柱体,每次加5ml,重力流速流干,重复5次;然后再用0.01m ph7.4的pbs缓冲液纯化获得核素标记的病毒受体结合域。
[0034]
本发明的有益效果在于:
[0035]
本发明提供的放射性核素标记的病毒受体结合域具有较高的标记率和放射性化学纯度,并且具有较好的体外稳定性,可作为新型pet分子探针;
124
i/
64
cu/
89
zr标记后对前体的活性影响较小,标记后的探针对ace2具有较高的亲和力、特异性和功能活性,能够与细胞表面的ace2特异性结合;显像效果好,ace2阳性肿瘤具有较高的摄取;肝脏、肠道、肾脏有较高摄取,与ace2在体内的分布有一定关系,可用于实时、无创地监测全身的ace2表达情况。核素标记的rbd探针能够竞争性结合sars-ncov-2病毒在人体的代谢,有望实现病毒诊疗一体的特效。
[0036]
本发明的其它特征和优点将在随后具体实施方式部分予以详细说明。
附图说明
[0037]
通过结合附图对本发明示例性实施方式进行更详细的描述,本发明的上述以及其它目的、特征和优势将变得更加明显。
[0038]
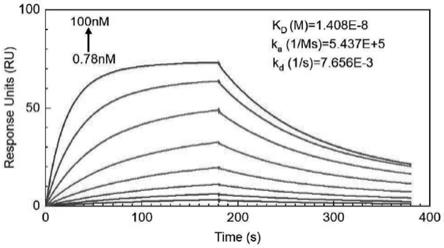
图1示出了采用spr研究rbd体外与hace2亲和力的结果。
[0039]
图2示出了小鼠尾静脉注射
124
i-rbd后的micro-pet/ct成像及分析。a:尾静脉注射后0.5h、2h、24h和60h的正常小鼠中
124
i-rbd的micro-pet/ct成像。b:不同时间点重要器官的suv值。c:
124
i-rbd在正常小鼠中的生物分布。
[0040]
图3示出了
124
i-rbd(a)及
124
i(b)在大鼠体内的代谢分析。
[0041]
图4示出了
124
i-rbd(a)及
124
i(b)在大鼠的micro-pet显像及基于roi的代谢分析对比(b-d),以及大鼠肺部组织的ace2表达分析(e)。
具体实施方式
[0042]
下面将更详细地描述本发明的优选实施方式。虽然以下描述了本发明的优选实施方式,然而应该理解,可以以各种形式实现本发明而不应被这里阐述的实施方式所限制。
[0043]
以下实施例中,所有试剂均从商业供应商处获得,无需任何进一步纯化即可使用。磷酸盐缓冲液(pbs,0.01m,ph 7.4)购自中国上海阿拉丁。重组sars-cov-2刺突rbd-his-avi(宿主细胞受体结合域-rbd)与n端his标签(货号#bp003052)和人ace2-his-avi(货号#bp003061)购自syd labs,美国马萨诸塞州波士顿。n-溴代琥珀酰亚胺(nbs,0.1m)购自sigma-aldrich chemie gmbh,steinheim,germany(catalog#b9252)。人血清白蛋白(10%)购自csl behring ag,bern,switzerland(catalog#b14200811350)。pd-10色谱柱来自英国白金汉郡的ge healthcare(目录号17001651)。同位素
124
i由实验室利用
124
te(p,n)
124
i核反应自产,活度浓度为370kbq/μl(huang hf,zhu h,li gh,xie q,yang xt,xu xx,et al.construction of anti-hpd-l1 hcab nb6 and in situ124i labeling for noninvasive detection of pd-l1 expression in human bone sarcoma.bioconjug chem.2019;30(10):2614-2623.)。
[0044]
放射性核素标记的病毒受体结合域
124
i-rbd的制备
[0045]
向0.5ml的60-90kbq/μl的na
124
i溶液中加入0.5ml、0.1m ph 7.2的pb缓冲液、0.1mg病毒受体结合域rbd和20μg n-溴代琥珀酰亚胺,于常温反应1min,向反应体系中加入0.1ml、10%人血清白蛋白终止反应;所得反应液用pd-10柱纯化后,得到
124
i标记的病毒受体结合域
124
i-rbd。放射化学产率为83.9%
±
4.6%(n=10,非衰变校正)。radio-tlc分析表明
124
i-rbd的放射化学纯度(rcp)超过99%。比活在25.3和28.9gbq/nmol之间。在盐水(室温,120小时)或5%人血清白蛋白(室温,120小时)中孵育后,在放射性tlc色谱图上观察到单峰(超过99%rch),表明
124
i-rbd在体外稳定至少5天。
[0046]
124
i-rbd的生物学评价
[0047]
通过表面等离子体共振(spr)结合研究rbd与人ace2受体的结合能力。该方法可用于确定结合特异性,以及配体与蛋白质受体相互作用的结合率和解离率。ace2固定在传感器芯片上,肽通过传感器表面。相互作用的亲和力取决于平衡时的结合水平。应用亲和模型来拟合数据并计算解离常数,kd=14.08nm。结果表明
124
i-rbd在体外与hace2具有高亲和力(图1)。
[0048]
124
i-rbd和ace2 mapping的micro pet成像
[0049]
正常小鼠在静脉注射3.7mbq 124
i-rbd后0.5h、2h、24h、60h的代表性pet成像如图2所示。观察到
124
i-rbd的典型肠肝代谢和胃吸收。如图2所示,
124
i-rbd主要在肝脏、肾脏和血液中积累,在感染后1h的吸收值分别为14.76
±
3.85、14.54
±
3.16和12.22
±
2.58id%/g,随后经肺、心、脾、大肠。在感染后24h,它从大多数吸收率低的器官中迅速清除。
[0050]
为了研究rbd在肺中的滞留,采用肺内经支气管给药的方法,注射体积约50μl的0.927mbq 124
i-rbd。micro-pet成像结果如图3所示。
[0051]
通过气管内和肺内注射给正常小鼠注射
124
i-rbd后,对正常小鼠进行pet/ct成像,
结果显示肺、胃和甲状腺的高摄取(参见图3的a)。通过勾勒感兴趣的目标区域测量的每个器官的suv如图3的c所示。4h后,肺和肾的suvmean分别为4.9
±
0.49和0.21
±
0.06,肺与肾的比率为23.73。24h后,肺和肾的suvmean分别为0.53
±
0.04和0.03
±
0.01,肺肾比为19.88。通过气管内和肺内注射在正常小鼠中注射相同剂量的na
124
i(参见图3的b、d),4h肺摄取较低,肺和肾suvmean分别为0.16
±
0.01和0.29
±
0.10,肺肾比为0.55。即使在1h时,肺中
124
i的摄取也相对低于
124
i-rbd(参见图3的b、d)。注射na
124
i后肺中的suv为0.4
±
0.04,而注射
124
i-rbd后肺中的suv为6.70
±
0.33。
[0052]
图4示出了
124
i-rbd(a)及
124
i(b)在大鼠的micro-pet显像及基于roi的代谢分析对比(b-d),以及大鼠肺部组织的ace2表达分析(e)。根据图4的a,肺内注射
124
i-rbd和na
124
i后4h和24h肺摄取的pet图像。可以发现
124
i-rbd在肺脏器官中长期驻留,注射后4h和24h可见肺内浓度,而注射后1小时na
124
i在肺内几乎消失。同时,通过免疫组化证实ace2存在于小鼠的肺中(参见图4的e),则可以证明由于rbd靶向肺中的ace2导致
124
i-rbd长期驻留。
[0053]
碘及其放射性同位素标记rbd在体辐射剂量
[0054]
根据
124
i-rbd在balb/c小鼠的生物分布数据,利用olinda/exm 2.0程序估算了
124
i-rbd在成年男性模型中的人类器官辐射剂量。假设碘及其放射性同位素(
124
i、
123
i、
125
i或
131
i)标记rbd在小鼠体内有相似的分布,对
123/125/131
i-rbd的辐射剂量进行了估算,结果如表1所示。
[0055]
其中,成骨细胞是辐射剂量最高的部分,值为0.242mgy/mbq,其次是红骨髓、脾脏、结肠和小肠。整体有效剂量是0.0642msv/mbq,表明一个人类注射74.8mbq 124
i-rbd后,其吸收的有效剂量是4.80msv,在合理范围内。
123
i-rbd、
125
i-rbd和
131
i-rbd显示出具有类似的器官辐射损伤风险,但有效剂量较低,分别为0.0106、0.00564and 0.0379msv/mbq.
[0056]
表1碘及其放射性同位素标记rbd在体辐射剂量估算
[0057]
[0058][0059]
本发明观察了
124
i-rbd在哺乳动物体内的生物学分布,评价了
124
i-rbd对ace2在人体表达的检测能力,利用
124
i-rbd pet观察治疗过程中ace2表达的变化。新探针在一定程度上模拟了sars-cov-2病毒在人体内与ace2的结合。通过放射性标记rbd探测体内ace2表达,可用于非侵入性ace2映射,提示用碘同位素标记的rbd进行人-ace2靶向监测是可行的,为放射治疗提供了临床前经验。同时利用更换碘的其它同位素,能够实现rbd探针对ace2高表达部位的一体化诊疗。
[0060]
以上已经描述了本发明的各实施例,上述说明是示例性的,并非穷尽性的,并且也不限于所披露的各实施例。在不偏离所说明的各实施例的范围和精神的情况下,对于本技术领域的普通技术人员来说许多修改和变更都是显而易见的。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。