一种靶向cd47与pd-l1双功能融合蛋白的制剂
技术领域
1.本发明属于生物医药领域,具体涉及一种靶向cd47与pd-l1的双功能融合蛋白的制剂。
背景技术:
2.癌细胞的“免疫逃逸”被认为是肿瘤发生、发展和抗药的主要机制。肿瘤一般通过直接或间接抑制t细胞的信号来保护自己躲过免疫系统的清除。肿瘤的免疫检查点疗法(immune chenkpoint therapy)是一类通过共抑制或共刺激信号等一系列途径调节t细胞活性来提高抗肿瘤免疫应答的治疗方法。
3.免疫检查点通过免疫应答过程中的共刺激和共抑制分子,发出“打开”或“关闭”免疫应答的信号,在调节t细胞应答的幅值与持续时间和维持自身耐受方面具有重要作用,防止损伤自身组织。目前已发现的免疫检查点分子有pd-1/pd-l1、cd47/sirpα、ctla-4/cd80/ cd86等。
4.由于pd-1/pd-l1信号通路仅作用于t细胞的效应阶段,抗pd-1/pd-l1药物效果的发挥需要肿瘤抗原的递呈,临床上对于低免疫原性的肿瘤往往治疗无效(70%),需要与化疗、放疗、单抗药物连用;靶向cd47的抗体具有激活巨噬细胞、增强t细胞抗原递呈等功能,与抗pd-1/pd-l1在功能上互补。然而cd47的表达并非严格意义上的肿瘤特异性,在健康的血红细胞表面也有表达,而且肿瘤细胞表面cd47表达仅仅高于正常细胞3.3倍,因此体内使用cd47抗体往往会引起贫血等不良反应。为了减轻副反应,与cd47高亲和力的sirpα突变体只能以免疫增强剂的形式,以无fc单体形式与其他抗体联用进行治疗。
5.靶向cd47与pd-l1的双功能融合蛋白(专利申请号cn201610372954.4)是一种人工设计的具有新型结构的重组蛋白,由二硫键链接的3条肽链组成,分别是sirpα(cd47配体)突变体-fc融合肽链和重组抗pd-l1抗体轻链、重链。该融合蛋白既能与pd-l1结合、阻断pd-1/pd-l1信号通路,又能与cd47结合、阻断cd47/sirpα信号通路,能解决现有免疫检查点抗体药在疗效和安全性上不足的问题。然而由于该融合蛋白具有独特的氨基酸序列(一级结构)和高级结构,为了提高蛋白的稳定性、延长保质期,需要有针对性的开发一种制剂配方和/或制剂方法。
技术实现要素:
6.为了提高靶向cd47与pd-l1的双功能融合蛋白(专利申请号cn201610372954.4,命名为iab)在储存中的稳定性、延长保质期,本发明提供了一种制剂配方,技术方案如下:所述的iab蛋白由具有seq id no: 1(sirpα突变体-fc融合肽链)、seq id no:2(重组抗pd-l1单克隆抗体轻链)、seq id no:3(重组抗pd-l1单克隆抗体重链)所示的氨基酸序列的三条肽链组成,三条肽链之间通过二硫键链接。
7.所述的制剂配方包括以下剂量或浓度的iab蛋白和辅料:
iab,100
±
10 mg/ml;一水合磷酸二氢钠,1.41
±
0.14 mg/ml;七水合磷酸氢二钠,2.63
±
0.26 mg/ml;精氨酸,10.0
±
1.0 mg/ml;聚山梨酯80(peg80),0.50
±
0.05 mg/ml蔗糖,50
±
5 mg/ml;配好后溶液的ph值为6.8
±
0.3。
8.更具体而言,所述的制剂配方包括以下剂量或浓度的iab蛋白和辅料:iab,100 mg/ml;一水合磷酸二氢钠,1.41 mg/ml;七水合磷酸氢二钠,2.63 mg/ml;精氨酸,10 mg/ml;peg80,0.50 mg/ml蔗糖,50 mg/ml;配好后溶液的ph值为6.8。
9.所使用的溶剂是水,应达到注射用水的质量标准。
10.所述的辅料磷酸二氢钠、磷酸氢二钠、精氨酸、聚山梨酯80、蔗糖等的生产过程和质量管理应符合行政机构对药用辅料的要求,达到中国药典规定的质量标准。
11.所述的制剂配方适用于静脉注射的给药方式。
12.本发明的有益效果是,能够显著提高iab蛋白在20~100 mg/ml浓度下的储存的稳定性,减少储存过程中聚集体和电荷异质体的产生。
附图说明
13.图1 储存后的iab重组蛋白的pd-l1结合能力的检测结果;图2 储存后的iab重组蛋白的cd47结合能力的检测结果。
具体实施方式
14.实施例1、重组抗egfr全人源单抗前体iab的制剂配方将重组抗egfr全人源单抗前体iab(专利申请号cn201410724477.4)按表1所示配方溶解于水溶液中,形成注射液制剂,用于静脉注射。
15.表1 iab的制剂配方
上述制剂配方中的磷酸盐浓度换算成摩尔浓度后是20 mmol/l。
16.该制剂配方的实现方法:将含有iab的细胞培养液通过一系列层析、过滤等步骤进行纯化、除病毒后,将获得的含有目的蛋白的溶液浓缩,然后透析、稀释,配制入按照上述配方配置的缓冲液中。
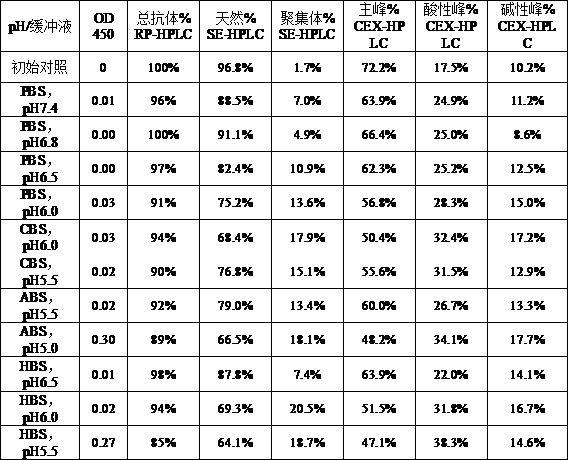
17.实施例2、不同缓冲液和ph对目的蛋白稳定性的影响将iab蛋白分别以20 mg/ml的浓度溶解于不同ph的20 mm磷酸盐缓冲液(pbs)、柠檬酸盐缓冲液(cbs)、醋酸缓冲液(abs)、组氨酸缓冲液(hbs)中,在45℃放置28天,然后分别用反相层析(rp-hplc)、分子排阻层析(se-hplc)、阳离子交换层析(cex-hplc)分析溶液中的蛋白分布情况,并以未经45℃温育的初始样品作为对照。层析方法如下:(1)反相层析用waters uplc系统和waters c4层析柱(2.1 x 50 mm, 1.7
ꢀµ
m)进行反相色谱,流动相为含0.1%甲酸、梯度浓度从25%到35%的含水乙腈,流速0.4 ml/min,温度为60℃,检测波长280 nm。具有最大面积和高度的峰被确定为主峰。
18.(2)分子排阻层析用waters uplc系统和waters acquity uplc protein beh200 sec 4.6
×ꢀ
150 mm排阻层析柱进行分子排阻色谱,流动相采用0.2 mol/l磷酸盐缓冲液(加15%异丙醇),流速0.5 ml/min,上样量10 μl浓度为1.0 mg/ml的蛋白样品,检测波长280 nm。具有最大面积和高度的峰被确定为天然单体峰,在其之前检测到的峰为聚集体峰。使用以下公式计算目标峰的峰面积比:目标峰的峰面积比(%)=100
×
(目标峰的峰面积)/(目标峰的峰面积 其他峰总峰面积)(3)离子交换层析用waters uplc系统和mabpac scx-10(4 mm
×
250 mm)分析柱进行阳离子交换色谱,流动相a为ph6.0的20 mmol/l磷酸盐缓冲液,流动相b为含有100 mmol/l氯化钠的ph6.0的20 mmol/l磷酸盐缓冲液,流速1.0 ml/min,柱温40℃,检测波长280 nm。具有最大面积和高度的峰被确定为主峰,并且在主峰之后检测到的峰统称为酸性峰,之前的峰为碱性峰。计算所有峰的峰面积,并使用以下公式计算目标峰的峰面积比:目标峰的峰面积比(%)=100
×
(目标峰的峰面积)/(目标峰的峰面积 其他峰的总峰面积)。
19.层析分析结果列示在表2。
20.表2 不同缓冲液对iab重组蛋白稳定性的影响
结果表明,从聚集体和电荷异质体形成情况来看,使用ph6.8的20 mm磷酸盐缓冲液(pbs)最有利于iab重组蛋白的稳定,但是效果仍不够理想。
21.为了进一步优化缓冲液的浓度,分别采用20 mm、10 mm、5 mm的ph6.8磷酸盐缓冲液重复上述分析步骤,并添加10 mg/ml精氨酸,分析结果见表3。
22.表3 不同磷酸盐缓冲液对iab重组蛋白稳定性的影响结果表明,添加10 mg/ml精氨酸的20 mm磷酸盐缓冲液有最佳的结果,而10 mm、5 mm浓度的结果显著降低,因此选择添加10 mg/ml精氨酸的20 mm的ph6.8磷酸盐缓冲液作为iab重组蛋白制剂的缓冲液。
23.实施例3、不同表面活性剂对目的蛋白稳定性的影响将iab蛋白分别以100 mg/ml的浓度溶解于添加不同浓度聚山梨酯20(peg20)、聚山梨酯80(peg80)以及10 mg/ml精氨酸的20 mm的ph6.8磷酸盐缓冲液中,在45℃放置28天,然后
分别用反相层析(rp-hplc)、分子排阻层析(se-hplc)、阳离子交换层析(cex-hplc)分析溶液中的蛋白分布情况,并分别以未经45℃温育的初始样品和未添加聚山梨酯的样品作为对照,分析结果列示在表4。
24.表4 不同表面活性剂对iab重组蛋白稳定性的影响
※ꢀ
上表中peg20、peg80的浓度单位为mg/ml。
25.结果表明添加非离子型表面活性剂peg80有助于增强iab在100 mg/ml浓度下的稳定性,其中0.5 mg/ml聚山梨酯80(peg80)的添加量取得了最好的结果。
26.实施例4、不同糖类对目的蛋白稳定性的影响将iab蛋白分别以100 mg/ml的浓度溶解于添加不同浓度糖类和0.5 mg/ml聚山梨酯80、10 mg/ml精氨酸的20 mm ph6.8磷酸盐缓冲液中,在45℃放置28天,然后分别用反相层析(rp-hplc)、分子排阻层析(se-hplc)、阳离子交换层析(cex-hplc)分析溶液中的蛋白分布情况,并分别以未经45℃温育的初始样品和未添加糖类的样品作为对照,分析结果列示在表5。
27.表5 不同糖类对iab重组蛋白稳定性的影响
结果表明添加蔗糖对iab的稳定性改善最强,10%、5%浓度的蔗糖效果接近,因此选择5%(相当于50 mg/ml)蔗糖作为制剂组分。
28.实施例5、iab重组蛋白制剂在不同储存温度稳定性的检测将iab蛋白按照实施例1所述的配方和方法制成制剂,然后在-80℃、-20℃、4℃、25℃的条件下分别储存6个月,取出后分别用反相层析(rp-hplc)、分子排阻层析(se-hplc)、阳离子交换层析(cex-hplc)分析溶液中的蛋白分布情况,分析结果列示在表6。
29.表6 iab重组蛋白制剂在不同储存温度稳定性的检测结果表明该制剂在-80℃、-20℃、4℃的条件下储存6个月分子的分布基本无变化,se-hplc分析蛋白纯度仍在95%以上,聚集体、酸性峰、碱性峰比例无明显变化。但在25℃条件下储存6个月分子的分布略有值得关注的变化。
30.实施例6、酶联免疫法检测储存后的iab重组蛋白的靶向结合能力采用elisa的方法检测实施例5中在-80℃、-20℃、4℃、25℃的条件下储存6个月的iab制剂对pd-l1和cd47的亲和性。
31.elisa检测方法如下:在 96 孔酶标板上包被溶于 pbs(磷酸盐缓冲液,ph=6.80)中的重组人cd47(购自sigma-aldrich公司,货号srp6392)或重组人pd-l1(购自sigma-aldrich公司,货号srp6434),重组蛋白包被浓度为500 ng/ml,使用含有10%脱脂奶粉的pbs进行封闭。在室温
下,使用经梯度稀释的待检抗体孵育1小时。接下来,在37℃条件下使用了辣根过氧化物酶(hrp)偶联的抗人fc 抗体(1:5000, 西格玛)孵育 30 分钟,最后使用了tmb(四甲基联苯胺)进行了显色,450nm波长下读数。以od450对抗体浓度的对数作图,结果见图1(pd-l1亲和性)、图2(cd47亲和性),并计算各个样品的ec50(半数效应浓度),计算结果见表7。
32.表7 elisa法检测不同温度下保存的iab样品的ec50值(ng/ml)样品储存条件pd-l1(图1)cd47(图2)iab-80℃7.51410.202iab-20℃7.4419.913iab4℃7.28910.616iab25℃8.26916.256通过分析表明,在使用实施例1所列配方后,在-80℃、-20℃、4℃条件下储存6个月的iab样品很好的保持了对pd-l1和cd47亲和的生物学活性。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。