1.本发明涉及疫苗技术领域,特别是涉及一种裂解疫苗的裂解效果检测,具体涉及一种裂解疫苗裂解效果的检测方法。
背景技术:
2.流感病毒裂解疫苗是用世界卫生组织(who)推荐的并经国家药品管理部门批准的流感病毒株接种健康鸡胚,经培养、收获,灭活、纯化、裂解制成的生物制品。目前流感病毒裂解疫苗已广泛应用于预防流感病毒引起的流行性感冒。
3.流感病毒属于正黏病毒科,具有容易聚合成团的性质。在制备流感疫苗过程中,需要进行病毒裂解处理。一般在现在的流感病毒裂解疫苗生产过程中,常使用去氧胆酸钠、tritonx100、trintonn101、乙醚和聚山梨酯80等裂解剂裂解病毒。病毒的裂解程度或者说裂解效果(即已裂解病毒占病毒总量的百分数)会直接影响疫苗的免疫原性和安全性。例如如果裂解不足,会有部分病毒保持完整形态,就会影响疫苗的使用安全性;病毒裂解过度,血凝素形态被破坏,就会影响疫苗的免疫原性。因此,在生产过程中以及产品质检时,都需要对裂解疫苗的裂解效果进行检测评价,为流感病毒裂解疫苗的生产和质量控制提供科学依据。
4.目前通用的流感病毒裂解疫苗裂解效果的评价手段是电镜观察法,采用负染技术进行病毒形态电镜观察,即用重金属染液里的金属原子作为电子“颜料”,把密度较低的生物标本(病毒)包绕而形成具有明显反差的方法。电镜中的电子束能够通过低电子密度的病毒颗粒却无法通过金属粒子背景,从而使病毒颗粒呈现出明亮清晰的结构,即负反差。因此通过透射电子显微镜即可观察病毒形态,从而对裂解效果进行判断。实际应用中通常会选取多个视野,观察不同视野中完整病毒的数量,综合评价病毒的裂解效果。电镜观察法虽有可直接观察病毒颗粒微观结构和高分辨率的优点,但也存在取样量小和视野选择受限等问题,导致检测结果不够准确且无法定量评价病毒的裂解效果。因此,有必要开发一种新的裂解疫苗裂解效果的检测方法,以期能准确评价病毒的裂解效果。
技术实现要素:
5.本发明主要解决的技术问题是提供一种裂解疫苗裂解效果的检测方法,可以定量评价裂解疫苗中病毒的裂解程度,提高裂解效果检测数据的可靠性。
6.具体地,本发明提供了一种裂解疫苗裂解效果的检测方法,采用聚合物分析系统(aggregates sizer)进行检测,检测条件包括:采用高浓度池测定装置sald-hc75s,采集软件为wing sald bio-7500。
7.作为一种优选的实施方案,所述的检测方法,包括:采用聚合物分析系统对不同裂解程度的系列工作液进行检测,分别得到不同裂解程度的工作液中不同粒径病毒颗粒的分布丰度,之后进一步得到不同裂解程度的工作液中病毒颗粒的累积分布丰度,以病毒颗粒的累积分布丰度为纵坐标,裂解程度为横坐标,进行线性回归,求得标准曲线方程和相关系
数;以及,
8.采用聚合物分析系统对待测样本进行检测,得到待测样本中病毒颗粒的累积分布丰度,再根据标准工作曲线计算得到所测样本的裂解程度。
9.作为一种优选的实施方案,所述系列工作液的裂解程度在60%~100%之间。当裂解程度为50%或者小于50%时,检测时会出现多重散射,信号偏移,造成检测结果不准确,因此本发明方法标准曲线裂解程度的检测下限为60%。
10.作为一种优选的实施方案,所述不同裂解程度的系列工作液的裂解程度分别为60%、70%、80%、90%、100%。
11.作为一种优选的实施方案,所述检测条件还包括:样品量为0.1~0.2ml,优选0.125ml。
12.作为一种优选的实施方案,所述不同裂解程度的系列工作液由病毒颗粒完全裂解的裂解病毒液和病毒颗粒未发生裂解的病毒液混合配制而成;进一步优选地,分别取0.6ml、0.7ml、0.8ml、0.9ml和1.0ml病毒颗粒完全裂解的裂解病毒液于各离心管中,之后依次分别加入0.4ml、0.3ml、0.2ml、0.1ml及0ml病毒颗粒未发生裂解的病毒液,配制成裂解程度分别是60%、70%、80%、90%和100%的系列工作液。
13.作为一种优选的实施方案,所述病毒颗粒完全裂解的裂解病毒液由裂解疫苗生产过程中的裂解液膜滤得到。
14.作为一种优选的实施方案,所述病毒颗粒未发生裂解的病毒液为裂解疫苗生产过程中的裂解前纯化液。
15.作为一种优选的实施方案,本发明所述的检测方法,检测的所述裂解疫苗为流感病毒裂解疫苗。
16.本发明还提供了所述的检测方法在检测裂解疫苗裂解程度中的应用。
17.优选地,所述检测方法在检测流感病毒裂解疫苗裂解程度中的应用。
18.本发明提供的裂解疫苗裂解效果的检测方法,采用聚合物分析系统(aggregates sizer)进行检测。aggregates sizer是一种高稳定、高灵敏和自动化程度高的分析工具,以半导体激光为光源,依据光的散射与衍射现象建立数学模型,散射与衍射的光能角度只与颗粒粒径有关。当检测对象为颗粒群时,各不同粒径颗粒的多少决定了对应各特定角获得的光能量大小,各特定角光能量在总光能量中所占比例可以反应各颗粒的分布丰度。aggregates sizer可以检测7nm~800μm范围内粒子的粒径范围,并且可以定量检测40nm~20μm范围内生物制药颗粒物的浓度,并可检测颗粒物的形成过程及浓度变化。
19.本发明将聚合物分析系统(aggregates sizer)首次用于裂解疫苗裂解效果的检测,通过制备病毒颗粒完全裂解的裂解病毒液标准品和病毒颗粒未发生裂解的病毒液标准品,并将二者按一定配比混合,配制得到具有不同裂解程度的系列工作液,之后对其分别进行检测,得到了标准工作曲线,可以用于裂解疫苗裂解程度的检测。聚合物分析系统对检测粒子浓度的上下限均有要求,为避免稀释或浓缩过程对检测结果造成的影响,本发明采用了高浓度池测定装置sald-hc75s,可以有效避免稀释或浓缩过程对检测结果造成的影响。稀释或浓缩过程均可能会造成样品病毒颗粒状态的改变,例如发生裂解或聚集,此外,人为的处理过程必然伴随着偏差,因而应该尽量减少对样品的处理操作。本发明采用高浓度池测定装置sald-hc75s,就可以减少对样品的人为处理,一方面可以有效避免稀释或浓缩过
程对检测结果造成的影响,另一方面也可以减少人为处理过程产生的偏差。
20.本发明提供的裂解疫苗裂解效果的检测方法,相比现有的采用电镜观察法来评价流感病毒裂解疫苗的裂解效果,本发明的检测方法可以定量评价病毒的裂解程度,提高了数据的可靠性。
21.经检测实验发现,本发明的裂解疫苗裂解效果的检测方法准确度re均在2%以内,精密度rsd均小于0.05%,表明该方法准确、可靠,且重复性好,检测结果较稳定,符合生物样品分析方法指导原则的要求。
附图说明
22.图1是本发明实施例2中标准品b工作液的分布丰度图;
23.图2是本发明实施例3得到的不同裂解程度的系列工作液的检测图;
24.图3是本发明实施例3得到的标准工作曲线图;
25.图4是本发明实施例3得到的质量控制样本的检测图。
具体实施方式
26.下面通过具体实施例对本发明的技术方案进行详细说明。
27.实施例1
28.制备标准品a和标准品b。
29.制备病毒颗粒完全裂解的裂解病毒液标准品,即标准品a;制备过程如下:
30.取流感病毒裂解疫苗原液生产过程中的裂解液,使用滤膜过滤,除去其中未裂解的病毒颗粒,收集滤液,得到标准品a。
31.制备病毒颗粒未发生裂解的病毒液标准品,即标准品b;制备过程如下:
32.取流感病毒裂解疫苗原液生产过程中裂解前的纯化液作为标准品b。
33.实施例2
34.对标准品b进行检测。
35.采用聚合物分析系统aggregates sizer,检测条件是:采用高浓度池测定装置sald-hc75s,样品量0.125ml,采集软件wing sald bio-7500for english(us)v3.3,仪器厂家岛津企业管理(中国)有限公司北京分公司。
36.取实施例1制得的标准品b,稀释标准品b,得到工作液;
37.采用上述聚合物分析系统aggregates sizer进行检测,得到了0.04~20μm粒径颗粒的分布丰度图,见图1所示。图1中a表示不同粒径颗粒的分布丰度,对应右纵坐标数值,b表示0.04~20μm粒径颗粒的累积分布丰度,对应左纵坐标数值。由图1可知,在0.04~20μm粒径检测范围内,标准品b工作液中主要分布0.04~0.3μm粒径的颗粒,且以100nm左右的颗粒居多。这与文献报道的流感病毒颗粒直径约为80~120nm基本吻合。
38.实施例3
39.对流感裂解疫苗裂解效果进行检测,采用实施例2所述的聚合物分析系统aggregates sizer和检测条件进行检测,具体如下。
40.(一)配制具有不同裂解程度的系列工作液
41.分别取实施例1制得的标准品a 0.6ml、0.7ml、0.8ml、0.9ml和1.0ml于不同的离心
管中,之后向离心管中分别依次加入0.4ml、0.3ml、0.2ml、0.1ml及0ml的标准品b,此时离心管中均具有1ml的溶液;配制得到裂解程度分别是60%、70%、80%、90%和100%的系列工作液;
42.另取裂解程度为60%、80%和100%的工作液作为质量控制(quality control,qc)样本。
43.(二)分析方法
44.使用aggregates sizer检测待测样本的颗粒粒径、浓度和分布,光源发出的光照射到待测样本上产生散射衍射光和散射光,wing saldⅱ软件采集散射衍射光光强数据,并根据光强数据换算得出颗粒粒径大小和分布数据,根据wing sald bio内置曲线,可求出各不同粒径颗粒的分布丰度。
45.(三)检测过程
46.1、病毒颗粒粒径检测
47.将标准品b加入到激光粒度仪样品池中进行检测,得到各粒径的分布丰度,具体为:
48.取实施例1制得的标准品b,稀释标准品b,得到工作液;
49.采用实施例2所述的聚合物分析系统aggregates sizer和检测条件进行检测,得到了0.04~20μm粒径颗粒的分布丰度图,见图1所示。图1中a表示不同粒径颗粒的分布丰度,对应右纵坐标数值,b表示0.04~20μm粒径颗粒的累积分布丰度,对应左纵坐标数值。由图1可知,在0.04~20μm粒径检测范围内,标准品b工作液中主要分布0.04~0.3μm粒径的颗粒,且以100nm左右的颗粒居多。这与文献报道的流感病毒颗粒直径约为80~120nm基本吻合。
50.2、标准工作曲线的建立
51.采用实施例2所述的聚合物分析系统aggregates sizer和检测条件,对步骤(一)配制好的裂解程度分别为60%、70%、80%、90%和100%的系列工作液分别进行检测,分别得到不同裂解程度的工作液中不同粒径病毒颗粒的分布丰度,之后进一步得到不同裂解程度的工作液中病毒颗粒的累积分布丰度,不同裂解程度的系列工作液的检测图如图2所示。图中a表示不同粒径颗粒的分布丰度,对应右纵坐标数值,b表示0.04~20μm粒径颗粒的累积分布丰度,对应左纵坐标数值。对0.04~0.3μm颗粒粒径区间内的累积分布丰度进行统计,以病毒颗粒的累积分布丰度为纵坐标,以裂解程度为横坐标,得到了标准工作曲线,如图3所示,求得标准工作曲线方程为y=-2600x 2610,相关系数r2为0.995,说明标准工作曲线在60%~100%裂解程度范围内呈良好线性相关。
52.在实验中设置了0~100%多个不同裂解程度的系列梯度工作液,当裂解程度为50%或小于50%时,仪器检测出现多重散射,信号偏移,造成检测结果不准确,因此该标准工作曲线裂解程度的检测下限为60%。
53.3、检测样本的测定
54.采用聚合物分析系统对待测样本进行检测,得到待测样本中病毒颗粒的累积分布丰度,再根据标准工作曲线计算得到所测样本的裂解程度。具体如下。
55.取步骤(一)配制得到的裂解程度分别为60%、80%和100%的工作液,即质量控制样本(qc样本)进行检测。采用实施例2所述的聚合物分析系统aggregates sizer和检测条
件,重复3次得到各自检测图,检测得到的质量控制样本的检测图见图4。图中a为不同粒径颗粒的分布丰度,对应右纵坐标数值,b为0.04~20μm粒径颗粒的累积分布丰度,对应左纵坐标数值。
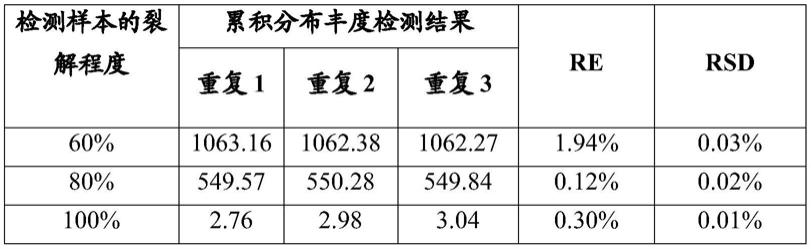
56.以当日的标准工作曲线计算qc样本的裂解程度,重复3次求算精密度和准确度。准确度用相对误差re表示,精密度用相对标准偏差rsd表示,对数据进行统计,结果见表1。
57.表1
[0058][0059]
由表1可知,准确度re均在2%以内,精密度rsd均小于0.05%,表明该方法准确、可靠,且重复性好,检测结果较稳定,符合生物样品分析方法指导原则的要求。
[0060]
虽然,上文中已经用一般性说明、具体实施方式及试验,对本发明作了详尽的描述,但在本发明基础上,可以对之作一些修改或改进,这对本领域技术人员而言是显而易见的。因此,在不偏离本发明精神的基础上所做的这些修改或改进,均属于本发明要求保护的范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。