乙烯醇
‑
氨基酸酯共聚物
技术领域
1.本发明涉及乙烯醇
‑
氨基酸酯共聚物。
背景技术:
2.以往,在医疗领域、化妆品领域、食品容器领域等生命科学领域中使用大量的高分子,其中多数需要以用于人体为前提来确保安全性。作为这些领域中使用的聚合物,广为人知的有聚苯乙烯、聚甲基丙烯酸甲酯、聚氯乙烯、聚乙烯醇、聚乙烯、聚丙烯、聚丙烯酰胺等,并以粒子、容器、板、膜、管等多种形态进行使用。
3.其中,聚乙烯醇由于与聚乳酸同样地具有在废弃处理时不对环境产生负荷的生物降解性,同时为水溶性高分子,因此作为基体高分子而受到关注。
4.例如,专利文献1中记载了通过在聚乙烯醇中导入胺从而使pva具有生物相容性。另外,专利文献2中记载了介由硫原子等而键合有氨基的氨基改性聚乙烯醇。
5.现有技术文献
6.专利文献
7.专利文献1:日本特开平11
‑
302973号公报
8.专利文献2:日本特开平11
‑
199632号公报
技术实现要素:
9.发明要解决的课题
10.然而,在利用专利文献1及2中记载的方法来键合氨基的情况下,由于并不是与氨基酸酯的共聚物结构,因此有性能不充分的情况。例如,不易用于在体内使用的再生医疗用途那样的需要进行细胞培养的用途。另外,与生物组织的亲和性也不充分,需要提高生物相容性。
11.此外,关于对有机溶剂的溶解性,也未获得满意的结果。
12.本发明的目的在于,提供一种细胞培养性、生物相容性、抗菌性及对有机溶剂的溶解性等优异且能够应用于医疗领域、生物材料领域、农业领域(医学、生命科学领域)的乙烯醇
‑
氨基酸酯共聚物。
13.用于解决课题的手段
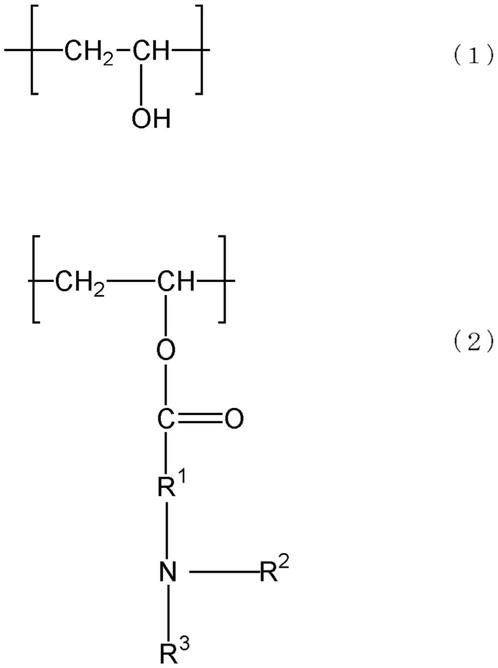
14.本发明是一种具有下述式(1)及式(2)所示的单元的乙烯醇
‑
氨基酸酯共聚物。
15.以下对本发明进行详细说明。
16.[化1]
[0017][0018]
式(2)中,r1表示任选具有取代基的烃基,r2及r3各自独立地表示氢原子或烃基。另外,r1和r2、或者、r2和r3任选键合而成为环状结构。
[0019]
本发明的乙烯醇
‑
氨基酸酯共聚物具有上述式(1)所示的单元(以下,乙烯醇单元)。
[0020]
通过具有这样的乙烯醇单元,能够控制亲水性。
[0021]
本发明的乙烯醇
‑
氨基酸酯共聚物中的上述式(1)所示的单元的含量的优选的下限为0.1摩尔%,更优选的下限为0.5摩尔%,进一步优选的下限为1摩尔%,进一步更优选的下限为5摩尔%,特别优选的下限为10摩尔%,尤其优选的下限为20摩尔%,非常优选的下限为30摩尔%。另外,优选的上限为99.9摩尔%,更优选的上限为99.5摩尔%,进一步优选的上限为99摩尔%,进一步更优选的上限为95摩尔%,特别优选的上限为90摩尔%,尤其优选的上限为80摩尔%,非常优选的上限为75摩尔%,例如为70摩尔%以下,尤其是65摩尔%以下。
[0022]
通过设为这样的范围,能够控制亲水性、疏水性、反应性,并且能够得到细胞培养性、生物相容性、抗菌性及对有机溶剂的溶解性等优异的共聚物。
[0023]
需要说明的是,上述式(1)所示的单元的含量可以通过1h
‑
nmr测定(关于其他单元也同样)。
[0024]
本发明的乙烯醇
‑
氨基酸酯共聚物具有上述式(2)所示的单元(以下,氨基酸酯单元)。
[0025]
通过具有这样的氨基酸酯单元,能够对乙烯醇
‑
氨基酸酯共聚物赋予生物相容性、细胞培养性、抗菌性及对有机溶剂优异的溶解性等迄今为止没有的性能。
[0026]
上述式(2)中,r1表示任选具有取代基的烃基。
[0027]
通过具有上述任选具有取代基的烃基,从而可以进一步赋予生物相容性、细胞培养性、抗菌性及对有机溶剂的溶解性等功能。
[0028]
需要说明的是,上述烃基包括脂肪族烃基、脂环式烃基、芳香族烃基、2个以上的上述烃基键合而得的烃基。
[0029]
作为上述烃基,优选为2价烃基。
[0030]
作为上述2价烃基,可举出:碳原子数1~20(优选为1~15,更优选为1~10,进一步优选为1~7,进一步更优选为1~5,特别优选为1~3)的直链状或支链状的亚烷基。另外,可举出:碳原子数2~20(优选为2~15,更优选为2~10,进一步优选为2~7,进一步更优选为2~5,特别优选为2~3)的直链状或支链状的亚烯基、环烷撑基(日文:
シクロアルキレン
基)、环烷叉基(日文:
シクロアルキリデン
基)、亚芳基、亚苄基等。
[0031]
作为上述碳原子数1~20的直链状或支链状的亚烷基,可举出:亚甲基、甲基亚甲基(乙叉基)、乙基亚甲基(丙叉基)、二甲基亚甲基(异丙叉基)、乙基甲基亚甲基、亚乙基、亚丙基、三亚甲基、四亚甲基、六亚甲基等。
[0032]
作为上述碳原子数2~20的直链状或支链状的亚烯基,可举出亚丙烯基等。
[0033]
作为上述环烷撑基,可举出:1,3
‑
环戊撑基、1,2
‑
环己撑基、1,3
‑
环己撑基、1,4
‑
环己撑基等。
[0034]
作为上述环烷叉基,可举出:亚环丙基(日文:
シクロプロピレン
)、环戊叉基、环己叉基等。
[0035]
作为上述亚芳基,可举出:1,2
‑
亚苯基、1,3
‑
亚苯基、1,4
‑
亚苯基等。
[0036]
作为上述取代基,可举出:碳原子数1~20(优选为1~15,更优选为1~10,进一步优选为1~7,进一步更优选为1~5,特别优选为1~3)的烷氧基、碳原子数6~30(优选为6~20,更优选为6~10)的芳氧基。另外,可举出:碳原子数2~20(优选为2~15,更优选为2~10,进一步优选为2~7)的烷氧基羰基、碳原子数7~30(优选为7~20,更优选为7~1,进一步优选为7~10)的芳氧基羰基。此外,可举出:碳原子数1~20(优选为1~15,更优选为1~10,进一步优选为1~7,进一步更优选为1~5,特别优选为1~3)的酰氧基、碳原子数1~20(优选为1~15,更优选为1~10,进一步优选为1~7,进一步更优选为1~5,特别优选为1~3)的酰基等。此外,可举出:碳原子数1~20(优选为1~15,更优选为1~10,进一步优选为1~7,进一步更优选为1~5,特别优选为1~3)的氨基甲酰基、碳原子数0~30(优选为1~20,更优选为1~15,进一步优选为1~10,进一步更优选为1~5)的氨磺酰基。另外,可举出:卤原子、碳原子数1~20的烷硫基、碳原子数6~30的芳硫基、碳原子数0~20的烷基磺酰基、碳原子数6~30的芳基磺酰基、酚基、羟基、羧基、氰基、肼基、碳原子数1~20的脲基、碳原子数1~20的硫脲基、硝基等。这些取代基可以单独使用,也可以组合使用两种以上。另外,作为上述取代基,从进一步提高生物相容性及生物降解性的观点出发,优选具有亲水性的官能团(例如,羟基、羧基、酚基、氨基)。
[0037]
其中,作为上述r1,从进一步提高生物相容性的观点出发,优选使用具有酚基作为取代基的碳原子数1~20的直链状或支链状的亚烷基、以及、具有碳原子数2~20的烷氧基羰基作为取代基的碳原子数1~20的直链状或支链状的亚烷基。另外,更优选为具有酚基作为取代基的碳原子数1~20的直链状或支链状的亚烷基,进一步优选为具有酚基作为取代基的乙叉基。
[0038]
[化2]
[0039][0040]
上述式(2)中,上述r2及r3各自独立地表示氢原子或烃基。另外,r1和r2、或者、r2和r3任选键合而成为环状结构。
[0041]
需要说明的是,r2及r3可以相同,也可以不同。作为上述烃基,优选为烷基、亚烷基,作为上述烷基、亚烷基,优选为碳原子数1~20的烷基、亚烷基。
[0042]
需要说明的是,在r2和r3键合而形成环状结构的情况下,r2及r3与n原子一同形成环状结构。在r2及r3与n原子一同形成环状结构的情况下,r2及r3的合计碳原子数优选为2~20,更优选为3~10,进一步优选为4~8。
[0043]
另外,在r1和r2键合而形成环状结构的情况下,r1及r2与n原子一同形成环状结构。在r1及r2与n原子一同形成环状结构的情况下,r1及r2的合计碳原子数优选为2~20,更优选为3~10,进一步优选为4~8。
[0044]
作为上述r1和r2、或者、r2和r3键合而形成环状结构的情况下的结构,可举出吡咯烷、哌啶等。
[0045]
本发明中,在上述式(2)所示的单元中,优选的是r1为任选具有取代基的2价烃基,r2及r3为氢原子或烷基,尤其优选的是上述r2及r3均为氢原子。
[0046]
本发明的乙烯醇
‑
氨基酸酯共聚物中的上述式(2)所示的单元的含量的优选的下限为0.1摩尔%,更优选的下限为0.5摩尔%,进一步优选的下限为1摩尔%,进一步更优选的下限为5摩尔%,特别优选的下限为10摩尔%,尤其优选的下限为20摩尔%,非常优选的下限为25摩尔%。例如为30摩尔%以上,特别是35摩尔%以上,优选的上限为99.9摩尔%,更优选的上限为99.5摩尔%,进一步优选的下限为99摩尔%,进一步更优选的下限为95摩尔%,特别优选的下限为90摩尔%,尤其优选的下限为80摩尔%,非常优选的下限为70摩尔%。
[0047]
通过设为这样的范围,能够对乙烯醇
‑
氨基酸酯共聚物赋予生物相容性、细胞培养性、抗菌性及对有机溶剂的优异的溶解性等功能。
[0048]
作为本发明的乙烯醇
‑
氨基酸酯共聚物的重均分子量,没有特别限制,重均分子量优选为1000~100万。
[0049]
另外,本发明的乙烯醇
‑
氨基酸酯共聚物的聚合度优选为200~3000,更优选为250
~2500,进一步优选为300~2000。通过设为上述范围内,能够表现出在宽泛领域中的可使用性。
[0050]
本发明中,聚合度、数均分子量及重均分子量例如能够在凝胶渗透色谱法中,使用dmso作为洗脱液,使用1根shodex lf
‑
804(8.0mmid
×
300ml)作为柱,通过聚乙二醇标准进行测定。
[0051]
就本发明的乙烯醇
‑
氨基酸酯共聚物而言,制成4重量%水溶液并在20℃下测定的粘度的优选的下限为1.0mpa
·
s,更优选的下限为2.0mpa
·
s,优选的上限为500mpa
·
s,更优选的上限为400mpa
·
s。通过设为上述范围内,能够提高制成水溶液的情况下的处置性。
[0052]
需要说明的是,上述粘度可以根据jis k 6726进行测定。
[0053]
本发明的乙烯醇
‑
氨基酸酯共聚物优选具有下述通式(3)所示的单元(以下,也称为缩醛单元)。若上述乙烯醇
‑
氨基酸酯共聚物具有缩醛单元,则亲疏水性的控制变容易,并且能够提高强度。
[0054]
[化3]
[0055][0056]
上述式(3)中,r4表示氢原子或碳原子数1~20的烷基。
[0057]
上述式(3)中,在r4为碳原子数1~20的烷基的情况下,作为该烷基,例如可举出:甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基等。另外,可举出:戊基、己基、庚基、2
‑
乙基己基、辛基、壬基、癸基、十一烷基、十二烷基、十三烷基、十四烷基、十五烷基、十八烷基等。其中,从提高机械强度的观点出发,优选为甲基、正丙基,优选为正丙基。
[0058]
在本发明的乙烯醇
‑
氨基酸酯共聚物中,上述通式(3)所示的具有缩醛基的单元的含量的优选的下限为0.5摩尔%,更优选的下限为1.0摩尔%,进一步优选的下限为5.0摩尔%,进一步更优选的下限为10.0摩尔%。另外,优选的上限为90摩尔%,更优选的上限为80摩尔%,进一步优选的上限为70摩尔%,进一步更优选的上限为65摩尔%。
[0059]
若上述缩醛单元的含量为上述下限以上,则能够提高对有机溶剂的溶解性。若上述缩醛单元的含量为上述上限以下,则能够制成强韧性优异的聚乙烯醇缩醛树脂。
[0060]
需要说明的是,本说明书中,作为缩醛单元的含量的计算方法,由于乙烯醇
‑
氨基酸酯共聚物的缩醛基是使具有2个羟基的结构单元进行缩醛化而得的,因此采用对被缩醛化的具有2个羟基的结构单元进行计数的方法来计算缩醛单元的含量。
[0061]
从控制亲疏水性及熔点的观点出发,本发明的乙烯醇
‑
氨基酸酯共聚物优选具有下述通式(4)所示的包含乙酸乙烯酯的单元(以下,也称为乙酸乙烯酯单元)。
[0062]
[化4]
[0063][0064]
在本发明的乙烯醇
‑
氨基酸酯共聚物中,上述通式(4)所示的乙酸乙烯酯单元的含量的优选的下限为0.5摩尔%,更优选的下限为1.0摩尔%,进一步优选的下限为1.5摩尔%。另外,优选的上限为99.5摩尔%,更优选的上限为99摩尔%,进一步优选的上限为90摩尔%,进一步更优选的上限为80摩尔%,特别优选的上限为70摩尔%,尤其优选的上限为60摩尔%,例如为50摩尔%以下,特别是30摩尔%以下。
[0065]
通过设为这样的范围,能够控制乙烯醇
‑
氨基酸酯共聚物的疏水性。
[0066]
本发明的乙烯醇
‑
氨基酸酯共聚物可以还具有包含其他单体的单元。
[0067]
上述其他单体没有特别限定,优选为:在分子内具有选自由羧基、酰胺基及环氧基、醚基组成的组中的至少1个极性基和1个烯烃性双键的单体。作为这样的单体,例如可举出巴豆酸、马来酸、富马酸、柠康酸、中康酸、衣康酸等。
[0068]
本发明的乙烯醇
‑
氨基酸酯共聚物中所含的包含其他单体的单元的含量根据用途进行设计,因此没有特别限定,相对于乙烯醇
‑
氨基酸酯共聚物整体,优选为20摩尔%以下,更优选为10摩尔%以下,进一步优选为5摩尔%以下。
[0069]
在本发明的乙烯醇
‑
氨基酸酯共聚物中,上述通式(1)及通式(2)所示的单元、以及根据需要的通式(3)及通式(4)所示的单元及包含其他单体的单元的单元排列可以是无规的,也可以是嵌段的。
[0070]
作为制造本发明的乙烯醇
‑
氨基酸酯共聚物的方法,例如优选使用具有以下工序的方法,所述工序为:使用下述式(5)所示的二阴离子型锌酸根型络合物,使原料聚乙烯醇进行酯交换反应的工序(酯交换反应法)。
[0071]
本发明的乙烯醇
‑
氨基酸酯共聚物的制造方法(酯交换反应法)具有以下工序:使用下述式(5)所示的二阴离子型锌酸根型络合物,使原料聚乙烯醇进行酯交换反应。
[0072]
通过使用上述二阴离子型锌酸根型络合物,能够合适地制作具有规定的乙烯醇单元及氨基酸酯单元的乙烯醇
‑
氨基酸酯共聚物。此外,通过使用上述二阴离子型锌酸根型络合物,从而能够以非常短的反应时间进行酯交换反应。具体而言,与使用了ch3ona的酯交换相比,能够以10分之1左右的时间进行反应。
[0073]
[化5]
[0074]
t
‑
bu
n
r4‑
n
znm
m
ꢀꢀ
(5)
[0075]
式(5)中,n为1~4的整数,m为1或2,在n为1或2时r各自可以相同也可以不同,为碳原子数1~8的烷基、烯基、芳基或芳烷基,m为锂或镁。
[0076]
作为上述碳原子数1~8的烷基、烯基、芳基、芳烷基的具体例,例如可举出甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基、正己基、乙烯基、苯基、苄基
等。
[0077]
上述m表示锂或镁,m为锂时m为2,m为镁时m表示1。
[0078]
上述式(5)所示的二阴离子型锌酸根型络合物记载于日本特开2004
‑
292328号公报,可以通过该公报所记载的方法获取。
[0079]
具体而言,例如,作为二锂盐,可举出:四叔丁基锌酸二锂、三叔丁基甲基锌酸二锂、三叔丁基乙基锌酸二锂、三叔丁基正丙基锌酸二锂、三叔丁基正丁基锌酸二锂、三叔丁基异丁基锌酸二锂、三叔丁基仲丁基锌酸二锂、二叔丁基二甲基锌酸二锂、二叔丁基二乙基锌酸二锂、二叔丁基二正丙基锌酸二锂、二叔丁基二正丁基锌酸二锂、二叔丁基二异丁基锌酸二锂、二叔丁基二仲丁基锌酸二锂、叔丁基三甲基锌酸二锂、叔丁基三乙基锌酸二锂、叔丁基三正丙基锌酸二锂、叔丁基三正丁基锌酸二锂、叔丁基三异丁基锌酸二锂、叔丁基三仲丁基锌酸二锂等。
[0080]
另外,作为镁盐,可举出:四叔丁基锌酸镁、三叔丁基甲基锌酸镁、三叔丁基乙基锌酸镁、三叔丁基正丙基锌酸镁、三叔丁基正丁基锌酸镁、三叔丁基异丁基锌酸镁、三叔丁基仲丁基锌酸镁、二叔丁基二甲基锌酸镁、二叔丁基二乙基锌酸镁、二叔丁基二正丙基锌酸镁、二叔丁基二正丁基锌酸镁、二叔丁基二异丁基锌酸镁、二叔丁基二仲丁基锌酸镁、叔丁基三甲基锌酸镁、叔丁基三乙基锌酸镁、叔丁基三正丙基锌酸镁、叔丁基三正丁基锌酸镁、叔丁基三异丁基锌酸镁、叔丁基三仲丁基锌酸镁等。
[0081]
其中,作为上述式(5)所示的二阴离子型锌酸根型络合物,优选为使用二锂盐,优选具有碳原子数1~4的烷基。特别是优选为四叔丁基锌酸二锂(tbzl)。
[0082]
需要说明的是,上述二阴离子型锌酸根型络合物可以仅使用1种,也可以组合使用两种以上。
[0083]
上述tbzl的制备可以根据日本特开2004
‑
292328号公报的实施例1中记载的方法进行。
[0084]
上述酯交换反应时的反应温度没有特别限定,可以从
‑
80℃~200℃的范围适当选择。优选为0℃~80℃的范围。
[0085]
上述酯交换反应可以在常压下进行,或者可以在减压下进行。
[0086]
另外,上述酯交换反应的反应时间可以按照使酯交换反应结束的方式进行调整,优选为0.1~100小时,更优选为1~70小时,进一步优选为5~50小时。
[0087]
此外,在进行上述酯交换反应时,也能够采用将副产的醇通过与有机溶剂进行共沸而除去的方法。
[0088]
在上述酯交换反应中,二阴离子型锌酸根型催化剂的用量相对于原料聚乙烯醇中的乙烯醇单元1摩尔,优选的下限为0.001摩尔,优选的上限为0.5摩尔。更优选的下限为0.001摩尔,更优选的上限为0.1摩尔,进一步优选的下限为0.005摩尔,进一步优选的上限为0.05摩尔。
[0089]
使用上述二阴离子型锌酸根型络合物进行酯交换反应的工序例如优选使用以下方法:使原料聚乙烯醇溶解于溶剂后,添加二阴离子型锌酸根型络合物、氨基酸酯化合物进行酯交换反应,进一步通过添加酸而使酯交换反应停止。
[0090]
上述溶剂没有特别限定,例如可举出甲苯、二甲基亚砜、丙酮、二乙醚、四氢呋喃、水、及它们的混合溶剂等。
[0091]
作为上述氨基酸酯化合物,可举出:甘氨酸烷基酯、天冬氨酸丙烯酸酯、l
‑
酪氨酸甲酯、l
‑
蛋氨酸甲酯、l
‑
蛋氨酸乙酯、dl
‑2‑
氨基丁酸甲酯、l
‑
丙氨酸甲酯、n
‑
boc
‑
甘氨酸甲酯、β丙氨酸甲酯、n
‑
苄氧羰基甘氨酸甲酯、l
‑
叔亮氨酸甲酯、2
‑
哌啶甲酸甲酯、2
‑
哌啶甲酸乙酯、4
‑
哌啶甲酸甲酯(异哌啶甲酸甲酯)、4
‑
哌啶甲酸乙酯、dl
‑
焦谷氨酸甲酯、l
‑
谷氨酸1
‑
甲酯、l
‑
天冬氨酸1
‑
甲酯、3
‑
氨基苯甲酸甲酯、2
‑
氨基噻吩
‑3‑
甲酸甲酯、2
‑
氨基
‑
4,5
‑
二氟苯甲酸甲酯、4
‑
氨基苯甲酸甲酯、1
‑
氨基环丙烷甲酸甲酯、1
‑
氨基环己烷甲酸甲酯、1
‑
氨基
‑1‑
环戊烷甲酸甲酯、5
‑
氨基
‑
2,4
‑
二氟苯甲酸甲酯、3
‑
氨基吡唑
‑4‑
甲酸甲酯、2
‑
(乙酰基氨基)异烟酸甲酯、5
‑
氨基
‑2‑
糠酸甲酯等。
[0092]
在上述进行酯交换反应的工序中,可以添加分子筛等载体。
[0093]
通过添加上述载体,从而引起向载体的吸附,化学平衡倾斜。结果载体发挥反应助剂的作用。
[0094]
作为上述分子筛,优选为使用沸石,可举出分子筛3a、分子筛4a等,优选可举出分子筛4a。
[0095]
上述进行酯交换反应的工序可以在均匀体系中进行,也可以在不均匀体系中进行。
[0096]
需要说明的是,均匀体系是指物质以均匀的浓度存在的体系,是指成分溶解于溶剂中的状态。不均匀体系是指反应体系不均匀的情况,是随着反应的进行而物质变得局部地存在的体系,是指一部分树脂等成分在反应的过程中未溶解的状态。
[0097]
本发明的乙烯醇
‑
氨基酸酯共聚物例如能够用于水溶液的粘度调整剂、阻气涂布剂、悬浮剂、乳化剂、偏振板、水溶性膜、分散剂、细胞培养培养基、生物材料、农业膜、抗菌树脂等各种树脂的原材料等用途中。
[0098]
作为本发明的乙烯醇
‑
氨基酸酯共聚物的形态,没有特别限定,可举出纤维、无纺布等布帛、网、膜、涂膜、片状、块状、粒子状、棒状、板状、海绵状、溶液状、涂料、凝胶状、乳膏状等各种形状。其中,优选为无纺布等布帛、片状、涂膜、粒子状。另外,还可以优选使用溶解或分散于水或醇等有机溶剂与水的混合物中并进行喷雾的方法。
[0099]
本发明的乙烯醇
‑
氨基酸酯共聚物例如能够以上述形态而有利地用作例如细胞的培养基、生物材料、农业用膜、抗菌剂。
[0100]
发明效果
[0101]
根据本发明,可以提供细胞培养性、生物相容性、抗菌性及对有机溶剂的溶解性等优异,能够应用于医疗领域、生物材料领域、农业领域(医学、生命科学领域)的乙烯醇
‑
氨基酸酯共聚物。
具体实施方式
[0102]
以下,列举实施例来更加详细地说明本发明,但本发明不仅限于这些实施例。
[0103]
(实施例1)
[0104]
将原料聚乙烯醇(pva
‑
1,皂化度98.5,聚合度300)1重量份添加至dmso 49重量份中使其溶解(浓度2重量%)。然后,添加l
‑
酪氨酸甲酯4.4重量份、四叔丁基锌酸二锂(tbzl,溶剂:四氢呋喃,浓度13重量%)6重量份,在30℃下搅拌6小时,由此进行酯交换反应。
[0105]
然后,在四氢呋喃中进行再沉淀,利用四氢呋喃进行清洗,由此得到产物(乙烯醇
‑
氨基酸酯共聚物)。
[0106]
(实施例2)
[0107]
将酯交换反应中的搅拌时间从“6小时”变更为“24小时”,除此以外,利用与实施例1同样的方法,得到产物(乙烯醇
‑
氨基酸酯共聚物)。
[0108]
(实施例3)
[0109]
将l
‑
酪氨酸甲酯的添加量从“4.4重量份”变更为“8.9重量份”,除此以外,利用与实施例1同样的方法,得到产物(乙烯醇
‑
氨基酸酯共聚物)。
[0110]
(实施例4)
[0111]
将l
‑
酪氨酸甲酯的添加量从“4.4重量份”变更为“17.7重量份”,除此以外,利用与实施例1同样的方法,得到产物(乙烯醇
‑
氨基酸酯共聚物)。
[0112]
(实施例5)
[0113]
将酯交换反应中的搅拌时间从“6小时”变更为“24小时”,用水进行再沉淀、清洗,除此以外,利用与实施例4同样的方法,得到产物(乙烯醇
‑
氨基酸酯共聚物)。
[0114]
(实施例6)
[0115]
使用原料聚乙烯醇(pva
‑
3,皂化度98.5,聚合度600)来代替原料聚乙烯醇(pva
‑
1,皂化度98.5,聚合度300),除此以外,利用与实施例5同样的方法,得到产物(乙烯醇
‑
氨基酸酯共聚物)。
[0116]
(实施例7)
[0117]
使用原料聚乙烯醇(pva
‑
4,皂化度98.5,聚合度1000)来代替原料聚乙烯醇(pva
‑
1,皂化度98.5,聚合度300),除此以外,利用与实施例5同样的方法,得到产物(乙烯醇
‑
氨基酸酯共聚物)。
[0118]
(实施例8)
[0119]
将原料聚乙烯醇缩丁醛(pvb,乙烯醇单元含量34摩尔%,缩醛单元含量65摩尔%,乙酸乙烯酯单元含量1摩尔%,聚合度1700)1重量份添加至dmso 19重量份中而使其溶解(浓度5重量%)。然后,添加l
‑
酪氨酸甲酯2.5重量份、四叔丁基锌酸二锂(tbzl,浓度13重量%)0.25重量份,在30℃下搅拌6小时,由此进行酯交换反应。
[0120]
然后在水中进行再沉淀,用热水进行清洗,由此得到产物(乙烯醇缩丁醛
‑
氨基酸酯共聚物)。
[0121]
(实施例9)
[0122]
使用4
‑
cep(4
‑
哌啶甲酸乙酯)来代替l
‑
酪氨酸甲酯,并且将酯交换反应中的tbzl(浓度13重量%)的添加量从“6重量份”变更为“10重量份”,将搅拌时间从“6小时”变更为“24小时”,除此以外,利用与实施例1同样的方法,得到产物(乙烯醇
‑
氨基酸酯共聚物)。
[0123]
(实施例10)
[0124]
将4
‑
cep(4
‑
哌啶甲酸乙酯)的添加量从“4.4重量份”变更为“17.7重量份”,除此以外,利用与实施例9同样的方法,得到产物(乙烯醇
‑
氨基酸酯共聚物)。
[0125]
(实施例11)
[0126]
使用原料聚乙烯醇(pva
‑
3,皂化度98.5,聚合度600)来代替原料聚乙烯醇(pva
‑
1,皂化度98.5,聚合度300),除此以外,利用与实施例10同样的方法,得到产物(乙烯醇
‑
氨基酸酯共聚物)。
[0127]
(实施例12)
[0128]
使用原料聚乙烯醇(pva
‑
4,皂化度98.5,聚合度1000)来代替原料聚乙烯醇(pva
‑
1,皂化度98.5,聚合度300),除此以外,利用与实施例10同样的方法,得到产物(乙烯醇
‑
氨基酸酯共聚物)。
[0129]
(实施例13)
[0130]
使用4
‑
cep(4
‑
哌啶甲酸乙酯)来代替l
‑
酪氨酸甲酯,除此以外,利用与实施例8同样的方法,得到产物(乙烯醇
‑
氨基酸酯共聚物)。
[0131]
(参考例)
[0132]
使用2
‑
cep(2
‑
哌啶甲酸乙酯)来代替l
‑
酪氨酸甲酯,并且将酯交换反应中的tbzl(浓度13重量%)的添加量从“6重量份”变更为“10重量份”,将搅拌时间从“6小时”变更为“24小时”,除此以外,利用与实施例1同样的方法,得到产物(乙烯醇
‑
氨基酸酯共聚物)。
[0133]
(比较例1)
[0134]
使用皂化度98.5、聚合度300的乙烯醇
‑
乙酸乙烯酯共聚物(pva
‑
1)。
[0135]
(比较例2)
[0136]
使用皂化度88.0、聚合度600的乙烯醇
‑
乙酸乙烯酯共聚物(pva
‑
2)。
[0137]
(比较例3)
[0138]
使用皂化度99.5、聚合度1000的乙烯醇
‑
乙烯胺共聚物(胺改性pva
‑
1,乙烯胺单元含量12摩尔%)。
[0139]
(比较例4)
[0140]
使用皂化度99.5、聚合度500的乙烯醇
‑
乙烯胺共聚物(胺改性pva
‑
2,乙烯胺单元含量6摩尔%)。
[0141]
(评价方法)
[0142]
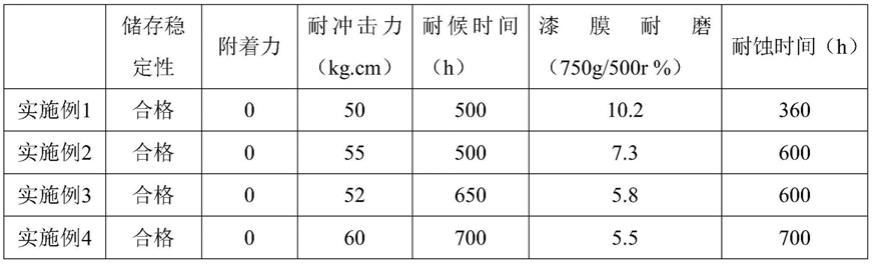
将上述得到的产物利用以下的方法进行评价。结果示于表1。
[0143]
(1)1h
‑
nmr测定
[0144]
通过对所得的产物进行1h
‑
nmr测定,从而测定产物的组成比(乙烯醇单元、氨基酸酯单元、缩醛单元、乙酸乙烯酯单元、乙烯胺单元)。需要说明的是,在1h
‑
nmr测定中,使用jeol jnm
‑
ecx500,并使用dmso
‑
d6溶液(1wt/vol%),在60℃下实施测定。
[0145]
(2)细胞培养性评价
[0146]
用dmso将所得的产物溶解后进行干燥,由此涂布于96孔板的底面,将在dulbecco改良eagle培养基(dmem)中添加了5%胎牛血清(fbs)而得者作为培养基,在每1孔中播种1
×
104个小鼠成纤维细胞用细胞株(nih/3t3细胞),在5%co2/37℃的培养箱中进行培养。然后,如以下所示地评价培养第1天的初始粘附、及培养第4天的经时增殖
·
粘附保持。
[0147]
针对培养后的活细胞数,使用一次性细胞计数盘(wakenbtech公司制)算出培养后的活细胞数相对于播种细胞数的比率。针对所得的活细胞数的比率,利用以下的基准评价细胞培养性。
[0148]
初始粘附(第1天)
[0149]
〇〇〇:培养后的活细胞数相对于播种细胞数的比率为1.5以上
[0150]
〇〇:培养后的活细胞数相对于播种细胞数的比率为1.0以上且小于1.5
[0151]
〇:培养后的活细胞数相对于播种细胞数的比率为0.5以上且小于1.0
[0152]
△
:培养后的活细胞数相对于播种细胞数的比率为0.2以上且小于0.5
[0153]
×
:培养后的活细胞数相对于播种细胞数的比率小于0.2
[0154]
经时增殖
·
粘附保持(第4天)
[0155]
〇〇〇:培养后的活细胞数相对于播种细胞数的比率为3.0以上
[0156]
〇〇:培养后的活细胞数相对于播种细胞数的比率为2.5以上且小于3.0
[0157]
〇:培养后的活细胞数相对于播种细胞数的比率为2.0以上且小于2.5
[0158]
△
:培养后的活细胞数相对于播种细胞数的比率为1.0以上且小于2.0
[0159]
×
:培养后的活细胞数相对于播种细胞数的比率小于1.0
[0160]
(3)生物相容性评价
[0161]
通过在上述细胞培养性评价中在1天后及6天后进行atp测定来进行评价。从培养后的孔中除去培养基,利用磷酸缓冲液进行清洗后,添加100μl的atp提取试剂(intracellular atp assay kit ver.2:toyo b
‑
net公司制),进行5次移液,在室温下静置5分钟后,提取atp。从上述atp提取溶液中取出1010μl,添加atp发光试剂(相同套件)100μl并进行搅拌后,使用mithraslb940(berthold公司制)来测定其发光量。
[0162]
使用下述式由测定的发光量算出细胞毒性,按照以下的基准进行评价。细胞毒性=(培养6天后的发光量)/(培养1天后的发光量)
×
100
[0163]
〇:细胞毒性小于30%
[0164]
×
:细胞毒性为30%以上
[0165]
(4)血栓附着性
[0166]
使所得的产物溶解于dmso,进行喷雾涂布并干燥,由此将其涂布于内径10mm
×
长度100mm的pet制试验管(对照)的内表面,在pet管中添加1ml人血液,将口部密封并倒置混和而使pet管整个内表面被血液沾湿。
[0167]
使其正立,在室温下静置4小时左右,确认静置血液凝固后,用离心分离机进行1500g
×
5分钟离心处理,然后观察附着于pet管的顶部空间内表面的血液(附着有粉色或浅红色的极薄膜的部分)的程度。
[0168]
综合地判断发红强度、附着面积的程度,将附着按照从少到多的顺序设为
○
、
△
、
×
来进行相对评价。
[0169]
(5)对有机溶剂的溶解性
[0170]
对在实施例1~7、9~12、比较例1~4中得到的产物(pva系的产物)添加甲苯(70℃),对在实施例8、13中得到的产物(pvb系的产物)添加丁醇(室温),以产物的浓度成为1.0质量%的方式进行调整。然后,以500rpm搅拌6小时,根据未溶解物的含量并按照以下的基准来评价溶解性。
[0171]
〇:未溶解物小于20质量%
[0172]
×
:未溶解物为20质量%以上
[0173]
[表1]
[0174][0175]
产业上的可利用性
[0176]
根据本发明,能够提供细胞培养性、生物相容性、抗菌性及对有机溶剂的溶解性等
优异,能够应用于医疗领域、生物材料领域、农业领域(医学、生命科学领域)的乙烯醇
‑
氨基酸酯共聚物。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。