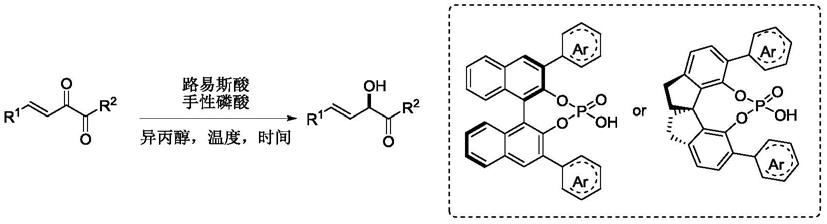
1.本发明公开了属于有机合成技术领域的一种利用双酸催化绿色合成光学纯的烯丙醇类化合物的方法。
背景技术:
2.光学纯的烯丙醇类化合物是一类重要的有机合成中间体,可广泛应用于有机合成及化工领域。此类化合物可以通过α,β
‑
不饱和羰基化合物还原得到。传统的还原方法多数使用化学计量的,昂贵的、对水及空气敏感的氢化试剂,且此类试剂无法再生,从而造成浪费;反应时往往存在一定风险,对环境也不友好。(green chem.,2020,22,3323
‑
3357)。鉴于光学纯的烯丙醇类化合物在合成中的重要性,以及日益增长的绿色可持续合成要求,发展一种新型的绿色合成光学纯的烯丙醇类化合物的方法具有重大意义。
技术实现要素:
3.本发明的目的是为了克服现有的光学纯的烯丙醇类化合物的合成方法中存在的使用化学计量的,不可回收且昂贵的氢化试剂,反应存在风险以及对环境不友好等问题,提供了一种条件温和的绿色合成光学纯的烯丙醇类化合物的方法。
4.为了实现上述目的,本发明提供了一种双酸催化绿色合成光学纯的烯丙醇类化合物的方法,所述光学纯的烯丙醇类化合物的结构式具有式i所示的结构:
[0005][0006]
其中,r1选自饱和烷基、取代烷基、烷氧基、芳基、取代芳基、噻吩基中的任意一种。
[0007]
其中,r2选自烷氧基、烷基、芳基中的任意一种。
[0008]
所述烷氧基为甲氧基、乙氧基、异丙氧基、叔丁氧基、环戊氧基、环己氧基或苄氧基。
[0009]
所述取代烷基、取代芳基的取代基为卤素原子、饱和烷基、芳基、酯基、氰基、硝基、烷氧基中的任意一种。
[0010]
在反应器中,加入β,γ
‑
不饱和
‑
α
‑
羰基化合物,路易斯酸,手性磷酸及异丙醇,一定温度下反应完毕,旋转蒸发仪浓缩反应液得到的粗产品,柱层析分离得到产品。其化学过程见反应式ii:
[0011]
[0012]
所述路易斯酸选自氯化铟、氯化铁、氯化铪、溴化铁、溴化钪、溴化铟、三氟甲磺酸铜、三氟甲磺酸铪、三氟甲磺酸钪、三氟甲磺酸铟中的任意一种。
[0013]
所述手性磷酸具有式iii所示的结构:
[0014][0015]
其中,ar选自芳基及取代芳基。
[0016]
所述芳基为苯基、萘基、蒽基或芘基中的任意一种。
[0017]
所述取代芳基的取代基为单取代或多取代的卤素原子、饱和烷基、芳基、酯基、氰基、硝基、烷氧基或三氟甲基中的任意一种。
[0018]
所述β,γ
‑
不饱和
‑
α
‑
羰基化合物、路易斯酸和手性磷酸的摩尔比为1.0:(0.001
‑
0.01):(0.0005
‑
0.005)。
[0019]
反应时间为6
‑
36h。
[0020]
反应温度为0
‑
60℃。
[0021]
在反应后用石油醚和乙酸乙酯的混合溶剂进行柱层析分离。
[0022]
本发明的有益效果为:本发明提供的双酸催化绿色合成光学纯的烯丙醇类化合物的方法科学合理,相较于传统方法,具有如下显著优点:
[0023]
所用路易斯酸及手性磷酸用量低,催化效率高;
[0024]
所用醇类氢化试剂绿色环保,价格便宜且使用方便,可同时作为溶剂使用;
[0025]
合成条件温和,产率高,对映选择性好;
[0026]
所得产品易于纯化,适合大规模生产。
附图说明
[0027]
图1为实施例1制备的化合物(2a)的nmr及高效液相色谱图谱;
[0028]
图2为实施例2制备的化合物(2b)的nmr及高效液相色谱图谱;
[0029]
图3为实施例3制备的化合物(2c)的nmr及高效液相色谱图谱;
[0030]
图4为实施例4制备的化合物(2d)的nmr及高效液相色谱图谱;
[0031]
图5为实施例5制备的化合物(2e)的nmr及高效液相色谱图谱。
具体实施方式
[0032]
在本文中通过具体实施例对本发明的方法进行说明,但本发明并不局限于此,在本发明的技术构思范围内,进行任何的修改、等同替换和改进等,均应包括在本发明的保护范围之内。
[0033]
实施例1:
[0034]
反应方程式如下:
[0035][0036]
将化合物1a(5mmol),三氟甲磺酸钪(0.025mmol)及手性磷酸(0.01mmol)加入反应器中,加入异丙醇50ml,室温下搅拌12小时。反应完成后,旋转蒸发仪浓缩反应液得到的粗产品,用石油醚和乙酸乙酯的体积比30:1的混合溶剂柱层析分离,得到纯2a,产率为97%,ee值为99%。
[0037]
2a的核磁数据如下:
[0038]1h nmr(500mhz,cdcl3)δ7.29(d,j=8.0hz,2h),7.13(d,j=7.9hz,2h),6.82
‑
6.73(m,1h),6.19(dd,j=15.8,5.6hz,1h),5.17
‑
5.08(m,1h),4.77(s,1h),3.12(d,j=4.9hz,1h),2.34(s,3h),1.31(d,j=6.3hz,3h),1.27(d,j=6.3hz,3h)ppm.
[0039]
13
c nmr(125mhz,cdcl3)δ172.99,137.85,133.50,131.94,129.28,126.58,124.59,71.39,70.16,21.76,21.73,21.21ppm.
[0040]
实施例2
[0041]
反应方程式如下:
[0042]
将化合物1b(5mmol),氯化铪(0.025mmol)及手性磷酸(0.01mmol)加入反应器中,加入异丙醇50ml,室温下搅拌12小时。反应完成后,旋转蒸发仪浓缩反应液得到的粗产品,用石油醚和乙酸乙酯的体积比30:1的混合溶剂柱层析分离,得到纯2b,产率为97%,ee值为95%。
[0043]
2b的核磁数据如下:
[0044]1h nmr(500mhz,cdcl3)δ7.16(t,1h),6.91(d,j=7.7hz,1h),6.85(t,2h),6.76
‑
6.67(m,2h),6.16(dd,j=15.8,5.4hz,1h),5.11
‑
5.00(m,1h),4.70(t,j=4.2hz,1h),3.74(s,3h),3.10(d,j=5.5hz,1h),1.24(d,j=6.3hz,3h),1.20(d,j=6.3hz,3h)ppm.
[0045]
13
c nmr(125mhz,cdcl3)δ172.86,159.80,137.73,131.83,129.59,125.99,119.34,113.50,112.12,71.27,70.29,55.24,21.77,21.74ppm.
[0046]
实施例3
[0047]
反应方程式如下:
[0048]
将化合物1c(5mmol),三氟甲磺酸钪(0.025mmol)及手性磷酸(0.01mmol)加入反应器中,加入异丙醇50ml,室温下搅拌12小时。反应完成后,旋转蒸发仪浓缩反应液得到的粗产品,用石油醚和乙酸乙酯的体积比30:1的混合溶剂柱层析分离,得到纯2c,产率为93%,ee值为97%。
[0049]
2c的核磁数据如下:
[0050]1h nmr(500mhz,cdcl3)δ7.58(d,j=8.0hz,1h),7.51(d,j=7.8hz,1h),7.29(t,j=7.5hz,1h),7.22
‑
7.11(m,2h),6.24(dd,j=15.8,5.3hz,1h),5.23
‑
5.11(m,1h),4.87(s,1h),3.36(d,1h),1.36(d,j=6.3hz,3h),1.32(d,j=6.3hz,3h)ppm.
[0051]
13
c nmr(125mhz,cdcl3)δ172.59,136.30,132.99,130.85,129.18,128.88,127.49,127.25,123.85,71.29,70.32,21.76ppm.
[0052]
实施例4
[0053]
反应方程式如下:
[0054]
将化合物1d(5mmol),三氟甲磺酸钪(0.025mmol)及手性磷酸(0.01mmol)加入反应器中,加入异丙醇50ml,室温下搅拌12小时。反应完成后,旋转蒸发仪浓缩反应液得到的粗产品,用石油醚和乙酸乙酯的体积比30:1的混合溶剂柱层析分离,得到纯2d,产率为98%,ee值为97%。
[0055]
2d的核磁数据如下:
[0056]1h nmr(500mhz,cdcl3)δ7.37(d,j=7.7hz,2h),7.34
‑
7.28(m,2h),7.27
‑
7.22(m,1h),6.80(d,j=15.9hz,1h),6.22(dd,j=15.9,5.4hz,1h),5.33
‑
5.23(m,1h),4.83
‑
4.73(m,1h),3.25(d,j=5.8hz,1h),1.94
‑
1.82(m,2h),1.80
‑
1.67(m,4h),1.65
‑
1.55(m,2h)ppm.
[0057]
13
c nmr(125mhz,cdcl3)δ171.17,134.36,129.97,126.65,126.00,124.71,123.76,77.41,69.37,30.76,30.66,21.72,21.70ppm.
[0058]
实施例5
[0059]
反应方程式如下:
[0060]
将化合物1e(5mmol),三氟甲磺酸钪(0.025mmol)及手性磷酸(0.01mmol)加入反应器中,加入异丙醇50ml,室温下搅拌12小时。反应完成后,旋转蒸发仪浓缩反应液得到的粗产品,用石油醚和乙酸乙酯的体积比30:1的混合溶剂柱层析分离,得到纯2e,产率为93%,ee值为99%。
[0061]
2e的核磁数据如下:
[0062]1h nmr(500mhz,cdcl3)δ7.21
‑
7.18(m,1h),7.14
‑
7.10(m,2h),6.73(dd,j=15.8,1.3hz,1h),6.02(dd,j=15.8,5.5hz,1h),5.10
‑
4.99(m,1h),4.67(dd,j=5.5,1.5hz,1h),3.08(s,1h),1.24(d,j=6.3hz,3h),1.20(d,j=6.3hz,3h)ppm.
[0063]
13
c nmr(125mhz,cdcl3)δ172.91,138.87,126.17,126.14,125.41,125.05,122.98,71.19,70.23,21.77,21.73ppm.
[0064]
由上述实例可以看出,按照本发明所述可实现光学纯的烯丙醇类化合物在双酸催化下的绿色合成。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。