α
‑
突触核蛋白感测薄膜及其制造方法与用途
技术领域
1.本发明是关于一种α
‑
突触核蛋白感测薄膜及其制造方法与用途,是使用α
‑
突触核蛋白印迹于高分子聚合物上,以制得α
‑
突触核蛋白感测薄膜,并用于检测样本中的α
‑
突触核蛋白。
背景技术:
2.α
‑
突触核蛋白(α
‑
synuclein)在人脑组织中的含量高,其在细胞中主要分布于神经细胞的尖端,目前认为α
‑
突触核蛋白与调节多巴胺(dopamine)的释放有关。正常的α
‑
突触核蛋白为可溶性蛋白,但是发生变异后的α
‑
突触核蛋白会大量堆积在神经元内部,且无法被清除,进而影响到脑部的正常功能,甚至会使神经元大量死亡;目前认为α
‑
突触核蛋白与多种神经性退化疾病,例如巴金森氏症(parkinson’s disease)、路易氏体失智症(dementia with lewy bodies)或是多发性系统萎缩症(multiple system atrophy)都有关连性。
3.现今检测血清或血浆中α
‑
突触核蛋白的方法主要是利用抗体检测α
‑
突触核蛋白,例如cn109001452a公开揭露了一种α
‑
突触核蛋白积聚的检测探针,是以磁性颗粒为载体,并在其表面连接α
‑
突触核蛋白单株抗体,以合成一种可检测帕金森氏病的探针;cn109180812a公开揭露了一种识别α
‑
突触核蛋白的抗体,此抗体会结合到α
‑
突触核蛋白的第118~126氨基酸,以诊断α
‑
突触核蛋白的相关疾病。然而,抗体的筛选与制备不易,且以抗体检测α
‑
突触核蛋白的方法所需要的时间也较高,因此在使用上不仅成本较高,且不方便。
技术实现要素:
4.本发明是关于一种α
‑
突触核蛋白感测薄膜及其制造方法与用途,是使用α
‑
突触核蛋白的多肽片段印迹于高分子聚合物上,以制得α
‑
突触核蛋白感测薄膜,并用于检测样本中的α
‑
突触核蛋白。
5.本发明揭露的α
‑
突触核蛋白感测薄膜,包含一基板以及一聚合于基板上的多个α
‑
突触核蛋白辨识聚合物,其中每一所述α
‑
突触核蛋白辨识聚合物表面具有多个可辨识α
‑
突触核蛋白的微孔洞。
6.本发明亦揭露一种制备α
‑
突触核蛋白感测薄膜的方法,是将一α
‑
突触核蛋白多肽与一高分子聚合物单体混合,以电聚合方法设置于一导电基板上,其中所述α
‑
突触核蛋白多肽序列是选自由seq id no:1、seq id no:2、seq id no:3以及seq id no:4所构成的群组。
7.本发明也揭露一种检测α
‑
突触核蛋白的方法,是将一待测样本与一α
‑
突触核蛋白感测薄膜反应,以检测所述待测样本中的α
‑
突触核蛋白,其中所述α
‑
突触核蛋白感测薄膜包含一基板以及一聚合于所述基板上的多个α
‑
突触核蛋白辨识聚合物,且其中每一所述α
‑
突触核蛋白辨识聚合物表面具有多个可辨识α
‑
突触核蛋白的微孔洞。
8.于本发明的一实施例中,基板为导电基板,α
‑
突触核蛋白辨识聚合物为α
‑
突触核蛋白多肽印迹的高分子聚合物。
9.于本发明的一实施例中,导电基板为氧化铟锡(indium tin oxide,ito)基板、pet可挠式导电玻璃基板、掺铝氧化锌(azo)导电基板、掺氟氧化锡(fto)导电基板与二氧化硅导电基板其中至少一种,且所述高分子聚合物的单体为3,4
‑
亚乙基二氧噻吩(3,4
‑
ethylenefioxythiophene,简称edot)以及羟甲基3,4
‑
二氧乙基噻吩(hydroxymethyl 3,4
‑
ethylenedioxy
‑
thiophene,简称edot
‑
oh)其中至少一种。
10.于本发明的一实施例中,α
‑
突触核蛋白多肽序列是选自由seq id no:1、seq id no:2、seq id no:3以及seq id no:4所构成的群组。
11.于本发明的一实施例中,α
‑
突触核蛋白感测薄膜的电流密度介于0.01~500ma。
12.于本发明的一实施例中,待测样本为一血液样本、一尿液样本、一唾液样本、一汗液样本、一泪液样本、一脑脊液样本或是自组织或器官中获得的样本其中至少一种。
13.由此,本发明制得的α
‑
突触核蛋白感测薄膜,是将α
‑
突触核蛋白多肽与高分子材料混合后,经过电聚合反应,以在一基板上形成可辨识α
‑
突触核蛋白的聚合物,其能专一性辨识并结合α
‑
突触核蛋白,且使用上相当方便。
附图说明
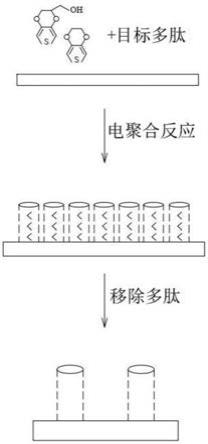
14.图1为本发明α
‑
突触核蛋白感测薄膜的制造方法示意图。
15.图2为本发明α
‑
突触核蛋白感测薄膜的安培法检测分析图。
16.图3为本发明α
‑
突触核蛋白感测薄膜的接触角分析图。
17.图4为本发明α
‑
突触核蛋白感测薄膜的扫描式电子显微镜照片。
18.图5为本发明α
‑
突触核蛋白感测薄膜的扫描式原子力显微镜照片以多肽1、多肽2或多肽3印迹的α
‑
突触核蛋白感测薄膜的电流密度差值分析图。
19.图6为本发明以多肽1、多肽2或多肽3印迹的α
‑
突触核蛋白感测薄膜的电流密度差值分析图。
20.图7为本发明的多肽3印迹的α
‑
突触核蛋白感测薄膜的电流密度差值分析图。
21.图8为本发明α
‑
突触核蛋白感测薄膜的电流密度差值分析图。
22.图9为本发明α
‑
突触核蛋白感测薄膜的电流密度对应扫描速率的平方根分析图。
23.图10为本发明以多肽4与硫化钨印迹的α
‑
突触核蛋白感测薄膜的电流密度分析图。
24.图11为本发明α
‑
突触核蛋白感测薄膜的循环伏安分析图。
25.图12为本发明α
‑
突触核蛋白感测薄膜的氧化峰值(oxidation peak current)电流密度分析图。
26.图13为本发明α
‑
突触核蛋白感测薄膜的交流阻抗(ac impedance)分析图。
27.图14为本发明α
‑
突触核蛋白感测薄膜与snca蛋白质作用的电流密度分析图。
28.图15为本发明α
‑
突触核蛋白感测薄膜的重复使用次数分析图。
29.图16为本发明α
‑
突触核蛋白感测薄膜吸附snca能力分析图(一)。
30.图17为本发明α
‑
突触核蛋白感测薄膜吸附snca能力分析图(二)。
31.图18为本发明α
‑
突触核蛋白感测薄膜吸附snca能力分析图(三)。
具体实施方式
32.为了对本发明的技术特征、目的和有益效果有更加清楚的理解,现对本发明的技术方案进行以下详细说明,但不能理解为对本发明的可实施范围的限定。
33.本发明揭露一种α
‑
突触核蛋白感测薄膜、其制造方法与用途,α
‑
突触核蛋白感测薄膜包含一基板以及聚合于基板上的多个α
‑
突触核蛋白辨识聚合物,其中每一α
‑
突触核蛋白辨识聚合物表面具有多个可辨识α
‑
突触核蛋白的微孔洞;基板为导电基板,可为但不限于氧化铟锡基板、pet可挠式导电玻璃基板、掺铝氧化锌(azo)导电基板、掺氟氧化锡(fto)导电基板与二氧化硅导电基板,且α
‑
突触核蛋白辨识聚合物是为一α
‑
突触核蛋白多肽印迹的高分子聚合物,其中的高分子聚合物的单体可为3,4
‑
亚乙基二氧噻吩以及羟甲基3,4
‑
二氧乙基噻吩其中至少一种,且高分子聚合物是经过电聚合反应后所获得;此外,用于印迹的α
‑
突触核蛋白多肽序列是选自由seq id no:1、seq id no:2、seq id no:3以及seq id no:4所构成的群组,而制得的α
‑
突触核蛋白感测薄膜可用于检测待测样品中的α
‑
突触核蛋白。
34.请参见图1,本发明中制备α
‑
突触核蛋白感测薄膜的方法,是将一目标多肽与一高分子聚合物单体混合,以电聚合方法设置于一导电基板上,其中所述目标多肽为α
‑
突触核蛋白多肽,且序列是选自由seq id no:1、seq id no:2、seq id no:3以及seq id no:4所构成的群组;电聚合反应后,再将目标多肽移除,便可获得α
‑
突触核蛋白感测薄膜。
35.一、α
‑
突触核蛋白感测薄膜的制备
36.准备一可导电的氧化铟锡(ito)基板,并依序以去离子水、异丙醇以及酒精清洁后烘干。
37.首先,于ito基板上以循环伏安法沉积一聚羟甲基3,4
‑
二氧乙基噻吩(poly(edot
‑
oh))薄层,以获得一预沉积基板,制作方法简述如下:将ito基板为工作电极、以银/氯化银(ag/agcl)作为参考电极、以及以含有10mm的edot
‑
oh、100mm的过氯酸锂(liclo4)、以及50mm的十二烷基硫酸钠(sodium dodecyl sulfate,sds)的水溶液作为电解溶液,以
‑
0.6v~1.1v的循环电位、扫描速率100mv/sec的条件,进行小于3次循环的扫描,以在ito基板上沉积一poly(edot
‑
oh)薄层,poly(edot
‑
oh)可以提高后续电聚合反应中、聚合物与ito基板的附着力。
38.接着,将3,4
‑
亚乙基二氧噻吩(edot)、羟甲基3,4
‑
二氧乙基噻吩(edot
‑
oh)以及含有等摩尔数的edot与edot
‑
oh的混合物分别溶解于含有100mm的高氯酸四丁基铵(tetrabutylammonium perchlorate,tbap)的二氯甲烷(ch2cl2)溶剂中,以配置10mm(浓度)的edot溶液、10mm(浓度)edot
‑
oh溶液以及包含10mm的edot/edot
‑
oh混合溶液;接着,先将电极浸泡于0℃的溶液中3分钟,再实施电聚合反应,本实施例的电聚合反应是于固定电压1.1v vs ag/ag
的条件,作用10秒,以于上述的预沉积基板的表面沉积具有微纳米结构的pedot(poly
‑
edot)、poly(edot
‑
oh)以及edot/edot
‑
oh的共聚物。
39.于进行多肽印迹时,先将α
‑
突触核蛋白的多肽,溶解于去离子水中,以获得一α
‑
突触核蛋白多肽溶液,本次实验中分别使用四段α
‑
突触核蛋白的多肽进行印迹,以下称为多肽1、多肽2、多肽3与多肽4,多肽1的序列为seq id no:1,多肽2的序列为seq id no:1,多肽3的序列为seq id no:3,以及多肽4的序列为seq id no:4。
40.接着将上述配置的edot溶液、edot
‑
oh溶液以及edot/edot
‑
oh混合溶液,分别与四种α
‑
突触核蛋白多肽溶液混合,并使α
‑
突触核蛋白多肽混合溶液中的多肽浓度为0.01mg/
ml,以获得一α
‑
突触核蛋白多肽混合溶液;接着进行电聚合反应,步骤简述如下:以上述准备的可导电的ito基板为工作电极(working electrode),以白金电极作为辅助电极(counter electrode),以及使用银/氯化银(ag/agcl)电极作为参考电极,并以上述的α
‑
突触核蛋白多肽混合溶液作为导电液,固定电压1.1v vs ag/ag
的条件,进行电聚合反应,接着取出氧化铟锡基板,依序以去离子水、5(v/v)%酒精水溶液交替清洗两次,以洗去未聚合化合物单体以及多肽,便可获得α
‑
突触核蛋白感测薄膜(后续简称mips);在α
‑
突触核蛋白感测薄膜上形成有多个α
‑
突触核蛋白辨识聚合物,且每一α
‑
突触核蛋白辨识聚合物上具有多个可辨识α
‑
突触核蛋白的微孔洞。此外,同时制备仅使用edot溶液、edot
‑
oh溶液以及edot/edot
‑
oh混合溶液、而没有加入多肽溶液进行电聚合反应的组别,以获得一无印迹感测薄膜,以作为对照组,后续将其简称为nips。
41.此外,为了区分不同材料与α
‑
突触核蛋白多肽制备的α
‑
突触核蛋白感测薄膜,后续的mips将以“mips_高分子材料_多肽种类”方式呈现,例如“mips_edot_多肽1”代表用于电聚合的高分子材料为edot,且是使用多肽1作为印迹模板,以此类推。
42.接着,将面积1平方公分的α
‑
突触核蛋白感测薄膜作为工作电极,以白金电极、钨钼合金电极或是陶瓷铜合金作为辅助电极(counter electrode),以及使用银/氯化银电极、铜钨合金、银钨合金、钨钼合金或铬铜合金等等作为参考电极,再将三种电极浸泡于铁氯化钾/亚铁氰化钾电解液中,再以恒电位仪进行电化学测量分析;以下实施例中,辅助电极为白金电极、参考电极为银/氯化银电极。
43.首先,请参见图2中的(a),为不同单体溶液以及以多肽1搭配不同单体溶液,于给予1.1v的电压强度进行电聚合反应时,电聚合过程中不同时间的电流密度分析图,于多肽1印迹的组别中,mips_edot
‑
oh具有最高的电流密度,约为350~400μm/cm2,mips_edot的电流密度最低,约为200~250μm/cm2;再请参见图2中的(b),为各感测薄膜于通电后20秒时的电流密度,于无多肽印迹的组别中,nips_pedot的电流密度约为50μm/cm2,低于mips_pedot的电流密度,于另外二组别中,经多肽印迹所制得的感测薄膜(mips),其电流密度都高于无印迹感测薄膜(nips)。
44.请再参见图3中的(a),为nips_edot
‑
oh以及mips_edot
‑
oh的水接触角分析图,根据图3中的(a),在感测薄膜合成后、未移除模板的状态下,nips_edot
‑
oh的接触角约为35.0
±
1.1
°
,低于mips_edot
‑
oh感测薄膜的接触角(54.2
±
0.6
°
),表示mips_edot
‑
oh感测薄膜的表面疏水性较强;在将模板移除后,nips_edot
‑
oh与mips_edot
‑
oh的接触角都增加,表示二者的表面疏水性也都提高了;又,将nips_edot
‑
oh与mips_edot
‑
oh与印迹模板作用后,二者的接触角度相近,都约为102.9
±
3.7
°
。再请参见图3中的(b),为以5(v/v)%乙醇清洗后的mips_edot
‑
oh感测薄膜的化学分析电子光谱的分析结果,结果显示5(v/v)%乙醇确实能清洗掉所有的印迹模板。
45.请参见图4,为nips_edot
‑
oh与mips_edot
‑
oh的扫描式电子显微镜观察照片,照片中较亮的区域具有高度的光散射性,通常代表粗糙度较高的区域;图4中的(a)是mips_edot
‑
oh于模板未移除时的扫描式电子显微镜照片,图4中的(b)是nips_edot
‑
oh于模板未移除时的扫描式电子显微镜照片,都呈现出类似的管状构造,表示电聚合过程中,模板多肽的存在并不会影响edot
‑
oh聚合物纳米结构的形成。
46.图4中的(c)是mips_edot
‑
oh于移除模板后的扫描式电子显微镜照片,图4中的(d)
是nips_edot
‑
oh于移除模板后的扫描式电子显微镜照片,二者也具有类似的管状构造;图4中的(e)是mips_edot
‑
oh重新与模板作用后的扫描式电子显微镜照片,图4中的(f)则是nips_edot
‑
oh重新与模板作用后的扫描式电子显微镜照片,二者也具有类似的管状构造。
47.又,图5为nips_edot
‑
oh与mips_edot
‑
oh的原子力显微镜(atomic force microscope)观察照片,图5中的(a)是未移除模板的mips_edot
‑
oh,图5中的(b)是未移除模板的nips_edot
‑
oh,图5中的(c)是移除模板后的mips_edot,图5中的(d)是移除模板后的nips_edot,图5中的(e)是重新与模板结合后的mips_edot,图5中的(f)则是重新与模板结合后的nips_edot,于所有的这片中都可以观察到管状构造,表示模板多肽的存在并不会影响电聚合过程edot
‑
oh聚合物纳米结构的形成。
48.将制得的α
‑
突触核蛋白感测薄膜以循环伏安法分析,扫描电压为
‑
0.85~0.8伏特(v),扫描速率为0.1v/秒,并将所得到的结果计算印迹效率;印迹效率的计算公式为:
49.印迹效率(α)=mips电流量/nips电流量
50.请参见图6中的(a),为使用多肽1印迹所得到的mips,mips_edot_多肽1的电流密度差值(current density differences,δcurrent density)为0.586ma/cm2,而nips_edot的电流密度差值则为0.361ma/cm2;又,mips_edot/edot
‑
oh_多肽1的电流密度差值也为0.572ma/cm2,而nips_edot/edot
‑
oh的电流密度差值则为0.552ma/cm2;此外,mips_edot_oh
‑
多肽1的电流密度差值为0.439ma/cm2,而nips_edot的电流密度差值则为0.173ma/cm2;而各组的印迹效率分别为:edot_多肽1的α值为1.623,edot/edot
‑
oh_多肽1的α值为1.036,以及edot
‑
oh_多肽1的α值为2.537,表示在使用多肽1为印迹模板的各组别中,以edot
‑
oh作为高分子原料所获得的α
‑
突触核蛋白感测薄膜具有较佳的印迹效率。
51.请参阅图6中的(b),为使用多肽2印迹所得到的mips,mips_edot_多肽2的电流密度差值为0.369ma/cm2,而nips_edot的电流密度差值则为0.203ma/cm2;又,mips_edot/edot
‑
oh_多肽2的电流密度差值也为0.740ma/cm2,而nips_edot/edot
‑
oh的电流密度差值则为0.475ma/cm2;此外,mips_edot
‑
oh_多肽2的电流密度差值为0.530ma/cm2,而nips_edot的电流密度差值则为0.444ma/cm2;而各组的印迹效率分别为:edot_多肽2的α值为1.82,edot/edot
‑
oh_多肽2的α值为1.56,以及edot
‑
oh_多肽2的α值为1.19,表示在使用多肽2为印迹模板的各组别中,以edot作为高分子原料所获得的α
‑
突触核蛋白感测薄膜具有较佳的印迹效率。
52.请再参阅图7,为使用多肽3印迹所得到的mips,mips_edot_多肽3的电流密度差值为0.6205ma/cm2,而nips_edot的电流密度差值则为0.565ma/cm2;又,mips_edot/edot
‑
oh_多肽3的电流密度差值为0.688ma/cm2,而nips_edot/edot
‑
oh的电流密度差值则为0.602ma/cm2;此外,mips_edot
‑
oh_多肽3的电流密度差值为0.333ma/cm2,而nips_edot的电流密度差值则为0.144ma/cm2;各组的印迹效率分别为:edot_多肽3的α值为1.10,edot/edot
‑
oh_多肽3的α值为1.14,以及edot
‑
oh_多肽3的α值为2.31,表示在使用多肽3为印迹模板的各组别中,以edot
‑
oh作为高分子原料所获得的α
‑
突触核蛋白感测薄膜具有较佳的印迹效率。
53.再请参见图8,再将edot
‑
oh_多肽1、edot_多肽2与edot
‑
oh_多肽3组别的α
‑
突触核蛋白感测薄膜进行检测,mips_edot
‑
oh_多肽1的电流密度差值为0.439ma/cm2,而nips_edot
‑
oh的电流密度差值则为0.173ma/cm2,印迹效率α值为2.54;mips_edot_多肽2的电流
密度差值为0.369ma/cm2,而nips_edot的电流密度差值则为0.203ma/cm2,印迹效率α值为1.82;mips_edot
‑
oh_多肽3的电流密度差值为0.333ma/cm2,而nips_edot
‑
oh的电流密度差值则为0.144ma/cm2,印迹效率α值为2.31;此结果表示以edot
‑
oh作为高分子原料、以多肽1作为印迹模板所获得的α
‑
突触核蛋白感测薄膜具有较佳的印迹效率。
54.请再参见图9,为mips_edot
‑
oh_多肽1(图中标示为mips)与nips_edot
‑
oh(图中标示为nips)的电流密度对应扫描速率的平方根的分析图,是用于分析二者电流峰值(peak current)的线性关系,又根据randles
‑
sevcik方程式,可计算出mips_edot
‑
oh_多肽1的表面积为1.746cm2,以及nips_edot
‑
oh的表面积为1.726cm2。
55.又,图10为使用50μg的多肽4与50μg硫化钨(ws2)进行印迹所获得α
‑
突触核蛋白感测薄膜(mips_多肽4 ws2),以及使用无印迹感测薄膜(nips),感测浓度介于0.001~1000pg/ml的α
‑
突触核蛋白,再进行电流密度差值分析的结果,根据图10,mips_多肽4 ws2的印迹效率α值为2.3。
56.请参见图11中的(a),为使用浓度为0.000065nm~65nm的多肽1溶液,与mips_edot
‑
oh_多肽1作用后,再以循环伏安法分析,以获得的循环伏安分析图,图11中的(b)则为nips_edot
‑
oh与0.000065nm~65nm的多肽1溶液作用后的循环伏安分析图,其中mips_edot
‑
oh_多肽1的氧化峰值为410
‑
420mv,且还原电压介于90
‑
100mv;根据图11中的(a),未与多肽1作用的mips_edot
‑
oh_多肽1,其氧化峰值电流密度为7.4ma/cm2,但与多肽1作用后,其氧化峰值电流密度会逐渐上升;又根据图11中的(b),未与多肽1作用的nips_edot
‑
oh,其氧化峰值电流密度为6.9ma/cm2,但与0.65nm(1.0ng
·
ml
‑1)多肽1作用后,其氧化峰值电流密度会上升,为7.1ma/cm2。
57.再请参见图12中的(a),为使用不同聚合物单体、以多肽1印迹获得的α
‑
突触核蛋白感测薄膜,与不同浓度的多肽1作用后,以循环伏安分析法所获得的氧化峰值(oxidation peak current)电流密度的变化曲线图,其中有多肽印迹所获得的α
‑
突触核蛋白感测薄膜,与无多肽印迹的组别相比,都具有较高的氧化峰值电流密度,且各组别的α
‑
突触核蛋白感测薄膜,与越高浓度的多肽1作用后,其电流密度氧化峰值也都会随之上升,表示所制备的α
‑
突触核蛋白感测薄膜都具备有感测α
‑
突触核蛋白的能力;又,mips_edot
‑
oh
‑
多肽1与nips_edot
‑
oh,二者的电流密度氧化峰值差异最大。再请参见图12中的(b),为以多肽1印迹的各种α
‑
突触核蛋白感测薄膜(mips),以及无印迹感测薄膜(nips),与0.65nm的多肽1溶液作用后,所获得的电流密度分析图,其中以mips_edot
‑
oh的电流密度为高,次高者为mips_edot/edot
‑
oh,而以mips_edot的电流密度最低;但是在无多肽印迹的组别中,nips_edot
‑
oh的电流密度最低、nips_edot/edot
‑
oh与nips_edot的电流密度则近似。
58.请参见图13,为mips_edot
‑
oh
‑
多肽1与nips_edot
‑
oh的奈奎斯特图(nyquist plot),是用于表示其交流阻抗(ac impedance)特性,于印迹后洗去多肽模板(图中标示为“after washing”),以及再与多肽1结合后(图中标示为“rebound”)的电阻抗讯号测量结果;其中,nips_edot
‑
oh的电阻抗讯号,于洗去多肽模板以及与多肽1结合后,都无明显变化,但是mips_edot
‑
oh
‑
多肽1于结合多肽1后,其交流电阻抗讯号会下降。
59.请参见图14,为nips_edot
‑
oh与mips_edot
‑
oh_多肽1,分别与0.65nm的多肽1、于第53个氨基酸丙氨酸由(alanine)突变成苏氨酸(threonine)的α
‑
突触核蛋白(snca_a53t)、以及于第64号氨基酸由谷氨酸(glutamic acid)突变成赖氨酸(lysine)以及第53个
氨基酸丙氨酸由(alanine)突变成苏氨酸(threonine)的双突变的α
‑
突触核蛋白(snca_e64k/a53t)作用后,所检测到的电流密度差值,与突变scna作用的mips_edot
‑
oh_多肽1,其电流密度差值有明显下降的情形。
60.请参见图15,为本发明mips_edot
‑
oh_多肽1的重复使用次数分析图,将mips_edot
‑
oh_多肽1与0.65nm(1ng/ml)的多肽1溶液作用后,测量其电流密度,以获得第一次的测量结果;接着以清水清洗mips_edot
‑
oh_多肽、阴干,再与1ng/ml的多肽1溶液作用,再测量电流密度,以获得第二次的测量结果;重复上述步骤,总共进行六次的测量,并将第一次测量结果视为100%,计算第2~6次测量结果的相对电流(relative current);根据图15,六次测量结果的差距都不大,只有第六次测量结果的相对电流有些微下降的情形,表示本发明的α
‑
突触核蛋白感测薄膜确实可以重复使用,且重复使用后的测量结果也具有可信度。
61.请再参见图16,为本发明mips_edot
‑
oh_多肽1,以及nips_edot
‑
oh,与不同浓度的α
‑
突触核蛋白(snca)溶液,分别作用5分钟、10分钟与20分钟后,其电流密度差值的测量结果;图16显示,作用20分钟后,mips_edot
‑
oh_多肽1具有最高的电流密度差值,且与nips_edot
‑
oh具有明显差异,其次为作用10分钟的组别,也与nips_edot
‑
oh具有明显差异;而作用5分钟的组别,mips_edot
‑
oh_多肽1,以及nips_edot
‑
oh的电流密度差值并无明显差异。
62.接着请参见图17,是先将mips_edot
‑
oh_多肽1,以及nips_edot
‑
oh分别与不同浓度的α
‑
突触核蛋白(snca)作用,之后再以elisa的方式检测mips_edot
‑
oh_多肽1,以及nips_edot
‑
oh可结合的snca量;图17的结果显示,mips_edot
‑
oh_多肽1的snca最大结合量约为3.65μg/cm2。
63.接着,使用以snca未突变(图中标示为“wt”)以及snca基因具有三重复突变(图中标示为“3x”)的两株诱导性多能干细胞株(induced pluripotent stem cells),先将其诱导成腹侧神经上皮干细胞(ventralized neural epithelial stem cell,简称为vnescs),再使vnescs发育成中脑类器官(midbrain organioid);将中脑类器官培养持续于培养基中,每三日换一次培养基,并于培养后第29日以及第38日收集培养基,进行后续试验。图18中的(a)为以mips_edot
‑
oh_多肽1测量培养基中α
‑
突触核蛋白(snca)浓度的试验结果,培养后第29日,wt组培养基中的snca浓度为186.7(
±
11.1%)fm,而3x组培养基中的snca浓度为228.2(
±
12.1%)fm;培养后第38日,wt组培养基中的snca浓度为172.9(
±
8.0%)fm,而3x组培养基中的snca浓度为325.0(
±
8.5)fm,显然3x组的中脑类器官确实表现较高量的snca。图18中的(b)是将所培养的中脑类器官,以免疫荧光染色法检测其中的snca表现情形,表现有snca的区域会呈现红色;根据图18中的(b),wt组的中脑类器官内并无明显表现snca,但是3x组的中脑类器官内并确实可检测到大量的snca。
64.此外,本发明制得的α
‑
突触核蛋白感测薄膜,可用于检测多种样本中的α
‑
突触核蛋白含量,这些样本可为但不限于血液样本、尿液样本、唾液样本、脑脊液样本、或是自组织或器官中萃取得到的样本内的α
‑
突触核蛋白含量,使用方便且准确性高。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。