1.本发明属于医疗图像处理技术领域,涉及一种视网膜眼底图像分割的方法,特别涉及一种基于深度卷积神经网络的眼底视网膜图像分割方法。
背景技术:
2.视网膜图像已广泛用于心血管和眼科疾病的诊断、筛查和治疗,包括老年黄斑变性、青光眼、高血压、动脉硬化和心血管疾病等全身性疾病。血管、视盘和视杯分割是定量分析视网膜图像所需的基本步骤。首先,视盘视杯的分割通常用于青光眼的检测,视神经乳头评估方法是一种比较方便且被临床医生广泛接受也使用的,这种方式通过使用垂直杯盘比的比率计算青光眼的风险,因此准确的视盘视杯分割至关重要。其次,视网膜图像中的上下支动脉血管和分叉出的毛细血管共同构成了各类方法需要学习的数据分布。通过视网膜血管形态的变化可以发现人体内的一些病理性疾病,诸如糖尿病性视网膜疾病、动脉粥样硬化等等。例如,糖尿病视网膜疾病会导致由于高血糖和后期高血压引起的视力丧失。糖尿病视网膜病变是全球老年人失明的主要原因。世界卫生组织建议每年进行眼部筛查,因为如果在早期发现糖尿病性视网膜疾病,可以通过激光疗法进行有效治疗。因此对视网膜血管形态的变化进行观测能够早日诊断和治疗这些危及人体健康的疾病。
3.由于大量患者需要进行检测并接受治疗,手动分割视网膜图像中的视盘和视杯是一项繁琐的任务,需要经验和技巧,且不适合这种大规模的检查,造成许多患者无法获得足够的治疗。其次医学图像采集的成本昂贵,过程复杂,在大多数情况下医疗图像的训练缺乏标准的标注。因此需要研究一种对视网膜图像中的血管、视盘和视杯进行自动化分割的方法。使用深度卷积神经网络强大的特征学习能力对视网膜图像中的病变组织进行分割,可以有效解决视网膜图像辅助诊断中存在的诸多问题,并减少医务人员工作量,同时可为医务人员提供有价值的医疗影像参考。
4.现有技术中已有一些方法,将卷积神经网络(convolutional neural networks,cnns)成功应用于自动分割视网膜血管。这些方法已经证明了有助于恢复网络输出处的全局空间分辨率。然而,这些方法存在一定的问题:1)简单图像预处理方法不能有效地利用特征图的结构信息,可能会阻碍分割性能;2)使用下采样的方式提高感受野,但是联合分割视盘和视杯时,由于标签图上的视盘区域比较小,过大的下采样因子会造成这些特征信息的损失;3)对于过大的分割区域,这些方法中的感受野不够大,不能够充分的对全局信息进行理解,对于一些大的分割区域不能够准确的识别;4)这些方法都是使用反卷积的方式进行上采样,这样会增加模型的参数和计算量,影响模型的性能。
技术实现要素:
5.本发明的目的是提供一种基于深度卷积神经网络的眼底视网膜图像分割方法,减少模型参数数量、提高模型的感受野和对上下文理解,提高视网膜血管、视盘和视杯分割模型准确率和速度。
6.为了解决上述技术问题,本发明提供了如下的技术方案:
7.本发明一种眼底视网膜图像预处理的方法,包括以下步骤:
8.a、获取视网膜图像数据集;
9.b、预处理:对视网膜图像依次执行灰度处理、归一化、对比度受限的自适应直方图均衡化和伽马非线性化处理,得到预处理图像。
10.优选的,所述灰度处理包括以下步骤:
11.采用rgb三个分量将视网膜图像分解为红色r通道、绿色g通道、蓝色b通道,对三个通道的图像按比例进行融合转换为灰度图像;
12.转换公式如下:
13.igray=0.299
×
r 0.587
×
g 0.114
×
b
14.式中:r、g、b分别表示r通道、g通道和b通道的值;
15.所述归一化包括以下步骤:
16.令x={x1,x2,...,x
n
}为图像数据集;使用z分数归一化方法对数据集x进行维度归一化;z分数归一化公式如下:
17.xnorm=(x-μ)/σ
18.式中,μ是x的均值,σ是x的标准差;此时,x中存在正负值,且x的均值为0、标准差为1;
19.再对数据集x中的每张图像数据通过最小-最大规范化,将x的值重新映射到0~255的范围内;最小-最大规范化公式如下:
[0020][0021]
式中,x
i
∈x
norm
,i∈[1,2,...,n]
[0022]
所述对比度受限的自适应直方图均衡化采用clahe算法来增强整个数据集的血管与背景对比度,再由伽马非线性化对图像中的辉度或是三色刺激值进行非线性运算,得到预处理后的图像,所述伽玛值为1.2。
[0023]
本发明基于深度卷积神经网络的视盘和视杯图像分割方法,包括以下步骤:a1、采用上述所述的图像预处理的方法对视盘和视杯进行图像预处理;
[0024]
b1、生成器:对预处理后的图像采用不同扩充率的卷积层进行级联卷积,输出特征图,将特征图经过尺度重构对特征图中的信息进行周期性重排,生成与目标尺寸相同的视盘和视杯的分割图像;
[0025]
c1、判别器:构建一个与生成器具有相同的卷积单元形式的判别器,判别器与生成器构成生成对抗网络模型,自动调整调节参数,输出生成器的最终图像。
[0026]
优选的,所述生成器包括编码器和解码器,所述生成器的训练数据样本为x
i
为眼底图像,y
i
为视盘视杯标签图;h为图片长度,w为图片宽度,c1为x
i
的通道数,c2为y
i
的通道数,所述编码器采用级联扩充卷积来进行下采样,得到输出特征图所述解码器采用尺度重构进行下采样,将特征图u转换成与y
i
相同的尺寸,得到尺寸相同的特征图生成器输出分割结果c(x
i
);
[0027]
所述判别器对训练数据样本图像集和生成器生成的图像集进行判别,若判别器将训练数据样本图像集和生成器生成的图像集归为一类,则调整判别器的调节参数,若判别器将训练数据样本图像集和生成器生成的图像集分为两类,则调整生成器的调节参数,并令生成器重新生成分割图像,生成器的最终图像的计算公式为:
[0028][0029]
式中,θ
c
表示编码器的参数;θ
d
表示解码器的参数;e
x,y
[]代表期望值。
[0030]
优选的,所述级联卷积每次级联n个扩充卷积层,卷积核的大小为k
×
k,扩充率分别为[r1,
…
,r
i
,
…
,r
n
],经过n个卷积层后,感受野区域内的所有特征信息能够完全覆盖;
[0031]
将扩充卷积核中第i层的扩充率的最大值定义为r
i
,且扩充率r
i
≤r
i
,r
i
的计算公式为:
[0032][0033]
并且(r
1-1) (r
2-1)<k,当r
i
>0,r
i
≠r
i 1
;每组内的扩充率r
i
不能成公因子关系;r
i
代表扩充卷积核中第i层的扩充率,k为卷积核的大小。
[0034]
本发明基于深度卷积神经网络的视网膜血管图像分割方法,包括以下步骤:
[0035]
1、采用上述所述的图像预处理的方法对视网膜血管进行图像预处理;
[0036]
2、将预处理后的图像经过平均池化层对图像进行下采样,形成不同层次的下采样图像,然后使用普通卷积层来扩展下采样图像的通道,将该层次扩充后的下采样图像与上一层次多路径fcn模型编码器的输出图像融合为该层次的输入图像输入至多路径fcn模型编码器中;
[0037]
3、多路径fcn模型编码器对输入的图像进行编码,获取视网膜图像中的血管特征图像,形成不同层次的血管特征图像,将该层次的血管特征图像与下一层次多路径fcn模型解码器的输出图像融合为该层次的输入图像输入至多路径fcn模型解码器中,多路径fcn模型解码器为编码器的逆运算,对输入的图像进行解码,形成不同深度的输出特征图像;
[0038]
4、将不同深度的输出特征图像使用上采样方法将特征扩展与输入图像相同的大小,然后将它们分别输入到不同的卷积层进行通道压缩,再使用softmax函数中进行分类,将得到的多个概率图融合为一张双通道的概率图,再进行阈值分割以得到最终的血管分割图。
[0039]
优选的,所述多路径fcn模型由两个编码器路径和两个解码器路径组成,所述编码器路径和解码器路径均包括卷积层、残差模块、批归一化层和relu激活层,所述编码器路径利用残差模块和卷积层生成一组编码器特征图,并使用批处理归一化层对每层特征图进行归一化,然后使用relu激活函数将其激活,所述解码器路径使用反卷积层和残差模块对编码器生成的图像进行解码,并使用批处理归一化层归一化每个层特征图,然后使用relu激活函数进行激活。
[0040]
与现有技术相比,本发明的有益效果如下:
[0041]
1)多种深度神经网络结合,拟解决眼底图像分割中不同方面的问题。提出多种以深度卷积网络为基础,结合降噪卷积自动编码器、卷积网络、注意力机制等模型的新型深度模型。以期新模型通过提出的数据增强方法可以实现原始视网膜图像去噪、增强、特征映射、分割等处理功能。
[0042]
2)具有实用价值和参考价值的医学图像分割方案。构建多种针对不同医学图像的分割方法。可以在分割得到相关组织的基础上,结合整幅图像的整体特征,对患者进行辅助诊断,具有重要的实用价值。对于医务人员而言,本发明分割方法的各个阶段成果都具有很大的参考价值。在往后的科研方面,本发明中的多种深度学习算法资料也具有很大的参考价值。
[0043]
3)提出了一种新型视网膜图像预处理模型,有效提升了模型对图像特征的提取和识别能力;通过堆叠扩充卷积用来提高模型对局部上下文信息的理解能力,并且保持感受野内特征信息的关联性;使用尺度重构层代替反卷积、双线性插值等上采样方式,不需要带入额外的参数和计算量,又保留着学习能力对细节信息进行还原。
附图说明
[0044]
附图用来提供对本发明的进一步理解,并且构成说明书的一部分,与本发明的实施例一起用于解释本发明,并不构成对本发明的限制。在附图中:
[0045]
图1是本发明分割方法对眼底视网膜图像的数据预处理图。
[0046]
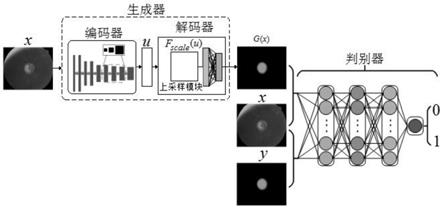
图2是视盘和视杯分割网络结构图。
[0047]
图3是本发明分割方法中采用的级联扩充卷积结构图。
[0048]
图4是本发明分割方法中采用的尺度重构层结构图。
[0049]
图5:视网膜血管分割网络结构图;
[0050]
图6:视盘和视杯分割结果图;
[0051]
图7:视网膜血管分割结果图。
具体实施方式
[0052]
以下结合附图对本发明的优选实施例进行说明,应当理解,此处所描述的优选实施例仅用于说明和解释本发明,并不用于限定本发明。
[0053]
此外,如果已知技术的详细描述对于示出本发明的特征是不必要的,则将其省略。
[0054]
实施例1
[0055]
本发明分割方法是基于深度卷积神经网络的方法,涉及眼底视网膜图像的数据预处理模型、端对端的多标签深度卷积网络模型和模型在眼底视网膜血管、视盘和视杯分割上的应用。
[0056]
本发明分割方法采用深层卷积神经网络来映射医学图像中血管组织、视盘视杯组织和病变组织的特征,使用卷积网络对图像进行分割。此外,为增加分割准确率,使用眼底视网膜图像的数据预处理新方法对图像增强处理;使用端到端的深度卷积网络解决细小血管分割的问题,获取病变区域深层显著特征并将其可视化;使用多种深度神经网络结合的方法应对各类医学图像像素较大引发的一系列问题。本发明分割方法具体按以下步骤进行:
[0057]
1)选取数据集
[0058]
视网膜血管分割数据集:digital retinal images for vessel extraction(drive)、structured analysis of the retina(stare)、chase_db1(chase)。这三个数据集的视网膜图像分别在不同采集设备、光线照明等条件下获得的,这可以验证本文所提出框架的鲁棒性和泛化性。drive数据集包含40张图像,分辨率为565
×
584px;stare数据集有20张700
×
605px的图像,其中有一半图像中存在不同情况的病变;chase数据集由28张图像组成,分辨率为999
×
960px;
[0059]
视盘视杯分割数据集:drishti-gs1数据集中总共包含101张眼底图像,31张正常的和70张患病;其中训练集包含50张图像、测试集包含51张图像;所有图像视盘和视杯区域均由4位具有不同临床经验的眼科专家进行标记;
[0060]
2)眼底视网膜图像的数据预处理新方法
[0061]
在对图像实施适当的预处理之后,模型可以更有效地学习其蕴含的数据分布。本发明分割方法提出了四步预处理策略来依次处理图像。图1显示了不同处理下的图像。第一种预处理策略是将彩色图像转换为灰度图像。通过将图1(a)所示的彩色的视原始网膜图像分解为图1(b)所示的r通道、图1(c)所示的g通道、图1(d)所示的b通道。可以看出,g通道具有更高的血管和背景区分度,而r通道和b通道中的噪声更多、对比度更低。虽然r通道和b通道存在着更多的噪声,但是依旧有相应的血管特征信息。因此,为了保证特征信息损失最低和使血管背景之间的区分度更高,以g通道为基础,将r通道和b通道按比例融入g通道以转化为灰度图像。转换公式如下:
[0062]
i
gray
=0.299
×
r 0.587
×
g 0.114
×
b
ꢀꢀꢀ
(1)
[0063]
(1)式中:r、g、b分别表示r通道、g通道和b通道的值;根此(1)式,转换后的图1(e)所示的灰度图像中,原图像的r通道、g通道和b通道分别占29.9%、58.7%和11.4%,这样既保留了r通道和b通道的部分特征信息,又最大限度的利用了g通道的信息。
[0064]
第二种预处理策略是数据归一化。令x={x1,x2,...,x
n
}为图像数据集;首先使用z分数归一化方法对数据集x进行维度归一化。z分数归一化公式如下:
[0065]
x
norm
=(x-μ)/σ
ꢀꢀꢀ
(2)
[0066]
(2)式中,μ是x的均值,σ是x的标准差。此时,x中存在正负值,且x的均值为0、标准差为1。接下来对数据集x中的每张图像数据通过最小-最大规范化,将x的值重新映射到0~255的范围内。最小-最大规范化公式如下:
[0067][0068]
(3)式中,x
i
∈x
norm
,i∈[1,2,...,n]。数据归一化的效果如图1(f)。图1(f)通过归一化减少了眼底视网膜图像由于光线不均匀造成的干扰,使得图片可以抵抗几何变换的攻击,能够找出图片中的那些不变量,有助于视网膜血管细节的分割。
[0069]
第三种预处理策略是使用clahe来增强整个数据集的血管与背景对比度。clahe图像如图1(g)所示,它是在图1(f)的基础之上来使用clahe来增强视网膜血管与背景的对比度,凸显出细小血管。最后一种预处理策略是使用伽马非线性化(gamma nonlinearity)来处理图1(g)所示图像中的辉度或是三色刺激值所进行的非线性的运算,通过平衡因光照不
均匀导致的色彩范围来扩大不同类别的像素值之间的差异。在本发明分割方法中,伽玛值设置为1.2,对图像进行处理后的可视化如图1(h)所示。本发明使用opencv来实现clahe和伽马非线性化策略。
[0070]
针对不同数据集采集设备、拍摄角度、照明等不同的问题,通过对视网膜图像执行灰度处理、归一化、对比度受限的自适应直方图均衡化和伽马非线性化这四步处理,增强血管与背景的区分度,降低采集过程中其他干扰因素带来的影响。通过对比实验对每一步预处理的效果进行验证,证明了这四步预处理策略具有积极有效的影响,能够提升模型对图像特征的提取和识别能力。
[0071]
3)眼底视盘和视杯分割新模型
[0072]
视盘和视杯的分割是目前仅由专业人员进行的一项非常耗时的任务。利用计算机来自动分割视盘和视杯很具吸引力,因为计算机比人类分割更客观、更快。本发明分割方法使用一个端对端的多标签深度学习模型实现对眼底图像中的视盘和视杯同时进行分割,该多标签深度学习模型的网络结构如图2所示,主要由生成器(c)和判别器(d)两个网络结构组成。c为一个全卷积分割网络,主要由编码器和解码器两组成;c的训练数据样本为x
i
为眼底图像,y
i
为视盘视杯标签图。h为图片长度,w为图片宽度,c1为x
i
的通道数,c2为y
i
的通道数。编码器使用眼底图像x
i
作为输入,对其进行特征的提取,为了提高特征提取的能力,本发明分割方法减少了下采样因子进行密集特征采样,引入扩充卷积扩大感受野,并级联不同扩充率的扩充卷积避免了扩充卷积中存在的
‘
网格化’问题。编码器最终输出特征图解码器模块使用特征图u作为输入,通过尺度重构的方式代替上采样,将特征图u转换成与y
i
相同的尺寸,通过应用尺度重构后输出尺寸相同的特征图最终c输出分割结果c(x
i
)。d用于判别
‘
真/伪’(1/0),模型根据输出的结果d(x,*),*为两种,分别为y
i
和c(x
i
)来,分别引导c进行训练。训练时,d的输入样本图像分两种:和因此输出也分两种:当输入(x,y)时,输出d(x,y)=1;当输入(x,c(x))时,输出d(x,c(x))=0。模型最终的目标函数如下:
[0073][0074]
(4)式中,θ
c
表示编码器的参数;θ
d
表示解码器的参数;e
x,y
[]代表期望值。
[0075]
级联扩充卷积:由于较大的感受野可以促进模型对眼底图像全局上下文的理解,更加准确地辨别视盘视杯区域与病灶区域之间的差异。通常,标准的网络结构fcn中使用池化层(pooling)或者带步伐的卷积层进行下采样来扩大模型的感受野。但过多的下采样操作会造成特征信息的损失,不利于模型的学习,且会增加上采样的复杂性。
[0076]
为了缓解上述问题,让模型在减少下采样操作的同时保持模型感受野不变或者更大。本发明分割方法采用不同扩充率的卷积层进行级联,如图3中的(a)所示。假设每次级联n个扩充卷积层,卷积核的大小为k
×
k,扩充率分别为[r1,
…
,r
i
,
…
,r
n
],经过n个卷积层后,感受野区域内的所有特征信息能够完全覆盖。
[0077]
将扩充卷积核中第i层的扩充率的最大值定义为:
[0078][0079]
并且(r
1-1) (r
2-1)<k,当r
i
>0,r
i
≠r
i 1
。因此扩充率r
i
≤r
i
。但是,每组内的扩充率r
i
不能成公因子关系(例如2,4,8等)。r
i
代表扩充卷积核中第i层的扩充率,k为卷积核的大小。
[0080]
在图3(b)中,设置(r1,r2,r3)=(1,2,5),三个卷积核的大小(k
r1
,k
r2
,k
r3
)=(3,5,11),经过一系列的卷积操作后,l4层中特征值p4的感受野r
b
=17,对p4有贡献的特征来自r
b
区域内的所有特征,且没有出现图3(a)中有空缺部分的情况。使得有效的特征值占的比例为100%,保证了各个特征值之间的关联性。因此,按照定义合理的设置r1,r2,r3的值,可以使得最终的卷积核可以完全取得与其感受野区域内所有特征值的关联性,从而有效的缓解
‘
网格化’的问题。图3中f
a
代表扩充率(r1,r2,r3)=(2,2,4)的特征值的贡献区域,f
b
代表扩充率(r1,r2,r3)=(1,2,5)的特征值的贡献区域。
[0081]
尺度重构层:为了提高模型的性能,减少模型的参数和计算量,本发明分割方法使用尺度重构层的方式进行上采样,尺度重构层通过对特征图中的信息进行周期性重排,将特征图的通道数进行压缩从而对高和宽进行扩充达到上采样的效果,如图4所示。假设输入的特征图的维度为w
×
h
×
(d
×
d
×
c),d为下采样因子,通过尺度重构层得到的特征图维度为(w
×
d)
×
(h
×
d)
×
c。尺度重构层作为上采样方式存在以下优势:1、与反卷积方式相比,尺度重构层没有增加额外的参数和计算开销,可以提高了模型的速度。并且尺度重构层是可以学习的,因此能够捕获和恢复损失下采样中损失的详细信息。2、与双线性插值方式相比,双线性插值进行上采样方式虽然不需要带入额外的参数和计算量,但是不能够进行学习,无法精确的还原损失的特征信息。因此尺度重构层结合着两者的优点。
[0082]
视盘和视杯的准确分割对于帮助医生进行青光眼的筛选有着重大的实际意义。本发明分割方法提出的多标签深度卷积神经网络模型对眼底图像中的视盘和视杯进行分割。使用gan的的思想,将gan结合到模型中,生成器分成编码器和解码器两部分,在编码器中减少下采样因子,避免了一些特征信息的损失。并使用扩充卷积代替传统的卷积,扩大模型的感受野,通过级联不同扩充率的扩充卷积增加感受野的同时避免了“网格化”问题。在解码器中,提出尺度重构层代替反卷积等上采样方式,减少了参数,并保持着学习的能力,提高了模型的性能。最后在drishti-gs1数据集上对网络模型进行了验证,分割结果如图6所示,图6(a)为分割前的眼底视网膜图像;图6(b)为专家手动分割出的视盘和视杯区域,小圈代表视杯,大圈代表试盘;图6(c)为我们提出的多标签深度学习模型分割的结果。从图6(b)和6(c)的对比中我们可以看出,模型分割的结果和专家手动分割的视盘视杯区域非常接近,表明我们提出的方法具有很好的分割性能。
[0083]
4)眼底视网膜血管分割
[0084]
眼底是人体唯一能够直接观察到血管的部位,其自身的变化,如血管宽度、角度、分支形态等,为疾病的早期诊断提供了依据。眼底血管分析是目前诊断眼底疾病的主要方式,而眼底图像血管分割则是疾病定量分析的必要步骤。受fcn的启发,本发明设计了一个用于眼底视网膜血管分割的新的结构,命名为基线全卷积神经网络,结构如图5。网络包括结构对称的编码路径和解码路径,编码路径和解码路径均由卷积层、残差模块、批归一化层、relu激活层等组成。编码器使用丰富的卷积层来对低维度输入图像进行编码,以提取上
下文语义信息、降低背景噪声的影响,获取视网膜图像中的血管特征。解码器设计为执行编码的逆运算,并通过对低维特征进行上采样和融合来恢复空间信息,从而可以精确定位视网膜血管。网络主要包括三个部分:第一是构建多尺度输入层,用于构建图像金字塔输入以实现多层次的重复利用图像特征信息;第二是多路径fcn,用作主干结构以学习丰富的层次表示形式;最后是多输出融合模块,它将低级特征和高级特征相结合,以充分利用不同深度的特征信息,通过特征融合来达到更好的效果。下面是三个部分的详细介绍。
[0085]
多路径fcn:网络由两个编码器路径(
①
,
③
)和两个解码器路径(
②
,
④
)组成。每个编码器路径利用残差模块和卷积层生成一组编码器特征图,并使用批处理归一化层对每层特征图进行归一化,然后使用relu激活函数将其激活。
②
和
④
路径使用反卷积层和残差模块对(
①
,
③
)路径的特征进行解码,并使用批处理归一化层归一化每个层特征图,然后使用relu激活函数进行激活。跳过连接将编码器的特征图与解码器的特征图融合在一起,以减少特征信息损失和融合特征信息;
[0086]
多尺度输入层:多尺度输入被集成到编码器路径
①
中,以确保原始图像的特征传递并有效提高分割质量。在多尺度输入层中,本发明分割方法使用平均池化层对图像进行下采样,然后使用普通卷积层来扩展下采样图像的通道,然后将扩充后的下采样图像与编码器路径
①
中不同层次的输出融合后作为下一层的输入;
[0087]
多输出融合层:在解码器路径
④
中,提取不同深度的残差模块的输出特征,使用上采样方法将特征扩展与输入图像相同的大小,然后将它们分别输入到不同的卷积层进行通道压缩,再使用softmax函数中进行分类,将得到的多个概率图融合为一张双通道的概率图,其中第0维度的通道是分割为背景概率,第1维度的通道是分割为视网膜血管的概率。最后,只取第0维度通道特征图进行阈值分割以得到最终的血管分割图。
[0088]
以上三个模块改进能够提高网络的特征识别、复用能力,通过构建多尺度输入层、多路径fcn和多输出融合模块来得到优于fcn的结构。使得模型具有更深的网络结构,这增加了模型的容量,通过不同距离的跳过连接将低级特征与高级特征相融合,大大降低了训练模型的难度,并在训练中可以根据血管的形状特征自适应地训练卷积核的参数,这些都可提高网络对血管和背景的区分能力,提升模型的分割准确率。最后,本发明在drive、stare和chase这三个数据集上对本文提出的框架进行了训练和测试。实验结果表明,提出的网络结构在drive、stare和chase这三个数据集上已达到具有竞争力的实验结果,改进后的模型可以获得优于fcn的结果,其中,以drive数据集为例,分割结果如图7所示。图7(a)为分割前的眼底视网膜图像;图7(b)为专家手动分割出的视网膜血管;图7(c)为我们提出的基线全卷积神经网络模型分割的结果。从图7(b)和7(c)的对比中我们可以看出,模型分割的结果和专家手动分割的视网膜血管非常接近,对于细小的血管也分割的非常完整,这表明我们提出的方法具有很好的分割性能。
[0089]
处理结果分析
[0090]
本发明所有实验均在相同硬件平台和软件环境下运行,详见表1。实验基于开源的视觉处理库opencv,在cpu上运行代码。实验基于pytorch框架实现了数据预处理方法,视盘视杯分割网络和视网膜血管分割网络,在gpu上进行网络训练。本文提出的方法对实验环境的硬件和软件要求不高,在实际应用过程中,无需或仅需对现有设备进行简单升级即可训练使用。
[0091]
表1实验硬件平台及软件环境
[0092][0093]
超参数的设置对于训练模型和复现模型的实验结果至关重要。本发明实验的超参数设置详见表2。使用pytorch卷积层默认的初始化方法对网络权重和偏差进行赋值,然后使用adam优化器对网络进行端到端的反向传播训练。
[0094]
表2实验参数设置
[0095][0096]
本发明使用几种常用的评价指标来量化评估所提出方法的性能,包括准确率(accuracy)、灵敏度(sensitivity)、特异度(specificity)和f1分数(f1 scores)。通过综合评估,本发明视网膜血管分割方法的各个指标在drive、stare和chase数据集上获得了非常具有竞争力的实验结果,其中分割准确率达到97%以上、f1分数超过80%。且视盘视杯分割方法在drishti-gs1数据集上也取得很好的分割,f1分数在视盘上达到了97%,视杯上达到了92%。
[0097]
最后应说明的是:以上所述仅为本发明的优选实施例而已,并不用于限制本发明,尽管参照前述实施例对本发明进行了详细的说明,对于本领域的技术人员来说,其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。