用于监测用于尿节制的可植入装置的设备
1.要求优先权
2.本技术要求于2019年6月24日提交的美国专利申请序列号16/450,246的优先权的权益,该美国专利申请要求于2019年2月14日提交的美国临时申请序列号62/805,503的优先权的权益,美国专利申请和美国临时申请各自的公开内容通过引用整体并入本文。
技术领域
3.本文件总体上涉及可植入医疗装置,并且更具体地涉及用于监测用于治疗尿失禁的可植入装置的放置和/或调节的方法和系统。
背景技术:
4.用于治疗尿失禁的可植入装置的示例包括通过导管连接至后端口的可调节膜元件例如球囊。可以通过微创手术将可植入装置植入患者体内,其中可调节膜元件放置成邻近患者的尿道并且后端口放置在患者的皮肤下面。可以通过使用针头将流体注入后端口或从后端口经皮抽取流体来在手术期间和之后调节可调节膜元件。在示例性治疗中,将这种可植入装置中的两个放置在患者体内,使得两个可调节膜元件在患者的膀胱颈提供压力和支承,以防止在打喷嚏、咳嗽或身体活动期间尿液的意外泄漏。这种治疗的效果取决于在患者体内的适当放置以及放置之后对可调节膜元件的调节。
技术实现要素:
5.一个或更多个传感器并入可植入装置以及用于可植入装置的放置和/或调节的手术工具中的一个或更多个上。可植入装置包括用于身体内腔的可控接合例如尿道的接合作为尿失禁的治疗的可调节膜元件。在各种实施方式中,一个或更多个传感器可以被配置成检测指示可调节膜元件的形状、可调节膜元件相对于身体内腔的位置或身体内腔的形状中的至少一个的信息。
6.在各种实施方式中,用于身体内腔的可控接合的可植入装置可以包括可调节膜元件和细长导管。可调节膜元件可以包括具有限定腔室的内表面的连续壁。细长导管可以包括连接至并密封到可调节膜元件的外围表面、后端、前端和在细长导管中从后端处的第一开口纵向地延伸至与可植入装置的腔室流体连通的第二开口的内腔,用于通过经由第一开口引入的所施加的可流动材料来可调节地扩展或收缩可调节膜元件。一个或更多个传感器可以被并入可植入装置和/或传感器探针中,用于监测可植入装置的定位、可植入装置的调节和/或身体内腔的接合的状态。在一个实施方式中,一个或更多个传感器被并入可植入装置的可调节膜元件或细长导管中的至少一个上。在另一实施方式中,传感器探针包括其中并入有传感器的前端。在一个实施方式中,细长导管的内腔被构造成容纳传感器探针的包括其前端的一部分。在另一实施方式中,可植入装置包括在细长导管中纵向地延伸并且具有以下的另一内腔:入口,该入口被构造成接收传感器探针的一部分;以及用于止动传感器探针的封闭端;或者出口,该出口被构造成允许传感器探针的包括其前端的一部分的退出。
在各种实施方式中,一个或更多个传感器可以包括一个或更多个光学传感器例如摄像装置或管道镜、以及/或者用于产生超声波图像的一个或更多个超声波换能器。
7.该发明内容是对本技术的一些教导的概述,并不旨在作为对本主题的排他性或详尽性处理。在具体实施方式和所附权利要求中可以找到关于本主题的更多细节。本发明的范围由所附权利要求及其法律等同内容限定。
附图说明
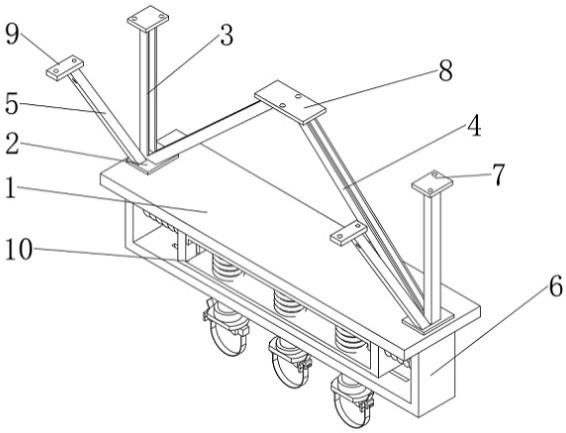
8.图1是根据本主题的实施方式的可植入装置和用于向可植入装置的可调节膜元件提供可流动材料的注射器源的透视图。
9.图2是根据本主题的实施方式的图1所示的可植入装置的纵向截面图。
10.图3是根据本主题的实施方式的沿图2的线3
‑
3截取的截面图。
11.图4示出了根据本主题的实施方式的在插入可植入装置之前插入身体组织中到邻近患者的身体内腔的植入位置的导引探针。
12.图5示出了根据本主题的实施方式的放置在导引探针上并且部分地推进到期望位置的可植入装置,其中可调节膜元件被放气。
13.图6示出了根据本主题的实施方式的在患者的身体组织中的期望位置处扩展以将身体组织移向身体内腔以引起身体内腔的可调节限制之后的植入装置。
14.图7是根据本主题的实施方式的沿图6的线7
‑
7截取的截面图。
15.图8示出了根据本主题的实施方式的插入后的可植入装置,其中其后端口在患者的皮肤下面。
16.图9是根据本主题的实施方式的另一可植入装置的示意图。
17.图10是根据本主题的实施方式的另一可植入装置的示意图。
18.图11是示出根据本主题的实施方式的用于改善尿道的接合的可植入装置的放置的大致目标部位的俯视图。
19.图12是根据本主题的实施方式的沿植入的区域中尿道的长度的视图,示出了用于改善尿道的接合的可植入装置的放置的大致目标部位。
20.图13是根据本主题的实施方式的可植入装置和传感器探针的图示。
21.图14是根据本主题的实施方式的传感器探针的一部分的图示。
22.图15是根据本主题的实施方式的传感器探针的前端的图示。
23.图16是根据本主题的实施方式的可植入装置的前端的一部分的截面图。
24.图17是根据本主题的实施方式的可植入装置的前端的一部分的截面图。
25.图18是根据本主题的实施方式的具有一个或更多个传感器的可植入装置的图示。
26.图19是根据本主题的实施方式的可植入装置套件的图示。
27.图20是根据本主题的实施方式的使用可植入装置的身体内腔的接合的图示。
28.图21是根据本主题的实施方式的使用两个可植入装置的身体内腔的接合的图示。
29.图22是示出根据本主题的实施方式的在邻近身体内腔的患者体内植入的用于所述身体内腔的接合的两个可植入装置的图像。
30.图23是根据本主题的实施方式的单内腔可植入装置和传感器探针的图示。
具体实施方式
31.本主题的以下具体实施方式是指附图中的主题,附图通过图示的方式示出了可以在其中实践本主题的具体方面和实施方式。以足够的细节描述这些实施方式以使得本领域技术人员能够实践本主题。在本公开内容中对“一”、“一个”或“各种”实施方式的提及不一定是指相同的实施方式,并且这种提及考虑了多于一个的实施方式。以下具体实施方式是说明性的,而不应视为限制意义的。本主题的范围由所附权利要求以及这些权利要求所享有的法律等同内容的完整范围限定。
32.除了其他方面,该文件还讨论了用于监测用于治疗尿失禁的可植入装置的放置和/或调节的系统和方法。可植入装置可以包括例如通过导管连接至后端口的可调节膜元件,该导管具有提供可调节膜元件的腔室与后端口的腔之间的流体连通的内腔。本文件中讨论的可植入装置(例如,图1所示的可植入装置110)的各种结构元件均可以通过各种术语来指代。“可调节膜元件”(例如图1所示的可调节膜元件112)也可以称为例如可调节元件、可扩展元件、可扩展膜元件、前向可扩展膜元件、球囊、或可调节球囊。“导管”(例如,图1所示的导管114)也可以称为例如中心导管元件、装置导管、连接导管、连接导线管或管状细长主体。“后端口”(例如,图1所示的后端口116)也可以称为例如后端口部分或后端口元件。“内腔”(例如,图2中所示的第一内腔215和第二内腔217)也可以称为例如通道、内通道或内部通道。
33.在一个示例中,可植入装置包括用导管连接至端口的可调节球囊。将球囊放置成邻近尿道以对尿道壁施加非周向压缩。理疗的有效性取决于球囊在患者的身体内的正确定位,例如在靠近尿道壁的泌尿生殖隔膜上方的尿道膀胱吻合处附近的耻骨后空间(由根治性前列腺切除术产生)。当使用(例如,两个可植入装置的)两个球囊时,它们的优选位置通常是对称的并且相对于尿道横向。可以使用荧光镜透视检查或经直肠超声检查来在可植入装置的植入期间以视觉方式监测球囊的位置。荧光镜透视检查已成为标准技术,但是荧光镜透视检查将患者暴露在辐射下并且提供在某些情况下造成观看困难的二维视图。例如,当患者在手术台上时,荧光镜透视检查图像不示出球囊在前后平面上的位置,因此不示出球囊是否正确定位以对尿道壁施加压力。经直肠超声(trus)可以提供更好的观察(例如,球囊在前后平面上的位置),但是需要外科医生熟悉这种成像技术。在可植入过程期间,可植入装置最初放置在患者体内,其中球囊定位在目标空间中。球囊可以处于略微充气以允许在不从目标空间移出的情况下(由患者的组织)进行封装。封装后,患者将经历一个或更多个调节程序,在此期间调节球囊以获得并保持尿节控,而不会造成不期望的阻塞。
34.本主题使用并入可植入装置上和/或用于植入可植入装置的手术工具上的一个或更多个传感器来监测可植入装置的放置和/或调节。这种监测技术避免了荧光镜透视检查或经直肠超声检查的使用及其缺点,例如暴露于x射线或超声波探针的直肠插入。在一个实施方式中,一个或更多个传感器包括可植入装置和/或手术工具上的一个或更多个超声波换能器,允许在装置植入期间使用超声波成像来监测球囊的放置和调节。可植入装置上的超声波传感器可以进一步允许球囊的手术后调节。
35.在各种实施方式中,本主题提供用于监测例如每个球囊的位置和每个球囊的充气(扩展)量的感测装置。在各种实施方式中,感测装置还可以用于监测尿道的各种状态,该状态可以指示由球囊扩展程度产生的压缩量,例如球囊的过度充气产生的过度压缩、充分压
缩(治疗的目标)、以及由球囊充气不足而产生的压缩不足。治疗的目标是为患者提供没有不期望的阻塞的节制,并且这需要由将球囊放置在正确的位置并给予每个球囊正确的充气量产生的尿道的接合的正确量。本主题允许针对每个球囊确定正确位置和正确的充气量。
36.图1至图10示出了可植入医疗装置和手术工具的各种实施方式。手术工具包括细长主体并且可以用作一个或更多个传感器可以并入其上的基础装置。可植入医疗装置可以与包括传感器的手术工具一起使用,或者可以用作一个或更多个传感器可以并入其上的基础装置。可植入装置和手术工具的各种实施方式示出在图1至图10中并且下面通过示例的方式而非通过限制的方式进行讨论。可植入装置和手术工具的这些示例以及其他示例在美国专利第5,964,806号、美国专利第6,045,498号、美国专利第6,419,624号、美国专利第6,579,224号和美国专利第8,926,494号中进行了讨论,这些美国专利全部转让给uromedica,inc.,这些美国专利通过引用整体并入本文。图11至图23示出了并入诸如在文件中讨论的那些的可植入装置和/或手术工具上的一个或更多个传感器的各种实施方式。
37.根据如由图1示出的本主题,提供了细长的可植入装置110,其包括以其完全扩展尺寸示出的可调节膜元件112,并且压密地附接至细长的导管114,该细长的导管114连接至通过第一内腔215(见图2)与可扩展元件112连通的后端口116。导管114具有略微延伸超出可扩展元件112的尖头前端114a。提供包括中空针头121和后轴向可移动柱塞122的注射器120,用于通过后端口116可调节地将合适的可流动材料注射到可植入装置110中以扩展可调节膜元件112。
38.如图2和3进一步所示,导管114包含两个细长的内腔或通道。第一内腔215提供内通道,可流动材料通过该内通道从后端口116中的腔216a被引导以扩展可调节膜元件112。导管114在其后端一体地附接至后端口116。第二内腔217从前开口117a延伸到后开口117b并且用于接收细长的导引探针(参见图4)并且实现将可植入装置110递送到患者的身体组织中的期望位置。
39.具有第一内腔215的可植入装置110的重要特征包括第一开口端口215a,该第一开口端口215a位于弹性隔板218与导管114之间的后端口116的腔216a中并且连接至第一内腔215,使得可流动材料可以通过第一开口端口215a注入,并且第二端口215b用于将工作流体引导至可调节膜元件112。在调节从注射器120的空心针头121提供的膜流体的体积期间,膜流体通过隔板218注入并且通过连接至可调节膜元件112的导管114继续。后端口116优选地具有比导管114大的直径以容纳腔216a和隔板218,隔板218由夹环119牢固地保持。
40.包括可调节膜元件112的整个可植入装置110由诸如硅树脂或聚氨酯弹性体的生物相容性材料形成,并且导管114和后端口116可以形成为整体结构。可选地,可调节膜元件112、后端口116和导管114可以模制为一体。如图2所示,可调节膜元件112在213处通过合适的粘附材料在其前端处粘附至导管114。
41.根据本主题的可植入装置和组件可包括三个主要构件。所提供的第一构件是呈刚性实心细长的导引探针424(见图4)形式的细长的导引件,其被配置用于将可植入装置110递送至患者的身体组织中的期望部位,如由图4和图5大体所示。替选地,细长的导引构件可以是柔性导引线的形式,该导引线最初已经通过已经插入到身体组织中的期望位置的单独的中空刚性探针递送到身体组织中。组件的第二构件是可植入装置110,其包括可调节膜元件112、包含两个内腔215和217的导管114以及后端口116。在其植入期间,在细长实心的导
引探针424首先通过外科手术插入患者的身体组织中以建立初始通路之后,可植入装置110被导引至邻近患者的身体中的身体内腔的预定位置。可植入装置110的内腔前端开口117a然后设置在导引探针424的后端上方以导引可植入装置110并且将可调节膜元件112(处于其收缩形状)递送至邻近身体组织中的将被可调节地限制的内腔的预定位置。第二内腔217的直径被制成略微大于导引探针424的直径以允许可植入装置110容易地在探针构件上方滑动。
42.在可植入装置110的植入期间,医生可以首先在患者需要限制的身体内腔432附近的皮肤430上做小切口,然后通过诸如荧光镜透视检查或超声波成像的可视化手段,根据患者的解剖结构,将实心的导引探针424引导至期望位置。此后,导管114的第二内腔117的开口117a在可调节膜元件112处于其初始放气或收缩状态的情况下在导引探针424的后端424a上方滑动。导引探针424滑动通过导管114的第二内腔217并且在向后开口117b处离开。如图2所示,开口117b在可调节膜元件112与后端口116之间。然而,将开口117b定位成在可调节膜元件112附近或替选地使第二内腔217延伸穿过后端口116可能是有利的。
43.如果需要,可以在导引探针424上提供标记533,当与可植入装置110上的特征例如后端口116对准时,标记533可以确保可植入装置110适当地放置在患者的身体组织430中的正确的深度处。可能需要提供多种长度的导管114以有利于将隔板218放置在患者的皮肤附近。替选地,导管114的有效长度可以通过其具有类似于螺旋弹簧的螺旋形状的螺旋形状而被制成可调节的。
44.在可植入装置110已经在导引探针424上方推进使得收缩的可调节膜元件112处于邻近身体内腔432的期望位置之后,身体内腔432可以通过用注射器120的针头121刺穿隔板218并且通过第一内腔215将可流动材料注射到可调节膜元件112中来被限制到期望的程度。医生可以通过诸如注入流体通过身体内腔超过限制并且测量背压的方式来确定身体内腔432的期望限制程度。
45.如由图1和图6所示,可流动材料的来源通常是带有用于刺穿弹性隔板218的空心针头的注射器120。然而,可以使用具有用于与可植入装置110进行可逆连接的装置的替选流体容器。可流动材料可以是例如盐水溶液、可流动凝胶或液体载体中的颗粒的浆液。使可流动材料不透射线可能是有利的,使得可以通过x射线查看膜充气的程度。
46.递送可植入装置110的替选方法可以是首先从身体组织中抽取导引探针24,然后对可调节膜元件112进行充气。另一替选方法是首先将可植入装置110放置在身体外部的实心导引探针424上方,然后将它们两者作为单元插入到身体组织中。为了促进该后一程序,可能需要在实心导引探针424与导管114中的第二内腔217之间存在一些摩擦。
47.在可植入装置110已被适当定位后,其中可调节膜元件112位于身体内腔432附近,并且后端口116中的隔板218位于皮肤430附近,该装置被注射来自注射器120的可流动材料。可扩展构件可以被充气到某一程度,然后放气到适于通过身体组织封装可扩展构件的程度。然后从装置中抽取导引探针24,将略微扩展的膜元件留在身体组织中。然后皮肤切口431通过诸如缝合线834的方式在端口116上方闭合,如图8所示。
48.本主题为可植入装置110提供术后膜扩展的可调节性。由于隔板218被定位成远离可调节膜元件112但在患者的皮肤附件并且位于患者的皮肤下面,因此实现了这种可调节性。端口和隔板通过例如皮肤区域的手动触诊定位,并且注射器的针头插入通过皮肤和隔
板以从可扩展构件添加或移除材料,从而增加或减少身体内腔的限制。
49.为了确保隔板218的适当密封,通过提供围绕后端口116并且直径小于端口的紧密金属环119,隔板218被压缩放置在腔216a内。当注射器120的针头121在可调节膜元件112扩展或调节之后从隔板218中抽取时,隔板218的周边的周围存在积极的密封。
50.图4至图8大体示出了用于将可植入装置110适当地植入患者的身体组织中的方法或程序。如由图4所示,医生在定位患者的诸如尿道的身体内腔之后,做小切口431并且将导引探针424插入身体组织中至邻近身体内腔432的期望位置。该程序通常由医生在具有视觉导引例如在荧光镜透视检查下的局部麻醉剂下执行。接下来,医生拿着可植入装置110并将其通过如图1和图2所示的第二内腔217放置在导引探针424上方。导引探针424进入后开口117b并离开前开口117a。在导管114足够柔性的情况下,可植入装置110沿导引探针424推进到身体组织中。
51.在到达身体组织内的所需位置之后,将合适的可流动材料从诸如注射器120的来源引入至可植入装置110中,注射器120具有插入通过隔板218的空心针头121以至少部分地扩张可调节膜元件112,如由图6所示。接下来,导引探针424被移除并且可调节膜元件112被进一步扩展至期望的扩大尺寸用于身体内腔432的限制。注射器120从可植入装置110移除,之后期望尺寸的可调节膜元件112由弹性隔板218保持。接下来,患者在431处的切口通过834处的缝合线在端口116和隔膜218上方进行手术闭合。
52.图9是根据本主题的一个实施方式的可植入装置套件940的图示,示出了截面图。可植入装置套件940包括具有可调节膜元件912和细长的导管914的可植入装置910,其中导管914包括在导管914中从后端(也称为近端)962处的第一开口915a纵向地延伸至第二开口915b的至少第一内腔915,并且其中可植入装置910被示出定位在护套946的通道944内。
53.可植入装置套件940还包括后端口916,其中后端口916耦接至导管914的后端962。在一个实施方式中,后端口916使用化学粘合剂,或者替选地使用如本领域已知的声波焊接技术耦接至细长的主体914的后端962。在另外的实施方式中,后端口916和后端962在聚合物模制工艺例如如本领域已知的液体注射模制中一起形成。
54.后端口916包括腔916a,其中腔916a与导管914的第一开口915a流体连通。在一个实施方式中,后端口916还包括弹性隔板918,通过弹性隔板918进入腔916a,其中弹性隔板918在例如用针头反复刺穿之后是可密封的。在一个实施方式中,弹性隔板918通过位于后端口916周围的夹环919保持在后端口916中。在一个实施方式中,夹环919由生物相容性材料诸如例如钛制成。在一个实施方式中,弹性隔板918由诸如例如硅树脂或聚氨酯的生物相容性材料制成。后端口916具有由后端口916的外表面954限定的外直径。在一个实施方式中,后端口916具有1至15毫米的外直径,其中4.5毫米是具体示例。
55.在一个实施方式中,后端口916的外表面和可调节膜元件912具有小于通道944的内部尺寸(例如直径)的尺寸(例如直径)以允许可植入装置910纵向地移动通过护套946的通道944。在替选实施方式中,后端口916由足够柔性的至少一种材料构成以允许后端口916在其松弛状态下的尺寸被压缩到足够小使得可植入装置910可以纵向地移动通过护套946的通道944的尺寸。在各种实施方式中,导管914具有足够的刚性以允许在其管状细长主体的后端处施加的力移动可植入装置910至少部分地通过护套946的通道944。在一个实施方式中,导管914的刚性基于用于构成其管状细长主体的材料的类型来确定。替选地,可以将
支承元件添加到管状细长主体。例如,金属线圈可以纵向放置在管状细长主体内以增加管状细长主体的刚性。
56.一旦可植入装置910被定位在身体内,可调节膜元件912通过将可流动材料源可释放地连接至后端口916来充气。在一个实施方式中,可流动材料源包括具有无芯针头的注射器,其中针头插入通过弹性隔板918。可以将测得的流体体积供应引入可植入装置910中,并且可调节膜元件912由于从可流动材料源引入后端口916的腔916a中的可流动材料的体积而扩展或收缩。可调节膜元件912然后用于至少部分地且可调节地限制身体内腔。适合注入假体的流体包括但不限于无菌盐水溶液;聚合物凝胶,例如硅凝胶或例如聚乙烯吡咯烷酮、聚乙二醇、羧甲基纤维素的水凝胶;高粘度液体,例如透明质酸、葡聚糖、聚丙烯酸、聚乙烯醇或例如不透射线的流体。一旦可调节膜元件912已被充气,针头就从后端口916的隔板中抽取。在另外的实施方式中,可检测标记物970嵌入可调节膜元件912的连续壁中。可检测标记物970允许使用任何数目的可视化技术将可调节膜元件912定位在患者的组织内,所述可视化技术采用电磁能作为将物体定位在身体内的手段。在一个实施方式中,可检测标记物970包括钽并且用于可视化可调节膜元件912的可视化技术是如本领域已知的x射线或荧光镜透视检查。
57.在另外的实施方式中,可检测标记物被嵌入可植入装置910中。例如,可检测标记物970位于导管914的前端(也称为远端)960(例如尖端)处。替选地,可检测标记物可以位于可调节膜元件912的连续壁中。可检测标记物970允许前端960或可调节膜元件912使用任何数目的采用电磁能作为在体内定位物体的手段的可视化技术。在一个实施方式中,可检测标记物970包括钽并且用于使前端960或可调节膜元件912可视化的可视化技术是如本领域已知的x射线或荧光镜透视检查。在另外的实施方式中,护套也可以具有可检测标记物,其中标记物可以并入护套壁中或护套壁上。替选地,整个护套可以被构造成不透射线的。
58.图10是根据本主题的可植入装置1010的附加实施方式的图示。可植入装置1010包括可调节膜元件1012和导管1014。导管1014具有前端1060。在一个实施方式中,导管1014的外周表面连接至并密封到可调节膜元件1012。在一个实施方式中,可调节膜元件1012包括具有限定腔室的内表面的连续壁。
59.导管1014包括第一内腔1015和第二内腔1017。在一个实施方式中,第一内腔1015在导管1014中从第一开口1015a纵向地延伸至一个或更多个第二开口1015b(例如,如图10所示的两个开口)。第二开口1015b与可调节膜元件1012的腔室流体连通,以通过经由第一开口1015a引入的可流动材料可调节地扩展或收缩可调节膜元件1012。
60.第二内腔1017沿导管1014从入口1017b纵向地延伸到前端1060处的封闭端1017a。在一个实施方式中,第二内腔1017和入口1017b均具有足够的直径以接收可以用于在组织中推进可植入装置1010的推杆。
61.可植入装置1010还包括耦接至导管1014的后端的后端口1016。在一个实施方式中,后端口1016类似于后端口916并且包括腔1016a和弹性隔板1018。腔1016a在第一开口1015a处耦接至第一内腔1015并且与第一内腔1015流体连通。弹性隔板1018允许使用针头过度到腔1016a,用于引入和/或抽取流体以扩展和/或抽出可调节膜元件1012。
62.图11是膀胱1101和尿道1102的俯视图,示出了根据本主题的实施方式的放置可植入装置1110以改善尿道的接合的大致目标位置。可植入装置1110可以呈现如本文件中讨论
的可植入装置的任何实施方式(其中图中示出了可扩展膜元件或可调节膜元件以示出其位置),包括但不限于可植入装置110、可植入装置910、可植入装置1010、或包括可植入装置110、910和1010的特征的各种组合的可植入装置。具有x轴、y轴和z轴的笛卡尔坐标系在图11至图21中示出(其中这些图中的每一个中都看到了x轴、y轴和z轴中的两个)作为这些图中所示结构的示例性定向的参考。z轴的定向沿尿道1002沿植入的大致位置的方向。在根治性前列腺切除术的情况下,该位置在膀胱颈和尿道膀胱吻合处附近,或者在经尿道前列腺切除术(turp)后,在前列腺的顶端处的尿道进一步向下。
63.图12是根据本主题的一个实施方式的沿植入区域中的尿道1102的长度(或沿y轴)的视图,示出了放置可植入装置1110以改善尿道的接合的大致目标位置。本主题可以帮助在植入患者体内期间可植入装置1110的适当放置和/或在植入可植入装置1110后的调节。特别地,本主题的应用促进了可植入装置1110沿y轴(矢状视图)的准确放置。
64.图13是根据本主题的实施方式的包括可植入装置1310和传感器探针1324的可植入装置套件1320的图示。可植入装置1310和传感器探针1324可以作为装置套件提供,该装置套件还可以包括其他附件。可植入装置1310可以用于接合身体内的内腔,并且可以包括可调节膜元件1312、细长导管1314和后端口1316。可调节膜元件1312被构造成接合内腔并且包括具有限定腔室的内表面的连续壁。导管1314具有后端1315、耦接至可调节膜元件1312的前端1313、在前端1313附近连接至并密封到可调节膜元件1312的外围表面、以及沿导管1314从后端1315处的第一开口纵向地延伸到与腔室流体连通的在前端1313处或附近的第二开口的内腔(图13中未示出)。后端口1316耦接至后端1315,并且包括与第一内腔的第一开口流体连通的腔室和允许通过针头进入腔的弹性隔板。在一些实施方式中,后端口1316可释放地耦接至导管1314的后端。可植入装置1310可以呈现如本文件中讨论的可植入装置的任何实施方式,包括但不限于可植入装置110、可植入装置910、可植入装置1010或包括可植入装置110、910和1010的特征的各种组合的可植入装置。
65.传感器探针1324具有包括后端1327和前端1325的细长主体1326,以及并入细长主体1326上的一个或更多个传感器1328。在各种实施方式中,传感器探针1324可以通过将传感器并入在可植入装置1310的植入和/或调节期间使用并且具有细长主体的任何手术工具中。这种手术工具的示例包括推杆(例如,推杆1450)和导引探针(或导引杆或导引线,例如导引探针424)。在一个实施方式中,如图13所示,示出了前端1325处的一个传感器1328。在另一实施方式中,如图14所示,该图示出了根据本主题的实施方式的传感器探针1424的一部分,多个传感器1328分布在细长主体1326的至少一部分上。
66.在各种实施方式中,传感器1328可以通过旋转细长主体1326,例如通过旋转后端1327来旋转。细长主体1326可以包括例如在后端1327处的传感器连接电路1330。导体1329在细长主体1326内延伸以提供传感器1328与传感器连接电路1330之间的连接。在一个实施方式中,传感器连接电路1330包括用于连接至处理由传感器1328感测的信号的外部系统的连接器。在另一实施方式中,传感器连接电路1330包括遥测电路和电池,使得它可以与外部系统以无线方式进行通信。遥测电路可以使用例如电磁、磁、声或光遥测来执行无线通信。
67.在各种实施方式中,传感器1328可以包括一个或更多个超声波换能器,每个超声波换能器将电输入信号转换为超声,发射该超声,接收所反射的超声(所发射的超声的回声),并且将接收到的所反射的超声转换为电图像信号。外部系统可以接收电图像信号并且
基于电图像信号产生超声波图像。一个或更多个超声波换能器可以各自包括压电换能器或电容换能器,并且各自具有超声波束方向和超声波束角度。
68.在各种实施方式中,传感器1328可以包括一个或更多个光学传感器。一个或更多个光学传感器可以各自包括电荷耦接器件(ccd)图像传感器或有源像素传感器(aps,也称为互补金属氧化物半导体(cmos)图像传感器)以将所捕获的图像转换为电图像信号。外部系统可以接收电图像信号并且基于该电图像信号产生视觉图像。
69.在各种实施方式中,与腔室流体连通的可植入装置1310的内腔也被构造成接收用作推杆(例如,如图9所示)的传感器探针1324。前端1313处的内腔的端部被构造成接收通过传感器探针1324施加的力以移动可植入装置1310。内腔包括在前端1313附近的封闭端。该封闭端具有足够的强度和硬度以接收传感器探针1324的前端1325并将在传感器探针的后端1327处施加的力传递到可植入装置1310。
70.在各种其他实施方式中,可植入装置1310的第一内腔与腔室流体连通以调节腔室的容积,并且可植入装置1310包括在导管1314的至少一部分内纵向地延伸的第二内腔并且被构造成接收传感器探针1324(例如,如图2、图3、图5和图10所示)。第二内腔包括在导管1314的后端1315处或附近的入口和在导管1314的前端1313处或附近的出口。前端1313被构造成接收通过传感器探针1324施加的力以移动可植入装置1310。
71.在一个实施方式中,第二内腔包括在导管1314的前端1313附近的封闭端。该封闭端具有足够的强度和硬度以接收传感器探针1324的前端1325并且将在传感器探针1324的后端1327处施加的力传递至可植入装置1310。图16是根据本主题的实施方式的细长导管1614的前端1613的一部分的截面图,示出了第一内部通道或第二内部通道的封闭端,该封闭端被构造成接收通过传感器探针1324施加的力以移动可植入装置1310。前端1613可以代表前端1313的示例。在一个实施方式中,前端1613包括传感器窗口1635以提供对要感测的信号的透明度。例如,超声透明材料可以用于传感器窗口1635。传感器窗口1635可以被配置用于指定的整体超声波束角度,高达360度(即,传感器窗口具有等于第二内腔的周长的长度)。
72.在另一实施方式中,传感器探针1324包括适合穿透组织的尖锐尖端,如图10所示的示例中。图15是示出根据本主题的实施方式的传感器探针1524的前端1525的图示。传感器探针1524可以代表传感器探针1324的示例并且包括在前端1525处的尖锐尖端1531。第二内腔包括在导管1314的前端1313附近的出口。出口允许包括尖锐尖端1531的传感器探针1524的一部分从导管1314突出。图17是根据本主题的实施方式的细长导管1714的前端1713的一部分的截面图。前端1713可以代表前端1313的示例。第二内腔包括第一肩部1736并且传感器探针1524包括第二肩部1532,该第二肩部1532被构造成邻接第一肩部1736以允许在传感器探针1324的后端1327处施加的力传递至可植入装置1310。在一个实施方式中,如图15和图17所示,第一肩部1736由第二内腔的直径的变化形成,并且第二肩部1532由传感器探针1524的直径的变化形成。传感器1328可以在前端1525处并入传感器探针1524的细长主体1526上,使得尖锐尖端1531和传感器1328两者可以从可植入装置1310的导管1314突出。
73.图18是根据本主题的实施方式的具有一个或更多个传感器的可植入装置1810的图示。可植入装置1810包括如上文所讨论的可植入装置1310和并入可植入装置1310上的一个或更多个传感器1828。可植入装置1810还包括例如在后端1315处的传感器连接电路
1840,以及在细长主体1314内延伸以提供传感器1828与传感器连接电路1840之间的连接的导体1841。在所示实施方式中,可植入装置1810包括在可调节膜元件1312与导管1314之间的远端连接处、在可调节膜元件1312与导管1314之间的后连接处、以及沿垂直于导管(即,垂直于z轴)的可调节膜元件1312的中线的六个传感器1828。在各种实施方式中,任何数目的传感器并入可植入装置1810上的任何位置。例如,一个或更多个传感器1828可以并入导管1314上(例如,在前端1313处或邻近前端1313、在可调节膜元件1312与导管1314之间的远端连接处或邻近该远端连接、和/或在可调节膜元件1312与导管1314之间的后连接处或邻近该后连接)和/或可调节膜元件1312(例如,在垂直于导管1314的可调节膜元件1312的中线上、邻近可调节膜元件1312与导管1314之间的远端连接、和/或邻近可调节膜元件1312与导管1314之间的后连接)。
74.在各种实施方式中,传感器1828可以包括一个或更多个超声波换能器,每个超声波换能器将电输入信号转换为超声,发射该超声,接收所反射的超声(所发射的超声的回声),并且将接收到的所反射的超声转换为电图像信号。外部系统可以接收电图像信号并且基于电图像信号产生超声波图像。一个或更多个超声波换能器可以各自包括压电换能器或电容换能器,并且各自具有超声波束方向和超声波束角度。多个超声波换能器可以布置在可植入装置1810上以提供指定的整体超声波束角度(例如,90、180、270或360度)。
75.在各种实施方式中,传感器1828可以包括一个或更多个光学传感器。一个或更多个光学传感器可以各自包括ccd图像传感器或aps以将所捕获的图像转换为电图像信号。外部系统可以接收电图像信号并基于该电图像信号产生视觉图像。
76.在各种实施方式中,传感器1828可以包括可以感测有助于协助可植入装置1810的放置和调节的信号的任何类型中的一种或更多种,例如压力传感器和应变计。
77.传感器连接电路1840可以在后端口1316内并且提供经由后端口1316对一个或更多个传感器1828的访问。在一个实施方式中,可植入装置1810可以使用有线连接与外部系统进行通信。传感器连接电路1840包括连接器。外部系统包括经皮连接器以刺穿后端口1316的弹性隔板并且与后端口1316中的连接器配合。在另一实施方式中,可植入装置1810可以以无线方式与外部系统进行通信。传感器连接电路1840包括遥测电路和电池或感应功率接收器。遥测电路可以向可植入装置1810传输电力并且从可植入装置1810接收感测到的信号。
78.图19是根据本主题的实施方式的可植入装置套件1920的图示。可植入装置套件至少包括可植入装置1810和传感器探针1324,如图19所示,并且还可以包括用于可植入装置1810的植入的其他工具或附件。选自传感器1828和传感器1328的一个或更多个传感器可以用于在植入和/或调节期间提供对可植入装置1810的监测。出于各种目的和情况,用户可以使用仅可植入装置1810的一个或更多个传感器、仅传感器探针1324的一个或更多个传感器、或可植入装置1810和传感器探针1324两者的传感器来进行监测。
79.图20是根据本主题的实施方式的使用可植入装置2010和探针2024的身体内腔1102的接合的图示。可植入装置2010的示例包括但不限于本文件中讨论的(具有或不具有一个或更多个传感器的)任何可植入装置,例如可植入装置110、910、1010、1310和1810。探针2024的示例包括但不限于本文件中讨论的(具有或不具有一个或更多个传感器的)任何探针,例如导引探针424、推杆1450和传感器探针1324、1424和1524。传感器2028代表并入可
植入装置2010和/或探针2024上的任何一个或更多个传感器。在一个实施方式中,传感器2028提供诸如图22所示的图像的图像用于导引可植入装置2010邻近内腔1102(例如,尿道)的放置以实现内腔的接合,和/或允许身体内腔是否接合到期望的程度的确定。
80.图21是根据本主题的实施方式的使用两个可植入装置2010和两个探针2024的身体内腔1102的接合的图示。图22示出了该疗法的图像的示例。当身体内腔(例如,尿道)被适当地接合时,观察到每个可植入装置的面向内腔的可调节膜元件1312变平。在各种实施方式中,传感器2028可以用于提供指示可植入装置2010中的每一个的位置、可调节膜元件1312的变平程度、和/或身体内腔的形状的图像和/或其他信息,从而在放置和/或调节可植入装置2010时提供导引。身体内腔的形状可以指示身体内腔的接合程度。在各种实施方式中,放置在可植入装置2010中的每一个中的传感器2028可以检测指示同一可植入装置的可调节膜元件1312的形状、同一可植入装置的可调节膜元件1312(例如,相对于身体内腔1102)的位置、另一个可植入装置2010的可调节膜元件1312的形状、另一个可植入装置2010的可调节膜元件1312(例如,相对于身体内腔1102)的位置、和/或身体内腔1102的形状的信息。在各种实施方式中,放置在可植入装置2010中的传感器2028可以检测指示另一可植入装置或其一部分的形状和/或位置的信息,该另一可植入装置或其一部分存在于可植入装置2010附近的组织中。
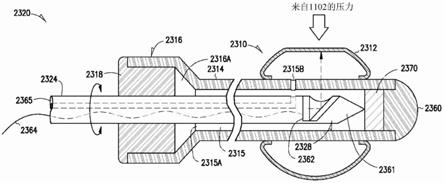
81.图23是根据本主题的实施方式的包括单内腔可植入装置2310和传感器探针2324的可植入装置套件2320的图示。可植入装置套件2320可以代表可植入装置套件1320的示例,其中可植入装置2310用于尿道的接合,并且传感器探针2324用于检测尿道的接合状态或程度的一个或更多个指示并且调节可植入装置2310的可调节膜元件2312中的容积,以获得在治疗尿失禁时的最佳功效,而不会造成尿道的阻塞。可植入装置2310包括前端2360、后端口2316和连接在前端2360与后端口2316之间的细长导管2314。可调节膜元件2312固定至在前端2360附近的导管2314上并且包括具有限定腔室的内表面的连续壁。内腔2315在导管2314内纵向地延伸并且在远端开口2315b处与可调节膜元件2312的腔室流体连通并且在后开口2315a处与后端口2316的腔2316a流体连通。在所示的实施方式中,传感器探针2324是也可以用作以下的三合一装置:(1)在传感器探针2324的前端处包括传感器2328的感测装置、(2)用于通过在前端2360处对内腔2315的封闭前端施加力来在组织中推进可植入装置2310的推杆、以及(3)包括内腔2365的中空针头,通过内腔2365可以引入和抽取流体以通过内腔2315的远端开口2315b分别对可调节膜元件2312进行充气和放气。内腔2315被构造成容纳传感器探针2324的前部,其中传感器探针2324的前端到达内腔2315的封闭前端。如图23所示,当可调节膜元件2312被放置成邻近尿道并放气时,来自尿道的压力可以使可调节膜元件2312的一侧变平。传感器2328可以允许观察到这种变平,这表明可以针对治疗尿失禁的光学功效而调节的压力量。
82.如图23所示,可调节膜元件2312被充气以提供尿道接合并且在其遇到来自尿道的扩展阻力的地方具有变平的部分。可植入装置2310包括在前端2360处的不透射线标记物2370。不透射线标记物2370还用作感测探针2324的止动件以确保其处于用于感测的正确位置。止动件还用作推杆(例如,用作推杆的传感器探针2324)的止动件,用于在初始植入程序中可植入装置2310的放置。当传感器探针2324用作推杆时,可以使用传感器2328来导引可植入装置2310的放置和/或初始调节以观察尿道的接合。后端口2316包括自密封隔板2318
以允许传感器探针2324(以及其他推杆或推线,如果使用的话)进入内腔2315。传感器探针2324的前端具有用于刺穿隔板2318的尖锐尖端。单内腔可植入装置的优点包括提供更大的横截面积以在给定直径的导管2314中容纳传感器2328。
83.在所示的实施方式中,传感器2328是用于以视觉方式观察可调节膜元件2312抵靠尿道的变平的光学传感器,作为尿道内接合的实际可视化的指标。在另一实施方式中,传感器2328是超声波传感器。除了直接观察尿道的接合之外,如果超声波传感器传输在组织内具有足够穿透深度的超声,它还可以允许可调节膜元件2312相对于诸如膀胱颈和直肠的解剖结构的可视化。这种可视化可以用于在可植入装置2310的植入期间帮助可调节膜元件2312的放置。在各种实施方式中,传感器2328可以包括允许检测可调节膜元件2312的变平和/或可调节膜元件2312在组织中相对于各种解剖结构的可视化的任何类型的传感器。
84.在所示的实施方式中,传感器2328(即,光学传感器)包括用于利用借助于镜2363获得径向视图的ccd或cmos芯片2362观察可调节膜元件2312的变平的光学感测元件2361。芯片2362被供电,并且经由电加热丝2364返回由传感器2328获取的数据。电加热丝2364还可以用于为诸如led的光源供电以帮助可视化(如果芯片2362是红外ccd或cmos芯片,则没有必要)。传感器探针2324可以在内腔2315内绕其纵向轴旋转以周向地扫描以找到可调节膜元件2312变平的最大接合点。旋转传感器探针2324还可以帮助将其穿过导管2314中的弯曲,特别是当后端口2316被引向阴囊或阴唇中时。至少出于这个原因,传感器探针2324被提供有一定量的灵活性。在一个实施方式中,具有光学传感器2328的传感器探针2324配备有广角镜头以允许观看可调节膜元件2312的整个内表面,使得不需要周向扫描。
85.在另一实施方式中,传感器探针2324可以包括用于光学可视化的管道镜,其中光纤束延伸穿过传感器探针。传感器探针2324内的光源是不必要的,因为光纤还可以用于传输来自外部地连接至传感器探针的光源的光。当与ccd或cmos芯片的尺寸相比,光纤束可以具有显着更小的直径,从而减小传感器探针2324的直径,并因此减小导管2314和后端口2316的直径。这允许减小可植入装置2310的整体尺寸和传感器探针2328的整体尺寸。传感器探针2324的较小直径是可取的,原因是在可植入装置植入患者体内后,传感器探针2324必须穿过阴囊或阴唇的皮肤才能到达可植入装置的后端口2316。此外,当与具有ccd或cmos芯片的光学传感器实现方式相比时,传感器探针2324的光纤实现方式可以降低生产成本,从而提高将传感器探针2324制成一次性装置的可承受性。
86.本技术旨在涵盖本主题的自适应或变型。应当理解,以上描述旨在是说明性的而非限制性的。本主题的范围应当参考所附权利要求以及这些权利要求所享有的法律等同内容的完整范围来确定。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。