1.本发明属于医用材料领域,具体涉及一种酯化改性淀粉在制备止血材料中的应用。
背景技术:
2.止血材料主要分为止血器械和止血药物两大类别,其中止血器械主要有止血带、止血钳和止血敷料,止血药物分为化学止血剂、生物止血剂和中药。这些止血材料的止血性能各有优缺点,止血带和止血钳可用于大动脉止血,但不适用于特殊部位止血,过紧可能会造成组织坏死;止血敷料可用于不规则创面的止血,但清创可能会导致伤口二次出血。化学止血剂见效快,但性质不稳定,全身副作用较为明显;生物止血剂止血效果好,但是容易发生免疫反应,成本高;中药止血药来源丰富,成本低,但见效慢。虽然目前已有多种止血材料,且临床效果良好,但开发高效、生物安全、低成本、易制备、可生物降解性和生物相容性好的新型止血材料已成为当务之急。国内外创伤救治专家致力于研究一种成本低、见效快、免清创的速效止血材料。
技术实现要素:
3.本发明的目的是提供一种酯化改性淀粉的应用。
4.本发明所提供的酯化改性淀粉的应用是其在制备止血材料中的应用。
5.本发明所述的酯化改性淀粉主要原料来源丰富、安全性好、无残留,可广泛用于体内实质性脏器及弥漫性出血等不规则出血的止血应用,止血后不需清创,止血效果可延续至术后,术后可在人体降解吸收。
6.本发明所述酯化改性淀粉即载氨甲环酸交联多孔淀粉具体可按照包括下述步骤的方法制备得到:1)将淀粉溶于磷酸氢二钠柠檬酸缓冲溶液中,水浴加热,机械搅拌;然后再加入α淀粉酶和糖化酶,再继续搅拌;加入碱溶液,使体系ph值为10~14,搅拌,使α淀粉酶和糖化酶灭活,离心、洗涤,冷冻干燥得酶解淀粉;2)将boc
‑
氨甲环酸与n,n
‑
二甲基甲酰胺、氯化亚砜在二氯甲烷中进行反应,得到boc
‑
氨甲酰氯;3)将步骤1)得到的酶解淀粉与步骤2)得到的boc
‑
氨甲酰氯进行反应,反应结束后离心、洗涤,冷冻干燥,得到所述载氨甲环酸交联多孔淀粉。
7.上述方法步骤1)中,所述淀粉与磷酸氢二钠柠檬酸缓冲溶液的配比为(2~3)g:(50~100)ml;所述磷酸氢二钠柠檬酸缓冲溶液的ph值为4~5。所述机械搅拌的转速为300~600rpm。
8.上述方法步骤1)中,所述水浴的温度为45~55℃;上述方法步骤1)中,所述加入α淀粉酶和糖化酶,再继续搅拌的时间可为5~10h。
9.上述方法步骤1)中,所述α淀粉酶的用量为25~75knu/g淀粉(具体如50knu/g淀
粉);所述糖化酶的用量为5000~15000u/g淀粉(具体如10000u/g淀粉)。
10.上述方法步骤1)中,所述碱溶液具体可为氢氧化钠溶液,如0.5m氢氧化钠溶液。
11.上述方法步骤1)中,加入碱溶液后,所述搅拌的时间可为20~40min。
12.上述方法步骤1)中,所述离心的条件可为5500rpm*5min。
13.上述方法步骤1)中,所述洗涤是用去离子水洗涤,具体可洗涤三次。
14.上述方法步骤1)中,所述冷冻干燥的条件为
‑
60℃、24h。
15.上述方法步骤1)具体可按照下述步骤进行:称取2~3g淀粉,溶于50~100ml磷酸氢二钠柠檬酸缓冲溶液中,50℃水浴,500rpm机械搅拌,加入适量的α淀粉酶和糖化酶,搅拌5~10h,加入15~20ml 0.5m氢氧化钠溶液,使ph值为10~14,搅拌30min,离心5500rpm*5min,去离子水洗涤三次,冷冻干燥得酶解淀粉。
16.上述方法步骤2)中,所述boc
‑
氨甲环酸、n,n
‑
二甲基甲酰胺、氯化亚砜、二氯甲烷的配比为(5~10 )g:(200~400)μl :(5~11)ml :(50~100)ml。
17.上述方法步骤2)中,所述反应的反应温度为25~30℃;反应时间为2~4h。所述反应在搅拌状态下进行,搅拌的转速为300~600rpm。
18.上述方法步骤2)具体可按照下述步骤进行:5~10 g boc
‑
氨甲环酸,50~100 ml二氯甲烷溶解,30℃、500rpm回流磁力搅拌10min,加入200~400 μl n,n
‑
二甲基甲酰胺,5~11 ml氯化亚砜搅拌2~4h。旋蒸,得boc
‑
氨甲酰氯粉末。
19.上述方法步骤3)中,所述酶解淀粉与boc
‑
氨甲酰氯的质量比为1~2 g:5~10 g。
20.上述方法步骤3)中,所述反应的反应温度为40~80℃(具体如40℃、60℃或80℃),反应时间为4~12h(具体如4h、8h或12h)。所述反应在搅拌状态下进行,搅拌的转速为300~600rpm。
21.上述方法步骤3)中,所述离心的条件可为5500rpm*5min。
22.上述方法步骤3)中,所述洗涤是用去离子水洗涤,具体可洗涤三次。
23.上述方法步骤3)中,所述冷冻干燥的条件为
‑
60℃、24h。
24.上述方法步骤3)具体可按照下述步骤进行:1~2 g 酶解淀粉,40~80℃、500rpm磁力搅拌,加入1~10 g boc
‑
氨甲酰氯,搅拌4~12h,离心5500rpm*10min,去离子水洗涤3次,离心,冷冻干燥24h得载氨甲环酸交联多孔淀粉。
附图说明
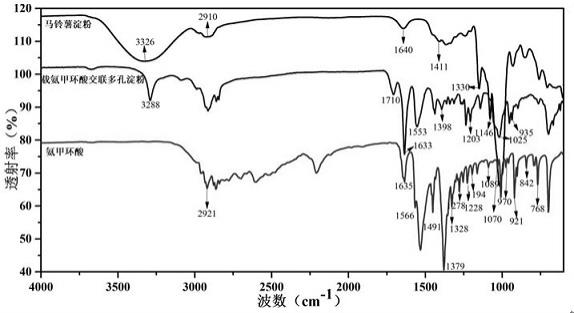
25.图1为实施例1制备的载氨甲环酸交联多孔淀粉的红外光谱分析结果图;图2为实施例1制备的载氨甲环酸交联多孔淀粉的扫描电镜结果图:a1, a2 和 a3: 马铃薯淀粉;b1, b2 和b3:酶解淀粉;c1, c2 和 c3:载氨甲环酸交联多孔淀粉;图3为实施例1制备的载氨甲环酸交联多孔淀粉吸液率结果图;图4为实施例1制备的载氨甲环酸交联多孔淀粉的体外细胞毒性试验结果图;图5为实施例1制备的载氨甲环酸交联多孔淀粉的急性毒性试验结果图;图6为实施例制备的载氨甲环酸交联多孔淀粉的体外凝血时间结果图(*:p小于0.05,结果均与阳性对照欣速聆止血颗粒对比);图7为小鼠断尾出血模型止血后各组止血材料的止血照片:a载氨甲环酸交联多孔淀粉,b欣速聆止血颗粒组,c空白纱布组;
图8为小鼠断尾出血模型止血过程中失血量的统计(*:p小于0.05,**:p<0.01,结果均与阳性对照欣速聆止血颗粒对比)。
具体实施方式
26.下面结合具体实施例对本发明作进一步阐述,但本发明并不限于以下实施例。所述方法如无特别说明均为常规方法。所述原材料如无特别说明均能从公开商业途径获得。
27.下述实施例中所使用的酶的来源如下:α淀粉酶购自上海阿拉丁生化科技股份有限公司,批号:l2008186 ,酶活≥500knu/g。
28.糖化酶购自上海阿拉丁生化科技股份有限公司,批号:d2102059,酶活100000u/ml。
29.下述实施例中所使用的欣速聆止血颗粒购自杭州协和医疗用品有限公司,规格1.0g/支。
30.下述实施例中所使用的淀粉均为马铃薯淀粉。
31.实施例1:制备载氨甲环酸交联多孔淀粉(1)称取2g淀粉,溶于100ml ph=4.5的磷酸氢二钠柠檬酸缓冲溶液中,50℃水浴,500rpm机械搅拌,加入50knu/g α淀粉酶和10000u/g糖化酶,搅拌6h,加入17ml 0.5m氢氧化钠溶液,使ph值为12,搅拌30min,离心5500rpm*5min,去离子水洗涤三次,冷冻干燥得酶解淀粉。
32.(2)10 g boc
‑
氨甲环酸,100 ml二氯甲烷溶解,30℃、500rpm回流磁力搅拌10min,加入200 μl n,n
‑
二甲基甲酰胺,5.646 ml氯化亚砜搅拌3h。旋蒸,得boc
‑
氨甲酰氯粉末。
33.(3)1 g 酶解淀粉,40℃、500rpm磁力搅拌,加入3g boc
‑
氨甲酰氯,搅拌8h,离心5500rpm*10min,去离子水洗涤3次,离心,
‑
60℃冷冻干燥24h得载氨甲环酸交联多孔淀粉。
34.实施例2:制备载氨甲环酸交联多孔淀粉(1)称取2g淀粉,溶于100ml ph=4.5的磷酸氢二钠柠檬酸缓冲溶液中,50℃水浴,500rpm机械搅拌,加入50knu/g α淀粉酶和10000u/g糖化酶,搅拌6h,加入17ml 0.5m氢氧化钠溶液,使ph值为12,搅拌30min,离心5500rpm*5min,去离子水洗涤三次,冷冻干燥得酶解淀粉。
35.(2)10 g boc
‑
氨甲环酸,100 ml二氯甲烷溶解,30℃、500rpm回流磁力搅拌10min,加入200 μl n,n
‑
二甲基甲酰胺,5.646 ml氯化亚砜搅拌3h。旋蒸,得boc
‑
氨甲酰氯粉末。
36.(3)1 g 酶解淀粉,60℃、500rpm磁力搅拌,加入3g boc
‑
氨甲酰氯,搅拌8h,离心5500rpm*10min,去离子水洗涤3次,离心,
‑
60℃冷冻干燥24h得载氨甲环酸交联多孔淀粉。
37.实施例3:制备载氨甲环酸交联多孔淀粉(1)称取2g淀粉,溶于100ml ph=4.5的磷酸氢二钠柠檬酸缓冲溶液中,50℃水浴,500rpm机械搅拌,加入50knu/g α淀粉酶和10000u/g糖化酶,搅拌6h,加入17ml 0.5m氢氧化钠溶液,使ph值为12,搅拌30min,离心5500rpm*5min,去离子水洗涤三次,冷冻干燥得酶解淀粉。
38.(2)10 g boc
‑
氨甲环酸,100 ml二氯甲烷溶解,30℃、500rpm回流磁力搅拌10min,加入200 μl n,n
‑
二甲基甲酰胺,5.646 ml氯化亚砜搅拌3h。旋蒸,得boc
‑
氨甲酰氯粉末。
39.(3)1 g 酶解淀粉,80℃、500rpm磁力搅拌,加入3g boc
‑
氨甲酰氯,搅拌8h,离心5500rpm*10min,去离子水洗涤3次,离心,
‑
60℃冷冻干燥24h得载氨甲环酸交联多孔淀粉。
40.实施例4:制备载氨甲环酸交联多孔淀粉(1)称取2g淀粉,溶于100ml ph=4.5的磷酸氢二钠柠檬酸缓冲溶液中,50℃水浴,500rpm机械搅拌,加入50knu/g α淀粉酶和10000u/g糖化酶,搅拌6h,加入17ml 0.5m氢氧化钠溶液,使ph值为12,搅拌30min,离心5500rpm*5min,去离子水洗涤三次,冷冻干燥得酶解淀粉。
41.(2)10 g boc
‑
氨甲环酸,100 ml二氯甲烷溶解,30℃、500rpm回流磁力搅拌10min,加入200 μl n,n
‑
二甲基甲酰胺,5.646 ml氯化亚砜搅拌3h。旋蒸,得boc
‑
氨甲酰氯粉末。
42.(3)1 g 酶解淀粉,80℃、500rpm磁力搅拌,加入3g boc
‑
氨甲酰氯,搅拌4h,离心5500rpm*10min,去离子水洗涤3次,离心,
‑
60℃冷冻干燥24h得载氨甲环酸交联多孔淀粉。
43.实施例5:制备载氨甲环酸交联多孔淀粉(1)称取2g淀粉,溶于100ml ph=4.5的磷酸氢二钠柠檬酸缓冲溶液中,50℃水浴,500rpm机械搅拌,加入50knu/g α淀粉酶和10000u/g糖化酶,搅拌6h,加入17ml 0.5m氢氧化钠溶液,使ph值为12,搅拌30min,离心5500rpm*5min,去离子水洗涤三次,冷冻干燥得酶解淀粉。
44.(2)10 g boc
‑
氨甲环酸,100 ml二氯甲烷溶解,30℃、500rpm回流磁力搅拌10min,加入200 μl n,n
‑
二甲基甲酰胺,5.646 ml氯化亚砜搅拌3h。旋蒸,得boc
‑
氨甲酰氯粉末。
45.(3)1 g 酶解淀粉,80℃、500rpm磁力搅拌,加入3g boc
‑
氨甲酰氯,搅拌12h,离心5500rpm*10min,去离子水洗涤3次,离心,
‑
60℃冷冻干燥24h得载氨甲环酸交联多孔淀粉。
46.实施例6、制备载氨甲环酸交联多孔淀粉(1)称取2g淀粉,溶于100ml ph=4.5的磷酸氢二钠柠檬酸缓冲溶液中,50℃水浴,500rpm机械搅拌,加入50knu/g α淀粉酶和10000u/g糖化酶,搅拌6h,加入17ml 0.5m氢氧化钠溶液,使ph值为12,搅拌30min,离心5500rpm*5min,去离子水洗涤三次,冷冻干燥得酶解淀粉。
47.(2)10 g boc
‑
氨甲环酸,100 ml二氯甲烷溶解,30℃、500rpm回流磁力搅拌10min,加入200 μl n,n
‑
二甲基甲酰胺,5.646 ml氯化亚砜搅拌3h。旋蒸,得boc
‑
氨甲酰氯粉末。
48.(3)1 g 酶解淀粉,80℃、500rpm磁力搅拌,加入5g boc
‑
氨甲酰氯,搅拌8h,离心5500rpm*10min,去离子水洗涤3次,离心,
‑
60℃冷冻干燥24h得载氨甲环酸交联多孔淀粉。
49.实施例7:制备载氨甲环酸交联多孔淀粉(1)称取2g淀粉,溶于100ml ph=4.5的磷酸氢二钠柠檬酸缓冲溶液中,50℃水浴,500rpm机械搅拌,加入50knu/g α淀粉酶和10000u/g糖化酶,搅拌6h,加入17ml 0.5m氢氧化钠溶液,使ph值为12,搅拌30min,离心5500rpm*5min,去离子水洗涤三次,冷冻干燥得酶解淀粉。
50.(2)10 g boc
‑
氨甲环酸,100 ml二氯甲烷溶解,30℃、500rpm回流磁力搅拌10min,加入200 μl n,n
‑
二甲基甲酰胺,5.646 ml氯化亚砜搅拌3h。旋蒸,得boc
‑
氨甲酰氯粉末。
51.(3)1 g 酶解淀粉,80℃、500rpm磁力搅拌,加入1g boc
‑
氨甲酰氯,搅拌8h,离心5500rpm*10min,去离子水洗涤3次,离心,
‑
60℃冷冻干燥24h得载氨甲环酸交联多孔淀粉。
52.对比例1、
×
0.5
×
140.21
×
100%]/1=37.612%取代度=162a/[m
氨甲环酸残基
×
100
‑
(m
氨甲环酸
‑
1)
×
a]=162*0.37612/[14021
‑
(140.21
‑
1)
×
0.37612]=0.436(中取代)载氨甲环酸交联多孔淀粉取代度的测定是通过酸碱滴定法测定的,取代度小于0.2属于低取代,在0.2
‑
2之间属于中取代,大于0.2属于高取代,载氨甲环酸交联多孔淀粉取代度为0.436,属于中取代。
[0060]
4吸液率:(1)分别称取0.1g*3马铃薯淀粉、0.1g*3酶解淀粉、0.1g载氨甲环酸交联多孔淀粉,备用。
[0061]
(2)连通器原理:砂芯漏斗筛板与移液管相平,漏斗内及橡胶管内全部储满pbs液(实验装置图见图3(左))。
[0062]
(3)样品均匀洒在砂芯漏斗筛板上,初始20s记录体积,之后每隔10s记录一次。
[0063]
结果见图3(右)。根据吸液率实验结果可知:相对于酶解过程,酯化过程对淀粉吸液率的影响较大,结合扫描电镜结果图可知,淀粉酯化后,颗粒表面出现粗糙现象,同时颗粒表面出现较多的微孔,大大增加材料的比表面积,增加吸液体积。
[0064]
实施例9、载氨甲环酸交联多孔淀粉的安全性测试1体外细胞毒性实验:(一)样品浸提参照“国家标准医疗器械生物学评价
‑
第十二部分:样品制备与参照样品”(gb/t16886.12
‑
2017),0.4g载氨甲环酸交联多孔淀粉加入4.4ml的无血清dmem培养基,37℃浸提24h,所得浸提液上清按体积比加入10 %胎牛血清混匀即为100 %浸提液,另将该100 %浸提液以含10 %胎牛血清的dmem培养基等比稀释混匀即为75%浸提液、50 %浸提液、25%浸提液。
[0065]
1g马铃薯淀粉加入5ml的无血清dmem培养基,37℃浸提24h,浸提液处理方式同载氨甲环酸交联多孔淀粉,分别得到100%浸提液、75%浸提液、50%浸提液、25%浸提液。
[0066]
(二)实验步骤:(1)取生长旺盛的l929细胞,常规0.25%胰酶
‑
edta溶液消化,血细胞板计数,完全培养基稀释成1
×
10
5 /ml细胞悬液,每孔100 μl接种于96孔培养板。置于5%(v/v)二氧化碳混合空气、37℃恒温细胞培养箱内预培养24 h。
[0067]
(2)培养24h后弃去旧培养基,实验组分别加入100 μl100 %浸提液、75 %浸提液、50 %浸提液和25 %浸提液,阴性对照组加入100 μl 含10%肽牛血清培养基,阳性对照组加入100 μl0.2%的苯酚溶液,继续培养24 h。
[0068]
(3)培养24 h后取出培养板,弃去各孔中的液体,每孔加入50 μl新鲜配制的mtt溶液,继续放入培养箱培养3~5 h。
[0069]
(4)取出培养板,弃去各孔内液体,每孔加入 100 μl异丙醇,震荡摇匀至充分溶解。酶标仪570 nm波长测定吸光度(o.d.值)。参比波长 650 nm。
[0070]
按下述计算细胞相对增殖度(relative growth rate,rgr)。
[0071]
rgr (%)=(试验样品100%浸提液光密度平均值/空白光密度平均值)
×
100%注:存活率较低时,试验样品潜在的细胞毒性较高。如存活率下降到<空白的70%,
则具有潜在的细胞毒性。
[0072]
结果见图4。由图4可知,以阴性对照组细胞增殖率为100%参照,阳性对照组细胞相对增殖率仅为阴性对照组的2.0%,说明建模成功,结果数据可靠。载氨甲环酸交联多孔淀粉和马铃薯淀粉的100%浸提液、75%浸提液、50%浸提液和25%浸提液相对于阴性对照组的相对细胞增殖率均值均大于70%,提示样品载氨甲环酸交联多孔淀粉在体外对l929成纤维细胞无细胞毒性。
[0073]
2急性毒性试验:(一)样品浸提参考gb/t 16886.12
‑
2017医疗器械生物学评价第十二部分 样品制备与参照样品。准确称取0.88 g载氨甲环酸交联多孔淀粉,用10.4ml生理盐水在37℃条件下浸提24小时。准确称取2g马铃薯淀粉,用10ml生理盐水在37℃条件下浸提24小时。
[0074]
(二)实验步骤(1)健康昆明种小鼠,18只,18
‑
22 g,雄性,随机分成3组,分别随机设定为生理盐水组、马铃薯淀粉实验组和载氨甲环酸交联多孔淀粉实验组。
[0075]
(2)给药剂量和途径:实验组按50 ml/kg剂量腹腔注射给予对应组的生理盐水浸提液;对照组动物按 50 ml/kg 剂量腹腔注射给予生理盐水。
[0076]
(3)观察:给药后观察各实验组和对照组动物的一般状态(精神状态、外观、大小便、进食情况)、毒性表现,记录死亡动物数。给药后一周记录动物体重。
[0077]
结果见图5。两实验组与对照组动物的一般状态均良好,小鼠饮食、行为等一般情况无异常,各组动物均无死亡。如图5所示,马铃薯淀粉和载氨甲环酸交联多孔淀粉实验组浸提液小鼠腹腔注射后,1天后小鼠体重呈稳定上升趋势,与对照生理盐水组小鼠反应一致,表明马铃薯淀粉和载氨甲环酸交联多孔淀粉无全身急性毒性反应。
[0078]
实施例10、载氨甲环酸交联多孔淀粉的有效性1体外凝血时间试验:载氨甲环酸交联淀粉体外凝血而时间测定:(1)取若干规格5ml离心管,备用。精确称量30mg所得载氨甲环酸交联多孔淀粉样品置于离心管中,以空白离心管做阴性对照,欣速聆止血粉为阳性对照(用量为30mg),对比例1物理混合物的用量为30mg。
[0079]
(2)新西兰兔(雄性,2.0
‑
2.5kg)称重,1ml/kg剂量耳缘静脉注射、兔子仰卧固定,股动脉快速取血,立即向每个离心管管内加入1ml新鲜血液,轻轻晃动,使材料与血液充分接触,37℃水浴条件,每15s倾斜一次离心管,以血液不流动为止,记录凝血时间。
[0080]
结果见图6。由图6可知,新西兰兔空白组血液凝固时间为830s,与空白组相比较,其他实验组显著缩短凝血时间。与阳性对照组欣速聆止血颗粒相比较,实施例6载氨甲环酸交联多孔淀粉血液凝固时间显著降低(p<0.05)。而且载氨甲环酸交联多孔淀粉可以与血液充分接触,发挥止血性能,而不会形成一层膜,进而阻止血液与止血材料的接触,导致在材料的表面发挥止血的功效。
[0081]
小鼠断尾止血:空白纱布、欣速聆止血颗粒和载氨甲环酸交联多孔淀粉分别准确称取100mg,置于2ml离心管中作为样品。雄性昆明小鼠33
‑
39g左右,30只,按体重随机分成3组,每组10只,按
50mg/kg剂量腹腔注射3%戊巴比妥钠水溶液麻醉,将小鼠固定于鼠板,尾巴自由下垂,量取尾巴长度,自尾尖,使用手术剪刀断尾1/2长度,自由出血10s(记录自由出血量),后插入至离心管中,轻轻按压。按压2min后,取出,如继续出血则插入另外一份样品中,同样止血2min,取出观察。鼠尾自然下垂,十分钟内,无活动性出血则记为止血成功;如两次按压止血后,仍未止住出血则记为止血失败,每只小鼠止血过程中最多按压两次;如第一次按压止血后便止血成功,则不再进行第二次按压止血。小鼠断尾出血模型止血后各组止血材料的止血照片见图7。
[0082]
表1止血材料在小鼠断尾模型中止血效果的比较(n=10)根据图8和表1可知,各组小鼠断尾10s内自由出血量组间无显著性差异(p>0.05),说明模型创建成功,重现性良好,各实验组具有可比性。载氨甲环酸交联多孔淀粉止血迅速、效果稳定,止血成功率100%,并且止血按压次数小于另外两组止血材料,出血量显著小于欣速聆止血颗粒(p<0.05)。综上所述,在小鼠断尾模型止血实验中,与国内同类止血材料相比,载氨甲环酸交联多孔淀粉可以有效的应对小型动静脉的出血情况。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。