plerixafor在上调eftud2表达和抑制hbv药物中的用途
技术领域
1.本发明涉及药学领域,尤其涉及plerixafor在上调eftud2表达和抑制hbv药物中的用途。
背景技术:
2.慢性乙型肝炎病毒(hbv)感染是肝硬化和肝细胞癌的主要危险因素。作为治疗慢性hbv感染的主要药物之一,干扰素对实现临床治愈有特定价值,但其病毒学应答率不高、不良反应较多,且最终疗效受宿主因素影响,临床应用受限。因此,hbv的免疫治疗迫切需要新的分子靶点。
技术实现要素:
3.为了解决上述技术问题,申请人对抑制hbv进行了深入且长期的研究,研究发现,延伸因子结合蛋白2(eftud2)是剪接体复合物的一种,相对于干扰素治疗应答良好的慢乙肝患者,eftud2在干扰素应答不佳者的肝组织中的表达水平更低。在体外,eftud2可通过pre
‑
mrna剪接作用调控干扰素通路下游抗病毒基因的表达,从而发挥抗hbv作用。有鉴于此研究,申请人设想,筛选出的靶向eftud2的小分子化合物plerixafor有望为干扰素治疗应答不佳的hbv患者提供全新的免疫治疗选择。
4.为此,申请人对plerixafor进行了专项研究,plerixafor是一种高度特异性的趋化因子受体cxcr4的拮抗剂,其对cxcr4的拮抗作用适用于广泛的病理生理过程,包括治疗癌症、保护心脏功能、对抗关节炎等。早在2008年12月,美国正式批准plerixafor用于非霍奇金淋巴瘤或多发性骨髓瘤患者的骨髓细胞自体移植;随后,plerixafor亦在中国获批上市。随着cxcr4受体及其配体sdf
‑
1在多种病理生理过程中的作用不断发展,plerixafor的潜在应用范围也在不断扩展。
5.事实上,plerixafor最初作为一种抗hiv药物而问世,因其对嗜t4淋巴细胞的hiv毒株具有特异作用。申请人检索了相关文献发现,包括plerixafor在内的这类拮抗cxcr4等趋化因子受体的小分子通过作用于宿主细胞因子而非作用于病毒酶来控制病毒的转录和复制。换言之,这类小分子的抗病毒方式从根本上区别于大多数其他类别的抗逆转录病毒药物,诸如核苷(酸)类似物、蛋白酶抑制剂等。除hiv外,plerixafor还对其他许多免疫缺陷病毒、流感病毒等存在拮抗作用,但是,其是否具有抗hbv作用尚无文献报道。
6.申请人在多次实验的基础上,发现plerixafor可以在体外上调eftud2表达,并可抑制hbsag、总hbv rna、3.5
‑
kbrna及hbvdna水平。这项发现表明,可能揭示了plerixafor上调eftud2并有效对抗hbv的全新药学用途。
7.为此,本发明提出plerixafor在上调eftud2表达和抑制hbv中的用途;
8.其中,所述plerixafor的结构式如下:
[0009][0010]
进一步的,提出plerixafor在上调eftud2表达和抑制hbv药物中的用途。
[0011]
进一步的,所述的上调eftud2表达为,对eftud2启动子作用、基因、蛋白表达等的上调。
[0012]
进一步的,所述抑制hbv为抑制hbsag、总hbv rna、3.5
‑
kb rna及hbv dna水平。
[0013]
进一步的,plerixafor在体外上调eftud2表达,并可抑制hbsag、总hbv rna、3.5
‑
kb rna及hbv dna水平的用途。
[0014]
进一步的,plerixafor在体外上调eftud2表达,并可抑制hbsag、总hbv rna、3.5
‑
kb rna及hbv dna水平药物中的用途。
[0015]
进一步的,所述抑制hbv为,单独或联合使用plerixafor抑制hbv dna、和或hbsag、和或hbeag、和或hbv dna、和或总hbv rna、和或hbv 3.5
‑
kb rna、和或hbv cccdna等指标。
[0016]
进一步的,plerixafor在体外或体外上调eftud2表达,并抑制hbsag、和或总hbv rna、和或3.5
‑
kb rna、和或hbv dna药物中的用途。
[0017]
进一步的,plerixafor在hepad38和或hepg2
‑
ntcp细胞中上调eftud2药物中的用途。
[0018]
进一步的,plerixafor在hepad38细胞中抗hbv药物中的用途。
[0019]
进一步的,plerixafor在hbv体外感染细胞模型中抑制hbv复制和转录,且与etv联用后增强抗hbv效果药物中的用途。
[0020]
进一步的,本发明还提出一种plerixafor与etv药物组合物联合提高抗hbv疗效的用途。
[0021]
本发明涉及的plerixafor化合物可以购买获得,也可通过合成制备。
[0022]
有益效果:本发明涉及的化合物plerixafor对eftud2具有很好的上调作用,对hbv多种指标,尤其是对hbsag、总hbv rna、hbv 3.5
‑
kb rna具有很好的抑制效果,可以为干扰素治疗应答不佳的hbv患者提供更多选择。在一个具体实施例中,plerixafor与etv联合使用可以进一步提高抗hbv疗效,具有良好的药物应用前景。
附图说明:
[0023]
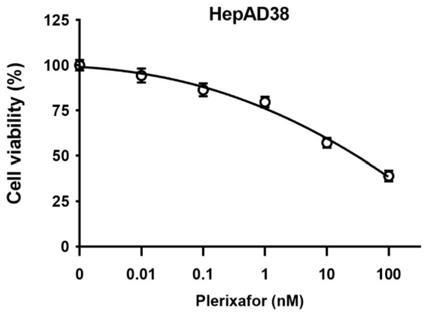
图1.plerixafor对hepad38细胞作用的抑制曲线
[0024]
图2.plerixafor对hepg2
‑
ntcp细胞作用的抑制曲线
[0025]
图3.plerixafor在hepad38细胞中对eftud2的上调作用
[0026]
图4.plerixafor在hepg2
‑
ntcp细胞中对eftud2的上调作用
[0027]
图5
‑
1,plerixafor在hbv复制细胞模型中可抑制上清hbv dna
[0028]
图5
‑
3,plerixafor在hbv复制细胞模型中可抑制胞内hbv dna
[0029]
图5
‑
2,plerixafor在hbv复制细胞模型中可抑制上清hbsag分泌
[0030]
图5
‑
4,plerixafor在hbv复制细胞模型中可抑制hbv总rna
[0031]
图5
‑
5,plerixafor在hbv复制细胞模型中可抑制hbv 3.5
‑
kb rna
[0032]
图6.构建hbv体外感染细胞模型的效果
[0033]
图7
‑
1,plerixafor在hbv体外感染细胞模型中可抑制上清hbv dna
[0034]
图7
‑
2,plerixafor在hbv体外感染细胞模型中可抑制上清hbsag
[0035]
图7
‑
3,plerixafor在hbv体外感染细胞模型中可抑制胞内hbv dna
[0036]
图7
‑
4,plerixafor在hbv体外感染细胞模型中可抑制hbv总rna
[0037]
图7
‑
5,plerixafor在hbv体外感染细胞模型中可抑制hbv 3.5
‑
kb rna
具体实施方式:
[0038]
下面结合附图,对本发明技术方案进行更进一步的描述。
[0039]
以下实施例涉及的引物序列:
[0040]
hbv dna:
[0041]
hbv dna forward 5
’‑
cctagtagtcagttatgtcaac
‑3’
[0042]
hbv dna reverse 5
’‑
tctataagctggaggagtgcga
‑3’
[0043]
总hbv rna:
[0044]
total hbv rnas forward 5
’‑
accgaccttgaggcatactt
‑3’
[0045]
total hbv rnas reverse 5
’‑
gcctacagcctcctagtaca
‑3’
[0046]
hbv 3.5
‑
kb rna:
[0047]
hbv 3.5
‑
kb rna forward 5
’‑
gccttagagtctcctgagca
‑3’
[0048]
hbv 3.5
‑
kb rna reverse 5
’‑
gagggagttcttcttctagg
‑3’
[0049]
药效实验
[0050]
(一)主要实验材料
[0051]
plerixafor购自mce公司;胎牛血清购自美国gibco公司;dmem培养基购自美国gibco公司;opti
‑
mem养基购自美国gibco公司;pbs购自苏州赛默飞世尔仪器有限公司;d
‑
hank's solution购自武汉普诺赛生命科技有限公司;双抗购自上海碧云天公司;trypsin
‑
edta solution购自上海碧云天公司;l
‑
glutamine solution购自美国sigma
‑
aldrich公司。
[0052]
(二)细胞培养
[0053]
本研究应用了以下两种细胞株:人肝癌细胞株hepad38t和hepg2
‑
ntcp。细胞在5%c02
‑
95%空气、饱和湿度以及37℃的条件下,培养于含有10%胎牛血清的dmem培养液中。
[0054]
(三)mtt实验
[0055]
将生长状态良好的hepad38和hepg2
‑
ntcp细胞分别以5000/孔接种96孔板,加入不同浓度的plerixafor,设3个复孔、阴性对照孔和空白孔,置于培养箱中并用药物处理48小时。取出培养板,每孔加入浓度为5mg/ml的mtt溶液10μl,继续在培养箱中避光培养4小时。弃细胞上清,向每孔加入100μl formazan溶解液,并以加入100μl formazan溶解液的空白孔为调零孔。将培养板置于摇床上振荡10分钟,使formazan结晶完全溶解,在酶联免疫分析仪的570nm波长处检测各孔od值。
[0056]
以药物浓度为横坐标,以相应的细胞活性为纵坐标,用graphpad prism 8(graphpad software公司)软件拟合抑制曲线。plerixafor对hepad38细胞的抑制曲线如图1所示,对hepg2
‑
ntcp细胞的抑制曲线如图2所示。
[0057]
(四)检测plerixafor对eftud2的上调作用
[0058]
将生长状态良好的hepad38和hepg2
‑
ntcp细胞分别以5
×
105/孔接种于6孔板。实验组分别加入终浓度为0.2nm和0.5nm的plerixafor处理48小时,设置0.1%dmso为阴性对照组。
[0059]
使用rna
‑
quick purification kit(奕杉生物,上海)提取细胞内总rna,并用nanodrop 2000(thermo fisher scientific,usa)对产物的纯度和浓度进行检测,a260/a280均在1.90
‑
2.00之间,浓度(c)调整至100
‑
1000ng/μl之间。采用taraka公司的反转录试剂盒(rr036a)逆转录生成cdna。以gapdh为内参基因,采用taraka公司的实时荧光定量pcr试剂盒(rr820a)检测eftud2表达。
[0060]
结果如图3、图4所示,在hepad38和hepg2
‑
ntcp细胞中,0.2nm plerixafor可上调eftud2 mrna表达3倍以上,0.5nm plerixafor可上调eftud2 mrna表达4倍以上,效果良好。
[0061]
(五)检测plerixafor在hepad38细胞中的抗hbv效果
[0062]
将生长状态良好的hepad38细胞以5
×
105/孔接种于6孔板。实验组分别加入终浓度为0.2nm、0.5nm、1nm的plerixafor,设置0.1%dmso为阴性对照组、25nm的恩替卡韦(etv)为阳性对照组。分别在第3、6、9天检测细胞上清中的hbv dna(乙型肝炎病毒核酸定量检测试剂盒(荧光探针pcr法),广州达安)、hbsag(乙型肝炎病毒表面抗原诊断试剂盒(酶联免疫法),上海科华),操作方法均按照试剂盒说明进行;检测细胞内hbv dna、hbv总rna、hbv 3.5
‑
kb rna。
[0063]
提取细胞内dna方法:
[0064]
用0.5ml裂解缓冲液(10mmtris
‑
hcl[ph 8.0]、1mm edta、1%np
‑
40、2%蔗糖)在37℃下裂解15分钟,离心去除细胞碎片和细胞核。上清液用终浓度40u/ml的dnase i和10mm的mgcl2处理4小时,然后与200μl含有1.5m nacl的35%peg 8000混合,在冰上孵育1小时。病毒核衣壳在4℃下以11000
×
g离心5分钟沉淀,然后在500μl消化缓冲液(含有0.5mg/ml蛋白酶k、0.5%sds、150mm nacl、25mm tris
‑
hcl[ph 8.0]和10mm edta)中45℃消化过夜。消化混合物用苯酚抽提两次,加乙醇沉淀dna,溶解在te(10mmtris
‑
hcl[ph 8.0],1mm edta)缓冲液中。
[0065]
其余方法同前。pcr结果显示,plerixafor在hbv复制模型即hepad38细胞中,以时间、剂量依赖的方式降低上清hbv dna、胞内hbv dna、hbv总rna、hbv3.5
‑
kb rna的表达;此外,通过elisa法检测上清hbsag,发现hbsag随plerixafor的作用时间、剂量下降。以上结果均验证了plerixafor在hbv复制模型中对hbv有抑制作用,结果如图5所示。
[0066]
(六)检测plerixafor在hbv体外感染细胞模型中的抗hbv效果
[0067]
利用hepg2
‑
ntcp细胞构建hbv体外感染细胞模型的方法:
[0068]
hbv浓缩液的制备。hepad38细胞在含有2μg/ml强力霉素和400μg/ml g418的培养基中生长至80%融合,换用不含强力霉素和g418的培养基继续培养10
‑
14天,每隔2天收集上清液、保存于4℃。将收集的所有上清液在4℃下250
×
g离心20分钟,取上清,0.45μm无菌过滤后,加入peg 8000,终浓度为8%。反复颠倒混匀,4℃过夜。次日在4℃、10000
×
g离心1
小时,弃掉上清液,即得到纯化的hbv病毒。以适量deme重悬,pcr确定病毒滴度,储存在
‑
80℃备用。
[0069]
hepg2
‑
ntcp细胞在培养基中用2μg/ml强力霉素预处理2
‑
3天以诱导ntcp受体表达。随后,在4%peg 8000存在下,将制备的hbv病毒与经强力霉素处理的细胞分别以100、200、500geq/cells的感染复数(moi)孵育24小时。用pbs洗涤细胞3次,并进一步用含有强力霉素的培养基维持培养。
[0070]
上述操作后,分别在第12、24、48、72h检测上清中hbv dna载量,结果如图6所示,当moi=500geq/cells时,上清中hbv dna随时间显著上升,幅度较moi=100、200geq/cells组更加显著;此外,72h后moi=500geq/cells组上清中hbv dna>1.2x 105,根据以上结果可确定感染成功。
[0071]
在构建完成的感染模型中,实验组为:1nm plerixafor处理组和1nm plerixafor 25nm etv联合治疗组,设置0.1%dmso为阴性对照组、25nm的恩替卡韦(etv)为阳性对照组。在第10天检测细胞上清中的hbv dna、hbsag,检测细胞内hbv dna、总hbv rna、hbv 3.5
‑
kb rna。方法同前。
[0072]
与在hbv复制模型中类似地,pcr和elisa结果显示,在hbv体外感染细胞模型中单独使用plerixafor同样有效抑制了上清hbv dna、hbsag、胞内hbv dna、hbv总rna、hbv 3.5
‑
kb rna的表达;相对地,单用etv仅能降低hbv dna,并不能减少hbsag的分泌和hbv rna的表达。此外,plerixafor etv的组合提高了plerixafor的抗病毒活性,结果如图7所示。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。