诱导treg细胞的酵母衍生多糖的结构和功能特征
【技术领域】
1.本发明涉及一种诱导treg细胞的酵母衍生多糖及其用途,并且更特别地涉及一种含有甘露聚糖和β
‑
葡聚糖的多糖、一种包含所述多糖作为活性成分的用于免疫调节的组合物、一种含有所述多糖作为活性成分的用于预防或治疗免疫疾病或炎性疾病的药物组合物或食品、一种使用所述多糖制备调节t细胞的方法、一种含有通过所述方法制备的调节t细胞作为活性成分的细胞治疗剂、以及一种治疗免疫疾病或炎性疾病的方法,所述方法包括向受试者施用所述细胞治疗剂。
背景技术:
2.哺乳动物含有与免疫系统持续相互作用的微生物群。共生微生物与宿主形成共生关系,并在各种过程(如免疫系统的消化、行为和成熟化)中与宿主相互作用(cerf
‑
bensussan n.,gaboriau
‑
routhiau v.the immune system and the gut microbiota:friends or foes?nat.rev.immunol.2010;10(10):735
‑
44.)。类似地,真菌存在于人体中并影响宿主的免疫系统(wheeler m.l.,limon j.j.,underhill d.m.immunity to commensal fungi:detente and disease.annu.rev.pathol.2017;12:359
‑
85.)。先天免疫细胞通过模式识别受体(prr)(如toll样受体(tlr))检测真菌细胞表面上的多种病原体相关分子模式(pamp),包括多糖。检测到信号后,先天免疫细胞改变基因表达谱并产生免疫信号传导分子(如细胞因子),以调节获得性免疫(iliev i.d.,leonardi i.nat.rev.immunol.2017;17(10):635
‑
46.、underhill d.m.,iliev i.d.nat.rev.immunol.2014;14(6):405
‑
16.和brubaker s.w.,bonham k.s.,zanoni i.,等人annu.rev.immunol.2015;33:257
‑
90.)。
3.这些共生微生物调节某些cd4细胞谱系(如t辅助17细胞(th17)或调节t细胞(treg细胞))的发育和分化。treg细胞属于具有免疫抑制功能的cd4 细胞子集,并且其特征在于转录因子foxp3的表达。treg细胞主要分为胸腺衍生细胞(ntreg细胞)和非胸腺衍生细胞,这取决于其产生的位置,并且在次级免疫系统中分为源自cd4 t幼稚细胞的treg细胞(itreg或ptreg)。在体内的treg细胞富集可以控制各种超免疫疾病,如自身免疫疾病和过敏性疾病。尚未清楚阐明这些treg细胞的产生所蕴含的分子机制,但是若干研究报告已经报道,细菌产生的代谢物或源自细胞壁的具有特定化学结构的多糖可以促进treg细胞的分化。例如,已经报道了丁酸酯作为主要效应分子在梭菌属(clostridia)的存在下诱导结肠treg细胞的分化(furusawa等人,nature504:446
‑
450,2013)。多糖a(psa)作为脆弱拟杆菌(b.fragilis)的两性离子多糖已被鉴定为诱导il
‑
10产生treg细胞所必需的效应免疫调节剂(mazmanian等人,cell 122:107
‑
118,2005;ochoa
‑
reparaz等人,the journal of immunology 185:4101
‑
4108,2010)。还已经报道,csgg等作为源自两歧双歧杆菌(bifidobacterium bifidum)的细胞表面多糖可以诱导treg细胞的分化(ravi verma等人,science immunology 3(28),eaat6975)。
4.为了将此类微生物或其代谢产物用于治疗患者的疾病,一些患者必须调节过度活
跃的免疫应答(即,在过敏或自身免疫疾病的情况下),而其他患者必须增强免疫系统(即,在癌症或病毒感染的情况下)。例如,当将作为th17诱导的益生菌的双歧杆菌施用于类风湿性关节炎动物模型时,关节炎症状加重(tze guan tan,113(50):e8141
‑
e8150,2016)。因此,鉴定有益微生物并阐明其激动剂的机制在治疗上非常重要。
5.同时,酵母衍生多糖具有免疫调节功能,并被用作激活或调节免疫系统的治疗剂(tzianabos a.o.clin.microbiol.rev.2000;13(4):523
‑
33.)。β
‑
葡聚糖是真菌细胞壁中最丰富的多糖,具有复杂多样的结构(camilli g.,tabouret g.,quintin j.the complexity of fungal beta
‑
glucan in health and disease:effects on the mononuclear phagocyte system.)。已知它们调节影响免疫应答的生物反应(silva vdo,de moura n.o.,de oliveira l.j.r.,等人promising effects of beta
‑
glucans on metabolism and on the immune responses:review article.)。
6.一般来说,研究人员已经使用β
‑
葡聚糖作为感染性疾病的治疗剂或癌症的治疗佐剂(sun b.,yu s.,zhao d.,等人vaccine 2018;36(35):5226
‑
34.和novak m.,vetvicka v.j.immunotoxicol.2008;5(1):47
‑
57.)。同时,一些研究已经报道β
‑
葡聚糖具有抗炎功能(dalonso n.,goldman g.h.,gern r.m.appl.microbiol.biotechnol.2015;99(19):7893
‑
906.和lee k.h.,park m.,ji k.y.,等人bacterial beta
‑
(1,3)
‑
glucan prevents dss
‑
induced ibd by restoring the reduced population of regulatory t cells.)。与真菌β
‑
葡聚糖类似,也已经报道真菌甘露聚糖起免疫调节作用(saijo s.,ikeda s.,yamabe k.,等人dectin
‑
2recognition of alpha
‑
mannans and induction of th17 cell differentiation is essential for host defense against candida albicans.)。然而,尽管已经报道多糖作为免疫调节剂的作用,但多糖调节免疫系统的确切元件和机制尚未被明确阐明。特别地,根据所述多糖的结构和分子量而以不同方式发生的免疫应答(免疫增强或超免疫调节反应)尚未被准确地定义。阐明这一点非常重要,以便以所需的模式重新设计(改变)关于特定疾病的不期望的免疫应答,以应用于疾病的治疗剂的开发。
7.酵母聚糖是酵母血影细胞(酿酒酵母(saccharomyces cerevisiae)),并且大多数酵母具有类似的细胞壁组分。酵母细胞壁具有两层结构,分为由甘露聚糖构成的外膜和由葡聚糖构成的具有复杂结构的内膜,所述复杂结构包括通过β
‑
1,6
‑
葡聚糖连接的多层β
‑
1,3
‑
连接的葡聚糖(gow nar,latge j.p.,munro c.a.the fungal cell wall:structure,biosynthesis,and function.microbiol.spectr.2017;5(3))。酵母聚糖的多糖主要由β
‑
葡聚糖和甘露聚糖构成,这在结构上与酵母的那些类似。在许多其他研究中,酵母聚糖已被用于研究真菌多糖对免疫系统的作用,但这些研究的结果存在争议。一些研究已经表明酵母聚糖通过激活免疫系统加剧了炎性疾病(sanguedolce m.v.,capo c.,bongrand p.,等人zymosan
‑
stimulated tumor necrosis factor
‑
alpha production by human monocytes和gantner b.n.,simmons r.m.,canavera s.j.,等人j.exp.med.2003;197(9):1107
‑
17),并且其他研究证明酵母聚糖可以通过诱导il
‑
10产生免疫耐受抗原呈递细胞来免疫地诱导抗性,所述il
‑
10产生免疫耐受抗原呈递细胞抑制抗原特异性t细胞反应以缓解自身免疫疾病(karumuthil
‑
melethil s等人diabetes 2015;64(4):1341
‑
57.和dillon s.,agrawal s.,banerjee k.,等人j.clin.invest.2006;116(4):916
‑
28.)。
8.在上述技术背景下,由于广泛努力以准确地鉴定在酵母衍生多糖中具有免疫调节
功能的元件及其机制以及找到即使在基于此的低剂量下也能有效诱导treg分化或产生的物质,因此本发明人从酵母细胞壁纯化了新型多糖,并将其命名为相同的“mgcp(含甘露聚糖/β
‑
葡聚糖的多糖)”。此外,本发明人发现,可以在体外和体内由mgcp诱导treg细胞,并且β
‑
1,6
‑
葡聚糖是由mgcp诱导treg细胞所必需的,并且mgcp或由mgcp诱导的treg细胞的施用可以抑制结肠炎。基于这些发现,完成了本发明。
9.此背景技术章节中公开的信息仅为更好地理解本发明背景而提供,并且因此所述信息可能不包括形成对本领域技术人员而言已经清楚的现有技术的信息。
技术实现要素:
10.【技术问题】
11.因此,本发明是鉴于上述问题而做出的,并且本发明的一个目的是提供一种包含甘露聚糖和贝塔
‑
葡聚糖(β
‑
葡聚糖)的新型多糖。
12.本发明的另一个目的是提供一种用于免疫调节的组合物,其包含所述多糖作为活性成分。
13.本发明的另一个目的是提供一种用于预防和治疗免疫疾病或炎性疾病的药物组合物,其包含所述多糖作为活性成分。
14.本发明的另一个目的是提供一种用于预防或改善免疫疾病或炎性疾病的食品,其包含所述多糖作为活性成分。
15.本发明的另一个目的是提供一种预防或治疗免疫疾病或炎性疾病的方法,其包括向受试者施用包含所述多糖作为活性成分的组合物。
16.本发明的另一个目的是提供包含所述多糖作为活性成分的组合物用于预防或治疗免疫疾病或炎性疾病的用途。
17.本发明的另一个目的是提供一种使用所述多糖产生调节t细胞(treg细胞)的方法。
18.本发明的另一个目的是提供一种用于预防、治疗或改善免疫疾病或炎性疾病的细胞治疗剂,其包含通过所述方法产生的调节t细胞(treg细胞)作为活性成分。
19.本发明的另一个目的是提供一种用于预防或治疗免疫疾病或炎性疾病的方法,其包括向受试者施用所述细胞治疗剂。
20.本发明的另一个目的是提供所述细胞治疗剂用于预防或治疗免疫疾病或炎性疾病的用途。
21.【技术解决方案】
22.为了实现上述目的,根据一个方面,本发明提供了一种包含甘露聚糖和贝塔
‑
葡聚糖(β
‑
葡聚糖)的多糖。
23.根据另一方面,本发明提供了一种用于免疫调节的组合物,其包含所述多糖作为活性成分。
24.根据另一方面,本发明还提供了一种用于预防和治疗免疫疾病或炎性疾病的药物组合物,其包含所述多糖作为活性成分。
25.根据另一方面,本发明还提供了一种用于预防或改善免疫疾病或炎性疾病的食品,其包含所述多糖作为活性成分。
26.根据另一方面,本发明还提供了一种预防或治疗免疫疾病或炎性疾病的方法,其包括向受试者施用包含所述多糖作为活性成分的所述组合物。
27.根据另一方面,本发明还提供包含所述多糖作为活性成分的组合物用于预防或治疗免疫疾病或炎性疾病的用途。
28.根据另一方面,本发明还提供了一种产生调节t细胞(treg细胞)的方法,所述方法包括用所述多糖处理抗原呈递细胞,然后获得致耐受性抗原呈递细胞;以及将所述致耐受性抗原呈递细胞与cd4 t细胞共孵育,然后诱导调节t细胞(treg细胞)。
29.根据另一方面,本发明还提供了一种用于预防、治疗或改善免疫疾病或炎性疾病的细胞治疗剂,其包含通过所述方法产生的调节t细胞(treg细胞)作为活性成分。
30.根据另一方面,本发明还提供了一种用于预防或治疗免疫疾病或炎性疾病的方法,其包括向受试者施用所述细胞治疗剂。
31.根据另一方面,本发明提供了所述细胞治疗剂用于预防或治疗免疫疾病或炎性疾病的用途。
【附图说明】
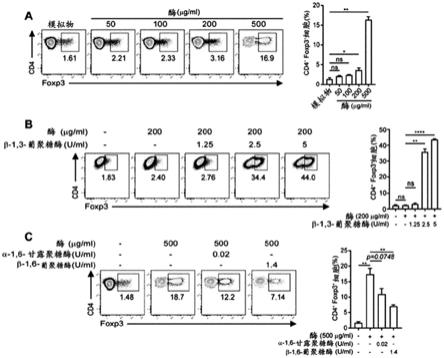
32.图1显示了源自酵母聚糖的多糖组分对体外产生treg细胞的不同影响,其中用指示剂量的酵母聚糖刺激脾脏cd11c dc,然后将其与未分化(幼稚)cd4 t细胞共孵育,流式细胞术图表示三个独立实验,图中的所有数据表示平均值
±
sem,*表示p<0.05,**表示p<0.01,***表示p<0.001,并且****表示p<0.0001(student's t检验)。
33.图1a显示了由不同浓度的酵母聚糖诱导的cd4 foxp3 t细胞的频率。
34.用每种切割酶消化指示量的酵母聚糖,然后在添加幼稚cd4 t细胞之前用切割的酵母聚糖引发脾脏cd11c dc(图1b和图1c)。
35.图1b显示了由β
‑
1,3
‑
葡聚糖酶处理的酵母聚糖诱导的cd4 foxp3 t细胞的频率。
36.图1c显示了由指示的酶和切割的酵母聚糖诱导cd4 foxp3 t细胞。
37.图2显示了酵母聚糖的多糖在免疫应答中的作用。
38.用不同剂量的酵母聚糖刺激脾脏cd11c dc,然后将其在th1和th17细胞的方向上的次最佳偏移条件下与幼稚cd4 t细胞共孵育,图中所有数据表示平均值
±
sem,*表示p<0.05,**表示p<0.01,***表示p<0.001,并且****表示p<0.0001(student's t检验)。
39.图2a显示了在th1和th17细胞的方向上的最佳偏移条件下t
‑
bet或rorγt的流式细胞术图和mfi。
40.在刺激脾脏dc之前,通过用同源切割酶处理从指示剂量的酵母聚糖去除某些多糖。用修饰的酵母聚糖处理在th1或th17操作环境中与幼稚cd4 t细胞共孵育的dc。
41.图2b显示了通过去除了β
‑
1,3
‑
葡聚糖的酵母聚糖得到的t
‑
bet或rorγt的mfi。
42.图2c显示了通过甘露糖苷酶或β
‑
1,6
‑
葡聚糖酶处理的酵母聚糖得到的t
‑
bet或rorγt的mfi。
43.图3显示了mgcp的化学组成和功能特性。
44.图3a显示了mgcp的组成。
45.在与幼稚cd4 t细胞共孵育之前,用指示的多糖刺激脾脏dc。
46.图3b显示了由甘露聚糖或凝胶多糖(β
‑
1,3
‑
葡聚糖)诱导的cd4 foxp3 t细胞的频
率。
47.图3c显示了由石耳多糖(线性β
‑
1,6
‑
葡聚糖)诱导的cd4 foxp3 t细胞的频率。
48.图3d显示了由不同浓度的d
‑
( )甘露糖诱导的cd4 foxp3 t细胞的频率。
49.图3e显示了由在完整的酵母细胞壁或已去除了β
‑
1,3
‑
葡聚糖的酵母细胞壁中纯化的mgcp诱导的cd4 foxp3 t细胞的频率。
50.条形图中的所有数据表示平均值
±
sem,*表示p<0.05,**表示p<0.01,***表示p<0.001,并且****表示p<0.0001(student's t检验)。
51.图4是显示mgcp的组成的分析结果的表。
52.图5显示了β
‑
1,6
‑
葡聚糖在通过mgcp分化treg细胞中的作用。
53.图5a显示了mgcp的质子nmr谱。
54.图5b显示了甘露聚糖的化学结构。
55.图5c显示了mgcp的β
‑
1,6
‑
葡聚糖部分的化学结构。
56.以图1中相同的方式,在与幼稚cd4 t细胞共孵育之前,用指示的分子处理脾脏cd11c dc(图5d和图5e)。
57.图5d显示了由mgcp诱导的cd4 foxp3 t细胞的频率。
58.图5e显示了由用指示的酶切割的mgcp诱导treg细胞。
59.流式细胞术图表示具有类似结果的三个独立实验,图中所有数据表示平均值
±
sem,*表示p<0.05,**表示p<0.01,***表示p<0.001,并且****表示p<0.0001(student's t检验)。
60.图6显示了使用hplc对整个mgcp进行分析的结果,其中hplc分析条件如下:使用tsk g
‑
5000pwxl尺寸排阻柱,洗脱液是碳酸氢铵50mm,并且流速为0.8ml/min,在206nm的波长下使用折射率检测器和uv检测器检测分析结果,并且用于检测分子量的标准材料是右旋糖酐标准品,并且关于其信息如表2中所示,并且a、b和c表示基于hplc分析结果通过分馏获得的三种级分。
61.图7显示了图6中mgcp的级分a、b和c的hplc分析结果,其中在与图6中相同的条件下进行分析,用于检测分子量的标准材料是右旋糖酐标准品,并且关于其信息如表2中所示。
62.图8显示了由mgcp(体内)诱导的treg细胞的炎性免疫应答的调节。itreg细胞是通过将脾脏dc与幼稚cd4 t细胞(cd45.1 cd4 foxp3egfp
‑
cd44locd62lhi)(与脾脏dc同类系标记的)在体外共孵育而产生的,itreg细胞(cd45.1 cd4 foxp3egfp )是选择的fac,并且与幼稚cd4 t细胞(cd45.1
‑
cd4 foxp3thy1.1cd44locd62lhi)一起被过继转移至rag1
‑
/
‑
小鼠。在终点对小鼠进行分析。每个点表示单独小鼠,并且条形图中的所有数据表示平均值
±
sem。*表示p<0.05,**表示p<0.01,***表示p<0.001,并且****表示p<0.0001(student's t检验)。
63.图8a显示了体重的变化。
64.图8b是显示结肠长度的图像。
65.图8c是显示h&e染色的结肠的图像。
66.图8d显示了结肠炎的组织病理学得分。
67.图8e显示了在供体幼稚cd4 t细胞(cd45.1
‑
)中ifn
‑
γ的产生。
68.图9显示了在体内补充mgcp促进新treg细胞的产生,其中小鼠(cd45.1
‑
)每天用模拟物或200μg的mgcp进行处理,持续2周,然后接受同类系标记的幼稚cd4 t细胞(cd45.1 cd4 foxp3egfp
‑
cd44locd62lhi),在转移细胞之后,进一步施用mgcp持续一周,分析了在接受者小鼠的结肠固有层中的cd4 t细胞,每个点表示单独小鼠,流式细胞术图表示独立实验,条形图中的所有数据表示平均值
±
sem,*表示p<0.05,**表示p<0.01,并且***表示p<0.001(student's t检验)。
69.图9a显示了源自供体细胞的treg细胞(cd45.1 cd4 foxp3egfp )的频率。
70.图9b显示了源自供体细胞(cd45.1 )的cd4 foxp3egfp
‑
和cd4 foxp3egfp cd4 t细胞中ctla
‑
4的mfi。
71.图9c显示了接受者衍生细胞(cd45.1
‑
cd4 foxp3egfp )中treg细胞的频率。
72.图9d显示了ctla
‑
4在宿主(cd45.1
‑
)衍生cd4 foxp3
‑
细胞和cd4 fo xp3 细胞中的表达。
73.图9e显示了在结肠固有层中接受者衍生treg细胞的数量。
74.图9f显示了在宿主衍生treg细胞(cd45.1
‑
cd4 foxp3egfp helios
‑
)中外周treg细胞的频率。
75.图9g显示了从结肠treg细胞(cd4 foxp3egfp )产生的il
‑
10。
76.图9h显示了在效应cd4 t细胞(cd4 foxp3egfp
‑
)中ifn
‑
γ和il
‑
17a的量。
77.图10显示mgcp的补充诱导小肠中的treg细胞,但不诱导淋巴结组织中的treg细胞。以与图9中所示相同的方式,每天施用mgcp(200μg),持续2周,然后接受同类系标记的幼稚cd4 t细胞。将mgcp补充再持续一周。评价了小肠粘膜中的cd4 t细胞(a
‑
h)。每个点表示单独小鼠。流式细胞术图表示具有类似结果的三个独立实验。条形图中的所有数据表示平均值
±
sem。*表示p<0.05,**表示p<0.01,并且***表示p<0.001(student's t检验)。
78.图10a显示了从供体细胞向cd4 foxp3 t细胞的分化。
79.图10b显示了来自供体衍生cd4 t细胞的ctla
‑
4表达。
80.图10c显示了cd4 foxp3 t细胞在受体细胞中的频率。
81.图10d显示了宿主衍生cd4 t细胞中ctla
‑
4的mfi。
82.图10e显示了小鼠结肠中cd4 foxp3 t细胞的数量。
83.图10f显示了在接受者衍生cd4 foxp3 t细胞中诱导型treg细胞的比例。
84.图10g显示了在cd4 foxp3 t细胞中il
‑
10的产生。
85.图10h显示了在效应cd4 t细胞(cd4 foxp3
‑
)中ifn
‑
γ和il
‑
17a的产生。
86.图10i显示了源自mln中的受体和供体细胞的cd4 foxp3 t细胞。
87.图10j显示了源自脾脏中的受体和供体细胞的cd4 foxp3 t细胞。
88.图11显示mgcp的施用诱导了抗原反应性treg细胞并减轻了实验性结肠炎。将从cbir小鼠分离的幼稚cd4 t细胞(cd4 foxp3egfp
‑
cd44locd62lhi)过继转移至rag1缺乏型小鼠。在整个实验中,在细胞过继转移前一天开始每隔一天补充dw(模拟物)或200μg的mgcp。在终点对受体进行分析。在终点对小鼠进行分析。每个点表示单独小鼠。数据表示三个独立实验。条形图中的所有数据表示平均值
±
sem,*表示p<0.05,**表示p<0.01,并且***表示p<0.001(student's t检验)。
89.图11a显示了体重的变化。
90.图11b是显示结肠的代表性图像。
91.图11c显示了初始体重时的正常结肠长度。
92.图11d是显示h&e染色的结肠的图像。
93.图11e显示了结肠炎的组织病理学得分。
94.图11f显示了在体重减轻早期从结肠固有层诱导cd4 foxp3 t细胞的分析结果。
95.图11g显示了在实验终点从结肠cd4 t细胞(cd4 foxp3egfp
‑
)产生的ifn
‑
γ。
96.图12显示了在患有结肠炎的状态下施用mgcp对免疫的影响。
97.图12a显示了在施用了模拟物和mgcp并且在体重减轻之前接受了结肠cd4 foxp3 t细胞的rag1缺乏型小鼠中cd103和ctla
‑
4的表达水平。
98.图12b显示了在实验的结束阶段由源自结肠固有层的cd4 t细胞产生的il
‑
17a。
99.条形图中的所有数据表示平均值
±
sem,*表示p<0.05,**表示p<0.01,并且***表示p<0.001(student's t检验)。
100.图13显示了mgcp调节dc关于调节表型的转录组构型。dc子集(mhcii cd11c )是根据cd103和cd11b的表达从小肠分类的fac,并且使用与图1中相同的实验程序测试了mgcp诱导treg细胞的能力。流式细胞术图表示具有类似结果的三个独立实验,并且条形图中的所有数据表示平均值
±
sem。*表示p<0.05,**表示p<0.01,并且***表示p<0.001(student's t检验)。
101.图13a显示了每个dc子集中由mgcp介导的对cd4 foxp3 t细胞的诱导的数据。
102.将模拟物或mgcp施用于gf小鼠(n=6),持续2周。从结肠cd11c dc纯化转录物。
103.图13b显示了施用了模拟物和mgcp的gf小鼠的结肠dc中的免疫调节相关标记。
104.图13c显示了免疫耐受dc标记在结肠dc中的表达。
105.在用mgcp处理之前cox2在脾脏dc中受到抑制,并且在存在cox2选择性抑制剂塞来昔布的情况下,将幼稚cd4 t细胞与dc孵育72小时。
106.图13d显示了cd4 foxp3 t细胞的流式细胞术图。
107.图13e显示了在存在/不存在塞来昔布以及用模拟物或mgcp处理的情况下诱导的的cd4 foxp3 t细胞的频率。
108.图14显示了肠巨噬细胞对通过mgcp产生treg细胞的影响。在与幼稚cd4t细胞共孵育之前,将纯化的肠巨噬细胞(mhcii cd11c cd11b f4/80 cd103
‑
)fac用mgcp刺激。流式细胞术图表示具有类似结果的两个独立实验。
109.图15显示了由mgcp诱导的treg细胞的产生与各种prr之间的关系。以类似于图1中所示的方式用mgcp处理从特定的先天免疫受体缺陷小鼠纯化的脾脏dc。将幼稚cd4 t细胞与mgcp刺激的dc一起孵育。
110.图15a显示了当用mgcp或模拟物处理每个受体缺乏型dc时cd4 foxp3 t细胞的频率。
111.图15b显示了当用mgcp或模拟物处理myd88信号传导系统缺乏型dc时cd4 foxp3 t细胞的频率。
112.图15c显示了产生的cd4 foxp3 t细胞的频率。在图15c中,在用mgcp处理脾脏dc之前,用拮抗剂阻断某些clr。洗出残留的拮抗剂和mgcp之后,将dc与幼稚cd4 t细胞共孵育。
113.条形图中的所有数据是平均值
±
sem,*表示p<0.05,**表示p<0.01,并且***表示p
<0.001(student's t检验)。
114.图16显示了dectin1对由mgcp诱导treg细胞的影响。用mgcp刺激decti n1富有型/缺乏型小鼠的肠系膜淋巴结cd11c dc,持续8小时。dectin1受损/完整小鼠每天补充200μg的mgcp,持续2周,并接受“同类系”标记的ot
‑
ii幼稚cd4 t细胞(thy1.1 vα2 cd4 foxp3egfp
‑
cd44locd62lhi)。从细胞转移前一天开始,每隔一天向受体施用ova蛋白(20mg),并且同时每天进一步施用mgcp,持续一周。
115.图16a显示了用模拟物或mgcp处理的dc中cox2转录物的表达。
116.图16b显示了源自小肠固有层中的供体ot
‑
ii cd4 t细胞的treg细胞的流式细胞术图。
117.图16c显示了源自供体ot
‑
ii cd4 t细胞的treg细胞在小肠固有层中的频率。
118.图16d显示了从小肠中的受体细胞分化的诱导型treg细胞的比例的流式细胞术图。
119.图16e显示了从小肠中的受体细胞分化的诱导型treg细胞比例的频率。
120.数据表示具有类似结果的三个独立实验。条形图中的所有数据表示平均值
±
sem。*表示p<0.05,**表示p<0.01,***表示p<0.001,并且****表示p<0.0001(student's t检验)。
121.图17显示了dectin1识别mgcp并诱导treg细胞的产生。刺激dectin1富有型/缺乏型小鼠的肠系膜淋巴结cd11c dc,持续8小时。在图17b至图15d中,在接受ot
‑
ii幼稚cd4 t细胞(thy1.1 vα2 cd4 foxp3egfp
‑
cd44locd62lhi)之前,每天向dectin1受损/完整小鼠补充200μg的mgcp,持续2周。每隔一天施用ova蛋白(20mg/小鼠)并且进一步施用mgcp,持续一周。
122.图17a显示了指示的免疫耐受dc相关转录物的表达水平。
123.图17b显示了小肠中接受者衍生cd4 foxp3 t细胞的频率。
124.图17c显示了小肠中接受者衍生cd4 foxp3 t细胞的数量。
125.图17d显示了肠系膜淋巴结中供体衍生ova反应性cd4 foxp3 t细胞的频率。
126.每个点表示单独小鼠。数据表示具有类似结果的三个独立实验。条形图中的所有数据是平均值
±
sem。*表示p<0.05,**表示p<0.01,***表示p<0.001,并且****表示p<0.0001(student's t检验)。
【具体实施方式】
127.除非另外定义,否则本文所用的所有技术和科学术语的含义与由本发明所属领域中的技术人员所理解的含义相同。通常,本文所用的命名法是本领域中熟知的,并且是通常使用的。
128.许多研究已经报道了酵母聚糖可以刺激前炎性免疫应答,并且已经报道了一些结果,表明酵母聚糖在降低免疫方面发挥作用。然而,决定免疫应答的酵母的确切多糖结构仍然未知。
129.在本发明的一个实施方案中,酵母聚糖的实验数据显示大量(500μg/ml)的酵母聚糖促进treg细胞的分化,而低剂量(50μg/ml)反而促进rorγt的表达,并且不促进treg的分化。另外,发现多糖的组分中的β
‑
1,6
‑
葡聚糖和甘露聚糖促进treg细胞的分化,并且β
‑
1,3
‑
葡聚糖抑制treg细胞的分化。
130.在本发明的另一个实施方案中,从酵母的细胞壁纯化包含甘露聚糖和β
‑
葡聚糖的新型多糖并且被称为相同的“包含甘露聚糖/β
‑
葡聚糖的多糖(mgcp)”,它们是本发明人在实施方案中鉴定出的treg细胞诱导组分,并且发现即使通过在体外和体内用低浓度的所述多糖治疗或施用也可以有效地诱导treg细胞。因此,关于受体、基因转录物形态变化和细胞因子表达,建立了基于源自酵母细胞壁的新型多糖的构型和结构的treg细胞分化机制,并且发现了所述多糖或由此诱导的treg细胞的施用在体内有效地抑制结肠炎。
131.在一个方面,本发明涉及一种包含甘露聚糖和贝塔
‑
葡聚糖(β
‑
葡聚糖)的多糖。
132.在本发明中,所述多糖可以具有这样的结构,其中具有α
‑
1,6
‑
连接的甘露糖骨架的甘露聚糖与具有β
‑
1,6
‑
连接的葡萄糖骨架的贝塔
‑
葡聚糖(β
‑
葡聚糖)结合。
133.在本发明的一个实施方案中,作为源自酵母的新型多糖(mgcp)的结构/功能分析的结果,鉴定了甘露聚糖与β
‑
葡聚糖之间的特定结合结构,并且发现β
‑
1,6
‑
葡聚糖骨架和甘露聚糖促进treg细胞的分化,并且β
‑
1,3
‑
葡聚糖抑制treg细胞的分化。
134.在本发明的一个实施方案中,发现所述多糖具有甘露糖(80.6%):葡萄糖(14.9%):半乳糖(4.5%)的组成比率。发现甘露聚糖单元的详细结构具有α
‑
1,6
‑
连接的甘露糖骨架,并通过α
‑
1,2
‑
连接或α
‑
1,3
‑
连接与作为侧链的单个单元甘露糖(30%)、二单元甘露糖(16.8%)或三单元甘露糖(28.4%)连接(无侧链的甘露糖(24.8%))(图5b)。
135.在本发明中,所述多糖可以包含甘露糖、葡萄糖和半乳糖,其含量比率为80.5%:15.0%:4.5%、特别地为80.6%:14.9%:4.5%、更特别地为79.4%:14.7%:4.4%,但本发明不限于此。
136.因此,在本发明中,所述多糖可以包含含量比率为70%至90%:10%至30%的甘露糖和葡萄糖。在一些情况下,所述多糖还可以包含多于0%且少于10%的量的半乳糖。
137.在本发明中,所述甘露聚糖包含i)α
‑
1,6
‑
连接的甘露糖骨架以及ii)作为侧链,选自α
‑
1,2
‑
连接的或α
‑
1,3
‑
连接的单个单元甘露糖、α
‑
1,2
‑
连接的或α
‑
1,3
‑
连接的二单元甘露糖和α
‑
1,2
‑
连接的或α
‑
1,3
‑
连接的三单元甘露糖的至少一种。特别地,所述甘露聚糖可以包含i)α
‑
1,6
‑
连接的甘露糖骨架以及ii)作为侧链的α
‑
1,2
‑
连接的或α
‑
1,3
‑
连接的单个单元甘露糖、二单元甘露糖和三单元甘露糖。
138.在本发明中,所述多糖可以包含所述单个单元甘露糖侧链、所述二单元甘露糖侧链、所述三单元甘露糖侧链和无侧链的甘露糖骨架,其含量比率为20%至40%:10%至30%:20%至40%:20%至40%。
139.特别地,所述多糖的甘露聚糖可以包含30%的所述单个单元甘露糖、17.0%的所述二单元甘露糖和28.5%的所述三单元甘露糖,特别地30%的所述单个单元甘露糖、16.8%的所述二单元甘露糖和28.4%的所述三单元甘露糖,更特别地25.7%的所述单个单元甘露糖、22.6%的所述二单元甘露糖和27.0%的所述三单元甘露糖,但不限于此。
140.在本发明的一个实施方案中,所述甘露聚糖具有30%的所述单个单元甘露糖、16.8%的所述二单元甘露糖和28.4%的所述三单元甘露糖的组成。
141.此外,在本发明中,所述贝塔
‑
葡聚糖(β
‑
葡聚糖)包含β
‑
1,6
‑
连接的葡萄糖骨架和作为侧链的β
‑
1,3
‑
连接的单个单元葡萄糖。优选地,所述β
‑
1,3
‑
连接的葡萄糖侧链相对于总葡萄糖的比例可以为20.0%、特别地为18.0%,但不限于此。在本发明的一个实施方案
中,发现所述贝塔
‑
葡聚糖(β
‑
葡聚糖)以相对于总葡萄糖的18%的量包含β
‑
1,3
‑
连接的葡萄糖侧链。
142.在本发明中,发现β
‑
1,6
‑
葡聚糖和甘露聚糖促进treg细胞的分化,并且β
‑
1,3
‑
葡聚糖抑制treg细胞的分化。因此,所述β
‑
葡聚糖可以仅由β
‑
1,6
‑
连接的葡萄糖构成,而不含β
‑
1,3
‑
连接的葡萄糖。
143.在本发明的一个实施方案中,作为检测源自酵母的新型多糖(mgcp)的分子量的结果,鉴定出两个宽峰,并且检测到所述多糖的分子量为约4kda至60kda。作为从总多糖分出的三大级分的检测的结果,观察到所述多糖具有约3.5kda至60kda的分子量。此外,当所述多糖的分子量小、优选20kda或更小时,treg诱导活性优异,而当所述多糖的分子量大于100kda时,treg诱导活性变差。
144.因此,在本发明中,所述多糖可以具有3.5kda至60kda的分子量,并且可以优选具有4kda至20kda的分子量。
145.在本发明中,所述多糖可以诱导调节t细胞(treg)的产生,所述调节t细胞优选地为cd4 foxp3 调节t细胞,但不限于此。
146.如本文所用,术语“调节t细胞(treg)”是一种类型的分化t细胞,并且其功能是调节免疫功能,从而维持对自身抗原的耐受性并调节自身免疫疾病的发作。调节t细胞通常表达免疫抑制细胞因子如il
‑
10,并抑制效应t细胞的诱导和增殖。
147.如本文所用,术语“诱导”意指诱导所需细胞的分化或产生,并且在本发明中用于指示幼稚t细胞向调节t细胞的分化。
148.在本发明中,术语“诱导”可以与“分化”、“生成”、“产生”等互换使用。
149.如本文所用,术语“幼稚t细胞”是指在胸腺中的祖t细胞在骨髓中成熟化之前预分化的t细胞。在用il
‑
2、il
‑
4和tgf
‑
β刺激后,幼稚t细胞可以分化为效应t细胞、辅助t细胞(th)、调节t细胞(treg)等。
150.在本发明中,调节t细胞的诱导可以由树突细胞(dc)介导,并且dc可以表达模式识别受体(prr)。模式识别受体可以优选地包含选自dectin1、dectin2、tlr2、tlr4和tlr6的至少一种,但不限于此。
151.在本发明中,通过dc介导可以包括通过以下方式来介导treg细胞的诱导:基于通过用所述多糖处理进行刺激,将转录组景观(landscape)修饰为致耐受性dc。优选地,转录组景观的修饰可以是选自il
‑
10、cd274、吲哚胺2,3
‑
双加氧酶(ido)、tgfβ1和cox2(环氧合酶编码基因,ptgs2)的至少一种的过表达,但不限于此。
152.另外,在本发明中,所述多糖可以改善来自treg的helios、il
‑
10和ctla
‑
4的表达,并且可以降低效应t细胞的ifn
‑
γ。
153.在本发明的一个实施方案中,所述新型多糖源自酵母提取物,并从酵母的细胞壁特异性地分离。源自去除了β
‑
1,3
‑
葡聚糖的酵母细胞壁的包含甘露聚糖/β
‑
葡聚糖的多糖(mgcp)展现出增加的treg细胞诱导能力。
154.在本发明中,所述多糖可以源自酵母,可以优选地源自酵母细胞壁,并且可以更优选地源自已经去除了β
‑
1,3
‑
葡聚糖的酵母细胞壁。
155.在本发明中,所述多糖优选地具有调节抗炎功能或免疫功能的活性,更优选地具有免疫抑制活性,但不限于此。例如,当不恰当地施用益生菌时,具有肠道伤口(如肠出血)
的患者可能会遭受副作用。在这种情况下,可以通过施用多糖来获得治疗效果。
156.在另一方面,本发明涉及一种用于免疫调节的组合物,其包含所述多糖作为活性成分。
157.如本文所用,术语“免疫调节”意指解决血液中的免疫失衡并维持免疫稳态。免疫稳态的维持是指这样的状态,其中获得在调节免疫的免疫耐受与促进免疫的免疫应答之间的平衡。维持这种状态对于治疗免疫疾病、特别是治疗自身免疫疾病至关重要。
158.用于免疫调节的组合物可以用作调节免疫活性和预防、改善或治疗免疫疾病的药物组合物或保健功能食品,并且使用的量和形式可以根据目的适当调整。
159.在本发明的一个实施方案中,发现口服施用mgcp增加结肠treg细胞的诱导。另外,口服施用mgcp显著增加treg细胞中ctla
‑
4和il
‑
10的表达,并显著降低效应t细胞中的ifn
‑
γ表达。
160.在本发明的另一个实施方案中,在用mgcp喂养具有微生物鞭毛蛋白反应性cd4 t细胞的小鼠中,显著减少了体重减轻和结肠长度缩短,并且有效地抑制了上皮细胞的增殖和淋巴细胞向结肠的渗透。与施用模拟物的小鼠相比,组织病理学评分也显示出显著的缓解。
161.在另一方面,本发明涉及一种用于预防和治疗免疫疾病或炎性疾病的药物组合物,其包含所述多糖作为活性成分。
162.如本文所用,术语“免疫疾病”是指可能直接由免疫系统异常引起的疾病,并且可以选自皮炎、过敏、鼻炎、痛风、强直性脊柱炎、风湿热、狼疮、纤维肌痛、肌腱炎、1型糖尿病、硬皮病、神经退行性疾病、2型糖尿病、矽肺、动脉粥样硬化、白癜风、结膜炎和自身免疫疾病,但不限于此。
163.如本文所用,术语“自身免疫疾病”是指当生物体中的免疫细胞将生物体自身的组织或细胞而不是外部入侵抗原识别为抗原并对其进行攻击时发生的疾病。所述自身免疫疾病可以选自类风湿性关节炎、系统性硬皮病、特应性皮炎、银屑病、哮喘、格林
‑
巴利综合征、重症肌无力、皮肌炎、多发性肌炎、多发性硬化、自身免疫性脑脊髓炎、结节性多动脉炎、颞动脉炎、儿童糖尿病、斑秃、水泡、口疮性口炎、克罗恩病和白塞病,但不限于此。
164.如本文所用,术语“炎性疾病”是伴有炎症作为主要病变的疾病的通用术语,特别是选自以下的一种:水肿、过敏、哮喘、结膜炎、牙周炎、鼻炎、中耳炎、咽喉痛、扁桃体炎、肺炎、胃溃疡、胃炎、克罗恩病、结肠炎、痔疮、痛风、强直性脊柱炎、风湿热、狼疮、纤维肌痛、银屑病关节炎、骨关节炎、类风湿性关节炎、肩周炎、肌腱炎、腱鞘炎、肌炎、肝炎、膀胱炎、肾炎、舍格伦综合征、严重的重症肌无力和多发性硬化,但不限于此。
165.如本文所用,术语“预防”或“预防的”是指可以通过施用根据本发明的药物组合物调节或延迟免疫疾病或炎性疾病发作的任何作用。
166.如本文所用,术语“治疗”或“治疗的”是指可以通过施用根据本发明的药物组合物改善或有益地改变免疫疾病或炎性疾病的症状的任何作用。
167.本发明的药物组合物展现出对各种免疫疾病的预防或治疗作用以及基于活性成分的免疫增强作用或超免疫调节作用的抗炎作用。
168.除了所述多糖之外,所述药物组合物还可以包含常用于药物组合物中的合适的载体、赋形剂和稀释剂。
169.可以包含在所述药物组合物中的载体、赋形剂和稀释剂的例子可以包括乳糖、右旋糖、蔗糖、山梨醇、甘露醇、木糖醇、赤藓糖醇、麦芽糖醇、淀粉、阿拉伯树胶橡胶、藻酸盐、明胶、磷酸钙、硅酸钙、纤维素、甲基纤维素、微晶纤维素、聚乙烯吡咯烷酮、水、羟基苯甲酸甲酯、羟基苯甲酸丙酯、滑石、硬脂酸镁、矿物油等。在配制所述组合物时,可以使用通常使用的稀释剂或赋形剂,如填充剂、增量剂、粘合剂、润湿剂、崩解剂或清洁剂。
170.可以根据常规方法以各种形式配制和使用根据本发明的药物组合物。合适的配制品包括口服配制品(如片剂、丸剂、粉末、颗粒、糖衣片剂、硬胶囊或软胶囊、溶液、悬浮液、乳液、注射剂和气溶胶)、外用制剂、栓剂、无菌注射溶液等,但不限于此。
171.可以使用药学上无活性的有机或无机载体将根据本发明的药物组合物制备成合适的配制品。也就是说,当所述配制品是片剂、包衣片剂、糖衣片剂或硬胶囊时,其可以包含乳糖、蔗糖、淀粉或其衍生物、滑石、碳酸钙、明胶、硬脂酸或其盐。另外,当所述配制品是软胶囊时,其可以包含植物油、蜡、脂肪或半固体或液体多元醇。另外,当所述配制品呈溶液或糖浆形式时,其可以包含水、多元醇、甘油、植物油等。
172.除了上述载体之外,根据本发明的药物组合物还可以包含防腐剂、稳定剂、润湿剂、乳化剂、增溶剂、调味剂、着色剂、渗透压调节剂、抗氧化剂等。
173.可以将根据本发明的药物组合物以药学有效量施用,并且术语“药学有效量”是指对于以适用于所有医学治疗的合理的益处/风险比治疗疾病的足够的量,并且有效剂量水平可以根据多种因素来确定,包括患者的疾病类型、疾病的严重程度、药物的活性、患者对药物的敏感性、施用时间、施用途径、排出率、治疗期、与其同时使用的药物以及药物领域熟知的其他因素。可以将本发明的药物组合物作为单一治疗剂或与其他治疗剂组合施用,可以与常规治疗剂依序或同时施用,并且可以以一个或多个剂量施用。考虑到这些因素,重要的是施用足以在没有副作用的情况下实现最大功效的最小量,并且所述量可以由本领域技术人员容易地确定。
174.可以将本发明的组合物与免疫相关蛋白、特别是自身免疫或过敏相关的蛋白组合施用。特别地,此类蛋白质的例子包括涉及自身免疫疾病的自身抗原,例如用于类风湿关节炎的热休克蛋白(hsp)、瓜氨酸化聚丝蛋白、葡萄糖
‑6‑
磷酸异构酶、p205、胶原蛋白等,作为与重症肌无力有关的自身抗原的胰岛素、锌转运体8蛋白(znt8)、胰腺和十二指肠同源盒1(pdx1)、嗜铬粒蛋白a(chga)、胰岛淀粉样多肽(iapp)和乙酰胆碱受体。另外,此类蛋白质不仅包括已知引起自身免疫疾病的所有种类的自身抗原,还包括已知引起食物过敏的各种过敏原,如花生、牛奶、鸡蛋、树坚果、大豆、甲壳纲动物(如虾)、源自鱼的物质等。
175.可以通过各种途径将根据本发明的药物组合物施用于受试者。施用方式可以是例如,皮下、静脉内、肌内、子宫硬膜内(intrauterine dural)或脑血管注射。本发明的药物组合物是根据以下来确定的:作为有效成分的药物的类型,以及诸如待治疗疾病的类型、施用途径、患者的年龄、性别和体重以及疾病的严重程度的各种相关因素。
176.可以根据配制品容易地选择根据本发明的药物组合物的施用方法,并且可以口服或肠胃外施用所述药物组合物。剂量可能根据患者的年龄、性别和体重、疾病的严重程度和施用途径而变化。
177.在另一方面,本发明涉及一种预防或治疗免疫疾病或炎性疾病的方法,其包括向受试者施用本发明的多糖或包含所述多糖作为活性成分的组合物。
178.在另一方面,本发明涉及本发明的多糖或包含所述多糖的组合物用于预防或治疗免疫疾病或炎性疾病的用途。
179.在另一方面,本发明涉及本发明的多糖用于制备预防或治疗免疫疾病或炎性疾病的药物的用途。
180.根据本发明的药物组合物不仅提供对免疫增强和超免疫作用的优异调节作用,而且几乎没有毒性和副作用,如通常由药物引起的毒性和副作用,因此可以长时间施用以用于治疗或预防免疫疾病的目的。
181.在另一方面,本发明涉及一种用于预防或改善免疫疾病或炎性疾病的食品,其包含作为活性成分的多糖。
182.用于预防或改善免疫疾病或炎性疾病的食品可以是具有通过增强免疫活性或者调节或缓解超免疫来维持免疫功能的稳态的活性的保健功能食品。
183.术语“食品”包括肉、香肠、面包、巧克力、糖果、零食、蜜饯、披萨、其他类型的面条、口香糖、乳制品、包括冰淇淋、各种汤、饮料、茶、饮品、酒精饮料、维生素复合物、保健功能食品和保健食品等,并且涵盖任何普通食品。
184.术语“功能食品”具有与术语“用于特殊保健用途的食品(foshu)”相同的含义,并且是指具有强大的医疗和药物作用的食品,其已经被加工以有效地提供生物调节功能以及营养供应功能。此处,术语“功能”意指获得用于保健目的的有益作用,如控制营养素或展现出关于人体的结构和功能的生理作用。本发明的食品可以通过本领域常用的方法来制备,并且可以使用本领域通常添加的原料和成分进行制备。另外,所述食品也可以制备成任何被认为是食品的配制品而不加以限制,并且根据本发明的保健功能食品可以呈粉末、颗粒、片剂、胶囊或饮料的形式。
185.术语“保健食品”是指除了一般食品之外具有积极的健康维持或促进作用的食品,并且“保健补充食品”是指为了改善健康的目的而摄入的食品。在一些情况下,术语“保健功能食品”、“保健食品”和“保健补充食品”可互换使用。
186.所述食品组合物还可以包含生理上可接受的载体,并且对载体的种类没有特别的限制,并且可以使用本领域中常用的任何载体。
187.另外,所述组合物可以包含通常用于食品组合物中以改善气味、味道、视觉效果(外观)等的另外的成分。例如,所述组合物可以包含维生素a、c、d、e、b1、b2、b6和b12,烟酸,生物素,叶酸,泛酸等。另外,可以包含矿物质,如锌(zn)、铁(fe)、钙(ca)、铬(cr)、镁(mg)、锰(mn)、铜(cu)和铬(cr)。另外,可以包含氨基酸,如赖氨酸、色氨酸、半胱氨酸和缬氨酸。
188.另外,所述组合物可以包含食品添加剂,如防腐剂(山梨酸钾、苯甲酸钠、水杨酸、脱氢乙酸钠等)、消毒剂(漂白粉和高度漂白粉、次氯酸钠等)、抗氧化剂(丁基羟基茴香醚(bha)、丁基羟基甲苯(bht)等)、着色剂(焦油色剂等)、显色剂(亚硝酸钠、亚硝酸钠等)、漂白剂(亚硫酸钠)、调味料(msg等)、甜味剂(甘素、甜蜜素、糖精、钠等)、调味剂(香草醛、内酯等)、膨胀剂(明矾、d
‑
酒石酸氢钾等)、增强剂、乳化剂、增稠剂、包衣剂、胶基剂、发泡剂、溶剂和改良剂。所述添加剂可以根据食品的类型来选择并以适当的量使用。
189.除了本发明的多糖以外,所述组合物还可以包含食品上可接受的食品补充添加剂,可以与其他食品或食品成分组合使用,并且可以根据常规方法适当地使用。可以根据使用目的(预防、保健或治疗性治疗)适当地确定混合的活性成分的量。
190.在本发明的一个实施方案中,发现mgcp诱导结肠treg细胞,增加treg细胞中il
‑
10和ctla
‑
4的表达,并且在体内和体外均抑制效应t细胞中ifn
‑
γ的表达,从而抑制免疫功能。
191.在本发明的另一个实施方案中,发现所述多糖介导dc以诱导treg细胞。特别地,发现当dc的dectin1、dectin2、tlr2、tlr4和tlr6缺乏时,treg的细胞分化减少,并且降低是显著的,特别是当dectin1和tlr4缺乏时。还发现即使当myd88信号传导系统缺乏时,treg细胞的诱导也会减少。
192.在本发明的另一个实施方案中,通过prr识别多糖将dc的转录组景观(如il
‑
10、cd274、吲哚胺2,3
‑
双加氧酶(ido)、tgfβ1和cox2)改变为致耐受性dc表型。特别地,作为用塞来昔布治疗后的实验的结果,发现cox2过表达,从而诱导treg细胞。除树突细胞以外,treg细胞还可以被任何识别并呈递抗原的细胞诱导。
193.在另一方面,本发明涉及一种产生调节t细胞(treg细胞)的方法,所述方法包括用根据本发明的多糖处理抗原呈递细胞,然后获得致耐受性抗原呈递细胞;以及将所述致耐受性抗原呈递细胞与cd4 t细胞共孵育,然后诱导调节t细胞(treg细胞)。
194.如本文所用,术语“抗原呈递细胞”是指通过以下方式诱导分化的细胞:接受和响应于抗原,然后将抗原衍生片段与抗原呈递分子(如mhc ii类分子)一起呈递至t细胞。例如,所述抗原呈递细胞包括巨噬细胞、b细胞、树突细胞(dc)和朗格汉斯细胞,但不限于此。
195.如本文所用,术语“致耐受性抗原呈递细胞”是指具有使免疫系统对各种抗原产生耐受性的免疫抑制特性的一种类型的抗原呈递细胞。致耐受性抗原呈递细胞主要通过t细胞调节(如诱导t细胞的无反应性和死亡以及诱导treg细胞)影响免疫环境。由于这些免疫抑制特性,因此致耐受性抗原呈递细胞作为应对过敏相关疾病和自身免疫疾病的细胞疗法的候选物质而受到关注。所述致耐受性抗原呈递细胞可以是例如致耐受性巨噬细胞、致耐受性树突细胞(dc)或致耐受性b细胞,但不限于此。
196.在本发明中,所述抗原呈递细胞可以表达模式识别受体(prr)。所述模式识别受体优选地包含选自dectin1、dectin2、tlr2、tlr4和tlr6的一种或多种,但不限于此。
197.在本发明中,所述致耐受性抗原呈递细胞过表达选自il
‑
10、cd274、吲哚胺2,3
‑
双加氧酶(ido)、tgfβ1和cox2的一种或多种,但不限于此。
198.在本发明中,所述调节t细胞优选地是cd4 foxp3 调节t细胞,但不限于此。
199.另外,在本发明中,所述多糖可以增加来自treg细胞的helios、il
‑
10和ctla
‑
4的表达,并且可以降低效应t细胞中的ifn
‑
γ。
200.在本发明的一个实施方案中,为了确定mgcp诱导的treg细胞在体内是否具有功能活性以及是否可以缓解结肠炎,将由mgcp处理的dc产生的treg细胞(cd45 )与幼稚cd4 t细胞一起过继递送至小鼠。在接受mgcp
‑
treg的小鼠中,显著降低了接受者小鼠中的体重减轻和结肠长度缩短,预防了结肠组织中上皮细胞结构的破坏,并且抑制了淋巴细胞向结肠粘膜的渗透,如可从组织病理学得分观察到的。另外,显著降低了供体幼稚cd4 t细胞中产生的ifn
‑
γ水平。
201.在另一方面,本发明涉及一种用于预防或治疗免疫疾病或炎性疾病的细胞治疗剂,其包含通过所述方法产生的调节t细胞(treg细胞)作为活性成分。
202.在另一方面,本发明涉及所述细胞治疗剂用于预防或治疗免疫疾病或炎性疾病的
用途。
203.在本发明中,所述调节t细胞优选地是cd4 foxp3 调节t细胞,但不限于此。
204.在另一方面,本发明涉及所述多糖或所述细胞治疗剂用于制备预防或治疗免疫疾病或炎性疾病的药物的用途。
205.在下文中,将参考实施例更加详细地描述本发明。然而,对本领域技术人员明显的是,提供这些实施例仅用于举例说明本发明,而不应解释为限制本发明的范围。
206.材料和方法
207.1.小鼠
208.小鼠在postech生物技术中心的动物设施中繁殖。所有实验程序均在经postech实验室的机构动物护理与使用委员会(institutional animal care&use committee of postech laboratories)批准的情况下进行。c57bl/6小鼠在postech连续近交。foxp3
‑
egfp、tlr2
‑
/
‑
、tlr4
‑
/
‑
、tlr6
‑
/
‑
和myd88
‑
/
‑
小鼠是从jackson实验室获得的。cd45a
‑
rag1
‑
/
‑
tcr ot
‑
ii(rag1
‑
/
‑
otii tcr转化体)和rag1
‑
/
‑
小鼠是从taconic biosciences,inc获得的。dectin1
‑
/
‑
和dectin2
‑
/
‑
动物是由yoichiro iwakura博士(日本东京理科大学)提供的。无菌(gf)c57bl/6小鼠集落是由育种者在andrew macpherson博士(瑞士伯尔尼大学)和david artis博士(当时在美国宾夕法尼亚大学,现今在美国康奈尔大学)的帮助下建立的。将gf小鼠保存在无菌柔性薄膜隔离器(classbiological clean ltd.,美国)中。cbir小鼠是由伯明翰阿拉巴马大学的charles o.elson提供的。使用合适的性别和年龄的6至12周龄小鼠。
209.2.从酵母细胞壁纯化mgcp
210.将20g酵母提取物(bd biosciences)、2g聚山梨酯80(sigma
‑
aldrich)、4g柠檬酸铵(sigma
‑
aldrich)、10g乙酸钠(sigma
‑
aldrich)、硫酸镁(sigma
‑
aldrich)、0.1g硫酸锰(sigma
‑
aldrich)和4g磷酸氢二钾(sigma
‑
aldrich)溶解在2l蒸馏水中。将溶液高压灭菌,然后冷却至室温。将溶液用三氯乙酸(tca,sigma aldrich)处理至终浓度为0.4%,并用磁力搅拌在4℃下孵育过夜。将经tca处理的溶液与3滴冷却的乙醇一起在
‑
20℃下孵育过夜。将培养的溶液离心,去除上清液,然后将沉淀物干燥以去除剩余的乙醇,并悬浮于含有20mm mgcl2和20mm cacl2的10mm tris缓冲液(ph 7.5)中。将悬浮溶液用rna酶(sigma
‑
aldrich)和dna酶(roche)处理至终浓度为0.4mg/ml,并在37℃下孵育过夜。然后,将溶液用叠氮化钠处理至终浓度为0.05%,并在37℃下孵育30分钟。在孵育之后,将所得物用0.3mg/ml的链霉蛋白酶(蛋白酶,灰色链霉菌,sigma
‑
aldrich)溶液处理,并在37℃下孵育过夜。再次向溶液中添加链霉蛋白酶以获得0.3mg/ml的终浓度,接着进一步孵育2小时。添加tca以获得0.4%的终浓度,接着在37℃下孵育2小时。将溶液离心并将上清液转移至3滴冷却的乙醇中,并在
‑
20℃下孵育过夜。在离心之后,去除上清液并将沉淀物干燥以去除残留的乙醇。将沉淀物悬浮于100mm tris缓冲液(ph 7.5)中,用相同量的苯酚处理,并倒转若干次以将其充分混合。将溶液离心,并将上管转移至新管中,并用苯酚反复处理。将溶液离心,并将上清液转移至新管中,并用相同量的异戊醇:氯仿1:29(v:v)溶液处理,接着充分混合。在离心之后,转移上清液,并再次重复此过程。通过在蒸馏水中透析3天,接着冷冻干燥,从而获得多糖。通过酸性苯酚分析测量多糖的浓度。
211.3.淋巴细胞分离和流式细胞术分析
212.根据制造商的方案,使用fac分选仪(astrios,beckman coulter)或easysep
tm
小鼠cd4 t细胞分离试剂盒(stemcell technology)从pln、mln和脾脏获得幼稚cd4 t细胞。在从大肠和小肠分离的过程中,将肠竖直切开,打开并用pbs洗涤以去除粘液和粪便。从肠上切下一小段,然后使用含有10mm edta、20mm hepes、1mm丙酮酸钠和3%fbs的pbs在用磁棒搅拌的同时在37℃下孵育20分钟。将组织捣碎并在补充有3%fbs、20mm hepes、1mm丙酮酸钠、0.5mg/ml胶原酶d(roche)和dna酶i(sigma
‑
aldrich)的rpmi 1640培养基中在37℃下孵育45分钟。将组织在存在10mm edta的情况下进一步孵育5分钟。将上清液通过100mm细胞过滤器过滤并转移至冷却的pbs以去除剩余的酶和edta。将细胞以40%和75%加载在percoll
tm
(ge healthcare)梯度上。从percoll梯度膜的表面收获淋巴细胞,并将其用补充有1%fbs和1%青霉素/链霉素的dmem培养基洗涤。为了分析细胞因子,将细胞在含有10%fbs、1%青霉素/链霉素、2mm l
‑
谷氨酰胺、1mm丙酮酸钠、非必需氨基酸和0.1%β
‑
me(v/v)的完全rpmi培养基中在存在golgistop(bd biosciences)的情况下用pma(calbiochem)和离子霉素(calbiochem)在37℃下刺激4至5小时。根据制造商的流式细胞术分析方案对细胞进行染色。
213.使用以下试剂对细胞进行染色:
214.活/死可固定染料(life technologies)、固定/渗透缓冲液(ebioscience)、渗透缓冲液(ebioscience)、ic固定缓冲液(ebioscience)和抗体。
215.本实验中使用了以下抗体克隆:
216.cd4(rm4
‑
5)、cd44(im7)、cd62l(mel
‑
14)、cd45.1(a20)、cd103(2e7)、foxp3(fjk
‑
16s)、ctla4(uc10
‑
4b9)、nrp1(3e12)、il
‑
10(jes5
‑
16e3)、ifn
‑
γ(xmg1.2)、il
‑
17a(17b7)、cd11c(n418)、cd11b(m1/70)、f4/80(bm8)、mhcii(m5/114.15.2)。
217.4.抗原呈递细胞依赖性t细胞的体外分化
218.将2x 104个源自指示组织的cd11c dc用指示多糖或mgcp处理,并在存在10ng/ml gm
‑
csf(peprotech)的情况下在rpmi 1640完全培养基中孵育14小时。在通过用mgcp处理刺激dc的情况下,在大多数体外实验中用50μg/ml的mgcp刺激dc,除非mgcp浓度另有指示。将刺激的dc洗涤并与2
×
105个幼稚cd4 t细胞共孵育3天。大多数实验是在次最佳treg细胞偏移条件下进行的,所述偏移条件包括0.1μg/ml抗cd3(bioxcell)、100u/ml il
‑
2、0.1或0.05ng/ml的tgf
‑
β1(miltenyi biotech)和10ng/ml gm
‑
csf。对于次最佳th1操作环境,将细胞在存在0.1μg/ml抗cd3、100u/ml il
‑
2、2.5ng/ml il
‑
12、10ng/ml gm
‑
csf和10μg/ml抗il
‑
4的情况下孵育。在孵育3天之后,通过上述流式细胞术分析细胞。在一些实验中,在用mgcp刺激之前,用拮抗剂处理脾脏dc。在使用多糖裂解酶的实验程序的情况下,在处理脾脏dc之前,将酵母聚糖或mgcp根据制造商的方案用相同的酶进行消化,并与幼稚cd4 t细胞一起孵育。在使用塞来昔布的实验中,用抑制剂的处理进行30分钟,之后用mgcp刺激脾脏dc,接着在存在塞来昔布的情况下与幼稚cd4t细胞组合孵育。
219.实验中使用了以下试剂:
220.α
‑
(1
‑
6)核心甘露糖苷酶(qabio)、石耳多糖酶(prokazyme)、酵母裂解酶(mp biomedicals)、mincle单克隆抗体(抗mincle mab,mbl)、dc
‑
sign抗体(抗dc
‑
sign ab,abcam)、重组小鼠mmr蛋白(r&d systems)。
221.5.通过cd4 t细胞递送诱导实验性结肠炎
222.根据先前描述的方法诱导实验性结肠炎(powrie f.,leach m.w.,mauze s.,等人immunity 1994;1(7):553
‑
62.和leach m.w.,bean a.g.,mauze s.,等人am.j.pathol.1996;148(5):1503
‑
15.)。特别地,将从同类系(cd45.1 )foxp3
‑
egfp小鼠或cbir小鼠分选的cd4 foxp3
gfp
‑
cd44
lo
cd62l
hi
幼稚t细胞(1x106)fac递送至rag1缺乏型小鼠。为了评价产生的mgcp在体外诱导的treg细胞的功效,将幼稚cd4 t细胞与标记的treg细胞(2
×
105)同时过继转移。为了用来自cbir小鼠的幼稚cd4 t细胞诱导结肠炎,在整个实验时期每隔一天向接受者口服施用模拟物或mgcp。通过每周两次测量体重来监测结肠炎的进展,并且在其体重减少至约20%后处死小鼠。通过测量结肠的长度、组织学评价以及从供体幼稚cd4 t细胞产生的细胞因子来分析疾病严重程度。
223.6.体内过继递送
224.在递送幼稚cd4 t细胞之前,每天向c57bl/6或dectin1
‑
/
‑
小鼠口服施用200μg的mgcp,持续2周。将从具有同类系等位基因的foxp3
‑
egfp或ot
‑
ii小鼠分离的cd4 foxp3
egfp
‑
cd44
lo
cd62l
hi
幼稚t细胞(纯化>99%,1.5
‑
2x106)通过静脉内施用转移至施用了mgcp的缺乏型小鼠,并且每天向其另外施用mgcp,持续一周。从细胞递送前一天到实验结束,每隔一天向接受ot
‑
ii幼稚cd4 t细胞的小鼠补充20mg的ova蛋白,持续1周。
225.7.rna测序
226.每天向gf小鼠施用模拟物和mgcp,持续2周。根据制造商的方案,使用微珠从结肠固有层的全细胞分离源自补充了模拟物和mgcp的gf小鼠的结肠cd11c dc。从喂养了模拟物或mgcp的小鼠的结肠dc纯化总rna。使用ribospin tmii(geneall biotechnology)分离总rna。使用truseq链mrna样品制备试剂盒(illumina,加利福尼亚州圣地亚哥)进行文库制备。使用nextseq 500测序平台进行rna测序。rna序列数据存放在基因表达综合(gene expression omnibus,ncbi)数据库(注册号geo:rna
‑
seq数据:gse126937)中。
227.8.定量逆转录聚合酶pcr(qrtpcr)
228.从源自补充了模拟物和mgcp的gf小鼠的结肠cd11c dc纯化完整转录物。收集细胞,然后将其在trizol试剂中裂解。根据制造商的方案纯化总rna。使用m
‑
mlv逆转录酶(promega)将纯化的总rna合成为cdna。使用下表中所示的引物对和通过上述方法制备的cdna分析指示的标记的表达水平。将所有数据针对次黄嘌呤
‑
鸟嘌呤磷酸核糖转移酶(hprt)的表达水平进行归一化。将结果进一步分析为相对于模拟物组和对照组的表达水平的表达水平。
229.[表1]引物核苷酸序列
[0230][0231][0232]
9.组织学分析
[0233]
由组织学分析通过h&e染色测量实验性结肠炎的临床得分。简而言之,将1cm的结肠固定在10%甲醛中并包埋在石蜡段中。将石蜡段切成3μm的厚度,并用苏木精(sigma
‑
aldrich)和曙红(sigma
‑
aldrich)染色。
[0234]
10.统计分析
[0235]
使用graphpad prism软件(美国拉荷亚)进行统计分析。采用双尾、未配对的student's t检验评价对照组与实验组之间的差异。数据表示为平均值
±
sem。
[0236]
实施例1:酵母聚糖诱导treg细胞的能力的确认
[0237]
为了研究酵母多糖在免疫系统中的免疫调节功能,将酵母多糖用dc处理,然后与幼稚cd4 t细胞一起孵育。酵母聚糖处理的dc以浓度依赖性方式促进treg细胞的诱导,并且酵母聚糖在500μg/ml下展现出最高的诱导性能(图1a)。接下来,确定酵母聚糖是否以类似的浓度依赖性方式诱导效应t细胞。酵母聚糖在最低浓度下诱导rorγt的表达,但不影响t
‑
bet的表达(图2a)。令人惊讶的是,对t
‑
bet和rorγt在效应t细胞中的表达的抑制与酵母聚糖的浓度成比例(图2a)。
[0238]
另外,为了清楚地鉴定参与诱导treg细胞的源自酵母聚糖的多糖,使用切割酶切割具有不同结构的多糖。酵母聚糖中β
‑
1,3
‑
葡聚糖的去除显著增加了treg细胞的诱导(图1b)。同时,酵母聚糖的β
‑
1,6
‑
葡聚糖和甘露聚糖的切割抑制treg细胞的诱导,从而展现出相反的作用(图1c)。与未处理的对照组相比,β
‑
1,3
‑
葡聚糖和β
‑
1,6
‑
葡聚糖的切割导致rorγt的表达增加,这与酵母聚糖介导的rorγt抑制的补偿无关(图2b和图2c)。以上结果表明了酵母聚糖的特定多糖结构的免疫作用。上述结果显示,β
‑
1,6
‑
葡聚糖和甘露聚糖对treg细胞的产生是必要的,而β
‑
1,3
‑
葡聚糖诱导th1免疫应答并抑制treg细胞的产生。
[0239]
实施例2:mgcp的纯化及其结构和功能表征
[0240]
以与上述材料和方法中所述相同的方式从酵母细胞壁纯化多糖,并确认了其结构特性与免疫功能相关性。组成分析的结果显示,酵母衍生多糖由甘露糖(80.6%)、葡萄糖(14.9%)和半乳糖(4.5%)组成(图3a和图4)。通过质子核磁共振(nmr)光谱学对所述多糖结构和形态的进一步分析支持了以下概念:所述多糖含有甘露聚糖和β
‑
1,6
‑
葡聚糖作为主要成分(图5a)。发现甘露聚糖单元的详细结构具有α
‑
1,6
‑
连接的甘露糖骨架和用α
‑
1,2
‑
连接或α
‑
1,3
‑
连接接合的作为侧链的单个单元甘露糖(30%)、二单元甘露糖(16.8%)或三单元甘露糖(28.4%)(无侧链的甘露糖(24.8%))(图5b)。所述甘露聚糖组分的结构与酿酒酵母(s.cerevisiae)细胞壁中发现的典型甘露聚糖结构类似。β
‑
1,6
‑
葡聚糖含有β
‑
1,6
‑
连接的葡萄糖骨架作为主要成分,并且18%的骨架葡萄糖具有β
‑
1,3
‑
连接的单个单元葡萄糖作为侧链(图5c)。具有这种结构的酵母衍生多糖是新型的,并且纯化的多糖被命名为“含有甘露聚糖/β
‑
葡聚糖的多糖(mgcp)”。
[0241]
为了检测mgcp的分子量,使用hplc通过本领域已知的方法对其进行分析。使用tsk g
‑
g5000pwxl尺寸排除柱,并且50mm碳酸氢铵作为洗脱液以0.8ml/min的流速进行冲洗。使用差示折射率检测器和uv检测器在206nm的波长下检测分析结果。用于确定分子量的参考材料是右旋糖酐标准品,并且其信息示于下表2中。
[0242]
[表2]
[0243][0244]
作为hplc的结果,鉴定出两个宽峰,并且发现mgcp的分子量为4kda至60kda(图6和以下表3)。基于整个mgcp的hplc分析的结果(如图6所示),将总mgcp分馏成三种级分a、b和c,并通过hplc确定每种级分的分子量(图7和以下表3)。
[0245]
[表3]
[0246][0247]
分析了mgcp的免疫功能关系,并特别确定了其诱导treg细胞的能力。用mgcp处理的脾脏dc以剂量依赖性方式诱导了treg细胞(图5d)。为了分析mgcp的每种结构的treg细胞诱导相关性,首先独立地处理常用的甘露聚糖、β
‑
1,6
‑
葡聚糖(石耳多糖)或β
‑
1,3
‑
葡聚糖(凝胶多糖)。作为结果,没有发现它们其中任何一个能够独立地诱导treg细胞(图3b和图3c)。同时,如先前所报道,发现d
‑
( )甘露糖可以诱导treg细胞(图3d)。为了确定与诱导treg细胞分化有关的gmcp必需位点,对甘露聚糖、β
‑
1,6
‑
葡聚糖和β
‑
1,3
‑
葡聚糖的每种结构进行了实验,用切割它们的酶进行切割。mgcp中β
‑
1,6
‑
葡聚糖的切割显著降低了treg细胞的产生,并且甘露聚糖的切割展现出降低的treg细胞分化,但这不是显著的值(图5e)。另外,关于treg细胞的诱导,两种多糖的同时去除显示出与单独切割β
‑
1,6
‑
葡聚糖的情况类似的结果,这意味着treg细胞的诱导主要依赖于β
‑
1,6
‑
葡聚糖(图5e)。有趣的是,从去除了β
‑
1,3
‑
葡聚糖的酵母细胞壁纯化的多糖比从完整酵母细胞壁纯化的mgcp诱导更多的treg细胞产生(图3e)。这些结果表明,mgcp的所有组分都是诱导treg细胞的必要因素。包含作为侧链的β
‑
1,3
‑
连接的单个葡萄糖的β
‑
1,6
‑
葡聚糖部分对于mgcp诱导treg细胞的能力是必需的,而β
‑
1,3
‑
葡聚糖部分调节treg细胞的诱导。
[0248]
尽管未示出,但发现当多糖的分子量增加时,特别是当分子量为100kda或更大时,treg细胞的诱导活性减小。
[0249]
实施例3:体内mgcp诱导的treg细胞的炎性结肠炎缓解功效的确认
[0250]
如上所述,发现mgcp促进treg细胞的分化。在此,确定了体外分化的treg细胞在患有结肠炎的小鼠体内是否展现出缓解作用。通过用mgcp处理dc在体外产生具有同类系标记(cd45.1 )的treg细胞,并将其与幼稚cd4t细胞在相同的时间过继转移至接受者小鼠,并确定了由mgcp诱导的treg细胞的免疫调节功能。结果显示,由mgcp诱导的treg细胞妨碍了结肠炎的进展。特别地,在接受了mgcp
‑
treg细胞的小鼠中,显著降低了体重减轻和结肠长度缩短(图8a和图6b)。关于结肠炎的临床症状,由mgcp诱导的treg细胞的转移预防结肠组织的上皮细胞结构的破坏,并抑制淋巴细胞向结肠固有层的渗透,其由组织病理学得分指示(图8c和图6d)。由于已知ifn
‑
γ在结肠炎的发病机制中起重要作用,因此评价了结肠固有
层中cd4 t细胞产生的作为致病性细胞因子的ifn
‑
γ。与仅接受了幼稚cd4 t细胞的受试者相比,在接受了mgcp
‑
treg细胞的受试者中供体幼稚cd4 t细胞的ifn
‑
γ产生水平显著降低(图8e)。上述结果显示,mgcp诱导的treg细胞抑制炎性细胞因子的产生并改善炎性结肠炎。
[0251]
实施例4:通过口服施用mgcp诱导结肠treg细胞的产生
[0252]
在体外,mgcp促进了在体内具有功能活性的treg细胞的诱导。为了确定mgcp是否可以在体内产生treg细胞,向小鼠口服施用mgcp,接着转移结肠幼稚cd4 t细胞(cd45.1 )。有趣的是,与对照组相比,mgcp的施用从结肠中的供体cd4 t细胞产生了显著更高频率的treg细胞(图9a)。treg细胞表达ctla
‑
4,其是treg细胞的抑制活性的重要指示物(图9b)。另外,在小肠中,在供体细胞之中观察到treg细胞频率的类似增加,并且它们也表达ctla
‑
4(图10a和图8b)。同时,接受者衍生treg细胞的频率和宿主treg细胞中的ctla
‑
4表达水平与结肠和小肠中的对照组的那些是类似的(图9c、图7d、图8c和图8d)。用mgcp处理的小鼠中结肠treg细胞的绝对数量在结肠中增加,但这种增加不是显著的值(图9e和图8e)。观察到在施用了mgcp的小鼠的整个肠道中的受体treg细胞之中,表达helios的细胞数量增加(图9f和图8f)。在功能上,mgcp的施用仅显著增加了结肠固有层中treg细胞的il
‑
10产生,但没有增加小肠中treg细胞的产生(图9g和图8g)。在mgcp处理后,通过结肠固有层中的效应t细胞产生的ifn
‑
γ降低,但il
‑
17a的水平没有改变(图9h)。与此相对照,在模拟物和mgcp处理的小鼠中,小肠的cd4t细胞中ifn
‑
γ和il
‑
17a的表达是类似的(图10h)。mgcp的施用诱导来自肠中的供体cd4 t细胞的treg细胞分化,但用mgcp处理不能诱导来自脾脏或mln中的宿主或供体衍生cd4 t细胞的treg细胞分化(图10i和图8j)。总体而言,在体内,mgcp不仅降低了作为结肠效应cd4 t细胞中的炎性细胞因子的ifn
‑
γ,而且促进了新的功能性结肠treg细胞的产生,且增强了il
‑
10产生。上述结果意味着在稳态的条件下mgcp可以影响结肠免疫调节环境。
[0253]
实施例5:由mgcp诱导的微生物群特异性treg细胞的结肠炎的改善
[0254]
为了确定mgcp是否在体内诱导微生物抗原特异性treg细胞并调节炎性免疫应答,使用携带微生物鞭毛蛋白反应性cd4 t细胞的cbir小鼠。将来自cbir小鼠的幼稚cd4 t细胞转移至rag1
‑
/
‑
小鼠,并每天口服模拟物(dw)或mgcp。已经报道,由于对共生微生物群的过度免疫应答,因此将微生物反应性幼稚cd4 t细胞过继转移至免疫力减弱的小鼠可诱导实验性结肠炎(图11a)。然而,补充mgcp显示出对体重减轻的显著抵抗(图11a)。除了对体重变化的影响以外,还通过施用mgcp来预防结肠长度的缩短(图11b和图9c)。与临床体征一致,施用了mgcp的小鼠抑制上皮细胞的增殖和淋巴细胞向结肠的渗透(图11d)。另外,与模拟物处理的小鼠相比,显示出组织病理学得分降低(图11e)。这些结果表明,mgcp可以通过促进新的功能性treg细胞的产生来抑制前炎性环境中致病性细胞因子的产生(图8和图9)。
[0255]
因此,确定用mgcp处理是否可以抑制接受者小鼠的共生抗原特异性cd4 t细胞产生有害的细胞因子,同时促进treg细胞的产生。与模拟物处理的小鼠相比,施用了mgcp的小鼠增加来自幼稚cd4 t细胞的微生物反应性treg细胞的分化(图11f),并且作为对于treg细胞的稳定性和功能而言重要的分子的cd103和ctla
‑
4的表达在mgcp处理和模拟物处理的小鼠的treg细胞中是类似的(图12a)。与结肠炎的临床体征一致,与模拟物处理的小鼠相比,在施用了mgcp的小鼠中大量调节了来自供体cd4 t细胞的ifn
‑
γ的产生(图11g),但发现在结肠固有层中的il
‑
17a水平是类似的(图12b)。总体而言,上述结果表明mgcp诱导treg细胞
的转移,并且mgcp的施用促进响应于共生抗原而产生treg细胞,并抑制炎性结肠炎的发展和ifn
‑
γ的产生。
[0256]
实施例6:cox2对于通过肠cd103
cd11b
dc诱导由mgcp介导的treg细胞的必要性
[0257]
为了建立mgcp使用抗原呈递细胞诱导treg细胞的机制,评价了dc子集和巨噬细胞通过mgcp刺激诱导treg细胞分化的能力。根据肠中cd11b和cd103的表达来划分dc。用mgcp刺激每个肠的dc子集和巨噬细胞,然后将其与幼稚cd4 t细胞一起孵育。与模拟物处理的情况相比,用mgcp处理的肠cd103
cd11b
dc诱导treg细胞的产生的约10倍增加(图13a)。cd103
cd11b
‑
dc和巨噬细胞在mgcp刺激之后没有增加treg细胞的水平,但是即使在没有用mgcp处理时也有效地诱导了treg细胞(图13a和图14)。为了建立mgcp刺激dc以允许dc诱导treg细胞以及通过微生物刺激剂抑制dc激活功能的机制,每天向无菌小鼠(gf)口服dw(模拟物)或mgcp,持续2周。为了分析转录组构型,从模拟物或mgcp处理的小鼠的结肠分离cd11c
dc。mgcp的施用增强了致耐受性dc相关标记(如il10、cd274(pd
‑
l1编码基因)、吲哚胺2,3
‑
双加氧酶(ido)和tgfβ1)的表达(图13b和图11c)。有趣的是,与模拟物(dw)处理的小鼠的dc相比,mgcp处理的小鼠的dc使ptgs2(环氧合酶
‑
2编码基因,cox2)的表达增加约20倍(图13b和图11c)。由于已知cox2在肿瘤环境中诱导treg细胞,因此评价了cox2在由mgcp得到的treg细胞分化中的作用。用mgcp刺激脾脏dc,并在存在作为cox2选择性抑制剂的塞来昔布的情况下将其与幼稚cd4 t细胞一起孵育。通过抑制cox2显著降低了由mgcp诱导的treg细胞(图13d和图11e)。这些结果表明,mgcp诱导的treg细胞的增加是通过cd103
cd11b
肠dc子集以cox2依赖性方式特异性介导的。另外,mgcp将dc转录组景观修饰为致耐受性dc表型。
[0258]
实施例7:模式识别受体在由mgcp诱导的treg细胞产生机制中的重要性
[0259]
dc表达模式识别受体(prr),从而识别存在于肠中的包括多糖的微生物抗原。为了研究多糖识别受体在mgcp介导的免疫调节中的作用,使用特异性受体受损的来自小鼠的dc确认treg细胞的分化。dectin1缺乏型脾脏dc显著降低了通过mgcp实现的treg细胞产生,但是dectin2的缺乏在相对较小的程度上减少了treg细胞的分化(图15a)。另外,与wt dc相比,缺乏tlr2、tlr4和tlr6中每一种的dc降低了通过mgcp实现的treg细胞分化,其中tlr4展现出最显著的作用(图15a)。与由于dc中的tlr缺乏而导致的treg细胞产生的减少相一致,具有受损myd88信号传导的dc显示出treg细胞分化的显著减少(图15b)。另外,使用dc
‑
sign、mincle和甘露糖受体中每一种的拮抗阻断抗体来研究不同c型凝集素受体的可能作用。dc中dc
‑
sign信号的阻断显示通过mgcp实现的treg细胞分化的部分减少,但对于其他受体没有观察到显著的影响(图15c)。总体而言,上述结果表明dectin1和tlr4在由mgcp诱导treg细胞中起重要作用,并且mgcp通过各种先天受体诱导treg细胞。
[0260]
实施例8:dectin1对于通过mgcp诱导treg细胞的重要性的确认
[0261]
为了确定dectin1在由mgcp诱导的treg细胞产生中的作用,用模拟物或mgcp刺激dectin1富有型或dectin1缺乏型小鼠的mln dc。dectin1富有型dc在mgcp刺激之后显示cox2和其他调节标记的表达增加,但mgcp不促进dectin1缺乏型dc中cox2的表达(图16a和图15a)。与dectin1对mgcp处理后cox2的表达的作用一致,ido和tgfβ1转录物通过mgcp刺激在dectin1富有型dc中特异性增加,但在受损dc中没有特异性增加(图17a)。令人惊讶的是,不存在dectin1没有导致mgcp介导的其他调节dc标记(如il10和cd274)表达的增加的变化(图17a)。为了支持dectin1在mgcp诱导的treg细胞产生中的必要作用,测试了mgcp在
dectin1缺乏型小鼠中的作用。将mgcp施用于接受了来自ot
‑
ii小鼠的幼稚cd4 t细胞并每隔一天补充卵白蛋白的小鼠。在整个实验中,将mgcp施用于接受者小鼠。有趣的是,mgcp的施用显著增加了卵白蛋白激活的treg细胞在dectin1富有型受体的小肠中的分化,而mgcp诱导treg细胞分化的作用在dectin1缺乏型小鼠中降低(图16b和图14c)。同时,在dectin1缺乏型或dectin1富有型受体中的受体衍生细胞之中的treg细胞的频率在模拟物和mgcp处理的情况下是类似的(图17b)。源自mgcp处理的dectin1完整小鼠的宿主细胞的treg细胞的频率与模拟物处理的小鼠的所述频率是类似的,但是在存在mgcp的情况下,treg细胞的数量仅在dectin1富有型小鼠中显著增加,而在dectin1缺乏型小鼠中并非如此(图17c)。有趣的是,mgcp施用在dectin1富有型小鼠中增加了接受者衍生细胞之中的诱导型treg细胞的频率,但在dectin1敲除型小鼠中并非如此(图16d和图14e)。另外,评价了mgcp是否影响这些小鼠的肠系膜淋巴结中treg细胞的诱导。尽管在dectin1完整小鼠中treg细胞分化的频率增加,但在dectin1敲除型小鼠中mgcp的作用可以被忽略(图17d)。总体而言,这些发现表明,由mgcp在体内诱导treg细胞的分子机制取决于dectin1,其是由dc的cox2上调介导的。
[0262]
尽管已经详细描述了本发明的具体配置,但本领域技术人员应理解,本说明书是为了阐述用于说明性目的的优选实施方案而提供,并且不应理解为限制本发明的范围。因此,本发明的实质范围由所附权利要求及其等同物限定。
[0263]
【工业实用性】
[0264]
根据本发明的新型多糖即使在低剂量下也通过所述多糖的β
‑
葡聚糖和甘露聚糖结构产生致耐受性抗原呈递细胞,并且诱导抗原特异性调节t细胞(treg细胞)的分化或产生,从而在很少副作用的情况下调节靶免疫系统。因此,mgcp和由所述多糖诱导的treg细胞可用于免疫疾病和炎性疾病的预防和治疗。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。