1.本发明涉及分析化学领域,具体地,本发明涉及用于生物样本中季铵盐肟类重活化剂快速检测的检测方法和试剂盒。
背景技术:
2.季铵盐肟类(quaternary oximes,qao)重活化剂是预防和治疗有机磷化合物中毒的一类非常重要的药物,有机磷毒剂能同乙酰胆碱酯酶(acetylcholinesterase,ache)活性部位的丝氨酸羟基发生反应,形成稳定的p
‑
o共价键(op
‑
ache),对ache形成不可逆抑制,从而导致中毒。重活化剂中的肟羟基能进攻磷原子,破坏p
‑
o共价键,将乙酰胆碱酯酶活性部位的丝氨酸羟基重新复原,使酶恢复活性。该类化合物对外周神经系统的解毒效果明显,但季铵盐结构的强电荷使它们很难通过血脑屏障(blood brain barrier,bbb)在中枢神经系统发挥解毒作用。通过剂型改造对重活化剂进行包裹可提高其通过血脑屏障的能力,进而提升对中枢神经性系统的重活化效果。目前针对生物样品中该类化合物的分析手段多为高效液相色谱法(hplc)、液相色谱
‑
串联质谱法(lc
‑
ms/ms)、毛细管电泳(ce)等,这些检测方法灵敏度高、重现性好,但需要复杂的样品前处理过程、较长的分析时间以及较为专业的操作人员。并且由于这类化合物具有强极性,色谱保留行为差,需要选用特殊的色谱柱或离子对试剂改善其分离效果;且肟类化合物在生物样本中易发生降解,样品前处理步骤复杂、检测速率慢、灵敏度差的方法已不能满足定性定量检测的需求。为有效评价各类季铵盐肟类重活化剂自身及剂型改造后透过bbb的能力,也为快速精准检测生物样本中抗毒药物的浓度、时效/量效关系,为应对nas中毒提供重要技术支撑,目前仍然需要探索可适用于生物样本中季铵盐肟类重活化剂的快速高灵敏检测方法。
技术实现要素:
3.发明人经过实验探索,获得了一种基于表面增强拉曼光谱的季铵盐肟类抗毒剂检测方法及检测试剂盒,发明人发现,本发明的检测方法或检测试剂盒具有操作简便、检测速度快、灵敏度高等诸多优点,可用于生物样本中针对神经性毒剂中毒季铵盐肟类救治药物的快速检测。
4.为此,在本发明的第一方面,本发明提供了一种检测季铵盐肟类抗毒剂的方法,其包括:
5.1)利用表面增强拉曼光谱仪,检测待测样本中季铵盐肟类抗毒剂的信号;
6.2)基于检测获得的信号,确定待测样本中季铵盐肟类抗毒剂的种类和/或含量。
7.表面增强拉曼光谱(surface
‑
enhanced raman spectroscopy,简称sers)技术是一种指纹光谱技术,具有灵敏度高、可实时无损分析、无需复杂样品前处理、操作简便以及检测速度快等优势。直接将sers应用于生物基质中季铵盐肟类重活化剂的检测,灵敏度很低,且生物样本中的各类生物大分子,如血细胞、蛋白质、氨基酸等,会严重抑制sers检测信
号,导致无检测信号或是灵敏度极低。针对这一难点问题,本发明通过构建“叠加式”au
‑
i
‑
‑
qao特异传感体系,利用荷正电的qao化合物与包覆碘负离子(i
‑
)纳米金之间的强静电相互作用,不仅有效清除了吸附于纳米金表面的蛋白质、氨基酸等化合物的干扰,还将目标分析物吸引至纳米溶胶的热点区域(hot
‑
spot),从而有效简化了样品预处理过程,显著提升生物样本中qao化合物的检测灵敏度和分析速度,避免因自降解所导致的生物样本分析过程中平行性差等不足;实现了血液、脑提取液等样本中肟类重活化剂的定性定量分析,为评价该类化合物的血脑屏障透过能力,提供了较为有力的技术支撑。
8.为此,在一些实施方案中,所述表面增强拉曼光谱的增强基底选自金纳米溶胶、银纳米溶胶、金磁纳米溶胶或其它形式的纳米检测基底。
9.在一些实施方案中,所述表面增强拉曼光谱的增强基底为有孔壳层隔绝金纳米粒子(pinhole shell
‑
isolated nanoparticles,pinshins)。
10.在一些实施方案中,所述表面增强拉曼光谱的增强试剂选自kf、ki、nacl、mgso4、na2co3、na2so4、nabr、nahco3、na2so3。
11.在一些实施方案中,所述表面增强拉曼光谱的增强试剂为ki。
12.在一些实施方案中,所述增强试剂的浓度为50
‑
200mmol/l(如50、70、90、100、110、130、150、170、190或200mmol/l),优选为50
‑
150mmol/l,更优选为100mmol/l,其中,所述增强试剂的浓度指的是所述增强试剂与所述增强基底和所述待测样本混合后所述增强试剂的终浓度。
13.在一些实施方案中,所述方法的步骤1)包括:
[0014]1‑
1)将增强基底进行离心,弃上清液;
[0015]1‑
2)将增强试剂与步骤1
‑
1)所得产物进行混合;优选地,将增强试剂缓慢加入到步骤1
‑
1)所得产物的底部;
[0016]1‑
3)将待测样本与步骤1
‑
2)所得产物进行混合;
[0017]1‑
4)利用表面增强拉曼光谱仪,对步骤1
‑
3)所得产物进行检测,获得待测样本中季铵盐肟类抗毒剂的信号。
[0018]
在一些实施方案中,所述表面增强拉曼光谱的激光功率为0
‑
300mw,优选为60
‑
180mw,更优选为60
‑
120mw。
[0019]
在一些实施方案中,所述检测的检测时间为8
‑
12s,优选为10s。
[0020]
在一些实施方案中,所述检测的检测波长为785nm。
[0021]
在一些实施方案中,所述检测的定量峰为1638cm
‑1拉曼位移处的峰高。
[0022]
在一些实施方案中,所述表面增强拉曼光谱仪为便携式或手持式拉曼光谱仪。
[0023]
在一些实施方案中,所述待测样本选自血液样本、组织样本(如脑组织样本)。
[0024]
在一些实施方案中,所述血液样本预先经过离心处理以弃去红细胞,获得血浆样本。
[0025]
在一些实施方案中,所述组织样本预先经过沉淀处理以去除蛋白和/或脂肪组织。
[0026]
在一些实施方案中,所述沉淀处理中使用的沉淀剂选自三氟乙酸、甲酸、乙腈、氯化钠、硫酸锌、乙酸、乙醇、乙腈,优选为氯化钠。
[0027]
在一些实施方案中,所述沉淀剂(优选为氯化钠)的浓度为0.5
‑
1.5mol/l,优选为1mol/l,其中,所述沉淀剂的浓度指的是所述沉淀剂与所述组织样本混合后所述沉淀剂的
终浓度。
[0028]
在一些实施方案中,所述季铵盐肟类抗毒剂选自tmb
‑
4(双解磷,双
‑
4,4
′‑
吡啶甲醛肟
‑
n,n
′
二溴三甲烯盐)、hi
‑
6(酰胺磷定)、obi(双复磷)、mmb
‑
4(1,1
′‑
亚甲基二[4
‑
[(羟亚胺基)甲基]
‑
吡啶二溴酸盐)、pam(解磷定,吡啶甲醛肟碘甲烷盐)。
[0029]
在一些实施方案中,所述有孔壳层隔绝金纳米粒子包括核芯和壳层,所述壳层包覆所述核芯,所述核芯为aunps,所述壳层为sio2壳层。
[0030]
在一些实施方案中,所述aunps的粒径为50
‑
60nm,优选为55nm。
[0031]
在一些实施方案中,所述sio2壳层的厚度为1
‑
2nm。
[0032]
在一些实施方案中,所述有孔壳层隔绝金纳米粒子是通过如下方法制备的:
[0033]
1)将aunps与3
‑
氨丙基三甲氧基硅烷进行第一混合;
[0034]
2)将第一混合产物与na2sio3进行第二混合,获得所述有孔壳层隔绝金纳米粒子。
[0035]
在一些实施方案中,所述3
‑
氨丙基三甲氧基硅烷是以溶于水的形式提供的。
[0036]
在一些实施方案中,所述3
‑
氨丙基三甲氧基硅烷的水溶液中,所述3
‑
氨丙基三甲氧基硅烷的浓度为0.5
‑
1.5mm,优选为1mm。
[0037]
在一些实施方案中,所述na2sio3是以溶于水的形式提供的。
[0038]
在一些实施方案中,所述na2sio3水溶液中,所述na2sio3的浓度(w/w)为0.5%
‑
0.6%,优选为0.54%。
[0039]
在一些实施方案中,所述na2sio3水溶液的ph大于11。
[0040]
在一些实施方案中,所述第一混合的时间为10
‑
20min,优选为15min。
[0041]
在一些实施方案中,所述第二混合的时间为2
‑
5min,优选为3min。
[0042]
在一些实施方案中,所述aunps(金纳米粒子)是采用frens的柠檬酸钠还原四氯金酸法制备的。
[0043]
在一些实施方案中,所述aunps是通过如下方法制备的:
[0044]
1)将三水合四氯金酸与水进行混合,获得母液;
[0045]
2)取部分母液加水进行稀释;
[0046]
3)将稀释后的母液加热至沸腾,待冷凝回流后向其中加入柠檬酸三钠水溶液,继续加热30
‑
50min(如40min),获得所述aunps。
[0047]
在一些实施方案中,所述母液中,所述三水合四氯金酸的浓度为0.5
‑
1.5mg/ml,优选为1mg/ml。
[0048]
在一些实施方案中,取部分母液加水进行稀释时,稀释倍数为8
‑
12倍,优选为10倍。
[0049]
在一些实施方案中,所述柠檬酸三钠水溶液中,所述柠檬酸三钠的浓度(w/w)为0.5
‑
1.5%,优选为1%。
[0050]
在一些实施方案中,所述稀释后的母液与所述柠檬酸三钠水溶液的体积比为100:0.8
‑
0.9,优选为100:0.85。
[0051]
在一些实施方案中,确定待测样本中季铵盐肟类抗毒剂的种类是通过如下步骤进行的:
[0052]
1)利用表面增强拉曼光谱仪,检测待测样本中季铵盐肟类抗毒剂的信号;
[0053]2‑1‑
a)将检测获得的信号与每种季铵盐肟类抗毒剂的特征指纹图谱进行比对;
[0054]2‑2‑
a)基于比对结果,确定待测样本中季铵盐肟类抗毒剂的种类。
[0055]
在一些实施方案中,确定待测样本中季铵盐肟类抗毒剂的含量是通过如下步骤进行的:
[0056]
1)利用表面增强拉曼光谱仪,检测待测样本中季铵盐肟类抗毒剂的信号;
[0057]2‑1‑
b)利用表面增强拉曼光谱仪,检测预设的不同浓度(例如倍数稀释)的季铵盐肟类抗毒剂的信号;
[0058]2‑2‑
b)基于预设的季铵盐肟类抗毒剂的不同浓度,以及检测获得的预设的不同浓度的季铵盐肟类抗毒剂的信号强度,绘制信号强度
‑
浓度工作曲线;
[0059]2‑3‑
b)基于检测获得的待测样本中季铵盐肟类抗毒剂的信号,以及绘制的所述信号强度
‑
浓度工作曲线,确定待测样本中季铵盐肟类抗毒剂的含量。
[0060]
在一些实施方案中,步骤2
‑1‑
b)中,检测预设的不同浓度(例如倍数稀释)的季铵盐肟类抗毒剂的信号时,各浓度的增强基底是通过如下方法制备的:将第一预设体积(如1ml)的增强基底置于ep管中离心并弃去上清液后,将底部残留增强基底混合均匀,之后从所述底部残留增强基底中取第二预设体积(如10μl)的增强基底分装于ep管中待用。
[0061]
在本发明的第二方面,本发明提供了一种基于表面增强拉曼光谱的季铵盐肟类抗毒剂检测试剂盒,其包括:
[0062]
(1)增强基底,所述增强基底如前所述;
[0063]
(2)增强试剂,所述增强试剂如前所述;
[0064]
任选地,所述试剂盒还包括:(3)待测样本前处理试剂。
[0065]
在一些实施方案中,所述增强基底为有孔壳层隔绝金纳米粒子;
[0066]
在一些实施方案中,所述有孔壳层隔绝金纳米粒子如前所述。
[0067]
在一些实施方案中,所述待测样本前处理试剂为沉淀剂。
[0068]
在一些实施方案中,所述沉淀剂如前所述。
附图说明
[0069]
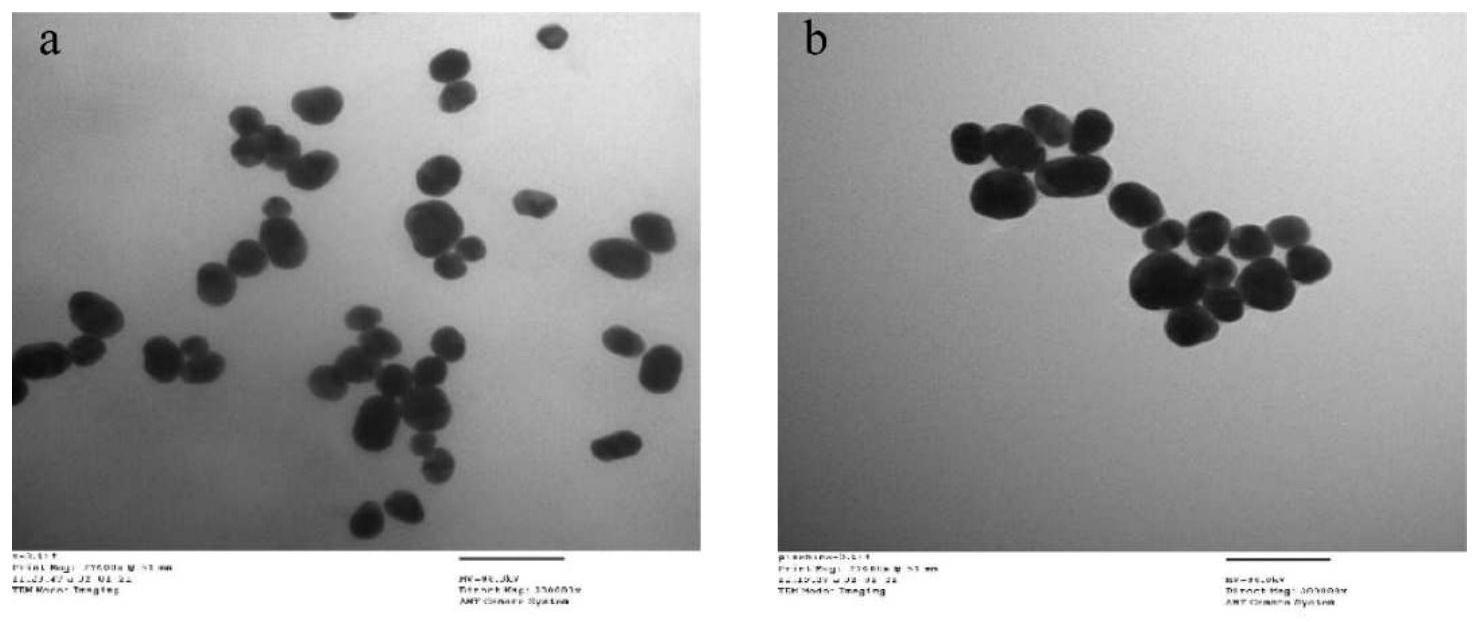
图1.aunps(a)和pin shins(b)的透射电镜表征图;
[0070]
图2.tmb
‑
4水溶液中(100ppb)加入不同种类无机盐的sers谱图(a),以及对1638cm
‑1峰强度(b)的影响;
[0071]
图3.添加浓度为0,20,30,50,100,200,300,400,500mmol/l ki tmb
‑
4水溶液(100ppb)sers检测谱图(a);ki浓度对tmb
‑
4 1638cm
‑1处sers峰强度的影响(b);
[0072]
图4.五种季铵盐肟类重活化剂pam(10μg/ml),hi
‑
6、mmb4、tmb4、obi(1μg/ml)水溶液sers检测谱图;
[0073]
图5a.不同浓度下tmb
‑
4的sers检测谱图;
[0074]
图5b.1638cm
‑1处sers峰强度
‑
tmb
‑
4浓度(0.5
‑
20ng/ml)工作曲线;
[0075]
图5c.不同浓度下obi的sers检测谱图;
[0076]
图5d.1638cm
‑1处sers峰强度
‑
obi浓度(0.5
‑
20ng/ml)工作曲线;
[0077]
图5e.不同浓度下hi
‑
6的sers检测谱图;
[0078]
图5f.1638cm
‑1处sers峰强度
‑
hi
‑
6浓度(0.5
‑
20ng/ml)工作曲线;
[0079]
图5g.不同浓度下mmb
‑
4的sers检测谱图;
[0080]
图5h.1638cm
‑1处sers峰强度
‑
mmb
‑
4浓度(0.5
‑
20ng/ml)工作曲线;
[0081]
图6.aunps和pinshins为增强基底,hi
‑
6血浆样品(50ng/ml)sers检测谱图;
[0082]
图7.采用pinshins检测hi
‑
6血浆样品(1mg/ml)不同放置时间对1638cm
‑1峰强变化的影响;
[0083]
图8.不同采血时间点hi
‑
6血浆样品sers检测谱图(a);hi
‑
6血浆样品时间
‑
强度曲线(b);
[0084]
图9.待测样本为hi
‑
6浓度为200ppb的脑匀浆液时,不同蛋白质沉淀剂对脑匀浆组织处理后sers检测图(a),其中,直接检测表示不添加沉淀剂直接检测脑匀浆组织,离心检测表示不添加沉淀剂将脑匀浆组织离心处理后取上清液进行检测,乙酸(pinshins)表示沉淀剂为乙酸和预备实施例制备的pinshins,tfa(pinshins)表示沉淀剂为三氟乙酸和预备实施例制备的pinshins;待测样本为hi
‑
6浓度为200ppb的脑匀浆液时,不同蛋白沉淀剂处理脑匀浆对1638cm
‑1处峰强度的影响(b);沉淀剂为nacl时,不同浓度hi
‑
6脑组织样品sers检测谱图(c);以及沉淀剂为nacl时,1638cm
‑1处sers峰强度
‑
hi
‑
6浓度(10
‑
500ng/ml)工作曲线(d)。
具体实施方式
[0085]
下面详细描述本发明的实施例,下面描述的实施例是示例性的,旨在用于解释本发明,而不能理解为对本发明的限制。
[0086]
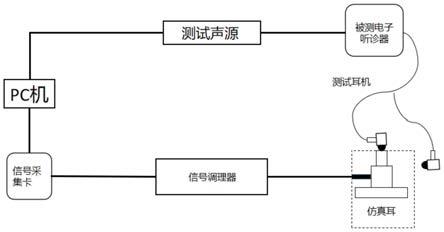
本发明属于分析化学领域,涉及一种针对有机磷神经性毒剂中毒的肟类重活化剂快速检测试剂盒。具体地,本发明涉及sers增强基底的选择;团聚剂种类及浓度的优化;生物样本蛋白质沉淀剂优选;检测试剂施加步骤;复杂基质样品中的检测方法以及相关检测试剂包的配制。
[0087]
本发明属于分析化学领域,涉及一种基于表面增强拉曼光谱(surface
‑
enhanced raman spectroscopy,sers)技术和季铵盐肟类(quaternary oximes,qao)重活化剂的快速检测试剂盒。具体的,本发明涉及增强基底的制备、检测条件及试剂的优选、生物样本中系列肟类重活化剂的快速检测方法。所述试剂盒内包括sers基底、增强试剂及简易样品前处理附件等检测试剂包。本发明以金纳米粒子(aunps)作为基底,利用季铵盐肟类化合物氮原子荷正电的结构特性,基于层层自组装原理,构建了au
‑
i
‑
‑
qao特异性传感体系,通过引入i
‑
与au核形成au
‑
i键,不仅有效清除了吸附在au表面的基质干扰物,同时利用荷正电的季铵盐重活化剂与包覆i
‑
的au之间的强静电相互作用,大幅提升了生物样品中qao检测灵敏度,有效简化了样品预处理过程,该检测试剂盒具有操作简便、检测速度快、灵敏度高等诸多优点,可用于生物样本中针对神经性毒剂中毒季铵盐肟类救治药物快速检测。
[0088]
本发明的目的是提供生物基质中季铵盐肟类重活化剂快速、简便、灵敏的检测方法,利用au
‑
i
‑
‑
qao特异传感体系,采用sers检测手段,对生物基质中的qao进行快速检测。具体地,本发明包括以下几方面:
[0089]
本发明第一方面涉及增强基底的制备与优化,所述方法包括以下步骤:
[0090]
aunps的制备:采用frens的柠檬酸钠还原四氯金酸法制备粒径约为55nm的金纳米粒子。准确称取100mg三水合四氯金酸于100ml容量瓶定容得1mg/ml母液(溶剂为水),取10ml母液稀释至100ml,倒入250ml三颈瓶中油浴加热,在快速搅拌下加热至沸,待冷凝回流
后迅速加入0.85ml 1%柠檬酸三钠水溶液,继续加热搅拌40min,制备得粒径约为55nm的aunps。
[0091]
pinshins的制备:向制备好的55nm aunps中加入3
‑
氨丙基三甲氧基硅烷(aptms)水溶液(1mm),搅拌15min后,加入na2sio3水溶液(0.54%,w/w)后再搅拌3min,使aunps表面包覆生成sio2壳层。na2sio3水溶液的ph大于11时,即可生成厚度为1
‑
2nm的有孔sio2壳层,完成后储存于4℃冰箱待用。
[0092]
本发明第二方面涉及增强试剂种类的优化,所述方法包括以下步骤:
[0093]
选取kf、ki、nacl、mgso4、na2co3、na2so4、nabr、nahco3、na2so3作为增强试剂,加到离心后的前述制备获得的增强基底中,向基底中加入200μl 100ppb的qao样品,使无机盐终浓度为100mmol/l,进行sers检测,最终结果显示ki的团聚效果最优。
[0094]
本发明第三方面涉及团聚剂浓度的优化,所述方法包括以下步骤:
[0095]
在离心后的前述制备获得的增强基底中添加ki溶液(溶剂为水),加入200μl 100ppb的qao样品,使ki终浓度为0,20,30,50,100,200,300,400,500mmol/l,进行检测,最终结果显示,当ki终浓度为100mmol/l时,团聚效果最优。
[0096]
本发明第四方面涉及血液样本中qao的检测,所述方法包括以下步骤:
[0097]
取1ml前述制备获得的增强基底于ep管中,离心后弃去上清液,另取10μl 2mol/l的碘化钾溶液,缓慢加入到离心后的增强基底中,将离心弃去红细胞的血浆样本按倍数稀释后,取200μl样品液快速加到增强基底中,充分混匀后,用手持式拉曼谱仪进行检测。
[0098]
本发明第五方面涉及脑组织样本中qao的检测,所述方法包括以下步骤:
[0099]
取800μl脑匀浆液加入无机盐沉淀剂(nacl),充分沉淀蛋白后,离心取上清液200μl。另取1ml增强基底,离心后弃去上清液,加入10μl 2mol/l的碘化钾溶液,混合均匀,之后再加入前面的离心后的上清液样本200μl,混合均匀,直接用手持式拉曼谱仪进行检测。
[0100]
具体地,本发明提供了一种基于sers的季铵盐肟类抗毒剂快速检测试剂盒,其特征在于,所述试剂盒包括sers增强基底、增强试剂。操作步骤包括如下:
[0101]
a)纳米增强基底的制备;
[0102]
b)增强试剂的优选;
[0103]
c)针对溶液样品季铵盐肟类重活化剂的检测:吸取适量的纳米增强基底,离心机中离心后,吸出上清液,将增强试剂与纳米溶胶混和,再将样品加入其中,混匀后用便携式或手持式拉曼谱仪进行检测;
[0104]
d)配制不同浓度的季铵盐肟类重活化剂溶液,按步骤c)中所述,采集不同浓度季铵盐肟类重活化剂溶液的特征拉曼信号强度,根据信号强度和浓度绘制工作曲线;
[0105]
e)根据样品指纹图谱和特征拉曼峰强度对样品中季铵盐肟类重活化剂进行定性和定量检测。
[0106]
f)针对生物样本中各类神经性毒剂中毒重活化剂的检测,为提高检测灵敏度,其操作步骤需按照既定顺序实施。
[0107]
在一些实施方案中,所述sers纳米增强基底为金纳米溶胶、银纳米溶胶、金磁纳米溶胶或其它形式的纳米检测基底,优选基底为有孔壳层隔绝金纳米粒子(pinhole shell
‑
isolated nanoparticles,pinshins)。
[0108]
在一些实施方案中,所述的增强试剂优选部分,主要涉及各类无机盐团聚剂的筛
选、最佳施加浓度的优化。
[0109]
在一些实施方案中,所述的无机盐包括kf、ki、nacl、mgso4、na2co3、na2so4、nabr、nahco3、na2so3,优选无机盐为ki。
[0110]
在一些实施方案中,所述的无机盐团聚剂最佳施加浓度优化部分,主要是指与纳米溶胶及样品混合后的终浓度,优选浓度范围为50~200mmol/l。
[0111]
在一些实施方案中,所述季铵盐肟类重活化剂检测部分,生物样品中检测步骤为:取适量增强基底离心后弃去上清液,将增强试剂缓慢加入到增强基底底部,生物样本按倍数稀释后,快速加入到增强基底中,充分混匀后,用便携式或手持式拉曼谱仪进行检测。
[0112]
在一些实施方案中,所述不同浓度季铵盐肟类重活化剂的工作曲线绘制部分,为呈现良好的线性关系,分别取1ml增强基底于ep管中离心弃去上清液后,将底部纳米金溶胶混合均匀,以保持纳米金溶胶形态的均一性,取10μl混合的纳米金溶胶分装于ep管中待用。
[0113]
在一些实施方案中,所述检测过程,其特征在于:所用拉曼光谱仪为便携式拉曼光谱仪,其激光功率在0
‑
300mw,优选激光功率为60
‑
120mw,最佳检测基底为:pinshins纳米溶胶。
[0114]
在一些实施方案中,所述的生物样本中重活化剂的检测步骤,最佳顺序为:
①
离心纳米溶胶,吸出上清液;
②
在纳米溶胶中加入增强试剂;
③
加入待测样本;
④
采集sers光谱图。该顺序不宜颠倒和随意调换。
[0115]
在一些实施方案中,对于组织样本,需先对其中的蛋白、脂肪组织进行有效沉淀以避免对目标物检测信号的强烈抑制。常用的蛋白质沉淀剂有三氟乙酸、甲酸、乙腈、氯化钠、硫酸锌等,优选为氯化钠,其浓度为1mol/l。
[0116]
下面结合具体实施例对本发明进行进一步的解释说明。
[0117]
预备实施例
[0118]
1、aunps的制备:
[0119]
采用frens的柠檬酸钠还原四氯金酸法制备粒径约为55nm的金纳米粒子。准确称取100mg三水合四氯金酸于100ml容量瓶定容得1mg/ml母液(溶剂为水),取10ml母液稀释至100ml,倒入250ml三颈瓶中油浴加热,在快速搅拌下加热至沸,待冷凝回流后迅速加入0.85ml 1%柠檬酸三钠水溶液,继续加热搅拌40min,制备得粒径约为55nm的aunps。
[0120]
2、pinshins的制备:
[0121]
向制备好的55nm aunps中加入3
‑
氨丙基三甲氧基硅烷(aptms)水溶液(1mm),搅拌15min后,加入na2sio3水溶液(0.54%,w/w)后再搅拌3min,使aunps表面包覆生成sio2壳层。na2sio3水溶液的ph大于11时,即可生成厚度为1
‑
2nm的有孔sio2壳层,完成后储存于4℃冰箱待用。
[0122]
制备的aunps和pinshins如图1a和1b所示。
[0123]
实施例1
[0124]
取kf、ki、nacl、mgso4、na2co3、na2so4、nabr、nahco3、na2so3作为增强试剂,分别加到离心后去除上清的纳米溶胶(即预备实施例中制备的aunps)中混匀,加入200μl 100ng/ml的tmb
‑
4水溶液,使前述各无机盐终浓度为100mmol/l,充分混匀后,进行sers检测,激光功率为60mw,检测时间为10s,结果显示ki的增强效果最优(如图2a.2b.)。
[0125]
实施例2
[0126]
将ki作为增强试剂,加到离心后去除上清的纳米溶胶(即预备实施例中制备的aunps)中混匀,再加入200μl 100ng/ml的tmb
‑
4水溶液,使ki终浓度分别为0,20,30,50,100,200,300,400,500mmol/l,进行sers检测,激光功率为60mw,检测时间为10s,结果显示,当ki终浓度为100mmol/l时,增强效果最优(如图3a.3b.)。
[0127]
实施例3
[0128]
用超纯水配制浓度为1μg/ml的tmb
‑
4、hi
‑
6、obi、mmb
‑
4和10μg/ml的pam溶液。
[0129]
将ki作为增强试剂,加到离心后去除上清的纳米溶胶(即预备实施例中制备的aunps)中混匀,再分别加入200μl前述配置的tmb
‑
4、hi
‑
6、obi、mmb
‑
4和pam水溶液,使ki的终浓度为100mmol/l,进行sers检测,tmb
‑
4、hi
‑
6、obi、mmb
‑
4的检测激光功率为60mw,pam的检测激光功率为180mw,检测时间均为10s。检测结果如图4所示。不同重活化剂有其特征的指纹图谱,能够进行明确区分。该实施说明,本发明的方法能够对不同的季铵盐肟类重活化剂进行快速、准确的定性分析。
[0130]
实施例4
[0131]
用超纯水配制梯度浓度的tmb
‑
4、hi
‑
6、obi、mmb
‑
4溶液。
[0132]
将ki作为增强试剂,加到离心后去除上清的纳米溶胶(即预备实施例中制备的aunps)中混匀,再分别加入200μl前述配置的梯度浓度的tmb
‑
4、hi
‑
6、obi、mmb
‑
4水溶液,使ki的终浓度为100mmol/l。
[0133]
分别对不同浓度的qao重活化剂进行sers检测,激光功率120mw,检测时间10s,建立标准曲线,1638cm
‑1峰强度与qao重活化剂浓度在一定范围内呈正比关系,结果如图5a
‑
5h所示。tmb
‑
4(y=1210x 4567,r2=0.987)、mmb
‑
4(y=1023x 1363,r2=0.990),hi
‑
6(y=1673x 2092,r2=0.962),obi(y=1180x 3110,r2=0.996)的线性范围均为0.5
‑
20ng/ml,检测限为0.5ng/ml。表明本发明的方法可用作季铵盐肟类重活化剂的高灵敏定量检测,且无需样品前处理过程,其sers检测只需10s,非常适合于大批量样品的快速检测。
[0134]
实施例5
[0135]
用自制aunps与pinshins增强基底(即预备实施例中制备的aunps和pinshins)测定50ppb hi
‑
6的血浆样品。将10μl 2mol/l增强试剂ki分别加到离心后去除上清的前述两种增强基底中混匀,取200μl的血浆样品与增强基底混匀,进行sers检测,激光功率为120mw,检测时间为10s,如图6所示,裸金纳米粒子aunps无信号响应,pinshins有明显的信号增强。由此可见,pinshins超薄的sio2壳层能起到有效保护au核的作用,使其具有更优异的抗复杂生物基质干扰能力。
[0136]
实施例6
[0137]
以pinshins(即预备实施例中制备的pinshins)为增强基底,检测hi
‑
6血浆样品。将10μl 2mol/l增强试剂ki加到离心后去除上清的增强基底中混匀,取200μl的血浆样品与增强基底混匀,于室温放置0min、5min、10min、20min、30min、40min、1h、2h、3h、4h、5h、6h、7h、8h、9h、10h、11h、12h、24h,在各个时间点采集溶液的sers光谱进行sers检测,激光功率为120mw,检测时间10s,如图7所示,血浆中含有大分子物质以及pinshins的核壳结构,能对样品起到稳定的作用,sers信号能保持至少12h无明显变化。
[0138]
实施例7
[0139]
以pinshins(即预备实施例中制备的pinshins)为增强基底,进行实际血浆样品的
测定。
[0140]
向小鼠体内注射负荷剂量的hi
‑
6重活化剂溶液后,在0,5min,15min,30min,1h取血,离心后取上清。
[0141]
将10μl 2mol/l增强试剂ki加到离心后去除上清的增强基底中混匀,之后分别取200μl的前述各时间点所取的小鼠血浆样品离心后的上清与增强基底混匀,进行sers检测,激光功率为120mw,检测时间为10s,如图8所示,5min时药物的血浆浓度最高,该方法在实际样品检测中能够实现准确的定性及定量分析。
[0142]
实施例8
[0143]
由于脑内含大量复杂基质,严重抑制拉曼信号,脑匀浆需进行蛋白沉淀后进行检测。配制hi
‑
6浓度为500ppb,200ppb,100ppb,50ppb,20ppb,10ppb的脑匀浆液,取800μl上述脑匀浆液加入200μl的不同的沉淀剂(各沉淀剂终浓度为1m,沉淀剂优选为终浓度1m的nacl),涡旋3min,12000rpm/min,5min离心取上清。
[0144]
将10μl 2mol/l增强试剂ki加到离心后去除上清的增强基底(即预备实施例中制备的pinshins)中混匀,之后分别取200μl的前述离心后的上清脑浆匀液与增强基底混匀,进行sers检测,激光功率为120mw,检测时间为10s,结果如图9a
‑
d所示。综合信号强度与经济效益,建议以nacl为沉淀剂。脑匀浆液中hi
‑
6(y=35x 892,r2=0.965)的线性范围10~500ng/ml。
[0145]
以上所述的具体实施例,对本发明的目的、技术方案和有益效果进行了进一步详细说明,所应理解的是,以上所述仅为本发明的具体实施例而已,并不用于限定本发明的保护范围,凡在本发明的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。