一种
β
2-微球蛋白检测试剂盒及其临床应用
技术领域
1.本发明属于医学免疫体外诊断领域,尤其是一种重组人β
2-微球蛋白(β
2-microglobulin,β
2-mg)及其在定量检测人血清β
2-mg含量的检测试剂盒中的应用。
背景技术:
2.β
2-微球蛋白(β
2-microglobulin,β
2-mg)是一种分子量为11.8kd的蛋白质,存在于所有有核细胞(除红细胞、胎盘滋养层之外),尤其在淋巴细胞和单核细胞中含量丰富。同一个体每日生产β2-mg的量保持恒定,并分泌于各种体液中。测定血液、尿液、等中的β
2-mg对诊断疾病有着重要意义,以下情况均会引起血液中β
2-mg含量升高:
①
肾功能减退:急慢性肾炎、肾功能衰退、肾肿瘤等,
②
恶性肿瘤:原发性肝癌、肺癌等,
③
自身免疫性疾病:系统性红斑狼疮,aids病等,
④
器官移植排斥反应。
3.对β
2-mg的检测方法主要有酶联免疫比浊法、放射免疫比浊法,这些方法都是基于免疫学,利用抗原抗体的特异性结合,定量检测血清中β
2-mg含量。但这些方法由于操作繁琐、周期长或费用高等劣势,阻碍了其在临床上广泛使用。而全自动生化分析仪已在临床上(从二级到三级医院)几乎全面使用,加上生化比浊法本身具备反应时间短,精密度好,易于自动化等优点,生化比浊法已成为国内外临床上主流检测方法。
4.本发明采用胶乳增强免疫比浊法,借助多个特异性鼠单抗包被的“胶乳”介质,抗原-抗体聚合物的粒径显著增大,从而提高了检测灵敏度和精密度。
技术实现要素:
5.本发明提供了一种重组人β
2-微球蛋白(以下简称β
2-mg),其氨基酸序列如seq id no:1,优化后的密码子序列如seq id no:2所示。
6.本发明还提供了5种鼠抗人β
2-mg单克隆抗体,第一种抗人β
2-mg单克隆抗体(bm15),其重链可变区含有以下的互补决定区:氨基酸序列如序列seq id no:3所示的hcdr1、如序列seq id no:4所示的hcdr2和/或如序列seq id no:5所示的hcdr3;
7.以及其轻链可变区序列含有以下的互补决定区:氨基酸序列如序列seq id no:6所示的lcdr1、如序列seq id no:7所示的lcdr2和/或如序列seq id no:8所示的lcdr3。
8.优选的是本发明中bm15抗体重链可变区的氨基酸序列如seq id no:9所示,轻链可变区的氨基酸序列如seq id no:10所示。
9.优选的bm15单克隆抗体氨基酸序列如seq id no:11所示;编码上述单克隆抗体的核苷酸序列如seq id no:12所示。
10.第二种抗人β
2-mg单克隆抗体(bm18),其重链可变区含有以下的互补决定区:氨基酸序列如序列seq id no:13所示的hcdr1、如序列seq id no:14所示的hcdr2和/或如序列seq id no:15所示的hcdr3;
11.以及其轻链可变区序列含有以下的互补决定区:氨基酸序列如序列seq id no:16所示的lcdr1、如序列seq id no:17所示的lcdr2和/或如序列seq id no:18所示的lcdr3。
12.优选的是本发明中bm18抗体重链可变区的氨基酸序列如seq id no:19所示,轻链可变区的氨基酸序列如seq id no:20所示。
13.优选的bm18单克隆抗体氨基酸序列如seq id no:21所示;编码上述单克隆抗体的核苷酸序列如seq id no:22所示。
14.第三种抗人β
2-mg单克隆抗体(bm20),其重链可变区含有以下的互补决定区:氨基酸序列如序列seq id no:23所示的hcdr1、如序列seq id no:24所示的hcdr2和/或如序列seq id no:25所示的hcdr3;
15.以及其轻链可变区序列含有以下的互补决定区:氨基酸序列如序列seq id no:26所示的lcdr1、如序列seq id no:27所示的lcdr2和/或如序列seq id no:28所示的lcdr3。
16.优选的是本发明中bm20抗体重链可变区的氨基酸序列如seq id no:29所示,轻链可变区的氨基酸序列如seq id no:30所示。
17.优选的bm20单克隆抗体氨基酸序列如seq id no:31所示;编码上述单克隆抗体的核苷酸序列如seq id no:32所示。
18.第四种抗人β
2-mg单克隆抗体(bm22),其重链可变区含有以下的互补决定区:氨基酸序列如序列seq id no:33所示的hcdr1、如序列seq id no:34所示的hcdr2和/或如序列seq id no:35所示的hcdr3;
19.以及其轻链可变区序列含有以下的互补决定区:氨基酸序列如序列seq id no:36所示的lcdr1、如序列seq id no:37所示的lcdr2和/或如序列seq id no:38所示的lcdr3。
20.优选的是本发明中bm22抗体重链可变区的氨基酸序列如seq id no:39所示,轻链可变区的氨基酸序列如seq id no:40所示。
21.优选的bm22单克隆抗体氨基酸序列如seq id no:41所示;编码上述单克隆抗体的核苷酸序列如seq id no:42所示。
22.第五种抗人β
2-mg单克隆抗体(bm23),其重链可变区含有以下的互补决定区:氨基酸序列如序列seq id no:43所示的hcdr1、如序列seq id no:44所示的hcdr2和/或如序列seq id no:45所示的hcdr3;
23.以及其轻链可变区序列含有以下的互补决定区:氨基酸序列如序列seq id no:46所示的lcdr1、如序列seq id no:47所示的lcdr2和/或如序列seq id no:48所示的lcdr3。优选的是本发明中bm23抗体重链可变区的氨基酸序列如seq id no:49所示,轻链可变区的氨基酸序列如seq id no:50所示。
24.优选的bm23单克隆抗体氨基酸序列如seq id no:51所示;编码上述单克隆抗体的核苷酸序列如seq id no:52所示。
25.本发明还提供了由上述重组鼠抗人β
2-mg单克隆抗体制备的胶乳增强免疫比浊检测试剂盒。本发明的一种β2-微球蛋白免疫胶乳增强比浊检测试剂盒,包含r1试剂、r2试剂、标准品,所述r1试剂包括:缓冲液1、稳定剂、增凝剂、保护剂、防腐剂、螯合剂;所述r2试剂包括:缓冲液2、防腐剂、稳定剂、保护剂;所述标准品包括:缓冲液3、保护剂、稳定剂。
26.优选的,所述r1试剂中:缓冲液1为0.01m-0.05m、ph7.0-7.4的磷酸盐缓冲液;稳定剂为40g/l-80g/l的nacl;增凝剂为10-20g/l的peg6000,保护剂为0g/l-40g/l的bsa,防腐剂为0.05-0.1g/l的proclin300,螯合剂为2g/l-10g/l的edta。
27.优选的,所述r2试剂中:缓冲液2为0.01m-0.05m、ph7.0-7.4的磷酸盐缓冲液;防腐
剂为为0.05-0.1g/l的proclin300;稳定剂为0g/l-20g/l的nacl和50-100g/l的蔗糖,保护剂为5g/l-20g/l的bsa;另外有标记五种重组鼠抗人β
2-mg蛋白抗体质量浓度为0.2%-0.5%的胶乳微球。
28.优选的,所述标准品包括一定数量封装有不同浓度的重组人β
2-mg的溶液,其中缓冲液3为0.01m-0.02m、ph7.0-7.4的磷酸盐缓冲液;保护剂为1g/l-10g/l的bsa,稳定剂9-13g/l的nacl。
29.优选的,标记有重组鼠抗人β
2-mg蛋白抗体的胶乳微球制备方法包括如下步骤:
30.将5种重组鼠抗人β
2-mg蛋白单克隆抗体等质量的混合物用磷酸盐缓冲液将抗体稀释至0.5-2mg/ml,制备成抗体工作液;用mes缓冲液将胶乳微球(聚苯乙烯胶乳,购自日本jsr公司,粒径80-200nm)稀释至1%(质量浓度),再加入1%-4%(edc/胶乳微球的质量比)的edc,在30℃下搅拌反应30min,反应结束后通过离心去除未反应的edc,然后加入0.001-0.2(抗体/胶乳微球的质量比)重组鼠抗人β
2-mg蛋白单克隆抗体等质量混合物工作液,在16℃-37℃下搅拌反应30min-120min,反应结束后通过离心去除未反应的抗体,再加入终止反应液终止反应,离心,最后加入由缓冲液2、防腐剂(例如:proclin 300)、稳定剂(例如:nacl,蔗糖)、保护剂(例如:bsa)组成的缓冲液搅拌混匀,即为r2试剂(其中标记有重组鼠抗人β
2-mg蛋白抗体的胶乳微球质量浓度为0.2%-0.5%)。
31.本发明采用大肠杆菌作为表达系统制备重组人β
2-mg蛋白,该制备方法具有周期短、表达量大、成本低的优势。制备的β
2-mg蛋白不仅可以作为检测试剂盒的校准品原料,而且作为一种有效的免疫原,可用于鼠单克隆抗体的制备,在获得鼠抗序列的基础上进行重组表达,获得的单链抗体应用于β
2-微球蛋白定量检测试剂盒中r2试剂的包被抗体。本发明对上述制备的多种单链抗体进行配对筛选,获得灵敏度及特异性均能满足需求的抗体组合;同时其方便大量生产,可满足日后大规模临床应用的需求。对上述抗体组合进行检测体系的调试优化工作,获得操作简便,灵敏度,特异性及相关检测性能均可满足人临床样本检测的β
2-微球蛋白定量检测试剂盒(胶乳免疫比浊法)。
附图说明
32.图1试剂盒的标准曲线绘制图,图中横坐标为β
2-mg校准品浓度,纵坐标为吸光度
△
a。
33.图2比对试验性能评价结果。
具体实施方式
34.下面通过实施例进一步详细描述本发明,但本发明不局限于这些实施例。
35.实施例1β2-mg鼠单抗的制备
36.1.动物免疫以重组人β2-mg蛋白(氨基酸序列如seq id no:1,优化后的密码子序列如seq id no:2所示)按照一般免疫程序免疫balb/c雌性小鼠(购自常州卡文斯实验动物有限公司)。具体免疫情况参见《抗体制备与使用实验指南》。采用间接elisa法跟踪免疫小鼠血清滴度,选取血清效价最高的免疫小鼠,进行小鼠脾细胞和小鼠骨髓瘤细胞进行融合实验。
37.2.细胞融合
38.(1).脾脏细胞的制备
39.将免疫小鼠,摘眼球取血,经断颈椎处死后置于75%(v/v)的酒精中浸泡10分钟,于无菌操作台中取出其脾脏,置于细胞筛网中,充分研磨细胞,过筛网,用无菌1640培养基(购自gibco公司)离心洗涤数次后,重悬细胞以制成单细胞悬液,并计数,备用。
40.(2).饲养细胞的制备
41.取8~10周龄的雌性balb/c小鼠一只,摘眼球获取阴性血清,经断颈椎处死后置75%(v/v)酒精中浸泡10分钟;无菌揭开腹部皮肤,暴露腹膜,用注射器将约10ml 1640ht培养基(购自sigma公司)注入小鼠腹腔,轻轻按摩腹部并吹打数次。吸取含有巨噬细胞的培养基注入20%1640hat培养基中备用;
42.取2~3周龄的雌性balb/c小鼠一只,经断颈椎处死后置于75%(v/v)酒精中浸泡10分钟;无菌取胸腺于细胞筛网中,研磨,过筛网,获得胸腺细胞置于上述含有巨噬细胞的20%1640hat培养基中,备用。
43.(3).细胞融合
44.选择处于对数生长期的小鼠骨髓瘤细胞株sp2/0,收集并计数。取约108个上述脾细胞与2
×
107个上述sp2/0细胞株加入融合管中混合,1000rpm离心10分钟后弃上清(尽量弃净),将融合管置手掌上来回轻轻摩擦以使沉淀松散。60秒内先慢后快地加入1ml预热的peg1450(聚乙二醇1450,购自sigma公司),加入1640ht培养基30ml终止,1000rpm离心10分钟,去上清,轻轻摩擦使沉淀松散,加入步骤2所获得的20%的1640hat培养基中。
45.将上述hat培养基充分混匀后,以200μl/孔分装至96孔细胞培养板中,置37℃,5%co2的细胞培养箱中培养。一周后用10%1640ht培养基替换20%1640hat培养基,3天后取上清进行检测。
46.3.抗人β2-mg特异性杂交瘤株筛选
47.(1).检测板的准备:用cb包被液稀释重组人β2-mg蛋白至1μg/ml,包被96孔elisa酶标板,100μl/孔,2~8℃包被过夜,洗涤一次拍干;含2%牛血清白蛋白的pbst缓冲液封闭(200ul/孔),37℃封闭2小时;拍干,备用。
48.(2).阳性克隆的筛选:将待检细胞培养上清100μl/孔加入上述检测板中,于37℃作用30分钟后洗涤并拍干,加入100μl/孔的hrp标记的羊抗鼠igg,于37℃作用30分钟后洗涤并拍干,加入100μl/孔的tmb显色液,于37℃避光显色15分钟,每孔加入50μl的2m h2so4终止反应,并于od450处读取数值。阳性孔确定原则:od450值/阴性对照值≥2.1。选取阳性克隆株进行细胞克隆化筛选。经过三至四轮的克隆化筛选后,单克隆细胞株阳性率100%即确定为稳定细胞株,对细胞株进行定株。杂交瘤细胞株bmg15、bmg18、bmg20、bmg22及bmg23均具有较高的效价,遂后续进一步对上述杂交瘤细胞株进行抗体可变区序列测序分析。
49.实施例2.单链抗体重组表达及纯化
50.根据实施例2中测序结果,将杂交瘤细胞株bm15、bm18、bm20、bm22及bm23的抗体重链及轻链可变区之间加入连接肽(ggggs)3,引入六个组氨酸,并将其全基因直接融合并用毕赤酵母表达系统进行单链抗体的重组表达。所表达得到的抗体分别命名为抗体bm15、bm18、bm20、bm22及bm23。上述单链抗体的重组表达具体如下:
51.a)单链抗体基因表达载体构建
52.单链抗体bm15的基因序列如seq id no:12所示、氨基酸序列如seq id no:11所
imidazole,ph7.5。洗脱时进行线性洗脱,并收集各个洗脱峰。纯化后的蛋白纯度均达到95%以上;合并符合要求的收集管,更换缓冲液为pbs溶液并超滤浓缩(1mg/ml),过滤除菌于-20℃保存备用。
64.实施例3检测试剂盒的制备及使用方法
65.本发明的检测试剂盒是液体双试剂,其中包括r1试剂、r2试剂、校准品,具体见下:
66.1、试剂r1:在缓冲液1中加入稳定剂(例如:nacl或者kcl)、增凝剂(例如:peg6000或者peg8000)、保护剂(例如:bsa或者酪蛋白)、防腐剂(例如:proclin 300)、螯合剂(例如:edta),搅拌混匀,即为r1试剂。
67.2、r2试剂:将5种重组抗人β
2-mg蛋白单克隆抗体用磷酸盐缓冲液将抗体稀释至1.0mg/ml,制备成抗体工作液;用mes缓冲液将胶乳微球(聚苯乙烯胶乳,购自日本jsr公司,粒径80-200nm)稀释至1%(质量浓度),再加入4%(edc/胶乳微球的质量比)的edc,在30℃下搅拌反应30min,反应结束后通过离心去除未反应的edc,然后加入0.1(抗体/胶乳微球的质量比)重组抗人β
2-mg蛋白单克隆抗体工作液,在30℃下搅拌反应30min-120min,反应结束后通过离心去除未反应的抗体,再加入终止反应液终止反应,离心,最后加入由缓冲液2、防腐剂(例如:proclin 300)、稳定剂(例如:nacl,蔗糖)、保护剂(例如:bsa)组成的缓冲液搅拌混匀,即为r2试剂(其中标记重组鼠抗人β
2-mg蛋白单克隆抗体混合物的胶乳微球质量浓度为0.2%-0.5%)。
68.3、校准品:分别向由缓冲液3、保护剂(例如:bsa)稳定剂(例如:nacl)、防腐剂(例如:proclin 300)组成的缓冲液加入不同体积的重组人β
2-mg蛋白,制备得到终浓度为22、12、5、2.5、0mg/l的一组校准品。
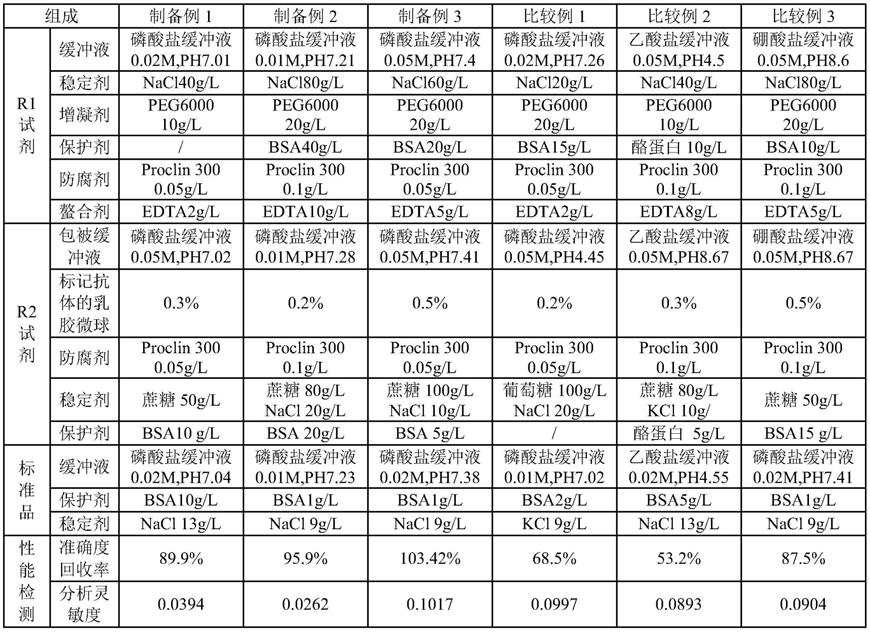
69.优选地,为了提高试剂盒的准确度和检测范围,制备了不同的r1、r2、校准品试剂进行准确度(回收率)、分析灵敏度的性能检测和比对,具体评价结果见下表1。选择本发明的各种缓冲液、稳定剂、保护剂、防腐剂、螯合剂等制备的试剂盒有更好的检测性能。
70.分析灵敏度:以已知β
2-微球蛋白(或简称β
2-mg)含量为(2.00
±
0.50)mg/l的人源血清作为样本进行检测,记录试剂盒在规定参数下的吸光度差值。换算为2.00mg/lβ
2-mg所引起的吸光度差值。
71.准确度(添加回收):选择合适浓度的人血清样本(简称:常规样本)中加入一定体积的校准品(β
2-mg理论浓度为c
理论
)制作成回收样本,在常规样本中加入相同体积的去离子水制作成基础样本,其中加入的校准品体积不超过总体积的1/10,回收样本和基础样本测定浓度对应为c1和c0。根据计算公式:回收率=(c
1-c0)/c
理论
*100%计算出各自的回收率。
72.表1试剂盒的制备比对结果
[0073][0074]
实施例4检测试剂盒的性能测试
[0075]
对照试剂盒:试剂r2中所使用的重组抗体替换为a厂家商品化兔抗人β
2-mg多克隆抗体,其他试剂及实验方案均同实施例3制备;
[0076]
本发明试剂盒:具体见实施例3制备例制备的β
2-mg检测试剂盒;
[0077]
商品化试剂盒:购买于知名b公司的临床用β
2-mg胶乳增强比浊试剂盒;
[0078]
对上述试剂盒关键性能进行比较。
[0079]
1、线性范围
[0080]
采用贝克曼全自动生化分析仪au480测定5个不同浓度的β
2-mg标准品在600nm处的吸光度,绘制校准品的工作曲线(见图1)。结果可以看出,本发明试剂盒的检测范围较对照试剂盒具有更宽的线性范围,更加有利于高浓度的病理样本直接检测,而不需要进行样本的稀释,操作简易化。
[0081]
因对照试剂盒的线性范围均无法满足临床应用需求,遂未对其进行进一步研究。下述性能评价仅针对本发明试剂盒及商品化试剂盒展开。
[0082]
2、精密度
[0083]
重复性:分别检测生理和病理两个浓度的样本,重复测试10次,分别计算变异系数(cv)。检测结果可见,本发明试剂盒和商品化试剂盒的重复性完全达到cv≤10%的行业标准,且本发明试剂盒cv值更低,优于商品化试剂盒(见表2)。
[0084]
批间差:分别用3个不同批号的本发明的检测试剂,测定生理和病理两个浓度的样本,每个批号重复测试3次,计算试剂(盒)批间差r。检测结果可见,本发明试剂盒批间差完全可满足行业标准r≤10%(见表2)。
[0085]
3、准确度
[0086]
添加回收:选择合适浓度的人血清样本(简称:常规样本)中加入一定体积的校准
品(β
2-mg理论浓度为c
理论
)制作成回收样本,在常规样本中加入相同体积的去离子水制作成基础样本,其中加入的校准品量不超过总体积的1/10,每个回收样本和基础样本检测3次,测定平均浓度对应为c1和c0。根据计算公式:回收率=(c
1-c0)/c
理论
*100%计算出各自的回收率。结果表明本发明试剂盒的回收率均能满足80%-120%的要求,而商品化试剂盒的高浓度样本的回收率显著超过120%,显示本发明试剂盒具有更好的的特异性和准确度(见表2)。
[0087]
表2准确度和精密度性能评价结果
[0088][0089]
4、比对试验
[0090]
分别用本发明试剂盒、同类产品商品化试剂盒检测57份人血清,在贝克曼au480生化分析仪同时测定,本发明试剂盒的参数设置见实施例3,商品化试剂盒参照说明书进行。将测定值与商品化试剂盒测定值进行相关性分析,图2显示本发明试剂盒与商品化试剂盒(即对照试剂盒)具有良好的相关性(r2=0.997),可达到临床使用的标准。
[0091]
实施例5检测试剂盒的适用性
[0092]
本发明的检测试剂盒应用于全自动生化仪,但不局限于此,其中主要参数设置及检测方法如下(举例贝克曼全自动生化分析仪au5800):
[0093]
检测波长:主波长600nm,副波长无;检测温度:37℃;
[0094]
检测方法:取110μl试剂r1与1.5μl样本混匀,孵育5min后,加入40μl试剂r2,立即读取吸光度a1,孵育5min后读取吸光度a2,计算吸光度变化
△
a=a2-a1。使用多点非线性校准,绘制校准品的工作曲线,样品中β
2-mg含量可根据
△
a变化值在工作曲线上计算获得。
[0095]
本发明试剂盒在贝克曼au5800生化分析仪上进行精密度、准确度等性能评价(具体见实施例4,其中准确度采用相对偏差法),结果见表3。结果显示本发明试剂盒精密度和准确度满足要求,表明本发明试剂盒也可以应用于贝克曼生化分析仪其他机型,具有较广的适用性。
[0096]
表3本发明试剂盒在au5800上的性能
[0097]
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
